Chinese Journal of Tissue Engineering Research ›› 2014, Vol. 18 ›› Issue (33): 5389-5395.doi: 10.3969/j.issn.2095-4344.2014.33.025
Previous Articles Next Articles
Androgen responses to resistance exercise
Wen An
- Sports School of Xi’an Technological University, Xi’an 710032, Shaanxi Province, China
-
Online:2014-08-13Published:2014-08-13 -
About author:Wen An, M.D., Associate professor, Sports School of Xi’an Technological University, Xi’an 710032, Shaanxi Province, China
CLC Number:
Cite this article
Wen An. Androgen responses to resistance exercise[J]. Chinese Journal of Tissue Engineering Research, 2014, 18(33): 5389-5395.
share this article
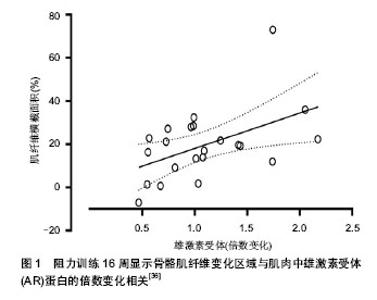
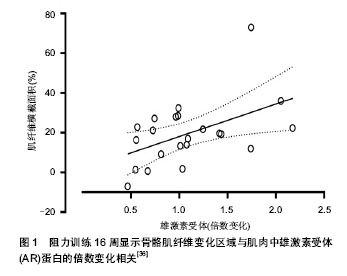
2.1 纳入文献基本情况 抗阻运动睾酮应答背景类文章3篇[1-3]。不同训练方式对抗阻运动睾酮应答的影响类文章11篇[4-14],年龄和性别因素对抗阻运动睾酮应答的影响类文章7篇[15-21],合并营养因素的抗阻运动睾酮应答文章8篇[22-29],抗阻运动睾酮应答的慢性适应——安静期睾酮应答3篇[30-32],抗阻运动对骨骼肌雄激素受体含量的调节类文章10篇[33-42],抗阻运动对睾酮前体的影响类文章4 篇[43-46]。 2.2 不同训练方式对抗阻运动睾酮应答的影响 2.2.1 参与运动肌群对抗阻运动睾酮应答的影响 举重(抓举、挺举)、深蹲、硬拉与小肌肉群相比较能产生更多的睾酮水平升高。这些大肌肉群的训练被视为强有力的代谢刺激因素。Madarame等[4]采用限制血流的方法观察下、上肢肌群(大、小肌肉群)参与运动后激素应答的变化,被试分别作屈伸膝和屈臂弯举,结果显示,下肢运动所产生激素应答明显高于上肢。Migiano等[5]观察单侧上肢和双侧上肢以80%最大力量(1-RM)度,3组×10次,完成5种哑铃运动,单侧组运动总量是双侧组的52.1%,运动后即刻、5,15,30 min,各组血清睾酮的应答无变化。Madarame 认为主要原因可能是参与运动的肌群较少,没有引起睾酮应答。Hansen等[6]观察9周屈肘抗阻训练后肌力的改变,只进行屈肘训练的被试者未产生睾酮应答,但是先进行下肢训练的被试者运动后睾酮明显升高,同样肌肉力量升高也比单纯上肢运动组明显。以上研究结果都支持对于加强肌肉力量的训练,训练课程序设计应该遵循先进行大肌肉群训练然后是小肌肉群训练的原则。 2.2.2 不同骨骼肌收缩形式对抗阻运动睾酮应答的影响 Kraemer等[7]年观察不同的肌肉收缩模式对抗阻训练激素应答的影响。训练计划为6个动作,4组×10次65% 1-RM,间歇时间是90 s,同一动作中,采用离心收缩和向心收缩(前者1-RM为后者1-RM的120%),2种训练方式后总睾酮均为明显升高,游离睾酮均升高。Robert认为在相同的相对负荷下,离心收缩和向心收缩产生同样的激素应答。 2.2.3 运动强度和量对抗阻训练睾酮应答的影响 充足的训练量和强度能确切的改变循环睾酮水平。Schwab 等[8]报道2种深蹲训练后循环睾酮水平显著升高,但是升高发生在完成4组动作之后。当抗阻训练继续进行,更高水平的睾酮应答发生在相对更多组数的训练方案中。同样如果重复次数相同,相对较高的负荷产生更大幅度的急性睾酮应答。但是,Ahtiainen等[9]报道2种相同重复次数,不同强度(一组轻微升高)的抗阻训练睾酮应答无差异。这些训练学变量的相互作用结果显示较大糖酵解的训练计划会产生较显著的激素应答,例如:中的强度、大运动量、相对较短的间歇时间。Guezennec等[10]报道传统的力量训练方法三四组×3-10次重复,70%-95%1-RM,间歇时间2.5 min产生轻微的睾酮升高,但是如果负荷进一步升高重复次数下降到3次,睾酮应答受到限制。 Uchida等[11]研究不同训练计划对激素应答(睾酮、皮质醇)的影响,4组被试完成的动作为卧推,不同训练计划主要表现在负荷、组数和重复次数上的差异:4组50%1-RM最大重复次数,5组75%1-RM最大重复次数,10组90%1-RM最大重复次数,8组110%1-RM最大重复次数,所有组运动量相同(重复次数×组数×负荷)。结果发现除75%1-RM组运动后即刻血清皮质醇升高外,其他运动训练计划未产生激素应答。Uchida认为主要原因是总运动量过小和参与运动肌群过少。 2.2.4 运动间歇时间对抗阻训练睾酮应答的影响 不同运动间歇时间对抗阻训练激素应答影响显著。Rahimi等[12]观察3种不同组间间歇时间对激素应答的影响,训练采用的动作为深蹲和卧推,强度为85%1-RM至每组重复次数为无法完成为止,间歇时间分别是60,90和120 s,结果发现运动后即刻间歇60 s组生长素升高较90,120 s明显;60 s血清睾酮水平升高显著高于120 s,而90 s组与120 s组之间差异无显著性意义。Buresh等[13]比较不同的抗阻间歇时间对应答的影响,训练计划为5-RM,3组,每组重复至不能完成为止,动作为深蹲和卧推,发现第1周短间隙时间1 min组血浆浓度显著高于长间歇时间2.5 min组。第5周、第10周无明显改变。10周后力量的增长各组间无差异。作者认为对于近期无训练个体1 min较2.5 min能产生显著的睾酮应答,随着长期训练时间的积累,间歇时间长短所引起差异消失。这些研究结果显示短间歇时间比长间歇时间更能产生睾酮应答性升高。 2.2.5 训练频率对抗阻训练睾酮应答的影响 训练频率对急性睾酮应答影响的报道较少。Häkkinen等[14]报道优秀举重运动员下午训练较上午训练表现出更明显的睾酮升高应答。但是这个结果比较难以解释睾酮分泌日的节律性对血清睾酮浓度的影响。另外,当训练频率减少到 1次/d时训练量影响的血清睾酮浓度改变恢复正常。 2.3 年龄和性别因素对抗阻训练睾酮应答的影响 2.3.1 年龄对抗阻训练睾酮应答的影响 一般研究结果发现青壮年男性比青少年和老年人群产生更显著抗阻训练激素应答。Kraemer等[15]发现大学生年龄男性表现出显著的急性抗阻训练睾酮应答,而高中年龄男性睾酮应答受限。Craig等[16]发现老年人和青年人渐进抗阻训练后睾酮值变化的差异无显著性意义。Craig认为力量训练能提高睾酮和生长素分泌,但对不同年龄影响程度不同。Nicklas等[17]观察55-70岁男性抗阻训练后的激素应答。被试以3-RM强度的完成6种器械训练。发现急性运动后血清睾酮浓度无改变,16周训练对于同化激素基础值也无影响。 Häkkinen等[18]年观察老年男性和青年男性上、下肢重抗阻训练的激素应答。训练采用等速抗阻收缩,上肢动作为卧推、下肢动作为伸膝和上下肢同步动作,单侧最大等速收缩动作持续5 s,4组,每组重复10次。青年男性组所有动作后总睾酮升高,老年男性仅见于完成下肢动作动作后。青年男性组完成下肢动作、上下肢同步动作动作后游离睾酮值升高,老年男性仅见于完成上下肢同步动作动作后。运动前后青年组较老年组游离睾酮升高明显。作者认为年龄升高重抗阻训练后激素应答下降。下降的游离睾酮应答可能是老年人肌肉体积下降力量下降的原因之一。 2.3.2 性别对抗阻运动睾酮应答影响 总体来说,与男性相比抗阻运动诱导女性同化激素应答升高较少。Kraemer等[19]观察不同的重抗阻运动对女性激素应答的改变,9名青年女性被试在卵泡早期在不同日进行不同的抗阻运动。运动方式有2种,增长力量运动方式和增肌运动方式,负荷为5-RM和10-RM,间歇时间为1 min和 3 min。3种条件两两配对。采集运动前、中、后即刻、5,15,30,60,90,120 min血清总睾酮和胰岛素样生长因子1水平没有明显变化。Linnamo等[20]男性和女性研究极量抗阻练习和爆发力抗阻练习和亚极量抗阻练习的急性激素应答。极量抗阻运动组包括5组×10RM仰卧起坐、卧推和双侧腿蹬伸,组间间歇时间为2 min,亚极量抗阻运动组(SME)为70%,爆发力抗阻运动为50%。结果仅在男性极量抗阻练习组显示运动后睾酮升高,作者认为,极量抗阻运动组急性睾酮对于长期训练同化激素适应和增肌及最大肌力发展起重要作用。 2.3.3 训练经验对抗阻训练睾酮应答的影响 14-18岁举重运动员中训练年限大于2年运动员较少于2年运动员显示出更明显的激素应答。Häkkinen等[21]观察不同年龄,不同性别进行重抗阻训练后的急性激素应答。完成卧推、仰卧起坐和双腿蹬伸,负荷为10-RM,组间休息3 min。青中老年女性均未见睾酮和皮质醇应答,青年男性、中年女性组血清睾酮浓度显著升高,中年女性组血清皮质醇浓度升高,老年男性组无改变。 2.4 营养干预对抗阻运动睾酮应答的影响 2.4.1 糖肽补充对抗阻运动睾酮应答的影响 营养补充会影响抗阻训练的急性睾酮应答。糖类/蛋白质补剂会限制抗阻运动后睾酮应答。机制目前尚不清楚,补充糖类和蛋白质后显示升高的循环胰岛素水平与睾酮水平降低相关,胰岛素和睾酮相互作用需要进一步研究。Kraemer等[22]年观察氨基酸补剂干预对抗阻训练生理适应性的影响。17名被试分为根据瘦体质量随机分为2组,实验组摄入以必需氨基酸为主要成分同时包含β-羟基-β丁酸甲酯的补剂,对照组摄入同等热量的安慰剂。12周中实验组安静睾酮水平高于对照组。Kraeme认为12周抗阻训练过程中补充含有β-羟基-β丁酸甲酯的必需氨基酸能提高激素应答,减轻肌肉损害。Hulmi等[23]观察老年男性摄入蛋白质对抗阻训练后循环睾酮、肌肉雄激素受体等物质的影响。被试随机分为蛋白质摄入组(15 g乳清蛋白,n=9)和安慰剂组(n=9),运动前后摄入补剂。完成5组×10RM训练计划,运动前1 h和后48 h股外侧肌活检。蛋白摄入降低了抗阻训练诱导的血清游离和总睾酮浓度升高,但是抗阻训练显著升高了肌肉雄激素受体mRNA水平。Ratamess等[24]研究一种氨基酸/肌酸能量补剂对急性抗阻运动激素应答的影响。被试分为补剂组(包括必需氨基酸、肌酸、牛磺酸、咖啡因和葡萄糖醛酸内酯)和对照组。采集基础值后摄入补剂,20 min后开始训练,采集运动前、运动后即刻、15,30 min静脉血。所有被试运后即刻和15 min后总睾酮水平升高。补剂组显示高强度运动能力轻微升高,但是对同化激素的应答无影响。Schumm等[25]观察在安静期和抗阻运动后补充糖类的激素应答。被试分为4组:安静+安慰剂,安静+糖类,抗阻运动+安慰剂,抗阻运动+糖类。抗阻运动方案是4组器械深蹲,10RM,组间间歇时间90 s。被试摄入安慰剂或糖类饮料(24%糖类,1.5 g/kg)。运动前,后即刻、15,30,60 min采静脉血。所有组皮质醇浓度无改变;运动前后安慰剂和糖类组睾酮浓度显著升高。糖类运动后60 min睾酮浓度显著低于运动前水平。Schumm认为抗阻运动后摄入糖类导致血清总睾酮在安静期下降,但是机制不清楚。Hulmi等[26]研究抗阻运动前摄入蛋白质对血清激素变化的影响。作者测定了被试的血液激素、能量代谢物、运动后额外氧消耗。被试以液体形式在重抗阻训练课前摄入25 g乳清蛋白或酪蛋白。被试先适应性训练7 d,训练内容为5×1RM深蹲、3×10RM深蹲和4×10RM腿蹬伸,组间间歇时间分别是2,3,2 min。结果发现补充运动前30 min补充25 g乳清蛋白或酪蛋白显著降低血清睾酮、生长素和游离脂肪酸(FFA)水平。 2.4.2 补充肌酸抗阻运动激素应答的影响 Eijnde等[27]观察短期补充肌酸对抗阻训练肌酸应答的影响。11名青年男性志愿者被试补充安慰剂或肌酸5 d后,进行1 h,3组,10RM一次抗阻训练,两次处理间5周清洗期。采集运动前、后即刻、30,60 min静脉血。结果显示运动后生长素升高与肌酸补充无关,肌酸补充对血清睾酮浓度无显著影响,恢复期血清皮质醇肌酸组表现轻微升高。Eijnde认为短期补充肌酸不能影响一次重抗阻训练后的血清睾酮和皮质醇应答。 2.4.3 补充左旋肉碱对抗阻运动激素应答的影响Kraemer等[28]研究补充左旋肉碱左旋酒石酸盐对抗阻运动激素应答和恢复的作用。Kraemer采用平衡、交叉和安慰剂控制的研究方法。结果未发现补充左旋肉碱左旋酒石酸盐对促进抗阻运动后恢复有效,对于激素应答也无直接影响。Kraemer等[29]又观察了在抗阻运动后摄入左旋肉碱3周对激素应答和雄激素受体的作用。作者还是采用平衡、交叉和安慰剂控制实验设计。被试补充左旋肉碱或安慰剂21 d,肌肉活检雄激素受体,然后进行抗阻运动,抗阻运动补充计划分为2种:一种是水,另外一种为预先设计的饮食方案。结果显示左旋肉碱组补充组较P安慰剂组上调抗阻训练雄激素受体含量。运动后进食组雄激素受体含量升高。饮食组血清总睾酮浓度抑制。Kraemer认为抗阻训练后进食增加雄激素受体含量,结果导致睾酮摄取增加睾酮浓度下降。左旋肉碱补充上调雄激素受体含量,能够促进RE运动后恢复。 2.5 抗阻运动睾酮应答的慢性适应——安静期睾酮应答 男性和女性安静期睾酮浓度变化许多研究结果不一致。无训练女性和国家级水平优秀运动员安静浓度相同。安静睾酮浓度反映肌肉组织利用睾酮和内分泌腺分泌睾酮的当前状态,睾酮浓度的升高或降低依赖于运动量和强度的改变[30]。Ahtiainen等[31]报道在7周大运动量训练期游离睾酮和总睾酮明显高于训练前基础值。在随后的7周训练中,运动量下降,强度升高,睾酮浓度下降。Raastad等[32]报道在2周重抗阻训练期后安静睾酮浓度下降12%。因此,改变运动强度和运动量会产生安静睾酮浓度改变,但恢复正常训练时,睾酮浓度回到基础值。 2.6 抗阻运动对雄激素受体含量的调节 组织内雄激素受体的含量与雄激素已知的功能高等相关。骨骼肌雄激素受体浓度依赖许多因素,如肌纤维类型,收缩活动和睾酮浓度。总的来说,抗阻运动能够调节雄激素受体含量。大鼠抗阻运动能够显著升高拇长伸肌的雄激素结合能力,但是也能降低比目鱼肌的雄激素结合能力,因此证明了纤维类型特异性训练效果[33]。3 d电刺激大鼠腓肠肌能提高25%的雄激素受体含量,随着刺激继续,5 d时达到平台期[34]。但是给予雄激素受体抑制剂如奥生多龙,在2周电刺激过程中,与对照组比较刺激诱导增肌下降70%。这些证据显示雄激素受体在训练诱导增肌最大化过程中的作用(图1)[35-36]。 抗阻运动能上调人类骨骼肌雄激素受体含量[37-38]。Bamman等[37]报道股外侧肌雄激素受体mRNA在完成8组×8次重复,离心(110%1-RM)、向心收缩(85%1-RM) 48 h后分别升高63%和102%。Kadi等[38]横断面研究17名力量训练者,其中9名周期性使用同化类固醇,与无训练者比较力量训练者斜方肌内雄激素受体-阳性肌细胞核百分比明显增高,使用同化类固醇力量训练者雄激素受体-阳性肌细胞核百分比高于不使用同化激素力量训练者。基础值测量时力量训练者与无训练者雄激素受体-阳性肌细胞核百分比差异无显著性意义。 有研究显示报道股外侧雄激素受体含量与1RM深蹲显著相关[1],这提示雄激素受体含量能够在抗阻训练中辅助调节力量改变,抗阻运动刺激能调节急性雄激素受体改变。Ratamess等[39]比较2种深蹲练习(1组和6组10次重复)1 h后雄激素受体含量变化。1组练习后雄激素受体含量无改变。但是,大运动量训练显著下调雄激素受体含量。考虑到雄激素受体是蛋白质分子,抗阻运动会增加蛋白质分解代谢,数据显示,如果达到充足的训练量,雄激素受体蛋白质含量在开始阶段下降(尽管循环睾酮水平升高),随后上调,原因还需进一步研究。另外运动前、后摄入蛋白质和糖类会降低大运动量抗阻训练后雄激素受体的下调。因此,营养干预在运动后雄激素受体调节过程中起着重要作用。 Willoughby等[40]观察连续3次抗阻运动后血清总睾酮、性激素结合球蛋白和游离雄激素指数及骨骼肌雄激素受体的mRMA和蛋白质表达和肌原纤维蛋白含量的变化。18名被试随机等分为抗阻运动组和对照组,抗阻运动组完成3次下肢抗阻运动,运动方案:深蹲、腿蹬伸和伸膝,3组×8-10次75%-80%1-RM。对照组不进行运动。3次运动前即刻、运动后48 h进行肌肉活检;运动前即刻、运动后即刻、30 min后采集血液样本。每次运动后血清总睾酮和游离雄激素指数显著升高,性激素结合球蛋白无变化。雄激素受体mRNA在第2次和第3次运动后显著升高且与总睾酮和雄激素指数相关。第3次运动后肌原纤维蛋白增加。作者认为连续3次重抗阻训练能升高血清总睾酮,有效地上调雄激素受体mRNA和蛋白质表达,与随后的肌原纤维蛋白质升高相一致。Ahtiainen等[41]观察重抗阻训练后青年和老年男性骨骼肌雄激素受体表达的变化。被试分为青年训练组,青年对照组,老年训练组和老年对照组,训练周期为21周。在训练周期前后各进行1次重抗阻训练,运动方案为5×10RM腿蹬伸。急性实验前1 h和后48 h进行股外侧肌活检,测定肌纤维横断面和雄激素受体mRNA表达及蛋白质含量。急性训练后睾酮浓度升高,但基础值不变。一次急性运动后与运动前比较平均雄激素受体mRNA表达和蛋白含量没变。但在青年训练组和老年训练组,个体训练前后雄激素受体蛋白质含量变化与肌纤维横断面、瘦体质量和1-RM变化相关。Ahtiainen认为虽然雄激素受体表达没有因抗阻训练改变,但是不论是青年还是老年男性骨骼肌内雄激素受体蛋白质随抗阻训练改变的结果显示抗阻运动诱导骨骼肌适应性变化。 Vingren等[42]年观察力量训练男性、女性急性抗阻训练对肌肉内类固醇受体蛋白含量的影响。15名青年被试(男性8名,女性7名)完成6组×10次重负荷深蹲。运动前、运动中3、6组后、运动后5,15,30,70 min采静脉血,运动前、后10,70 min进行骨骼肌活检。男性运动后循环总睾酮升高,所有被试游离睾酮运动后升高。男性运动后70 min雄激素受体显著下降,女性被试运动后10 min显著下降。作者认为该研究支持当前流行的雄激素受体应答范式,及男抗阻训练后雄激素受体先稳定、后下降、然后再反弹上升。同时男性、女性雄激素受体应答在时间上有差异。Roberts等[43]观察青年人和老年人一次抗阻训练前后雄激素调节基因的变化。被试完成3组×10次80%1-RM抗阻训练,动作有Smith深蹲、腿蹬伸和伸膝。运动前和后24 h肌肉活检;运动前,后即刻和24 h采静脉血。青年被试运动后即刻血清睾酮显著升高。老年男性安静雄激素受体水平较高。运动前游离睾酮与雄激素受体基因表达显著负相关(r=-0.59,P < 0.01)。结果提示雄激素受体表达模式活性与循环游离睾酮浓度有关。 2.7 抗阻运动对睾酮前体的变化的影响 抗阻运动对肾上腺雄激素水平有显著影响。由于女性睾酮水平很低,肾上腺雄激素可能起重要的作用。女性显示出较高的循环脱氢表雄酮转化率,在组织水平中脱氢表雄酮(DHEA)转化为雄烯二酮和睾酮的比例较高,一般情况下雄烯二酮基础值高于男性,但是,雄烯二酮生物效能远低于睾酮。Weiss等[44]报道男性和女性在完成4种练习方式,3组80% 1-RM,每组重复至不能完成,间歇时间为2 min的训练计划后,循环雄烯二酮升高8%-11%。Tremblay等[2]报道男性抗阻训练后脱氢表雄酮硫酸盐(DHEA)升高高于耐力训练。在完成一项24周的抗阻训练计划过程中,雄烯二酮、脱氢表雄酮和硫酸脱氢表雄酮的安静值无改变。但是女性24周抗阻训练后脱氢表雄酮和硫酸脱氢表雄酮升高,并且与升高的瘦体质量显著相关[45]。急性和慢性睾酮前体浓度的改变需要进一步研究。 Copeland等[46]评估激素替代疗法对绝经期后女性抗阻训练激素急性应答和慢性实验的影响。在12周训练中,4组被试(运动2组、控制2组)在第0,4,13周采安静期静脉血,同时在第0和13周运动后即刻采静脉血。各安静期激素浓度无改变,但脱氢表雄酮和皮质醇显示出明显的周、组相互作用,非激素替代组运动后脱氢表雄酮和皮质醇显著升高。结论认为,激素替代疗法对绝经期后女性抗阻训练急慢性激素激素无应答。Enea等[47]对运动诱导女性循环雄性激素(睾酮、雄烯二酮和脱氢表雄酮)改变的研究进行综述。虽然各项研究的训练方案不同、检测方法不同,但普遍显示急性运动训练能升高雄激素水平。慢性训练结果差异较大,表现出有升高降低或不变。 "
| [1]William J, Kraemer Nicholas A.Ratamess Hormonal Responses and Adaptations to Resistance Exercise and Training.Sports Med. 2005;35(4):339-361. [2]Tremblay MS, Copeland JL, Van Helder W. Effect of training status and exercise mode on endogenous steroid hormones in men.J Appl Physiol.2003;96:531-539. [3]Kraemer WJ, Häkkinen K, Newton RU, et al. Effects of heavyof resistance training on hormonal response patterns in younger vs older men.J Appl Physiol.1999;87:982-992. [4]Madarame H,Sasaki K,Ishii N.Endocrine responses to upper- and lower-limb resistance exercises with blood flow restriction. Acta Physiol Hung.2010;97(2):192-200. [5]Migiano MJ, Vingren JL, Volek JS, et al. Endocrine response patterns to acute unilateral and bilateral resistance exercise in men. J Strength Cond Res. 2010;24(1):128-134. [6]Hansen S, Kvorning T, Kjaer M, et al. The effect of short-term strength training on human skeletal muscle: the importance of physiologically elevated hormone levels. Scand J Med Sci Sport. 2001;11:347-354. [7]Kraemer RR, Hollander DB, Reeves GV, et al. Similar hormonal responses concentric and eccentric muscle actions using relative loading.Eur J Appl Physiol. 2006;96: 551-557. [8]Schwab R, Johnson GO, Housh TJ, et al. Acute effects of different intensities of weight lifting on serum testosterone. Med Sci Sports Exerc.1993;25:1381-1385. [9]Ahtiainen JP, Pakarinen A, Kraemer WJ, et al. Acute hormonal and neuromuscular responses and recovery to forced vs maximum repetitions multiple resistance exercises. Int J Sports Med.2003;24:410-418. [10]Guezennec Y,Leger L,Lhoste F, et al.Hormone and metabolite response to weight-lifting training sessions. Int J Sports Med. 1986;7:100-105. [11]Uchida MC, Crewther BT, Ugrinowitsch C, et al. Hormonal responses to different resistance exercise schemes of similar total volume.Strength Cond Res.2009;23(7):2003-2008. [12]Rahimi R, Qaderi M, Faraji H,et al. Effects of very short rest periods on hormonal responses to resistance exercise in men.J Strength Cond Res.2010;24(7):1851-1859. [13]Buresh R, Berg K, French J. The effect of resistive exercise rest interval on hormonal response, strength, and hypertrophy with training. J Strength Cond Res. 2009;23(1):62-71. [14]Häkkinen K, Pakarinen A, Alen M, et al. Neuromuscular and hormonal responses in elite athletes to two successive strength training sessions in one day.Eur J Appl Physiol.1988; 57:133-139. [15]Kraemer WJ, Fry AC, Warren BJ, et al. Acute hormonal responses in elite junior weightlifters.Int J Sports Med.1992; 13:103-109. [16]Craig BW, Brown R, Everhart J. Effects of progressive resistance training on growth hormone and testosterone levels in young and elderly subjects.Mech Ageing Dev. 1989; 49(2):159-169. [17]Nicklas BJ, Ryan AJ, Treuth MM, et al. Testosterone, growth hormone and IGF-I responses to acute and chronic resistive exercise in men aged 55-70 years.Int J Sports Med. 1995; 16(7):445-450. [18]Häkkinen K, Pakarinen A, Newton RU,et al. Acute hormone responses to heavy resistance lower and upper extremity exercise in young versus old men.Eur J Appl Physiol Occup Physiol. 1998;77(4):312-319. [19]Kraemer WJ, Fleck SJ, Dziados JE,et al. Changes in hormonal concentrations after different heavy-resistance exercise protocols in women.J Appl Physiol. 1993;75(2): 594-604. [20]Linnamo V, Pakarinen A, Komi PV, et al. Acute hormonal responses to submaximal and maximal heavy resistance and explosive exercises in men and women.J Strength Cond Res. 2005;19(3):566-571. [21]Häkkinen K, Pakarinen A.Acute hormonal responses to heavy resistance exercise in men and women at different ages.Int J Sports Med.1995;16(8):507-513. [22]Kraemer WJ, Hatfield DL, Volek JS, Fragala MS, Vingren JL Effects of amino acids supplement on physiological adaptations to resistance training.MEDICINE & SCIENCE IN SPORTS & EXERCISE.2009;41(5):1111-1121. [23]Hulmi JJ, Ahtiainen JP, Selänne H,et al. Androgen receptors and testosterone in men--effects of protein ingestion, resistance exercise and fiber type. J Steroid Biochem Mol Biol.2008;110(1-2):130-137. [24]Ratamess NA, Hoffman JR, Ross R,et al. Effects of an amino acid/creatine energy supplement on the acute hormonal response to resistance exercise. Int J Sport Nutr Exerc Metab. 2007;17(6):608-623. [25]Schumm SR, Triplett NT, McBride JM, et al. Hormonal response to carbohydrate supplementation at rest and after resistance exercise. Int J Sport Nutr Exerc Metab. 2008;18(3): 260-280. [26]Hulmi JJ, Volek JS, Selänne H, et al. Protein ingestion prior to strength exercise affects blood hormones and metabolism. Med Sci Sports Exerc. 2005;37(11):1990-1997. [27]Eijnde BO, Hespel P. Short-term creatine supplementation does not alter the hormonal response to resistance training. Med Sci Sports Exerc.2001;33(3):449-453. [28]Kraemer WJ, Volek JS, French DN, et al.The effects of L-carnitine L-tartrate supplementation on hormonal responses to resistance exercise and recovery.J Strength Cond Res. 2003; 17(3):455-462. [29]Kraemer WJ, Spiering BA, Volek JS,et al. Androgenic responses to resistance exercise: effects of feeding and L-carnitine.Med Sci Sports Exerc.2006;38(7):1288-1296. [30]Stoessel L, Stone MH, Keith R, et al. Selected physiological, psychological and performance characteristics of national-caliber United States women weightlifters.Journal of Strength & Conditioning Research.1991;5:87-95. [31]Ahtiainen JP,Pakarinen A, Alen M, et al. Muscle hypertrophy, hormonal adaptations and strength development during strength training in strength-trained and untrained men.Eur J Appl Physiol.2003;89:555-563. [32]Raastad T, Glomsheller T, Bjoro T, et al. Changes in human skeletal muscle contractility and hormone status during 2 weeks of heavy strength training.Eur J Appl Physiol.2001;84: 54-63. [33]Deschenes MR, Maresh CM, Armstrong LE, et al. Endurance and resistance exercise induce muscle fiber type specific sponses in androgen binding capacity.J Steroid Biochem Mol Biol.1994;50:175-179. [34]Inoue K, Yamasaki S, Fushiki T, et al. Rapid increase in the number of androgen receptors following electrical stimulation of the rat muscle.Eur J Appl Physiol 1993;66:134-140. [35]Inoue K, Yamasaki S, Fushiki T, et al. Androgen receptor antagonist suppresses exercise-induced hypertrophy of skeletal muscle.Eur J Appl Physiol.1994;69:88-91. [36]Mitchell CJ,Churchward-Venne TA,Bellamy L,et al.Muscular and systemic correlates of resistance training-induced muscle hypertrophy.PLoS One. 2013;8(10):e78636. [37]Bamman MM, Shipp JR, Jiang J, et al. Mechanical load in creases muscle IGF-1 and androgen receptor mRNA concen trations in humans.Am J Physiol.2001;280:E383-90. [38]Kadi F, Bonnerud P, Eriksson A, et al. The expression of androgen receptors in human neck and limb muscles: effects of training and self-administration of androgenic-anabolic steroids.Histochem Cell Biol.2000;113:25-29. [39]Ratamess NA, Kraemer WJ, Volek JS, et al. Effects of heavy resistance exercise volume on post-exercise androgen receptor content in resistance-trained men.J Steroid Biochem Molec Biol.2005:93:35-42. [40]Willoughby DS, Taylor L. Effects of sequential bouts of resistance exercise on androgen receptor expression. Med Sci Sports Exerc.2004;36(9):1499-1506. [41]htiainen JP, Hulmi JJ, Kraemer WJ,et al. Heavy resistance exercise training and skeletal muscle androgen receptor expression in younger and older men.Steroids. 2011;76(1-2): 183-192. [42]Vingren JL, Kraemer WJ, Hatfield DL,et al. Effect of resistance exercise on muscle steroid receptor protein content in strength-trained men and women.Steroids. 2009; 74(13-14):1033-1039. [43]Roberts MD,Dalbo VJ,Hassell SE,et al. The expression of androgen-regulated genes before and after a resistance exercise bout in younger and older men.J Strength Cond Res. 2009;23(4):1060-1067. [44]Weiss LW,Cureton KJ,Thompson FN.Comparison of serum testosterone and androstenedione responses to weight lifting in men and women.Eur J Appl Physiol 1983;50:413-419. [45]Häkkinen K,Pakarinen A,Kraemer WJ,et al.Basal concentrations and acute responses of serum hormones and strength development during heavy resistance training in middle-aged and elderly men and women.J Gerontol A Biol Sci Med Sci.2000;55:B95-105. [46]Copeland JL,Tremblay MS.Effect of HRT on hormone responses to resistance exercise in post-menopausal women. Maturitas.2004;48(4):360-371. [47]Enea C, Boisseau N, Fargeas-Gluck MA,et al.Circulating androgens in women: exercise-induced changes.Sports. Med.2011;41(1):1-15. |
| [1] | Zhang Yuantong. Body composition and bone mineral density of juvenile basketball players versus ordinary middle school students: data from a middle school [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(3): 341-347. |
| [2] | Lan Qingshi. Participation degree and control ability of human latissimus dorsi, trapezius, triceps, musculus and deltoid during cross support of hand ring: analysis on contribution rate of major muscle group [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(3): 361-366. |
| [3] | Kong Lingyao, Li Tao, Zeng Xinglin, Li Jian, Xiong Yan. Synovial chondromatosis: how to improve the diagnosis accuracy and clearance rate of tumor cells [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(28): 4570-4575. |
| [4] | Long Yanfang1, 2, Wang Xinlei2, Wang Mingpu3, Tang Xingjiang2. Effects of androgen on the expression of Bcl-2, Bax and Cyt-C in brain tissue of adult rat models of middle cerebral artery occlusion [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(27): 4344-4349. |
| [5] | Yu Hong, Liu Yan. Strength of knee flexor and extensor in football athletes after vibration training [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(15): 2327-2331. |
| [6] | Zhu Yaojia1, Huo Hongfeng1, 2. Balance ability and foot type characteristics during different postures of standing [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(15): 2345-2349. |
| [7] | Li Xintong1, Pan Weimin2, Qin Huasheng1, Qu Lei1, Zhang Hengyin1, Zhu Xinrui1. Blood flow restriction training: a new method for accelerating musculoskeletal rehabilitation [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(15): 2415-2420. |
| [8] | Wang Minjia1, Qi Ziyi2, Zhu Weihua1, Sun Junzhi1. Mechanism and clinical research advance of muscle atrophy: thinking based on the 65th Annual Meeting of American College of Sports Medicine [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(15): 2421-2426. |
| [9] | Yuan Yiwen, Gui Zhu, Zhang Hongchao. Changes in muscle injury and pulse wave velocity after exercise with compression leg cuffs in college students without fitness habits [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(11): 1687-1692. |
| [10] | Xie Hao-dong1, 2, Luo Jiong1, 2. Stiffness of the lower extremities during landing [J]. Chinese Journal of Tissue Engineering Research, 2018, 22(8): 1306-1312. |
| [11] | Wang Zhao-feng1, Gong Ming-ming2, Chen Jia-qun2, Mo Wei-bin3. Effects of Glycyrrhiza Flavone on the pathological changes of quadriceps and expression of fatty acid translocase/CD36 in training rats [J]. Chinese Journal of Tissue Engineering Research, 2018, 22(4): 529-534. |
| [12] | Ma Tao, Li Jian, Jin Jia-peng . Effects of different sports events on bone mineral density in the recent decade: a bibliometric analysis [J]. Chinese Journal of Tissue Engineering Research, 2018, 22(4): 631-634. |
| [13] | Huang Jie1, Bo Zhandong2, Liu Gang3, Luo Shixing4. Correlation between serum estradiol and testosterone levels and severity of early-stage knee osteoarthritis in patients [J]. Chinese Journal of Tissue Engineering Research, 2018, 22(36): 5760-5765. |
| [14] | Lei Bingkai1, 2, Sun Junzhi1, Zhao Xiaoqin3, Ding Haili1, Liu Yong2, Wang Ruiyuan2, Li Junping2. Role of Omi/Beclin-1 signaling pathway in the eccentric exercise-induced skeletal muscle autophagy [J]. Chinese Journal of Tissue Engineering Research, 2018, 22(36): 5791-5796. |
| [15] | Wang Dandan, Zhang Lei, Wu Xueping . Physical activity of people with intellectual disability measured by motion sensor [J]. Chinese Journal of Tissue Engineering Research, 2018, 22(36): 5889-5896. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||