Chinese Journal of Tissue Engineering Research ›› 2013, Vol. 17 ›› Issue (7): 1295-1304.doi: 10.3969/j.issn.2095-4344.2013.07.026
Previous Articles Next Articles
Difficulties in tissue engineering construction technology for repair of peripheral nerve injuries
Tang Yuan, Liu Xiang-hua, Liu Dan, Yu Hua-xu
- Changsha Medical University, Changsha 410219, Hunan Province, China
-
Received:2012-09-07Revised:2012-11-06Online:2013-02-12Published:2013-02-12 -
Contact:Yu Hua-xu, Changsha Medical University, Changsha 410219, Hunan Province, China xhuyu @yahoo.com -
About author:Tang Yuan, Changsha Medical University, Changsha 410219, Hunan Province, China Tangyuan81@yahoo.cn Yu Hua-xu☆, Doctor, Associate professor, Changsha Medical University, Changsha 410219, Hunan Province, China Tang Yuan and Yu Hua-xu contributed equally to this work.
CLC Number:
Cite this article
Tang Yuan, Liu Xiang-hua, Liu Dan, Yu Hua-xu. Difficulties in tissue engineering construction technology for repair of peripheral nerve injuries[J]. Chinese Journal of Tissue Engineering Research, 2013, 17(7): 1295-1304.
share this article
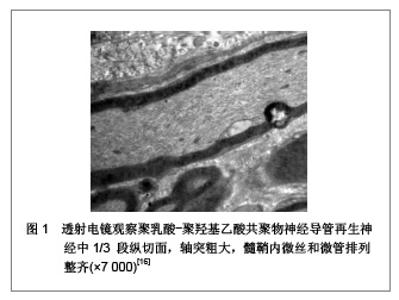
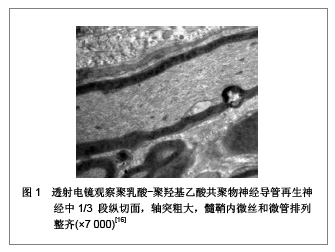
2.1 组织工程神经支架 传统的神经移植方法包括自体移植、异体移植和异种神经移植。自体神经移植由于来源困难,且有供区瘢痕、神经瘤形成、运动感觉障碍、误向支配等问题,无法满足临床需要。异体神经和异种神经移植面临免疫排斥反应,移植神经结构被破坏,基底膜管壁塌陷并纤维化,再生轴突无法通过,常导致移植失败。许多学者试图用其他组织替代来弥补以上不足,早期采用动脉、静脉、筋膜、输卵管、羊膜、无细胞肌肉等进行神经桥接,但效果均不满意[2]。因此,神经导管支架成为神经缺损修复的一个重要研究方向。 作为周围神经组织工程的支架材料,其基本要求包括:①生物降解可吸收性:即材料在细胞生长、繁殖和组织再生过程中能逐渐降解吸收。②良好的生物相容性:即支架材料及其降解产物对组织细胞无毒性和致突变作用,植入体内无抗原性和致畸作用。③良好的表面活性:即材料表面能使细胞良好的黏附和生长。④可塑性和适宜的力学性能:即易于加工成型,能够在体内外承受一定的压力,并在一定时限内保持其外形和结构的完整性[3]。⑤一定的导电性:已有实验证明,良好的导电性能够促进、刺激、引导神经细胞生长及轴突再生。⑥具有三维立体多孔结构:这种结构可提供宽大的表面积和空间,利于细胞黏附生长、细胞外基质沉积、营养和氧气进入及代谢产物的排出,也有利于血管和神经长入[4-5]。 2.1.1 神经支架材料的可降解性 Lundborg 等[6]设计的一种神经导管以硅胶管为外支架,管内平行放置8根尼龙线作为内支架,成功引导大鼠再生轴突通过15 mm的神经缺损段,组织学研究表明轴突沿着内支架迁移,而没有用内支架的硅胶管桥接者,轴突不能长入远端神经段。上述人工材料不可降解,术后会产生严重神经卡压现象及炎性刺激,另外需要再次外科手术取出,所以并不适合临床应用。生物可降解材料制备的神经导管可在合理的时间段内降解,并且组织排斥性小。另外,还通过对高聚物表面的物理化学改性而黏附许旺细胞和生物活性分子,并在降解过程中释放。因此,目前组织工程学中神经导管材料主要选择可降解材料。聚羟基乙酸(PGA)、聚乳酸(PLA)及其共聚物(PLGA)是较为普遍使用的可降解材料,运用这些材料制备导管进行动物实验及临床实验的报道很多[7-8]。Dunnen 等[9]则用聚乳酸与聚ε-己内酯的共聚物制成神经导管,其修复神经缺损的效果甚至比自体神经移植还好。几丁质作为人工室桥接神经损伤能有效阻止瘢痕组织侵入,引导轴突再生,同时为施加外源性神经生长因子提供了有益的空间,并能在一定时间内维持其有效浓度[10]。 2.1.2 神经支架材料的生物相容性 任何一种生物材料应用于临床,首先应具备使用安全性和良好的生物相容性,这是生物材料获准临床使用的前提。神经导管作为再生轴突生长的临时通道,必须与神经组织有良好的相容性。这要求材料本身或其降解产物对种子细胞无破坏,且对机体无致癌、致畸、致突变作用,不会引起炎症和免疫排斥反应,且能够为种子细胞提供良好的黏附和生长界面。Stanec等[11]报道将生物相容性较好的膨体聚四氟乙烯制成神经导管,临床上用于桥接正中神经和尺神经1.5-6.0 cm的缺损,损伤神经恢复了部分感觉和运动功能。Jiao等利用细胞周期检测与DNA倍体分析的方法对生物材料是否具有致癌性进行客观、有效的评价,证实了聚乳酸-聚羟基乙酸共聚物对嗅鞘细胞无致癌性,二者合用安全、可靠,具有良好的细胞生物相容性[12-13]。早期研究证实,几丁质与神经组织有良好的生物相容性,已被用作制备神经导管的常用材料[14]。 2.1.3 神经支架材料的表面活性及力学性能 支架材料的力学性能在结构上决定了缺损部位的强度大小,在组织再生过程中,能为体内外负重提供临时支撑作用,以及抵抗材料内接种的细胞在植入前和细胞滤过时所产生的收缩力。复合材料的力学性能能较好适应神经导管的要求,是近来组织工程支架材料研究的发展趋势之一。Li等[15]分别用85∶15和50∶50的聚乳酸-聚羟基乙酸共聚物导管桥接大鼠10 mm的坐骨神经缺损,发现构成比为50∶50组力学机械性能显著降低,4周时未能抵御大鼠正常活动的应力,神经导管发生断裂,而85∶15组8周时结构良好,12周时才出现较明显的吸收现象,此时再生神经外形上已近似正常的坐骨神经。李志跃等[16]同样应用85∶15构成比的聚乳酸-聚羟基乙酸共聚物三维神经导管有效引导了SD大鼠坐骨神经长过12 mm 的神经缺损,见图1,且采用层粘蛋白注入涂层方法改善了表面亲和力,提高了导管的表面活性。已有实验证明,材料具有良好的表面活性能促进细胞的黏附、扩散、迁移和增殖,壳聚糖因其具有良好的表面活性在神经导管方面已有较为广泛的研究与应用,其表面活性主要表现在材料表面的正电荷增强了被吸附蛋白和材料之间的相互作用,并且能与细胞膜发生非特异性吸附。研究证实,壳聚糖与许旺细胞不仅具有很好的相容性[17],而且许旺细胞容易在壳聚糖纤维上生长[18]。敖强等[19]证实,利用壳聚糖制备的多通道神经导管具有良好的表面活性,与N2a神经细胞亲和性大。"

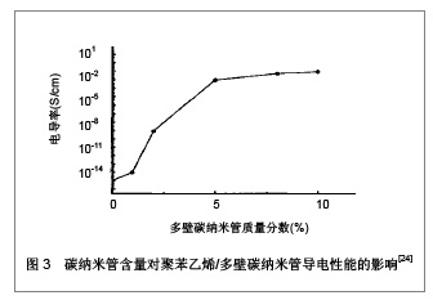
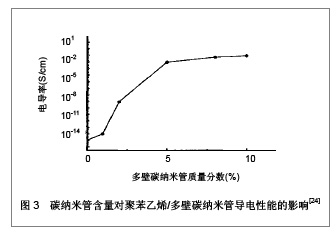
2.1.4 神经支架材料的电活性 具有导电性的生物材料对各种生长细胞例如神经细胞和骨细胞具有很好的支持和调节作用[20-22]。生物材料结合电刺激效应可调节细胞的黏附,增殖和分化。Runge等[23]研究发现,电刺激培养在聚吡咯酸(一种导电性生物材料)上的PC-12细胞与未经过电刺激培养的对照组相比,其神经伸长程度显著增加,较对照组增加达90%。近年来,随着人们对纳米材料的理化性质认识不断加深,纳米材料更多的运用于神经的再生与功能的重建,针对碳纳米管的研究成为组织工程神经材料的热点。碳纳米管具有许多独特的性质,其重要之处则是具有良好的导电性,并在一定范围内导电性可以提高。使用溶液共混法制备的聚苯乙烯/多壁碳纳米管复合导电材料,加入2%左右的多壁碳纳米管,电导率增加到10-9 S/cm;当碳纳米管含量为5%时,电导率增加到10-3 S/cm,再增加碳纳米管含量,聚苯乙烯/多壁碳纳米管复合材料的电导率则变化不大[24],见图2,3。"

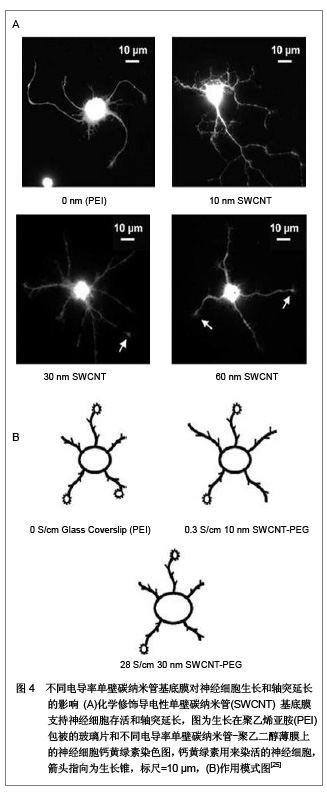
Malarkey 等[25]将聚乙二醇修饰的单壁碳纳米管制成厚度分别是10,30和60 nm的基底膜,电导率依次是0.3,28和60 S/cm,发现培养在0.3 S/cm电导率的基底膜上的神经细胞修复能力最强,见图4,证明了碳纳米管的导电性是影响神经细胞生长和分化的又一关键因素。Lee 等[26]发现单纯电刺激能够促进神经生长达40%-90%,但是当电刺激并匹配有导电性纳米纤维时神经生长长度显著增加,表明电刺激与导电性纳米生物材料有协同作用。 2.1.5 神经支架材料的制备要求 组织工程化移植物无论是在体外培养还是体内转化过程中,均需要一种三维多孔结构的立体支架,它不仅决定着新生组织的形状和大小,而且可以为最初种子细胞的黏附、停留、生长及新陈代谢提供场所。三维立体多孔结构需要有高度的孔隙率,合适的孔径和比表面积,以便给神经细胞提供良好的生长环境。早期,人们应用各种中孔导管修复周围神经缺损,但中孔导管不具有足够的内表面积,不利于神经纤维和许旺细胞黏附生长。Wang等[27]采用相分离法制备聚乳酸神经导管,分别为取向多孔结构和互穿网络多孔结构,细胞种植后,显微观察表明互穿网络多孔结构更有利于神经细胞的黏附和神经细胞的生长。因此,研究三维多孔结构的神经支架,以满足临床应用组织工程技术修复周围神经损伤的要求。 Li等[28]报道了一种具有较高孔隙结构的电纺聚乳酸-聚羟基乙酸共聚物支架,其孔隙率达到91.63%,孔径范围为2-465 μm。但大部分文献报道的平均孔径均小于100 μm,孔隙率在80%左右[28-30]。按照传统的支架加工观点这样的微孔结构能够满足细胞吸收养分和排出废物的要求,却不利于细胞长入和血管生成。而孔径范围达300-500 μm的互联大孔结构虽保证了一定程度的扩散速度,然而从支架材料的内部结构来看,大块支架内营养成分的传输和代谢物的排放不可能很充分。因此为便于细胞长入、养分吸收和代谢产物排出,组织工程支架的孔径范围应控制在100-400 μm[31]。孔隙率最好达90%以上,这样就具有较高的面积/体积比,为细胞和组织生长提供足够的空间和交换通道,而且呈一定的方向性排列能够保证细胞按单一方向生长。"
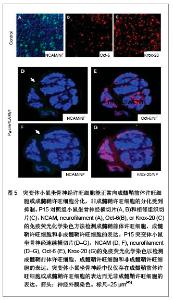
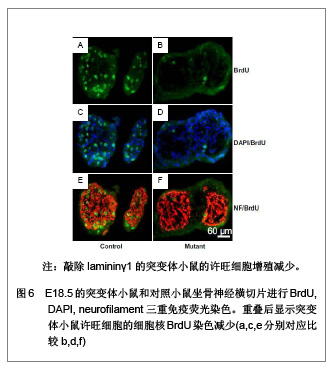
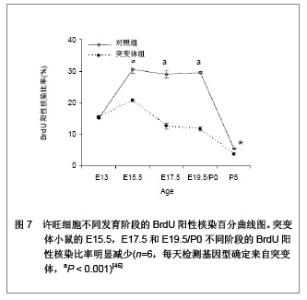
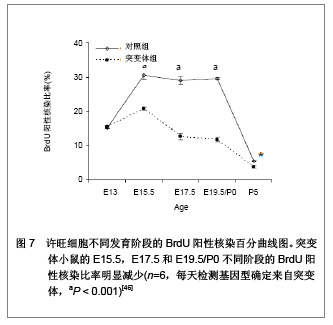
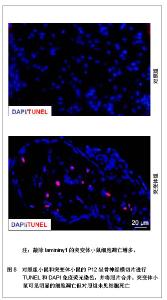
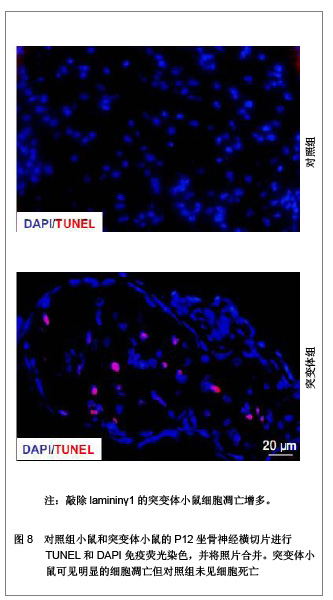
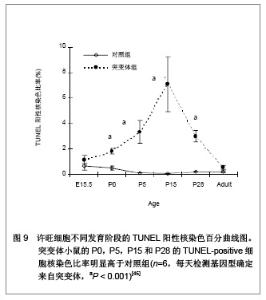
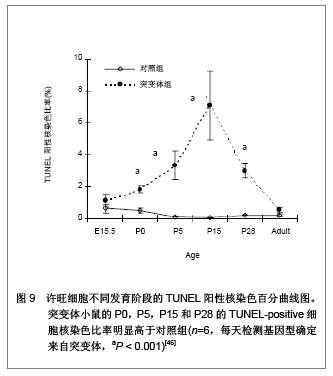
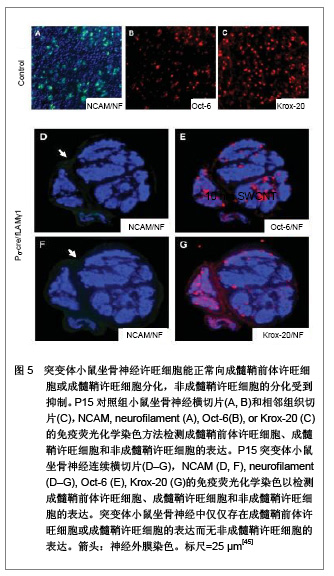
2.2 生物功能化 随着神经组织工程的研究深入与发展,人们逐渐认识到,单一的利用神经导管修复周围神经损伤的效果不佳,主要由于导管内不含有任何生物活性物质,神经导管仅作为神经再生的物理性通道。事实上,神经导管不仅仅是作为神经再生的临时通道,更重要的是应具有促进轴突再生的生物学活性。在神经损伤修复过程中,神经营养因子、支持细胞和种子蛋白的促再生作用是致关重要的,是加强生物功能化的重要因素。因此,如何增强导管的生物活性,改善神经再生的微环境,加大神经损伤修复的程度是周围神经组织工程研究的热点。 2.2.1 神经营养因子 神经营养因子可经轴突逆行转运至神经元胞体,与相应受体结合发挥生物学效应。神经营养因子在神经受损后神经元的存活中起重要作用,神经导管中适当加入神经营养因子可修复更长距离的神经缺损[32]。神经生长因子是最早被发现的一种神经营养因子,属于神经营养因子中的神经营养素家族,神经生长因子能促进神经元的增殖与分化,同时调节受损神经的修复[33-34]。已有研究报道,周围神经再生过程中,神经生长因子的含量上调[35]。神经受损后的神经生长因子蛋白重组促进了神经修复和功能的恢复[36]。其作用机制可能是神经生长因子与效应细胞上特异性的膜受体结合后形成复合体,然后沿轴浆逆行转运,经轴突入胞体,再与核受体结合,引起一系列生物学效应[37]。Yang 等[38]利用神经生长因子缓释技术先将神经生长因子与聚乳酸-聚羟基乙酸共聚物微球混和或封装在微球内,获得的神经导管可以持续释放神经生长因子至少6周。Fisher等[39]在Wistar大鼠单侧坐骨神经切断动物模型上,断端采用硅胶管桥接,硅胶管内给予神经生长因子+每日肌肉注射神经生长因子,连续7周。结果显示髓鞘碱性蛋白含量减少,神经生长因子神经功能明显改善,神经生长因子对损伤后周围神经功能的恢复、促进其再生起到显著作用,且以局部应用加肌肉给药治疗的效果最佳。 2.2.2 支持细胞 支持细胞主要包括许旺细胞、嗅神经鞘细胞、骨髓间充质干细胞、神经干细胞等。其中,许旺细胞是周围神经系统的主要支持细胞,在周围神经系统和中枢神经系统中都具有促进神经纤维再生的作用。周围神经系统中,植入神经导管内的许旺细胞经过一段时间后逐渐移居至缺损神经两端的纤维蛋白基质上,促进神经导管中短距离神经缺损的再生修复。另外,神经导管中植入的许旺细胞快速增殖形成Bungner带,再生轴突沿着Bungner带生长以桥接缺损神经并分泌大量细胞外基质和神经营养因子等机制引导和营养神经趋化性再生。这些机制提示了神经再生不是简单的轴突沿许旺细胞支架延伸,而是基于轴突与周围许旺细胞进行直接和动态的交流的复杂过程,许旺细胞利用紧密连接保持结构稳定,同时通过缝隙连接进行信息和物质交换。Sinis等[40]引用自体许旺细胞填充三甲烯二胺/己内酯导管修复大鼠正中神经缺损,修复效果满意,证实神经导管内填充许旺细胞是有效的周围神经损伤修复方法。研究表明,预种植许旺细胞的神经导管可修复更长距离的神经缺损,神经再生质量也得到改善[41]。大量实验证实含有许旺细胞的神经导管修复神经缺损后神经功能的恢复比没有许旺细胞者优越[42]。 尽管将许旺细胞加入导管中在一定程度上促进了周围神经再生,但其关键是生物工程技术能保证许旺细胞的活性[43]。且许旺细胞在神经导管内有序地排列结构需类似于Bungner带,但是现在不管是将许旺细胞通过注射的方法植入神经导管,还是将神经导管与许旺细胞联合培养,使许旺细胞迁移入神经导管。这些方法都不能保证许旺细胞在神经导管内的有序排列。 2.2.3 种子蛋白 许旺细胞基底膜对神经损伤后的再生起着重要作用,基底膜在轴突再生至神经远端的过程中起支架作用。而层粘连蛋白(laminin)是基底膜中的主要组成分子,其生物学功能首先表现为细胞粘连作用,通过细胞表面的laminin特异受体介导,结合于细胞表面或胶原,并与基膜中的各种大分子连成一个整体,因而在维持机制及将细胞锚定于基膜上起重要作用。此外,laminin是许旺细胞发育、增殖分化及形态建成中必不可少的调节蛋白。近期研究证实,laminin不仅保证了许旺细胞包绕轴突形成髓鞘,且在许旺细胞的发育及分化中起着关键作用[44]。Yu等[45-46]利用基因敲除技术敲除了许旺细胞中的laminin,进一步证实了突变体小鼠坐骨神经中的许旺细胞能正常向成髓鞘前体许旺细胞或成髓鞘许旺细胞分化,分化为非成髓鞘许旺细胞则受到抑制,且敲除laminin的突变体小鼠其许旺细胞的增值减少并影响了徐旺细胞的凋亡,见图5-9。"

不少组织工程实验研究证实,把laminin加入神经导管中对神经损伤修复有明显的促进神经再生的作用。Matsumoto等[47]将人胎盘laminin和胶原复合在聚乙醇酸支架上成功地桥接了犬的80 mm神经缺损。Cheng等[48]将laminin和鼠尾胶覆盖在可吸收材料上,发现许旺细胞增殖后能形成很好的Bungner带,产生更多的基质成分。使用laminin复合过的纳米银-胶原蛋白支架修复兔坐骨神经10 mm缺损,30 d后通过电生理、甲苯胺蓝和荧光金示踪技术证实坐骨神经通过神经支架的引导作用已经部分成功修复[49]。Verdu等[50]在用含有胶原或laminin的凝胶硅铜管来桥接6 mm长的小鼠坐骨神经缺损时发现:两者都能促进轴突再生并越过缺损成功长入远端,且laminin组在各种情况下都优于胶原组。因此,laminin与神经导管的组织工程技术的结合,成为周围神经损伤修复研究的热点"

| [1] Kim IY, Seo SJ, Moon HS,et al. Chitosan and its derivatives for tissue engineering applications. Biotechnol Adv. 2008; 26(1): 1-21.[2] Yao L, de Ruiter GC, Wang H, et al. Controlling dispersion of axonal regeneration using a multichannel collagen nerve conduit. Biomaterials. 2010;31(22):5789-5797.[3] Heath CA, Rutkowski GE.The development of bioartificial nerve grafts for peripheral-nerve regeneration.Trends Biotechnol. 1998;16(4):163-168.[4] Freed LE, Vunjak-Novakovic G, Biron RJ, et al. Biodegradable polymer scaffolds for tissue engineering. Biotechnology (N Y). 1994;12(7):689-693.[5] Kim BS, Mooney DJ. Development of biocompatible synthetic extracellular matrices for tissue engineering.Trends Biotechnol. 1998;16(5):224-230.[6] Lundborg G, Dahlin L, Dohi D, et al. A new type of "bioartificial" nerve graft for bridging extended defects in nerves. J Hand Surg Br. 1997;22(3):299-303.[7] Dellon AL, Mackinnon SE. An alternative to the classical nerve graft for the management of the short nerve gap. Plast Reconstr Surg. 1988;82(5):849-856.[8] Mackinnon SE, Dellon AL. Clinical nerve reconstruction with a bioabsorbable polyglycolic acid tube. Plast Reconstr Surg. 1990;85(3):419-424.[9] den Dunnen WF, van der Lei B, Schakenraad JM, et al. Poly(DL-lactide-epsilon-caprolactone) nerve guides perform better than autologous nerve grafts. Microsurgery. 1996; 17(7):348-357.[10] 张森林,孟昭业.含神经生长因子的几丁质管桥接兔面神经缺损的实验研究[J].中国修复重建外科杂志,2000,14(6):340-342.[11] Stanec S, Stanec Z. Reconstruction of upper-extremity peripheral-nerve injuries with ePTFE conduits. J Reconstr Microsurg. 1998;14(4):227-232.[12] Mao JS, Cui YL, Wang XH, et al. A preliminary study on chitosan and gelatin polyelectrolyte complex cytocompatibility by cell cycle and apoptosis analysis. Biomaterials. 2004;25 (18):3973-3981.[13] 矫树生,李兵仓,陈建梅,等.嗅鞘细胞与聚乳酸-聚羟基乙酸共聚物材料的细胞相容性研究[J].第三军医大学学报,2008,30(5): 370-373.[14] 苟三怀,侯春林,臧鸿声,等.几丁质室内植入雪旺氏细胞对神经再生影响的实验研究[J].中国修复重建外科杂志, 1995, 9(2):108.[15] Li BC, Jiao SS, Xu C,et al. PLGA conduit seeded with olfactory ensheathing cells for bridging sciatic nerve defect of rats. J Biomed Mater Res A. 2010;94(3):769-780.[16] 李志跃,李际才,赵群. 聚乳酸聚羟基乙酸共聚物三维神经导管修复周围神经缺损[J].中国组织工程研究与临床康复,2010, 14(34):6313-6318.[17] Cao W, Cheng M, Ao Q,et al. Physical, mechanical and degradation properties, and schwann cell affinity of cross-linked chitosan films.J Biomater Sci Polym Ed. 2005; 16(6):791-807.[18] Yuan Y, Zhang P, Yang Y, et al. The interaction of Schwann cells with chitosan membranes and fibers in vitro. Biomaterials. 2004;25(18):4273-4278.[19] 敖强,王爱军,孙志刚,等. 一种壳聚糖神经组织工程支架的制备及表征[J]. 中国组织工程研究与临床康复,2008,12(1):47-50.[20] Kotwal A, Schmidt CE. Electrical stimulation alters protein adsorption and nerve cell interactions with electrically conducting biomaterials. Biomaterials. 2001;22(10):1055-1064.[21] Schmidt CE, Shastri VR, Vacanti JP, et al. Stimulation of neurite outgrowth using an electrically conducting polymer. Proc Natl Acad Sci U S A. 1997;94(17):8948-8953.[22] De Giglio E, Sabbatini L, Zambonin PG. Development and analytical characterization of cysteine-grafted polypyrrole films electrosynthesized on Pt- and Ti-substrates as precursors of bioactive interfaces. J Biomater Sci Polym Ed. 1999;10(8):845-858.[23] Runge MB, Dadsetan M, Baltrusaitis J,et al. Development of Electrically Conductive Oligo(polyethylene glycol) Fumarate-Polypyrrole Hydrogels for Nerve Regeneration. Biomacromolecules. 2010. [Epub ahead of print][24] 赵金安.溶液共混法制备聚苯乙烯/多壁碳纳米管复合导电材料[J].化学研究与应用,2007,19(2):224-226.[25] Malarkey EB, Fisher KA, Bekyarova E, et al. Conductive single-walled carbon nanotube substrates modulate neuronal growth. Nano Lett. 2009;9(1):264-268.[26] Lee JY, Bashur CA, Goldstein AS,et al. Polypyrrole-coated electrospun PLGA nanofibers for neural tissue applications. Biomaterials. 2009;30(26):4325-4335.[27] Wang S, Cai Q, Hou J, et al. Acceleration effect of basic fibroblast growth factor on the regeneration of peripheral nerve through a 15-mm gap. J Biomed Mater Res A. 2003; 66(3):522-531.[28] Li WJ, Laurencin CT, Caterson EJ, et al. Electrospun nanofibrous structure: a novel scaffold for tissue engineering. J Biomed Mater Res. 2002;60(4):613-621.[29] Kwon IK, Kidoaki S, Matsuda T.Electrospun nano- to microfiber fabrics made of biodegradable copolyesters: structural characteristics, mechanical properties and cell adhesion potential.Biomaterials. 2005;26(18): 3929-3939.[30] Lee YH, Lee JH, An IG,et al. Electrospun dual-porosity structure and biodegradation morphology of Montmorillonite reinforced PLLA nanocomposite scaffolds. Biomaterials. 2005;26(16):3165-3172.[31] Currey J D.Bones:Structure and Mechanics. Princeton,NJ:Princeton University Press,2002.[32] Chang CJ.The effect of pulse-released nerve growth factor from genipin-crosslinked gelatin in schwann cell-seeded polycaprolactone conduits on large-gap peripheral nerve regeneration.Tissue Eng Part A. 2009;15(3):547-557.[33] Levi-Montalcini R.The nerve growth factor: thirty-five years later. EMBO J. 1987;6(5):1145-1154.[34] Petruska JC, Mendell LM.The many functions of nerve growth factor: multiple actions on nociceptors. Neurosci Lett. 2004; 361(1-3):168-171.[35] Campbell WW. Evaluation and management of peripheral nerve injury.Clin Neurophysiol. 2008;119(9):1951-1965.[36] Apfel SC, Kessler JA, Adornato BT, et al. Recombinant human nerve growth factor in the treatment of diabetic polyneuropathy. NGF Study Group. Neurology. 1998; 51(3): 695-702.[37] Luo J, West JR, Pantazis NJ. Nerve growth factor and basic fibroblast growth factor protect rat cerebellar granule cells in culture against ethanol-induced cell death. Alcohol Clin Exp Res. 1997;21(6):1108-1120.[38] Yang Y, De Laporte L, Rives CB, et al. Neurotrophin releasing single and multiple lumen nerve conduits. J Control Release. 2005;104(3):433-446.[39] Fisher J, Levkovitch-Verbin H, Schori H, et al. Vaccination for neuroprotection in the mouse optic nerve: implications for optic neuropathies. J Neurosci. 2001;21(1):136-142.[40] Sinis N, Schaller HE, Schulte-Eversum C, et al. Nerve regeneration across a 2-cm gap in the rat median nerve using a resorbable nerve conduit filled with Schwann cells. J Neurosurg. 2005;103(6):1067-1076.[41] Aszmann OC, Korak KJ, Luegmair M,et al. Bridging critical nerve defects through an acellular homograft seeded with autologous schwann cells obtained from a regeneration neuroma of the proximal stump. J Reconstr Microsurg. 2008; 24(3):151-158.[42] Bryan DJ, Wang KK, Chakalis-Haley DP. Effect of Schwann cells in the enhancement of peripheral-nerve regeneration. J Reconstr Microsurg. 1996;12(7):439-446.[43] Nadim W, Anderson PN, Turmaine M.The role of Schwann cells and basal lamina tubes in the regeneration of axons through long lengths of freeze-killed nerve grafts. Neuropathol Appl Neurobiol. 1990;16(5):411-421.[44] Yu WM, Yu H, Chen ZL. Laminins in peripheral nerve development and muscular dystrophy. Mol Neurobiol. 2007; 35(3):288-297.[45] Yu WM, Yu H, Chen ZL, et al. Disruption of laminin in the peripheral nervous system impedes nonmyelinating Schwann cell development and impairs nociceptive sensory function. Glia. 2009;57(8):850-859.[46] Yu WM, Feltri ML, Wrabetz L, et al. Schwann cell-specific ablation of laminin gamma1 causes apoptosis and prevents proliferation. J Neurosci.2005;25:4463-4472.[47] Matsumoto K, Ohnishi K, Sekine T, et al. Use of a newly developed artificial nerve conduit to assist peripheral nerve regeneration across a long gap in dogs. ASAIO J. 2000; 46(4):415-420.[48] Cheng B, Chen Z. Fabricating autologous tissue to engineer artificial nerve. Microsurgery. 2002;22(4):133-137.[49] 丁坦.纳米银组织工程外周神经支架对坐骨神经缺损修复的实验研究[D].西安:第四军医大学,2009.[50] Verdú E, Labrador RO, Rodríguez FJ,et al. Alignment of collagen and laminin-containing gels improve nerve regeneration within silicone tubes. Restor Neurol Neurosci. 2002;20(5):169-179.[51] Hung RJ, Yazdani U, Yoon J, et al. Mical links semaphorins to F-actin disassembly. Nature. 2010;463(7282):823-827.[52] Zheng L, Cui HF.Use of chitosan conduit combined with bone marrow mesenchymal stem cells for promoting peripheral nerve regeneration. J Mater Sci Mater Med. 2010;21(5): 1713-1720.[53] Jiang B, Zhang P, Jiang B.Advances in small gap sleeve bridging peripheral nerve injury. Artif Cells Blood Substit Immobil Biotechnol. 2010;38(1):1-4.[54] Shi W, Yao J, Chen X,et al. The delayed repair of sciatic nerve defects with tissue-engineered nerve grafts in rats. Artif Cells Blood Substit Immobil Biotechnol. 2010;38(1):29-37.[55] de Ruiter GC, Onyeneho IA, Liang ET, et al. Methods for in vitro characterization of multichannel nerve tubes. J Biomed Mater Res A. 2008;84(3):643-651.[56] Jiang B, Zhang P, Zhang D, et al. Study on small gap sleeve bridging peripheral nerve injury. Artif Cells Blood Substit Immobil Biotechnol. 2006;34(1):55-74. |
| [1] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [2] | Zeng Yanhua, Hao Yanlei. In vitro culture and purification of Schwann cells: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1135-1141. |
| [3] | Xu Dongzi, Zhang Ting, Ouyang Zhaolian. The global competitive situation of cardiac tissue engineering based on patent analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 807-812. |
| [4] | Wu Zijian, Hu Zhaoduan, Xie Youqiong, Wang Feng, Li Jia, Li Bocun, Cai Guowei, Peng Rui. Three-dimensional printing technology and bone tissue engineering research: literature metrology and visual analysis of research hotspots [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 564-569. |
| [5] | Chang Wenliao, Zhao Jie, Sun Xiaoliang, Wang Kun, Wu Guofeng, Zhou Jian, Li Shuxiang, Sun Han. Material selection, theoretical design and biomimetic function of artificial periosteum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 600-606. |
| [6] | Liu Fei, Cui Yutao, Liu He. Advantages and problems of local antibiotic delivery system in the treatment of osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 614-620. |
| [7] | Li Xiaozhuang, Duan Hao, Wang Weizhou, Tang Zhihong, Wang Yanghao, He Fei. Application of bone tissue engineering materials in the treatment of bone defect diseases in vivo [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 626-631. |
| [8] | Zhang Zhenkun, Li Zhe, Li Ya, Wang Yingying, Wang Yaping, Zhou Xinkui, Ma Shanshan, Guan Fangxia. Application of alginate based hydrogels/dressings in wound healing: sustained, dynamic and sequential release [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 638-643. |
| [9] | Chen Jiana, Qiu Yanling, Nie Minhai, Liu Xuqian. Tissue engineering scaffolds in repairing oral and maxillofacial soft tissue defects [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 644-650. |
| [10] | Xing Hao, Zhang Yonghong, Wang Dong. Advantages and disadvantages of repairing large-segment bone defect [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 426-430. |
| [11] | Chen Siqi, Xian Debin, Xu Rongsheng, Qin Zhongjie, Zhang Lei, Xia Delin. Effects of bone marrow mesenchymal stem cells and human umbilical vein endothelial cells combined with hydroxyapatite-tricalcium phosphate scaffolds on early angiogenesis in skull defect repair in rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3458-3465. |
| [12] | Wang Hao, Chen Mingxue, Li Junkang, Luo Xujiang, Peng Liqing, Li Huo, Huang Bo, Tian Guangzhao, Liu Shuyun, Sui Xiang, Huang Jingxiang, Guo Quanyi, Lu Xiaobo. Decellularized porcine skin matrix for tissue-engineered meniscus scaffold [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3473-3478. |
| [13] | Mo Jianling, He Shaoru, Feng Bowen, Jian Minqiao, Zhang Xiaohui, Liu Caisheng, Liang Yijing, Liu Yumei, Chen Liang, Zhou Haiyu, Liu Yanhui. Forming prevascularized cell sheets and the expression of angiogenesis-related factors [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3479-3486. |
| [14] | Li Xinping, Cui Qiuju, Zeng Shuguang, Ran Gaoying, Zhang Zhaoqiang, Liu Xianwen, Fang Wei, Xu Shuaimei. Effect of modification of β-tricalcium phosphate/chitosan hydrogel on growth and mineralization of dental pulp stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3493-3499. |
| [15] | Liu Chang, Li Datong, Liu Yuan, Kong Lingbo, Guo Rui, Yang Lixue, Hao Dingjun, He Baorong. Poor efficacy after vertebral augmentation surgery of acute symptomatic thoracolumbar osteoporotic compression fracture: relationship with bone cement, bone mineral density, and adjacent fractures [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3510-3516. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||