Chinese Journal of Tissue Engineering Research ›› 2019, Vol. 23 ›› Issue (34): 5523-5530.doi: 10.3969/j.issn.2095-4344.1970
Previous Articles Next Articles
Electroactive biomaterials in tissue engineering research
- 1School of Mechanical Engineering, Xinjiang University, Urumqi 830047, Xinjiang Uygur Autonomous Region, China; 2School of Mechanical Engineering, Xi'an Jiaotong University, Xi'an 710049, Shaanxi Province, China
-
Received:2019-06-20Online:2019-12-08Published:2019-12-08 -
Contact:Wang Kedian, Professor, Doctoral supervisor, School of Mechanical Engineering, Xinjiang University, Urumqi 830047, Xinjiang Uygur Autonomous Region, China; School of Mechanical Engineering, Xi'an Jiaotong University, Xi'an 710049, Shaanxi Province, China -
About author:Xiong Ying, Master, School of Mechanical Engineering, Xinjiang University, Urumqi 830047, Xinjiang Uygur Autonomous Region, China -
Supported by:the Natural Science Foundation of Xinjiang Uygur Autonomic Region, No. 2017D01C021 (to XY)
CLC Number:
Cite this article
Xiong Ying, Xu Yan, Zhou Jianping, Zhang Xujing, Wang Kedian. Electroactive biomaterials in tissue engineering research[J]. Chinese Journal of Tissue Engineering Research, 2019, 23(34): 5523-5530.
share this article
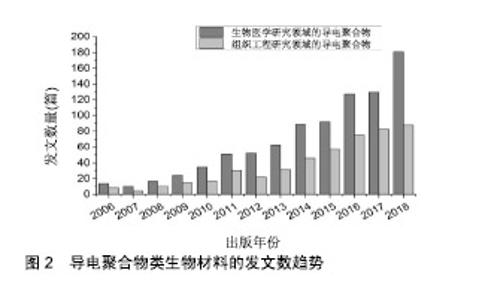
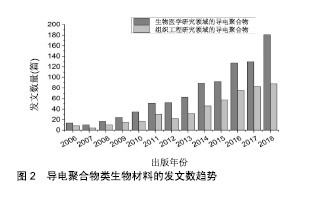
2.1 电活性生物材料的研究意义 生物材料作为组织修复与再生医学领域重要的研究内容,是生命科学、材料科学和工程技术等研发的重点和热点,也是实现组织器官构建与成功移植的前提[15]。生物材料的发展按其演变过程包括以下3个历程:首先是20世纪60年代,人们开发了第一代生物医学材料,这类材料因自身的“惰性”,始终为生物体的异已成分,所以并未能得到广泛的应用。为了解决第一代生物材料不与组织“生理性融合”的问题,20世纪80年代,第二代生物医学材料的研究完成了从“生物惰性”到“生物活性”的转变,并在进入21世纪时,相关研究人员开发了结合生物活性与生物可降解性能的第三代生物医学材 料[16]。虽然生物医学材料的发展完成了生物材料在组织工程应用研究中从短期“替代填充”到永久“替换修复”的突破,但依旧存在材料“生物性融合”欠佳,修复周期较长且不可控等问题[17]。为了解决上述问题,越来越多的生物医学材料被要求能仿生细胞或组织的微环境,最终实现对细胞黏附、增殖与分化以及组织结构和功能修复的调控[18]。 近年来,相关研究人员开始结合人体生物电系统,利用电活性生物材料对细胞直接传输电、电化学及机电信号,诱导细胞分化和组织再生,在组织再生领域中表现为如下优势:①可通过调控细胞生物电信号进而对组织结构和功能修复进行调控;②可监测细胞反应并通过生物电信号与宿主组织进行沟通交流。这些生物电信号可以反馈相关宿主响应于外部环境刺激的详细信息,最终根据反馈指导细胞的行为[19]。因此,电活性生物材料,如导电聚合物、压电材料和碳基材料已被广泛用作优良新型的支架材料。 2.2 电活性生物材料的性质及应用 导电聚合物、压电材料和碳基材料作为被广泛研究的3类电活性生物材料,在生物医学领域有着潜在的应用前景,已有研究证明,其在生物传感器、神经探针、药物释放的调节等方面具备应用潜力[20]。不仅如此,还可作为组织修复材料,与其他生物材料复合后弥补自身毒性较大、力学性能较差且不易降解的缺陷,最终有效诱导细胞分化和组织再生[21]。而这3类电活性生物材料因种类不同性质也有较大差别,在组织修复与再生医学领域的不同方面发挥各自独特的优势。下文分别具体介绍这3大类电活性生物材料的特性及在组织工程与再生医学研究领域的应用。 2.2.1 导电聚合物类生物材料 导电聚合物因易于制备,电学性能稳定、生物相容性良好以及可控释放生物分子等优势[22],从20世纪90年代起, 就开始被应用于生物医学研究相关领域。尤其是近十几年来,导电聚合物类生物材料的发文趋势反映出相关研究人员对其强烈的研究兴趣与热情,同时证明了导电聚合物作为生物材料的重要性及在组织修复方面的应用潜力,见图2。"
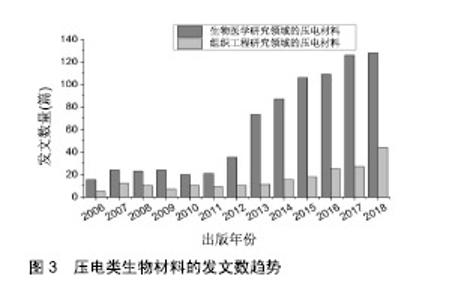
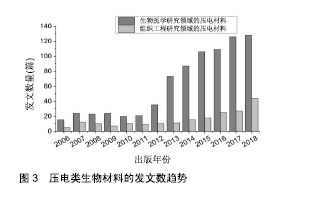
相关研究表明,神经、骨骼、肌肉和心肌细胞等对电脉冲有反应,因而有关导电聚合在组织工程研究中的应用主要涉及以上领域[23],且表现为如下应用潜力:①可在被施加电刺激的短时间内增加纤连蛋白的吸收[24];②可通过电刺激调节特定细胞的活动,并通过这种方式影响对电信号能做出反应的神经组织再生活动;③能将外部施加的电刺激集中在其周围区域,从而对加载的刺激进行空间调控[25]。当导电聚合物作为支架材料时,其作用机制表现如下:通过对外部施加的电刺激进行空间调控,使Na+在电刺激的作用下流入细胞内使细胞膜发生去极化,进而使Na+浓度增加促使线粒体释放Ca2+,从而促使细胞内Ca2+通道开放,增加细胞内游离Ca2+的浓度,最终促进DNA合成,加快细胞的分裂及增殖速度[26]。目前,以聚吡咯、聚苯胺及苯胺齐聚物为代表的导电聚合物已成为生物材料和组织工程领域关注的焦点[27]。 聚吡咯作为已知导电聚合物中被研究最多的聚合物,在刺激神经细胞、骨细胞再生、血管移植及体外肝脏培植等组织工程学领域的应用较为突出[28]。Ze 等[29]将聚吡咯作为支架材料培养PC12神经细胞,证明电刺激作用可以加快聚吡咯作为支架材料诱导神经细胞分化。Chen等[30]在铌酸钠钾压电陶瓷表面制备导电聚吡咯纳米阵列,用以模拟骨表面胶原纤维的电性能,并通过实验验证得出纳米阵列具有可接受的生物相容性,此外,纳米电场能够参与细胞行为的调控,且较高的表面电位能促进细胞增殖、附着和成骨分化。Ezazi等[31]采用浆液浇铸法制备了含导电聚吡咯聚合物的导电支架,并在支架上添加了模型抗生素万古霉素。通过对比含聚吡咯支架与不含聚吡咯支架在较长时间内的力学性能、蛋白吸附率及万古霉素释放率,最终发现含导电聚合物聚吡咯的支架表现出更优异的成骨性能。 与聚吡咯相比,聚苯胺在组织工程中的应用较晚,但其表面易通过改性处理,改变其诸如生物相容性及导电性等性能。而对聚苯胺表面改性的原理,简单而言就是在其表面引入功能基团,使两者发生共价键结合[32],最终实现相关功能的优化。Hu等[33]为提高聚苯胺的生物相容性,以壳聚糖为立体稳定剂对聚苯胺单体进行聚合,制备了一种表面功能化的聚苯胺-壳聚糖纳米复合材料,研究表明聚苯胺与壳聚糖之间存在相互作用,并随着复合材料中聚苯胺含量的增加,复合材料的导电率最高可达0.25 S/cm。Mohamadali等[34]以聚苯胺/聚丙烯腈共聚物为导电材料并对共聚物进行电纺丝后,用非热氧等离子体对其进行改性,采用扫描电镜、接触角、衰减全反射傅里叶变换红外光谱对支架进行表征,表征结果显示细胞在支架上增殖良好,具有良好的黏附性,纳米纤维可以支持细胞生长。虽然导电聚合物聚吡咯和聚苯胺在组织工程领域有较好的应用潜力,但其疏水性强、溶解性差,一般不可降解,长期存于生物体内会引发组织炎症,使其临床应用受到限制[35]。 因此,相关研究人员开发了导电高分子复合材 料——苯胺齐聚物。苯胺齐聚物不仅具有良好的生物相容性及生物可降解性,同时还有良好的电活性、可逆的氧化还原性及环境稳定性。许多报道表明,苯胺三聚体具有明确的电活性结构,良好的可加工性,易于降解,因而Xie等[36]将苯胺三聚体与星形聚乳酸通过交联剂合成制备了强电活性形状记忆聚合物,并通过qRT-PCR证明了此聚合物在碱性磷酸酶活性、免疫荧光染色、相关基因表达等方面可显著促进C2C12成肌细胞成骨分化的能力。不仅如此,还具有较强的机械性能及生物相容性,具有巨大的骨再生潜力。Zarrintaj等[37]通过结合琼脂糖和苯胺五聚物设计了可生物降解且导电的双功能电活性支架,通过植入PC12细胞检测该支架具有适当的细胞附着及相容性,且羧基包封的苯胺-五聚物提高了琼脂糖对细胞的黏附性,同时对细胞膜的传导性也达到了105 S/cm左右。Guo等[38]将苯胺齐聚物与线性聚已内酯进行共聚,采用溶剂浇筑/盐析方式制造出了管状、多孔的神经导管,并通过高倍电镜扫描与CT方式验证了该神经导管的多孔性符合组织工程应用的要求,不仅如此,上述苯胺齐聚物可被巨噬细胞吞噬、消化并由肾脏排出,减小了炎症反应与手术取出的风险。 2.2.2 压电类生物材料 使用压电材料作组织工程支架,具有如下优点:①可实现无需外加电源或植入电池就能增强生理电环境刺激的目的;②压电支架可通过瞬间变形产生电脉冲,且此瞬时变形通过细胞的附着、迁移或身体运动就能被施加[39]。不仅如此,压电类生物材料具有在体内模拟静态和动态微环境的能力,因而在20世纪80年代,就被提出用来修复骨组织缺损[40]。根据近十几年内压电类生物材料发文趋势的统计与分析,不难发现压电材料的研究热度在逐年上升,显示出其在生物医学研究中的重要性及应用潜力,见图3。而聚偏氟乙烯、无铅压电陶瓷及左旋聚乳酸等压电材料因具有较大的压电效应及较好的生物相容性,自然在诸如神经损伤修复、骨形成和创伤愈合等研究领域发挥着重要作用[39]。"
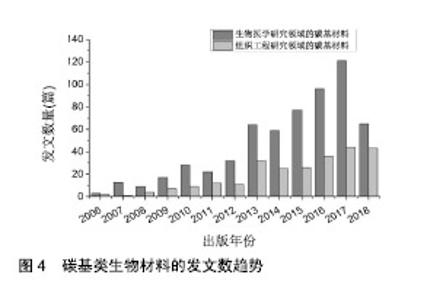
聚偏氟乙烯作为一种多晶型聚合物,常见的晶型主要有α、β及γ3种。其中α- 聚偏氟乙烯不显示压电性,但可通过通过机械拉伸或电场极化转变为压电性很强的β-聚偏氟乙烯[41]。不仅如此,Martins等[42]证明了聚偏氟乙烯支架的负电荷表面能促进成肌细胞更好的黏附和增殖,在骨骼肌的再生中有很好的应用前景。Ribeiro等[43]也通过实验证明了聚偏氟乙烯支架在很大程度上能促进人脂肪源性干细胞的成骨分化,即电活性膜可以为特定细胞的分化提供必要的机电刺激,从而支持合适的组织工程策略设计,特别是骨组织工程的设计。Li等[44]研究了新型氧化锌/聚偏氟乙烯支架对成骨细胞和细菌的影响,发现压电材料可以作为生物活性带电表面诱导骨组织再生,且随着成骨细胞密度增加,细菌明显减少,显示了氧化锌/聚偏氟乙烯新型支架具有很强的组织修复及抗菌潜力。 压电陶瓷作为压电材料中不可忽视的一部分,也表现出了在骨组织工程研究领域极高的应用潜力。但其制备过程较复杂,一般需经固相烧结粉体后得到无规则多晶体,然后进一步通过人工极化才能表现出较强的压电性。随着近年来生物材料的安全性被更多的关注,以钛酸钡和铌酸锂钠钾为代表的无铅压电陶瓷材料及复合材料显现出了在组织工程研究领域极高的关注度[45]。Zhang等[46]采用冷冻铸造羟基磷灰石/钛酸钡悬浮液,以制备定向多孔压电复合支架,实验表明随着悬浮液固体载荷和凝固速度的增加,压电系数d33得到改善。同时,制备支架使用的双模板法,能使板层孔隙和对齐的宏观孔隙共存,且该方法操作灵活,在骨替代物的应用中具有定制化需求的潜力。Wang 等[47]采用冷等静压法制备多孔铌酸锂钠钾试样。并通过扫描电镜和MTT法研究了该试样对新生大鼠头盖骨成骨细胞黏附和增殖的影响,结果显示冷等静压法增强了铌酸盐样品的压电性和生物性能,并促进了其胞外基质样形貌。 不同于以上2类压电材料,左旋聚乳酸因不需烧结、不需极化便可产生压电效应且降解性能优异,因此具有更加广阔的应用前景。Ikada等[48]将左旋聚乳酸制成薄膜和棒材,沿纵向拉伸赋予其压电特性后植入动物体内实验,实验结果显示随着左旋聚乳酸棒材拉伸比的增加,损伤组织处有明显的愈合趋势,而未拉伸即不具备压电效应的左旋聚乳酸棒材反而会延缓损伤组织的愈合。Rad等[49]以结晶聚乳酸和多壁碳纳米管为材料,采用热诱导相分离方法制备了具有微管定向结构的可生物降解多孔纳米复合材料支架,用其作为神经组织工程的模型,在2周内以小鼠P-19细胞系为合适的模型系统进行体外研究,采用免疫荧光法和DAPI染色法检测细胞在左旋聚乳酸/多壁碳纳米管纳米复合材料支架上的附着和分化情况,最终证明了左旋聚乳酸/多壁碳纳米管支架确实增强了神经细胞的分化和增殖。Liumin等[50]采用静电纺丝法制备了左旋聚乳酸纳米纤维,并对其表面进行了层粘连蛋白/壳聚糖聚电解质多层改性,研究显示层粘连蛋白修饰的左旋聚乳酸支架能显著诱导DRG神经元和神经干细胞的神经元突生长,且层粘连蛋白的吸附有助于促进细胞增殖。此外左旋聚乳酸经水解降解,副产物为无毒且水溶性好的乳酸,因而具有潜在的应用优势[51]。 2.2.3 碳基类生物材料 碳基材料如石墨烯、氧化石墨烯(石墨烯衍生物)及碳纳米管,因具有良好的导电性能、生物相容性,较高的机械强度,以及促进组织再生能力及抗菌等性能[52],近年来在组织工程与再生医学领域被普遍关注。根据碳基材料近十年来在生物医学研究领域的发文数,不难发现其呈现先增加后降低的趋势,但其在组织工程研究领域的热度近几年来一直在增加,见图4。"
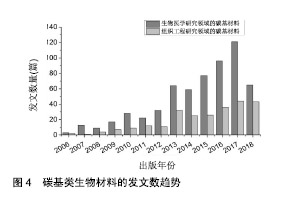
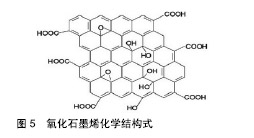
作为一种呈二维结构的纳米材料,石墨烯具有独特的电子特性、力学性能[53],以及在一定浓度下良好的生物相容性,可支撑细胞的黏附、增殖和分化。除此之外,石墨烯可与多种活性材料结合,从而设计出具备优异特性的材料[54]。Yi等[55]利用静电纺丝技术制备了丝素蛋白和石墨烯组成的导电纤维支架材料,发现当石墨烯质量分数为3%时,复合材料纤维支架具有较好的电活性(导电性)和力学性能。Golafshan等[56]用混合石墨烯纳米 片-海藻酸钠/聚乙烯醇制备具有优异韧性和导电性的神经组织工程纤维支架,发现质量分数为1%的混合石墨烯能明显提高支架的导电性及支持PC12细胞附着和扩散的潜力。氧化石墨烯是石墨烯的衍生物,其结构与石墨烯基本相同,且含有羟基(-OH)、羧基(-COOH)和羰基(-CO-),因此具有良好的亲水性,能提供更大的表面积且表面活性更强,同时其边缘的羟基(-OH)、羧基(-COOH)易于其他材料通过静电力结合,因而具有广阔的应用前景,其结构式如图5所示。 Jing等[57]以壳聚糖/氧化石墨烯复合水凝胶为研究对象,结合肌源性蛋白多巴胺制备了具有自粘性、自愈性和导电性的复合水凝胶,结果发现壳聚糖/氧化石墨烯的导电性可达到1.22 mS/cm,能增强人胚胎干细胞来源的成纤维细胞和心肌细胞的细胞活力与增殖能力。Feng等[58]采用可控组装技术制备了用于检测神经元活性的软石墨烯纳米纤维,此纤维具有可恢复的导电性及良好的物理化学稳定性,同时利用此纤维进行细胞电刺激可避免传统二维导电材料长期电刺激对神经生长发育的抑制作用。Annabi等[59]以甲基丙烯酰和氧化石墨烯纳米粒子为原料制备了一种高弹性的混合水凝胶,用作心脏组织工程的导电生物材料,通过实验证实氧化石墨烯纳米颗粒的加入可增加凝胶的导电性、力学性能及表面粗糙度,在心脏组织工程中具有广阔的利用前景。 碳纳米管是一种径向尺寸为纳米量级、轴向尺寸可达微米量级的一维量子材料,具有典型的层状中空结构特征。由于其独特的结构,碳纳米管具有机械强度高、电性能强、质量极轻、导热性强,表面积大等优点。Qingsu等[60]用溶剂浇铸/颗粒浸出支架制作而成碳纳米管/聚乳酸羟基乙酸复合支架,研究显示复合支架具有良好的机械强度,且碳纳米管的加入增加了电活性支架表面的粗糙度,导致成骨细胞的附着和增殖增加。关于心脏组织再生,Ahadian等[61]报道了碳纳米管在制造导电和机械强度高的聚合物支架中的应用,将聚合物-碳纳米管材料预聚体注入模具,在紫外光下交联构建复杂的支架结构,结果表明碳纳米管增强了弹性聚合物的导电性和结构支撑;与纯聚合物支架相比,含有0.5%碳纳米管的混合聚合物支架可促进在其上制备的心脏组织的成熟;同时,复合聚合物-碳纳米管支架上的心脏组织比纯聚合物支架上的心脏组织跳动更早。刘耀文等[62]针对心肌细胞的特点,通过将不同比例多壁碳纳米管加入聚乳酸溶液中制备出具有良好力学和导电性能的聚乳酸/多壁碳纳米管复合纤维膜,通过观察心肌细胞在纤维膜上的生长行为,发现多壁碳纳米管质量分数为3%的支架表现出最佳的力学和导电性能,能够确保心肌细胞的动作电位能迅速准确地通过纤维支架进行传导。碳纳米材料在组织工程领域的应用前景较好,但对其在生物体内的长期安全性一直没得到实验认可,进一步应用于临床仍需谨慎。 "
| [1]Ishikawa K,Ueyama Y,Mano T,et al.Self‐setting barrier membrane for guided tissue regeneration method: Initial evaluation of alginate membrane made with sodium alginate and calcium chloride aqueous solutions.J Biomed Mater Res. 2015;47(2):111-115.[2]白玉龙,高玉凤,衷鸿宾,等.同种异体及异种组织修复材料:如何选用适宜的病毒灭活工艺[J].中国组织工程研究, 2019,23(14): 2261-2268.[3]颜永年,李生杰,熊卓,等.基于快速原型的组织工程支架成形技术[J].机械工程学报,2010,46(5):93-98.[4]张治金,曾林如,朱芳兵,等.组织工程修复软骨缺损的研究进展[J].中国医药导报,2017,14(20):36-9,61.[5]邢飞,李浪,刘明,等.原位组织工程技术在骨与软骨修复领域的应用进展[J].中国修复重建外科杂志,2018,32(10):1358-1363.[6]黄明华,陈庆华,刘美红,等.组织工程支架材料研究进展及发展趋势[J].材料导报,2006,20(S2):365-368.[7]伍权华,陈旭翔,汪蕾,等.心脏脱细胞基质支架的制备及临床应用前景[J].中国组织工程研究,2018,22(6):964-970.[8]刘鑫,齐磊,左明星,等.天然生物材料在组织工程和再生医学中的应用[J].医疗卫生装备,2019,40(3):98-103.[9]毛文文,茹江英.羟基磷灰石类陶瓷在骨组织工程中的研究与更广泛应用[J].中国组织工程研究,2018,22(30):4855-4863.[10]Webber MJ,Khan OF,Sydlik SA,et al.A Perspective on the Clinical Translation of Scaffolds for Tissue Engineering.Ann Biomed Eng.2015;43(3):641-656.[11]Brown RT.Topics in applied physics.Proc IEEE. 1980;68(3): 429.[12]Guimard NK,Gomez N,Schmidt CE.Conducting polymers in biomedical engineering.Prog Polym Sci.2007;32(8):876-921.[13]Compton OC,Nguyen SBT.Graphene oxide, highly reduced graphene oxide, and graphene: versatile building blocks for carbon-based materials.Small.2010;6(6):711-723.[14]Finkenstadt V, Willett JL.Preparation and Characterization of Electroactive Biopolymers Macromol Symp. 2010;227(1): 367-372.[15]于洋.组织工程材料:支撑人类“再生”梦[EB/OL]. [2019-04-09]. http://www.cnpharm.com/content/201904/09/c275409.html[16]梅昕,马凤森,喻炎,等.高分子可降解生物材料的降解研究进展[J].材料导报,2016,30(S1):298-303.[17]王秀梅.生物材料[J].新型工业化,2015,5(12):37-68.[18]姜玉峰,胡添,付小兵.组织再生材料:从基础研究创新到临床转化应用[J].科学通报,2018,63(21):2111-2115.[19]Tandon B,Magaz A,Balint R,et al.Electroactive biomaterials: Vehicles for controlled delivery of therapeutic agents for drug delivery and tissue regeneration.Adv Drug Deliv Rev. 2018; 129:148-168.[20]邬海涛,于婷,朱庆三,等.电活性可生物降解纳米复合材料PAP/ op-HA/PLGA的制备及成骨活性[J].高等学校化学学报, 2011, 32(5):1181-1187.[21]Balint R,Cassidy NJ,Cartmell SH.Conductive polymers: towards a smart biomaterial for tissue engineering.Acta Biomater.2014;10(6):2341-2353.[22]邹东恢,梁敏.新型功能材料导电聚合物在生物医药工业中的应用[J].河南化工,2013,30(1):24-27.[23]Guimard NK,Gomez N,Schmidt CE.Conducting polymers in biomedical engineering.Prog Polym Sci. 2007;32(8-9): 876-921.[24]Kotwal A,Schmidt CE.Electrical stimulation alters protein adsorption and nerve cell interactions with electrically conducting biomaterials. Biomaterials. 2001;22(10): 1055-1064.[25]Guarino V,Alvarez-Perez MA,Borriello A,et al.Conductive PANi/PEGDA macroporous hydrogels for nerve regeneration.Adv Healthc Mater.2013;2(1):218-227.[26]Stewart E,Kobayashi NR,Higgins MJ,et al.Electrical Stimulation Using Conductive Polymer Polypyrrole Promotes Differentiation of Human Neural Stem Cells: A Biocompatible Platform for Translational Neural Tissue Engineering.Tissue Eng Part C Methods.2015;21(4):385.[27]Rajesh, Ahuja T, Kumar D.Recent progress in the development of nano-structured conducting polymers/ nanocomposites for sensor applications.Sens Actuator B-Chem. 2009;136(1):275-286.[28]危岩,李保松,付长奎,等.电活性导电聚合物在生物医学中的应用[J].高分子学报,2010,54(12):1399-1405.[29]Ze Z,Mahmoud R,Zhaoxu W,et al.Electrically conductive biodegradable polymer composite for nerve regeneration: electricity-stimulated neurite outgrowth and axon regeneration. Artif Organs.2010;31(1):13-22.[30]Chen J,Li W,Lei Z,et al.Built-in Electric Field with Nanoscale Distinction for Cell Behavior Regulation.J Mat Chem B. 2018; 6(18).DOI: 10.1039/C8TB00063H[31]Ezazi NZ,Shahbazi MA,Shatalin YV,et al.Conductive vancomycin-loaded mesoporous silica polypyrrole-based scaffolds for bone regeneration.Int J Pharm. 2017;536(1): 241.[32]Yslas EI,Cavallo P,Acevedo DF,et al.Cysteine modified polyaniline films improve biocompatibility for two cell lines.Mater Sci Eng C-Mater Biol Appl.2015;51(3):51-56.[33]Hu J,Huang L,Zhuang X,et al.Electroactive aniline pentamer cross-linking chitosan for stimulation growth of electrically sensitive cells. Biomacromolecules.2008;9(10): 2637.[34]Mohamadali M,Irani S,Soleimani M,et al.PANi/PAN copolymer as scaffolds for the muscle cell‐like differentiation of mesenchymal stem cells.Polym Adv Technol.2017;28(9).DOI:10.1002/pat.4000[35]Ravichandran R,Sundarrajan S,Venugopal JR,et al.Applications of conducting polymers and their issues in biomedical engineering.J R Soc Interface.2010;7 Suppl 5(Suppl_5):S559-579.[36]Xie M, Wang L, Ge J, et al.Strong electroactive biodegradable shape memory polymer networks based on star-shaped polylactide and aniline trimer for bone tissue engineering. ACS Appl Mater Interfaces.2015;7(12): 6772-6781.[37]Zarrintaj P,Bakhshandeh B,Rezaeian I,et al.A Novel Electroactive Agarose-Aniline Pentamer Platform as a Potential Candidate for Neural Tissue Engineering. Sci Rep. 2017;7(1):17187.[38]Guo B,Sun Y,Finne-Wistrand A,Mustafa K,et al. Electroactive porous tubular scaffolds with degradability and non-cytotoxicity for neural tissue regeneration.Acta Biomater. 2012;8(1):144-153.[39]Rajabi AH,Jaffe M,Arinzeh TL.Piezoelectric materials for tissue regeneration: A review.Acta Biomater.2015;24:12-23.[40]Tandon B,Blaker JJ,Cartmell SH.Piezoelectric materials as stimulatory biomedical materials and scaffolds for bone repair. Acta Biomater.2018;73:1-20.[41]Ohigashi H,Koga K,Suzuki M,et al.Piezoelectric and ferroelectric properties of P (VDF-TrFE) copolymers and their application to ultrasonic transducers.Ferroelectrics. 1984;60(1):263-276.[42]Martins PM,Ribeiro S,Ribeiro C,et al.Effect of poling state and morphology of piezoelectric poly(vinylidene fluoride) membranes for skeletal muscle tissue engineering.RSC Adv. 2013;3(39):17938-17944.[43]Ribeiro C,Pärssinen J,Sencadas V,et al.Dynamic piezoelectric stimulation enhances osteogenic differentiation of human adipose stem cells.J Biomed Mater Res A. 2015;103(6):2172-2175.[44]Li Y, Sun L,Webster TJ.The Investigation of ZnO/Poly (vinylidene fluoride) Nanocomposites with Improved Mechanical, Piezoelectric, and Antimicrobial Properties for Orthopedic Applications.J Biomed Nanotechnol. 2018; 14(3):536-545.[45]倪海民.无铅/少铅压电材料的制备与压电性能研究[D].宁波:宁波大学,2011.[46]Zhang Y,Chen L,Zeng J,et al.Aligned porous barium titanate/hydroxyapatite composites with high piezoelectric coefficients for bone tissue engineering. Mater Sci Eng C Mater Biol Appl.2014;39(1):143-149.[47]Wang Q,Yang J,Zhang W,et al.Manufacture and Cytotoxicity of a Lead-free Piezoelectric Ceramic as a Bone Substitute- Consolidation of Porous Lithium Sodium Potassium Niobate by Cold Isostatic Pressing.Int J Oral Sci. 2009;1(2):99-104.[48]Ikada Y,Shikinami Y,Hara Y,et al.Enhancement of bone formation by drawn poly(L-lactide).J Biomed Mater Res B Appl Biomater.2015;30(4):553-558.[49]Rad SM, Khorasani MT, Joupari MD.Preparation of HMWCNT/PLLA nanocomposite scaffolds for application in nerve tissue engineering and evaluation of their physical, mechanical and cellular activity properties.Polym Adv Technol. 2016;27(3):325-338.[50]Liumin H,Shuo T, Prabhakaran MP,et al.Surface Modification of PLLA Nano-scaffolds with Laminin Multilayer by LbL Assembly for Enhancing Neurite Outgrowth. Macromol Biosci. 2013;13(11):1601-1609.[51]王宇飞,郭占林.可吸收肋骨内固定装置的研究现状[J].中华胸部外科电子杂志,2018,5(1):47-52.[52]张金超,杨康宁,张海松,等.碳纳米材料在生物医学领域的应用现状及展望[J].化学进展,2013,25(Z1):397-408.[53]Bai J,Xing Z,Shan J,et al.Graphene nanomesh.Nat Nanotechnol. 2010;5(3):190-194.[54]张文毓,全识俊.石墨烯应用研究进展[J].传感器世界,2011, 17(5):6-11.[55]Yi Y,Ding X,Zou T,et al.Preparation and characterization of electrospun graphene/silk fibroin conductive fibrous scaffolds. RSC Adv.2017;7(13):7954-7963.[56]Golafshan N,Kharaziha M,Fathi MH.Tough and conductive hybrid graphene-PVA: Alginate fibrous scaffolds for engineering neural construct.Carbon.2017;111:752-763.[57]Jing X,Mi HY,Napiwocki BN,et al.Mussel-inspired electroactive chitosan/graphene oxide composite hydrogel with rapid self-healing and recovery behavior for tissue engineering.Carbon.2017;125:557-570.[58]Feng ZQ,Wang T,Zhao B,et al.Soft Graphene Nanofibers Designed for the Acceleration of Nerve Growth and Development.Adv Mater.2015;27(41):6462-6468.[59]Annabi N,Shin SR,Tamayol A,et al.Highly Elastic and Conductive Human-Based Protein Hybrid Hydrogels.Adv Mater.2016;28(1):40-49.[60]Qingsu C, Katy R, Ehsan J.Carbon nanotube-poly (lactide-co-glycolide) composite scaffolds for bone tissue engineering applications.Ann Biomed Eng. 2013;41(5): 904-916.[61]Ahadian S,Huyer LD,Estili M,et al.Moldable elastomeric polyester-carbon nanotube scaffolds for cardiac tissue engineering.Acta Biomater.2016;52:81-91.[62]刘耀文,王淑瑶,叶劲松,等.聚乳酸/碳纳米管导电复合纤维用于心肌组织工程的研究[J].化工新型材料, 2016,44(2):216-218. |
| [1] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [2] | Zeng Yanhua, Hao Yanlei. In vitro culture and purification of Schwann cells: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1135-1141. |
| [3] | Xu Dongzi, Zhang Ting, Ouyang Zhaolian. The global competitive situation of cardiac tissue engineering based on patent analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 807-812. |
| [4] | Wu Zijian, Hu Zhaoduan, Xie Youqiong, Wang Feng, Li Jia, Li Bocun, Cai Guowei, Peng Rui. Three-dimensional printing technology and bone tissue engineering research: literature metrology and visual analysis of research hotspots [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 564-569. |
| [5] | Chang Wenliao, Zhao Jie, Sun Xiaoliang, Wang Kun, Wu Guofeng, Zhou Jian, Li Shuxiang, Sun Han. Material selection, theoretical design and biomimetic function of artificial periosteum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 600-606. |
| [6] | Liu Fei, Cui Yutao, Liu He. Advantages and problems of local antibiotic delivery system in the treatment of osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 614-620. |
| [7] | Li Xiaozhuang, Duan Hao, Wang Weizhou, Tang Zhihong, Wang Yanghao, He Fei. Application of bone tissue engineering materials in the treatment of bone defect diseases in vivo [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 626-631. |
| [8] | Zhang Zhenkun, Li Zhe, Li Ya, Wang Yingying, Wang Yaping, Zhou Xinkui, Ma Shanshan, Guan Fangxia. Application of alginate based hydrogels/dressings in wound healing: sustained, dynamic and sequential release [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 638-643. |
| [9] | Chen Jiana, Qiu Yanling, Nie Minhai, Liu Xuqian. Tissue engineering scaffolds in repairing oral and maxillofacial soft tissue defects [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 644-650. |
| [10] | Li Jun, Zuo Xinhui, Liu Xiaoyuan, Zhang Kai, Han Xiangzhen, He Huiyu, . Effect of over expression of miR-378a on osteogenic and vascular differentiation of bone marrow mesenchymal stem cell sheet [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(31): 4939-4944. |
| [11] | Xing Hao, Zhang Yonghong, Wang Dong. Advantages and disadvantages of repairing large-segment bone defect [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 426-430. |
| [12] | Wang Hao, Chen Mingxue, Li Junkang, Luo Xujiang, Peng Liqing, Li Huo, Huang Bo, Tian Guangzhao, Liu Shuyun, Sui Xiang, Huang Jingxiang, Guo Quanyi, Lu Xiaobo. Decellularized porcine skin matrix for tissue-engineered meniscus scaffold [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3473-3478. |
| [13] | Mo Jianling, He Shaoru, Feng Bowen, Jian Minqiao, Zhang Xiaohui, Liu Caisheng, Liang Yijing, Liu Yumei, Chen Liang, Zhou Haiyu, Liu Yanhui. Forming prevascularized cell sheets and the expression of angiogenesis-related factors [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3479-3486. |
| [14] | Liu Chang, Li Datong, Liu Yuan, Kong Lingbo, Guo Rui, Yang Lixue, Hao Dingjun, He Baorong. Poor efficacy after vertebral augmentation surgery of acute symptomatic thoracolumbar osteoporotic compression fracture: relationship with bone cement, bone mineral density, and adjacent fractures [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3510-3516. |
| [15] | Liu Liyong, Zhou Lei. Research and development status and development trend of hydrogel in tissue engineering based on patent information [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3527-3533. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||