Chinese Journal of Tissue Engineering Research ›› 2018, Vol. 22 ›› Issue (17): 2783-2788.doi: 10.3969/j.issn.2095-4344.0509
Latest advances in high-throughput cell capture and arrangement
Hun Ting-ting1, 2, 3, Qiu Chang-jun1, 2, Zhao Ying-tong1, 2, Zhao Feng1, 2, He Jing-wen1, 2, Sun Yan1, 2, 3
- 1Key Laboratory for Biomechanics and Mechanobiology of Ministry of Education, School of Biological Science and Medical Engineering, Beihang University, Beijing 100083, China; 2Beijing Advanced Innovation Center for Biomedical Engineering, Beihang University, Beijing 102402, China; 3Shanghai Institute of Microsystem and Information Technology, Chinese Academy of Sciences, Shanghai 200050, China
-
Revised:2018-01-15Online:2018-06-18Published:2018-06-18 -
Contact:Sun Yan, M.D., Master’s supervisor, Associate professor, Key Laboratory for Biomechanics and Mechanobiology of Ministry of Education, School of Biological Science and Medical Engineering, Beihang University, Beijing 100083, China; Beijing Advanced Innovation Center for Biomedical Engineering, Beihang University, Beijing 102402, China; Shanghai Institute of Microsystem and Information Technology, Chinese Academy of Sciences, Shanghai 200050, China -
About author:Hun Ting-ting, Master candidate, Key Laboratory for Biomechanics and Mechanobiology of Ministry of Education, School of Biological Science and Medical Engineering, Beihang University, Beijing 100083, China; Beijing Advanced Innovation Center for Biomedical Engineering, Beihang University, Beijing 102402, China; Shanghai Institute of Microsystem and Information Technology, Chinese Academy of Sciences, Shanghai 200050, China -
Supported by:the National Natural Science Foundation of China, No. 31470942
CLC Number:
Cite this article
Hun Ting-ting, Qiu Chang-jun, Zhao Ying-tong, Zhao Feng, He Jing-wen, Sun Yan. Latest advances in high-throughput cell capture and arrangement[J]. Chinese Journal of Tissue Engineering Research, 2018, 22(17): 2783-2788.
share this article
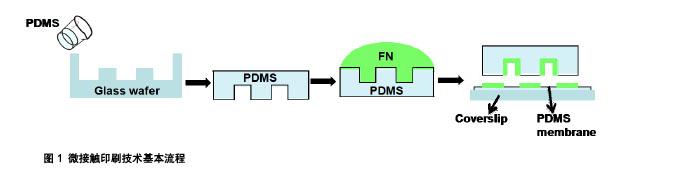
2.1 微流控技术 微流控技术(Microfluidics)是指使用尺寸为数十到数百微米的微管道处理或操纵体积为纳升或微升的微小流体所涉及的科学与技术。因为具有微型化、集成化等芯片的特征,微流控装置又被称为微流控芯片,或称为芯片实验室(Lab on a Chip)和微全分析系统(micro-Total Analytical System)。微流控装置不仅可以用来进行细胞捕获和排列,也可以用来后续细胞的体外培养。目前,微流控被认为在生物医学研究中具有巨大的发展潜力和广泛的应用前景,可用于单细胞捕获、细胞配对、细胞融合、细胞分选等很多领域。 微通道的作用主要是利用毛细管力、压力或电渗透力作用向基底的指定区域驱动流体,优点在于微流体为化合物的浓度提供了高空间和时间分辨率的精准定义。这为微小化精确控制细胞及分子等周围环境提供了一定的可能性[12],其优点是反应快、样品节约、占用体积小、高通量且结果较为精确等。但是相比较而言缺点也十分明显,如单细胞捕获率较低,细胞的进样系统较为复杂,操作有一定难度且芯片内产物难以再回收利用等,这些问题的存在使得微流控技术在单分子、单细胞的后续培养和研究上造成很大阻碍。目前的研究主要集中在利用微流控的流体驻点效应和通道固有的边界效应对单细胞进行捕获和排列。 利用流体驻点效应来捕获单细胞的方法可以对捕获的单细胞有效地加载动态生化信号便于后续研究[13]。但缺点是驻点位置不稳定性使得捕获后细胞处于不稳定状态,从而不利于长时间研究、观察、检测和分析;一些实验通过外加反馈控制系统来增强捕获的稳定性,但由于增加了外部控制装置,使装置的复杂性进一步加大[14-15]。除此之外利用通道的边界效应捕获单细胞的方法可以解决这一问题,且操作简单、成本低、易形成阵列型结构来高效捕获单细胞,但缺点是不便于对单细胞后续铺展及信号加载研究[1]。 2.1.1 物理驱动微流控技术 Toriello等[16]利用电场驱动法进行单细胞的捕获,先用已合成的含有巯基的九肽(CCRRGD-WLC)来标记中国仓鼠的卵巢细胞(CHO cells),再将标记的细胞引流进入微通道中,通过金太极与被标记的细胞结合形成金硫键来检测细胞捕获的效果。Arakawa等[17]则通过设计了一些捕获口袋,在蛇形通道两侧进行单细胞捕获,当细胞悬浮液流经通道时,这些直径20 μm的捕获口袋便可以捕获细胞并进行后续荧光标记、细胞裂解及内含物的检测。相似的研究还有设计一系列串联的T和反T型结对组成为核心陷阱结构[18],起到旁路通道和俘获收缩的作用。这个设备不需要部署很长和很复杂的通道来调整流动阻力,从而为每个捕集节省空间单元,陷阱以“确定性”的方式工作,从而节省了大量细胞样品并且紧凑的结构允许细胞在多个通道中的流动路径更短,因此增加了细胞捕获的速度和吞吐量。就目前看微流控进行单细胞捕获有着非常好的应用前景。例如在神经细胞间传递细胞递质、体外受精以及细胞间相互作用的相关研究。 2.1.2 微流体液滴技术 微流体液滴技术是通过将单细胞包裹在单位体积液滴内进行单细胞分析。液滴作为离散的微反应器,将细胞、反应物和产物包裹在一个狭小的区域内进行分析,能够有效地限制扩散,加速混合,降低样品消耗,已被成功应用于多种单细胞分析中。基于液滴的单细胞测定将单个细胞封装并限制在单个液滴中,使用高度全面的细胞毒性筛选和其他核酸测序实现全基因组表达谱分析。目前大多数实验的挑战在于随机性较强,且依靠泊松分布或者流体力学相关原理。 常用的微流体液滴技术依赖于曲面通道或者很长的微通道[19],这种方法需要固定间隔,高密度细胞及细胞和液滴的完美匹配。还有一些活性方法,利用激光诱发光子捕获和微喷射技术,这种方法的缺点是低通量[20-21]。相对应的惰性方法直接分散细胞到单个液滴。相关应用瑞 丽-泰勒不稳定性射流断裂作用可捕获细胞高达79.2%。但是这是一个复杂现象,依赖流量面、毛细数及剪切方式等[22]。这些方法前期投入较大,并且需要较为复杂的实验设备。Kamalakshakurup等[23]研究人员利用一个界面流体动力学技术制作了一个三维的微漩涡,提供了分散相和连续相的交接处。这项实验首先将细胞捕获在微漩涡中,随后再将它们释放到微滴中,由分离涡旋的外部流线的宽度来控制细胞液滴从靠近水-油界面的流动通道流出,从而控制每个液滴只有1个细胞。这种技术在细胞分选及细胞分装上都有很大的优势,且仅需要较低的细胞浓度即可应用于细胞排列等多个方面。 2.2 微接触印刷技术 微图案印刷技术是制备表面微图案获取细胞的常用方法之一,最初它建立并应用于微电子学中。之后,随着技术的改进与发展,微图案印刷技术广泛应用于医学和细胞生物学,为细胞的图案化提供合适的基底。该技术的优点是操作简单、方便观察、无需严格的实验室环境,所需的基底和材料制作成本较低,并且可能实现精确地平面表面图案化和非平面图案化。微接触印刷技术近几年内成为很多研究者在材料-细胞间相互作用、生物配体-受体间特异性识别及生物芯片制备新技术等方面研究的必要工具。 技术原理是通过软光刻技术制备具有微图案结构的硅片,在硅片表面浇注液相聚合物待其加热固化后,从硅片模具上剥离下来形成具有弹性的聚二甲基硅氧烷(PDMS)印章;在聚二甲基硅氧烷表面孵育有活性的蛋白分子,使蛋白沉降在图案化表面,再通过微接触印刷在基底上形成亲细胞和疏细胞的蛋白区域,使用封闭因子Pluronic F127封闭非图案位点后接种细胞,细胞便选择性的黏附在局部表面蛋白区域,如图1。不同细胞需要的黏附区域大小不同,过小会限制细胞的生长使细胞死亡,过大又会黏附2个或者2个以上的多细胞[24-25]。 研究表明在传统微接触印刷实验中1 200 μm2图案上C2C12单细胞捕获率明显高于800 μm2,1 000 μm2,1 400 μm2蛋白图案上单细胞的捕获率,是控制成肌细胞单细胞的最佳几何图案面积。随着基底几何图案长宽比的增加,相同面积微图案上的单细胞铺满率基本呈降低趋势。为了提高捕获率,Liu等[26]设计了较为复杂的图形,将同样面积的蛋白分割成捕获区域和铺展区域。能够大量捕获成肌细胞的同时,精确控制细胞的几何形状和位置。这项研究通过改进后的组合微图案能够实现在捕获成肌细胞单细胞的同时,精确控制细胞的形状、大小、相对位置和排列。通过对细胞微丝分布的探究,发现几何排列图案可能会通过作用于成肌细胞骨架而进一步影响成肌细胞的分化。缺点是捕获率相对较低,为(36.55±3.29)%。"
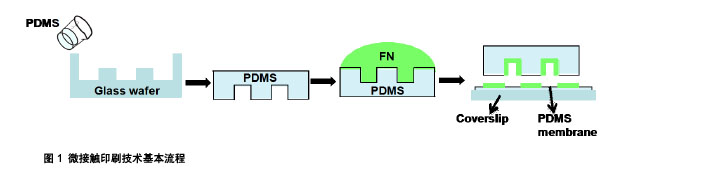
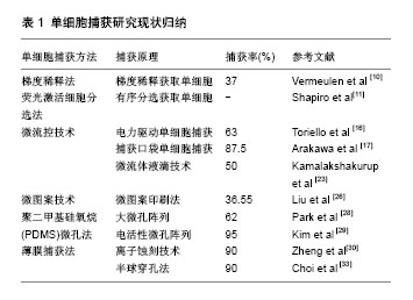
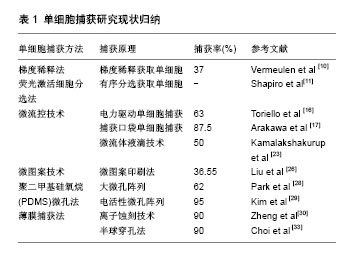
2.3 微孔阵列技术 微孔阵列技术主要是利用物理方法或者化学方法使细胞可以选择性地黏附到基底的限定区域,或者可以将细胞封闭到一个大的平行加工出很多微孔阵列的平行板结构上。这些微孔阵列在接种细胞的时候允许细胞进入到芯片表面的微孔内,并且控制每个微孔只允许1个细胞进入。其中后者不仅不限于贴壁细胞而且不需要先进的表面化学程序和复杂微加工设施,这样比较适合于对数千个细胞的高通量显微镜研究。而且在微孔中被动限制细胞(沉积细胞在基板上落入微孔中,细胞不容易移位)[27],由于其简单和较低的专业要求,使这种方法成为一个非常有吸引力的策略。 微孔阵列具有操作简单、方便观察等优点。但也有单细胞捕获方法通常存在的一些限制:在操作上,对于微孔捕获的单细胞的测定时间需要短于复制时间,否则细胞复制将造成子细胞的混杂;捕获的单细胞与组织中的细胞相比表现为缺乏支持细胞、细胞外基质或生长因子,所以一般的微孔阵列仅适用于短期细胞研究;除此之外,微孔孔壁对贴壁细胞的形状予以约束,可能会对细胞组织学功能造成一定影响。 为了克服孔径较小微孔对细胞形状的束缚,Park等[28]研究尝试用不同形状的较大尺寸微孔进行单细胞捕获和培养,用来提供足够的空间供细胞的黏附和生长。结果在三角形微孔阵列下细胞样品会出现再回流现象,并且在捕获细胞后液体流动方式会发生一定改变,从而实现更高的细胞捕获率。有研究利用磁力法捕获单细胞主要是先将细胞悬液通过一个连续流动的进出口引入聚二甲基硅氧烷(PDMS)微流体通道中,在捕获率很低的情况下附加的磁力辅助细胞捕获,3 min后微孔逐渐被占领,几乎所有孔都包含单一细胞[29]。常用于快速、稳定和高效的单细胞捕获。 2.4 薄膜阵列技术 滤膜是一种制备在微孔承托层(支撑体)上的布满更微小孔隙的薄膜。制作滤膜的材料有很多,因此滤膜可分为有机膜和无机膜。滤膜可以作为过滤原件是因为其结构滤层非常薄,因而它的过滤机制主要是筛除作用,而吸附效应很小。膜过滤器的过滤精度较高,粒径控制比较稳定,而且反冲洗容易恢复性能。薄膜捕获细胞主要是利用制作所过滤细胞大小孔径的膜孔,使得只能单细胞通过。 目前薄膜孔捕获单细胞的研究较少,大多都是用来过滤菌体等研究。其中较为成功的研究是Zheng等[30]用反应离子蚀刻技术捕获和电解人类血液中的循环肿瘤细胞。血液中循环肿瘤细胞的存在与否和数量的多少为转移性乳腺癌患者诊断的重要依据信息。实验是以微机电系统(MEMS)为基础的方法来简化这个复杂的过程,使它更加快速且降低成本。主要原理是此装置可以过滤掉血细胞,使循环肿瘤细胞保留于膜上,并且较短时间可以达到较好效果。之后的PCR分析,是通过把膜上的每个孔的位置埋上相应的电极来电解细胞。此装置最大的优点是将电极与细胞进行了直接接触,从而提高了膜上细胞的电解效率,便于下游的PCR扩增分析[30]。 2.5 多种技术结合进行细胞捕获 由于单细胞研究的必要性,越来越多的科学研究开始了对单细胞捕获以及对单细胞形态功能进行人为操控的研究。然而兼顾单细胞捕获及之后生长成功能性组织的研究却为较大难题。例如利用微孔捕获单个细胞是建立更大数字单细胞捕获的有力工具,由于其在装置制造和操作中的简单性倍受欢迎。为了提供足够的空间供细胞生长及功能性分析,必须制造较捕获单细胞更大的微孔的尺寸,从而导致了很低的单细胞捕获率[31-32]。微接触印刷法可以较好地控制细胞的黏附和生长,但细胞仅仅依靠物理黏附进行捕获,单细胞捕获率较低。微流控技术可以在捕获的基础上进行后续研究,但昂贵的进样系统、芯片内产物难以回收等限制了它的发展。所以多种方法结合来实现共赢的方法应运而生。 2.5.1 穿透微孔阵列技术 穿孔的微孔阵列用于单细胞的捕获和培养,其结合了微孔法和薄膜法,制作一些穿孔的聚二甲基硅氧烷(PDMS)微孔来克服微孔法限制细胞后续生长的问题。实验中将此方法用于单个藻类的分离和培养,主要是在半球形的微孔阵列底端穿孔,实现利用微孔使微藻迅速扩散再通过流体动力使突变体细胞通过底部微孔落入培养瓶中再培养。克服了从固相琼脂板中选择菌落的复杂耗时的过程,实现了快速精确地细胞分离[33]。 2.5.2 微孔法3D培养 微孔法和微接触印刷方法都只能做到二维的细胞培养,而3D细胞培养是能在细胞培养过程中为细胞提供一个更加接近体内生存条件的微环境的培养技术。Charnley等[34]研究利用微孔表面较强的吸附能力。首先利用倒置的微接触方法钝化上表面使其限制细胞的黏附,再通过物理吸附功能化在其余3个表面吸附纤连蛋白或者先使聚二甲基硅氧烷(PDMS)微孔芯片通过物理吸附功能化吸附纤连蛋白到整个区域微孔,随后孵育疏水物质钝化上表面。通过微孔法大面积捕获细胞进行细胞的3D培养[34]。这项研究为细胞的3D培养提供了思路,为建立细胞操纵平台提供了可能。 2.5.3 双向微孔法 在普通微孔阵列的基础上,有研究使用双阱(DW)装置来提高单细胞的捕获率[35],其原理是制作一些尺寸不同的大小微孔阵列分别用来细胞的捕获和铺展。利用小微孔捕获单细胞后翻转再通过重力作用将捕获的细胞转移到大的微孔中,使细胞在大的微孔中铺展及生长,从而提高大微孔中单细胞的捕获率。双阱的优点是可以高效率地将单细胞装载到大的微孔中,其中大微孔的尺寸可以显著大于单个细胞捕获微孔。克服了小尺寸微孔对细胞的的束缚,可以长时间培养细胞。 单细胞捕获研究现状见表1。"
| [1] Rettig JR, Folch A. Large-scale single-cell trapping and imaging using microwell arrays. Anal Chem. 2005;77(17): 5628-5634.[2] Bratten CD, Cobbold PH, Cooper JM. Single-cell measurements of purine release using a micromachined electroanalytical sensor. Anal Chem. 1998;70(6):1164-1170.[3] Inoue I, Wakamoto Y, Moriguchi H, et al. On-chip culture system for observation of isolated individual cells. Lab Chip. 2001;1(1):50-55.[4] Cahan P, Daley GQ. Origins and implications of pluripotent stem cell variability and heterogeneity. Nat Rev Mol Cell Biol. 2013;14(6):357-368.[5] Clevers H.The cancer stem cell: premises, promises and challenges. Nat Med. 2011;17(3):313-319.[6] Altschuler SJ, Wu LF. Cellular heterogeneity: do differences make a difference. Cell. 2010;141(4):559-563.[7] Di Carlo D, Tse HTK, Gossett DR. Introduction: Why Analyze Single Cells? Clifton:Humana Press. 2012. [8] Ulloa-Aguirre A, Conn PM. Cellular Endocrinology in Health and Disease. Elsevier, 2014.[9] Clark P, Dunn GA, Knibbs A, et al. Alignment of myoblasts on ultrafine gratings inhibits fusion in vitro. Int J Biochem Cell Biol. 2002;34(7):816-825.[10] Vermeulen L, Todaro M, de Sousa Mello F, et al. Single-cell cloning of colon cancer stem cells reveals a multi-lineage differentiation capacity. Proc Natl Acad Sci U S A. 2008; 105(36):13427-13432.[11] Shapiro E, Biezuner T, Linnarsson S. Single-cell sequencing-based technologies will revolutionize whole-organism science. Nat Rev Genet. 2013;14(9): 618-630.[12] Dertinger SKW, Chiu DT, And NLJ, et al. Generation of Gradients Having Complex Shapes Using Microfluidic Networks. Analytical Chemistry. 2001; 73(6):1240-1246.[13] Tanyeri M, Johnson-Chavarria EM, Schroeder CM. Hydrodynamic trap for single particles and cells. Appl Phys Lett. 2010;96(22):224101.[14] Tanyeri M, Ranka M, Sittipolkul N, et al. A microfluidic-based hydrodynamic trap: design and implementation Lab Chip. 2011;11(10):1786-1794.[15] Yu M, Chen Z, Xiang C, et al. Microfluidic-based single cell trapping using a combination of stagnation point flow and physical barrier. Acta Mechanica Sinica. 2016; 32(3):422-429.[16] Toriello NM, Douglas ES, Mathies RA. Microfluidic device for electric field-driven single-cell capture and activation. Anal Chem. 2005;77(21):6935-6941.[17] Arakawa T, Noguchi M, Sumitomo K, et al. High-throughput single-cell manipulation system for a large number of target cells. Biomicrofluidics. 2011;5(1):14114.[18] Jin D, Deng B, Li JX, et al. A microfluidic device enabling high-efficiency single cell trapping. Biomicrofluidics. 2015; 9(1):014101.[19] Kemna EW, Schoeman RM, Wolbers F, et al. High-yield cell ordering and deterministic cell-in-droplet encapsulation using Dean flow in a curved microchannel. Lab Chip. 2012;12(16): 2881-2887.[20] He M, Edgar JS, Jeffries GD, et al. Selective encapsulation of single cells and subcellular organelles into picoliter- and femtoliter-volume droplets. Anal Chem. 2005;77(6): 1539-1544.[21] Schoendube J, Wright D, Zengerle R, et al. Single-cell printing based on impedance detection. Biomicrofluidics. 2015;9(1):014117.[22] Chabert M, Viovy JL. Microfluidic high-throughput encapsulation and hydrodynamic self-sorting of single cells. Proc Natl Acad Sci U S A. 2008;105(9):3191-3196.[23] Kamalakshakurup G, Lee AP. High-efficiency single cell encapsulation and size selective capture of cells in picoliter droplets based on hydrodynamic micro-vortices. Lab Chip. 2017;17(24):4324-4333.[24] Ye F, Jiang J, Chang H, et al. Improved single-cell culture achieved using micromolding in capillaries technology coupled with poly (HEMA). Biomicrofluidics. 2015;9(4): 044106.[25] Ye F, Ma B, Gao J, et al. Fabrication of polyHEMA grids by micromolding in capillaries for cell patterning and single-cell arrays. J Biomed Mater Res B Appl Biomater. 2015;103(7): 1375-1380.[26] Liu X, Liu Y, Zhao F, et al. Regulation of cell arrangement using a novel composite micropattern. J Biomed Mater Res A. 2017;105(11):3093-3101.[27] Khademhosseini A, Yeh J, Jon S, et al. Molded polyethylene glycol microstructures for capturing cells within microfluidic channels. Lab Chip. 2004;4(5):425-430.[28] Park JY, Morgan M, Sachs AN, et al. Single cell trapping in larger microwells capable of supporting cell spreading and proliferation. Microfluid Nanofluidics. 2010;8(2):263-268.[29] Kim SH, Yamamoto T, Fourmy D, et al. Electroactive microwell arrays for highly efficient single-cell trapping and analysis. Small. 2011;7(22):3239-3247.[30] Zheng S, Lin H, Liu JQ, et al. Membrane microfilter device for selective capture, electrolysis and genomic analysis of human circulating tumor cells. J Chromatogr A. 2007;1162(2): 154-161.[31] Lindström S, Eriksson M, Vazin T, et al. High-density microwell chip for culture and analysis of stem cells. PLoS One. 2009;4(9):e6997.[32] Lecault V, Vaninsberghe M, Sekulovic S, et al. High-throughput analysis of single hematopoietic stem cell proliferation in microfluidic cell culture arrays. Nat Methods. 2011;8(7):581-586.[33] Choi J, Bae S, Kim K, et al. Capture and culturing of single microalgae cells, and retrieval of colonies using a perforated hemispherical microwell structure. Rsc Advances.2014; 4(106):61298-61304.[34] Charnley M, Textor M, Khademhosseini A, et al. Integration column: microwell arrays for mammalian cell culture. Integr Biol (Camb). 2009;1(11-12):625-634.[35] Lin CH, Hsiao YH, Chang HC, et al. A microfluidic dual-well device for high-throughput single-cell capture and culture. Lab Chip. 2015;15(14):2928-2938. |
| [1] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [2] | Zeng Yanhua, Hao Yanlei. In vitro culture and purification of Schwann cells: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1135-1141. |
| [3] | Xu Dongzi, Zhang Ting, Ouyang Zhaolian. The global competitive situation of cardiac tissue engineering based on patent analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 807-812. |
| [4] | Wu Zijian, Hu Zhaoduan, Xie Youqiong, Wang Feng, Li Jia, Li Bocun, Cai Guowei, Peng Rui. Three-dimensional printing technology and bone tissue engineering research: literature metrology and visual analysis of research hotspots [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 564-569. |
| [5] | Chang Wenliao, Zhao Jie, Sun Xiaoliang, Wang Kun, Wu Guofeng, Zhou Jian, Li Shuxiang, Sun Han. Material selection, theoretical design and biomimetic function of artificial periosteum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 600-606. |
| [6] | Liu Fei, Cui Yutao, Liu He. Advantages and problems of local antibiotic delivery system in the treatment of osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 614-620. |
| [7] | Li Xiaozhuang, Duan Hao, Wang Weizhou, Tang Zhihong, Wang Yanghao, He Fei. Application of bone tissue engineering materials in the treatment of bone defect diseases in vivo [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 626-631. |
| [8] | Zhang Zhenkun, Li Zhe, Li Ya, Wang Yingying, Wang Yaping, Zhou Xinkui, Ma Shanshan, Guan Fangxia. Application of alginate based hydrogels/dressings in wound healing: sustained, dynamic and sequential release [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 638-643. |
| [9] | Chen Jiana, Qiu Yanling, Nie Minhai, Liu Xuqian. Tissue engineering scaffolds in repairing oral and maxillofacial soft tissue defects [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 644-650. |
| [10] | Xing Hao, Zhang Yonghong, Wang Dong. Advantages and disadvantages of repairing large-segment bone defect [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 426-430. |
| [11] | Jiang Tao, Ma Lei, Li Zhiqiang, Shou Xi, Duan Mingjun, Wu Shuo, Ma Chuang, Wei Qin. Platelet-derived growth factor BB induces bone marrow mesenchymal stem cells to differentiate into vascular endothelial cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(25): 3937-3942. |
| [12] | Liu Chang, Li Datong, Liu Yuan, Kong Lingbo, Guo Rui, Yang Lixue, Hao Dingjun, He Baorong. Poor efficacy after vertebral augmentation surgery of acute symptomatic thoracolumbar osteoporotic compression fracture: relationship with bone cement, bone mineral density, and adjacent fractures [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3510-3516. |
| [13] | Liu Liyong, Zhou Lei. Research and development status and development trend of hydrogel in tissue engineering based on patent information [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3527-3533. |
| [14] | Bi Qingwei, Liu Chengpu, Li Yan, Zhao Wenwen, Han Mei. Structure analysis of platelet-rich fibrin derived from two centrifugation procedures [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3534-3539. |
| [15] | Tian Guangzhao, Yang Zhen, Zha Kangkang, Sun Zhiqiang, Li Xu, Sui Xiang, Huang Jingxiang, Guo Quanyi, Liu Shuyun. Regulatory effect of decellularized cartilage matrix on macrophage polarization [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3545-3550. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||