Chinese Journal of Tissue Engineering Research ›› 2019, Vol. 23 ›› Issue (4): 613-620.doi: 10.3969/j.issn.2095-4344.0381
Previous Articles Next Articles
Mechanism of bone growth factors regulating fracture healing and their application in bone regeneration and repair
Feng Yang1, Chen Yueping2, Zhang Xiaoyun2, Dong Panfeng2, Zhuo Yinghong1, Lan Jiao1, Hu Qinglei1, Tang Xianneng1
- 1Guangxi University of Chinese Medicine, Nanning 530001, Guangxi Zhuang Autonomous Region, China; 2Department of Orthopedics, Ruikang Hospital Affiliated to Guangxi University of Chinese Medicine, Nanning 530011, Guangxi Zhuang Autonomous Region, China
-
Online:2019-02-08Published:2019-02-08 -
Contact:Chen Yueping, Chief physician, Master’s supervisor, Department of Orthopedics, Ruikang Hospital Affiliated to Guangxi University of Chinese Medicine, Nanning 530011, Guangxi Zhuang Autonomous Region, China -
About author:Feng Yang, Master candidate, Guangxi University of Chinese Medicine, Nanning 530001, Guangxi Zhuang Autonomous Region, China
CLC Number:
Cite this article
Feng Yang, Chen Yueping, Zhang Xiaoyun, Dong Panfeng, Zhuo Yinghong, Lan Jiao, Hu Qinglei, Tang Xianneng . Mechanism of bone growth factors regulating fracture healing and their application in bone regeneration and repair [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(4): 613-620.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
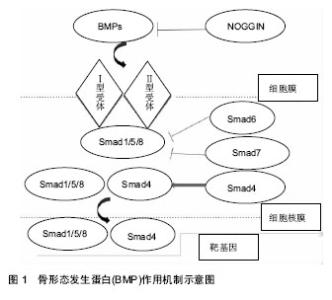
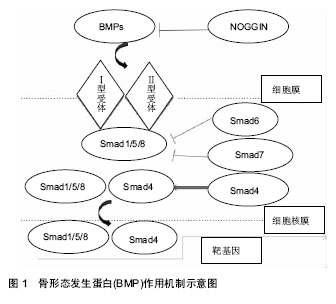
2.1 成纤维细胞生长因子 成纤维细胞生长因子(FGF)广泛存在于人体骨基质当中,作为一种潜在性丝分裂原,活体时能够加速软骨修复,离体形态则能促进软骨细胞的增殖、分化、成熟。机体出现骨折、组织损伤时,碱性成纤维细胞生长因子从坏死组织中释放出来,参与骨组织的自我修复过程,促进成骨细胞增殖及胶原形成。在小鼠实验中发现,成纤维细胞生长因子可通过促分裂原活化蛋白激酶及ERK介导的软骨细胞通路有效促进IFT88的表达,刺激原代纤毛发育,达到修复软骨的功效[1]。同时,成纤维细胞生长因子在活体内可有效促进骨膜源性增殖,促进未分化间充质细胞加速分裂。成纤维细胞生长因子同样也是一种毛细血管增殖刺激剂,能够有效促进骨折断端毛细血管生长,促进软骨形成,提前重建骨痂血运,加快骨痂的成熟和骨化[2]。Yamada等[3]通过调控成纤维细胞生长因子释放量的多少,探究受控的成纤维细胞生长因子对皮下新生血管床的形成影响,组织学评估显示脉管系统程度显著增加,证明了成纤维细胞生长因子能够有效的促进皮下血管床形成。 血管闭塞性脉管炎(Buerger病)作为一种肢体威胁极大的疾病,其疾病进展往往是导致肢体截肢,Patwa等[4]应用Ilizarov治疗60例Buerger病,增加了缺血肢体的血管性,最后只有2例截肢,其他疗效显著,但其治疗周期稍长。因此,作者认为可利用成纤维细胞生长因子对血管生成的刺激作用通过外源性注射成纤维细胞生长因子加快其治疗周期,提高疗效。 21世纪以来,Ilizarov理念给微创骨科带来了新的变化,骨搬运治疗骨缺损成为国内临床研究的热点,主要通过外源性机械调节刺激成骨作用及周围毛细血管生成,临床疗效显著,但有着外固定操作繁琐的特点[5],因此作者认为成纤维细胞生长因子等多种生长因子能够成为临床骨搬运治疗骨缺损或糖尿病足的一种辅助治疗以加速愈合,但其临床应用还有待进一步研究证实。 成纤维细胞生长因子目前在临床上多用于促进细胞分化、增殖。Caroti等[6]在对小鼠骨髓间充质干细胞持续多能性加速培养中提到,通过不同氧张力环境及成纤维细胞生长因子补充差异探究发现,在此条件下比传统细胞增殖速度快2.8倍,能够有效加速小鼠骨髓间充质干细胞前期培养,为临床实验研究提供了极大的便利,明显加快前期进程。成纤维细胞生长因子通过激活受体调节骨形成[7],促进骨基质形成。也有研究认为碱性成纤维细胞生长因子仅对软骨形成作用明显,Nakajima等[8]在探究单次注射碱性成纤维细胞生长因子对大鼠股骨缺损的愈合影响中发现,对照组注射纤维蛋白凝胶,实验组采用骨折部位局部注射纤维蛋白凝胶及碱性成纤维细胞生长因子,观察发现骨结合率、骨密度无明显差异性,作者认为在长骨闭合性骨折的愈合过程中,碱性成纤维细胞生长因子可加速骨痂形成,但不一定加速愈合过程。研究表明碱性成纤维细胞生长因子单独应用效果较差,和骨形态发生蛋白联合应用对于骨折愈合、骨缺损效果显著。在一项对大鼠成骨分化细胞研究中表明,成纤维细胞生长因子2协同骨形态发生蛋白2能够有效促进大鼠异位植入模型碱性磷酸酶活性及血管再生[9],证明了成纤维细胞生长因子2协同骨形态发生蛋白2的骨再生治疗潜力,联合应用骨形态发生蛋白及碱性成纤维细胞生长因子治疗股骨缺损,成骨作用明显。在单一的骨生长因子已被证实有效的情况下,为临床上应用多种骨生长因子协同治疗提供了切实的研究依据。 2.2 血小板衍生生长因子 血小板衍生生长因子(PDGF)最初在血小板和血清中鉴定,是间充质细胞迁移和增殖的关键调节剂[10],是血管生成、胚胎发生和癌症发展和进展的必要条件,能够有效诱导成纤维细胞、单核巨噬细胞、平滑肌细胞的增生。血小板衍生生长因子与靶细胞受体结合,激活酪氨酸激酶,促使靶细胞磷酸化并为信号蛋白提供结合点,如磷酸肌醇3激酶(PI3K)和mit原激活蛋白激酶(MAPK)路径,以达到促进增殖分化的目的。 大量临床试验证实血小板衍生生长因子在骨折愈合各阶段均能够有效诱导软骨细胞及成骨细胞增生,同时可提高破骨细胞活性、加速骨吸收,促进骨重塑。Li等[11]在重组外源血小板衍生生长因子培养鼠单核-巨噬细胞和骨髓衍生的巨噬细胞分析体外培养对破骨细胞生成的影响发现,局部使用血小板衍生生长因子β受体抑制剂抑制了血小板衍生生长因子诱导的STAT-3磷酸化,而血小板衍生生长因子有效增强了体外和体内破骨细胞的形成,证实了血小板衍生生长因子对破骨细胞前体细胞迁移和破骨细胞生成信号分子表达影响显著。Onweka等[12]使用血小板衍生生长因子和血小板衍生生长因子基因敲除(PDGF-KO)的骨髓移植物植入野生型小鼠中作为下腔静脉插入移植物,2周后发现,来自PDGF-KO小鼠移植物支架聚合物剩余更多且内膜发育组织较少,其巨噬细胞凋亡增加,平滑肌细胞增殖减少,胶原含量降低。得出血小板衍生生长因子通过调节巨噬细胞凋亡,平滑肌细胞增殖和细胞外基质沉积而促成血管新生组织形成。一项对重组血小板衍生生长因子与自体骨移植在足踝融合术中的荟萃分析中显示,两者同样对足踝融合术后骨愈合效果显著,但自体移植采集过程中存在供体部位疼痛和发病率增加、手术时间延长、失血及瘢痕形成等缺陷[13],而重组血小板衍生生长因子可以克服这一缺陷。因此推测重组血小板衍生生长因子有望成为足踝融合术中自体移植的可替代方案,当然这需要更多高质量的长期随访随机对照试验来作出最终结论。 大量临床及动物实验均表明血小板衍生生长因子能够有效促进骨折愈合,但相比于其他骨生长因子具有来源少、价格贵、局部转染作用性价比差等缺点,无法大规模临床应用。同时,血小板衍生生长因子半衰期短,无法精确控制,Davis等[14]在对异位骨化的研究中发现重组血小板衍生生长因子是组织工程化骨骼肌模型中有效的骨诱导因子,并且促炎细胞因子可调节其蛋白的成骨能力,这意味着重组血小板衍生生长因子能够成为一种可调控性的骨诱导方法,以改善血小板衍生生长因子半衰期短无法精确释放的缺点,为骨组织工程复合载体提供新的思维,显著拓宽其临床研究应用价值。 2.3 转化生长因子β 转化生长因子β(TGF-β)在血小板中含量最高,骨组织次之,约为血小板含量1/10。骨折后,炎性细胞浸润,血小板及巨噬细胞释放转化生长因子β,与受体结合行成二聚物,通过丝氨酸-苏氨酸激酶与同源蛋白(SMAD)蛋白酪氨酸激酶共同活化作用,诱导相关的转录因子2(Runx2)与SMAD蛋白结合形成复合物,刺激成骨细胞增殖分化,促进骨折断端膜内成骨及骨痂形成[15]。一项对间充质干细胞成骨分化的前瞻性研究中显示骨形态发生蛋白、转化生长因子β、细胞质衍生因子1(SDF-1),胰岛素样生长因子1型(IGF-1),组蛋白去甲基化酶JMJD3,细胞周期蛋白依赖性激酶1(CDK1),岩藻依聚糖,Runx2转录因子和TAZ转录共激活因子等均能有效促进间充质干细胞的成骨分化作用,促进并加速新骨形成[16]。Takayama等[17]在对青鳉鱼骨折模型中使用转化生长因子β受体激酶抑制剂(SB431542)抑制转化生长因子β信号,证明转化生长因子β的抑制强烈地削弱成骨细胞迁移和分化,另外这种转化生长因子β抑制剂降低了相关基因链的表达,并导致了破骨细胞分化的延迟。证明了转化生长因子β2在骨折愈合过程中具有特异性刺激成骨细胞的迁移以及成骨、破骨细胞的分化功能。 另外转化生长因子β对各种细胞类型均有着广泛的生物学效应[18],在调节细胞增殖、生长、分化的同时,也能进行抑制。而他的双向作用多取决于其浓度及作用时间,一般认为低浓度转化生长因子β刺激细胞增殖、分化,高浓度抑制。Wang等[19]在miR-21对瘢痕组织成纤维细胞的作用表达中发现,与正常皮肤成纤维细胞相比,损伤后瘢痕组织的成纤维细胞证实转化生长因子β1和miR-21的高表达,同时细胞生长和迁移达到峰值,转化生长因子β1和miR-21的表达与成纤维细胞数量呈正相关,高表达超过一定程度后,细胞生长和迁移出现显著降低,与成纤维细胞数量呈负相关,因而推测转化生长因子β的浓度在细胞增殖分化中具有双向调节作用。 骨折愈合期间,新生软骨形成及破骨细胞进行骨吸收时,均需要转化生长因子β参与表达。Wen等[20]发现在软骨细胞中高度表达的转化生长因子β是骨生长的负调节剂,转化生长因子β能够通过旁分泌机制调节骨形成和骨重塑,同时还能抑制破骨细胞产生及成熟破骨细胞的活性,从而抑制骨吸收。Wang等[21]在对小鼠的骨量模型中发现局部骨丢失,组织学结果提示主要由破骨细胞形成受损引起而不是骨形成阶段造成,得出在软骨细胞中转化生长因子β通过β-catenin信号调节破骨细胞形成,抑制破骨细胞产生从而在骨生长和骨重塑中起关键作用。 转化生长因子β在促进骨细胞增殖、分化方面疗效显著,目前转化生长因子β多适用于局部治疗,全身应用可能引起一些不良反应,因而临床外用较少。目前多项研究证实转化生长因子β信号表达参与骨肿瘤的发生及转移[22-23],转化生长因子β1可抑制所有淋巴细胞的增生及功能,抑制巨嗜细胞激活。因此很多学者通过阻断转化生长因子β信号通路相关蛋白转化因子在骨巨细胞瘤中的表达,探究骨肿瘤治疗的新靶点[24]。转化生长因子β失调是癌症及纤维化重要进程,近期有研究使用工程化的转化生长因子β单体可结合转化生长因子β受体但负性抑制其表达[25],从而提供了探测和操纵转化生长因子β信号传导的新途径,也为其他转化生长因子β家族成员提供了新探索。 2.4 骨形态发生蛋白 自1965年Urist首次应用脱钙骨基质(DBM)异位诱导间充质细胞向骨谱系细胞转化,骨形态发生蛋白骨诱导活跃在临床科研一线经久不衰。骨形态发生蛋白来源于骨与骨源性细胞,可作用于多种细胞,其信号最初产生于骨形态发生蛋白及其跨膜结合的受体,磷酸化后和同源蛋白(SMAD4)一起进入细胞核和靶目标骨形态发生蛋白反应基因如骨钙素,促使靶细胞结构功能发生改变(见图1)。"

目前骨形态发生蛋白2是骨形态发生蛋白20多种亚型中定向诱导骨形成能力最强的因子,大量实验证明骨形态发生蛋白2能够促进组织细胞增殖、分化[26-27],聚集间充质细胞,定向诱导成骨细胞前体细胞向成骨细胞分化,促进Ⅰ型胶原合成,提高碱性磷酸酶水平。 骨形态发生蛋白在骨科临床应用的最大亮点在于它对于间充质干细胞的定向分化诱导成为成骨细胞,加快骨折愈合时间,有效促进骨折愈合,因而备受青睐。随后,更多学者不满足于骨形态发生蛋白对于正常骨折的治疗,将其应用于骨缺损、骨不连的治疗。骨形态发生蛋白诱导骨缺损是当下治疗的热点,一项针对骨形态发生蛋白2及骨形态发生蛋白7在治疗长骨骨不连的临床调查中发现,随访17个月,骨形态发生蛋白2组无论是在血清浓度、骨折愈合时间、愈合率、影像学表现均高于骨形态发生蛋白7组[28]。骨形态发生蛋白不仅能用于骨骼疾病的治疗,而且在神经再生修复、造血系统修复等方面同样具有广阔的应用前景[29-30]。 骨形态发生蛋白促进细胞分化也诱导细胞凋亡,因此对多种肿瘤细胞有明显抑制作用[31-32]。Kallioniemi [33]将骨形态发生蛋白4称之为癌细胞迷人的调节器,阐述骨形态发生蛋白4在肿瘤细胞功能中表示,其功能性作用不限于诱导细胞增殖和迁移,也有助于调节细胞凋亡和血管生成,而新血管形成是癌细胞持续生长的必要条件,因为其抑制生长能力成为癌细胞治疗的新靶点,但同时促进细胞迁移一定程度降低了吸引力。因此骨形态发生蛋白衍生的肿瘤治疗的特定靶向疗法,还有一段距离。 最初骨形态发生蛋白的发现面临着提取过程复杂、成本高、产量低等一系列问题,随着基因重组技术的发展,重组骨形态发生蛋白的制备让骨形态发生蛋白广泛应用于临床成为可能。骨形态发生蛋白作为多生长因子广泛应用于临床,但骨形态发生蛋白在骨科使用也有着其特有的禁忌证。2008年,美国食品级药物管理局(FDA)禁止将其应用于颈椎前路手术当中,因为在脊柱骨科手术后易诱导骨过度生长或异位骨化出现局部血肿压迫脊髓。Eliaz等[34]记录一位59岁女性患者在接受腰椎前路融合(ALIF)手术中使用骨形态发生蛋白,几年后出现硬脑膜内骨生长。此后FDA给骨形态发生蛋白在脊柱手术的应用划定了界限,一项对骨形态发生蛋白应用于脊柱手术的系统评价中发现在遵从骨形态发生蛋白在脊柱手术的适应证后不良事件的发生明显降低,且临床疗效显著[35]。 随着骨组织工程的发展,发现生物复合支架载体诱导骨生长因子在骨折局部的充分表达能够有效缩减骨折愈合的时间[36-37],主要用于骨形态发生蛋白2缓释及控释。其载体系统多样,输送系统多是水凝胶,微球,纳米颗粒和纤维的形式,支撑载体由金属,陶瓷,聚合物和复合材料组成,这些载有蛋白质的植入载体导致细胞黏附、降解,最终在特定位置释放药物或蛋白质,但是在可用载体系统中均报道了诸如异位生长,蛋白质递送较少,蛋白质失活等问题,因此可控载体、双重递送载体等开始进入众多学者的眼球,适宜生长因子的寻找随着生物医学材料的不断发展仍将继续。 2.5 血管内皮生长因子 血管内皮生长因子(VEGF)是调节血管发育和血管生成最重要的生长因子之一。血管内皮生长因子配体能够结合受体,激活酪氨酸激酶、磷酸化信号蛋白,同时激活下游信号,促进内皮细胞生长因子受体、血管渗透性因子受体作用于相关靶细胞,促进血管形成[38]。由于骨是高度血管化的器官,在骨骼发育早期,血管内皮生长因子对软骨细胞在骨骼软骨缺氧区域的生存,骨骼血管形成以及成骨细胞的增殖和分化都作用重大,能够增强成骨细胞活性、刺激增殖、分化从而加速骨形成[39]。而成骨细胞衍生的血管内皮生长因子同时能够刺激间充质干细胞分化成成骨细胞并抑制它们向脂肪细胞分化从而维持人体骨稳态[40]。 血管内皮生长因子与骨形成关系密切,临床试验证明骨形成的同时多伴有新生血管形成[41-42]。Street等[43]在实验小鼠分别抑制软骨内成骨和膜内骨化中血管内皮生长因子的活性,探究血管内皮生长因子在骨愈合当中的必要性,发现血管内皮生长因子的抑制同时抑制了小鼠胫骨骨缺损愈合,和成骨细胞分化中血管内皮生长因子的自分泌作用一致。而在单独的实验中,外源性血管内皮生长因子显著增强了血管形成和骨化效果,促进骨缺损愈合,认为血管内皮生长因子参与了软骨内成骨及成骨两个骨形成过程。 血管内皮生长因子在增强骨折断端血管通透性,诱导新骨形成的同时也能加速破骨细胞的骨吸收,促进骨愈合。Motokawa等[44]在探究小鼠年龄和破骨细胞相关性研究发现,小鼠的股骨破骨细胞数量和血清血管内皮生长因子水平在出生后均逐渐增加,60至120日达到最高,血清血管内皮生长因子水平与之成正比,因而推测破骨细胞的出现可能受血清血管内皮生长因子水平的影响。也有学者认为血管内皮生长因子对破骨细胞形成无直接作用,Huang等[45]使用血管内皮生长因子A165处理前成骨细胞MC3T3-E1细胞作为培养基培养RAW264.7细胞,用含有或不含有核因子κ-B配体(RANKL)的受体活化剂媒介物及血管内皮生长因子处理前胶原RAW264.7细胞,抗酒石酸酸性磷酸酶染色测量破骨细胞形成,通过测量培养基中RANKL和骨保护素(OPG)的水平,发现血管内皮生长因子通过增加成骨细胞RANKL / OPG比例刺激破骨细胞分化,但对破骨细胞前体细胞没有直接作用。 临床上血管内皮生长因子和骨形态发生蛋白等其他骨生长因子联合比单独使用效果更佳[46-47]。生物组织工程是骨修复的热点,血管内皮生长因子加载能够克服多孔组织工程支架缺血性血管化的缺点[48]。临床实验证实血管内皮生长因子在牵张成骨下能够有效修复骨缺损,缓释情况下能够有效规避其半衰期短、释放速度快等缺点[49-50]。血管内皮生长因子通过血管调节作用调节成骨细胞、破骨细胞的增殖、分化,在大脑中,血管内皮生长因子介导血管生成、神经迁移和神经保护,作为一种渗透性因子,过度的血管内皮生长因子会破坏细胞内的屏障,增加脉络丛内神经的渗漏,引起水肿,激活炎症通路[51]。近期有报道称抗血管内皮生长因子治疗对通过使肿瘤脉管系统正常化神经保护的作用,能够缓解神经水肿并且将氧气更有效地输送到神经中,从而减少神经损伤和改善神经功能[52]。 2.6 胰岛素样生长因子 胰岛素样生长因子(IGF)是氨基酸结构与胰岛素系列相似的多肽,其结合蛋白(LGFbp1-6)通过调节胰岛素样生长因子浓度增强胰岛素样生长因子活性以调节生物活性、延长半衰期。胰岛素样生长因子1主要与胰岛素样生长因子1受体酪氨酸激酶受体结合,引起细胞内传导,促进细胞增殖分化。此外,胰岛素样生长因子1可上调蛋白激酶和c-Jun氨基端激酶,对成骨细胞特异性转录因子(OSX)表达有显著影响。另外,胰岛素样生长因子1上调I型胶原蛋白和碱性磷酸酶间充质干细胞的基因表达,是成骨细胞分化的关键标记物。 胰岛素样生长因子1参与软骨的合成代谢,维持正常软骨的代谢更替,软骨损伤时促进软骨细胞生成,修复软骨[53]。Zhang等[54]在小鼠实验中探究不同剂量胰岛素样生长因子1对全层关节软骨缺损修复过程中软骨层和软骨下骨的影响中发现,高浓度胰岛素样生长因子1调节软骨层邻近缺损的基因表达,改善新软骨的形成和完整性,低剂量胰岛素样生长因子1更有效地调节软骨下骨的基因表达,进而促进软骨下骨的重建,证实了胰岛素样生长因子在软骨修复的作用。胰岛素样生长因子1在骨骼中同样含量丰富,作为一种促有丝分裂剂,可促进成骨细胞募集、诱导增殖分化。在一项胰岛素样生长因子1在骨发育生长必要性探究实验中发现,实验组受体基因胰岛素样生长因子1敲除组小鼠对比正常小鼠股骨长骨显著减少4%-7%,颅盖骨厚度较正常组减少14%,从而证实了胰岛素样生长因子1在骨生长的必要性[55]。 外源性使用胰岛素样生长因子主要有3种方式,腹腔注射、静脉注射或局部应用,前两者对使用量需求较大,而且因其半衰期短在体内较易稀释降解,导致蛋白失活,因而临床使用疗效欠佳。胰岛素样生长因子对于细胞增殖分化明显,但有研究证明其对缺血性肌细胞无增殖分化效应,因此建议胰岛素样生长因子外用建议血管网丰富处为佳[56]。随着基因工程的发展,胰岛素样生长因子在关节腔内局部应用修复软骨成为临床首选,如通过基因工程转染胰岛素样生长因子1至软骨细胞,然后移植以供应胰岛素样生长因子1,或者将胰岛素样生长因子1复合载体置入关节腔内以达到缓释、控释的效果。 "

| [1] Zhan D, Xiang W, Guo F, et al. Basic fibroblast growth factor increases IFT88 expression in chondrocytes. Mol Med Rep. 2017;16(5):6590-6599.[2] Yu P, Wilhelm K, Dubrac A, et al. FGF-dependent metabolic control of vascular development.Nature. 2017;545(7653):224.[3] Yamada S, Nagai N, Saijo S, et al. Controlled basic fibroblast growth factor release device made of poly(ethyleneglycol) dimethacrylates for creating a subcutaneous neovascular bed for cell transplantation. J Biomed Mater Res A. 2017;105(11): 3017-3024. [4] Patwa JJ,Krishnan A.Buerger's Disease (Thromboangiitis Obliterans)- Management by Ilizarov's Technique of Horizontal Distraction. A Retrospective Study of 60 Cases. Indian J Surg. 2011;73(1):40-47.[5] 花奇凯,秦泗河,赵良军,等.Ilizarov技术胫骨横向骨搬移术治疗糖尿病足[J].中国矫形外科杂志,2017,25(4):303-307.[6] Caroti CM, Ahn H, Salazar HF, et al. A Novel Technique for Accelerated Culture of Murine Mesenchymal Stem Cells that Allows for Sustained Multipotency. Sci Rep. 2017;7(1):13334.[7] Kalomoiris S, Cicchetto AC, Lakatos K, et al. Fibroblast Growth Factor 2 Regulates High Mobility Group A2 Expression in Human Bone Marrow‐Derived Mesenchymal Stem Cells. J Cell Biochem. 2016;117(9):2128-372137.[8] Nakajima F, Nakajima A, Ogasawara A, et al.Effects of a Single Percutaneous Injection of Basic Fibroblast Growth Factor on the Healing of a Closed Femoral Shaft Fracture in the Rat. Calcif Tissue Int. 2007;81(2):132-138. [9] Song R,Wang D,Zeng R,et al. Synergistic effects of fibroblast growth factor-2 and bone morphogenetic protein-2 on bone induction. Mol Med Rep. 2017;16(4): 4483-4492.[10] Zhang Y, Ma Y, Wu C, et al. Platelet-derived growth factor BB gene-released scaffolds: biosynthesis and characterization. J Tissue Eng Regen Med. 2016;10(10):E372-E381.[11] Li DQ,Wan QL, Pathak JL,et al.Platelet-derived growth factor BB enhances osteoclast formation and osteoclast precursor cell chemotaxis. J Bone Miner Metab. 2017; 35(4):355-365.[12] Onwuka E,Best C,Sawyer A,et al.The role of myeloid cell-derived PDGF-B in neotissue formation in a tissue-engineered vascular graft. Regen Med. 2017;12(3): 249-261[13] Li F,Yu F,Xin X,et al.Evaluation of Recombinant Human FGF-2 and PDGF-BB in Periodontal Regeneration: A Systematic Review and Meta-Analysis.Scientific Reports. 2017;7(1):65.[14] Davies OG,Grover LM,Lewis MP,et al.PDGF is a potent initiator of bone formation in a tissue engineered model of pathological ossification. J Tissue Eng Regen Med. 2018; 12(1):e355-e367. [15] Wrana JL,Attisano L,Wieser R,et al.Mechanism of activation of the TGF-β receptor.Nature.1994; 370(6488): 341-347.[16] Garg P,Mazur MM,Buck AC,et al.Prospective Review of Mesenchymal Stem Cells Differentiation into Osteoblasts. Orthopaedic Surgery.2017;9(1):13-19.[17] Takeyama K, Chatani M, Inohaya K, et al.TGF-β2 signaling is essential for osteoblast migration and differentiation during fracture healing in medaka fish. Bone.2016;86: 68-78.[18] Padua D,Massagué J.Roles of TGFbeta in metastasis.Cell Res.2009;19(1):89-102.[19] Wang X, Liu Y, Chen X, et al. Impact of MiR-21 on the expression of FasL in the presence of TGF-β1. Aesthet Surg J. 2013;33(8):1186-1198.[20] Wen X,Li X,Tang Y,et al.Chondrocyte FGFR3 Regulates Bone Mass by Inhibiting Osteogenesis. J Biol Chem. 2016;291(48): 24912-24921. [21] Wang B,Jin H,Zhu M,et al.Chondrocyte β-catenin signaling regulates postnatal bone remodeling through modulation of osteoclast formation in a murine model. Arthritis Rheumatol. 2014;66(1):107-120.[22] Qin J,Wu SP,Creighton CJ,et al.COUP-TFII inhibits TGF-β induced growth barrier to promote prostate tumorigenesis.Nature.2013;493(7431):236-240.[23] Bjerke GA,Yang CS,Frierson HF,et al.Activation of Akt signaling in prostate induces a TGF-β mediated restraint on cancer progression and metastasis.Oncogene. 2014;33(28): 3660.[24] Johnson MD.Transforming growth factor β family in the pathogenesis of meningiomas. World Neurosurg. 2017;104: 113-119.[25] Sun KK,Barron L,Hinck CS,et al.An engineered transforming growth factorβ(TGF-β) monomer that functions as a dominant negative to block TGF-βsignaling. J Biological Chemistry. 2017; 292(17):7173-7188.[26] 周航宇,夏德林,甘生远,等.骨形态发生蛋白2和血管内皮生长因子165双基因转染骨髓基质干细胞的异位诱导成骨能力[J].中国组织工程研究, 2017, 21(9):1334-1339.[27] Bolander J, Ji W, Geris L, et al. The combined mechanism of bone morphogenetic protein- and calcium phosphate-induced skeletal tissue formation by human periosteum derived cells. Eur Cell Mater. 2016;31:11-25.[28] Conway JD,Shabtai L,Bauernschub A,et al.BMP-7 versus BMP-2 for the treatment of long bone nonunion. Orthopedics. 2014;37(12):1049-57.[29] Hegarty SV,Sullivan AM,O'Keeffe GW.Endocytosis contributes to BMP2-induced Smad signalling and neuronal growth. Neurosci Lett. 2017;643:32-37.[30] Su YH,Cai HB,Ye ZY,et al.BMP-7 improved proliferation and hematopoietic reconstitution potential of ex vivo expanded cord blood-derived CD34 +, cells.Human Cell. 2015;28(1): 14-21.[31] Lei H,Wang J,Lu P,et al.BMP10 inhibited the growth and migration of gastric cancer cells.Tumor Biology. 2016;37(3): 3025-3031.[32] Zhang N,Ye L,Wu L,et al.Expression of bone morphogenetic protein-10 (BMP10) in human urothelial cancer of the bladder and its effects on the aggressiveness of bladder cancer cells in vitro. Anticancer Res. 2013 ;33(5):1917-1925.[33] Kallioniemi A. Bone morphogenetic protein 4-a fascinating regulator of cancer cell behavior. Cancer Genet. 2012;205(6): 267.[34] Elias E, Nasser Z, Winegan L, et al. Bone Morphogenetic Proteins Usage in Anterior Lumbar Inter-Body Fusion: What Else Can Go Wrong? World Neurosurg. 2018;111:55-59.[35] Faundez A, Tournier C, Garcia M, et al. Bone morphogenetic protein use in spine surgery—complications and outcomes: a systematic review. Int Orthop. 2016;40(6):1309-1319.[36] Subbiah R, Hwang M P, Van S Y, et al. Osteogenic/ Angiogenic Dual Growth Factor Delivery Microcapsules for Regeneration of Vascularized Bone Tissue. Adv Healthc Mater. 2015;4(13):1982-1992.[37] Kargozar S, Hashemian SJ, Soleimani M, et al. Acceleration of bone regeneration in bioactive glass/gelatin composite scaffolds seeded with bone marrow-derived mesenchymal stem cells over-expressing bone morphogenetic protein-7. Mater Sci Eng C Mater Biol Appl. 2017; 1(75):688-698.[38] Ferrara N,Gerber HP,Lecouter J.The biology of VEGF and its receptors. Nat Med. 2003;9(6):669-676. Review.[39] Liu Y,Olsen BR.Distinct VEGF functions during bone development and homeostasis. Arch Immunol Ther Exp (Warsz). 2014;62(5):363-368.[40] Liu Y,Berendsen AD,Jia S,et al.Intracellular VEGF regulates the balance between osteoblast and adipocyte differentiation.J Clin Invest. 2012;122(9):3101-3113.[41] Yang YQ,Tan YY,Wong R,et al.The role of vascular endothelial growth factor in ossification. 2012;4(2):64-68. Review.[42] Bayer EA,Fedorchak MV,Little SR.The Influence of Platelet-Derived Growth Factor and Bone Morphogenetic Protein Presentation on Tubule Organization by Human Umbilical Vascular Endothelial Cells and Human Mesenchymal Stem Cells in Coculture. Tissue Eng Part A. 2016;22(21-22):1296-1304.[43] Street J,Bao M,Deguzman L,et al.Vascular Endothelial Growth Factor Stimulates Bone Repair by Promoting Angiogenesis and Bone Turnover. Proc Natl Acad Sci U S A. 2002;99(15):9656-9661.[44] Motokawa M,Tsuka N,Kaku M,et al.Age-related production of osteoclasts and the changes of serum levels of vascular endothelial growth factor (VEGF) and receptor activator for nuclear factor (NF)-κB ligand (RANKL) in osteopetrotic (op/op) mice. Arch Oral Biol. 2012;57(4):352-356.[45] Huang H,Ma L,Kyrkanides S.Effects of vascular endothelial growth factor on osteoblasts and osteoclasts. Am J Orthod Dentofacial Orthop. 2016;149(3):366-373.[46] Li CJ,Madhu V,Balian G,et al.Cross-Talk Between VEGF and BMP-6 Pathways Accelerates Osteogenic Differentiation of Human Adipose-Derived Stem Cells.J Cell Physiol. 2015; 230(11):2671-2682.[47] Zhang Y,Madhu V,Dighe AS,et al.Osteogenic response of human adipose-derived stem cells to BMP-6, VEGF, and combined VEGF plus BMP-6 in vitro. Growth Factors. 2012; 30(5):333-343. [48] Chen L,He Z,Chen B,et al.Loading of VEGF to the heparin cross-linked demineralized bone matrix improves vascularization of the scaffold. J Mater Sci Mater Med. 2010; 21(1):309-317.[49] Ogilvie CM,Lu C,Marcucio R,et al.Vascular endothelial growth factor improves bone repair in a murine nonunion model. Iowa Orthop J. 2012;32:90-94.[50] Zhu S,Segura T.Cell-Demanded VEGF Release via Nanocapsules Elicits Different Receptor Activation Dynamics and Enhanced Angiogenesis. Ann Biomed Eng.2016;44(6): 1983-1992.[51] Su YW, Zhou XF, Foster BK,et al. Roles of neurotrophins in skeletal tissue formation and healing. J Cell Physiol. 2018 ; 233(3):2133-2145.[52] Zhang N,Chen J,Ferraro G,et al.Anti-VEGF treatment improves neurological function in tumors of the nervous system. Exp Neurol. 2018 ;299(Pt B):326-333. [53] Yang ZQ,Zhang HL,Duan CC,et al.IGF1 regulates RUNX1 expression via IRS1/2: implications for antler chondrocyte differentiation.Cell Cycle.2017;16(6):522-532.[54] Zhang Z,Li L,Yang W,et al.The effects of different doses of IGF-1 on cartilage and subchondral bone during the repair of full-thickness articular cartilage defects in rabbits. Osteoarthritis Cartilage. 2017;25(2):309-320.[55] Sheng MH,Zhou XD,Bonewald LF,et al.Disruption of the insulin-like growth factor-1 gene in osteocytes impairs developmental bone growth in mice.Bone.2013;52(1): 133-144.[56] Oikonomopoulos N,Fincher M,Abraham D,et al.IGF-1 has no effect on the proliferation and differentiation of ischaemic myoblasts.British Journal of Surgery.2013:52-53. [57] Fujioka-Kobayashi M,Schaller B,Zhang Y,et al.Recombinant human bone morphogenetic protein (rhBMP)9 induces osteoblast differentiation when combined with demineralized freeze-dried bone allografts (DFDBAs) or biphasic calcium phosphate (BCP). Clin Oral Investig. 2017;21(5):1883-1893.[58] Inoue G,Uchida K,Matsushita O,et al.Effect of Freeze-Dried Allograft Bone with Human Basic Fibroblast Growth Factor Containing a Collagen-Binding Domain from Clostridium Histolyticum Collagenase on Bone Formation after Lumbar Posterolateral Fusion Surgery in Rats.Spine.2017; 42(17): E995-E1001. |
| [1] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [2] | Zeng Yanhua, Hao Yanlei. In vitro culture and purification of Schwann cells: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1135-1141. |
| [3] | Yang Weiqiang, Ding Tong, Yang Weike, Jiang Zhengang. Combined variable stress plate internal fixation affects changes of bone histiocyte function and bone mineral density at the fractured end of goat femur [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(6): 890-894. |
| [4] | Xu Dongzi, Zhang Ting, Ouyang Zhaolian. The global competitive situation of cardiac tissue engineering based on patent analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 807-812. |
| [5] | Wu Zijian, Hu Zhaoduan, Xie Youqiong, Wang Feng, Li Jia, Li Bocun, Cai Guowei, Peng Rui. Three-dimensional printing technology and bone tissue engineering research: literature metrology and visual analysis of research hotspots [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 564-569. |
| [6] | Chang Wenliao, Zhao Jie, Sun Xiaoliang, Wang Kun, Wu Guofeng, Zhou Jian, Li Shuxiang, Sun Han. Material selection, theoretical design and biomimetic function of artificial periosteum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 600-606. |
| [7] | Liu Fei, Cui Yutao, Liu He. Advantages and problems of local antibiotic delivery system in the treatment of osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 614-620. |
| [8] | Li Xiaozhuang, Duan Hao, Wang Weizhou, Tang Zhihong, Wang Yanghao, He Fei. Application of bone tissue engineering materials in the treatment of bone defect diseases in vivo [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 626-631. |
| [9] | Zhang Zhenkun, Li Zhe, Li Ya, Wang Yingying, Wang Yaping, Zhou Xinkui, Ma Shanshan, Guan Fangxia. Application of alginate based hydrogels/dressings in wound healing: sustained, dynamic and sequential release [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 638-643. |
| [10] | Chen Jiana, Qiu Yanling, Nie Minhai, Liu Xuqian. Tissue engineering scaffolds in repairing oral and maxillofacial soft tissue defects [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 644-650. |
| [11] | Cheng Shigao, , Wang Wanchun, Jiang Dong, Li Tengfei, Li Xun, Ren Lian. Comparison of the standard and long-stem bone cement prosthesis replacement in the treatment of intertrochanteric fractures in elderly patients [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 362-367. |
| [12] | Xing Hao, Zhang Yonghong, Wang Dong. Advantages and disadvantages of repairing large-segment bone defect [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 426-430. |
| [13] | Chen Siqi, Xian Debin, Xu Rongsheng, Qin Zhongjie, Zhang Lei, Xia Delin. Effects of bone marrow mesenchymal stem cells and human umbilical vein endothelial cells combined with hydroxyapatite-tricalcium phosphate scaffolds on early angiogenesis in skull defect repair in rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3458-3465. |
| [14] | Wang Hao, Chen Mingxue, Li Junkang, Luo Xujiang, Peng Liqing, Li Huo, Huang Bo, Tian Guangzhao, Liu Shuyun, Sui Xiang, Huang Jingxiang, Guo Quanyi, Lu Xiaobo. Decellularized porcine skin matrix for tissue-engineered meniscus scaffold [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3473-3478. |
| [15] | Mo Jianling, He Shaoru, Feng Bowen, Jian Minqiao, Zhang Xiaohui, Liu Caisheng, Liang Yijing, Liu Yumei, Chen Liang, Zhou Haiyu, Liu Yanhui. Forming prevascularized cell sheets and the expression of angiogenesis-related factors [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3479-3486. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||