Chinese Journal of Tissue Engineering Research ›› 2026, Vol. 30 ›› Issue (32): 8479-8486.doi: 10.12307/2026.297
Previous Articles Next Articles
Potential and application prospects of combined treatment of acute myocardial infarction with hydrogel cardiac patches and traditional Chinese medicine
Ding Hao1, 2, 3, Gao Yuan1, 2, 4, Li Bin1, 2, 4, Yu Rui1, 2, 4, Wang Jianru1, 2, 4, Sun Yudie1, 2, 3, Wang Xuanyang1, 2, 3, Zhang Wenping1, 2, 3, Zhu Mingjun1, 2, 4
- 1Cardiology Center/Experimental Center, First Affiliated Hospital of Henan University of Chinese Medicine, Zhengzhou 450000, Henan Province, China; 2Collaborative Innovation Center of Prevention and Treatment of Major Diseases by Chinese and Western Medicine, Zhengzhou 450000, Henan Province, China; 3First Clinical Medical College of Henan University of Chinese Medicine, Zhengzhou 450000, Henan Province, China; 4Henan Provincial Engineering Research Center for Safety Evaluation and Risk Prevention of Traditional Chinese Medicine, Zhengzhou 450000, Henan Province, China
-
Accepted:2025-12-19Online:2026-11-18Published:2026-04-28 -
Contact:Gao Yuan, MD, Chief physician, Doctoral supervisor, Cardiology Center/Experimental Center, First Affiliated Hospital of Henan University of Chinese Medicine, Zhengzhou 450000, Henan Province, China; Collaborative Innovation Center of Prevention and Treatment of Major Diseases by Chinese and Western Medicine, Zhengzhou 450000, Henan Province, China; Henan Provincial Engineering Research Center for Safety Evaluation and Risk Prevention of Traditional Chinese Medicine, Zhengzhou 450000, Henan Province, China -
About author:Ding Hao, MS candidate, Cardiology Center/Experimental Center, First Affiliated Hospital of Henan University of Chinese Medicine, Zhengzhou 450000, Henan Province, China; Collaborative Innovation Center of Prevention and Treatment of Major Diseases by Chinese and Western Medicine, Zhengzhou 450000, Henan Province, China; First Clinical Medical College of Henan University of Chinese Medicine, Zhengzhou 450000, Henan Province, China -
Supported by:National Natural Science Foundation of China (Key Project), No. 82030120 (to ZMJ); National Natural Science Foundation of China (Youth Science Fund Project), No. 81503435 (to GY); Henan Provincial International Science and Technology Cooperation Project, No. 252102521036 (to GY); Henan Provincial Key Research and Development and Promotion Project (Science and Technology Breakthrough), No. 242102310554 (to GY); Henan Provincial Traditional Chinese Medicine Scientific Research Special Project, No. 2022ZY2009 (to GY); National Clinical Research Base Scientific Research Project of Henan Provincial Administration of Traditional Chinese Medicine, No. 2018JDZX058 (to GY); Henan Provincial Key Research and Development and Promotion Project (Science and Technology Breakthrough), No. 242102310527, 252102310470 (to WJR); 2024 Graduate Student Scientific Research Innovation Capacity Improvement Plan Project of Henan University of Traditional Chinese Medicine, No. 2024KYCX059 (to SYD)
CLC Number:
Cite this article
Ding Hao, Gao Yuan, Li Bin, Yu Rui, Wang Jianru, Sun Yudie, Wang Xuanyang, Zhang Wenping, Zhu Mingjun. Potential and application prospects of combined treatment of acute myocardial infarction with hydrogel cardiac patches and traditional Chinese medicine[J]. Chinese Journal of Tissue Engineering Research, 2026, 30(32): 8479-8486.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
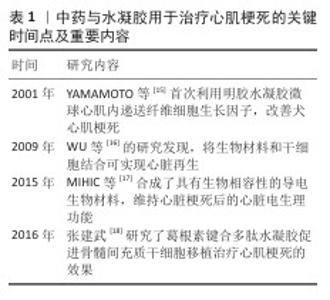
2.1 中药与水凝胶用于治疗心肌梗死的关键时间点及重要内容 见表1。 2.2 心脏贴片材料 2.2.1 传统合成材料和天然生物材料 传统合成材料:传统材料中应用较广泛的是涤纶材料和聚四氟乙烯/膨体聚四氟乙烯材料。涤纶材料具有良好的生物相容性、较强的机械强度和弹性、透气、易塑形、质地轻薄、取材容易且价格低廉等特点,被广泛用于心血管手术。但是涤纶浸润生理盐水或血液后的弹性变差,缝合后易发生褶皱,导致吻合口变形,并且植入人体后会有排异反应,可能引起感染、溶血、血栓栓塞的风险。膨体聚四氟乙烯和聚四氟乙烯都能够耐高温和低温,具有很强的热稳定性、耐腐蚀性,摩擦系数低,不宜粘连,是生物惰性材料,植入人体不易引起排斥反应[19]。 但膨体聚四氟乙烯具有电绝缘性,不利于心肌细胞的电传导联通修复;膨体聚四氟乙烯和聚四氟乙烯由于特有的不沾性,负载的生物活性分子容易脱落并很难贴附在心脏上,而且聚四氟乙烯可能引发较高的血栓发生率,分子通过率低,容易引起较严重的腹腔粘连[20-21]。通常聚四氟乙烯和膨体聚四氟乙烯补片多应用于伤口修复,两种材料较大的气孔结构能有利于血管的生成,加快伤口愈合,但同时也增加了粘连内脏的风险;虽经调整制成微孔补片后能减少粘连,但是不易整合细胞,易感染。若植入聚四氟乙烯补片后感染,只能将补片移除[22]。 天然生物材料:天然生物材料中较有代表性的材料是脱细胞细胞外基质。脱细胞细胞外基质是通过去除自体或同种异体天然组织中的细胞成分来保留天然组织的结构和功能性细胞外基质,具有良好的生物相容性。脱细胞细胞外基质中丰富的活性生长因子和基质细胞蛋白及其自然降解产物,通过生物诱导机制驱动内源性心脏修复和血管生成,有助于受损心肌的再生、修复和重塑。SARIG等[23]用猪心脏脱细胞细胞外基质来制作脱细胞心脏贴片,该贴片具备吸引和募集内源性祖细胞的能力,使细胞密度随着细胞外基质的降解而增加。 "
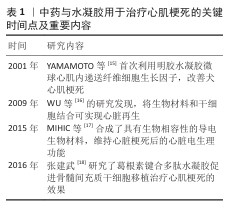
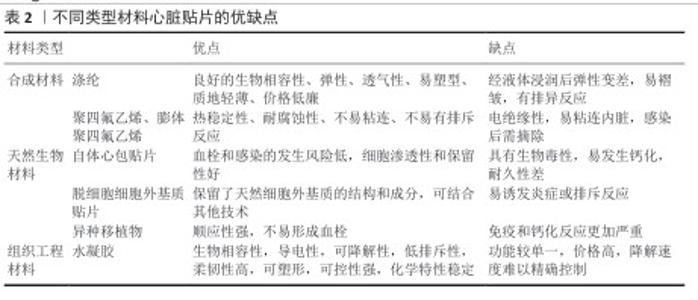
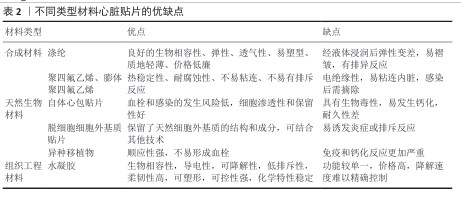
2.2.2 水凝胶材料 水凝胶的生物特性:水凝胶是一种具有三维网状结构的新型材料,这种聚合物拥有高吸水性和高保水性,能够在吸收大量水分后仍然保留原有的持物理性能,同时具有生物相容性、导电性、可降解性、低排斥性和类似细胞外基质的三维多孔结构等优势[24-25]。通过不同的物理或化学交联技术能够改变水凝胶的机械强度,以承受心脏的快速收缩以及支持心肌对心室壁的机械扩张重塑[26-27]。水凝胶的基底聚合物材料包括天然生物聚合物(如纤维蛋白、壳聚糖、海藻酸钠、胶原蛋白、透明质酸等)和合成聚合物(如聚己内酯、聚乙烯醇、聚氧乙烯、聚丙烯酰胺等)[28-29]。不同的基材与交联方法使水凝胶具有不同方面的突出优势,天然聚合物具有固有的生物相容性、生物活性和生物降解性,但稳定性和机械强度相对较弱;合成聚合物具有良好的稳定性,机械强度大,但生物相容性较差[30]。不同的基底材料和交联方式赋予水凝胶不同的状态和特点,水凝胶分为原位水凝胶、智能水凝胶、纳米复合水凝胶、互穿网络结构水凝胶等多种种类。 水凝胶的优劣:水凝胶具有卓越的生物相容性和仿生特性,能够为移植细胞或药物活性成分提供类生理微环境,显著提升细胞和生物分子活力;优异的生物环境适应性,使其在不同生理条件下都能保持结构稳定性,不易发生溶解或降解,这些特性使水凝胶成为心脏组织工程中极具前景的植入物和递送载体。基于水凝胶在心肌修复中的应用需求,BAR研究团队[31]提出了水凝胶三大关键设计标准:适宜的机械强度(弹性模量0.1-20 kPa),以匹配心肌组织的力学特性;能够维持负载细胞或生物分子存活的稳定物理化学微环境;足够的体内存留时间,以确保治疗效果的持续发挥。 尽管水凝胶具有实现多种功能的潜力,但其多功能化通常依赖于复杂的物理或化学交联策略,包括主客体相互作用、共价接枝、酶促交联和靶向修饰等,这些方法不仅增加了制备成本,也使工艺过程更为复杂;此外,多重加工步骤可能导致水凝胶的关键性能参数(如力学强度、降解速率和生物活性等)难以精确调控。然而,与其他生物材料相比,水凝胶在心肌梗死治疗用心脏贴片的开发中仍具有显著优势,主要体现在其优异的生物相容性、可调节的力学性能以及与心肌组织匹配的力学环境,使水凝胶在心脏修复领域展现出独特的应用潜力。表2详细列举了不同材料心脏贴片的优缺点。 水凝胶的应用:水凝胶的一些有利生物特性能和电导率相结合能够帮助心肌电活性组织传导电信号,恢复梗死瘢痕组织区域的节律性脉冲搏动,激活生物电信号通路,调节相关蛋白水平表达,重建心脏细胞间同收缩活动传导,促进组织恢复[32-34]。电导率可以增强心肌细胞间钙离子信号的传导,激活经典Wnt信号通路,建立健康心肌与梗死区域心肌细胞之间的电连接,消除内部心律不齐,促进心肌内部搏动速率,结合水凝胶的机械性能可以改善电解耦引起的室壁功能障碍,支持同步室壁收缩并改善心脏功能[35]。NAVAEI等[36]将金纳米棒嵌入水凝胶中增强水凝胶的导电特性,发现此导电构建体促进了细胞间信号传导和电信号传播。TARIQ等[10]研究发现,具有电子导电性的水凝胶贴片能够明显减弱大鼠心肌梗死模型中心肌细胞的重塑,改善心脏收缩力和心脏功能。YU等[34]通过动态共价/非共价交联开发了一种可注射的机械-电耦合水凝胶贴片,该贴片能够改善心脏健康与梗死区域之间的电连接,提高传导速度和同步率。 心肌梗死的细胞再生治疗目前主要采用间充质干细胞等多功能干细胞的直接移植策略,然而该方法的临床应用面临两大关键挑战:移植细胞的存活率低下以及植入后的滞留率不佳,这一困境亟需开发新型载体系统以改善细胞存活和定植效率。传统合成材料制备的心脏贴片虽然在机械性能方面表现良好,但在功能性方面存在明显不足,主要表现为缺乏主动募集内源性干细胞的能力,并且无法持续释放生物活性分子以促进组织再生[37]。水凝胶的高生物相容性和仿生性质能够满足细胞的生存需求,保持细胞活性,因此,水凝胶材料因独特的生物学特性成为解决这一问题的理想选择。 不同种类的水凝胶因结构特性差异而表现出多样化的功能。原位水凝胶在液态状态下具有良好的流动性,可通过注射精准定位至目标部位,在生理环境或外部刺激下能迅速发生相变形成固态凝胶,这一特性使其特别适合构建温敏型原位注射给药系统,实现药物的靶向递送与缓释控制[38]。互穿网络结构水凝胶具有独特的双网络架构,不仅能维持对pH值和温度变化的快速响应能力,还可通过调控网络结构来优化凝胶性能,这类水凝胶展现出优异的血液相容性和强大的力学性能,在细胞再生支架应用中具有显著潜力[39]。纳米水凝胶结合了纳米材料的刚性、尺寸稳定性、热稳定性与水凝胶的软湿特性,使材料机械性能显著提升,并且对外界刺激响应更为灵敏,这种独特的性能组合使它成为理想的药物递送载体[40]。智能水凝胶能够可逆响应环境变化(如温度、pH值、光、磁场等),其溶胀行为会随外界刺激发生显著改变,这种“突跃性”响应体现在水凝胶的形状、力学性能、光学特性、渗透速率及分子识别能力等多个方面,并且变化过程完全可逆。基于这一特性,智能水凝胶在医用敷料、可控药物释放系统等领域展现出广阔的应用前景[41]。因此,中药可以在这几种水凝胶心脏贴片的应用场景中联合应用,提高疗效。表3详细列举了中药联合水凝胶心脏贴片的应用场景。 "
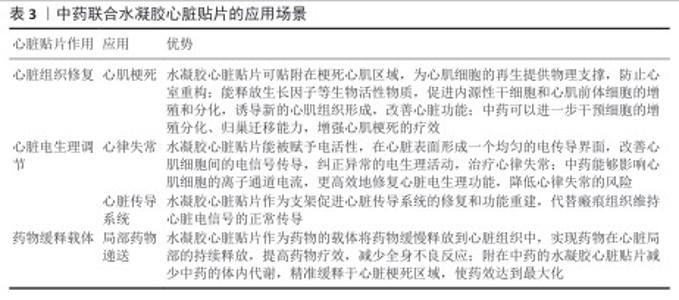
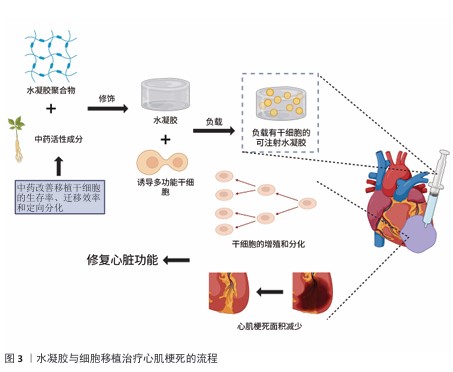
2.3 中药结合水凝胶心脏贴片的应用 2.3.1 基于细胞移植的水凝胶心脏贴片 水凝胶作为一种亲水的聚合物生物材料,其三维网络结构能够高度模拟天然心脏细胞外基质的物理特性(如孔隙率、力学强度和拓扑结构等),为负载的生物细胞提供繁殖或保持活性的微环境,并帮助细胞迁移、黏附、扩散、分化、形成细胞间连接[42-44],这种特性有效克服了传统细胞移植再生疗法中细胞保留、移植和存活困难的缺点。在干细胞治疗方面,多功能干细胞(如胚胎干细胞、间充质干细胞和诱导多功能干细胞)因强大的增殖能力和多向分化潜能,较成熟心肌细胞更具治疗优势。研究表明,多功能干细胞与水凝胶结合后可通过旁分泌信号激活心脏保护机制,显著改善心肌梗死治疗效果[45]。郎丽敏[46]将人子宫内膜间充质干细胞来源的心肌细胞与可注射导电水凝胶联合,用于修复心肌梗死。诱导多功能干细胞分化的心肌细胞不仅有成熟心肌细胞的超微结构如肌球蛋白、线粒体等,还具备心肌细胞典型的功能特征:自发性搏动、节律收缩、离子通道蛋白表达以及动作电位模式,相比平滑肌细胞和间充质干细胞能够显著的改善心脏功能[47]。 ISHIDA等[48]对比研究了人诱导多功能干细胞和人成体干细胞对猪心肌梗死的治疗效果,发现诱导多功能干细胞在恢复心脏功能、改善心肌梗死后心肌耗氧量和抑制心肌细胞凋亡方面更加优秀。水凝胶材料因可调的物理化学性质(如硬度、拓扑结构等)可作为理想的细胞培养支架,通过模拟心肌组织的微环境来促进干细胞向成熟心肌细胞分化[49]。HASHEMI等[50]开发了一种封装了诱导多功能干细胞的聚乙二醇-纤维蛋白原微球水凝胶,能实现高效的心脏分化和心肌细胞生成。有研究制备了含有糖原合酶激酶3α抑制剂CHIR99021和负载成纤维细胞生长因子1聚乳酸-羟基乙酸聚合物纳米颗粒的收缩性纤维蛋白基细胞心脏贴片,用于治疗在小鼠心肌梗死,给药后4周显著增加了人诱导多功能干细胞诱导的心肌细胞周期活性,促进血管新生并减少了细胞凋亡,减小梗死面积,改善心脏功能[51]。然而,诱导多功能干细胞的应用仍存在诸多障碍,例如分化效率低、安全风险等,现有的诱导剂毒性较大、靶点较多,可能引发不良反应,不适合在临床上使用;同时诱导多功能干细胞的无限增殖与自我更新的特性,在临床应用中易诱发心律失常与致瘤风险[52]。 中药在心肌梗死治疗中展现出独特的优势,不仅整体疗效显著,有着多靶点、多途径、毒性低的特点,在细胞层面还具有调控作用。中医药能够提高干细胞移植的存活率,抑制炎症反应与心肌细胞凋亡;能动员和迁移干细胞,促进干细胞向损伤部位定向迁移,抑制心肌损伤;能干预干细胞增殖分化过程,提高干细胞的定向分化能力,也赋予干细胞更好的疗效[53-54]。例如,柴胡疏肝散结合骨髓间质干细胞移植通过激活磷脂酰肌醇3激酶/蛋白激酶B/Bcl-2信号途径和磷脂酰肌醇3激酶/蛋白激酶B/糖原合酶激酶3β信号途径,提高抗氧化应激能力和促进血管内皮生长因子的蛋白表达,从而抑制心肌细胞凋亡[55]。银杏叶的有效成分也能改变心肌微环境,延缓心肌组织纤维化,减少心肌细胞死亡。丹红注射液能调节基质细胞衍生因子1/趋化因子受体 4信号通路,延长干细胞在心肌组织中的停留时间,提高移植效率[56]。活血化瘀药物不仅能够增强干细胞动员剂的效果,同时还能够提高骨髓间充质干细胞的出髓效率,增加心肌梗死区域外周血中骨髓间充质干细胞的含量,促进干细胞向梗死区域迁移[57]。丹参多酚酸盐可募集骨髓源性心肌干细胞至心肌梗死后的受损伤心肌募集损伤区域,增加外周血中基质细胞衍生因子1的表达,修复心肌损伤[58]。中药麦冬能够诱导骨髓间充质干细胞分化为心肌样细胞,该细胞在形态和电生理特征上均与人体生理的心肌细胞相似,并且诱导率与5-氮胞苷相当,同时中药麦冬还具备改善心肌收缩力、保护心肌细胞的作用[59]。 中药与水凝胶材料相结合构建的干细胞递送系统,是通过修饰方式将中药有效活性成分与水凝胶相融合。用中药修饰过的水凝胶负载干细胞,可对干细胞进行充分的诱导和调控,更有效地对心肌梗死区域进行细胞再生治疗(图3)。LEVIT等[60]研究发现,藻酸盐水凝胶可提高缺氧环境下人间充质干细胞的活力及其心肌中细胞的滞留水平。LI等[61]用叶酸修饰的水凝胶包封诱导多能干细胞移植治疗心肌梗死,发现叶酸水凝胶显著提升了诱导多功能干细胞的移植保留率和向心肌样细胞分化的比例,有效减少了心肌梗死面积,改善心肌梗死后的心脏功能。张建武[18]发现,葛根素键合多肽水凝胶可在过氧环境下提升骨髓间充质干细胞的存活率,增强细胞移植治疗大鼠心肌梗死的疗效。LIU等[62]将葛根素与多两性离子微凝胶交联并包埋骨髓间充质干细胞,用于促进心室功能和结构的高效修复。因此,用中药有效活性成分修饰水凝胶负载干细胞能更好地保存干细胞活性,提升细胞增殖与分化能力,促进心脏功能恢复。 "
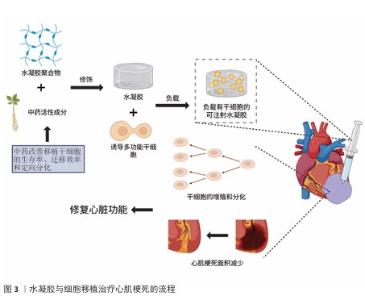
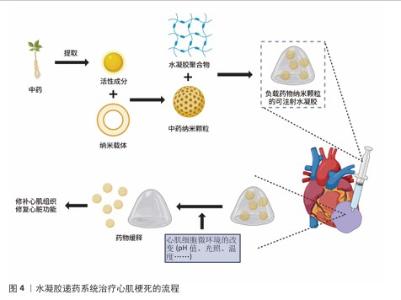
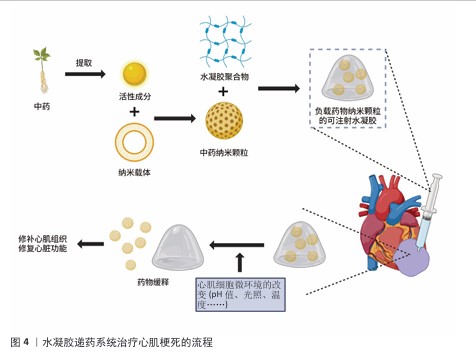
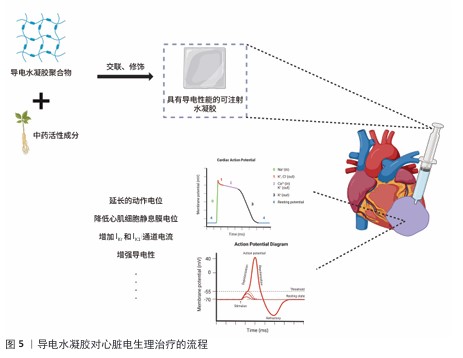
2.3.2 基于药物递送的水凝胶心脏贴片 水凝胶的生物相容性、药物包封能力、可控的降解性和灵活的物理性质能保护不稳定药物免于降解[63]。水凝胶作为药物递送平台具有局部药物递送浓度高、缓释性和低毒性等优点[64]。一些聚合物(如壳聚糖)会对刺激产生反应,这类材料制备的水凝胶能够根据周围环境(包括温度、pH值、电磁辐射、磁场、生物因素等)的改变而改变特性,如机械性能、溶胀能力、亲水性或生物活性分子的渗透性,并且水凝胶的网格尺寸会随着刺激而改变,具体取决于形成或断裂的交联键浓度。智能水凝胶是一种能够对外界刺激(如温度、pH值、光、化学物质等)产生敏感响应的高分子材料,具有可逆性和可调节性[65-66]。OMRANI等[67-68]设计了一种壳聚糖多响应纳米水凝胶网络的控制药物递送系统,这种合成的水凝胶对外部温度、pH值等刺激都有显著的响应。在心肌梗死治疗中,也可将水凝胶设计成高活性氧反应来释放药物。ZHENG等[69]研究了一种高活性氧反应性的脂质体复合水凝胶,局部递送脂质体以清除过量的活性,进而改善线粒体功能障碍和促进血管生成,改善心脏功能。 水凝胶递药系统仍然存在一些问题,比如药物在释放前被降解、给药时会存在爆发释放、包封某些药物的能力有限、调整结构控制药物精确释放的能力有限[70]。因此,纳米水凝胶开始出现。纳米水凝胶一种由化学或物理交联的可膨胀聚合物网络系统形成的三维纳米尺寸结构水凝胶,通过包埋技术将纳米颗粒载体加载到凝胶中,然后进行还原反应以形成纳米颗粒[71-72]。水凝胶的湿软特性可增强纳米颗粒的黏附性。FULLENKAMP等[73]开发了一种由银纳米颗粒和组织黏合水凝胶组成的银释放抗菌NP凝胶,在该设计中,水凝胶构建材料聚乙二醇被反应性邻苯二酚部分修饰来模拟贻贝黏附蛋白的功能,其中含有邻苯二酚的氨基酸3,4-二羟基苯丙氨酸使贻贝能够黏附在水性环境中的各种表面。纳米颗粒技术为药物递送提供了许多优势,包括高载样量、联合治疗、控释、延长循环和靶向递送[74]。药物掺入纳米载体有5种方法:溶解、包封、吸附、连接或包封在普通纳米水凝胶的表面进行配体或者抗体等修饰,能赋予纳米水凝胶在体内对相应受体、抗原等的主动靶向性,促进药物的摄取[75]。氧化还原反应性纳米载体是一种很有前途的细胞内药物释放策略,因为它可以保护有效载荷,防止其在细胞外运输过程中的不良泄漏,并有利于特定部位的药物递送[76]。 中药有效成分存在不够稳定、水溶性低、体内代谢迅速等问题[77],传统的口服中药在胃肠酸性环境与消化酶存在下会分解变性,经过机体代谢后的人体吸收利用率较低。纳米技术加工处理显著提高了中药有效成分的溶解性与稳定性[78],减少胃肠环境刺激下药量和药物活性的损失,促进细胞摄取并提高病理部位的靶向性,克服目前中药有效成分应用中面临的局部药物浓度低、见效慢、利用率低、用量大等难题[79]。纳米递药系统具有很好的缓释性,能避免药物过早或突然大量释放,使得递药系统在特定靶向部位均匀缓慢持续地释放药物[80]。已经有许多研究将中药血清或者中药活性成分负载在水凝胶中,通过水凝胶的多重响应机制将药物投放到心肌梗死区域进行治疗(图4)。WANG等[81]利用喜树碱与氧化铁制备了pH值与H2O2双重响应纳米囊,该纳米囊延长了药物体内循环时间、降低了药物全身毒性。柳成荫[82]使用可注射水凝胶携带牛蒡苷元增强了心肌缺血损伤的治疗效果。岳田等[83]发现,可注射水凝胶包裹姜黄素纳米胶束后显著改善了心肌细胞凋亡和心肌梗死后的高炎症与活性氧环境。ZHANG等[84]制备了pH值/活性氧双响应的可注射水凝胶,包封迷迭香酸钠实现微反应释放,促进心肌梗死心脏功能的恢复。YU等[85]设计了热敏可注射水凝胶装载丹参酮IIA,该载体可发挥抗炎作用,有利于心肌梗死后的左心室重塑。LIU等[86]将含有牛蒡苷元的水凝胶植入缺血再灌注大鼠心肌中改善了心功能,抑制了心肌纤维化。WANG等[87]设计了长效水凝胶平台心内注射递送三七皂苷,增强了心肌梗死过程中的抗炎反应。中药提取物中姜黄素、丹参酮ⅡA及秋水仙碱对心肌梗死都有治疗效果,但口服给药利用率低、中毒风险较高,所以利用水凝胶负载药物形成药物缓释系统,既改善了药物利用率还避免了毒性,同时可以借助水凝胶强大的力学性能为受损心脏组织提供支持[88]。纳米水凝胶还能与其他纳米递送系统结合,例如脂质体和外泌体,延缓其降解并提高递送效率[89]。 2.3.3 基于改善电生理特性的导电水凝胶心脏贴片 心肌梗死后会逐渐演变为缺血性心力衰竭,该过程中有很高的心律失常风险。梗死区域缺血缺氧造成心脏组织结构改变、细胞死亡与功能障碍,同时梗死区域的瘢痕组织无法进行正常电传导,导致心肌电生理改变、离子通道异常[90]。梗死环境缺血缺氧,导致钠钾泵抑制,钠钾通道交换减少,细胞内钠离子和细胞外钾离子浓度增加,引起心肌细胞静息膜电位绝对值降低,静息膜电位接近阈电位,使心肌细胞的兴奋性增强[91-92];但是瞬时外向钾电流(Ito)减少和钠通道开放降低,使细胞动作电位幅度、动作电位上升速度(Vmax)降低,易诱发2相折返。随着心肌梗死的发生,细胞内Mg2+和多胺等物质离子浓度改变,影响钾离子通道的通透性,导致内向整流钾电流(IK1)、延迟整流钾通道电流(IKr)减少[93-94]。IK1和IKr在动作电位晚期复极化(3期)中具有重要作用,IK1和IKr的减少导致细胞复极化时间延长,整个动作电位时程APD延长;复极化的时间延长引起复极化不应态,心肌梗死边缘区域的不同心室肌细胞Ito通道跨膜异质性增加,使心肌细胞有效不应期离散,易引起折返性心率 失常[95]。 导电水凝胶在维持心脏正常收缩的同时,帮助心脏进行梗死区域的电传导与电耦合,但是梗死区域的离子通道和电生理特性改变难以快速恢复,有引发心律失常的危险。中药活性成分具有来源广泛、生物活性强、靶点明确、毒性低等优势。有研究表明,中药活性成分能够作用于离子通道,例如苦参碱是苦参的有效活性成分,能够延长动作电位APD50、APD9和有效不应期,但不会影响动作电位幅度、动作电位上升速度和静息膜电位,能够抑制由于动作电位时程缩短引起的心肌细胞自律性增强、折返机制和心律失常易感性[96]。银杏叶提取物可以提高心室肌细胞的Ito电流、缩短动作电位时程、缓解细胞内钠离子和钙离子超载引发的心律失常和心肌损伤[97]。葛根素能够提高心肌细胞抗氧化能力、提高Na2+-K+ATP酶活性、增加钠钾离子交换、维持心肌细胞内外电平衡、维持正常静息膜电位,降低心律失常的发生[98]。 因此,可以借助导电水凝胶的高生物相容性封装中药活性成分,直接作用于梗死区域,改善区域电导率和离子通道改变,保护心脏正常电生理学,降低心肌梗死后心律失常的易感性(图5)。ZHANG等[84]制作了一种对pH值和活性氧有双重响应的可注射迷迭香酸导电水凝胶,研究了该水凝胶对心肌梗死后心脏功能和电生理学的影响,发现梗死区弱兴奋性的瘢痕组织会阻断非梗死心肌中电信号的传导,导致室性心律失常;相比其他对照组,迷迭香酸导电水凝胶可以降低心肌瘢痕组织的电阻率,恢复瘢痕区域到健康区域的电传导,激活存活的心肌细胞产生正常的动作电位,显著改善电脉冲信号在梗死心肌中的传递;此外,瘢痕中电传输的增加会减少电信号单向出口阻塞的数量,降低室性心律失常形成电路的可能性。LUO等[99]采用基质细胞衍生因子1α封装葛根素制备水凝胶来调节细胞间耦合、改善电传导,发现基质细胞衍生因子1α@葛根素水凝胶能限制动作电位APD90的延长,抑制由有效不应期过度延长引起的室性心律失常;抑制梗死区域引起的去极化峰值高度降低,保护心肌细胞的去极化和复极化,有利于维持心肌细胞正常的生理兴奋性;显著增强了瞬态Ca2+的传播,缩短了Ca2+瞬变时程,减轻心肌功能损伤。因此,将中药单体和导电水凝胶结合能够在电导率和离子通道两方面改善心脏功能,降低心肌梗死后心律失常的发生率。 "
| [1] 刘明波,何新叶,杨晓红,等.《中国心血管健康与疾病报告2023》要点解读[J].中国心血管杂志,2024,29(4):305-324. [2] BUGGER H, PFEIL K. Mitochondrial ROS in myocardial ischemia reperfusion and remodeling. Biochim Biophys Acta Mol Basis Dis. 2020;1866(7):165768. [3] 高东杰.心脉宁通过调节MLK3/JNK/P38MAPK信号通路干预心肌梗死后心力衰竭的实验研究[D].天津:天津中医药大学,2023. [4] 丁成斌,邵子怡,曾钰婷,等.仿生心肌微环境介导的材料生物学研究[J].广州医药,2024, 55(5):448-456,462. [5] ZHANG J, GUO Y, BAI Y, et al. Application of biomedical materials in the diagnosis and treatment of myocardial infarction. J Nanobiotechnology. 2023;21(1):298. [6] AJAJ Y, AKINGBESOTE ND, QYANG Y. PECUU-ECM Patches: The Future of Ischemic Heart Disease Repair. JACC Basic Transl Sci. 2021;6(5):464-466. [7] 梁婷婷.多功能水凝胶包裹Chrysin-7-O-glucuronide促进心肌梗死修复的研究[D].重庆:重庆理工大学,2024. [8] 吴学平,吕叶辉.生物材料在心脏再生修复过程中的应用[J].中国动脉硬化杂志,2024,32(6): 539-546. [9] 王颖薇,秦子夕,武征.心肌补片的制备与结构功能特点[J].中国组织工程研究,2015,19(38): 6211-6216. [10] TARIQ U, GUPTA M, PATHAK S, et al. Role of Biomaterials in Cardiac Repair and Regeneration: Therapeutic Intervention for Myocardial Infarction. ACS Biomater Sci Eng. 2022;8(8):3271-3298. [11] MEI X, CHENG K. Recent Development in Therapeutic Cardiac Patches. Front Cardiovasc Med. 2020;7:610364. [12] 周佳妮,蒋学俊.水凝胶补片改善心肌梗死后心室重构的研究进展[J/OL].中国心脏起搏与心电生理杂志,1-4[2025-11-25].https://link.cnki.net/urlid/42.1421.R.20240828.1410.004. [13] 邵茹冰,李杰华,王伦常,等.补片材料在心血管手术中的应用进展[J].中南大学学报(医学版),2023,48(2):285-293. [14] 张棂,祝雨辰,梁金萍,等.水凝胶负载中药的策略及在疾病治疗中的应用[J].中草药,2024, 55(24):8678-8690. [15] YAMAMOTO T, SUTO N, OKUBO T, et al. Intramyocardial delivery of basic fibroblast growth factor-impregnated gelatin hydrogel microspheres enhances collateral circulation to infarcted canine myocardium. Jpn Circ J. 2001;65(5):439-444. [16] WU J, ZENG F, WEISEL RD, et al. Stem cells for cardiac regeneration by cell therapy and myocardial tissue engineering. Adv Biochem Eng Biotechnol. 2009;114:107-128. [17] MIHIC A, CUI Z, WU J, et al. A Conductive Polymer Hydrogel Supports Cell Electrical Signaling and Improves Cardiac Function After Implantation into Myocardial Infarct. Circulation. 2015;132(8): 772-784. [18] 张建武.葛根素水凝胶在MSCs移植治疗心肌梗死中的作用及机制研究[D].广州:南方医科大学,2016. [19] ZHANG J, WANG Y, LIU C, et al. Polyurethane/polyurethane nanoparticle‐modified expanded poly(tetrafluoroethylene) vascular patches promote endothelialization. J Biomed Mater Res A. 2018;106(8):2131-2140. [20] 杜娟.疝修补补片的现状、分类和未来[J]. 透析与人工器官,2023,34(3):71-75. [21] ABURAHMA Z, WILLIAMS E, LEE A, et al. Long-term durability and clinical outcome of a prospective randomized trial comparing carotid endarterectomy with ACUSEAL polytetrafluoroethylene patching versus pericardial patching. J Vasc Surg. 2023;77(6): 1694-16999.e2. [22] LI Z, GIARTO J, ZHANG J, et al. Anti-thrombotic poly(AAm-co-NaAMPS)-xanthan hydrogel-expanded polytetrafluoroethylene (ePTFE) vascular grafts with enhanced endothelialization and hemocompatibility properties. Biomater Adv. 2023;154:213625. [23] SARIG U, SARIG H, DE-BERARDINIS E, et al. Natural myocardial ECM patch drives cardiac progenitor based restoration even after scarring. Acta Biomater. 2016;44:209-220. [24] HO TC, CHANG CC, CHAN HP, et al. Hydrogels: Properties and Applications in Biomedicine. Molecules. 2022;27(9):2902. [25] LIANG Y, HE J, GUO B. Functional Hydrogels as Wound Dressing to Enhance Wound Healing. ACS Nano. 2021;15(8):12687-12722. [26] RODNESS J, MIHIC A, MIYAGI Y, et al. VEGF-loaded microsphere patch for local protein delivery to the ischemic heart. Acta Biomater. 2016;45:169-181. [27] KHAN F, ATIF M, HASEEN M, et al. Synthesis, classification and properties of hydrogels: their applications in drug delivery and agriculture. J Mater Chem B. 2022;10(2):170-203. [28] TOADER G, PODARU AI, DIACON A, et al. Nanocomposite Hydrogel Films Based on Sequential Interpenetrating Polymeric Networks as Drug Delivery Platforms. Polymers. 2023; 15(15):3176. [29] QIN X, LIU H, GAN Z, et al. Application of hydrogel materials for organoids. Scientia Sinica Chimica. 2024;54(2):182-195. [30] GIL-CABRERIZO P, SCACCHETTI I, GARBAYO E, et al. Cardiac tissue engineering for myocardial infarction treatment. Eur J Pharm Sci. 2023;185: 106439. [31] BAR A, COHEN S. Inducing Endogenous Cardiac Regeneration: Can Biomaterials Connect the Dots? Front Bioeng Biotechnol. 2020;8:126. [32] SHI T, WANG P, REN Y, et al. Conductive Hydrogel Patches with High Elasticity and Fatigue Resistance for Cardiac Microenvironment Remodeling. ACS Appl Mater Interfaces. 2023; 15(11):14005-14018. [33] YANG B, YAO F, HAO T, et al. Development of Electrically Conductive Double‐Network Hydrogels via One‐Step Facile Strategy for Cardiac Tissue Engineering. Adv Healthc Mater. 2015;5(4):474-488. [34] YU C, YUE Z, SHI M, et al. An Intrapericardial Injectable Hydrogel Patch for Mechanical–Electrical Coupling with Infarcted Myocardium. ACS Nano. 2022;16(10):16234-16248. [35] YU C, YAO F, LI J. Rational design of injectable conducting polymer-based hydrogels for tissue engineering. Acta Biomater. 2022;139:4-21. [36] NAVAEI A, SAINI H, CHRISTENSON W, et al. Gold nanorod-incorporated gelatin-based conductive hydrogels for engineering cardiac tissue constructs. Acta Biomater. 2016;41:133-146. [37] FANG J, LI JJ, ZHONG X, et al. Engineering stem cell therapeutics for cardiac repair. J Mol Cell Cardiol. 2022;171:56-68. [38] LI Y, RODRIGUES J, TOMÁS H. Injectable and biodegradable hydrogels: gelation, biodegradation and biomedical applications. Chem Soc Rev. 2012; 41(6):2193-2221. [39] ZHANG J, WANG J, ZHANG H, et al. Macroporous interpenetrating network of polyethylene glycol (PEG) and gelatin for cartilage regeneration. Biomed Mater. 2016;11(3):035014. [40] HUANG S, HONG X, ZHAO M, et al. Nanocomposite hydrogels for biomedical applications. Bioeng Transl Med. 2022;7(3):e10315. [41] ZHANG Y, HUANG Y. Rational Design of Smart Hydrogels for Biomedical Applications. Front Chem. 2020;8:615665. [42] BEJLERI D, STREETER BW, NACHLAS LY, et al. A Bioprinted Cardiac Patch Composed of Cardiac-Specific Extracellular Matrix and Progenitor Cells for Heart Repair. Adv Healthc Mater. 2018; 7(23):e1800672. [43] SINGELYN JM, SUNDARAMURTHY P, JOHNSON TD, et al. Catheter-Deliverable Hydrogel Derived From Decellularized Ventricular Extracellular Matrix Increases Endogenous Cardiomyocytes and Preserves Cardiac Function Post-Myocardial Infarction. J Am Coll Cardiol. 2012;59(8):751-763. [44] AUGUSTINE R, DAN P, HASAN A, et al. Stem cell-based approaches in cardiac tissue engineering: controlling the microenvironment for autologous cells. Biomed Pharmacother. 2021;138:111425. [45] LI M, WU H, YUAN Y, et al. Recent fabrications and applications of cardiac patch in myocardial infarction treatment. View. 2021;3(2). doi:10.1002/viw.20200153 [46] 郎丽敏.可注射导电材料联合子宫内膜间充质干细胞诱导来源的心肌细胞修复大鼠心梗的实验研究 [D].太原:山西医科大学,2021. [47] WANG Q, YANG H, BAI A, et al. Functional engineered human cardiac patches prepared from nature’s platform improve heart function after acute myocardial infarction. Biomaterials. 2016; 105:52-65. [48] ISHIDA M, MIYAGAWA S, SAITO A, et al. Transplantation of Human-induced Pluripotent Stem Cell-derived Cardiomyocytes Is Superior to Somatic Stem Cell Therapy for Restoring Cardiac Function and Oxygen Consumption in a Porcine Model of Myocardial Infarction. Transplantation. 2019;103(2):291-298. [49] CHEN TA, ZHAO BB, BALBIN R, et al. Engineering a robust and anisotropic cardiac-specific extracellular matrix scaffold for cardiac patch tissue engineering. Matrix Biology Plus. 2024; 23:100151. [50] HASHEMI M, FINKLEA FB, HAMMONS H, et al. Hydrogel microsphere stem cell encapsulation enhances cardiomyocyte differentiation and functionality in scalable suspension system. Bioact Mater. 2024;43:423-440. [51] SIM K, ERSHAD F, ZHANG Y, et al. An epicardial bioelectronic patch made from soft rubbery materials and capable of spatiotemporal mapping of electrophysiological activit. Nat Electron. 2020; 3(12):775-784. [52] 毛庆,梁秀琳,庞毅恒,等.人诱导多能干细胞移植治疗大鼠心肌梗死[J].中国老年学杂志, 2021,41(20):4472-4477. [53] 李慧影,马亚珂,杨岳,等.中药干预骨髓干细胞治疗缺血性心脏病研究进展[J].湖北中医药大学学报,2015,17(6):107-109. [54] 赵鸿.中医药干预骨髓间充质干细胞移植治疗缺血性心脏病研究进展[J].中国中医药现代远程教育,2013,11(11):154-155. [55] 宣守松,牟芳芳,李涵,等.中药在干细胞治疗心肌梗死中的作用及机制[J].中国中西医结合杂志,2020,40(10):1277-1280. [56] CHEN J, WEI J, HUANG Y, et al. Danhong Injection Enhances the Therapeutic Efficacy of Mesenchymal Stem Cells in Myocardial Infarction by Promoting Angiogenesis. Front Physiol. 2018;9:991. [57] ZHANG JS, HE Q Y, HUANG T, et al. Effects of panax notoginseng saponins on homing of C-kit+ bone mesenchymal stem cells to the infarction heart in rats. J Tradit Chin Med. 2011;31(3):203-208. [58] 杜楠楠,汪引芳,张鹏,等.中药单体诱导骨髓间充质干细胞向心肌细胞分化的研究新进展[J].中国医药导报,2019,16(23):30-33. [59] 张慧,赵利平,郑骏,等.中药麦冬对骨髓间充质干细胞分化心肌样细胞的诱导作用研究[J].中华中医药学刊,2020,38(2):96-101,267-270. [60] LEVIT RD, LANDÁZURI N, PHELPS EA, et al. Cellular encapsulation enhances cardiac repair. J Am Heart Assoc. 2013;2(5):e000367. [61] LI H, GAO J, SHANG Y, et al. Folic Acid Derived Hydrogel Enhances the Survival and Promotes Therapeutic Efficacy of iPS Cells for Acute Myocardial Infarction. ACS Appl Mater Interfaces. 2018;10(29):24459-24468. [62] LIU Y, ZHANG XP, WU TL, et al. Chinese herb-crosslinked hydrogel bearing rBMSCs-laden polyzwitterion microgels: Self-adaptive manipulation of micromilieu and stemness maintenance for restoring infarcted myocardium. Nano Today. 2021;41:10136. [63] BRYANT SJ, VERNEREY FJ. Programmable Hydrogels for Cell Encapsulation and Neo‐Tissue Growth to Enable Personalized Tissue Engineering. Adv Healthc Mater. 2017;7(1):10.1002/adhm.201700605. doi:10.1002/adhm.201700605 [64] LUO W, YANG Z, ZHENG J, et al. Small Molecule Hydrogels Loading Small Molecule Drugs from Chinese Medicine for the Enhanced Treatment of Traumatic Brain Injury. ACS Nano. 2024;18(42): 28894-28909. [65] ÖZKAN SA, DEDEOĞLU A, KARADAŞ BAKIRHAN N, et al. Nanocarriers Used Most in Drug Delivery and Drug Release: Nanohydrogel, Chitosan, Graphene, and Solid Lipid. Turk J Pharm Sci. 2019;16(4): 481-492. [66] 段秀红,马华,尚宏周,等.智能水凝胶在生物医药领域的应用进展[J].中国医院药学杂志, 2024,44(16):1950-1955,1959. [67] OMRANI M, NAIMI-JAMAL MR, FAR BF. The design of multi-responsive nanohydrogel networks of chitosan for controlled drug delivery. Carbohydr Polym. 2022;298:120143. [68] ZHOU X, LIU H, YU Z, et al. Direct 3D printing of triple-responsive nanocomposite hydrogel microneedles for controllable drug delivery. J Colloid Interface Sci. 2024;670:1-11. [69] ZHENG Z, LEI C, LIU H, et al. A ROS‐Responsive Liposomal Composite Hydrogel Integrating Improved Mitochondrial Function and Pro‐Angiogenesis for Efficient Treatment of Myocardial Infarction. Adv Healthc Mater. 2022;11(19): e2200990. [70] KASS LE, NGUYEN J. Nanocarrier‐hydrogel composite delivery systems for precision drug release. Wiley Interdiscip Rev Nanomed Nanobiotechnol. 2022;14(2):e1756. [71] MAKHATHINI SS, MDANDA S, KONDIAH PJ, et al. Biomedicine Innovations and Its Nanohydrogel Classifications. Pharmaceutics. 2022;14(12):2839. [72] YUNIARSIH N, CHAERUNISAA A, ELAMIN K, et al. Polymeric Nanohydrogel in Topical Drug Delivery System. Int J Nanomed. 2024;19:2733-2754. [73] FULLENKAMP DE, RIVERA JG, GONG YK, et al. Mussel-inspired silver-releasing antibacterial hydrogels. Biomaterials. 2012;33(15):3783-3791. [74] GAO W, ZHANG Y, ZHANG Q, et al. Nanoparticle-Hydrogel: A Hybrid Biomaterial System for Localized Drug Delivery. Ann Biomed Eng. 2016; 44(6):2049-2061. [75] 赵静,刘艳,解军波,等.中药纳米递药系统的研究进展[J].中华中医药学刊,2022,40(5): 134-137,276. [76] DENG S, GIGLIOBIANCO M, MIJIT E, et al. Dually Cross-Linked Core-Shell Structure Nanohydrogel with Redox–Responsive Degradability for Intracellular Delivery. Pharmaceutics. 2021; 13(12):2048. [77] 汪子贵,尚瑞鹏,徐应怡,等.中药活性成分原位凝胶递送系统的构建及其药理学功效提升的研究进展[J].中国现代中药,2025,27(12): 2377-2387. [78] 李永吉.中药多成分纳米制剂技术的构建及释放行为研究[R].黑龙江省,黑龙江中医药大学, 2015-01-14. [79] 胡恢权,程国旺,吴一峰,等.“药辅合一”理念在中药制剂递药系统设计中的应用研究[J].中国中药杂志,2023,48(7):1800-1807. [80] 于亚行,李成哲,孙婷庭,等.纳米技术在中药传递系统和分析中的应用[J].畜牧与兽医,2024, 56(4):125-131. [81] WANG S, WANG Z, YU G, et al. Tumor‐Specific Drug Release and Reactive Oxygen Species Generation for Cancer Chemo/Chemodynamic Combination Therapy. Adv Sci. 2019;6(5):1801986. [82] 柳成荫.可注射水凝胶携带牛蒡苷元在心肌缺血损伤中的保护作用研究[D].武汉:武汉大学, 2021. [83] 岳田,黄刚,杨佳丽,等.姜黄素纳米颗粒联合可注射水凝胶用于改善心肌梗死后微环境的体外效果评价研究[J].心血管病学进展, 2024,45(2):187-192. [84] ZHANG L, BEI Z, LI T, et al. An injectable conductive hydrogel with dual responsive release of rosmarinic acid improves cardiac function and promotes repair after myocardial infarction. Bioact Mater. 2023;29:132-150. [85] YU L, LIANG YB, GAO L, et al. Reconstruction of Postinfarcted Cardiac Functions Through Injection of Tanshinone IIA@ Reactive Oxygen Species‐Sensitive Microspheres Encapsulated in a Thermoreversible Hydrogel. Energy Environ Mater. 2024;7(2):e12555. [86] LIU C, JIANG X, LIANG L, et al. Intramyocardial delivery of injectable hydrogel with arctigenin alleviated myocardial ischemia-reperfusion injury in rats. Biotechnol Appl Biochem. 2024;71(3): 501-511. [87] WANG K, ZHU K, ZHU Z, et al. Triptolide with hepatotoxicity and nephrotoxicity used in local delivery treatment of myocardial infarction by thermosensitive hydrogel. J Nanobiotechnology. 2023;21(1):227. [88] 毕玉杰,马笃军,彭力平,等.中医药联合医用水凝胶治疗疾病的策略及意义[J].中国组织工程研究,2024,28(3):419-425. [89] 王政纬,黎松波,黎建文,等.生物纳米材料作为药物递送系统用于退变椎间盘再生治疗的研究进展[J].广东医学,2024,45(7):924-928. [90] 周磊,徐承义,韩宏伟,等.急性心肌梗死相关心室电风暴的研究现状[J].心血管病学进展, 2024, 45(7):627-631. [91] 郭勇娟,李忠杰.超急性期心肌梗死的细胞电生理基础和心电图表现(一):心肌细胞电生理基础[J].心电与循环,2016,35(1):50-53. [92] 郭勇娟,葛海燕,李忠杰.超急性期心肌梗死的细胞电生理基础和心电图表现(二):心电图表现、电生理机制和临床诊断要点[J].心电与循环,2016,35(2):130-136. [93] 罗涛,李玉明.心肌梗死后心室电重构的细胞和分子生物学机制[J].中国病理生理杂志, 2008,24(11):2276-2281. [94] FRAMPTON J, ORTENGREN AR, ZEITLER EP. Arrhythmias After Acute Myocardial Infarction. Yale J Biol Med. 2023;96(1):83-94. [95] CHARTON J, BOUTEILLER X, GANDJBAKHCH E, et al. Overdrive pacing for ventricular fibrillation storm after myocardial infarction. Eur Heart J. 2024;45(46):4968-4970. [96] 王雪芳,刘艳明.苦参碱对休克血浆致豚鼠心室肌细胞电生理变化的影响[J].中国中医基础医学杂志,2012,18(1):66-68. [97] 王慈,曹雅雯,张璇,等.作用于钾离子通道的抗心律失常中药活性成分研究进展[J].中国中药杂志,2023,48(7):1792-1799. [98] 徐浩,张力,高钊,等.葛根素对大鼠心室肌细胞动作电位的影响[J].现代生物医学进展, 2014,14(19): 3635-3637,3641. [99] LUO L, LI Y, BAO Z, et al. Pericardial Delivery of SDF-1α Puerarin Hydrogel Promotes Heart Repair and Electrical Coupling Adv Mater. 2024;36(1):e2302686. |
| [1] | Fan Xiao, Li Huiyun, Dou Fuguo, Zhang Nan, Zhang Xinyan. Copper phosphate nanohydrogel dressing promotes skin wound healing in mice [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(32): 8413-8419. |
| [2] | Li Xuanze, Fang Hanhong, Xu Zhe. Preparation and cytocompatibility of sodium alginate-hydroxyapatite-graphene oxide hydrogels [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(32): 8420-8426. |
| [3] | Liu Bangding, Tang Yongliang, Li Ni, Ren Bo. Quercetin-loaded hydrogel materials for treatment of infected bone defects [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(32): 8427-8435. |
| [4] | Chen Shichao, Deng Yunyi, Zhao Renshengjie, Yu Ke, Li Guangwen. Antibacterial properties of photocrosslinkable hydrogel loaded with quercetin-silver nanoparticles for infected wounds [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(32): 8436-8442. |
| [5] | Fei Xiaoyuan, Xu Jiao, Shi Hui. Application strategies of DNA hydrogels for tissue repair [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(32): 8487-8495. |
| [6] | Li Minghui, Qie Haoyu, Pan Min, Bi Ruijie, Lyu Xiaomeng, Zhang Haoya, Han Yifei. Hydrogel-based drug delivery systems for rheumatoid arthritis treatment [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(32): 8496-8501. |
| [7] | Meng Yihao, Zhang Shuai. Application of self-healing hydrogels for sports injury prevention and rehabilitation#br# [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(32): 8502-8511. |
| [8] | Jin Yuan, Zhou Jiabing. Applications and advances of hydrogels in bone tissue engineering repair related to sports injuries [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(32): 8512-8520. |
| [9] | Qiu Jiajing, Huang Liqu. Hydrogel scaffolds in tissue engineering for urethral repair and reconstruction [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(32): 8521-8528. |
| [10] | Zheng Ying, Li Mengyao, Zheng Fanfan, He Zhao, Zhang Ning, Zou Jialun, Li Youlei, Gao Feng. Mechanism of action of extracellular vesicles loaded with biomaterials in repairing spinal cord injury [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(32): 8544-8554. |
| [11] | Shang Qingqing, Zhou Jianye. Combination of hyaluronic acid hydrogel and bone marrow mesenchymal stem cells promotes cardiac function after myocardial infarction in rats (II) [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(34): 5559-5563. |
| [12] | Fang Yulu, Yi Bingcheng, Shen Yanbing, Tang Han, Zhang Yanzhong. Potential of corn husk fibers reinforced chitosan-based hydrogels in cartilage tissue engineering scaffold [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(34): 5493-5501. |
| [13] | Zhou Pengfei, Lin Jing, Chen Yuying, Lin Minkui. Canine dental pulp stem cells-polyglycolic acid scaffold complex for canine periodontal tissue defect [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(34): 5526-5531. |
| [14] | Yu Xingge, Lin Kaili. Application of nanocomposite hydrogels in bone tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(34): 5441-5446. |
| [15] | Cui Xintao, Zhang Zhenyu. Physical factors and mechanisms affecting osteogenic ability of bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(31): 5064-5070. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||