Chinese Journal of Tissue Engineering Research ›› 2024, Vol. 28 ›› Issue (10): 1634-1640.doi: 10.12307/2024.365
Application of biomaterials in Masquelet technology
Han Fengping1, Li Huairen1, Chang Wenli2, Tian Baofang2, Feng Li2
- 1Jining Medical University, Jining 272000, Shandong Province, China; 2Jining No.1 People’s Hospital, Jining 272000, Shandong Province, China
-
Received:2023-04-12Accepted:2023-05-26Online:2024-04-08Published:2023-08-21 -
Contact:Feng Li, MD, Associate chief physician, Jining No.1 People’s Hospital, Jining 272000, Shandong Province, China -
About author:Han Fengping, Master candidate, Jining Medical University, Jining 272000, Shandong Province, China -
Supported by:Masquelet technique| induced membrane technique| induced membrane| biomaterial| bone regeneration| bone defect| bone healing| nonunion bone| bone fracture
CLC Number:
Cite this article
Han Fengping, Li Huairen, Chang Wenli, Tian Baofang, Feng Li. Application of biomaterials in Masquelet technology[J]. Chinese Journal of Tissue Engineering Research, 2024, 28(10): 1634-1640.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
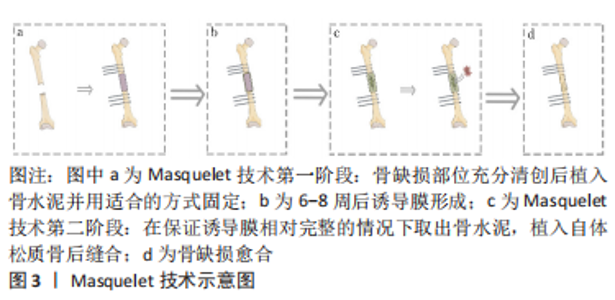
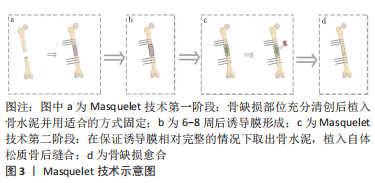
2.1 Masqulete技术概述 在1986年,Masquelet开发了一种通过两个阶段治疗大段骨缺损的技术,经过多年实验及临床应用,其团队于2000年在一篇基于他的病例结果的文章中介绍了诱导膜的概念[11],这种技术被称为Masquelet技术即诱导膜技术。 Masquelet技术作为一种简单有效地修复节段性骨缺损的方法,至今已有30多年的历史[8,11],在临床治疗骨缺损中广泛应用。该技术治疗骨缺损的过程分为两个阶段:第一阶段是在对骨和软组织彻底清创后将PMMA骨水泥填充到骨缺损部位,连接并包裹骨两断端进行固定,之后闭合创面,等待诱导膜的形成;第二阶段是在一阶段术后6-8周,切开诱导膜,在保持诱导膜相对完整的情况下取出骨水泥,并在诱导膜内植入自体颗粒状松质骨后固定、缝合[8,10-11],见图3。"
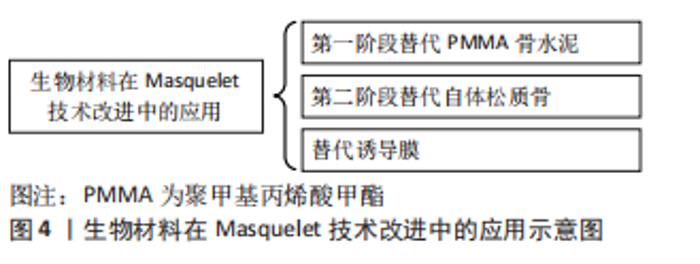
最初,PMMA骨水泥在治疗中被用来填充骨缺损,植入的PMMA骨水泥周围形成了生物膜——诱导膜。当时保留这层生物膜只是为了避免过度出血,然而,随后研究发现诱导膜有助于避免移植物被吸收,同时还能促进移植物的血管化和皮质化[12]。随着技术的发展、临床不断地实践和进一步的研究,Masquelet技术的应用逐步成熟,可用于临床治疗骨缺损。但是如今其作用机制与骨愈合的关系还未能完全确定,研究人员认为这项技术源于组织对封闭异物的反应——异物的植入可使其周围生成生物活性膜,即诱导膜。 PMMA骨水泥周围形成的诱导膜血运良好,能分泌生长因子,且含有间充质干细胞,而这些正是组织再生的条件,因而Masquelet技术治疗骨缺损被认为是一种有希望的血管化骨再生策略[13]。如今许多研究者尝试进一步降低该术式的操作难度,减少自体取骨和自体骨供量不足造成的不便,并希望将其改进为通过一个阶段完成的术式,改进方式见图4。"
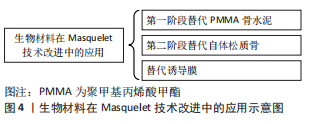
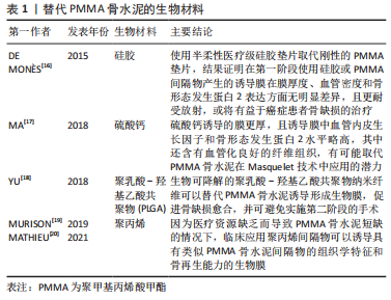
2.2 可以替代PMMA骨水泥的材料 在骨缺损部位中插入PMMA骨水泥间隔物,可以避免周围的软组织塌陷到骨缺损的部位之中[12]。PMMA骨水泥填充物的使用会引起异物反应,进而形成诱导膜。但是PMMA骨水泥的植入存在一定的缺点:如在诱导膜形成后第二阶段去除PMMA间隔物且要保留完整的诱导膜在操作上较为困难;PMMA骨水泥凝固过程中会释放大量的热,对软组织产生一定的热损伤等[8,14-15]。因此,针对这些问题,为了满足骨科医生临床的需求,找到一种在第一阶段手术过程中更易于放置且对人体损伤更小的间隔物,或者在第二阶段术中能简单方便的从已经形成的诱导膜腔中去除的间隔物材料将是该技术在未来的一个重要研究方向。研究者们通过动物实验或者临床应用去验证多种生物材料在Masquelet技术中能否成为替代PMMA骨水泥的材料,见表1。"
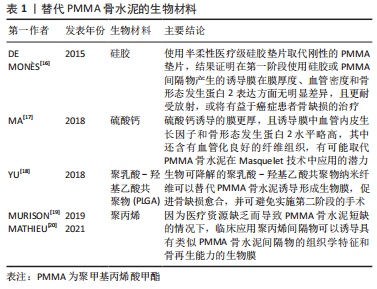
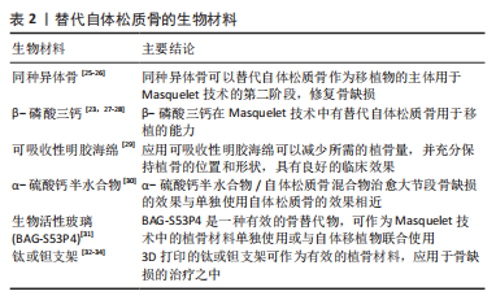
2.2.1 硅胶 众所周知硅胶也是一种常用的生物材料,标准的Masquelet技术中PMMA骨水泥诱导成膜的主要缺点之一是在诱导膜形成后第二阶段去除PMMA间隔物且需要保留完整的诱导膜在操作上较为困难。因此,有研究使用半柔性医疗级硅胶垫片取代刚性的PMMA垫片[16],结果证明在第一阶段使用硅胶或PMMA间隔物产生的诱导膜在膜厚度、血管密度和骨形态发生蛋白2表达方面无显著差异,此外,该研究还证实在放射治疗的作用下,医用硅胶诱导产生的生物膜比PMMA骨水泥形成的诱导膜具有更稳定的性质,且对放射治疗具有很大的耐受性,能更好地保存膜的血管,因此医用硅胶或可用在癌症患者的骨缺损治疗。但此实验的不足之处是仅验证了硅胶对诱导膜的诱导形成作用,并未验证该诱导膜在第二阶段时和植入的自体骨的结合能力,还需要对此进一步研究。除了以上因素,硅胶比起PMMA骨水泥更容易去除,可降低手术操作的难度,因此硅胶是一个值得探索研究的生物材料。 2.2.2 硫酸钙 硫酸钙是临床治疗骨缺损中常用的生物材料,常用于填补骨折手术复位后骨质缺损的部分,在临床上常应用粉剂或者颗粒状硫酸钙,它具有良好的生物相容性与成骨性,可以被人体吸收,此外,它还可以诱导骨髓间充质干细胞向成骨细胞分化。MA等[17]将硫酸钙与PMMA诱导的膜相比,发现硫酸钙诱导的膜更厚,且诱导膜中血管内皮生长因子和骨形态发生蛋白2水平略高,其中还含有血管化良好的纤维组织,有趣的是研究者在硫酸钙组的标本中发现了一些膜内骨化,该发现或将提示Maquelet技术存在简化为一步完成的可能。硫酸钙具有完全的生物降解性,避免植骨前取出时的困难。以该实验结果来看,硫酸钙与PMMA骨水泥相比其具有显著优势,这表明硫酸钙材料在该技术的改进中是一个有意义的研究方向。 2.2.3 聚乳酸-羟基乙酸共聚物[poly (latic-co-glycolic acid),PLGA] 其具有可控降解性和与人体组织的良好生物相容性而成为最具发展前景的生物降解聚合物之一,YU等[18]的研究成功地将PLGA纳米纤维作为一种可生物降解的材料应用于Masquelet技术中,它被证实可以诱导产生生物活性膜,包裹骨移植物,并促进骨结合。该研究还证明了这种材料有代替PMMA骨水泥治疗大面积骨缺损的可能性,而且PLGA不需要切除,随着骨缺损部位的愈合,PLGA纳米纤维降解也在同时进行,通过使用可生物降解的PLGA纳米纤维,有两阶段Masquelet技术减少到一个阶段的潜力。对PLGA在Masquelet技术中应用的研究或可减少大段骨缺损的治疗时间、成本和患者治疗相关的不适,并可降低手术部位感染的风险。尽管现阶段关于PLAG材料的研究较少,亦未有确凿的临床证据,但是PLGA应用于Masquelet技术是一个值得继续深耕的研究方向。 2.2.4 聚丙烯 聚丙烯是一种性能优良的热塑性合成树脂,是丙烯通过加聚反应而成的聚合物,为无色半透明的热塑性轻质通用塑料,具有耐化学性、耐热性、电绝缘性、高强度机械性能和良好的高耐磨加工性能。在战场前线或者医疗水平欠发达的地区,可能缺乏PMMA骨水泥,通过PMMA骨水泥进行Masquelet技术治疗骨缺损难以实现。 MURISON等[19]描述了2例病例——在资源有限的情况下通过Masquelet技术重建多个掌骨,治疗过程未使用PMMA骨水泥,他们使用聚丙烯注射器体替代PMMA骨水泥作为填充物,获得了良好的临床结果。MATHIEU等[20]使用了由聚丙烯一次性注射器制成的间隔物替代PMMA骨水泥,成功应用Masquelet技术完成治疗,这证明了聚丙烯间隔物可以像PMMA骨水泥那样诱导出具有类似组织学特征和骨再生能力的生物膜。这些发现支持了在因为资源缺乏而导致PMMA短缺的情况下使用非水泥Masquelet技术的可能性,虽然利用聚丙烯代替PMMA骨水泥更大程度上是一种无奈之举,但是也为研究者们带来了一种应用Masquelet技术的新思路,在未来对聚丙烯在该技术应用的研究或许不仅可以使更多的人在医疗条件不足的情况下获益,还可以进一步推进对Masquelet技术的研究。 2.2.5 钛 钛在现阶段被大家认为是“生物相容性”最好的金属之一,因此有研究者猜想它是比PMMA骨水泥更好的间隔物材料,可以在第一阶段替代PMMA骨水泥。有研究团队就此展开研究,结果实验数据表明虽然钛能诱导出组织结构与PMMA骨水泥诱导膜相似的生物活性膜,但是钛诱导产生的膜不能像PMMA骨水泥形成的诱导膜那样可以有效地促进移植物的结合和骨再生[21-22]。这种发现是令人失望的,单独使用钛间隔物替代PMMA骨水泥应用于Masquelet技术的第一阶段目前并不是一个可行的方案,在进一步的研究中研究者们可以将钛与各种生长因子、促血管因子或其他生物材料结合,寻找到一种合适的应用方案。 2.2.6 聚乙烯醇海绵 聚乙烯醇海绵是一种高度亲水性的生物材料,在现阶段用作各种类型的植入物,有研究尝试探寻使用该材料替代PMMA骨水泥作为填充物,诱导生物膜的形成,然而,MCBRIDE-GAGYI等[21]在验证使用聚乙烯醇海绵替换PMMA骨水泥的过程中,得到了与预想结果相反的结论,结果发现聚乙烯醇海绵间隔材料在实验中并没有诱导形成明显的膜,而且在第二阶段中聚乙烯醇海绵材料几乎无法与骨缺损末端分离,得到的结果不鼓励进一步研究聚乙烯醇海绵作为间隔材料替代PMMA骨水泥的应用,或许研究者们可以在以后的研究中探寻其作为缺损填充物的应用。 上述材料如硅胶、硫酸钙、聚乳酸-羟基乙酸共聚物和聚丙烯的研究集中于基础研究阶段,少部分应用于临床,虽然各种生物材料的安全性与生物相容性皆较好,但是现阶段在性能上还无法取代PMMA骨水泥,临床上仍采用PMMA骨水泥作为间隔物材料。尽管如此,这些研究为Masquelet技术的完善与发展提供了一些潜在的方向与研究思路,相信随着研究的深入,可以找到一种完美的替代材料,以缩短手术周期,减少患者治疗过程中的痛苦。 2.3 取代自体骨作为移植物的新材料 在Masquelet技术的第二阶段,移除了PMMA骨水泥后骨缺损仍然存在,在重建的最后阶段必须用最佳类型的材料填充该缺损,以达到骨缺损修复的效果。填充材料选取的金标准是从髂骨翼获得的松质骨,且自体松质骨在移植时应该制成小立方体,松质骨小块的放置要完全填满诱导膜的空腔。如果移植的自体松质骨没有被紧紧地放置,在重力的作用它们将会变得分布不均,这会导致骨缺损重建的节段不愈合或骨折[8]。此阶段中需要获得较多量的自体骨松质骨用来填充大节段的骨缺损,为了解决这个问题,有研究者推荐使用铰刀-冲洗吸引器获得较多量的自体松质骨,它允许外科医生定期收获50 mL以上的自体骨移植物[23-24],尽管在临床上提取自体骨并不困难,但是无论是取自髂骨冠还是通过铰刀-冲洗吸引器获取自体骨,都可能存在自体松质骨获取量不足、供区损伤和疼痛的问题。如何使用较少的自体骨即通过生物材料替代部分或全部自体骨是一个充满前景的研究方向。随着科技的发展,研究者对自体骨替代材料的探索将更加深入[25-34],现阶段对在Masquelet技术第二阶段自体骨植入物替代材料的研究和应用还处在一个不断发展的阶段,许多生物材料已经应用于Masquelet技术的第二阶段,见表2。"
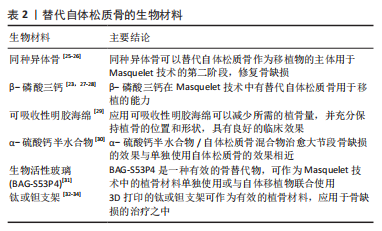
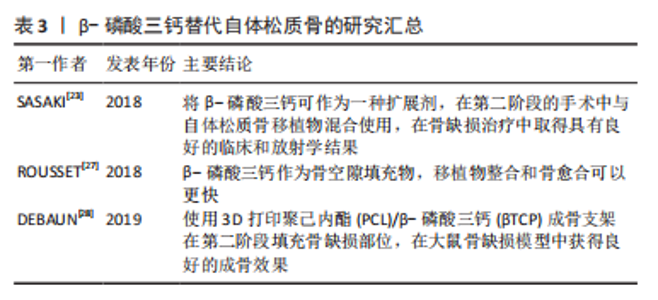
尽管自体骨松质骨的获取比起探究可替代材料更方便,但是自体骨的获得会对供区产生较大损伤并对患者带来的巨大痛苦,尤其是在髂骨大量取骨的患者在很长的一段时间内会在束腰带或翻身时感到疼痛,这促使研究者们不断对替代材料进行研究,期待未来有一天生物材料可以作为骨缺损治疗中的首选材料,而非在自体骨量不充足的情况下作为补充材料的无奈之举。 2.3.1 同种异体骨 同种异体骨可代替自体骨应用,尽管Masquelet认为由于同种异体骨中不含干细胞和生长因子,所以同种异体骨移植的比例不应超过1/3[8],很多研究者仍将目光聚焦于同种异体骨这一生物材料上,并谋求使用整块的同种异体骨。NICCOLAI等[25]通过改良Masquelet技术,在第二阶段中使用6 cm长的大块同种异体骨植入缺损部位,并添加部分自体骨,填补了患者股骨近端6 cm的骨间隙,患者术后3个月可以完全负重,1年后骨折顺利愈合。VIALE等[26]在第二阶段通过嵌套的方式采用14 cm的大段同种异体骨移植治疗创伤后10 cm的感染性股骨节段性缺损,利用伸缩式同种异体骨移植和髓内钉填补缺损,使患者康复。同种异体骨获取量远远高于自体松质骨,还可以减少供区的损伤与疼痛,减少患者的痛苦。尽管异体骨会带来一些医学伦理问题,但是在有临床证据的支持下研究者们可以开展更多关于异体移植物应用Masquelet技术治疗骨缺损的研究。 2.3.2 β-磷酸三钙 β-磷酸三钙是骨科领域应用最广泛的骨替代物之一,具有易吸收、高骨导及高再植能力等优点[35-37],众多研究者设想将β-磷酸三钙应用于Masquelet技术的第二阶段,作为自体松质骨的替代物治疗骨缺损,见表3。上述各研究皆获得了预期的结果,提示β-磷酸三钙在Masquelet技术中有替代自体松质骨用于移植的潜力,对β-磷酸三钙的进一步研究将有助于骨缺损的治疗,降低手术的难度,减轻患者的痛苦。"


2.3.3 可吸收性明胶海绵 在标准的Masquelet技术的第二阶段中,四肢骨的大段缺损需要的自体松质骨量巨大,而长骨是环形中空的,髓腔的位置可用间隔物填充,以减少植骨量。CHO等[29]选择在Masquelet技术第二阶段于可吸收性明胶海绵核心周围进行环形植骨,以减少自体骨移植物的使用,结果显示其中平均21.4%的缺损被明胶海绵填充,而且随着骨缺损的部位愈合,可吸收明胶海绵会被逐步吸收并仍可充分保持植骨的位置和形状,其应用具有良好的临床效果。提示研究者们可对此进行更深入的研究,如果能大范围应用于临床,或将给广大患者带来福音。 2.3.4 α-硫酸钙半水合物 α-硫酸钙半水合物因其易于获得、出色的生物相容性、生物降解性和骨传导性成为一种出色的骨骼替代品。有研究表明虽然在第二阶段单独使用α-硫酸钙半水合物替代自体松质骨作为移植物效果不如后者,但是两者混合的移植物在骨缺损修复时能力与单独使用自体松质骨相似[30],在Masquelet技术中使用α-硫酸钙半水合物可有效减少患者自体松质骨的获取量,以减少患者的痛苦。 2.3.5 生物活性玻璃(BAG-S53P4) S53P4型生物活性玻璃(53%SiO2,4%P2O5,23%Na2O,20%CaO)具有骨刺激、导电、抗菌等优点,是一种很有前途的骨替代材料[38]。有文献证据表明,BAG-S53P4是一种有效的骨替代物,可作为诱导膜技术中的植骨材料单独使用或与自体移植物联合使用,特别是在高概率发生骨感染的情况下[31]。 2.3.6 钛或钽支架 3D打印种植体是Masquelet技术修复大面积骨丢失的一种新手段,钛和钽作为生物材料已应用于骨科的治疗之中,研究人员将其应用于Masquelet技术中也是一种意料之中的选择。QIAO等[32]研究表明,在Ⅰ期感染控制后,3D打印钛笼与自体骨和同种异体松质骨植入诱导膜,治疗效果良好;GAVASKAR等[33]通过研究认为作为单纯骨移植的替代,3D打印钛假体可以为成骨提供稳定的支架,能提高临床疗效。WU等[34]在诱导膜形成后,将定制的3D打印多孔钽支架与解剖钢板连接,在未植入自体骨的情况下永久性植入骨缺损段,然后将诱导膜小心缝合以提供一个生物环境。患者通过治疗和锻炼后步态正常,无疼痛、跛行,治疗效果良好,因此3D打印钽假体也是一种可接受的替代材料,在其他生物技术不适合的情况下,该方法使感染性股骨大段骨缺损得以重建,让患者尽可能的享受健康的生活。作者认为类似于关节置换术,在完全没有办法的情况下通过生物材料完全替代自体骨也将是一种可行的治疗骨缺损的方案。 2.3.7 其他材料 目前自体骨移植中加入生物添加剂(细胞或生长因子)是为了支持骨缺损部位的新骨形成[5,39]。有研究表明,在兔体内加入浓缩生长因子或骨形态发生蛋白7后,骨连接得到改善[40-41]。然而,在临床实践中,使用补充骨形态发生蛋白2或7移植物的效果尚不清楚,生长因子的使用完全依赖于外科医生的偏好[5]。也有实验通过制备富血小板血浆-微骨粒混合体用于术式,得到了预期结果,提高了植骨的愈合速度,但是其植骨量与富血小板血浆用量之间的关系和最适宜的富血小板血浆浓度未能确定[42]。此外还有许多此类研究,但是现阶段,重组生长因子的添加是存在争议的,Masquelet等[8,12]专家通过实验结果的分析认为重组生长因子与移植物相关联可能是有害的,产物的局部高密度以及与膜分泌的生长因子可能导致移植物的部分吸收,因此这一方面的研究仍需继续,尚不能妄下定论。 Herafill?(Heraeus Medical GmbH,Wehrheim)是一种可生物吸收的骨空隙填充材料。Herafill?的主要成分是硫酸钙、碳酸钙、三酰甘油和庆大霉素。现有一项大鼠模型研究证实,靠近诱导膜的骨组织形成显著增加,从而促进骨缺损的愈合,该实验还评估了植骨替代物(Hemfill?)的颗粒大小对 Masquelet技术疗效的影响,发现小颗粒较大颗粒更能促进骨质愈合[43]。尽管作者将此复合材料单独列出,但由于其为商品成品,现在无法验证该物质中各部分单独使用和复合使用对骨缺损的修复是否有显著性差异,但是它在一定程度上启发研究者们着眼于复合材料。采取各种材料的优势制备复合材料用于骨缺损的治疗将是一个有价值的研究方向。 现阶段关于取代自体骨作为移植物的生物材料的研究分为2种思路,一种是作为混合物与自体松质骨混合使用,以减少自体骨用量;另一种则是完全替代自体骨移植。前者已经较多的在临床中使用,确实成功减少了患者自体骨的供应需求,而且疗效良好,但是这种方法只解决了供应量可能不足的问题,并未解决供区损伤的问题。后者虽然也有很多研究,大多却仍局限于基础实验阶段,暂时未应用于临床或者未能临床推广,尽管如此,这些研究为解决自体骨供应量不足和减少患者痛苦提供了有价值的思路与指导。 2.4 与诱导膜具有相同性能的膜材料 Masquelet技术的关键是诱导膜的形成,诱导膜是具有成骨潜力并有助于促进骨形成的生物膜[8,13],具有机械性屏障作用和生物学活性作用。对兔、绵羊以及大鼠模型的研究发现诱导膜外层主要由成纤维细胞和胶原蛋白构成,内层则由滑膜样上皮样细胞构成,内外两层共同构成生物学上的机械性屏障[12-13,44]。此外,与成骨和血管生成直接相关的血管内皮生长因子、骨形态发生蛋白2、转化生长因子β1、核心结合因子(Cbfa-1)等在诱导膜中含量丰富[15,44-46]。尽管如今诱导膜具体的作用机制尚不能确定,但是临床试验结果表明,诱导膜具有防止邻近软组织侵入骨缺损中、对填充的移植物固定和约束、保护移植物不被吸收和局部产生骨诱导物质促进骨缺损愈合等优势[5,8,44]。 虽然广大骨外科医生已经将Masquelet技术应用于临床,并在骨缺损(尤其是大段骨缺损或者伴有感染)的治疗中取得较好的效果。但是作为科研工作者不能止步于此,在对诱导膜的作用机制进行探究的同时,不少研究者期望于用稳定且更易制备的材料替代诱导膜或者通过对该技术改进使手术程序简化到一个阶段,从而节省时间和金钱,并降低患者的痛苦。 2.4.1 仿生诱导膜 REN等[47]将人脐静脉内皮细胞接种到未分化的人骨髓间充质干细胞片上,形成预血管化的内层,然后通过诱导人脐静脉内皮细胞成骨分化形成外层——成骨层,将这2个细胞片层包裹在一起,形成仿生诱导膜。此研究中描述的仿生诱导膜有治疗大段骨缺损的潜力,仿生诱导膜可以在大段骨缺损治疗时包裹植骨材料,替代PMMA间隔物诱导形成的膜,简化手术步骤,值得注意的是,此材料需要在未感染的情况下应用。或许随着研究的不断深入,会出现不同类型的仿生诱导膜用于骨缺损的治疗。 2.4.2 人羊膜 人羊膜是一种天然的、预先形成的薄片,含有生长因子和具有成骨潜力的高效干细胞,在再生医学领域中有着广泛的应用,可以用于骨修复,且人羊膜具有抗炎、抗纤维化、抗瘢痕和镇痛的特性[48],GINDRAUX等[49]研究证明在Masquelet技术的第一阶段使用人羊膜来模拟诱导膜的作用可能会改善骨愈合。尽管有研究结果认为人羊膜与诱导膜构建加载人源重组骨形态发生蛋白2的磷酸钙骨水泥的3D打印支架应用于动物骨缺损的修复时,并没有起到进一步促进骨愈合的作用[50],但是此实验中的变量过于繁杂,若就此否定人羊膜或者诱导膜的作用是欠妥的,研究者们应该对这些材料进行更进一步的研究,明确其作用机制。 2.4.3 人脱细胞真皮 人脱细胞真皮通常用于治疗烧伤创面或修复腹壁缺损,它具有与诱导膜相似的纤维层结构、高胶原含量和高拉伸强度[51-52]。 VERBOKET等[52]研究了人脱细胞真皮对大鼠股骨缺损愈合的影响,获得了人脱细胞真皮与诱导膜等效的愈合结果,这提示人脱细胞真皮可能替代诱导膜直接应用于一期植骨以治疗骨缺损,对人脱细胞真皮的进一步研究和应用可能会缩短大段骨缺损治疗的时间。 2.4.4 聚四氟乙烯 这种生物材料常被用来保护骨缺损的部位,分隔该部位与周围软组织,其与诱导膜的部分作用相似[53]。TARCHALA等[54]考虑将这一目前使用的材料应用到长骨临界大小的缺损模型中,探究聚四氟乙烯材料能否起到与诱导膜类似的治疗效果。而且该团队认为如果Masquelet技术中诱导膜的主要功能是屏障,那么用合成膜进行替代是未来临床治疗的一个改进方向,以便于单阶段重建骨缺损。研究结果证明与诱导膜相比,聚四氟乙烯膜具有相似的骨整合性能,该结果为今后优化Masquelet技术提供了证据,未来该技术可能进一步简化,可以一期完成骨缺损的治疗。 2.4.5 自体皮质骨 在第二阶段诱导膜内植入骨时,植入物的选择是松质骨而非皮质骨,在文献阅读时作者注意到了一个有关Masquelet技术改良的案例分析。该案例的对象是一名32岁的男性患者,由于摔倒导致右脚踝开放性骨折并伴有大量骨软骨缺损,治疗团队计划使用Masquelet技术进行分期手术治疗,在治疗过程中,骨缺损植骨部位的前表面覆盖了一层大而薄的皮质骨(取自髂内板),而不是缝合切开的诱导膜,患者骨缺损得以治愈[55]。这篇病例报告描述了一种改良的Masquelet技术用于踝关节融合术,并展示了该策略在治疗严重开放性四肢骨折伴严重骨软骨缺损中的应用,为进一步寻找诱导膜的替代材料提供了一个特殊的方向。 目前,诱导膜的作用机制并未完全探明,现阶段其作用机制仍存在争议,但是可以预见的是,如果能获得一种可以替代诱导膜的生物材料,Masquelet技术将会迈出关键性的一步。目前有关诱导膜替代材料的研究较少,且大多处于基础研究阶段,上述提到的材料,无论是仿生诱导膜、人羊膜、人脱细胞真皮还是聚四氟乙烯,尽管生物相容性较好,真正应用于临床还有较长的一段路途。现阶段的研究所提供的指导意义值得肯定,对于诱导膜替代的生物材料的研究充满价值。"

| [1] CLARKE B. Normal bone anatomy and physiology. Clin J Am Soc Nephrol. 2008;3 Suppl 3(Suppl 3):S131-S139. [2] XUE N, DING X, HUANG R, et al. Bone tissue engineering in the treatment of bone defects. Pharmaceuticals (Basel). 2022. doi: 10.3390/ph15070879. [3] PERIĆ K, RIDER P, ALKILDANI S, et al. An introduction to bone tissue engineering. Int J Artif Organs. 2020;43(2):69-86. [4] YONG KW, CHOI JR, CHOI JY, et al. Recent advances in mechanically loaded human mesenchymal stem cells for bone tissue engineering. Int J Mol Sci. 2020;21(16):5816. [5] MATHIEU L, MOURTIALON R, DURAND M, et al. Masquelet technique in military practice: specificities and future directions for combat-related bone defect reconstruction. Mil Med Res. 2022;9(1):48. [6] DALISSON B, CHARBONNIER B, AOUDE A, et al. Skeletal regeneration for segmental bone loss: vascularised grafts, analogues and surrogates. Acta Biomater. 2021;136:37-55. [7] LIODAKIS E, GIANNOUDIS VP, SEHMISCH S, et al. Bone defect treatment: does the type and properties of the spacer affect the induction of Masquelet membrane? Evidence today. Eur J Trauma Emerg Surg. 2022; 48(6):4403-4424. [8] MASQUELET AC. Induced membrane technique: pearls and pitfalls. J Orthop Trauma. 2017;31 Suppl 5:S36-S38. [9] KLEIN C, MONET M, BARBIER V, et al. The Masquelet technique: current concepts, animal models, and perspectives. J Tissue Eng Regen Med. 2020; 14(9):1349-1359. [10] 吴斗,刘强.Masquelet技术修复骨缺损的实验研究现状和展望[J].中华实验外科杂志,2020,37(11):1983-1987. [11] MASQUELET AC, FITOUSSI F, BEGUE T, et al. Reconstruction of the long bones by the induced membrane and spongy autograft. Ann Chir Plast Esthet. 2000;45(3):346-353. [12] MASQUELET AC, BEGUE T. The concept of induced membrane for reconstruction of long bone defects. Orthop Clin North Am. 2010;41(1): 27-37. [13] WANG W, ZUO R, LONG H, et al. Advances in the Masquelet technique: myeloid-derived suppressor cells promote angiogenesis in PMMA-induced membranes. Acta Biomater. 2020;108:223-236. [14] MCCONOUGHEY SJ, HOWLIN RP, WISEMAN J, et al. Comparing PMMA and calcium sulfate as carriers for the local delivery of antibiotics to infected surgical sites. J Biomed Mater Res B Appl Biomater. 2015;103(4):870-877. [15] MASQUELET A, KANAKARIS N K, OBERT L, et al. Bone repair using the masquelet technique. J Bone Joint Surg Am. 2019;101(11):1024-1036. [16] de MONÈS E, SCHLAUBITZ S, OLIVEIRA H, et al. Comparative study of membranes induced by PMMA or silicone in rats, and influence of external radiotherapy. Acta Biomater. 2015;19:119-127. [17] MA YF, JIANG N, ZHANG X, et al. Calcium sulfate induced versus PMMA-induced membrane in a critical-sized femoral defect in a rat model. Sci Rep. 2018;8(1):637. [18] YU Y, WU R, LEE D, et al. Artificial membrane induced by novel biodegradable nanofibers in the masquelet procedure for treatment of segmental bone defects. J Nanomater. 2018;2018:8246571. [19] MURISON J C, PFISTER G, AMAR S, et al. Metacarpal bone reconstruction by a cementless induced membrane technique. Hand Surg Rehabil. 2019; 38(2):83-86. [20] MATHIEU L, MURISON JC, de ROUSIERS A, et al. The masquelet technique: can disposable polypropylene syringes be an alternative to standard PMMA spacers? A rat bone defect model. Clin Orthop Relat Res. 2021; 479(12):2737-2751. [21] MCBRIDE-GAGYI S, TOTH Z, KIM D, et al. Altering spacer material affects bone regeneration in the Masquelet technique in a rat femoral defect. J Orthop Res. 2018. doi: 10.1002/jor.23866. [22] TOTH Z, ROI M, EVANS E, et al. Masquelet technique: effects of spacer material and micro-topography on factor expression and bone regeneration. Ann Biomed Eng. 2019;47(1):174-189. [23] SASAKI G, WATANABE Y, MIYAMOTO W, et al. Induced membrane technique using beta-tricalcium phosphate for reconstruction of femoral and tibial segmental bone loss due to infection: technical tips and preliminary clinical results. Int Orthop. 2018;42(1):17-24. [24] LE BARON M, VIVONA JP, MAMAN P, et al. Can the reamer/irrigator/aspirator system replace anterior iliac crest grafting when treating long bone nonunion? Orthop Traumatol Surg Res. 2019;105(3):529-533. [25] NICCOLAI F, Di MENTO L, MOCCHI M, et al. Modified masquelet’s technique with nail and allograft: a case report. Injury. 2018;49 Suppl 4:S21-S24. [26] VIALE GJ, GARABANO G, PESCIALLO C, et al. Structural allograft and induced membrane technique for treatment of 10-cm segmental femoral bone defect: a case report. JBJS Case Connect. 2021. doi: 10.2106/JBJS.CC.21.00372. [27] ROUSSET M, WALLE M, CAMBOU L, et al. Chronic infection and infected non-union of the long bones in paediatric patients: preliminary results of bone versus beta-tricalcium phosphate grafting after induced membrane formation. Int Orthop. 2018;42(2):385-393. [28] DEBAUN MR, STAHL AM, DAOUD AI, et al. Preclinical induced membrane model to evaluate synthetic implants for healing critical bone defects without autograft. J Orthop Res. 2019;37(1):60-68. [29] CHO JW, KIM J, CHO WT, et al. Circumferential bone grafting around an absorbable gelatin sponge core reduced the amount of grafted bone in the induced membrane technique for critical-size defects of long bones. Injury. 2017;48(10):2292-2305. [30] MENG ZL, WU ZQ, SHEN BX, et al. Reconstruction of large segmental bone defects in rabbit using the Masquelet technique with α-calcium sulfate hemihydrate. J Orthop Surg Res. 2019;14(1):192. [31] AURÉGAN JC, VILLAIN B, GLOMBITZA M, et al. Utilisation of bioactive glass S53P4 inside an induced membrane for severe bone defect with high risk of infection: a multi-center preliminary experience. Injury. 2022;53 Suppl 2: S13-S19. [32] QIAO S, WU D, LI Z, et al. The combination of multi-functional ingredients-loaded hydrogels and three-dimensional printed porous titanium alloys for infective bone defect treatment. J Tissue Eng. 2020;11:1542272091. [33] GAVASKAR AS, PARTHASARATHY S, BALAMURUGAN J, et al. A load-sharing nail-cage construct may improve outcome after induced membrane technique for segmental tibial defects. Injury. 2020;51(2):510-515. [34] WU Y, SHI X, ZI S, et al. The clinical application of customized 3D-printed porous tantalum scaffolds combined with Masquelet’s induced membrane technique to reconstruct infective segmental femoral defect. J Orthop Surg Res. 2022;17(1):479. [35] JIANG SD, JIANG LS, DAI LY. Surgical treatment of calcaneal fractures with use of beta-tricalcium phosphate ceramic grafting. Foot Ankle Int. 2008; 29(10):1015-1019. [36] DAI LY, JIANG LS. Single-level instrumented posterolateral fusion of lumbar spine with beta-tricalcium phosphate versus autograft: a prospective, randomized study with 3-year follow-up. Spine (Phila Pa 1976). 2008;33(12): 1299-1304. [37] GUPTA S, MALHOTRA A, JINDAL R, et al. Role of beta tri-calcium phosphate-based composite ceramic as bone-graft expander in Masquelet’s-induced membrane technique. Indian J Orthop. 2019;53(1):63-69. [38] TANNER MC, HELLER R, WESTHAUSER F, et al. Evaluation of the clinical effectiveness of bioactive glass (S53P4) in the treatment of non-unions of the tibia and femur: study protocol of a randomized controlled non-inferiority trial. Trials. 2018;19(1):299. [39] ALFORD AI, NICOLAOU D, HAKE M, et al. Masquelet’s induced membrane technique: Review of current concepts and future directions. J Orthop Res. 2021;39(4):707-718. [40] KARIMI GE, MEIMANDI-PARIZI A, ORYAN A, et al. Effects of combination of BMP7, PFG, and autograft on healing of the experimental critical radial bone defect by induced membrane (Masquelet) technique in rabbit. Arch Bone Jt Surg. 2021;9(5):585-597. [41] ARıCAN G, ÖZMERIÇ A, FıRAT A, et al. Micro-ct findings of concentrated growth factors (cgf) on bone healing in masquelet’s technique-an experimental study in rabbits. Arch Orthop Trauma Surg. 2022;142(1):83-90. [42] 高峻青,王朝辉,詹晓欢,等.Masquelet技术联合富血小板血浆修复胫骨大段骨缺损[J].中华创伤骨科杂志,2020,22(4):315-316. [43] LEIBLEIN M, WINKENBACH A, KOCH E, et al. Impact of scaffold granule size use in Masquelet technique on periosteal reaction: a study in rat femur critical size bone defect model. Eur J Trauma Emerg Surg. 2022;48(1): 679-687. [44] VIATEAU V, BENSIDHOUM M, GUILLEMIN G, et al. Use of the induced membrane technique for bone tissue engineering purposes: animal studies. Orthop Clin North Am. 2010;41(1):49-56. [45] HENRICH D, SEEBACH C, NAU C, et al. Establishment and characterization of the Masquelet induced membrane technique in a rat femur critical-sized defect model. J Tissue Eng Regen Med. 2016;10(10):E382-E396. [46] AHO OM, LEHENKARI P, RISTINIEMI J, et al. The mechanism of action of induced membranes in bone repair. J Bone Joint Surg Am. 2013;95(7):597-604. [47] REN L, KANG Y, BROWNE C, et al. Fabrication, vascularization and osteogenic properties of a novel synthetic biomimetic induced membrane for the treatment of large bone defects. Bone. 2014;64:173-182. [48] RICCI E, VANOSI G, LINDENMAIR A, et al. Anti-fibrotic effects of fresh and cryopreserved human amniotic membrane in a rat liver fibrosis model. Cell Tissue Bank. 2013;14(3):475-488. [49] GINDRAUX F, RONDOT T, de BILLY B, et al. Similarities between induced membrane and amniotic membrane: novelty for bone repair. Placenta. 2017;59:116-123. [50] FENELON M, ETCHEBARNE M, SIADOUS R, et al. Comparison of amniotic membrane versus the induced membrane for bone regeneration in long bone segmental defects using calcium phosphate cement loaded with BMP-2. Mater Sci Eng C Mater Biol Appl. 2021;124:112032. [51] VITACOLONNA M, MULARCZYK M, HERRLE F, et al. Effect on the tensile strength of human acellular dermis (Epiflex®) of in-vitro incubation simulating an open abdomen setting. BMC Surg. 2014;14:7. [52] VERBOKET RD, LEIBLEIN M, JANKO M, et al. From two stages to one: acceleration of the induced membrane (Masquelet) technique using human acellular dermis for the treatment of non-infectious large bone defects. Eur J Trauma Emerg Surg. 2020;46(2):317-327. [53] DIMITRIOU R, MATALIOTAKIS GI, CALORI GM, et al. The role of barrier membranes for guided bone regeneration and restoration of large bone defects: current experimental and clinical evidence. BMC Med. 2012;10:81. [54] TARCHALA M, ENGEL V, BARRALET J, et al. A pilot study: alternative biomaterials in critical sized bone defect treatment. Injury. 2018;49(3):523-531. [55] OH Y, YOSHII T, OKAWA A. Ankle arthrodesis using a modified Masquelet induced membrane technique for open ankle fracture with a substantial osteochondral defect: a case report of novel surgical technique. Injury. 2019;50(11):2128-2135. [56] NAU C, SEEBACH C, TRUMM A, et al. Alteration of Masquelet’s induced membrane characteristics by different kinds of antibiotic enriched bone cement in a critical size defect model in the rat’s femur. Injury. 2016;47(2): 325-334. [57] WANG X, LUO F, HUANG K, et al. Induced membrane technique for the treatment of bone defects due to post-traumatic osteomyelitis. Bone Joint Res. 2016;5(3):101-105. [58] HAN W, SHEN J, WU H, et al. Induced membrane technique: advances in the management of bone defects. Int J Surg. 2017;42:110-116. |
| [1] | Bai Chen, Yang Wenqian, Meng Zhichao, Wang Yuze. Strategies for repairing injured anterior cruciate ligament and promoting graft healing [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(9): 1457-1463. |
| [2] | Yang Yufang, Yang Zhishan, Duan Mianmian, Liu Yiheng, Tang Zhenglong, Wang Yu. Application and prospects of erythropoietin in bone tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(9): 1443-1449. |
| [3] | Dai Yuexing, Zheng Liqin, Wu Minhui, Li Zhihong, Li Shaobin, Zheng Desheng, Lin Ziling. Effect of vessel number on computational fluid dynamics in vascular networks [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(8): 1206-1210. |
| [4] | Wang Shanshan, Shu Qing, Tian Jun. Physical factors promote osteogenic differentiation of stem cells [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(7): 1083-1090. |
| [5] | Lan Weiwei, Yu Yaodong, Huang Di, Chen Weiyi. In vitro degradation behavior of Mg-Zn-Ca alloys [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 717-723. |
| [6] | Zhou Xiaowen, Fu Zuchang, Huang Fei, Ai Jianguo, Zhao Feng. Bone defect blocked by bone cement segmental filling in single-plane tibial bone transport [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 736-740. |
| [7] | Zhu Liwei, Wang Jiangyue, Bai Ding. Application value of nanocomposite gelatin methacryloyl hydrogels in different bone defect environments [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 753-758. |
| [8] | Yin Tong, Yang Jilei, Li Yourui, Liu Zhuoran, Jiang Ming. Application of core-shell structured nanofibers in oral tissue regeneration [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 766-770. |
| [9] | Wang Jiani, Chen Junyu. Angiogenesis mechanism of metal ions and their application in bone tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(5): 804-812. |
| [10] | Yang Yuqing, Chen Zhiyu. Role and application of early transient presence of M1 macrophages in bone tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 594-601. |
| [11] | Zhou Shibo, Guan Jianbin, Yu Xing, Zhao He, Yang Yongdong, Liu Tao. Animal models of femoral bone defects: preparation status and characteristics [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 633-638. |
| [12] | Dai Jing, Liu Shasha, Shen Mingjing. Exosome-loaded injectable hydrogel for repairing bone defects around implants [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 347-354. |
| [13] | Gao Xueyu, Zhang Wentao, Sun Tianze, Zhang Jing, Li Zhonghai. Application of metal ions in bone tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 439-444. |
| [14] | Yang Jie, Hu Haolei, Li Shuo, Yue Wei, Xu Tao, Li Yi. Application of bio-inks for 3D printing in tissue repair and regenerative medicine [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 445-451. |
| [15] | Chen Pinrui, Pei Xibo, Xue Yiyuan. Function and advantages of magnetically responsive hydrogel in bone tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(3): 452-457. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||