Chinese Journal of Tissue Engineering Research ›› 2022, Vol. 26 ›› Issue (36): 5875-5880.doi: 10.12307/2022.783
Previous Articles Next Articles
Accurate simulation of stress state in bone joint and related soft tissue injury by three-dimensional finite element analysis
Xiong Hengheng1, Nie Weizhi2
- 1Shandong University of Traditional Chinese Medicine, Jinan 250355, Shandong Province, China; 2Shandong Wendeng Osteopathic Hospital, Weihai 264400, Shandong Province, China
-
Received:2021-11-15Accepted:2021-12-28Online:2022-12-28Published:2022-04-28 -
Contact:Nie Weizhi, MD, Chief physician, Shandong Wendeng Osteopathic Hospital, Weihai 264400, Shandong Province, China -
About author:Xiong Hengheng, Master candidate, Shandong University of Traditional Chinese Medicine, Jinan 250355, Shandong Province, China
CLC Number:
Cite this article
Xiong Hengheng, Nie Weizhi. Accurate simulation of stress state in bone joint and related soft tissue injury by three-dimensional finite element analysis[J]. Chinese Journal of Tissue Engineering Research, 2022, 26(36): 5875-5880.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks

2.1 有限元分析的发展历程和基本原理 20世纪40年代,航天技术迅速发展,对飞机结构设计和建造材料提出了更严苛的要求。传统研究方法周期长、资金投入大,无法满足现实需求,迫切需要一种简易、精细、可行的实验手段。在这一背景下,有限元分析方法逐渐兴起。1956年,TURNER、CLOUGH、MARTIN及TOPP等4位学者在继承COURANT [3]研究成果的基础上,共同在《Journal of the Aeronautical Sciences》期刊上发表了一篇名为“Stiffness and Deflection Analysis of Complex Structures”的论文,文中采用有限元技术分析航天器的结构强度,并将其命名为刚性法,被认为是有限元技术实际应用的开端[4]。1960年,CLOUGH在美国土木工程学会第二届计算机会议上正式提出有限元分析方法名称,并将其应用范围扩展至其他领域,标志着有限元分析方法的正式诞生[5],见图4。"
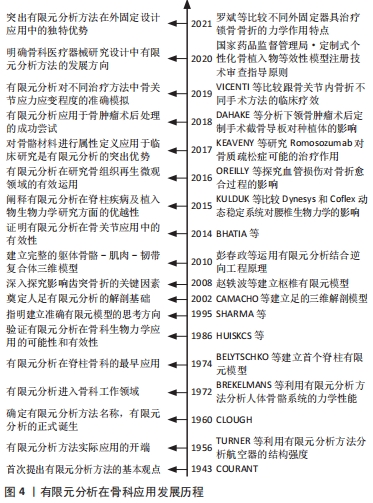
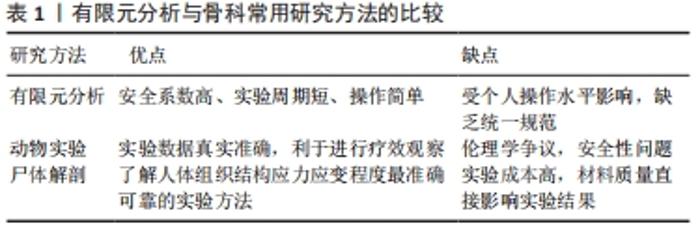
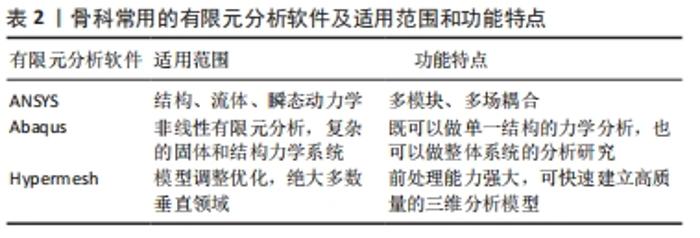
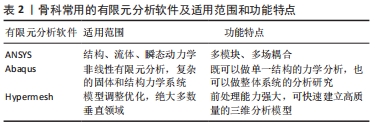
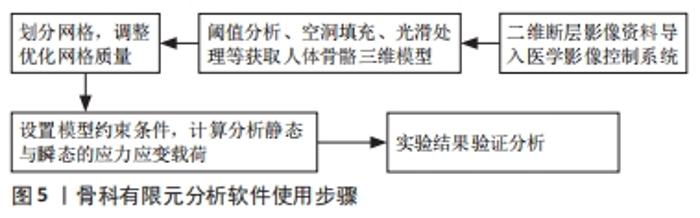
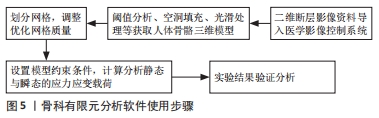
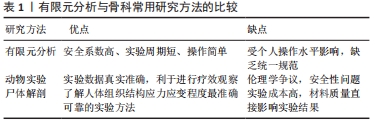
有限元分析的基本原理是利用数学方法将连续物体划分为有限个单元,根据单元间节点数及实际承受的节点载荷,对每一单元拟定一个适宜的近似结果,最后将各个单元所建立的关系式加以集成,推导出域总的满足条件,得出最终结果解释。因其划分出的单元个数及节点数目是有限的,故被称为有限元分析方法。基本步骤包括:①问题及求解域定义;②求解域离散化;③确定状态变量及控制方法;④单元推导;⑤总装求解;⑥联立方程组求解和结果解释。有限元分析尤其适用于复杂结构的力学状态分析[6],具有简便、高效、适用性广等优势,随着计算机技术的发展普及,在各领域科研中发挥着越来越重要的作用[7]。 2.2 骨科常用的有限元分析软件和使用方法 通过与体外实验结果对比,有限元分析在骨科应用的合理性和有效性已被众多学者证实[8-10],进一步推动了有限元分析在骨科的应用,使有限元分析方法与骨科工作的联系愈加密切,见表1。当前骨科常用的有限元分析软件包括ANSYS、Abaqus、Hypermesh等,每个软件的适用范围和功能特点各有不同,见表2。ANSYS适用范围最广,在结构、流体、瞬态动力学分析领域均具有突出作用,具有多模块、多场耦合的显著优势,也是临床使用最广泛的有限元分析软件。Abaqus擅长非线性有限元分析,不仅可以做单一结构的力学分析,还可以做整体系统的分析研究。Hypermesh最突出的特点就在于其强大的前处理能力,其先进的自动网格划分技术可极大地简化复杂几何有限元建模过程,并可兼容现有的常见求解器,提高临床使用效率。不同有限元分析软件实际应用的侧重点虽有所区别,但其总的使用方法基本类似。以ANSYS为例,首先将CT、MRI等影像学检查获取的二维断层影像资料导入医学影像控制系统(现在常用的软件为Mimics 19.0),进行阈值分析、空洞填充、光滑处理得到人体骨骼三维模型,然后划分ANSYS基本网格,调整优化网格质量,之后设置模型的约束条件,计算分析静态与瞬态的应力应变载荷,最后结合临床实际或可行性实验进行验证分析,归纳出一般规律,提高数据的可信度[11],见图5。整个操作过程的重点和难点在于网格的划分和质量控制,当前通常把骨骼三维模型划分为四面体或六面体网格,二者在使用中各有优缺点。四面体网格边界适用性强,可快速生成网格,但结果精度不及同等实验条件下的六面体网格,六面体计算收敛速度快,但需更多的时间进行几何简化切分,网格生成速度不及四面体网格。临床上应根据骨骼的具体形态和研究目的选择恰当的有限元分析软件,进行规范合理的建模分析,得到更加精准可信的实验结果。 "

2.3 有限元分析在骨科临床中的应用与进展 2.3.1 有限元分析在脊柱外科的应用 脊柱解剖结构复杂,其间穿行着多条重要神经血管,一旦发生骨折脱位,极易造成脊髓和马尾神经的损害,出现疼痛、活动受限等症状,严重者可导致瘫痪,甚至危及生命。以往对脊柱损伤的诊疗通常依赖于传统影像学检查,这种方法虽然能较清晰地显示损伤部位和类型,但却无法对损伤时脊柱的应力状态和术后内固定材料的负荷情况进行有效分析,在临床应用上存在一定的局限性。而通过建立脊柱有限元模型可以模拟脊柱在不同条件下的应力分布情况,提供传统检查方法无法直接获取的临床资料,具有其他研究方法不可替代的作用[12]。 1974年,BELYSCHKO等[13]将有限元分析方法应用于脊柱生物力学分析,建立了最早的脊柱有限元模型,为脊柱损伤的诊疗提供了新途径。但由于时代条件的限制,早期脊柱有限元模型具有设计不全面、精度低等困惑,在实际应用中存在较大误差,在当时没有得到广泛关注。但是随着数字诊疗技术和计算机技术的迅速发展,有限元分析方法在脊柱骨科的应用也愈加成熟。彭春政等[14]运用逆向工程原理构建人体躯干的三维几何模型,可用于人体脊柱生物力学变化规律的可视化分析。赵轶波等[15]探讨齿突在不同角度载荷下的损伤机制,明确外力作用的方向是决定齿突骨折类型的关键因素。GHEZELBASH等[16]通过对比体外实验和有限元模型在腰椎内部载荷分担的研究结果,提出建立脊柱有限元模型有助于在不同载荷时和不同运动状态下预测脊柱真实受力情况,为脊柱损伤的诊断和病机分析提供有力依据。在脊柱损伤治疗方面,对建立的脊柱有限元模型进行生物力学分析可有效评估植入物变异、外科技术和病理机制等,优化手术设计和预测疾病治疗结果[17]。OTTARDI等[18]通过建立腰椎前凸有限元模型,证实经椎弓根截骨术可用于矫正严重畸形。FAN等[19]通过对比腰椎融合模型和Topping-off模型在椎间盘退变中的应用,证明Topping-off技术可降低腰椎相邻节段的应力和活动度,减缓椎间盘退变。 如今,有限元分析正成为脊柱骨科普遍使用的临床研究方法。与传统研究法相比,有限元分析在脊柱疾病及植入物生物力学研究方面具有无可比拟的优越性[20]。但在实际使用过程中有限元分析还存在着软硬件获取受限、通用模型匮乏以及非骨性结构建模缺少精准度等问题[21],在今后使用过程中应加强与影像、检验等辅助医疗科室的合作,从解剖结构、材料属性、模型验证等多个方面入手,提高有限元模型的精确性[22],扩大有限元分析在脊柱外科的适用范围。 2.3.2 有限元分析在关节外科的应用 关节损伤是最常见的骨科疾患之一。近年来,关节损伤患者不断增加,发病率也在逐年升高,若得不到及时诊断治疗,将会对患者的生命健康产生危害。关节损伤主要包括骨折、脱位以及关节囊和韧带的损伤。在临床诊疗时,多数需对损伤机制(即受伤时骨与肌腱、韧带等组织的应力情况)进行分析。有限元分析凭借其在力学研究领域的独特优势随即被引入到骨关节临床诊疗和科研中。BHATIA等[23]通过对比有限元分析和传统尸体解剖力学分析方法,证明了有限元模型在骨关节应用中的有效性与准确性,2014年之后其在骨关节领域的应用愈加普遍。SADEGHIAN等[24]利用有限元模型分析Cam型髋关节撞击综合征发生发展中骺板的作用,证明来自股骨头后方的应力更易导致骺板的屈曲和凹凸化。VAN DER BRACHT等[25]通过建立膝关节有限元模型研究发现,外侧胫骨骨道重建前交叉韧带会导致移植物的峰值应力从股骨骨道口转移到胫骨骨道口,为临床治疗方案和内置物的选择提供重要依据。 在关节损伤的治疗中,有限元分析广泛应用于内、外固定器的选择置放和人工关节置换等方面[26]。KWON等[27]建立膝关节假体有限元模型进行关节应力分析,证明假体的接触面越大,越能有效分散人体受力,延缓假体磨损。CHEN等[28]对臼杯-骨界面应力影响的有限元分析,证明对于发育性髋关节发育不良患者,臼杯适度上移重建与解剖位置重建相比,远期生存率、假体磨损率及术后并发症发生率无明显差别。个性化治疗方案和医疗器械研发是当前骨科临床工作的发展方向,有限元分析通过对患者各自病理状态的准确模拟,在促进个性化医疗的发展中发挥了积极作用。 当前,有限元分析在骨关节领域应用极其广泛,其与传统影像学检查相结合,能提供全面准确的临床诊断资料,使治疗方案更加精细可靠。但目前有限元分析在骨关节生物力学应用范围仅限于静态结构,今后应用中可通过修改制定结构本身的模态参数,分析结构对动载荷的响应特点,从而确定节点位移,提高有限元分析在动态分析领域的准确性,满足骨关节动态分析的现实需求。 2.3.3 有限元分析在创伤骨科的应用 创伤骨科的诊疗范围包括四肢创伤、骨盆创伤、脊柱创伤以及关节创伤。以往关于有限元分析在创伤骨科应用的相关文献主要集中在四肢和骨盆创伤领域。然而无论是四肢创伤,还是骨盆创伤,其致伤因素绝大多数都包含外力伤害。有限元分析在分析外力伤害时损伤部位的应力情况具有突出优势,在创伤骨科得到广泛应用。CAMACHO等[29]重建人足三维解剖模型,奠定了人足有限元分析的解剖基础。VICENTI等[30]比较撬拨复位后空心螺钉加压内固定与切开复位锁定钢板内固定对SandersⅡ、Ⅲ型跟骨骨折的治疗作用,证明前种方法治疗后可更早地进行功能锻炼以恢复患肢功能。CHEN等[31]对锁定钢板和髓内钉治疗肱骨近端骨折时的力学特性进行有限元分析,证明锁定板能提供更可靠的稳定性。LUCATTELLI等[32]对拇外翻术后“8”字绷带固定应力状态进行有限元分析,证明微创治疗拇外翻在未行内固定的情况下,依靠弹性固定仍可保证截骨端稳定,促进断端愈合。创伤骨科常见的开放性骨折在多数情况下可明确诊断,但对于隐匿性开放骨折,软组织损伤不明显,单纯依靠传统检查方法难以确诊,通过对损伤部位的骨及肌肉、韧带等组织建立有限元模型,配合影像学检查,可明确损伤严重程度,指导制定治疗方案,减少并发症。OREILLY等[33]通过对骨折愈合过程进行有限元分析,证明在低氧环境下软组织增生受到抑制期间发生软骨细胞肥大和软骨内成骨。汪松等[34]利用有限元分析方法评估单臂和Taylor外固定治疗老年GustiloⅡ型胫腓骨骨折的临床疗效,证明Taylor外固定架在治疗开放性胫腓骨骨折方面具有更大优势,为指导制定临床治疗方案,促进骨折愈合提供了新方法和新思路。 有限元分析在创伤骨科的普遍应用,在推动临床诊疗技术发展、简化临床治疗工作方面发挥重要作用。但由于创伤骨科的疾病类型多数为开放性损伤,软组织损伤严重,病情复杂,对损伤部位建立准确数字模型存在较大困难,有限元分析在使用过程中存在一定的局限性。今后工作中可通过修改研究对象属性设定,增加参数因素等逐渐弥补这一缺陷,提高应用灵活性,扩大应用范围,满足创伤骨科临床工作需求。 2.3.4 有限元分析在骨内科的应用 骨内科是骨科学的一大分支,是指检查、诊断和非手术治疗肌肉骨骼系统损伤的一门学科[35]。主要诊疗范围包括骨炎、骨肿瘤、骨质疏松以及其他骨代谢性疾病,主要治疗手段是药物内服外敷和运动疗法。有限元分析在骨内科的应用主要集中在骨肿瘤以及骨质疏松症等领域,并在二者的临床诊疗中发挥重要作用。在骨肿瘤的治疗过程中,依靠X射线片和CT磁共振等影像学检查可明确病变部位和范围,但骨肿瘤体积对手术方案的选择有很大影响,其形状的多样化和不规则给临床治疗带来了难点[36]。单独利用影像学检查无法准确计算出骨肿瘤的实际体积,还需更加精确可行的测量方法。而通过建立损伤部位的有限元模型进行计算机断层扫描能够准确预测肿瘤假体的应力分布和稳定性,为指导假体设计和优化内固定方式提供依据[37]。IWAI等[38]通过有限元分析方法分析骨肿瘤活检后病理性骨折的危险因素,结果证明骨活检孔的宽度<周长的10%有助于将骨强度减弱降至最低。ZHAO等[39]通过有限元分析研究双支撑腓骨-踝关节融合术的生物力学效果,证明双支撑腓骨-踝关节融合术是治疗胫骨远端恶性肿瘤后缺损的一种可行方法。骨肿瘤分类复杂,在其治疗、预后和风险评估中,有限元分析都发挥着不可替代的作用。 骨质疏松症是一种以骨量低下、骨微结构损坏、骨强度下降、易发生骨折为特征的全身性骨病[40],是骨内科另一种常见疾病,多发生于60岁以上老年人,尤以女性多见,其主要病理变化是矿盐和骨基质比例减小,骨微观结构破坏。改善骨微结构是骨质疏松症治疗的主要目标[41]。在临床工作中建立骨组织有限元模型进行应力状态分析能准确计算骨强度,评价临床治疗效果,为骨质疏松症的治疗和预后提供有力依据。KEAVENY等[42]分别对罗莫苏单抗(Romosozumab)、安慰剂或特立帕肽治疗12个月的绝经后低骨量女性的L1椎体和股骨近端建立有限元模型,结果表明Romosozumab对于椎体或非椎体部位的骨强度和骨密度均有改善,为骨质疏松症提供了一种潜在高效的治疗方法。HE等[43]利用微有限元分析评估全髋关节置换术后骨小梁的力学性能,证明软骨下骨小梁的骨板和骨杆的变化在骨关节炎和骨质疏松症进展中起着关键作用,软骨下骨小梁的改善可能是很有前途的治疗方法。 有限元分析在骨内科的广泛应用,极大地提高了对骨及相关附属组织实际负荷状态分析的准确性,促进了临床诊疗技术的发展。但在目前使用过程中,有限元模型的准确度会受到图像扫描分辨率等因素的影响,导致实验结果的可信度受到质疑。因此在使用过程中必须加强对实验影响因素的控制调节,提高实验结果的准确性,符合临床要求。 2.4 有限元分析在骨科医疗器械研究设计中的应用 这里论述的骨科医疗器械主要是指固定器械。骨科固定器械包括内固定和外固定,二者在研究设计和临床应用过程中必须详细分析人体解剖结构的生物力学状态,符合各关节以及整个躯体的运动规律。有限元分析可通过对人体解剖结构建立三维模型,准确计算出机体在各种状态下的生理负荷状况,在指导各类型固定装置设计应用中发挥突出作用。在内固定设计应用中,李甜甜等[44]对比股骨干骨折新型与传统锁定加压接骨板的有限元模型生物力学性能,证明新型锁定加压接骨板拥有更有效的生物力学稳定性。在外固定设计应用中,罗斌等[45]利用该法对比新型外固定护具及改良的“8”字绷带加T型夹板治疗锁骨骨折的力学作用特点,证明前者复位固定骨折端的能力优于改良的“8”字绷带+T型夹板。有限元分析丰富了骨科固定器械的研发实验手段,可为临床应用提供更优选择。 骨科医疗器械设计应用步骤一般分为方案提出、实验设计、资料收集、资料验证以及产品制造等5个阶段。研究人员根据临床需求提出医疗器械研发方案,预测固定装置对疾病的疗效以及对人体正常生理功能的影响。通过制定相应的实验计划,利用有限元分析对固定装置在人体的生物力学状态进行模拟,获取固定装置对人体真实生理状态影响的相关资料。将收集到的实验资料与预测结果比较,确定固定装置的实际疗效及对正常生理功能的影响,最后决定该类固定装置是否值得制造推广。在各阶段工作中有限元分析都发挥了重要作用,不仅缩短了研发周期,同时节省了大量研发成本。 近年来,随着增材制造技术的推广,更多的新型医疗器械不断涌现,个性化器械成为骨科固定器械新的发展方向[46]。有限元分析可根据患者的具体情况灵活修改实验模型,指导设计出更符合患者实际需求的固定装置,与传统有创性研究方法相比,在个性化固定器械设计应用方面具有安全、经济、易操控等优点,极大地促进了个性化固定器械的发展,丰富了临床应用的可选性。目前,有限元分析在医疗器械设计应用过程中还缺乏统一标准,需制定相应的操作规范,对有限元分析在应用中的合理性进行评价,或提高有限元模型的精度,利用数字技术直接获得个性化器械的性能数据,确保个性化器械的风险受益可接受[47]。 有限元分析在骨科应用中存在的问题及解决方案,见表3。 "

| [1] BREKELMANS WA, POORT HW, SLOOFF TJ. A new method to analyse the mechanical behaviour of skeletal parts. Acta Orthop Scand. 1972; 43(5):301-317. [2] RYBICKI EF, SIMONEN FA, WEIS EB JR. On the mathematical analysis of stress in the human femur.J Biomech. 1972;5(2):203-215. [3] COURANT R.Variational methods for the solution of problems of equilibrium and vibrations. Bull Amer Math Soc.1943;49(1):1-23. [4] TUMER MS, CLOUGH RW, MANIN HC, et al. Stiffness and deflection analysis of complex structure. Journal of the Aeronautical Sciences. 1956;23(8):805-823. [5] CLOUGH RW. The finite element in plane stress analysis[C]. Pittsburg: Proceedings of the 2nd Conference on Electronic Computation of American Society of Civil Engineers. 1960:345-378. [6] BEN H, MAX W, MATT B. Improvements in finite element analysis for complex structural design. SESOC Journal. 2017;30(2):71-78. [7] LIU Y, LI XJ, ZHAO YP. State of the Art in Finite Element Analysis Technology.Advanced Materials Research. 2012;1823(529):205-209. [8] NIKKHOO M, CHENG CH, WANG JL, et al. Development and validation of a geometrically personalized finite element model of the lower ligamentous cervical spine for clinical applications. Comput Biol Med. 2019;109:22-32. [9] QIN JS, WANG Y, PENG XQ, et al. Three-dimensional finite element modeling of whole lumbar spine and its biomechanical analysis. J Med Biomech. 2013;28(3):321-325. [10] HUISKES R, CHAO EYS,胡家栋.骨科生物力学有限元分析头10年工作综述[J].力学进展,1986,16(1):98-116. [11] 倪鹏辉,张鹰,杨晶,等.临床骨科中应用的有限元分析法:新理论与新进展[J].中国组织工程研究,2016,20(31):4693-4699. [12] MACKIEWICZ A, BANACH M, DENISIEWICZ A, et al. Comparative studies of cervical spine anterior stabilization systems--Finite element analysis. Clin Biomech (Bristol, Avon). 2016;32:72-79. [13] BELYTSCHKO T, KULAK RF, SCHULTZ AB, et al. Finite element stress analysis of an intervertebral disc. J Biomech. 1974;7(3):277-285. [14] 彭春政,张胜年,陆爱云.人体躯干骨骼-肌肉-韧带结构三维有限元模型的建立和验证[J].中国运动医学杂志,2010,29(6):702-705. [15] 赵轶波,马迅,陈维毅,等.枢椎有限元模型建立及齿突骨折的有限元分析[J].中华骨科杂志,2008,28(5):392-395. [16] GHEZELBASH F, SCHMIDT H, SHIRAZI-ADL A, et al. Internal load-sharing in the human passive lumbar spine: Review of in vitro and finite element model studies. J Biomech. 2020;102:109441. [17] 肖广润,杨建东,林升元,等.有限元分析在脊柱外科中的应用及研究进展[J].国际骨科学杂志,2020,41(6):347-351. [18] OTTARDI C, GALBUSERA F, LUCA A, et al. Finite element analysis of the lumbar destabilization following pedicle subtraction osteotomy. Med Eng Phys. 2016;38(5):506-509. [19] FAN Y, ZHOU S, XIE T, et al. Topping-off surgery vs posterior lumbar interbody fusion for degenerative lumbar disease: a finite element analysis. J Orthop Surg Res. 2019;14(1):476. [20] KULDUK A, ALTUN NS, SENKOYLU A. Biomechanical comparison of effects of the Dynesys and Coflex dynamic stabilization systems on range of motion and loading characteristics in the lumbar spine: a finite element study. Int J Med Robot. 2015;11(4):400-405. [21] 高军伟,夏英鹏.有限元分析法在我国脊柱外科的应用现状及医工合作前景展望[J].中国医疗器械信息,2018,24(18):12-13,81. [22] SHARMA M, LANGRANA NA, RODRIGUEZ J. Role of ligaments and facets in lumbar spinal stability. Spine (Phila Pa 1976). 1995;20(8):887-900. [23] BHATIA VA, EDWARDS WB, TROY KL. Predicting surface strains at the human distal radius during an in vivo loading task--finite element model validation and application. J Biomech. 2014;47(11):2759-2765. [24] SADEGHIAN SM, LEWIS CL, SHEFELBINE SJ. Predicting growth plate orientation with altered hip loading: potential cause of cam morphology. Biomech Model Mechanobiol. 2020;19(2):701-712. [25] VAN DER BRACHT H, TAMPERE T, BEEKMAN P, et al. Peak stresses shift from femoral tunnel aperture to tibial tunnel aperture in lateral tibial tunnel ACL reconstructions: a 3D graft-bending angle measurement and finite-element analysis. Knee Surg Sports Traumatol Arthrosc. 2018;26(2):508-517. [26] SUH DS, KANG KT, SON J, et al. Computational study on the effect of malalignment of the tibial component on the biomechanics of total knee arthroplasty: A Finite Element Analysis. Bone Joint Res. 2017; 6(11):623-630. [27] KWON OR, KANG KT, SON J, et al. Importance of joint line preservation in unicompartmental knee arthroplasty: Finite element analysis. J Orthop Res. 2017;35(2):347-352. [28] CHEN M, LUO ZL, WU KR, et al. Cementless Total Hip Arthroplasty With a High Hip Center for Hartofilakidis Type B Developmental Dysplasia of the Hip: Results of Midterm Follow-Up. J Arthroplasty. 2016;31(5): 1027-1034. [29] CAMACHO DL, LEDOUX WR, ROHR ES, et al. A three-dimensional, anatomically detailed foot model: a foundation for a finite element simulation and means of quantifying foot-bone position. J Rehabil Res Dev. 2002;39(3):401-410. [30] VICENTI G, CARROZZO M, SOLARINO G, et al. Comparison of plate, calcanealplasty and external fixation in the management of calcaneal fractures. Injury. 2019;50 Suppl 4:S39-S46. [31] CHEN YN, CHANG CW, LIN CW, et al. Numerical investigation of fracture impaction in proximal humeral fracture fixation with locking plate and intramedullary nail. Int Orthop. 2017;41(7):1471-1480. [32] LUCATTELLI G, CATANI O, SERGIO F, et al. Preliminary Experience With a Minimally Invasive Technique for Hallux Valgus Correction With No Fixation. Foot Ankle Int. 2020;41(1):37-43. [33] OREILLY A, HANKENSON KD, KELLY DJ. A computational model to explore the role of angiogenic impairment on endochondral ossification during fracture healing. Biomech Model Mechanobiol. 2016;15(5):1279-1294. [34] 汪松,孙倩,冯硕,等.单臂和Taylor外固定治疗老年GustiloⅡ型胫腓骨骨折患者临床疗效及有限元分析[J].中华老年医学杂志, 2018,37(9):1004-1008. [35] 孙材江,彭力平.实用骨内科学[M].北京:人民军医出版社,2008: 75-77. [36] 陈禺,邓江.有限元分析在骨科应用的研宄进展[J].中国伤残医学, 2018,26(24):97-99. [37] DAHAKE S, KUTHE A, KULKARNI S, et al. Finite element analysis of customized implant in mandibular reconstruction after tumor resection with and without using customized surgical osteotomy guide. Int J Med Robot. 2018;14(1):e1854-e1854. [38] IWAI T, HOSHI M, OEBISU N, et al. Prediction of Risk Factors for Pathological Fracture After Bone Tumor Biopsy Using Finite Element Analysis. Cancer Manag Res. 2021;13:3849-3856. [39] ZHAO Z, YAN T, GUO W, et al. Is double-strut fibula ankle arthrodesis a reliable reconstruction for bone defect after distal tibia tumor resection?-a finite element study based on promising clinical outcomes. J Orthop Surg Res. 2021;16(1):230. [40] KARLSSON MK, KHERAD M, HASSERIUS R, et al. Characteristics of Prevalent Vertebral Fractures Predict New Fractures in Elderly Men. J Bone Joint Surg Am. 2016;98(5):379-385. [41] 王志鹏,宋敏,赵文韬,等.骨质疏松症药物治疗的有限元分析研究进展[J].中国骨质疏松杂志,2018,24(7):971-974,980. [42] KEAVENY TM, CRITTENDEN DB, BOLOGNESE MA, et al. Greater Gains in Spine and Hip Strength for Romosozumab Compared With Teriparatide in Postmenopausal Women With Low Bone Mass. J Bone Miner Res. 2017;32(9):1956-1962. [43] HE Z, CHU L, LIU X, et al. Differences in subchondral trabecular bone microstructure and finite element analysis-based biomechanical properties between osteoporosis and osteoarthritis. J Orthop Translat. 2020;24:39-45. [44] 李甜甜,李世芸,熊鹰,等.新型与传统锁定加压接骨板固定股骨干骨折的生物力学比较[J].医用生物力学,2021,36(5):757-761. [45] 罗斌,黄思聪,马俊昌,等.新型外固定护具治疗锁骨骨折有限元分析[J].新中医,2021,53(21):115-120. [46] 孙嘉怿,郭晓磊,郭亚娟.有限元分析在骨科植入器械研发中的应用探讨[J].生物骨科材料与临床研究,2021,18(5):86-88. [47] 国家药品监督管理局.定制式个性化骨植入物等效性模型注册技术审查指导原则[Z].国家药品监督管理局通告,2020年第48号. |
| [1] | Zhan Yi, Wang Biao, Ma Yuli, He Simin, Sun Honghui, Hao Dingjun. Biomechanical comparison between a novel bone cement screw system and common surgical methods for the treatment of Kummell’s disease [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 385-390. |
| [2] | Lu Hui, Wu Qimei, Liu Rong. Finite element analysis and application of unilateral and bilateral bone-filling mesh container in treatment of osteoporotic vertebral compression fracture [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 391-397. |
| [3] | Wang Jianping, Zhang Xiaohui, Yu Jinwei, Wei Shaoliang, Zhang Xinmin, Xu Xingxin, Qu Haijun. Application of knee joint motion analysis in machanism based on three-dimensional image registration and coordinate transformation [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(在线): 1-5. |
| [4] | Zhu Chan, Han Xuke, Yao Chengjiao, Zhou Qian, Zhang Qiang, Chen Qiu. Human salivary components and osteoporosis/osteopenia [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1439-1444. |
| [5] | Jin Tao, Liu Lin, Zhu Xiaoyan, Shi Yucong, Niu Jianxiong, Zhang Tongtong, Wu Shujin, Yang Qingshan. Osteoarthritis and mitochondrial abnormalities [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1452-1458. |
| [6] | Zhang Lichuang, Xu Hao, Ma Yinghui, Xiong Mengting, Han Haihui, Bao Jiamin, Zhai Weitao, Liang Qianqian. Mechanism and prospects of regulating lymphatic reflux function in the treatment of rheumatoid arthritis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1459-1466. |
| [7] | Wei Guoqiang, Li Yunfeng, Wang Yi, Niu Xiaofen, Che Lifang, Wang Haiyan, Li Zhijun, Shi Guopeng, Bai Ling, Mo Kai, Zhang Chenchen, Xu Yangyang, Li Xiaohe. Biomechanical analysis of non-uniform material femur under different loads [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1318-1322. |
| [8] | Zhang Yufang, Lü Meng, Mei Zhao. Construction and verification of a full spine biomechanical model of adolescent scoliosis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1351-1356. |
| [9] | Zhang Jichao, Dong Yuefu, Mou Zhifang, Zhang Zhen, Li Bingyan, Xu Xiangjun, Li Jiayi, Ren Meng, Dong Wanpeng. Finite element analysis of biomechanical changes in the osteoarthritis knee joint in different gait flexion angles [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1357-1361. |
| [10] | Bai Zixing, Cao Xuhan, Sun Chengyi, Yang Yanjun, Chen Si, Wen Jianmin, Lin Xinxiao, Sun Weidong. Construction and biomechanical analysis of ankle joint finite element model in gait cycle [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1362-1366. |
| [11] | Liu Feng, Feng Yi. Finite element analysis of different Kirschner wire tension bands on transverse patella fractures during gait cycle [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1367-1371. |
| [12] | Wang Jing, Xiong Shan, Cao Jin, Feng Linwei, Wang Xin. Role and mechanism of interleukin-3 in bone metabolism [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1260-1265. |
| [13] | Zhu Chan, Han Xuke, Yao Chengjiao, Zhang Qiang, Liu Jing, Shao Ming. Acupuncture for Parkinson’s disease: an insight into the action mechanism in animal experiments [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1272-1277. |
| [14] | Zhang Jinglin, Leng Min, Zhu Boheng, Wang Hong. Mechanism and application of stem cell-derived exosomes in promoting diabetic wound healing [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1113-1118. |
| [15] | Huang Chenwei, Fei Yankang, Zhu Mengmei, Li Penghao, Yu Bing. Important role of glutathione in stemness and regulation of stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1119-1124. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||