Chinese Journal of Tissue Engineering Research ›› 2022, Vol. 26 ›› Issue (16): 2596-2601.doi: 10.12307/2022.263
Previous Articles Next Articles
Topical simvastatin administration in the treatment of periodontitis: effect of loading on sustained drug release system or biomaterial scaffold system
Liu Xiaolin1, 2, Liu Shutai1, Han Xiaoqian2, Mu Xinyue3
- 1Periodontal Department, Yantai Stomatological Hospital, Yantai 264000, Shandong Province, China; 2Department of Prosthodontics, Affiliated Hospital of Binzhou Medical College, Binzhou 256600, Shandong Province, China; 3Binzhou Medical College, Yantai 264000, Shandong Province, China
-
Received:2020-12-14Revised:2020-12-23Accepted:2021-01-27Online:2022-06-08Published:2021-12-23 -
Contact:Liu Shutai, PhD, Associate chief physician, Periodontal Department, Yantai Stomatological Hospital, Yantai 264000, Shandong Province, China -
About author:Liu Xiaolin, Master candidate, Periodontal Department, Yantai Stomatological Hospital, Yantai 264000, Shandong Province, China; Department of Prosthodontics, Affiliated Hospital of Binzhou Medical College, Binzhou 256600, Shandong Province, China
CLC Number:
Cite this article
Liu Xiaolin, Liu Shutai, Han Xiaoqian, Mu Xinyue. Topical simvastatin administration in the treatment of periodontitis: effect of loading on sustained drug release system or biomaterial scaffold system[J]. Chinese Journal of Tissue Engineering Research, 2022, 26(16): 2596-2601.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
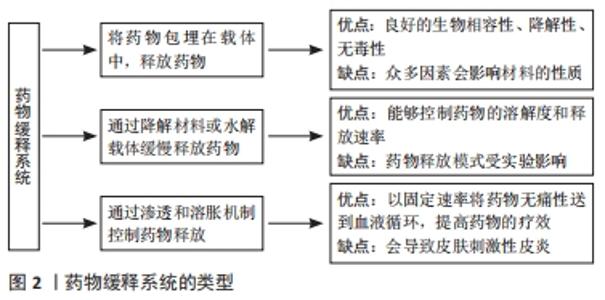
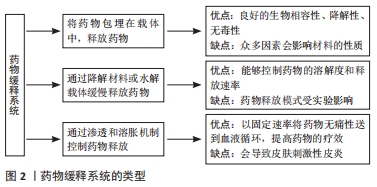
2.1 辛伐他汀治疗牙周炎的机制及使用方法 2.1.1 辛伐他汀促进骨再生机制 他汀类药物是羟甲基戊二酰辅酶A还原酶抑制剂,分为完全人工合成化合物(如罗伐他汀、西立伐他汀、氟伐他汀、阿托伐他汀)和天然化合物(如辛伐他汀、普伐他汀、洛伐他汀、美伐他汀),在临床中主要应用于防治心血管疾病、胆固醇水平的降低。近年的研究发现他汀类药物具有多重作用,包括促进骨再生、抗氧化、抑制炎症等作用。MUNDY等[1]首次发现他汀类药物能够促进成骨细胞的分化,促进新骨的形成。研究辛伐他汀促进骨再生的内在机制发现,辛伐他汀能够增强骨形态发生蛋白2的表达,而骨形态发生蛋白2能够刺激DNA的合成和细胞的复制,从而促进干细胞向成骨分化。骨血管在骨中分布密集,并为骨的形成提供必要的营养和氧,血管生成因子能够促进骨血管的形成,而辛伐他汀提高了血管生成因子的表达,促进了骨血管的形成,从而有利于新骨的形成[2]。另外,α5整合素在骨髓间充质干细胞成骨分化中起关键作用,辛伐他汀能够升高α5整合素的表达水平,增加细胞黏附斑激酶的磷酸化水平,从而促进骨髓间充质干细胞的成骨分化[3]。辛伐他汀能够显著增加氧化应激下骨髓间充质干细胞的自噬保护作用,通过改变自噬活性促进骨髓间充质干细胞的成骨分化。在研究辛伐他汀对破骨细胞的影响和机制时发现,辛伐他汀能导致破骨细胞的I型胶原的C端端肽和N端端肽显著降低,显著抑制破骨细胞的活性,减少骨破坏[4]。辛伐他汀通过下调活化T细胞的核因子、钙调磷酸酶依赖性1的表达调节破骨细胞的形成和功能,抑制磷酸化和核内转移,进而促进破骨细胞的凋亡[5]。将辛伐他汀应用到牙周炎骨缺损中,龈沟液检测发现核因子配体受体激活因子水平降低、骨蛋白水平升高,核因子配体受体激活因子与单核破骨细胞前体上的相应受体相互作用诱导激活多核骨吸收破骨细胞,而核因子配体受体激活因子的作用被骨蛋白阻断,从而抑制了破骨细胞的分化和活性[6]。在大鼠股骨和下颌骨骨性缺损中注射辛伐他汀,结果显示都促进了骨缺损部位的骨再生,减少了骨的损失[7-8]。这些研究说明生长因子中的他汀类药物尤其是辛伐他汀是合适的选择,机制是通过提高骨形态发生蛋白2基因的表达来促进干细胞的成骨分化;提高血管生成因子的表达促进骨血管的形成,为骨形成提供营养;升高α5整合素的表达水平,增加间充质干细胞的自噬作用,促进细胞的成骨分化,促进新骨的形成;降低破骨细胞活性,促进破骨细胞凋亡,导致骨吸收量减少。 2.1.2 辛伐他汀治疗牙周炎的机制 为研究辛伐他汀对牙周炎的影响,KAMI?SKA等[9]将他汀类药物应用到口腔生物膜上,结果发现牙龈链球菌对他汀类药物高度敏感,并且辛伐他汀和洛伐他汀对牙龈链球菌的抑菌活性最强。牙龈链球菌是牙周炎的致病菌,抑制致病菌活性可以抑制牙周炎的进展。为了研究辛伐他汀治疗牙周炎的内在机制,研究者应用辛伐他汀辅助治疗慢性牙周炎患者,结果发现辛伐他汀降低了促炎细胞因子白细胞介素6和白细胞介素8的表达,促进了抗炎细胞因子白细胞介素10的表达。其中白细胞介素6在急性炎症中处于中心地位,并且其增高程度与炎性反应程度一致,与晚期牙周炎骨质破坏有关;而白细胞介素8对中性粒细胞有细胞趋化作用,能够调节炎症反应,并且白细胞介素10通过对单核细胞和巨噬细胞的抑制作用抑制活化T辅助体克隆产生细胞因子,因此辛伐他汀可以减轻牙周的炎症,抑制牙周炎[10]。将辛伐他汀应用于牙周炎患者发现牙周探诊深度降低、临床附着丧失减少、牙周炎症减轻、龈沟液中肿瘤坏死因子α水平降低,肿瘤坏死因子α是由单核细胞和巨噬细胞分泌的,在炎症反应中起重要的作用,抑制肿瘤坏死因子α的表达可抑制牙周炎症[11]。另外,将辛伐他汀应用到牙周炎患者后,检测龈沟液后发现单核细胞金属蛋白酶1的水平降低,辛伐他汀是通过影响单核细胞金属蛋白酶1表达的信号和分子机制抑制单核细胞金属蛋白酶1的表达,而单核细胞金属蛋白酶1单核多态性与牙周炎易感性存在显著关系[12]。由此可见,辛伐他汀可以抑制牙龈链球菌的活性,降低促炎细胞因子白细胞介素6和白细胞介素8的表达,促进抗炎细胞因子白细胞介素10的表达,抑制牙周炎症的发展;抑制单核细胞金属蛋白酶1的表达,降低肿瘤坏死因子α的表达减少炎症因子的分泌,降低牙周炎的易感性,减轻牙周炎症,减少骨量损失,缓解牙周炎症状。 2.1.3 辛伐他汀的使用方法 为使辛伐他汀促进骨再生治疗牙周炎达到最好的效果,需要研究其使用时的最佳浓度及合适的给药途径。研究发现低剂量辛伐他汀能促进血管生成因子的表达、骨内血管的生成及干细胞向成骨细胞分化,显著促进骨的形成,而高剂量却抑制了该基因的表达,抑制了骨内血管的生成[13]。将辛伐他汀应用到临床发现,高剂量的辛伐他汀会使患者出现不良的肌肉反应,辛伐他汀主要是在肝脏代谢的,同时具有肝毒性及神经毒性[14]。在研究不同浓度辛伐他汀对成骨细胞活力和分化的影响时发现,辛伐他汀的浓度高于1×10-4 mol/L或1×10-3 mol/L时会导致细胞活力的下降,低于1×10-7 mol/L时不影响细胞的活性,而浓度为1×10-6 mol/L时的细胞活力最高,并能促进细胞的成骨分化[15]。在将辛伐他汀应用于大鼠口腔种植骨模型时发现,局部注射辛伐他汀较口服辛伐他汀能使大鼠形成更多的新骨[16]。将辛伐他汀应用到大鼠肌腱骨界面上时,在口服给药的对比组中出现一只老鼠死于肌肉坏死,而皮下注射辛伐他汀实验小鼠的血清水平升高、胆固醇水平降低,并且新骨形成量更多[17]。这些研究说明低剂量辛伐他汀能促进细胞的增殖及成骨分化,而高剂量反而会起到抑制作用,并且辛伐他汀的合适浓度为1×10-6 mol/L,要采用合适浓度的辛伐他汀才能使骨再生达到最佳效果。最佳辛伐他汀的给药方式为局部注射,局部注射辛伐他汀较口服能形成更多的新骨,口服他汀类药物可能会发生肌肉坏死的不良反应。 2.2 辛伐他汀药物缓释系统的特点与制备方法 2.2.1 药物缓释系统的特点 为了使辛伐他汀定量匀速地向外释放,采用药物缓释系统装载辛伐他汀。药物缓释系统是将药物包埋在聚合物载体中,然后缓慢释放药物出来,或者通过降解材料或者水解载体缓慢释放药物,再者是通过渗透和溶胀机制来控制药物释放。聚合物载体的聚乳酸-羟基乙酸共聚物微球有良好的生物相容性,并且其最终降解产物是乳酸和乙醇酸,能够参与人体的代谢且无毒性,并且这种方法装载辛伐他汀时能够长时间管理和精准控制释放速率,然而在制备过程中发现众多因素(如聚合物的浓度、聚合物的种类、分子质量、搅拌速度、pH值等)能够影响微球的性质(如形态、大小、载药量和释药量等)[18]。在研究pH值对聚乳酸-羟基乙酸共聚物微球性质的影响时发现,随着pH值环境由酸性向中性升高,微球的肽酰化越来越严重,当内部pH值由酸性变为中性时药物的滞留时间延长,聚合物的降解减慢,底物的浓度增加[19]。向聚乳酸-羟基乙酸共聚物微球制备过程中加载静压,设计常压加载、0.35 MPa、 4.0 MPa压力加载组和摇瓶震荡组,结果发现4.0 MPa压力加载组的微球降解速率和药物释放速率快于正常和其他组[20]。在采用不同比例及分子质量的聚乳酸-羟基乙酸共聚物制备微球时发现,微球表面光滑大小不一,并且微球的粒径随着分子量的增加而递减,粒径范围较宽,并且所制备的微球在负载辛伐他汀后能保持药物持续、长效的释放;同时观察不同搅拌速度对负载辛伐他汀微球的影响,结果发现搅拌速度增加,聚乳酸-羟基乙酸共聚物微球的粒径会随之减小,并且辛伐他汀的包封率增加[21]。将装载辛伐他汀的聚乳酸-羟基乙酸共聚物微球应用到大鼠时发现,聚乳酸-羟基乙酸共聚物微球具有无刺激性和非免疫原性,并且有优良的载药量、包封率和释放度,但同时发现聚乳酸-羟基乙酸共聚物微球在体内可能诱发更强的炎症反应,并且在体内降解完成需要更长的时间[22]。另外,采用水溶性乙基纤维素和水溶性羟丙基纤维素相分离膜可以用作药物的包衣来控制药物的溶解度和释放速率,其中水溶性羟丙基纤维素起到造孔的作用,在改变水溶性乙基纤维素或水溶性羟丙基纤维素的性质时可以改变薄膜的微观结构(如薄膜的渗透性和孔的大小),影响药物的释放。薄膜的孔径尺寸越大薄膜的通透性越高,药物通过包膜的扩散也越多,但是发现药物释放过程中受多种因素影响,如生产条件、药物溶解度、分子质量等。此外,药物释放模式也受体外实验条件的影响,如介质的pH值、缓冲液的组成和容量、释放介质的离子强度等[23]。透皮给药系统能够以固定的速率将药物无痛性的通过皮肤送到血液循环中,其是通过改变角质层的理化性质、水化特性、细胞间通道脂质和蛋白结构增加药物的渗透,相比传统的口服和侵入性给药具有众多优点,能够提高药物的疗效、维持稳定的血浆药物水平、预防肝脏的首通代谢,但发现会使皮肤敏感,产生刺激性皮炎[24]。这些研究说明,将药物包埋在聚合物载体的系统能够长时间管理和精准控制药物的释放速率,具有良好的生物相容性和生物降解性,但是制备过程中的pH值、施加压力、聚合物的分子质量、搅拌速度等都会对微球的粒径、孔径率、包封率、降解速率及药物释放速率等造成影响。各药物缓释系统的优缺点,见图2。"
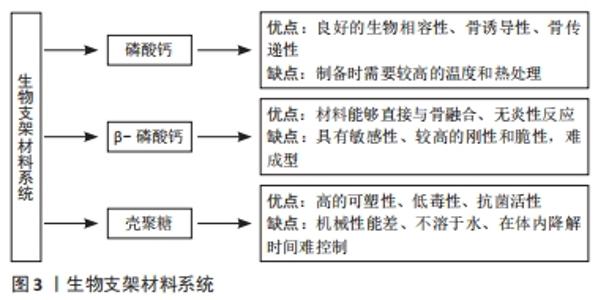
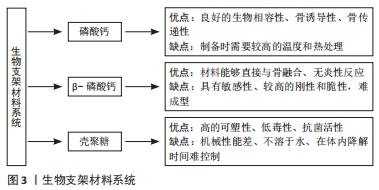
2.2.2 药物缓释系统的制备方法 为了控制药物缓释系统的性质,使其装载辛伐他汀的包封率、负载量,缓释效果达到最佳,并减少不良反应,学者们研究了最佳的制备方法。OGAWA等[25]为了延长药物的释放,首次采用复乳溶剂蒸发法制备出载药微球,该方法是将聚乳酸和聚乳酸/乙醇酸聚合物作包埋剂,将活性化合物的水溶液乳化成疏水聚合物的有机溶液,发现制备出的微球形态好、载药量高、粒径均匀,在体内能够缓慢释药。另外,采用水包油乳剂/溶剂蒸发法制备载辛伐他汀的聚乳酸-羟基乙酸共聚物微球,发现这种制备方法简单稳定,辛伐他汀以分子的形式分散到聚合物中,微球形态是均匀的,观察微球释放辛伐他汀的情况发现无初始爆裂性释放[26]。在比较溶剂萃取法、溶剂蒸发法、共溶剂法制备聚乳酸-羟基乙酸共聚物微球的实验中发现,3种方法制备的微球内部结构不同但粒径分布相似,与溶剂萃取法和共溶剂法相比,溶剂蒸发法制备的微球在前4周表现出相对稳定的释放速率,能够明显促进干细胞的成骨分化[27]。研究采用不同的涂层技术来制备药物的包衣,用以控制药物的缓释。采用静电干粉涂层技术制备胶囊包衣时发现,静电干粉涂层膜具有较高的延性、较低的强度、较低的致密性和缓释性能,并且提高了包衣的生产率、涂层均匀性和核心稳定性[28]。渗透作用能够控制药物的传递,能够在外部环境吸收液体到溶剂产生渗透压来调节渗透压,其中渗透泵给药装置是速率控制系统,由三部分组成:渗透剂、溶剂和药物,可以将药物以液体或固体形式有效集中储存,节省空间,能够在较长时间内持续地控制药物释放[29]。通过复乳溶剂蒸发的方式制备聚合物载体微球的方法获得了广泛认可和普遍运用;采用静电干粉涂层制备药物的包衣,能够控制药物的缓释;渗透泵给药装置通过渗透作用控制药物的释放,并且能够节省空间。 2.3 辛伐他汀生物材料支架系统的特点与制备方法 2.3.1 辛伐他汀生物材料支架系统的特点 在治疗骨缺损、促进骨再生中骨移植是常见的治疗方法,其中自体骨移植方法存在可获得的骨数量限制和骨吸收等问题。而理想促进骨形成的方法是采用人工合成的生物材料支架,包括磷酸钙(磷酸三钙、羟基磷灰石钙)、壳聚糖、硫酸钙等。研究者将包裹辛伐他汀的聚乳酸-羟基乙酸共聚物纳米颗粒装载在磷酸钙生物陶瓷支架中,发现生物陶瓷的力学性能得到了提高,并且具有骨诱导性和骨传导性,能联合辛伐他汀促进干细胞的体外成骨分化和体内骨诱导,但制备时需要较高的温度和热处理[30]。常用的生物材料支架是可降解β-磷酸三钙,其优点是生物相容性好、植入体内后能够直接与骨融合、无其他炎症性反应,在自然降解的过程中能释放出钙离子,为骨修复的愈合提供额外的补充,并且具有均匀的孔网络,能够负载更多的药物,但其具有高度敏感性,较高的刚性和脆性使其很难成型[31]。壳聚糖支架的生物相容性好且具有可塑性、低毒性和抗菌活性,具有显著的骨诱导性,与载辛伐他汀纳米颗粒结合促进了新骨的形成,并且其价格低廉、容易制备,但其机械性能差、不溶于水,并且在体内降解时间难以精准控制[32]。磷酸钙骨水泥是由一种或多种磷酸钙粉末组成与水相混合后的糊状物,具有良好的抗压强度和抗拉强度。在将辛伐他汀装载在磷酸钙骨水泥中缓释时,发现磷酸钙骨水泥在体内吸收快,其水化反应后得到羟基磷灰石等与人体骨组织相近的产物,具有良好的生物相容性,并与辛伐他汀一起促进了骨的新生。在骨水泥凝固过程中pH值会降低,但并不影响辛伐他汀的生物活性。在磷酸钙骨水泥水化反应中会出现放热反应,需要控制放热的时间及最高温度[33]。研究将辛伐他汀装载在磷酸钙骨水泥支架材料上,将大鼠骨髓基质干细胞接种在支架上观察,结果发现促进了干细胞的成骨分化,将其应用到大鼠骨缺损部位后促进了骨缺损内的新骨生成[34]。ZHANG 等[35]制备了装载辛伐他汀的聚乳酸-羟基乙酸共聚物微球磷酸钙复合支架,并将其应用于兔股骨中,结果发现改善了骨内血液循环,促进了坏死骨的修复,促进了新骨形成,并且将聚乳酸-羟基乙酸共聚物微球与磷酸钙支架混合提高了核心减压的效果,减少了骨坏死进程。由此可见,磷酸钙生物陶瓷支架具有良好的性能,但制备工艺复杂、要求严格。β-磷酸三钙材料可降解,具有良好的生物相容性,但其具有较高的刚性和脆性。壳聚糖支架具有良好的生物相容性、可塑性、低毒性和抗菌活性,但其机械性能差、不溶于水,并且在体内降解时间难精准控制。磷酸钙骨水泥具有高的抗压性和抗拉性,但在其凝固过程中pH值会降低,也会出现放热反应。 2.3.2 辛伐他汀生物支架材料系统的制备方法 为了改善生物支架材料的性能,需要找到合适的制备方法。磷酸钙骨水泥常用的制备方法是沉淀法和骨相反应法。研究发现,无机矿物与有机聚合物之间没有强的相互作用导致结合很复杂,为了促进结合,在制备出的磷酸钙支架表面上沉积矿物,发现通过钙离子的引入和交替矿化能够制备出具有良好附着性的磷酸钙复合支架,并且增强了聚合物支架的力学性能,提高了聚合物支架的细胞附着力[36]。采用阴离子表面活性剂十二烷基硫酸钠作为引气剂加入液相中,增加了磷酸钙骨水泥的大孔隙率,磷酸钙骨水泥的宏观孔隙度随着十二烷基硫酸钠浓度的升高而增加;在将其应用到新西兰家兔的踝骨后,发现增强了大孔磷酸钙骨水泥的成骨潜能,并且未见炎症反应[37]。由于人工骨植入材料磷酸钙骨水泥在生物活性和促进骨再生的治疗效果上满意度有限,有研究将锶加入到磷酸钙骨水泥中,锶是一种寻骨元素,能通过提高钙敏感受器的依赖机制,上调内源性骨形态发生蛋白2的表达,促进成骨细胞分化,促进骨缺损的愈合[38]。采用冷冻干燥法制备壳聚糖支架并掺入蒙脱土来改善其性能,由于蒙脱土具有阻隔性能够掩盖支架的亲水效应,阻碍溶剂基质的相互作用,降低支架的降解速率,当蒙脱土的浓度增加时支架的降解率会显著增加;并且蒙脱土带负电荷,在掺入壳聚糖后能够改变材料表面的静电荷,从而促进磷灰石晶体的沉积[39]。在研究壳聚糖多孔支架的性质时,采用不同浓度的壳聚糖溶液进行控制冷冻和冻干,制备多孔壳聚糖,发现随着壳聚糖浓度的增加,孔隙率有降低的趋势;支架的拉伸性能与壳聚糖浓度也有关,壳聚糖的浓度越高支架的极限拉伸强度越高。在体外释放实验表明,壳聚糖溶液浓度越高药物释放的时间越长[40]。各生物支架材料系统的优缺点,见图3。"
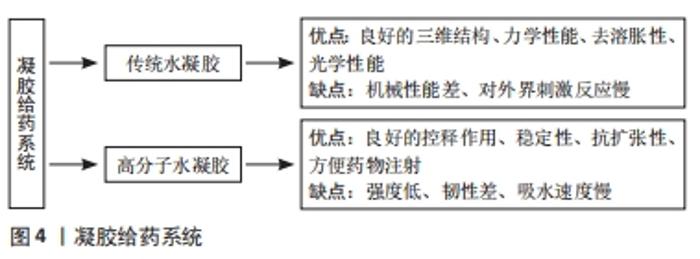
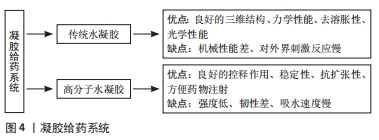
2.4 辛伐他汀凝胶给药系统的特点、制备方法及治疗牙周炎的效果 2.4.1 辛伐他汀凝胶给药系统的特点 水凝胶是一种水膨胀的高分子材料,分为传统水凝胶和敏感性的高分子水凝胶(温度敏感性、光敏感性、pH值敏感性水凝胶)。水凝胶具有独特的三维结构、优越的力学性能、去溶胀性和良好的光学性能,能够用来作为亲水的小分子的载体,但是传统水凝胶的机械性能差、对外界刺激的反应时间慢或延迟[41]。在研究纳米级可注射水凝胶作为生长因子输送材料时发现,可注射水凝胶系统可作为细胞再生的支持,具有良好的控释作用、稳定性、抗扩张性和生物相容性,水凝胶可以很容易地装载辛伐他汀并能在需要的地方控制药物释放,并且它的可注射性能够节省将植入物植入体内的过程,但是水凝胶的强度低、韧性差、吸水速度慢[42-43]。THORPE等[44]制成可注射性的骨形成水凝胶并皮下注射到大鼠股骨缺损模型,4周后评价其增强骨修复的效果,发现大鼠无炎症反应、器官毒性或全身毒性,具有良好的生物相容性,注射水凝胶后促进了骨的形成、促进细胞迁移、促进了与周围骨的融合。以上学者们的研究说明水凝胶的三维结构好、稳定性好,具有良好的抗扩张性、生物相容性,具有适当的孔隙和密度能够调节生物活性因子的释放,是微球理想的载体;具有流动性,能够更好地贴合不规则的骨缺损位置,使骨再生达到更好的效果。但是高分子水凝胶的强度低、韧性差、吸水速度慢。各凝胶给药系统的优缺点,见图4。"

2.4.2 辛伐他汀凝胶给药系统的制备方法及治疗牙周炎的效果 目前主要采用接枝共聚和化学交联方法制备水凝胶,制备出的水凝胶具有理想的性能和可调性能。采用壳聚糖、甘油磷酸酯等制备水凝胶时,甘油磷酸酯含量的增加会导致水溶解溶胀程度显著降低,并且壳聚糖和甘油磷酸酯的比例越大水凝胶的孔径增大,凝胶的成胶速度越快[45]。pH值会对水凝胶的物理化学性能造成影响,pH值可以有效调节水凝胶的凝胶化时间,而不会影响形成水凝胶的弹性,当pH值低至3.0时,水凝胶能在几分钟内有效凝胶化,在生理pH值下凝胶的动力学非常快[46]。以壳聚糖为基础的水凝胶具有黏性、低毒性和生物降解性等的特性,并能按照需要制备出温度敏感型水凝胶,使液态的水凝胶进入缺损部位后能够胶化,为细胞提供生长空间,支持细胞的生长增殖[47]。学者们制备出装载辛伐他汀的水凝胶,凝胶药物含量在89%-92%之间,pH值在6.5-7.0之间。体外释放实验表明,辛伐他汀从原位凝胶中释放较慢,早期具有爆发效应。将凝胶用于大鼠牙槽骨缺损及创面上发现,载辛伐他汀的原位凝胶能有效促进骨再生,促进大鼠创面愈合,减少炎性细胞数量[48]。LI等[49]研究发现,可注射辛伐他汀微球水凝胶可在5周后促进大鼠拔牙窝新骨生成,在骨修复和再生方面有很大的潜力,并且其可注射性极大方便了临床操作。有研究选择牙周炎患者作为试验对象,运用1.2%辛伐他汀凝胶辅助龈上洁治和龈下刮治,治疗3个月后检测发现菌斑指数、牙龈指数、探诊深度、附着丧失均显著下降,并且牙龈链球菌DNA拷贝数下降[50]。采用接枝共聚和化学交联方法制备的水凝胶具有良好的性能,pH值、共聚物的比例等会对凝胶产生影响,能根据需求调节条件制备出具有不同性能的水凝胶,并且通过细胞和动物实验证明水凝胶具有良好的生物相容性及促进骨再生治疗牙周炎的效果。需要更多的研究并找到更好的制备方法,并统一制备过程中的众多因素来制备出具有稳定性质的水凝胶。"

| [1] MUNDY G, GARRETT R, HARRIS S, et al. Stimulation of bone formation in vitro and in rodents by statins. Science. 1999;286(5446):1946-1949. [2] FENG C, XIAO L, YU JC, et al. Simvastatin promotes osteogenic differentiation of mesenchymal stem cells in rat model of osteoporosis through BMP-2/Smads signaling pathway. Eur Rev Med Pharmacol Sci. 2020;24(1):434-443. [3] SHAO PL, WU SC, LIN ZY, et al. Alpha-5 Integrin Mediates Simvastatin-Induced Osteogenesis of Bone Marrow Mesenchymal Stem Cells. Int J Mol Sci. 2019;20(3):506. [4] XU R, SHI G, XU L, et al. Simvastatin improves oral implant osseointegration via enhanced autophagy and osteogenesis of BMSCs and inhibited osteoclast activity. J Tissue Eng Regen Med. 2018;12(5): 1209-1219. [5] YU D, ZHAO D, YANG D, et al. Simvastatin promotes murine osteoclasts apoptosis in vitro through NFATc1 pathway. Nan Fang Yi Ke Da Xue Xue Bao. 2019;39(6):672-678. [6] SUTHANTHIRAN T, ANNAMALAI S, CHELLAPANDI S, et al. Gingival Crevicular Fluid Levels of RANKL and OPG After Placement of Collagen Membrane With Simvastatin in the Treatment of Intrabony Defects in Chronic Periodontitis. J Pharm Bioallied Sci. 2019;11(Suppl 2): S301-S304. [7] SHAHEEN MY, BASUDAN AM, NIAZY AA, et al. Impact of single or combined drug therapy on bone regeneration in healthy and osteoporotic rats. Tissue Eng Part A. 2020. doi: 10.1089/ten.TEA.2020.0122. [8] OZEÇ I, KILIÇ E, GÜMÜŞ C, et al. Effect of local simvastatin application on mandibular defects. J Craniofac Surg. 2007;18(3):546-550. [9] KAMIŃSKA M, ALIKO A, HELLVARD A, et al. Effects of statins on multispecies oral biofilm identify simvastatin as a drug candidate targeting Porphyromonas gingivalis. J Periodontol. 2019;90(6):637-646. [10] GROVER HS, KAPOOR S, SINGH A. Effect of topical simvastatin (1.2 mg) on gingival crevicular fluid interleukin-6, interleukin-8 and interleukin-10 levels in chronic periodontitis - A clinicobiochemical study. J Oral Biol Craniofac Res. 2016;6(2):85-92. [11] BAHAMMAM MA, ATTIA MS. Effects of Systemic Simvastatin on the Concentrations of Visfatin, Tumor Necrosis Factor-α, and Interleukin-6 in Gingival Crevicular Fluid in Patients with Type 2 Diabetes and Chronic Periodontitis. J Immunol Res. 2018;2018:8481735. [12] POSTON CJ, PIERCE TC, LI Y, et al. Statin intake is associated with MMP-1 level in gingival crevicular fluid of patients with periodontitis. Oral Dis. 2016;22(5):438-444. [13] NANTAVISAI S, RODPRASERT W, PATHANACHAI K, et al. Corrigendum to “Simvastatin enhances proliferation and pluripotent gene expression by canine bone marrow-derived mesenchymal stem cells (cBM-MSCs) in vitro” [Heliyon 5, (10), (October 2019), e02663]. Heliyon. 2019;5(11): e02805. [14] ANAND K, SKETRIS I, ZHANG Y, et al. The Impact of US FDA and Health Canada Warnings Related to the Safety of High-dose Simvastatin. Drugs Real World Outcomes. 2017;4(4):215-223. [15] CHEN PY, SUN JS, TSUANG YH, et al. Simvastatin promotes osteoblast viability and differentiation via Ras/Smad/Erk/BMP-2 signaling pathway. Nutr Res. 2010;30(3):191-199. [16] XU R, SHI G, XU L, et al. Simvastatin improves oral implant osseointegration via enhanced autophagy and osteogenesis of BMSCs and inhibited osteoclast activity. J Tissue Eng Regen Med. 2018;12(5): 1209-1219. [17] DEREN ME, EHTESHAMI JR, DINES JS, et al. Simvastatin Exposure and Rotator Cuff Repair in a Rat Model. Orthopedics. 2017;40(2):e288-e292. [18] HAMISHEHKAR H, EMAMI J, NAJAFABADI AR, et al. The effect of formulation variables on the characteristics of insulin-loaded poly(lactic-co-glycolic acid) microspheres prepared by a single phase oil in oil solvent evaporation method. Colloids Surf B Biointerfaces. 2009;74(1):340-349. [19] LIU J, XU Y, WANG Y, et al. Effect of inner pH on peptide acylation within PLGA microspheres. Eur J Pharm Sci. 2019;134:69-80. [20] XIONG Y, YU Z, LANG Y, et al. In vitro stress effect on degradation and drug release behaviors of basic fibroblast growth factor--poly(lactic-co-glycolic-acid) microsphere. Drug Des Devel Ther. 2016;10:431-440. [21] 李祥伟,张颖丽,林权,等.载辛伐他汀微球缓释软膏促进牙槽骨缺损修复的研究[J].北京口腔医学,2012,20(6):314-317. [22] ZHU K, ZHAO F, YANG Y, et al. Effects of simvastatin-loaded PLGA microspheres on treatment of rats with intervertebral disk degeneration and on 6-K-PGF1α and HIF-1α. Exp Ther Med. 2020; 19(1):579-584. [23] CHEN L, YANG G, CHU X, et al. Polymer Distribution and Mechanism Conversion in Multiple Media of Phase-Separated Controlled-Release Film-Coating. Pharmaceutics. 2019;11(2):80. [24] KOVÁČIK A, KOPEČNÁ M, VÁVROVÁ K. Permeation enhancers in transdermal drug delivery: benefits and limitations. Expert Opin Drug Deliv. 2020;17(2):145-155. [25] OGAWA Y, YAMAMOTO M, OKADA H, et al. A new technique to efficiently entrap leuprolide acetate into microcapsules of polylactic acid or copoly(lactic/glycolic) acid. Chem Pharm Bull (Tokyo). 1988; 36(3):1095-1103. [26] MASAELI R, JAFARZADEH KASHI TS, DINARVAND R, et al. Preparation, Characterization and Evaluation of Drug Release Properties of Simvastatin-loaded PLGA Microspheres. Iran J Pharm Res. 2016; 15(Suppl):205-211. [27] WANG X, QI F, XING H, et al. Uniform-sized insulin-loaded PLGA microspheres for improved early-stage peri-implant bone regeneration. Drug Deliv. 2019;26(1):1178-1190. [28] YANG Y, SHEN L, YUAN F, et al. Preparation of sustained release capsules by electrostatic dry powder coating, using traditional dip coating as reference. Int J Pharm. 2018;543(1-2):345-351. [29] HERRLICH S, SPIETH S, MESSNER S, et al. Osmotic micropumps for drug delivery. Adv Drug Deliv Rev. 2012;64(14):1617-1627. [30] WANG CZ, WANG YH, LIN CW, et al. Combination of a Bioceramic Scaffold and Simvastatin Nanoparticles as a Synthetic Alternative to Autologous Bone Grafting. Int J Mol Sci. 2018;19(12):4099. [31] CHOU J, ITO T, BISHOP D, et al. Controlled release of simvastatin from biomimetic β-TCP drug delivery system. PLoS One. 2013;8(1):e54676. [32] XUE Y, WU M, LIU Z, et al. In vitro and in vivo evaluation of chitosan scaffolds combined with simvastatin-loaded nanoparticles for guided bone regeneration. J Mater Sci Mater Med. 2019;30(4):47. [33] Montazerolghaem M, Engqvist H, Karlsson Ott M. Sustained release of simvastatin from premixed injectable calcium phosphate cement. J Biomed Mater Res A. 2014;102(2):340-347. [34] 于祥茹,韩晓谦,程梁,等.载辛伐他汀PLGA/CPC支架材料复合BMSCs修复大鼠颅骨缺损的实验研究[J].口腔医学研究,2015, 31(10):1032-1036. [35] ZHANG HX, ZHANG XP, XIAO GY, et al. In vitro and in vivo evaluation of calcium phosphate composite scaffolds containing BMP-VEGF loaded PLGA microspheres for the treatment of avascular necrosis of the femoral head. Mater Sci Eng C Mater Biol Appl. 2016;60:298-307. [36] KANG Z, ZHANG X, CHEN Y, et al. Preparation of polymer/calcium phosphate porous composite as bone tissue scaffolds. Mater Sci Eng C Mater Biol Appl. 2017;70(Pt 2):1125-1131. [37] YIN H, LI YG, SI M, et al. Simvastatin-loaded macroporous calcium phosphate cement: preparation, in vitro characterization, and evaluation of in vivo performance. J Biomed Mater Res A. 2012; 100(11):2991-3000. [38] TAO Z, ZHOU W, JIANG Y, et al. Effects of strontium-modified calcium phosphate cement combined with bone morphogenetic protein-2 on osteoporotic bone defects healing in rats. J Biomater Appl. 2018; 33(1):3-10. [39] MENG T, JIANG R, WANG S, et al. Corrigendum to “Stem Cell Membrane-Coated Au-Ag-PDA Nanoparticle-Guided Photothermal Acne Therapy”, Colloids and Surfaces B: Biointerfaces (2020) 192C/COLSUB_111145]. Colloids Surf B Biointerfaces. 2020;196:111314. [40] IKEDA T, IKEDA K, YAMAMOTO K, et al. Fabrication and characteristics of chitosan sponge as a tissue engineering scaffold. Biomed Res Int. 2014;2014:786892. [41] KOPECEK J. Hydrogel biomaterials: a smart future? Biomaterials. 2007;28(34):5185-5192. [42] DYONDI D, WEBSTER TJ, BANERJEE R. A nanoparticulate injectable hydrogel as a tissue engineering scaffold for multiple growth factor delivery for bone regeneration. Int J Nanomedicine. 2013;8:47-59. [43] REY-RICO A, MADRY H, CUCCHIARINI M. Hydrogel-Based Controlled Delivery Systems for Articular Cartilage Repair. Biomed Res Int. 2016; 2016:1215263. [44] THORPE AA, FREEMAN C, FARTHING P, et al. In vivo safety and efficacy testing of a thermally triggered injectable hydrogel scaffold for bone regeneration and augmentation in a rat model. Oncotarget. 2018;9(26):18277-18295. [45] TALAAT WM, HAIDER M, AL KAWAS S, et al. Chitosan-Based Thermosensitive Hydrogel for Controlled Drug Delivery to the Temporomandibular Joint. J Craniofac Surg. 2016;27(3):735-740. [46] SCHWEIKLE M, ZINN T, LUND R, et al. Injectable synthetic hydrogel for bone regeneration: Physicochemical characterisation of a high and a low pH gelling system. Mater Sci Eng C Mater Biol Appl. 2018;90:67-76. [47] BHATTARAI N, GUNN J, ZHANG M. Chitosan-based hydrogels for controlled, localized drug delivery. Adv Drug Deliv Rev. 2010;62(1): 83-99. [48] RUAN H, YU Y, GUO X, et al. The possibility of healing alveolar bone defects with simvastatin thermosensitive gel: in vitro/in vivo evaluation. Drug Des Devel Ther. 2018;12:1997-2003. [49] LI X, LIU X, NI S, et al. Enhanced osteogenic healing process of rat tooth sockets using a novel simvastatin-loaded injectable microsphere-hydrogel system. J Craniomaxillofac Surg. 2019;47(7):1147-1154. [50] RAHMAN S, GV G, MEHTA DS. A clinico-microbiological and biochemical study evaluating the adjunctive use of antimicrobial photodynamic therapy and local drug delivery of 1.2 % simvastatin gel compared to scaling and root planing alone. Photodiagnosis Photodyn Ther. 2020;32:102017. |
| [1] | Yao Xiaoling, Peng Jiancheng, Xu Yuerong, Yang Zhidong, Zhang Shuncong. Variable-angle zero-notch anterior interbody fusion system in the treatment of cervical spondylotic myelopathy: 30-month follow-up [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1377-1382. |
| [2] | Kang Kunlong, Wang Xintao. Research hotspot of biological scaffold materials promoting osteogenic differentiation of bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 597-603. |
| [3] | Li Hui, Chen Lianglong. Application and characteristics of bone graft materials in the treatment of spinal tuberculosis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 626-630. |
| [4] | He Yunying, Li Lingjie, Zhang Shuqi, Li Yuzhou, Yang Sheng, Ji Ping. Method of constructing cell spheroids based on agarose and polyacrylic molds [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 553-559. |
| [5] | Wang Jiajia, Liu Jie, Wang Min. Establishing a murine model of experimental apical periodontitis induced by Fusobacterium nucleatum [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(2): 176-181. |
| [6] | Fan Danyang, Fu Runze, Mi Jiajing, Liu Chunyan. Expression and role of cannabinoid receptors during bone remodeling [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(2): 283-288. |
| [7] | Fu Zheng, Li Runze, Luo Haotian, Chen Jun, Wang Weicai. Application of self-healing hydrogels in bone tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(16): 2590-2595. |
| [8] | Xu Yinghua, Jiang Long, Shi Chun. Changes in the expression of bromodomain-containing protein 4, an epigenetic molecule, in a rat model of chronic periapical periodontitis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(14): 2167-2171. |
| [9] | Liu Jie, Wang Min. Changes in programmed necrosis pathway in the occurrence and development of periapical periodontitis in a mouse model [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(14): 2179-2183. |
| [10] | Zhao Yuexin, Chen Bin. Progress of macrophage polarization in immunology of bone tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(13): 2120-2126. |
| [11] | Tan Xianyu, Liao Wenbo. Cell sheet technology applied in bone tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(12): 1944-1949. |
| [12] | Jing Jin, Zhao Shandi, Chen Long, Peng Shuanglin, Tang Hui, Guo Daijin, Zeng Xinyi, Xiao Jingang. Repair of calvarial defects in osteoporotic mice by adipose-derived stem cells combined with biphasic calcium phosphate ceramic scaffold [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(1): 90-95. |
| [13] | Zhang Mi, Wu Saixuan, Dong Ming, Lu Ying, Niu Weidong. Expression of interleukin-24 in a mouse model of periapical periodontitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 679-684. |
| [14] | Wu Zijian, Hu Zhaoduan, Xie Youqiong, Wang Feng, Li Jia, Li Bocun, Cai Guowei, Peng Rui. Three-dimensional printing technology and bone tissue engineering research: literature metrology and visual analysis of research hotspots [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 564-569. |
| [15] | Li Xiaozhuang, Duan Hao, Wang Weizhou, Tang Zhihong, Wang Yanghao, He Fei. Application of bone tissue engineering materials in the treatment of bone defect diseases in vivo [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 626-631. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||