Chinese Journal of Tissue Engineering Research ›› 2021, Vol. 25 ›› Issue (29): 4703-4708.doi: 10.12307/2021.172
Previous Articles Next Articles
Tissue engineering technology for treating bone defects: how far is it from bench to bed?
Qin Yuxing1, Ren Qiangui2, Shen Peifeng2, Wang Haoyu1
- 1Inner Mongolia Medical University, Hohhot 010000, Inner Mongolia Autonomous Region, China; 2The Second Affiliated Hospital of Inner Mongolia Medical University, Hohhot 010030, Inner Mongolia Autonomous Region, China
-
Received:2020-10-19Revised:2020-10-22Accepted:2020-11-11Online:2021-10-18Published:2021-07-22 -
Contact:Ren Qiangui, Master, Chief physician, The Second Affiliated Hospital of Inner Mongolia Medical University, Hohhot 010030, Inner Mongolia Autonomous Region, China -
About author:Qin Yuxing, Master candidate, physician, Inner Mongolia Medical University, Hohhot 010000, Inner Mongolia Autonomous Region, China
CLC Number:
Cite this article
Qin Yuxing, Ren Qiangui, Shen Peifeng, Wang Haoyu. Tissue engineering technology for treating bone defects: how far is it from bench to bed?[J]. Chinese Journal of Tissue Engineering Research, 2021, 25(29): 4703-4708.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
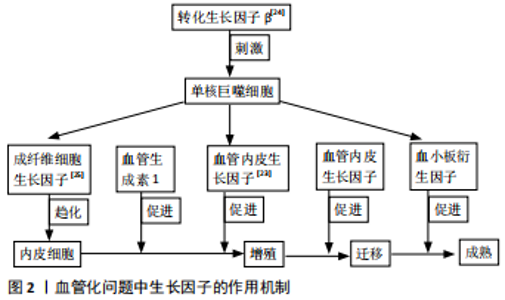
2.1 种子细胞的研究进展 骨组织工程的第一核心要素便是种子细胞,在选择理想种子时必须满足这些条件:①成骨作用;②取材容易;③体外可大量扩增;④对自身无害;⑤对骨骼周围组织及新生血管有一定的刺激作用。成骨细胞是骨形成的主要功能细胞,对骨基质的合成和矿化起着决定性的作用,其是最早应用于组织工程骨技术的种子细胞。耿海霞等[3]采用组织工程骨技术治疗兔颅骨缺损,从组织学和影像学方面证实了成骨细胞的成骨能力。成骨细胞使得Ⅰ型胶原大量分泌,促进成骨,然而成骨细胞的来源较少,只有部分松质骨可以获取,且成骨细胞的获取会对自身造成损伤及体外不易培养是其主要缺陷,所以未能广泛应用于临床。之后致力于组织工程技术研究的学者们把目光聚焦在成骨细胞的前体细胞,即骨髓间充质干细胞,骨髓间充质干细胞分化能力极强,在人体骨髓中其含量较为丰富,有研究证实体外大量培养和保存对其分化能力无影响,取材方面通过骨穿便可得到,因而被当作最有潜力的种子细胞,且近年来运用骨髓间充质干细胞作为种子细胞最为广泛。但最新研究发现,传代次数过多骨髓间充质干细胞增殖能力减弱[4]。随后的研究重点是胚胎干细胞,其有着增殖不受限制的优势和较强的骨化能力,但由于来源有限、难以获得,以及存在伦理问题,所以很快被否决了。近年来随着基因工程的不断进步,为种子工程带来了福音。KFOURY等[5]采用异体种子细胞解决了自身损伤的问题以及增殖问题,而后用基因工程技术修饰种子细胞,阻断机体识别信号或使T细胞无法识别从而产生免疫耐受,做到异体移植。但目前基因工程还处于发展阶段,不是很完善,有致瘤性可能,而且存在很多不可预知的危险。脂肪干细胞也具有成骨作用,在组织工程骨技术中同样有着广阔的前景,其在体内的浓度比骨髓间充质干细胞高100-300倍,且在诱导条件下可分泌与成骨、成血管相关的细胞因子,诸如血管内皮生长因子、基质细胞衍生因子等 [6-7];脂肪干细胞增殖能力也强于骨髓间充质干细胞,并在血运方面也有着一定的优势,但有研究证实成熟脂肪细胞对人成骨细胞的扩增有抑制作用,不是理想的种子细胞。 2.2 支架材料的研究进展 支架材料为种子载体和活性因子提供稳定的生长环境,充当种子细胞生长代谢的场所,使种子细胞按着预定的结构形态生长,血管可以在支架材料适宜的孔隙下生长,为种子细胞提供营养以及运输代谢产物。然而理想的支架材料还需要具备良好的生物组织相容性、降解性、表面活性、骨传导性、骨诱导性、机械强度以及合适的孔隙率等[8]。根据支架材料在组织工程骨中的作用,首先应用于骨组织工程的便是占骨骼一半以上成分的羟基磷灰石,其作为支架材料有着良好的生物相容性,目前使用的支架材料大部分都是基于羟基磷灰石发展演变而来的,但单一的使用羟基磷灰石存在着力学性能差、韧性不足等缺陷[9],不是理想的支架材料。随着骨组织工程技术的不断改进,广大学者先后对易被降解的聚乳酸、机械性能良好且在体内可无毒降解的聚已内酯以及可塑性良好的聚羟基乙酸等进行了研究。尽管这些支架材料在一些方面有着绝对的优势但在其他方面也存在一些不足,如聚乳酸降解时会导致机体出现炎症,聚已内酯存在降解缓慢的问题,而聚羟基乙酸则降解过快,所以目前仍未找到一种理想的支架材料。纳米技术的发展为支架材料带来了新的曙光,纳米材料以其独特的优势在支架材料方面占据着不可撼动的地位。纳米材料是指材料的尺寸处于纳米尺度(100 nm)之内的材料[10],其无论生物相容性或机械强度以及生物可控降解性都优于以上传统支架材料[11]。有研究通过对比纳米磷灰石与普通磷灰石的性质,得出纳米磷灰石的生物活性、吸附能力以及机械强度都优于普通磷灰石。纳米支架材料除了以上理化性质优于普通支架材料,还具备两种普通支架材料不可比拟的独特优势:①当异物植入会对机体造成炎症反应,而纳米支架材料的优势便是可以负载药物,通过逐步释放药剂量而解决支架带来的一些问题。夏德萌等[12]在纳米结构羟基磷灰石负载万古霉素治疗大鼠股骨慢性骨髓炎的实验中证实,其可负载药物有抗菌能力,并指出其有一定的成骨作用。②异物植入与原组织的相容性最为关键,纳米支架材料便可解决此问题,通过表面修饰来调节材料对细胞生物学行为的影响力。BAI等[13]在纳米支架材料表面修饰实验中指出,表面修饰后能够促进骨细胞和内皮细胞的增殖和分化,而且还可抑制巨噬细胞的炎症反应,并能够进行有利的骨免疫调节,从而促进骨/血管生成。然而纳米材料未广泛进入临床应用,或许遇到了一些瓶颈问题,即如何优化纳米材料的构造、质量、生物性质、材料细胞/界面及其安全评估将会是越来越紧迫的问题。 单一支架材料各有优点,但一种材料仍然难以满足骨骼作为支架的所有要求。复合材料以物理、化学或改性的方式来提高其力学和生物学特性,是目前应用最广泛的也是效果最好的,通过取长补短、修饰不足、增强优势、提高性能来得到一种近乎理想的支架材料,为组织工程骨技术带来了福音。LI等[14]在聚乳酸羟基乙酸共聚物/明胶/纳米羟基磷灰石复合支架治疗骨缺损的生物相容性研究中证实,该复合支架能够更好地支持成骨细胞的黏附、扩散和增殖,与单一聚乳酸羟基乙酸共聚物支架相比,该复合支架的细胞相容性和骨诱导活性更好。两种及以上的材料符合目前组织工程骨技术支架材料选择的主流趋势,并在不断地进步及完善。最新报道指出胶原–羟基磷灰石与微纤化纤维素复合所得的一种新型骨替代材料,与纯羟基磷灰石相比,该复合支架抗压强度提高了20-40 MPa[15]。随着国内中医药事业的发展,复合材料可以负载一定剂量的中药成分,而中药具有持久的缓释功能,能够很好地促进骨折愈合,为支架材料的发展提供了一个新思路,其中淫羊藿苷、骨碎补、丹参等都是支架材料常负载的中药,并取得了一定的成果。FAN等[16]在羟基磷灰石/壳聚糖复合支架中是否加入淫羊藿苷的研究中证实,淫羊藿苷的持久缓释能力对骨愈合有着明显效果,尽管在复合支架中加入了淫羊藿苷,但并不影响其力学强度及孔隙率问题。梁卫寰等[17]在羟基磷灰石/壳聚糖-柚皮苷缓释材料的制备及性能初探中得出,在加入柚皮苷后可以提高支架的力学强度,且证实其原理是柚皮苷中的羟基磷灰石/壳聚糖形成氢键。 2.3 细胞因子研究进展 新骨的形成是一个动态过程,是由一种或一类细胞在各种细胞因子的复杂调控下形成的,尽管有关成骨的全部信号通路尚未明确,但广大学者已经掌握了大部分与成骨相关的细胞因子,并了解了其作用机制,证实其效果。所以对于细胞因子的研究是组织工程骨技术的第三大核心要素,在组织工程技术中添加各种细胞因子来促进成骨及解决血管化问题,从而提高组织工程技术对于骨缺损的治愈率是现在的主要研究方向之一。骨形态发生蛋白是最早发现的具有诱导成骨能力的细胞因子,其在体内外均可诱导干细胞成骨。作者所在课题组在体外骨髓间充质干细胞的成骨能力的探究中证实,在支架材料中加入球囊包裹的骨形态发生蛋白2和血管内皮生长因子可以增加骨髓间充质干细胞成骨分化能力,以及早期血管形成能力和数量,并指出骨形态发生蛋白2可抑制骨髓间充质干细胞的成脂能力。转化生长因子β可以说是骨形态发生蛋白的增效剂,其可增加骨形态发生蛋白的骨化能力,且其本身便可促进受损部位细胞聚集,刺激成骨细胞增殖及胶原合成。对于转化生长因子β对骨骼的作用证实,转化生长因子β可减缓骨骼吸收过程,主要是抑制破骨细胞的合成,且其可增加成骨相关胶原的合成,以及刺激单核巨噬细胞分泌成骨相关因子。目前广大学者都在不断地对其他细胞因子如血小板衍生因子、成纤维细胞生长因子、血管内皮生长有因子、转化生长因子β和血管生成素1等进行探索研究,来模拟体内骨组织生长的微环境,旨在实现成骨的可控调节,从而解决骨缺损的问题。 2.4 血管化问题 在组织工程的研究中,能够将氧气和营养物质转移到细胞的功能性血管网络,对于结构在体内植入后的存活和最佳功能是最为关键的。目前组织工程技术没有进入临床的主要因素便是血运问题未彻底解决,随着广大学者对于组织工程技术应用于骨缺损方向的研究深入,证实组织工程骨技术的缺陷在于未能尽早为修补过程解决血运问题,而导致所植入支架多形成纤维囊性包裹,阻断血运,导致细胞增殖、分裂停滞,进而因缺血导致成骨坏死修复失败[4]。在这一难题,广大学者一直在不断努力着,最早采用血管束植入,当管束植入组织工程骨内部以后,可明显提高组织工程骨技术治疗骨缺损的成功率,并进一步促进新骨形成,但其由于操作难度大,所以不易于临床广泛推广。目前对于血管化问题的解决主要在选择种子细胞时采用多项技术结合,如细胞共培养、加入细胞生长因子和设计个性化支架结构等。 2.4.1 细胞共培养解决血管化问题 骨组织是一种高度血管化的组织,伴随着血管系统和矿化基质的发展,需要成骨细胞和血管母细胞的协同作用。内皮祖细胞是血管内皮细胞的前体细胞,该细胞在机体受到损伤或某些刺激时,它可通过血液循环动员到该处,形成新的血管[19]。因此,将骨髓间充质干细胞和内皮祖细胞复合培养,能更好地促进早期血管生成[20],既能有效促进组织工程骨血管化,又能促进成骨细胞的增殖活性,有助于增强组织工程骨修复骨缺损的能力。此外,内皮祖细胞可通过成人外周血和脐带血从组织工程治疗受体中无创分离,衍生自诱导的人多能干细胞,避免了免疫原性问题,徐荣胜[21]通过骨髓间充质干细胞和人脐静脉内皮细胞共培养构建组织工程骨来解决血管化问题,证实新生血管明显增加,并指出了人脐静脉内皮细胞可促进骨髓间充质干细胞向成骨分化,增加组织工程骨在机体的存活及成骨能力。对于骨髓间充质干细胞的选取是由于间充质干细胞可分化为血管壁细胞,从而稳定血管结构,但对于这一实验仍存在的问题便是如何优化构建策略,在成骨和成血管之间取得最佳的平衡点,亦需进一步的探讨。韦惠平[22]在大鼠骨髓间充质干细胞/内皮祖细胞联合培养与聚乳酸支架构建组织工程骨的实验研究中证实,内皮祖细胞在成骨方面有着促进作用;与单纯复合支架骨髓间充质干细胞相比,血管有着明显增多现象。 2.4.2 生长因子添加解决血管化问题 在生物材料内嵌入生长因子是促进血管化和新形成血管稳定的另一种策略。目前常用的生长因子主要包括血小板衍生因子、成纤维细胞生长因子、血管内皮生长因子、转化生长因子β和血管生成素1等[23-25],见图2。 最新报道张丽丽[26]采用浓缩生长因子对兔骨膜来源细胞增殖、成骨分化及成血管潜能的实验中指出,多种生长因子的浓缩物能够上调骨膜来源细胞的成血管相关因子及蛋白的表达,这一实验为组织工程领域早期快速血管化问题的解决提供了新思路。 对生长因子作用的大量研究表明,单一生长因子的使用不足以创造稳定的血管结构,因为许多生长因子是协同作用的。STONE等[27]的一项研究发现,仅靠内源性血管内皮生长因子A不能正确地诱导血管生成和动脉生成,因此在骨组织工程中多因子联合促血管化作用更值得被研究。HUANG等[28]在血管内皮生长因子和成纤维细胞生长因子2联合促进骨髓基质细胞驱动骨再生的研究中,对比单因子与联合因子对血管构建的作用,证实在促进新血管形成上双因子明显优于单因子。此外,作为第一代血小板浓缩物的富血小板血浆,含有多种高浓度的生长因子,刘双阳等[29]已经证实其可加快修复骨缺损,增加血管数量,缩短愈合时间,尤其能促进骨髓间充质干细胞增殖,但也指出单独应用富血小板血浆作用不明显。综上,多个生长因子联合作用的疗效已得到证实,但何种因子组合最佳还需要进一步探索[30]。 对于生长因子解决血管化问题目前还有一项研究热点便是如何保证生长因子稳定地发挥作用与可控释放,大多报道是采用生长因子与适宜的支架材料联合使用于特定的目标位置,如血管生成生长因子的包裹技术是一种有效的控制释放的方法。ROBERTS等[31]证实了肝素介导的血管内皮生长因子和碱性成纤维细胞生长因子从聚乙烯醇-肝素水凝胶中的负载和释放,与对照聚乙烯醇凝胶相比,突发性释放减少。控制和稳定的生长因子释放是理想的方式,过度释放可能对周围细胞产生有毒影响,导致血管功能失调,甚至产生肿瘤。如GOLUB等[32]应用聚乳酸-羟基乙酸纳米球囊包裹血管内皮生长因子进行持续给药,比单独直接注射组和空白对照组的成血管能力好,且对周围细胞无毒性影响。因此,缓慢而持久的生长因子输出不仅是安全的,而且有助于加速血管生成过程。 2.4.3 设计个性化支架材料解决血管化问题 支架结构可影响植入前后实现的血管化水平,特别是移植物的孔隙率是一个至关重要的参数,因为它决定了材料内部细胞的迁移,促进血管长入,且孔隙之间的连接对于毛细血管之间发生吻合和构建功能性血管网络至关重要。近年来通过使用计算机辅助设计个性化支架创造血管生长的空间结构是目前的研究热点。3D打印技术(快速成型技术)是使用计算机辅助设计法设计出合适的模型,然后由快速成型机一层一层的打印出3D实体[33]。由于其可以精准控制材料的内部结构,所以已有研究将3D打印技术与骨组织工程技术结合,针对特殊部位的骨缺损进行修复并取得较好效果[34]。目前所提出的骨支架微孔联通结构的设计理念被广泛接受,即通过计算机辅助设计为支架材料设计合适的孔隙,且孔隙之间相互连通,并不影响其机械强度及传导性,已有实验证实采用微孔联通理念用计算机辅助设计法设计出合适的支架材料对于早期血管长入及支架降解都有着极大的帮助[18]。3D打印最大的优势便是控制细胞微观的排列分布,调整组织工程支架的形状、大小、孔径、孔隙率、连通性以及材料内部的比表面积[35],通过比对分析从而制出最优的支架材料。FERLIN等[36]研究发现,采用3D打印技术制备的具有有序立方孔的支架比有序圆柱孔的支架更有利于骨髓间充质干细胞的富集和分化,以及新生血管的增加。 "
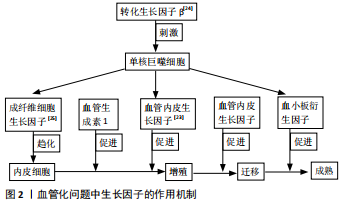
| [1] 秦宇星,任前贵,沈佩锋.组织工程骨技术治疗骨缺损的优越性[J].中国组织工程研究,2020,24(24):3877-3882. [2] 刘杰,吴雪晖,罗飞,等.自体间充质干细胞构建组织工程骨修复人长骨缺损的临床观察[J].第三军医大学学报,2008,30(9):851-854. [3] 耿海霞,封伟,钱君荣,等.羟基磷灰石-凝胶支架复合成骨细胞修复兔颅骨缺损的组织学评价[J].临床口腔医学杂志,2014,30(9): 519-521 [4] LI X, PENG B, PAN Y, et al. Icariin stimulates osteogenicdifferentiation and suppresses adipogenic differentiation ofrBMSCs via estrogen receptor signaling. Mol Med Rep. 2018;18(3):3483-3489. [5] KFOURY Y , SCADDEN DT. Mesenchymal cell contributions to the stem cell niche. Cell Stem Cell. 2015;16(3):239-253. [6] MOON KM, PARK YH, LEE JS, et al. The effect of secretory factors of adipose-derived stem cells on human keratinocytes. Int J Mol Sci. 2012; 13(1):1239-1257. [7] SIEGEL KR, CLEVENGER TN, CLEGG DO, et al. Adipose Stem Cells Incorporated in Fibrin Clot Modulate Expression of Growth Factors.Arthroscopy. 2018;34(2):581-591. [8] BANFI A, MURAGLIA A, DOZIN B, et al.Proliferation kinetics and differentiation potential of ex vivo expanded human bone marrow stromal cells:Implications for their use in cell therapy. Exp Hematol. 2001;28(6):707-715. [9] 唐文胜,蒋电明.羟基磷灰石及其复合材料在骨修复中的作用及研究进展[J].中华创伤骨科杂志,2003,5(4):370-373. [10] Wahajuddin,Arora S. Superparamagnetic iron oxide nanoparticles: magneticnanoplatforms as drug carriers. Int J Nanomedicine. 2012;7: 3445-3471. [11] 周静,冯卓卓,罗洁,等.纳米支架材料在骨组织工程应用中的优势[J].临床口腔医学杂志,2018,34(10):633-635. [12] 夏德萌,冯拥璞,夏琰,等.纳米结构羟基磷灰石负载万古霉素对大鼠股骨慢性骨髓炎的治疗作用[J].中国骨与关节损伤杂志,2019, 34(9):936-940. [13] BAI L, DU Z, DU J,et al. A multifaceted coating on titanium dictates osteoimmunomodulation and osteo/angio-genesis towards ameliorative osseointegration. Biomaterials. 2018;162:154-169. [14] LI D, SUNH, JIANGL, et al. Enhanced biocompatibility of PLGAnanofibers with gelatin/nano-hydroxyapatite bone biomimetics incorporation.ACS Appl Mater Interfaces. 2014;6(12):9402-9410. [15] HE X, FAN X, FENG W, et al. Incorporation of microfibrillated cellulose into collagen-hydroxyapatite scaffold for bone tissue engineering. Int J Biol Macromol. 2018;115(6):385-392. [16] FAN J, BI L, WU T, et al. A combined chitosan/nano-size hydroxyapatite system for the controlled release of icariin. J Mater Sci Mater Med. 2012;23(2):399-407. [17] 梁卫寰,谭竹钧,区硕俊,等.羟基磷灰石/壳聚糖-柚皮苷缓释材料的制备及性能初探[J].功能材料,2015(19):19131-19135. [18] 丁焕文,涂强,王迎军,等.数字化骨科手术新方法的建立及其临床广泛应用[J].中国骨科临床与基础研究杂志,2010,2(2):92-97. [19] ASAHARA T, MUROHARA T, SULLIVAN A, et al. Isolation of putative progenitor endothelial cells for angiogenesis. Science. 1997;275(5302): 964-967. [20] 徐荣胜,何芸,李彪,等.血管内皮生长因子165转染脐静脉内皮细胞与骨髓间充质干细胞共培养在血管形成中的作用[J].中国组织工程研究,2017,21(33):5268-5273. [21] 徐荣胜.BMSCs和HUVECs复合HA-TCP支架共培养对大鼠颅骨缺损修复的成骨能力影响[D].泸州:西南医科大学,2018. [22] 韦惠平. 大鼠BMSCs/EPCs联合培养与聚乳酸支架构建组织工程骨的实验研究[D].南宁:广西医科大学,2011. [23] HARRIS GM, RUTLEDGE K, CHENG Q, et al. Strategies to Direct Angiogenesis within Scaffolds for Bone Tissue Engineering. Curr Pharm Des. 2013;19(19):3456-3465. [24] DONG QS, LIN C, SHANG HT, et al. Modified approach to construct a vascularized coral bone in rabbit using an arteriovenous loop. J Reconstr Microsurg.2010,26(2):95-102. [25] 陈凯,张超,王路,等.骨组织工程中促进血管化策略的研究进展[J].中国骨伤,2015,28(4):383-388. [26] 张丽丽. 浓缩生长因子对兔骨膜来源细胞增殖、成骨分化及成血管潜能的研究[D].沈阳:中国医科大学,2019. [27] STONE OA, CARTER JG, LIN PC, et al. Differential regulation of blood flow‐induced neovascularization and mural cell recruitment by vascular endothelial growth factor and angiopoietin signalling. J Physiol. 2017; 595(5):1575-1591. [28] HUANG YC, KAIGLER D, RICE KG, et al. Combined angiogenic and osteogenic factor delivery enhances bone marrow stromal cell-driven bone regeneration. J Bone Miner Res. 2005;20(5):848-857. [29] 刘双阳,田雅光,王洪一,等.富血小板血浆促进骨髓间充质干细胞对大鼠骨缺损的修复作用[J].中国美容整形外科杂志,2019,30(4): 210-213. [30] 任前贵,王瞾,张坤.仿生控释BMP-2和VEGF的PELA微球支架对骨髓间充质干细胞向成骨细胞分化的Wnt/β-catenin通路的影响[J].中国生物制品学杂志,2018,31(10):1118-1121+1125. [31] ROBERTS JJ, FARRUGIA BL, GREEN RA, et al. In situ formation of poly(vinyl alcohol)–heparin hydrogels for mild encapsulation and prolonged release of basic fibroblast growth factor and vascular endothelial growth factor. J Tissue Eng. 2016;7:153-170. [32] GOLUB JS, KIM YT, DUVALL CL, et al. Sustained VEGF delivery via PLGA nanoparticles promotes vascular growth. Am J Physiol Heart Circ Physiol. 2010;298(6):1959-1965. [33] 兰红波,李涤尘,卢秉恒.微纳尺度3D打印[J].中国科学:技术科学,2015,45(9):919-940. [34] 易灿. 计算机辅助临床大段骨缺损的精确修复[D].广州:广州中医药大学,2011:27-38. [35] 胡超然,邱冰. 3D生物打印技术在骨组织工程中的应用[J]. 中国组织工程研究,2018,22(2):316-322. [36] FERLIN KM, PRENDERGAST ME, MILLER ML, et al. Influence of 3D printed porous architecture on mesenchymal stem cell enrichment and differentiation. Acta Biomaterialia. 2016;32:161-169. (责任编辑:GD,ZN,DL) |
| [1] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [2] | Wu Xun, Meng Juanhong, Zhang Jianyun, Wang Liang. Concentrated growth factors in the repair of a full-thickness condylar cartilage defect in a rabbit [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1166-1171. |
| [3] | Zeng Yanhua, Hao Yanlei. In vitro culture and purification of Schwann cells: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1135-1141. |
| [4] | Hou Jingying, Yu Menglei, Guo Tianzhu, Long Huibao, Wu Hao. Hypoxia preconditioning promotes bone marrow mesenchymal stem cells survival and vascularization through the activation of HIF-1α/MALAT1/VEGFA pathway [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 985-990. |
| [5] | Li Cai, Zhao Ting, Tan Ge, Zheng Yulin, Zhang Ruonan, Wu Yan, Tang Junming. Platelet-derived growth factor-BB promotes proliferation, differentiation and migration of skeletal muscle myoblast [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1050-1055. |
| [6] | Luo Xuanxiang, Jing Li, Pan Bin, Feng Hu. Effect of mecobalamine combined with mouse nerve growth factor on nerve function recovery after cervical spondylotic myelopathy surgery [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 719-722. |
| [7] | Nie Huijuan, Huang Zhichun. The role of Hedgehog signaling pathway in transforming growth factor beta1-induced myofibroblast transdifferentiation [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 754-760. |
| [8] | Xu Dongzi, Zhang Ting, Ouyang Zhaolian. The global competitive situation of cardiac tissue engineering based on patent analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 807-812. |
| [9] | Wu Zijian, Hu Zhaoduan, Xie Youqiong, Wang Feng, Li Jia, Li Bocun, Cai Guowei, Peng Rui. Three-dimensional printing technology and bone tissue engineering research: literature metrology and visual analysis of research hotspots [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 564-569. |
| [10] | Chang Wenliao, Zhao Jie, Sun Xiaoliang, Wang Kun, Wu Guofeng, Zhou Jian, Li Shuxiang, Sun Han. Material selection, theoretical design and biomimetic function of artificial periosteum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 600-606. |
| [11] | Liu Fei, Cui Yutao, Liu He. Advantages and problems of local antibiotic delivery system in the treatment of osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 614-620. |
| [12] | Li Xiaozhuang, Duan Hao, Wang Weizhou, Tang Zhihong, Wang Yanghao, He Fei. Application of bone tissue engineering materials in the treatment of bone defect diseases in vivo [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 626-631. |
| [13] | Zhang Zhenkun, Li Zhe, Li Ya, Wang Yingying, Wang Yaping, Zhou Xinkui, Ma Shanshan, Guan Fangxia. Application of alginate based hydrogels/dressings in wound healing: sustained, dynamic and sequential release [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 638-643. |
| [14] | Chen Jiana, Qiu Yanling, Nie Minhai, Liu Xuqian. Tissue engineering scaffolds in repairing oral and maxillofacial soft tissue defects [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 644-650. |
| [15] | Wu Dandan, Liu Qi. Epigenetic mechanisms in periodontal disease, periodontal cell osteogenesis and bone regeneration [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(35): 5716-5722. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||