Chinese Journal of Tissue Engineering Research ›› 2021, Vol. 25 ›› Issue (29): 4709-4714.doi: 10.12307/2021.173
Previous Articles Next Articles
Effect of B lymphocytes and related cytokines on osteoclast differentiation in the osteoimmunology system
He Yixiang1, Zhao Yuhao1, Gao Zhao1, Zhao Haiyan2, Wang Wenji2
- 1First Clinical Medical College of Lanzhou University, Lanzhou 730000, Gansu Province, China; 2Department of Orthopedics, First Hospital of Lanzhou University, Lanzhou 730000, Gansu Province, China
-
Received:2020-09-18Revised:2020-09-23Accepted:2020-11-09Online:2021-10-18Published:2021-07-22 -
Contact:Wang Wenji, Professor, Chief physician, Master’s supervisor, Department of Orthopedics, First Hospital of Lanzhou University, Lanzhou 730000, Gansu Province, China -
About author:He Yixiang, Master candidate, First Clinical Medical College of Lanzhou University, Lanzhou 730000, Gansu Province, China
CLC Number:
Cite this article
He Yixiang, Zhao Yuhao, Gao Zhao, Zhao Haiyan, Wang Wenji. Effect of B lymphocytes and related cytokines on osteoclast differentiation in the osteoimmunology system[J]. Chinese Journal of Tissue Engineering Research, 2021, 25(29): 4709-4714.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
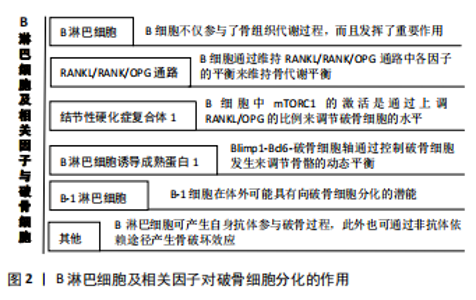
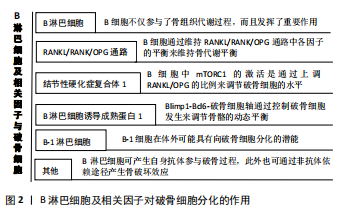
2.1 骨骼系统与免疫系统 骨骼系统为机体提供了结构上的稳定性,骨骼不仅是人体内主要的造血部位,还是钙磷贮存库[5]。在骨骼形态结构的改建过程中,成骨细胞产生类骨质,主导骨形成,破骨细胞进行骨吸收,成骨细胞与破骨细胞作用相互协调,完成旧骨吸收和新骨形成的过程。破骨细胞的分化涉及许多细胞和因子的相互作用,是整个骨重建的开端[6]。而体内免疫系统则主要通过非特异性免疫及特异性免疫机制,帮助机体抵御病原体入侵,维持体内稳态,主要参与结构有体内各种屏障以及T细胞介导的细胞免疫及B细胞介导的体液免疫过程。 除了早期发现的T淋巴细胞导致类风湿性关节炎患者出现骨质破坏的作用外,两系统间还存在许多重叠且相互作用的调控机制。TAICHMAN等[7]发现,成骨细胞可分泌粒细胞集落刺激因子与肝细胞生长因子等活性物质,这些细胞因子的协同作用可能是使成骨细胞具有干细胞刺激活性的原因。VISNJIC等[8]使用Ⅰ型胶原启动子片段对胸腺嘧啶激酶的表达进行调控,从而抑制成骨细胞的增殖与活化后,可致骨髓内细胞数量急剧减少,提示早期分化的成骨细胞对维持破骨细胞和造血功能的必要性。另外有研究表明髓样前体细胞在分化为抗原呈递树突细胞前仍具有分化为破骨细胞的潜能[9]。也有学者研究报道,认为B细胞可表达骨形态发生蛋白6和骨形态发生蛋白7来刺激新骨形成[10]。体内的多种活性物质在调控免疫细胞分化的同时,也可对成骨细胞及破骨细胞产生调控作用,进一步发展了骨免疫学理论。 在经典骨免疫学理论中,T淋巴细胞被认为是影响骨组织细胞分化过程中最重要的免疫细胞。Th1细胞可表达干扰素γ,进而通过明显降低破骨细胞前体CXCR4的表达,抑制破骨细胞形成[11]。Th2细胞可分泌白细胞介素4通过作用于RANKL/RANK/OPG通路,使核因子κB受体活化因子配体(receptor activator of nuclear factor kappa B ligand,RANKL)、核因子κB受体活化因子(receptor activator of nuclear factor-κB,RANK)表达减少以及骨保护素(osteoprotegerin,OPG)表达增加来抑制破骨细胞分化[12];也可通过细胞表面受体,如Th17细胞表面的白细胞介素23受体与白细胞介素23结合后正向刺激白细胞介素17的分泌增加,进而对破骨细胞形成产生诱导作用[13]。同时,作为重要的免疫细胞,B淋巴细胞也可以多种方式参与骨组织代谢过程,如产生肿瘤坏死因子α、骨保护素、RANKL等调节骨代谢平衡;B细胞也可接受来自T细胞的信号而产生作用,Th1及Th2分泌的细胞相关因子,可激活B细胞分化,继而由B细胞产生肿瘤坏死因子α、转化生长因子β等细胞介质,去促进或抑制破骨细胞的分化过程,从而参与调节骨代谢。 2.2 B淋巴细胞及相关因子与破骨细胞 2.2.1 B淋巴细胞 在骨髓中,造血干细胞经过不断分化发育成为成熟B淋巴细胞,其在骨髓中的发育过程不受外来抗原影响,继而离开骨髓环境到达外周的B细胞区定居,接受外来抗原刺激而活化增殖,进一步分化为浆细胞和记忆B细胞。B细胞的主要生理功能是产生抗体介导体液免疫应答,也可提呈可溶性抗原,产生细胞因子参与免疫调节。 活化的T淋巴细胞与破骨细胞间的相互作用是骨免疫学的核心理论[14],在针对类风湿性关节炎的研究中,T细胞的作用也已经有了较为明确的认识,而B细胞在其中的影响不甚清晰。但B细胞在骨免疫学的调控中也发挥着不可忽视的作用。MEEDNU等[15]检测正常人及类风湿性关节炎患者外周血和滑膜组织中B细胞亚群产生RANKL的情况,发现与健康人相比,类风湿性关节炎患者外周血中记忆B细胞能够表达更多的RANKL。这些发现提示B细胞在骨稳态中的重要作用,以及在导致类风湿性关节炎关节破坏中的作用。贾淑媛等[16]测定不同活动度类风湿性关节炎患者外周血中淋巴细胞亚群的数量,发现CD3-CD19+B细胞显著增多,这项研究首次证实了B细胞在类风湿性关节炎骨破坏组中增多,表明B细胞可能参与了骨破坏形成,并与疾病的活动度相关。同时,有研究表明,采用B细胞耗竭疗法治疗类风湿性关节炎患者,不仅能减轻患者的临床症状,也通过改变骨吸收和骨形成之间的平衡关系抑制了关节损伤的进展[17-18],表明B细胞不仅参与了骨组织代谢过程,而且发挥了重要作用,同时为治疗该病提供了新的思路。 2.2.2 B淋巴细胞在RANKL/RANK/OPG通路中的作用 破骨细胞受到的调控作用通过多种信号通路产生效应,如RANKL/RANK/OPG通路、Wnt/β-catenin通路等,其中最主要的是RANKL/RANK/OPG通路,T、B淋巴细胞均可作用于此通路,进而调节破骨细胞的分化发育产生效应,其在骨骼系统发育及获得性免疫的建立过程中均发挥了重要作用[19]。LI等[20]通过小鼠的基因敲除实验发现,敲除RANKL相关基因的小鼠因缺乏破骨细胞而表现出骨吸收和改建过程的严重缺陷;而过度表达RANKL相关基因的小鼠因破骨细胞增加而表现出骨密度下降。TAKAHASHI等[21]将骨髓源性单核/巨噬细胞系细胞和破骨细胞组成支持细胞在体外形成共培养系统后发现,不仅产生了破骨前体细胞生存所必须的巨噬细胞集落刺激因子,还分泌了一种破骨细胞分化必须的破骨细胞分化因子(Osteoclast differentiation factor,ODF)。后有研究证实,破骨细胞分化因子即为RANKL[22]。 RANKL可表达于骨髓间充质干细胞、成骨细胞系细胞、淋巴细胞、滑膜成纤维细胞等[23-24],可通过与破骨细胞前体细胞上的受体RANK结合后,产生广泛的级联反应,促使破骨细胞分化发育。而在人体内环境中,B淋巴系细胞则是骨髓内源性ODF/RANKL的主要表达来源,并可在体外环境支持破骨细胞分化[25]。MEEDNU等[15]检测正常人及类风湿性关节炎患者外周血和滑膜组织中B细胞亚群产生RANKL的情况,发现外周血B细胞在刺激下能表达RANKL,其中记忆B细胞(CD27+IGD-)产生RANKL的倾向最高,甚至超过T细胞所产生的RANKL,能够有效促进破骨细胞的分化。另外,对发育早期的B淋巴系细胞进行巨噬细胞集落刺激因子和可溶性DOF/RANKL的刺激后,发现它具有向破骨细胞分化的潜能。有实验证实,在基因敲除的小鼠中,巨噬细胞集落刺激因子或ODF/RANKL基因缺乏后,将导致小鼠骨量增加[26]。因此,B淋巴系细胞参与破骨细胞的发生可能通过两种方式:①表达ODF/RANKL以支持破骨细胞分化;②细胞自身作为破骨细胞前体。 除了产生ODF/RANKL外,髓内B淋巴细胞在骨髓微环境下产生的骨保护素也发挥着重要作用。骨保护素是目前发现的唯一能够对破骨细胞进行直接负向调控的因子,它作为RANKL的可溶性诱饵受体,其与RANKL亲和力高,能与RANKL竞争性结合[27],阻断RANKL/RANK结合后的级联反应,从而抑制破骨细胞的形成及分化,调节骨代谢过程。有实验证实,骨保护素能阻断成熟破骨细胞的激活及分化[28]。SIMONET等[29]通过转基因小鼠实验,发现骨保护素在小鼠中的表达与破骨细胞分化后期的减少一致,且同样的情况可发生在正常小鼠上,提示骨保护素作为一种可溶性因子,明显参与了骨吸收的调节。在人体内,产生骨保护素的重要来源即为髓内B细胞。LI等[30]通过对免疫磁珠分离后获得的骨髓内B细胞和B细胞前体产生的骨保护素进行定量分析发现,B细胞系产生了髓内总骨保护素水平的约64%,45%的骨保护素由成熟的B细胞产生。ONAL等[31]通过敲除小鼠T细胞和B细胞RANKL发现,B细胞和T细胞产生的RANKL不影响小鼠骨骼的生长发育过程;而敲除B细胞RANKL的小鼠,CD19+B细胞和B220+CD43-前B细胞百分比降低,CD3+T细胞无明显变化,提示B细胞发育过程中需要自身RANKL的表达。另外,敲除小鼠T细胞RANKL后不能缓解卵巢摘除术后的骨丢失,而敲除B细胞RANKL后,可抑制破骨细胞,从而部分缓解骨量的丢失。这都表明了在调节骨骼代谢的过程中,B淋巴细胞发挥着重要的作用,B细胞通过维持RANKL/RANK/OPG通路中各因子的平衡,来维持骨代谢平衡。 破骨细胞的分化发育是骨骼重建的开始,RANKL与RANK的结合在破骨细胞发育过程中发挥了重要作用,同时骨保护素又具有抑制促破骨细胞成熟的作用,三者的相互作用使代谢过程趋于平衡。 2.2.3 结节性硬化症复合体1(tuberous sclerosis complex 1,TSC1) TSC/mTORC1已被广泛证实在细胞代谢及代谢性疾病中具有明确作用。另有多项研究表明,结节性硬化症复合体在骨髓基质细胞、破骨细胞及成骨细胞的增殖分化过程中起重要作用[32-34]。LIU等[35]通过实验建立了结节性硬化症复合体1缺失小鼠的模型,以激活哺乳动物雷帕霉素靶蛋白复合物1(mammalian target of rapamycin complex 1,mTORC1),发现破坏骨细胞结节性硬化症复合体1后减少了骨硬化素的表达,促进了骨形成,提示了TSC1/mTORC1信号机制在调节骨细胞硬化素分泌和骨形成过程中具有重要作用。 小鼠的B细胞中结节性硬化症复合体1是 mTORC1的上游负调控因子,其缺失后导致mTORC1的激活。XU等[36]通过动物实验,首次证实了mTORC1在B细胞中被激活后,可进而激活RANKL,抑制骨保护素的表达,促进破骨细胞形成,导致小鼠出现骨质疏松;并证明了mTORC1通过对Akt和β-catenin的负性调控促进RANKL的表达和破骨细胞的形成。通过显微CT分析实验小鼠的股骨参数,发现B细胞中结节性硬化症复合体1的缺失导致骨量表型降低,使用mTORC1特异性抑制剂雷帕霉素治疗后,能部分恢复小鼠的低骨量表型,这些结果表明,B淋巴细胞中结节性硬化症复合体1的破坏和mTORC1的激活促进了破骨细胞的形成。同时小鼠骨髓中RANKL水平升高而骨保护素水平下降,与破骨细胞生成增加一致,提示B细胞中mTORC1的激活是通过上调RANKL/OPG的比例来调节破骨细胞的水平。 2.2.4 B淋巴细胞诱导成熟蛋白1(B lymphocyte induced maturation protein 1,Blimp1) B淋巴细胞诱导成熟蛋白1是由人类PRDM1基因编码的蛋白质。TURNER等[37]诱导小鼠B淋巴细胞分化发现,在细胞向有分泌功能的浆细胞分化过程中,可测得B淋巴细胞诱导成熟蛋白1的水平上调,提示B淋巴细胞诱导成熟蛋白1对B细胞向浆细胞分化过程有作用。后B淋巴细胞诱导成熟蛋白1被证实是生发中心内B淋巴细胞向浆细胞进一步分化过程中重要的转录抑制因子[38]。 B淋巴细胞诱导成熟蛋白1是在破骨细胞形成过程中由RANKL通过NFATc1诱导的、IRF8和Mafb等抗破骨细胞基因的转录抑制因子[39]。有研究发现,破骨细胞生成抑制基因可受B淋巴细胞诱导成熟蛋白1的调控。NISHIKAWA等[39]研究发现,B淋巴细胞诱导成熟蛋白1的过表达可显著恢复受损的破骨细胞的形成,表明B淋巴细胞诱导成熟蛋白1具有促进破骨细胞生成的能力。PRDM1基因缺陷的破骨细胞前体细胞不能有效的进行分化。B淋巴细胞诱导成熟蛋白1也被描述为参与早期B细胞分化基因的抑制因子,这些基因使B细胞能够向浆细胞终末转化[40]。 研究表明,有多种物质可通过上调或下调B淋巴细胞诱导成熟蛋白1水平,参与破骨细胞的调控。WU等[41]发现肿瘤坏死因子α可促进破骨细胞分化过程中B淋巴细胞诱导成熟蛋白1的表达,参与了破骨细胞生成。ZHAO等[42]发现毛壳素会通过下调B淋巴细胞诱导成熟蛋白1,从而诱导IRF8和Mafb等的表达,进而抑制RANKL诱导的破骨细胞生成,然后诱导抗破骨细胞生成基因和细胞生长抑制因子。白细胞介素33可通过调节B淋巴细胞诱导成熟蛋白1和IRF-8的表达,抑制RANKL诱导的破骨细胞,从而保护骨质,避免过分吸收[43-44]。JEONG等[45]发现,SiRNA降低B淋巴细胞诱导成熟蛋白1的表达,下调RANKL诱导的EEIG1水平,而过表达B淋巴细胞诱导成熟蛋白1则增强EEIG1水平。EEIG1与B淋巴细胞诱导成熟蛋白1形成复合物,负调控抗破骨细胞生成基因IRF8的表达。结果表明Blimp1-EEIG1-IRF8轴在炎性骨吸收和骨稳态中起重要作用。 MIYAUCHI等[46]报道了Bcl6是B淋巴细胞诱导成熟蛋白1的直接靶点,在破骨细胞中B淋巴细胞诱导成熟蛋白1缺乏的小鼠表现出由于破骨细胞生成受损而致的骨化症。表明Blimp1-Bcl6-破骨细胞轴通过控制破骨细胞发生来调节骨骼的动态平衡。 2.2.5 B-1淋巴细胞 B淋巴细胞由两种亚群组成,即传统B淋巴细胞(又可称B-2淋巴细胞)及B-1淋巴细胞。B-1细胞最初被定义为表达Ly-1(即CD5)的高IgM低IgD淋巴细胞群体[47],后经研究发现,B-1细胞与传统B细胞相比,细胞表面不表达表面分子CD23[48]。此外也存在有不表达CD5、但具有B-1表型的细胞存在,因此又可将其分为两亚群:CD5阳性的B-1a群和CD5阴性的B-1b群[49]。 有报道称B-1细胞在体外环境可分化为巨噬细胞,因而将其命名为B-1细胞源性巨噬细胞(B-1CDP)。BOGSAN等[50]也经过实验,对小鼠腹腔细胞培养中获得的B-1细胞与X连锁免疫缺陷小鼠进行重组后分析小鼠体内巨细胞的形成情况,证实了在体内环境下B-1淋巴细胞可形成多核巨细胞,表明B-1细胞在小鼠异物巨细胞形成中可能起关键作用。PUGLIESE等[51]使用B-1基因缺陷的小鼠实验后发现动物的骨吸收过程受损,用B-1细胞重建后,骨吸收增加。同时,当使用RANKL和巨噬细胞集落刺激因子共同培养后,B-1细胞可表现为典型的破骨细胞表型,且具有破骨细胞活性,进一步证实了B-1细胞可在结构和功能上分化为破骨细胞样细胞。此外,在诱导B-1CDP分化时用RANKL和巨噬细胞集落刺激因子处理B-1细胞,可观察到巨噬细胞集落刺激因子受体或RANK阳性的多核细胞的形成,提示B-1细胞在体外可能具有向破骨细胞分化的潜能。 2.2.6 其他 B淋巴细胞可产生自身抗体参与破骨过程,此外也可通过非抗体依赖途径产生骨破坏效应。有研究表明,B细胞可通过产生抗瓜氨酸蛋白抗体(anti-citrullinated protein antibodies,ACPA)识别破骨细胞及其前体细胞表面的瓜氨酸波形蛋白,进而增加破骨细胞的形成和分化[52]。抗瓜氨酸蛋白抗体存在于大多数类风湿性关节炎患者中,是一种特异性抗体,在类风湿性关节炎患者发病前即已出现,并参与骨质破坏。KRISHNAMURTHY等[53]从类风湿性关节炎患者滑液和外周血中分离多克隆抗瓜氨酸蛋白抗体,并从患者的滑液B细胞中分离单克隆抗瓜氨酸蛋白抗体,实验发现部分单克隆抗瓜氨酸蛋白抗体可来源于类风湿性关节炎患者的滑液B细胞,在细胞培养中促进破骨细胞的分化发育。另外,抗瓜氨酸蛋白抗体刺激破骨细胞后,可发现白细胞介素8的释放量明显增加,使用白细胞介素8拮抗剂后,由此导致的小鼠的骨丢失可被逆转,进一步提示白细胞介素8是抗瓜氨酸蛋白抗体诱导破骨细胞活化的关键物质,阻断白细胞介素8或其受体可抑制骨的丢失。 此外,B淋巴细胞作为重要的免疫活性细胞,也可以产生多种细胞因子,如肿瘤坏死因子α、肿瘤坏死因子β、转化生长因子β、干扰素γ等,它们也可产生调节破骨细胞的作用,后两种可产生负向抑制作用[54]。而肿瘤坏死因子α及肿瘤坏死因子β在破骨细胞的分化过程中,可刺激破骨细胞前体细胞由骨髓向髓外迁移,同时刺激破骨细胞相关免疫球蛋白受体等表面受体表达,促进破骨细胞分化[55]。在骨质疏松症患者中,可发现白细胞介素31表达量增加,诱导趋化因子及促炎性破骨细胞生成素刺激骨质的吸收,导致破骨细胞前体细胞的分化激活[56]。 B淋巴细胞及相关因子对破骨细胞分化作用的示意图见图2。 2.3 骨骼系统对B淋巴细胞的作用 在人体内环境中,免疫系统和骨骼系统除了二者的关键细胞直接作用外,也可通过转录因子、细胞因子及相关受体等间接联系,并对二者的发育过程产生相互调节的作用。B细胞来源于髓内造血干细胞,在骨髓中发育成熟后迁移。成骨细胞作为造血干细胞龛的重要组成部分,在体内外均可表现出对B细胞的调节作用。VISNJIC等[57]使用成骨细胞特异表达单纯病毒胸苷激酶的小鼠模型并使用更昔洛韦诱导成骨细胞损伤发现,髓内B细胞系前体细胞数量明显下降,停用更昔洛韦后回升,从而表现出成骨细胞对维持髓内B细胞数量和发育的作用。另外发现,骨内膜表面的成骨细胞联合甲状旁腺激素诱导的血管内皮细胞黏附因子1、白细胞介素7、CXCL12等可共同调控前体B细胞的分化发育;骨髓基质细胞和成骨细胞分泌生长因子、CXC12、巨噬细胞集落刺激因子可刺激前B细胞发育[58]。"
| [1] TAKAYANAGI H. New developments in osteoimmunology. Nat Rev Rheumatol. 2012;8(11):684-689. [2] SCHETT G, GRAVALLESE E. Bone erosion in rheumatoid arthritis: mechanisms, diagnosis and treatment. Nat Rev Rheumatol. 2012;8(11): 656-664. [3] MARINOVA-MUTAFCHIEVA L, WILLIAMS RO, FUNA K, et al. Inflammation is preceded by tumor necrosis factor-dependent infiltration of mesenchymal cells in experimental arthritis. Arthritis Rheum. 2002;46(2):507-513. [4] ARRON JR, CHOI Y. Bone versus immune system. Nature. 2000;408 (6812):535-536. [5] Sims NA, Vrahnas C. Regulation of cortical and trabecular bone mass by communication between osteoblasts, osteocytes and osteoclasts.Arch Biochem Biophys. 2014;561:22-28. [6] 刘伟,宋慧,董鹏.骨免疫学研究进展[J].骨科临床与研究杂志, 2020,5(2):124-126. [7] TAICHMAN R, REILLY M, VERMA R, et al. Hepatocyte growth factor is secreted by osteoblasts and cooperatively permits the survival of haematopoietic progenitors. Br J Haematol. 2001;112(2):438-448. [8] VISNJIC D, KALAJZIC I, GRONOWICZ G, et al. Conditional ablation of the osteoblast lineage in Col2.3deltatk transgenic mice. J Bone Miner Res. 2001;16(12):2222-2231. [9] ALNAEELI M, PENNINGER JM, TENG YT. Immune interactions with CD4+ T cells promote the development of functional osteoclasts from murine CD11c+ dendritic cells. J Immunol. 2006;177(5):3314-3326. [10] 王凌,李大金.免疫活性细胞对骨代谢的调控作用[J].中国免疫学杂志,2006,22(3):287-290. [11] 喻晶. IFN-γ对小鼠破骨细胞前体CXCR4表达的调节及意义[D].武汉:华中科技大学,2010. [12] 董锡亮,赵宏斌.IL-4抑制骨吸收的研究进展[J].中国老年学杂志, 2009,29(5):634-636. [13] BRIOLAY A, LENCEL P, BESSUEILLE L, et al. Autocrine stimulation of osteoblast activity by Wnt5a in response to TNF-α in human mesenchymal stem cells. BiochemBiophys Res Commun. 2013;430(3): 1072-1077. [14] TAKAYANAGI H. Osteoimmunology and the effects of the immune system on bone. Nat Rev Rheumatol. 2009;5(12):667-676. [15] MEEDNU N, ZHANG H, OWEN T, et al. Production of RANKL by Memory B Cells: A Link Between B Cells and Bone Erosion in Rheumatoid Arthritis. Arthritis Rheumatol. 2016;68(4):805-816. [16] 贾淑媛,李萍.淋巴细胞亚群在类风湿关节炎患者外周血中的表达及意义[J].中国实验诊断学,2019,23(11):1943-1946. [17] WHEATER G, HOGAN VE, TENG YK, et al. Suppression of bone turnover by B-cell depletion in patients with rheumatoid arthritis. OsteoporosInt. 2011;22(12):3067-3072. [18] BOUMANSM J, THURLINGSR M, YEO L, et al. Rituximab abrogates joint destruction in rheumatoid arthritis by inhibiting osteoclastogenesis.Ann Rheum Dis. 2012;71(1):108-113. [19] ROSSI SW, KIM MY, LEIBBRANDT A, et al. RANK signals from CD4(+)3(-) inducer cells regulate development of Aire-expressing epithelial cells in the thymicmedulla. J ExpMed. 2007;204(6):1267-1272. [20] LI J, SAROSI I, YAN XQ, et al. RANK is the intrinsic hematopoietic cell surface receptor that controls osteoclastogenesis and regulation of bone mass and calcium metabolism. Proc Natl AcadSci U S A. 2000; 97(4):1566-1571. [21] TAKAHASHI N, AKATSU T, UDAGAWA N, et al. Osteoblastic cells are involved in osteoclast formation. Endocrinology. 1988;123(5):2600-2602. [22] YASUDA H, SHIMA N, NAKAGAW AN, et al. Osteoclast differentiation factor is a ligand for osteoprotegerin/osteoclastogenesis-inhibitory factor and is identical to TRANCE/RANKL. Proc Natl AcadSci U S A. 1998; 95(7):3597-3602. [23] O’BRIEN CA. Control of RANKL gene expression. Bone. 2010;46(4):911-919. [24] WAL SH MC, KIM N, KADONO Y, et al. Osteoimmunology: interplay between the immune system and bone metabolism. Annu Rev Immunol. 2006;24:33-63. [25] MANABE N, KAWAGUCHI H, CHIKUDA H, et al. Connection between B lymphocyte and osteoclast differentiation pathways.J Immunol. 2001; 167(5):2625-2631. [26] YOSHIDA H, HAYASHI S, KUNISADA T, et al.The murine mutation osteopetrosis is in the coding region of the macrophage colony stimulating factor gene. Nature. 1990;345(6274):442-444. [27] 陈之光,薛今琦,付勤.干扰素-γ在骨免疫系统中作用的研究进展[J].中国骨质疏松杂志,2015,21(3):361-366. [28] DOUGALL WC, GLACCUM M, CHARRIER K, et al. RANK is essential for osteoclast and lymph node development. Genes Dev. 1999;13(18): 2412-2424. [29] SIMONET WS, LACEY DL, DUNSTAN CR, et al. Osteoprotegerin: a novel secreted protein involved in the regulation of bone density. Cell. 1997; 89(2):309-319. [30] LI Y, TORALDO G, LI A, et al. B cells and T cells are critical for the preservation of bone homeostasis and attainment of peak bone mass in vivo. Blood. 2007;109(9):3839-3848. [31] ONAL M, XIONG J, CHEN X, et al. Receptor activator of nuclear factor κB ligand (RANKL) protein expression by B lymphocytes contributes to ovariectomy-induced bone loss .J BiolChem. 2012;287(35):29851-29860. [32] HUANG J, MANNING BD. TheTSC1-TSC2 complex: a molecular switchboard controlling cell growth. BiochemJ. 2008;412(2):179-190. [33] HUANG B, WANG Y, WANG W, et al. mTORC1 Prevents Preosteoblast Differentiation through the Notch Signaling Pathway. PLoS Genet. 2015;11(8):e1005426. [34] CHEN J, LONG F. mTOR signaling in skeletal development and disease. Bone Res. 2018;6:1. [35] LIU W, WANG Z, YANG J, et al. OsteocyteTSC1 promotes sclerostin secretion to restrain osteogenesis in mice. OpenBiol. 2019;9(5):180262. [36] XU S, ZHANG Y, LIU B, et al. Activation of mTORC1 in B Lymphocytes Promotes Osteoclast Formation via Regulation of β-Catenin and RANKL/OPG. J Bone Miner Res. 2016;31(7):1320-1333. [37] TURNER CA JR, MACK DH, DAVIS MM. Blimp-1, a novel zinc finger-containing protein that can drive the maturation of B lymphocytes into immunoglobulin-secreting cells. Cell. 1994;77(2):297-306. [38] 刘国生,王姣平,褚志华,等.骨髓单个核细胞中B淋巴细胞诱导成熟蛋白-1表达对多发性骨髓瘤患者预后的影响[J].中国实验血液学杂志,2017,25(5):1449-1453. [39] NISHIKAWA K, NAKASHIMA T, HAYASHI M, et al. Blimp1-mediated repression of negative regulators is required for osteoclast differentiation. Proc Natl AcadSci U S A. 2010;107(7):3117-3122. [40] MARTINS G, CALAME K. Regulation and functions of Blimp-1 in T and B lymphocytes. Annu Rev Immunol. 2008;26:133-169. [41] WU L, GUO Q, YANG J, et al. Tumor Necrosis Factor Alpha Promotes Osteoclast Formation Via PI3K/AktPathway-Mediated Blimp1 Expression Upregulation. J Cell Biochem. 2017;118(6):1308-1315. [42] ZHAO N, TSUDA H, MUROFUSHI T, et al. Chaetocin inhibits RANKL-induced osteoclast differentiation through reduction of Blimp1 in Raw264.7cells. Life Sci. 2015;143:1-7. [43] GINALDIL, DE MARTINIS M, SAITTA S, et al. Interleukin-33 serum levels in postmenopausal women with osteoporosis. Sci Rep. 2019;9(1):3786. [44] KIYOMIYA H, ARIYOSHI W, OKINAGA T, et al. IL-33 inhibits RANKL-induced osteoclast formation through the regulation of Blimp-1 and IRF-8 expression. BiochemBiophys Res Commun. 2015;460(2):320-326. [45] JEONG E, KIM J, GO M, et al. Early estrogen-induced gene 1 facilitates osteoclast formation through the inhibition of interferon regulatory factor 8 expression. FASEB J. 2020;34(9):12894-12906. [46] MIYAUCHI Y, NINOMIYA K, MIYAMOTO H, et al. The Blimp1-Bcl6 axis is critical to regulate osteoclast differentiation and bone homeostasis. J Exp Med. 2010;207(4):751-762. [47] HARDY RR, HAYAKAWA K, HAAIJMAN J, et al. B-cell subpopulations identified by two-colour fluorescence analysis. Nature. 1982;297(5867): 589-591. [48] WALDSCHMIDT TJ, KROESE FG, TYGRETT LT, et al. The expression of B cell surface receptors. III. The murine low-affinity IgE Fc receptor is not expressed on Ly 1 or ‘Ly 1-like’ B cells. Int Immunol. 1991;3(4):305-315. [49] STALL AM, ADAMS S, HERZENBERG LA, et al. Characteristics and development of the murine B-1b (Ly-1 B sister) cell population. Ann N Y AcadSci. 1992;651:33-43. [50] BOGSAN CS, NOVAES E BRITO RR, PALOS MDA C, et al. B-1 cells are pivotal for in vivo inflammatory giant cell formation. Int J Exp Pathol. 2005;86(4):257-265. [51] PUGLIESE LS, GONÇALVES TO, POPIAF, et al. B-1 lymphocytes differentiate into functional osteoclast-like cells. Immunobiology. 2012;217(3):336-344. [52] HARRE U, GEORGESS D, BANG H, et al. Induction of osteoclastogenesis and bone loss by human autoantibodies against citrullinatedvimentin. J Clin Invest. 2012;122(5):1791-1802. [53] KRISHNAMURTHY A, JOSHUA V, HAJHENSVOLD A, et al. Identification of a novel chemokine-dependent molecular mechanism underlying rheumatoid arthritis-associated autoantibody-mediated bone loss. Ann Rheum Dis. 2016;75(4):721-729. [54] 张益祥,谭心辰,吴耀持.免疫与炎症对破骨细胞分化的影响[J].上海医药,2020,41(14):30-33+55. [55] HERMAN S, MÜLLER RB, KRÖNKE G, et al. Induction of osteoclast-associated receptor, a key osteoclast costimulationmolecule,in rheumatoid arthritis. Arthritis Rheum. 2008;58(10):3041-3050. [56] GINALDI L, DE MARTINIS M, CICCARELLI F, et al. Increased levels of interleukin 31 (IL-31) in osteoporosis. BMCImmunol. 2015;16:60. [57] VISNJIC D, KALAJZIC Z, ROWED W, et al. Hematopoiesis is severely altered in mice with an induced osteoblast deficiency. Blood. 2004; 103(9):3258-3264. [58] ZHU J, GARRETT R, JUNG Y, et al. Osteoblasts support B-lymphocyte commitment and differentiation from hematopoietic stem cells. Blood. 2007;109(9):3706-3712. (责任编辑:WZH,ZN,DL) |
| [1] | Zhou Quan, Zhang Yanan, Bai Yiguang, Zhang Qiong, Nong Haibin, Liu Mingfu, Zeng Gaofeng, Zong Shaohui. Effect of 3-phosphoinositide-dependent protein kinase 1 regulating osteoclasts on bone mineral density in osteoporotic mice [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(29): 4680-4684. |
| [2] | Zhang Mingjin, Zhou Yanheng, Liu Dawei. Reopening the fused suture provides a new idea for maxillary expansion [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(29): 4721-4727. |
| [3] | Li Ruozhen, Tian Yaping, Wen Ning. Biological effect of magnetic fields to promote bone responses to biomaterials [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(28): 4510-4515. |
| [4] | Wei Congcong, Yao Mengxuan, Yang Meng, Li Huijie. Mechanism and treatment of osteolysis around artificial joint prosthesis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(27): 4401-4407. |
| [5] | Yang Caihui, Liu Qicheng, Dong Ming, Wang Lina, Zuo Meina, Lu Ying, Niu Weidong. Serine/threonine protein kinases can promote bone destruction in mouse models of chronic periapical periodontitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(23): 3654-3659. |
| [6] | Huo Hua, Cheng Yuting, Zhou Qian, Qi Yuhan, Wu Chao, Shi Qianhui, Yang Tongjing, Liao Jian, Hong Wei. Effects of drug coating on implant surface on the osseointegration [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3558-3564. |
| [7] | Jiang Shengyuan, Li Dan, Jiang Jianhao, Shang-you Yang, Yang Shuye. Biological response of Co2+ to preosteoblasts during aseptic loosening of the prosthesis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(21): 3292-3299. |
| [8] | Wu Yukun, Han Jie, Wen Shuaibo. Mechanism of Runx2 gene in fracture healing [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(14): 2274-2279. |
| [9] | Xu Nuo, Cao Zhen, Li Xiaojie, Shi Chun. MicroRNA-21 regulates proliferation and differentiation of osteoclasts in periodontitis [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(8): 1225-1230. |
| [10] | Ge Juncheng, Ma Jinhui, Wang Bailiang, Yue Debo, Sun Wei, Wang Weiguo, Guo Wanshou, Li Zirong. Application of bisphosphonates in avascular necrosis of the femoral head [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(5): 753-759. |
| [11] | Zhang Yanan, Yan Xia, Meng Zengdong. Zn and Mg increase the bioactivity and osteogenic induction of hydroxyapatite biomaterial in bone repair: clinical application and mechanism [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(4): 606-611. |
| [12] | Song Shilei, Chen Yueping, Zhang Xiaoyun. Mechanism of PI3K/AKT signaling pathway regulating osteonecrosis of the femoral head [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(3): 408-415. |
| [13] | Shi Dongmei, Dong Ming, Lu Ying, Niu Weidong. PI3K/Akt signaling pathway and bone destruction: problems and mechanisms [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(23): 3716-3722. |
| [14] | Ye Nan, Huang Jian, Wang Dan. Important roles of growth hormone-releasing peptide in bone growth and development [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(20): 3226-3233. |
| [15] | Feng Yang, Yan Xu, Wang Yongkui, Yang Tengyue, Shang Lijie, Zhang Chunlin. Relationship between degenerative lumbar disc disease and peripheral blood lymphocyte subsets [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(17): 2630-2635. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||