Chinese Journal of Tissue Engineering Research ›› 2021, Vol. 25 ›› Issue (27): 4401-4407.doi: 10.12307/2021.204
Previous Articles Next Articles
Mechanism and treatment of osteolysis around artificial joint prosthesis
Wei Congcong, Yao Mengxuan, Yang Meng, Li Huijie
- Department of Orthopedics, the Third Hospital of Hebei Medical University, Shijiazhuang 050051, Hebei Province, China
-
Received:2020-11-27Revised:2020-12-04Accepted:2021-01-07Online:2021-09-28Published:2021-04-10 -
Contact:Li Huijie, MD, Chief physician, Department of Orthopedics, the Third Hospital of Hebei Medical University, Shijiazhuang 050051, Hebei Province, China -
About author:Wei Congcong, Master candidate, Department of Orthopedics, the Third Hospital of Hebei Medical University, Shijiazhuang 050051, Hebei Province, China
CLC Number:
Cite this article
Wei Congcong, Yao Mengxuan, Yang Meng, Li Huijie. Mechanism and treatment of osteolysis around artificial joint prosthesis[J]. Chinese Journal of Tissue Engineering Research, 2021, 25(27): 4401-4407.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
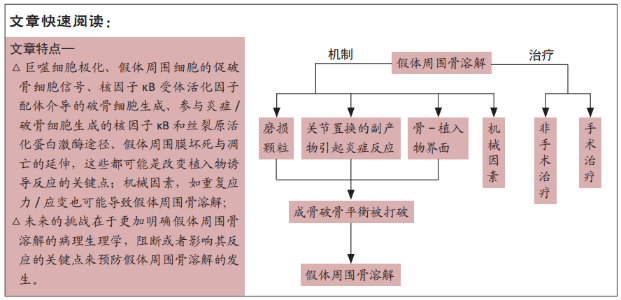
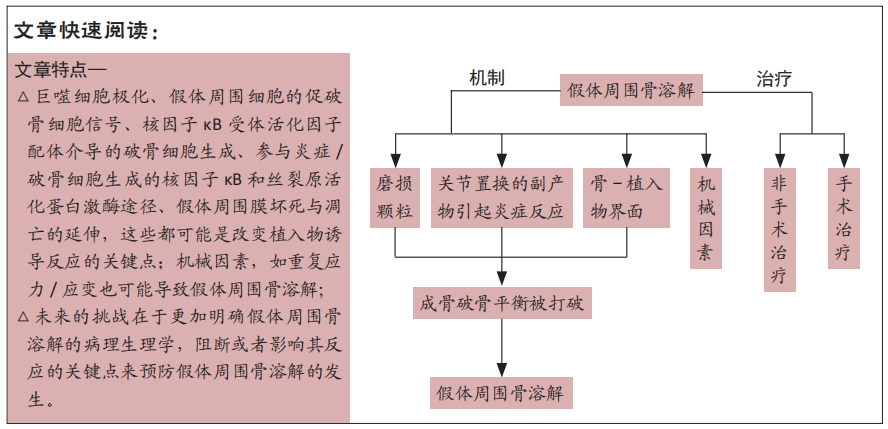
2.1 PPOL的机制 2.1.1 假体副产品致骨溶解 有强有力的证据表明慢性低度炎症在PPOL机制中的关键作用[3]。人工假体的副产品与免疫细胞接触后,免疫细胞表达促炎细胞因子、趋化因子和其他物质,最终导致PPOL以及无菌性松动的发生。同样的促炎物质在PPOL和无菌性松动再次手术时取回的组织中被广泛检测到[4]。重要的是,同样的炎症因子参与了先天免疫系统的生物学过程,包括那些对细菌病原体的免疫反应。由于植入物周围炎症反应的长期激活,破骨细胞在骨-植入物界面被激活,并开始骨吸收。 2.1.2 炎症的进展 炎症是免疫系统对外部和内部危险或非自身、坏死组织以及不利的机械或代谢刺激的普遍反应[5]。在某种程度上,这种反应的强度可能与人工粒子(特别是聚乙烯)和细菌在大小和化学成分方面的相似性有关[6]。假体和细菌副产物与位于免疫细胞表面和或细胞内的一组先天性免疫受体接触,天然免疫受体触发急性炎症反应,导致炎症细胞因子、趋化因子和活性氧的上调和释放。肿瘤坏死因子α、白细胞介素1,6,17 和γ-干扰素被认为是骨吸收的强效促成因素[7]。肿瘤坏死因子 α 和白细胞介素1能促进人成骨细胞骨保护素配体的表达,而骨保护紊配体能促进破骨细胞分化成熟并增强破骨细胞的活性[8]。一些细胞因子受体(如白细胞介素6 受体)的特征为与其胞内Janus 激酶(JAK)家族的酪氨酸激酶的结构域相关[9],例如白细胞介素1/Toll样受体通过白细胞介素1受体相关激酶和白细胞介素17信号通过肿瘤坏死因子受体相关因子2激活。此外,低度炎症会降低受累组织中的氧气和营养物质。缺氧可导致组织坏死,通过促进危险相关分子模式进一步增加局部免疫原性[10]。重要的是,活化的巨噬细胞与中性粒细胞相似,产生活性氧和一氧化氮以及其他炎症物质[11],活性氧也被证明有助于破骨细胞的分化[12]。尽管进行了深入的研究,但磨损颗粒引发的炎症和PPOL的许多方面仍无法解释,例如在复杂的假体周围环境中,不知道特定的细胞或细胞簇是如何通信的。最近,生长和分化因子15被揭示为炎症反应中组织耐受的中心介质[13]。理论上,患者的耐受机制也可能参与PPOL和无菌性松动,但是还需要进一步的研究。先天免疫的细胞能够识别假体周围环境中的磨损颗粒和受损组织,巨噬细胞是该反应的“导体”[14],有研究观察到巨噬细胞的M1极化与植入物诱导的炎症和坏死相关[15-16]。越来越多的证据表明淋巴细胞在 无菌性松动和PPOL机制中发挥作用,尤其是与超敏反应相 关[17];中性粒细胞在对磨损颗粒的反应中也很重要;另一方面,肥大细胞和树突状细胞在假体周围炎症和骨吸收机制中的作用知之甚少[18];非免疫细胞群,如成纤维细胞、成骨细胞、骨细胞也有助于假体周围炎症和骨-植入物界面的破骨细胞激活、存活[19-21]。 2.1.3 颗粒诱导炎症的调节 机体严格调控炎症以防止过度的组织损伤,假体周围组织耐受假体副产物长期负荷的能力似乎是关节置换长期成功的必要先决条件。与通常植入物功能稳定的适应性结局相比,PPOL可能是适应不良炎症(骨吸收的驱动因素)的特殊结果。因此,种植体周围的组织在炎症消退、维持其细胞代谢和结构稳定方面受到严格调控。大量证据支持炎症刺激引起的抗炎机制具有较强且快速的活 性[22];此外,组织稳态和调节机制激活,可以防止炎症导致的过度组织损伤[23];通过这些机制,假体周围炎症受到严格调控。一些研究表明,许多因素与炎症诱导的耐受介质相关,例如通过巨噬细胞的代谢重编程,这可能会改变其可塑性和表型,包括抗炎功能[24]。许多细胞因子(白细胞介素10,15)、转化生长因子?和激素有利于组织稳态,并触发与降低假体周围炎症活性相关的分子程序。人们才刚刚开始了解 miRNA在假体周围炎症中的作用[25];泛素编辑酶A20的失调也可能导致 PPOL和无菌性松动的发生[26];神经调节与植入物副产物诱导的慢性炎症有关[27]。 2.1.4 炎症相关骨吸收 有强有力的证据表明破骨细胞在PPOL中起主要作用。不管导致骨溶解的特殊生物学机制是什么(炎症、肿瘤还是全关节置换相关),破骨细胞是唯一的骨吸收细胞[28]。 一般来说,RANK-RANKL-骨保护素依赖和独立途径介导破骨细胞成熟[28]。RANKL刺激破骨细胞前体表面的RANK,RANK激活之后是涉及衔接分子的进一步生化反应步骤,如肿瘤坏死因子受体相关因子6,其导致有丝分裂原激活蛋白激酶和核因子κB和激活蛋白1的激活。活化的核因子κB通过活化T细胞核因子1的核因子影响破骨细胞的分化、活化和存活,活化T细胞核因子1是破骨细胞生成的关键调节因子[29]。 骨的大部分由富含胶原的矿化细胞外基质组成,必须被金属蛋白酶分解才能引起骨吸收。骨髓源性基质细胞对多种信号通路表达金属蛋白酶[30],多种金属蛋白酶参与了溶骨作用的诱导和放大[31],骨金属蛋白酶及其组织抑制剂之间的平衡失调也是慢性炎症的结果。特异性基质金属蛋白酶可在骨-种植体界面过度表达,以这种方式促进PPOL的加剧[32]。此外,活性氧升高可损害蛋白酶体功能,导致PPOL和无菌性松 动[33]。组织蛋白酶K是组织蛋白酶家族中一种类似木瓜蛋白酶的半胱氨酸蛋白酶,由破骨细胞合成并进入其封闭区,在骨吸收中也发挥着重要作用[34],它能降解骨基质中的Ⅰ型胶原和其他有机结构。 2.1.5 植入物-骨界面:一系列骨多细胞单位 虽然许多关于假体周围微环境的研究主要集中在颗粒病、炎症和骨的降解过程,但植入物的副产物对骨的形成和重建也有影响。骨-植入物界面本质上是一系列骨多细胞单元,由破骨细胞、成骨细胞和其他骨髓间充质干细胞-成骨细胞谱系的细胞组 成[35]。虽然PPOL的研究主要集中在单核细胞/巨噬细胞/异物巨细胞/破骨细胞系的细胞上,但骨多细胞单元中的其他细胞以及成纤维细胞、血管祖细胞等在PPOL的发育过程中发挥着重要作用。一般来说,与磨损副产物相关的慢性炎症通过抑制祖细胞的增殖、分化、成熟和功能来抑制骨形成,这些有害的影响导致骨形成和吸收之间的失调,倾向于骨溶解。持续的炎症也有助于细胞坏死和纤维化,破坏假体的稳定性和承受生理负荷的能力。 2.1.6 颗粒形态影响 一般来说,可以分为磨损相关的副产品和非磨损相关的副产品。通过人工关节承载面的黏附和磨损,小颗粒从较软材料的表面释放出来,关于磨损颗粒引起的炎症的触发和持续,许多参数起着重要作用(直径、起源材料、形状、含量、表面电荷等),所有下肢关节置换在使用期间的每一步都会产生磨损颗粒。聚乙烯颗粒在PPOL和无菌性松动形成机制中的病理作用有充分的证据[35]。实验表明,即使是陶瓷这样的硬材料也会产生纳米级的颗粒,从而引发炎症[36]。金属植入物产生的腐蚀性和纳米级磨损副产物也会通过微粒碎片产生不良反应[36];金属碎片具有特殊的意义,因为它可能导致迟发性超敏反应[37]。骨水泥颗粒与碎屑诱导的炎症和超敏反应有关[38-39]。 然而,关于假体颗粒大小、形状和表面电荷与破骨细胞分化、成熟、存活功能之间的相互关系的研究还很有限。基于新的、非常敏感的细菌分子鉴定方法的数据,细菌的副产物可能有助于无菌PPOL的发病和/或长期存在。有长期的临床经验证明,如果不及时诊断和治疗人工关节感染,可能会引起侵蚀性骨吸收;同样,尽管没有临床感染,血流中循环的细菌残留物也可能会加重无菌假体副产物诱导的炎 症[40]。原则上,产生骨吸收的机制与假体副产物的作用机制相似。一些研究表明,当在假体颗粒中加入内毒素或其他细菌特异性蛋白质时,碎片引起的炎症更剧烈[41];此外,一些证据表明假体表面生物膜的形成与慢性炎症引起的无菌性松动有关[42],而抗生素可以减弱PPOL和无菌性松动[43];另一方面,添加灭活的细菌会通过细菌诱导的炎症增加骨形成。综上所述,需要对这一问题进行进一步研究。最后,危险相关分子模式可以通过表面细胞或细胞内受体对假体周围炎症产生强大的刺激,有几项研究检测了危险相关分子模式在PPOL中的作用[44]。 2.1.7 机械性骨溶解及与炎症因子 机械负荷是骨形成的主要合成代谢刺激[45],相反,与特定植入物设计相关的应力遮挡、其弹性模量和其他因素可导致假体周围的骨丢失[46]。每个关节都受到机械力和载荷的作用,因此人工关节是传递机械力的生物工具。关节假体的设计用于承受步态、跑步和其他活动中重复出现的高负荷,不稳定的植入物可以引起逐渐的骨吸收,类似于骨折部位的机械运动导致骨吸收相关的不愈合的发展[47]。一些研究表明,关节液或种植体表面产生的机械力也会导致骨吸收[48]。迄今为止,还没有完全研究清楚机械力对PPOL的作用机制,直接传递的力与压力诱导的骨吸收密切相关;间接力可能通过炎症过程和破骨细胞生成的调节作用发挥作用[49]。基于上述内容,可以得出结论,有相对有力的证据表明机械力和压力在 PPOL 中的作用;此外,这些机械力和压力可与PPOL的生物过程相互作用。总之,无论机械负荷对假体周围骨结构的重要作用如何,炎性PPOL的证据更有力[50]。 2.2 PPOL的治疗 2.2.1 非手术治疗 目前没有长期研究证明非手术药物治疗PPOL的有效性。虽然体外和体内研究可能显示短期内骨溶解的缓解有限,但人体内与磨损颗粒相关的骨溶解是渐进的;当金属股骨头与金属外壳接触时,聚乙烯内衬完全磨损,尤其后一种情况是灾难性的,因为其结果是多种类型的磨损颗粒,所以必须切除而不是部分修复关节。因此,在检测到假体的严重损坏之前,应该更早地进行非手术治疗,这种干预的目的是限制骨缺损的大小以及推迟再次手术的时间。此外,这种干预可能使易受PPOL影响的患者较早发展PPOL,并且可能在较低的假体副产品负荷下出现PPOL。最后,对于不能立即再手术的患者,非手术治疗可能是一种选择,可能会减少骨缺损的进一步扩大。传统上,药物疗法分为影响骨降解和影响骨形成的疗法,这种分类是误导性的,因为骨骼的形成和退化是相互联系的,而且通常情况下,治疗会影响骨骼重建过程的两个方面。因此,下面将回顾一些更常见的治疗骨溶解症的方法。 (1)双膦酸盐:双膦酸盐是一种口服或注射药物,用于治疗骨质疏松症和与代谢性和转移性骨疾病相关的骨溶解症。作用机制主要是作用于破骨细胞,破骨细胞发生凋亡,从而抑制骨吸收,对成骨细胞功能也有一定效应。尽管双膦酸盐在减轻与假体植入相关的不良机械骨重建方面可能有一些效用,但双膦酸盐的使用对颗粒相关PPOL无太多效应[51]。针对双膦酸盐类药物的不良反应或不良后果,研究表明长时间应用双膦酸盐可能会导致食管癌、下颌骨坏死、心房颤动发生[52]。目前,对双膦酸盐类药物治疗PPOL的应用时间、最佳剂量、用药频率等还没有明确的共识,仍需大量的临床研究提供统计学证据。 (2)针对破骨细胞的治疗:RANKL是成骨细胞和其他细胞释放的一种蛋白,可激活破骨细胞表面的跨膜蛋白RANK。RANK调节破骨细胞活性和随后的骨吸收[53]。地诺单抗是RANKL的人单克隆抗体,可阻断RANKL与RANK结合,从而抑制破骨细胞活性和功能[54]。临床还开发了其他破骨细胞活性抑制剂,如活性组织蛋白酶K。尽管可能正在使用地诺单抗进行人体试验,但尚未报道其在微粒诱导人体骨质溶解情况下的疗效[55]。 (3)针对特定促炎细胞因子的治疗:巨噬细胞和其他细胞释放的物质通过增加巨噬细胞-异物巨细胞-破骨细胞谱系细胞的骨吸收,并降低间充质干细胞成骨细胞的增殖、分化和功能来刺激PPOL[56]。事实上,巨噬细胞是这个过程的重要细胞,巨噬细胞和其他细胞实现骨溶解的机制是通过在先天性免疫系统的保护下释放促炎性细胞因子、趋化因子、活性氧和其他物质,与先天性免疫相关的炎症过程通常对特定刺激无特异性,但似乎也存在先天性免疫系统的记忆[57]。此外,该系统是过度冗余的,因此抑制一个细胞因子通路不会显著影响整体后果。由于炎症途径的复杂性和干扰炎症(即感染)潜在的不良影响,人体内的研究尚未开展。 (4)针对炎症细胞因子上游过程的治疗:PPOL是磨损颗粒诱导的微环境的生物学结果,在这种微环境中,促炎细胞因子、趋化因子、活性氧物质和其他物质刺激细胞降解骨并抑制骨基质的形成过程[58]。由于炎症过程的整体冗余性,以及抑制单一细胞因子的无效性,人们提出了更上游的治疗方法来缓解骨溶解,包括干扰关键的促炎转录因子——核因子κB,可改变巨噬细胞的极化状态,从促炎症表型转变为抗炎表型,并抑制局部巨噬细胞的转运[15]。抑制核因子κB已经在体外和动物体内进行了报道[59],Toll样受体和有丝分裂原激活蛋白激酶似乎也是这个级联过程中的重要途径[60]。可能很难将这些策略转化至人类,虽然已在体外和体内完成了将巨噬细胞表型从M1促炎变为M2抗炎颗粒诱导的炎症[15],这种方法最好使用局部给药。巨噬细胞向炎症部位的迁移是由于对局部环境信号的反应释放了特定的趋化因子,体外和体内动物模型已经确定,巨噬细胞的耗竭或重要巨噬细胞通路如单核细胞趋化蛋白1- C-C趋化因子受体2轴的抑制可以抑制全身转运和骨溶解[61]。 (5)合成代谢疗法:甲状旁腺激素的1-34氨基酸部分 (1-34)是一种合成代谢物质,通过蛋白激酶A和β-连环蛋白途径增加骨形成,并增加RANK拮抗剂骨保护素的效应。这种药物是间歇性的,并被批准用于治疗绝经后骨质疏松症,可能会减轻颗粒物引起的骨溶解。重组骨保护素基因治疗在动物模型中也显示出抑制骨溶解的作用,但是这种治疗的副反应不会立即转化[62]。雷尼酸锶是颗粒诱导骨溶解的另一种潜在治疗方法,该药目前被批准用于治疗绝经后骨质疏松症,可刺激前成骨细胞增殖,抑制破骨细胞分化并增加破骨细胞凋亡[63]。 (6)细胞疗法:局部治疗性细胞输送可直接或间接影响骨溶解。自体骨移植是局部细胞治疗的一种形式,即骨移植复合物中的成骨细胞和其他细胞可以进行移植,调节炎症级联反应,并提供自分泌和旁分泌因子来支持骨愈合。巨噬细胞和间充质干细胞之间的相互作用是所有炎症性骨疾病和骨愈合过程中的一个持续过程[64]。事实上,局部输送间充质干细胞是许多器官系统急性和慢性炎症的一种假定治疗方法。 2.2.2 手术治疗 与人工假体的磨损颗粒和副产品相关的骨溶解被视为一种“外科疾病”[65]。换句话说,一旦从影像学上观察到骨溶解,人工假体的磨损将继续,因此PPOL将不可避免地进展,这些事件将危及全关节置换人工假体及其周围骨骼和软组织的寿命。手术的目的是纠正关节功能的衰退,并解决之前和正在进行的潜在骨丢失问题。虽然翻修手术的外科方面不是此文的重点,但作者将简要介绍手术方法。下面概述的方法适用于PPOL的全髋关节置换,虽然原理相似,但其他关节PPOL的手术方法会因解剖位置、结构、设计、功能和所用材料的不同而有所不同。 如果假体稳定(固定良好)、对线良好、功能正常,并且可以获得合适的组配式置换部件,那么翻修手术仅限于翻修关节承载面,并可能通过同种异体骨或骨副产物、骨移植替代品(如各种骨传导或骨诱导材料)、生物制剂(如骨形态发生蛋白2)或其组合重建骨丢失[66]。关于组配式部件部分翻修(例如仅聚乙烯内衬/股骨头置换)的结局是否优于整个部件翻修(例如髋关节置换的聚乙烯内衬和髋臼金属髋臼杯)存在争议。然而,当对整个部件进行翻修时,由于磨损副产物引起的慢性炎症反应,会出现额外的手术引发的骨丢失。因此,如果结果相同,通常首选最简单的方法,即仅更换内衬/股骨头,而不是对整个部件进行翻修;一旦通过翻修手术纠正了“磨损发生器”,溶骨区域可能发生骨化或停止其进展[67]。骨水泥型部件可能出现骨水泥裂纹和碎裂,导致大量骨内膜骨质溶解,甚至病理性骨折。在重新植入更长的带柄部件(通常是非骨水泥型)之前,通常使用延长的股骨截骨术切除所有碎屑和固定良好的丙烯酸骨水泥,对这些病例进行翻修。固定良好的非骨水泥型植入物可能由于有效关节间隙中聚乙烯碎屑的生物学反应而出现股骨近端骨溶 解[68],首先要处理关节面,如果股骨柄稳定,可能需要使用压碎的同种异体移植物对股骨近端进行骨移植。如果假体被破坏到假体或骨可能断裂或松动的程度,则需要进行翻修手术,以及通过松质骨移植重建丢失的骨[69];如果股骨近端骨量无法支撑传统假体,则可能需要骨肿瘤假体或结构性股骨同种异体移植物-假体复合体[69]。金属对金属植入物产生的副产品以及假体部件连接处发生金属腐蚀的情况可能导致骨溶解甚至大的假瘤,损害骨骼和软组织。对溶骨区和假瘤进行清创,并将组配式金属对金属关节面更换为其他关节面,通常是陶瓷对聚乙烯关节面。组配式连接处的腐蚀可能需要更换关节面(例如,在全髋关节置换中用陶瓷股骨头代替钴铬合金股骨头),或者如果严重影响股骨颈的结构完整性,甚至需要取出整个固定良好的部件。 "
| [1] 蒋营军,吴连国. 人工关节置换术后磨损颗粒与假体周围骨溶解的研究进展[J]. 中国骨伤,2016,29(10):968-972. [2] LIAO L, LIN Y, LIU Q, et al. Cepharanthine ameliorates titanium particle-induced osteolysis by inhibiting osteoclastogenesis and modulating OPG/RANKL ratio in a murine model. Biochem Biophys Res Commun. 2019;517(3):407-412. [3] DYSKOVA T, KRIEGOVA E, SLOBODOVA Z, et al. Inflammation time-axis in aseptic loosening of total knee arthroplasty: A preliminary study. PLoS One. 2019;14(8):e221056. [4] GALLO J, VACULOVA J, GOODMAN SB, et al. Contributions of human tissue analysis to understanding the mechanisms of loosening and osteolysis in total hip replacement. Acta Biomater. 2014;10(6): 2354-2366. [5] GÜLER-YÜKSEL M, HOES JN, BULTINK IEM, et al. Glucocorticoids, Inflammation and Bone. Calcif Tissue Int. 2018;102(5):592-606. [6] GOODMAN SB, GALLO J, GIBON E, et al. Diagnosis and management of implant debris-associated inflammation. Expert Rev Med Devices. 2020;17(1):41-56. [7] ZHAO B. Does TNF Promote or Restrain Osteoclastogenesis and Inflammatory Bone Resorption? Crit Rev Immunol. 2018;38(4): 253-261. [8] ZHENG W, GU X, HU D, et al. Co-culture with synovial tissue in patients with rheumatoid arthritis suppress cell proliferation by regulating MAPK pathway in osteoblasts. Am J Transl Res. 2019;11(6):3317-3327. [9] EL-ADAWI H, DENG L, TRAMONTANO A, et al. The functional role of the JAK-STAT pathway in post-infarction remodeling. Cardiovasc Res. 2003;57(1):129-138. [10] GONG T, LIU L, JIANG W, et al. DAMP-sensing receptors in sterile inflammation and inflammatory diseases. Nat Rev Immunol. 2020; 20(2):95-112. [11] MARLA JS, LAUREN JJ, JAVAD P, et al. The Role of Oxidative Stress in Aseptic Loosening of Total Hip Arthroplasties. J Arthroplasty. 2014; 29(4):843-849. [12] TAIWO SA, CHAEKYUN K. Reactive Oxygen Species in Osteoclast Differentiation and Possible Pharmaceutical Targets of ROS-Mediated Osteoclast Diseases. Int J Mol Sci. 2019;20(14):3576. [13] MARMOTTI A, MESSINA D, CYKOWSKA A, et al. Periprosthetic osteolysis: a narrative review. J Biol Regul Homeost Agents. 2020; 34(4 Suppl 3):405-417. [14] JAMSEN E, PAJARINEN J, LIN TH, et al. Effect of Aging on the Macrophage Response to Titanium Particles. J Orthop Res. 2020;38(2): 405-416. [15] JIANG J, JIA T, GONG W, et al. Macrophage Polarization in IL-10 Treatment of Particle-Induced Inflammation and Osteolysis. Am J Pathol. 2016;186(1):57-66. [16] 巩栋,甄平,王荣. 巨噬细胞极化在假体周围骨溶解中的作用:研究现状和进展[J]. 中国组织工程研究,2018,22(7):1120-1125. [17] CHRISTIANSEN RJ, MÜNCH HJ, BONEFELD CM, et al. Cytokine Profile in Patients with Aseptic Loosening of Total Hip Replacements and Its Relation to Metal Release and Metal Allergy. J Clin Med. 2019;8(8):1259. [18] VACULOVÁ J, HURNÍK P, GALLO J, et al. Immunohistochemical Detection of Mast and Dendritic Cells in Periprosthetic Tissues of Aseptically Loosened Total Prostheses. Acta Chir Orthop Traumatol Cech. 2018; 85(5):351-358. [19] JONITZ-HEINCKE A, LOCHNER K, SCHULZE C, et al. Contribution of human osteoblasts and macrophages to bone matrix degradationand proinflammatory cytokine release after exposure to abrasive endoprostheticwear particles. Mol Med Rep. 2016;14(2):1491-1500. [20] LIAO L, LIN Y, LIU Q, et al. Cepharanthine ameliorates titanium particle-induced osteolysis by inhibiting osteoclastogenesis and modulating OPG/RANKL ratio in a murine model. Biochem Biophys Res Commun. 2019;517(3):407-412. [21] KOEHLER MI, HARTMANN ES, SCHLUESSEL S, et al. Impact of Periprosthetic Fibroblast-Like Cells on Osteoclastogenesis in Co-Culture with Peripheral Blood Mononuclear Cells Varies Depending on Culture System. Int J Mol Sci. 2019;20(10):2583. [22] CHOVATIYA R, MEDZHITOV R. Stress, inflammation, and defense of homeostasis. Mol Cell. 2014;54(2):281-288. [23] DYSKOVA T, KRIEGOVA E, SLOBODOVA Z, et al. Inflammation time-axis in aseptic loosening of total knee arthroplasty: A preliminary study. PLoS One. 2019;14(8):e221056. [24] MISHRA PK, PALMA M, BUECHEL B, et al. Sterile particle-induced inflammation is mediated by macrophages releasing IL-33 through a Bruton’s tyrosine kinase-dependent pathway. Nat Mater. 2019;18(3): 289-297. [25] 刘国印,王瑞,赵建宁. MicroRNA在无菌性松动中的研究进展[J]. 中国骨伤,2014,27(3):232-236. [26] YUN Z, PENG HZ, WANG W, et al. A20 inhibits the release of inflammatory cytokines by suppressing the activation of the nuclear factor-kappa B pathway in osteoarthritic fibroblast-like synoviocytes. Biochem Biophys Res Commun. 2019;508(3):877-881. [27] MEDIERO A, WILDER T, SHAH L, et al. Adenosine A2A receptor (A2AR) stimulation modulates expression of semaphorins 4D and 3A, regulators of bone homeostasis. FASEB J. 2018;32(7):3487-3501. [28] YAN L, LU L, HU F, et al. Piceatannol attenuates RANKL-induced osteoclast differentiation and bone resorption by suppressing MAPK, NF-kappaB and AKT signalling pathways and promotes Caspase3-mediated apoptosis of mature osteoclasts. R Soc Open Sci. 2019;6(6): 190360. [29] PARK JH, LEE NK, LEE SY. Current Understanding of RANK Signaling in Osteoclast Differentiation and Maturation. Mol Cells. 2017;40(10): 706-713. [30] CHEN Y, AIKEN A, SAW S, et al. TIMP Loss Activates Metalloproteinase-TNFalpha-DKK1 Axis To Compromise Wnt Signaling and Bone Mass. J Bone Miner Res. 2019;34(1):182-194. [31] NIARAKIS A, GIANNOPOULOU E, SYGGELOS SA, et al. Effects of proteasome inhibitors on cytokines, metalloproteinases and their inhibitors and collagen type-I expression in periprosthetic tissues and fibroblasts from loose arthroplasty endoprostheses. Connect Tissue Res. 2019;60(6):555-570. [32] 李干,李奇. 金属对金属髋关节置换术后金属离子的影响及有关对策[J]. 中华关节外科杂志(电子版),2010,4(5):666-670. [33] YANG F, TANG J, DAI K, et al. Metallic wear debris collected from patients induces apoptosis in rat primary osteoblasts via reactive oxygen speciesmediated mitochondrial dysfunction and endoplasmic reticulum stress. Mol Med Rep. 2019;19(3):1629-1637. [34] 王东,顾建红,刘宗平. 组织蛋白酶K在骨吸收中的作用研究进展[J]. 动物医学进展,2014,35(6):114-116. [35] ARIAS CF, HERRERO MA, ECHEVERRI LF, et al. Bone remodeling: A tissue-level process emerging from cell-level molecular algorithms. PloS One. 2018;13(9):e204171. [36] VEIGL D, VAVŘÍK P, POKORNÝ D, et al. Comparison of in vivo characteristics of polyethylene wear particles produced by a metal and a ceramic femoral component in total knee replacement. Acta Chir Orthop Traumatol Cech. 2011;78(1):49-55. [37] TEO WZW, SCHALOCK PC. Metal Hypersensitivity Reactions to Orthopedic Implants. Dermatol Ther. 2017;7(1):53-64. [38] STATHOPOULOS IP, ANDRIANOPOULOS N, PASCHALOGLOU D, et al. Revision total knee arthroplasty due to bone cement and metal hypersensitivity. Arch Orthop Trauma Surg. 2017;137(2):267-271. [39] JONITZ-HEINCKE A, LOCHNER K, SCHULZE C, et al. Contribution of human osteoblasts and macrophages to bone matrix degradation and proinflammatory cytokine release after exposure to abrasive endoprosthetic wear particles. Mol Med Rep. 2016;14(2):1491-1500. [40] HOENDERS CS, HARMSEN MC, VAN LUYN MJ. The local inflammatory environment and microorganisms in “aseptic” loosening of hip prostheses. J Biomed Mater Res B Appl Biomater. 2008;86(1):291-301. [41] BECHTEL CP, GEBHART JJ, TATRO JM, et al. Particle-Induced Osteolysis Is Mediated by TIRAP/Mal in Vitro and in Vivo: Dependence on Adherent Pathogen-Associated Molecular Patterns. J Bone Joint Surg Am. 2016; 98(4):285-294. [42] 吴岳嵩,王志伟,徐卫东. 细菌生物膜与人工关节感染[J]. 中华关节外科杂志(电子版),2012,6(6):952-961. [43] POUDEROUX C, BECKER A, GOUTELLE S, et al. Subcutaneous suppressive antibiotic therapy for bone and joint infections: safety and outcome in a cohort of 10 patients. J Antimicrob Chemother. 2019; 74(7):2060-2064. [44] STUART BG, YRJO TK, MICHIAKI T. Joint Replacement Surgery and the Innate Immune System. J Long Term Eff Med Implants. 2014;24(4): 253-257. [45] LI FF, ZHANG B, CUI JH, et al. Alterations in betacatenin/Ecadherin complex formation during the mechanotransduction of Saos2 osteoblastic cells. Mol Med Rep. 2018;18(2):1495-1503. [46] TOMASZEWSKI PK, VAN DIEST M, BULSTRA SK, et al. Numerical analysis of an osseointegrated prosthesis fixation with reduced bone failure risk and periprosthetic bone loss. J Biomech. 2012;45(11):1875-1880. [47] BERGH MS, MUIR P, MARKEL MD, et al. Femoral bone adaptation to unstable long-term cemented total hip arthroplasty in dogs. Vet Surg. 2004;33(3):238-245. [48] NAM D, BOSTROM MP, FAHLGREN A. Emerging ideas: Instability-induced periprosthetic osteolysis is not dependent on the fibrous tissue interface. Clin Orthop Relat Res. 2013;471(6):1758-1762. [49] LIQIN X, JEFFREY MJ, EDNA SC, et al. Low-level mechanical vibrations can influence bone resorption and bone formation in the growing skeleton. Bone. 2006;39(5):1059-1066. [50] PAJARINEN J, GALLO J, TAKAGI M, et al. Particle disease really does exist. Acta Orthop. 2018;89(1):133-136. [51] WILKINSON JM, LITTLE DG. Bisphosphonates in orthopedic applications. Bone. 2011;49(1):95-102. [52] SALARI P, ABDOLLAHI M. Long term bisphosphonate use in osteoporotic patients; a step forward, two steps back. J Pharm Pharm Sci. 2012; 15(2):305-317. [53] PARK JH, LEE NK, LEE SY. Current Understanding of RANK Signaling in Osteoclast Differentiation and Maturation. Mol Cells. 2017;40(10): 706-713. [54] 张萌萌. Denosumab与破骨细胞RANKL/RANK通路[J]. 中国骨质疏松杂志,2019,25(3):385-387. [55] NYSTRÖM A, KIRITOPOULOS D, ULLMARK G, et al. Denosumab Prevents Early Periprosthetic Bone Loss After Uncemented Total Hip Arthroplasty: Results from a Randomized Placebo-Controlled Clinical Trial. J Bone Miner Res. 2020;35(2):239-247. [56] GALLO J, GOODMAN SB, KONTTINEN YT, et al. Particle disease: Biologic mechanisms of periprosthetic osteolysis in total hip arthroplasty. Innate Immun. 2013;19(2):213-224. [57] 彭锂,宋科官. 磨损颗粒诱导的假体周围骨溶解相关免疫学研究进展[J]. 医学研究杂志,2015,44(10):12-14. [58] LIN TH, TAMAKI Y, PAJARINEN J, et al. Chronic inflammation in biomaterial-induced periprosthetic osteolysis: NF-kappaB as a therapeutic target. Acta Biomater. 2014;10(1):1-10. [59] CLOHISY JC, HIRAYAMA T, FRAZIER E, et al. NF-kB signaling blockade abolishes implant particle-induced osteoclastogenesis. J Orthop Res. 2004;22(1):13-20. [60] JAMSEN E, KOURI VP, AINOLA M, et al. Correlations between macrophage polarizing cytokines, inflammatory mediators, osteoclast activity, and toll-like receptors in tissues around aseptically loosened hip implants. J Biomed Mater Res A. 2017;105(2):454-463. [61] REN W, MARKEL DC, SCHWENDENER R, et al. Macrophage depletion diminishes implant-wear-induced inflammatory osteolysis in a mouse model. J Biomed Mater Res A. 2008;85(4):1043-1051. [62] GOATER JJ, O’KEEFE RJ, ROSIER RN, et al. Efficacy of ex vivo OPG gene therapy in preventing wear debris induced osteolysis. J Orthop Res. 2002;20(2):169-173. [63] GENG T, SUN S, CHEN X, et al. Strontium ranelate reduces the progression of titanium particle-induced osteolysis by increasing the ratio of osteoprotegerin to receptor activator of nuclear factor-kappaB ligand in vivo. Mol Med Rep. 2018;17(3):3829-3836. [64] 张礼国,葛少华. 巨噬细胞对间充质干细胞成骨分化的作用及机制研究进展[J]. 口腔医学,2018,38(11):1026-1030. [65] BRIAN K, JOSEPH L, ZAIN S, et al. Osteolysis as it Pertains to Total Hip Arthroplasty. Orthop Clin North Am. 2018;49(4):419-435. [66] HALL A, EILERS M, HANSEN R, et al. Advances in acetabular reconstruction in revision total hip arthroplasty: maximizing function and outcomes after treatment of periacetabular osteolysis around the well-fixed shell. J Bone Joint Surg Am. 2013;95(18):1709-1718. [67] SHETH NP, ROZELL JC, PAPROSKY WG. Evaluation and Treatment of Patients With Acetabular Osteolysis After Total Hip Arthroplasty. J Am Acad Orthop Surg. 2019;27(6):e258-e267. [68] LACHIEWICZ PF, SOILEAU ES, MARTELL JM. Wear and Osteolysis of Highly Crosslinked Polyethylene at 10 to 14 Years: The Effect of Femoral Head Size. Clin Orthop Relat Res. 2016;474(2):365-371. [69] SHETH NP, NELSON CL, PAPROSKY WG. Femoral bone loss in revision total hip arthroplasty: evaluation and management. J Am Acad Orthop Surg. 2013;21(10):601-612. |
| [1] | Xue Yadong, Zhou Xinshe, Pei Lijia, Meng Fanyu, Li Jian, Wang Jinzi . Reconstruction of Paprosky III type acetabular defect by autogenous iliac bone block combined with titanium plate: providing a strong initial fixation for the prosthesis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1424-1428. |
| [2] | Zhuang Zhikun, Wu Rongkai, Lin Hanghui, Gong Zhibing, Zhang Qianjin, Wei Qiushi, Zhang Qingwen, Wu Zhaoke. Application of stable and enhanced lined hip joint system in total hip arthroplasty in elderly patients with femoral neck fractures complicated with hemiplegia [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1429-1433. |
| [3] | Zhang Lichuang, Xu Hao, Ma Yinghui, Xiong Mengting, Han Haihui, Bao Jiamin, Zhai Weitao, Liang Qianqian. Mechanism and prospects of regulating lymphatic reflux function in the treatment of rheumatoid arthritis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1459-1466. |
| [4] | Wang Jing, Xiong Shan, Cao Jin, Feng Linwei, Wang Xin. Role and mechanism of interleukin-3 in bone metabolism [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1260-1265. |
| [5] | Xiao Hao, Liu Jing, Zhou Jun. Research progress of pulsed electromagnetic field in the treatment of postmenopausal osteoporosis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1266-1271. |
| [6] | Huang Hao, Hong Song, Wa Qingde. Finite element analysis of the effect of femoral component rotation on patellofemoral joint contact pressure in total knee arthroplasty [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(6): 848-852. |
| [7] | Yuan Jing, Sun Xiaohu, Chen Hui, Qiao Yongjie, Wang Lixin. Digital measurement and analysis of the distal femur in adults with secondary knee valgus deformity [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(6): 881-885. |
| [8] | Zhou Jianguo, Liu Shiwei, Yuan Changhong, Bi Shengrong, Yang Guoping, Hu Weiquan, Liu Hui, Qian Rui. Total knee arthroplasty with posterior cruciate ligament retaining prosthesis in the treatment of knee osteoarthritis with knee valgus deformity [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(6): 892-897. |
| [9] | Huang Shibo, Xie Hui, Wang Zongpu, Wang Weidan, Qin Kairong, Zhao Dewei. Application of degradable high-purity magnesium screw in the treatment of developmental dysplasia of the hip [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 493-498. |
| [10] | Wang Jinzi, Ding Hai, Zhang Heng, Chang Wenju, Liu Fendou. Coverage of the acetabular cup under different perspective angles: assessing the position of the total hip arthroplasty prosthesis for complex types of hip dysplasia [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(3): 350-353. |
| [11] | Li Kai, Liu Zhendong, Li Xiaolei, Wang Jingcheng. Risk factors for recurrent prosthesis dislocation after total hip arthroplasty through posterolateral approach [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(3): 354-358. |
| [12] | Wang Chong, Zhang Meiying, Zhou Jian, Lao Kecheng. Early gait changes after total hip arthroplasty through direct anterior approach and posterolateral approach [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(3): 359-364. |
| [13] | Pan Hao, Zhao Huihui, Wang Jiangjing, Wang Feng, Wang Peng, Shi Qiuling, Guo Jin, Li Lin, Liu Guoqiang. Comparison of kinematic alignment and mechanical alignment to guide gait after total knee arthroplasty [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(3): 365-370. |
| [14] | Qu Pengfei, Wang Huisheng, Li Xi. Correlation between blood loss during primary total knee arthroplasty and hypoalbuminemia and hypocalcemia after arthroplasty [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(3): 376-382. |
| [15] | Liu Shaohua, Zhou Guanming, Chen Xicong, Xiao Keming, Cai Jian, Liu Xiaofang. Changes in kinematic parameters after unicompartmental knee arthroplasty and high tibial osteotomy [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(3): 390-396. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||