骨髓干细胞
-
图1|大鼠骨髓间充质干细胞的鉴定
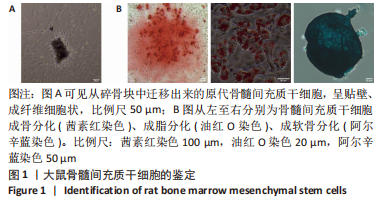
图2|大鼠施万细胞的鉴定
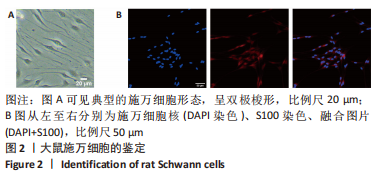
结果:BMSCs呈现典型的贴壁、成纤维细胞状,见图1A;同时成功诱导细胞三系分化,见图1B。施万细胞的典型细胞形态,见图2A;S100蛋白免疫荧光染色可见大多数施万细胞表达S100蛋白,见图2B。
图3|大鼠骨髓间充质干细胞(BMSCs)来源细胞外囊泡的鉴定
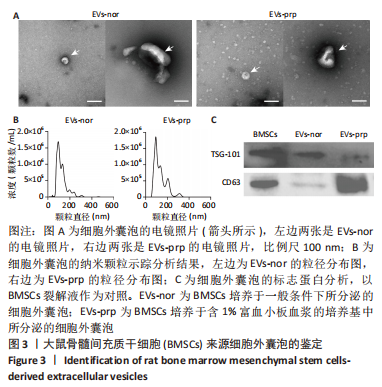
结果:EVs的鉴定结果见图3。图3A箭头所指即为EVs。为了显示EVs尺寸的异质性,该研究展示了小于100 nm和大于150 nm的EVs。EVs的纳米颗粒示踪分析结果见图3B,EVs-nor的粒径范围为(124.5±48.6) nm,EVs-prp的粒径范围为(130.6±55.8) nm。图3C可见EVs-nor和EVs-prp均表达有EVs的标志性蛋白TSG-101和CD63。
图4|骨髓间充质干细胞(BMSCs)来源细胞外囊泡对施万细胞重编程的效应
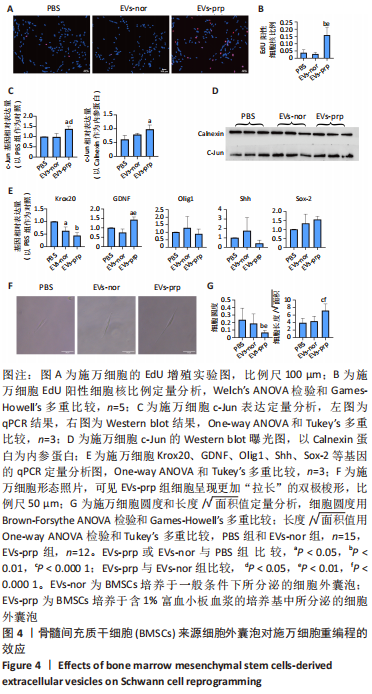
结果:对这些重编程特点的分析可以了解施万细胞的重编程状态。EdU细胞增殖实验结果见图4A,B。EVs-prp组EdU阳性细胞核比例显著高于PBS组和EVs-nor组(P < 0.01),且EVs-nor和PBS组之间没有显著差异,表明EVs-prp能够显著刺激施万细胞增殖。转录因子c-Jun的表达分析结果显示,EVs-prp能够刺激施万细胞 c-Jun表达,其基因和蛋白表达量显著高于PBS组(P < 0.05),同时基因表达量显著高于EVs-nor组(P < 0.05),见图4C,D。髓鞘化相关基因Krox20的 qPCR检测结果显示,与PBS组相比,EVs-nor和EVs-prp组Krox20表达均出现显著下调(EVs-nor,P < 0.05;EVs-prp,P < 0.01),EVs-nor和EVs-prp组之间无显著性差异;GDNF基因表达在EVs-prp组中上调,显著高于PBS组和EVs-nor组(PBS,P < 0.05;EVs-nor,P < 0.01),PBS组和EVs-nor组之间没有显著差异,见图4E。最后,施万细胞形态分析结果显示,EVs-prp组细胞的圆度显著低于PBS和EVs-nor组(PBS,P < 0.01;EVs-nor,P < 0.01),且细胞长度/√面积值显著高于PBS和EVs-nor组(PBS,P < 0.000 1;EVs-nor,P < 0.000 1),同时这2个值在PBS组和EVs-nor组之间没有显著差异,见图4F,G。这表明EVs-prp组细胞形态显著伸长。
图6|周围神经损伤修复的组织学评估结果
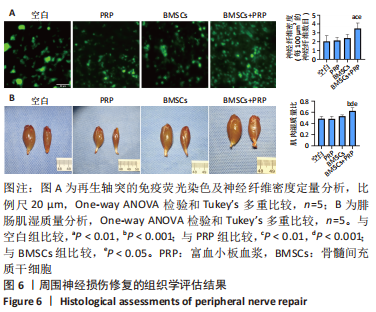
结果:神经纤维密度分析结果显示,BMSCs+PRP组神经纤维密度显著高于其他3组(空白组,P < 0.01;PRP组,P < 0.01;BMSCs组,P < 0.05),其他3组之间没有显著差异,见图6A。
腓肠肌湿质量分析结果显示,BMSCs+PRP组腓肠肌恢复情况最好,肌肉湿质量比显著高于其他3组(空白组,P < 0.001;PRP组,P < 0.001;BMSCs组,P < 0.05),其他3组之间没有显著差异,见图6B。