中国组织工程研究 ›› 2014, Vol. 18 ›› Issue (51): 8297-8300.doi: 10.3969/j.issn.2095-4344.2014.51.018
• 肌肉肌腱韧带组织构建 tissue construction of the muscle, tendon and ligament • 上一篇 下一篇
兔肌腱细胞的分离、培养及鉴定
王玉聪1,张前法2
- 1宁波市第九医院骨科,浙江省宁波市 315020;2上海市第一人民医院宝山分院骨科,上海市 200400
Isolation, culture and identification of rabbit tendon cells
Wang Yu-cong1, Zhang Qian-fa2
- 1Department of Orthopedics, Ninth People’s Hospital of Ningbo City, Ningbo 315020, Zhejiang Province, China; 2Department of Orthopedics, Baoshan Branch, First People’s Hospital of Shanghai, Shanghai 200400, China
摘要:
背景:肌腱细胞是一种高分化的细胞,其增殖相对缓慢,在体外经多次传代后甚至丧失增殖能力,因此有必要建立肌腱细胞良好的体外分离、培养模式。
目的:探讨兔肌腱细胞的分离、培养及鉴定。
方法:无菌条件下切取新西兰乳兔趾屈肌腱,显微镜下剥离腱外膜,采用Henderson分步酶消化法分离肌腱细胞,用含体积分数为20%胎牛血清的F-12培养液进行培养、传代。
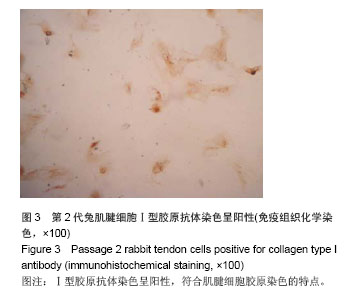
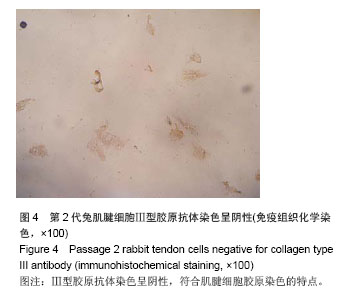
结果与结论:通过不同的酶消化分离可获得较纯肌腱细胞,体外培养细胞表现出良好的细胞增殖能力和传代能力。免疫组织化学染色见分离培养的第2代腱细胞Ⅰ型胶原抗体染色呈阳性,而Ⅲ型胶原抗体染色呈阴性,证明所获细胞为肌腱细胞。提示肌腱细胞能够在体外分离、扩增和传代。
中图分类号:


.jpg)