中国组织工程研究 ›› 2023, Vol. 27 ›› Issue (25): 3992-3998.doi: 10.12307/2023.550
• 药物控释材料 drug delivery materials • 上一篇 下一篇
淫羊藿苷联合可注射壳聚糖/胶原复合水凝胶对心肌梗死大鼠血管新生的作用
何文凤,薛 成,郑健康,帅 壮,岳荣川
- 川北医学院附属医院心内科,心血管疾病实验室,四川省南充市 637000
Effects of icariin combined with injectable chitosan/collagen composite hydrogel on angiogenesis in rats with myocardial infarction
He Wenfeng, Xue Cheng, Zheng Jiankang, Shuai Zhuang, Yue Rongchuan
- Department of Cardiology, Affiliated Hospital of North Sichuan Medical University, Cardiovascular Disease Laboratory, Nanchong 637000, Sichuan Province, China
摘要:
文题释义:
心肌梗死:是冠状动脉闭塞,血流中断,使部分心肌因严重的持久性缺血而发生局部坏死。临床上有剧烈而较持久的胸骨后疼痛、发热、白细胞增多、红细胞沉降率加快、血清心肌酶活力增高及进行性心电图变化,可发生心律失常、休克或心力衰竭。淫羊藿苷:是中药淫羊藿的有效单体成分之一,属于8-异戊烯基黄酮醇苷类化合物,能够改善心脑血管功能、血液流变学,促进造血功能,调节内分泌,促进成骨细胞的增殖与发育,增强免疫功能,抗肿瘤、抗衰老,具有广泛的药理作用。
背景:淫羊藿苷可用于心血管疾病的治疗,但是由于淫羊藿苷的脂溶性高、水溶性差、肝脏首过效应明显,导致其生物利用度较低,限制了其临床应用。
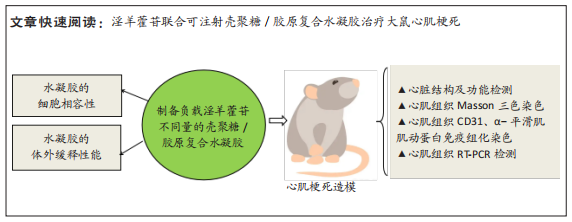
目的:将淫羊藿苷负载于壳聚糖/胶原复合水凝胶中,观察其治疗大鼠心肌梗死的效果。
方法:制备负载淫羊藿苷不同量(0.4,0.8,1.6 mg/mL)的壳聚糖/胶原复合水凝胶,分别记为CS/COI/ICA0.4、CS/COI/ICA0.8、CS/COI/ICA1.6,检测水凝胶的细胞相容性与体外缓释性能。取成年SD大鼠,结扎左冠状前支建立心肌梗死模型,将造模成功的96只大鼠随机4组治疗,模型对照组梗死区域、梗死区周围及后壁区域注射PBS,CS/COI/ICA0.4组、CS/COI/ICA0.8组、CS/COI/ICA1.6组梗死区域、梗死区周围及后壁区域分别注射对应的水凝胶,每组24只;同时选取造模外的24只大鼠作为正常对照。治疗28 d后检测相关指标。
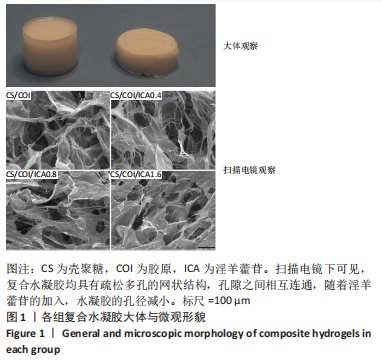
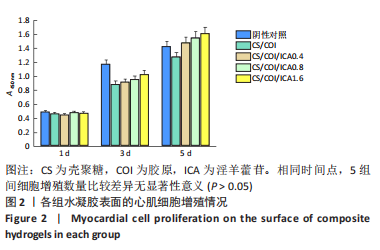
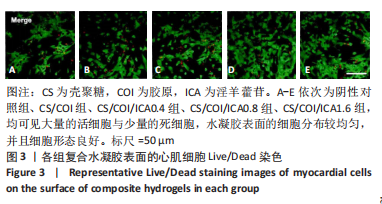
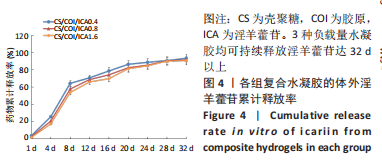
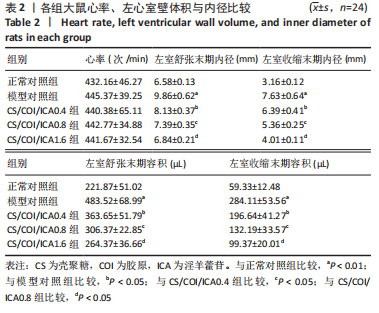
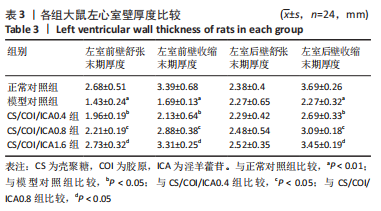
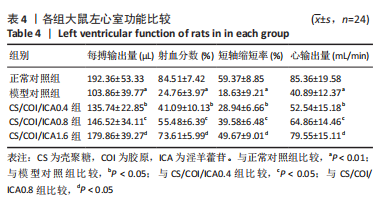
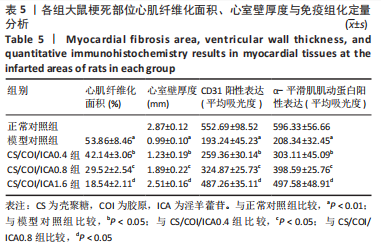
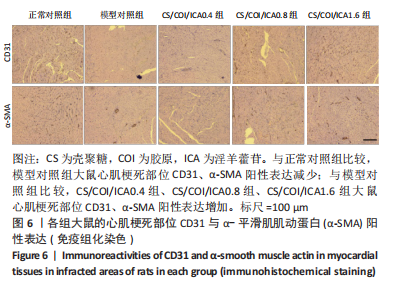
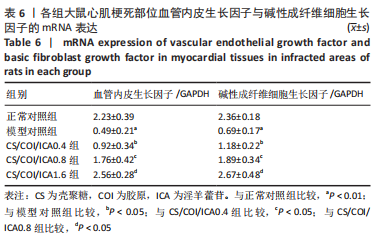
结果与结论:①体外细胞实验:负载淫羊藿苷不同量的壳聚糖/胶原复合水凝胶具有良好的细胞相容性,有利于心肌细胞的增殖与存活;3种负载量水凝胶均可持续释放淫羊藿苷达32 d以上。②动物实验:与正常对照组相比,模型对照组大鼠心脏结构发生严重重塑、心功能显著下降(P < 0.01);与模型对照组比较,各CS/COI/ICA组大鼠心脏结构、心功能均有明显改善(P < 0.05),其中以CS/COI/ICA1.6组改善最明显(P < 0.05)。Masson三色染色显示,各CS/COI/ICA组大鼠心肌组织纤维化程度显著轻于模型对照组(P < 0.05),心室壁厚度大于模型对照组(P < 0.05)。免疫组化染色显示,模型对照组大鼠心肌组织CD31、α-平滑肌肌动蛋白含量低于正常对照组(P < 0.05),各CS/COI/ICA组大鼠心肌组织CD31、α-平滑肌肌动蛋白含量高于模型对照组(P < 0.05)。RT-PCR检测显示,模型对照组心肌组织血管内皮生长因子、碱性成纤维细胞生长因子的mRNA表达量低于正常对照组(P < 0.05),各CS/COI/ICA组血管内皮生长因子、碱性成纤维细胞生长因子的mRNA表达量高于模型对照组(P < 0.05)。③结果表明,壳聚糖/胶原/淫羊藿苷复合水凝胶可能通过提升梗死部位血管内皮生长因子与碱性成纤维细胞生长因子的表达刺激血管新生,进而改善心肌组织有效灌注量不足的局部微环境,达到有效抑制心室重塑、改善心功能的治疗作用。
https://orcid.org/0000-0002-1173-8620(何文凤)
中国组织工程研究杂志出版内容重点:生物材料;骨生物材料;口腔生物材料;纳米材料;缓释材料;材料相容性;组织工程
中图分类号: