中国组织工程研究 ›› 2026, Vol. 30 ›› Issue (20): 5115-5124.doi: 10.12307/2026.343
• 组织工程口腔材料 tissue-engineered oral materials • 上一篇 下一篇
载唑来膦酸可溶性微针贴片抑制脂多糖诱导破骨细胞的分化
张 也1,安哲庆1,席 歆1,刘晓妍1,洪 伟2,廖 健1
- 1贵州医科大学口腔医学院/贵州医科大学附属口腔医院,贵州省贵阳市 550004;2贵州医科大学分子生物学重点实验室,贵州省贵阳市 550004
Zoledronic acid-loaded dissolvable microneedle patch inhibits lipopolysaccharide-induced osteoclast differentiation
Zhang Ye1, An Zheqing1, Xi Xin1, Liu Xiaoyan1, Hong Wei2, Liao Jian1
- 1School of Stomatology / Affiliated Stomatology Hospital, Guizhou Medical University, Guiyang 550004, Guizhou Province, China; 2Key Laboratory of Molecular Biology, Guizhou Medical University, Guiyang 550004, Guizhou Province, China
摘要:
文题释义:
可溶性微针贴片:由水溶性聚合物干燥成型制备而来,由数百个微米级针头组成的微针阵列,针头长度< 1 000 µm,能够有效刺穿角质层的同时避开与感觉神经接触,达到无痛微创透皮给药的目的。
破骨细胞:是骨吸收的主要功能细胞,起源于血系单核-巨噬细胞系统,具有多核的形态特征。破骨细胞的过度激活会导致骨吸收。
背景:唑来膦酸是治疗骨吸收的有效药物,但全身使用不良反应较大。可溶微针是一种高效的局部透皮给药方式,能够有效穿透黏膜屏障,局部递药以避免药物不良反应。
目的:制备载唑来膦酸的可溶性微针贴片,表征微针贴片的机械强度、穿透性以及对破骨细胞分化的影响。
方法:以聚乙烯醇溶液作为背衬基质溶液,以透明质酸溶液或含有不同质量浓度(1,5,10 mg/mL)唑来膦酸的透明质酸溶液作为微针针尖部基质溶液,通过两步浇筑法分别制备空白可溶性微针贴片与载唑来膦酸的可溶性微针贴片,表征微针的形貌、载药量。将载10 mg/mL唑来膦酸可溶性微针分别压入锡箔纸或猪牙龈组织中,评估微针的穿透能力;将载10 mg/mL唑来膦酸可溶性微针插入Parafilm M膜中,观察各层Parafilm M上微针穿透的孔洞,评估微针穿透深度。将载10 mg/mL唑来膦酸可溶性微针插入猪牙龈组织中,在不同时间点观察微针溶解情况。将空白可溶性微针浸提液、载1 mg/mL唑来膦酸可溶性微针浸提液分别与RAW264.7细胞共培养,通过CCK-8实验、活死染色检测微针的生物安全性。将RAW264.7细胞分3组培养:空白组不加入任何药物,脂多糖组加入100 ng/mL脂多糖(诱导破骨分化),唑来膦酸微针组同时加入100 ng/mL脂多糖与载1 mg/mL唑来膦酸可溶性微针浸提液,通过抗酒石酸酸性磷酸酶染色与RT-qPCR检测分析破骨细胞分化情况。
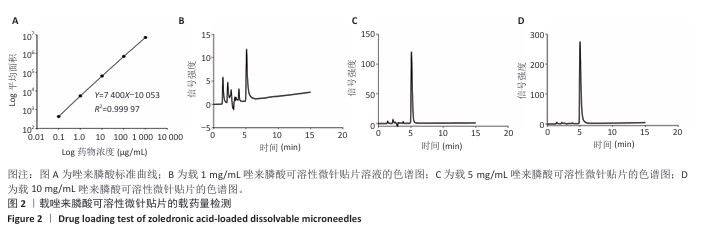
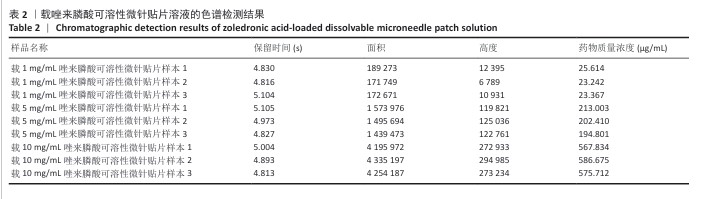
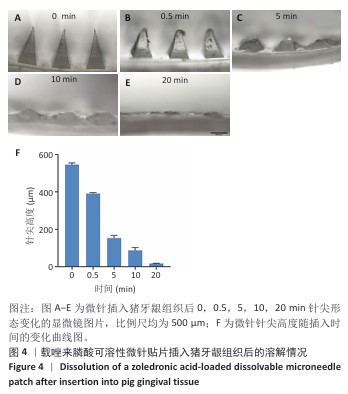
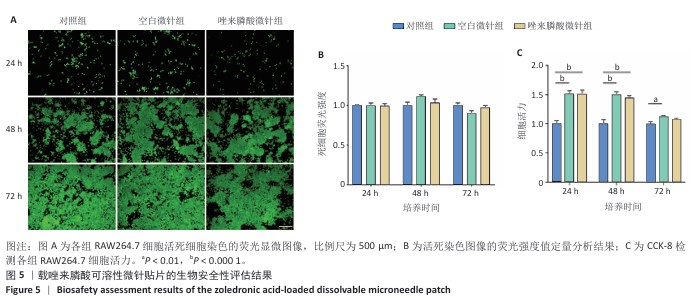
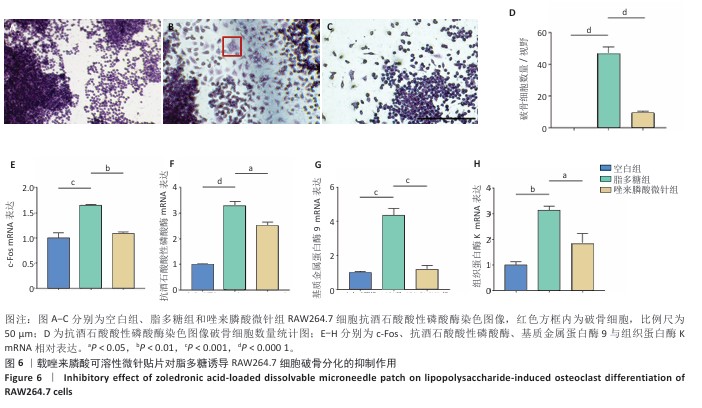
结果与结论:①普通光学显微镜下可见载唑来膦酸可溶性微针的结构均匀,针头锋利且整个针尖呈现良好的金字塔形态,与背衬结合紧密、无缺损和气泡,针尖高度约为595 µm,相邻针尖距离约495 µm。载1,5,10 mg/mL唑来膦酸可溶性微针的载药量分别为(24.07±1.33),(203.4±9.14),(576.74±9.46) µg,表明可以通过调节微针基质溶液中的药物浓度来控制微针的载药量。②将微针插入锡箔纸或猪牙龈组织后在组织表面形成有效的药物输送微孔,将微针插入Parafilm M膜后穿透深度大约为252 µm,说明微针具备足够的机械强度和组织穿透性能,能够穿透黏膜屏障形成有效微孔,输送药物到牙龈组织深部。③CCK-8实验、活死染色显示,空白可溶性微针、载唑来膦酸可溶性微针均无明显的细胞毒性。抗酒石酸酸性磷酸酶染色与RT-qPCR检测显示,脂多糖组破骨细胞数量及抗酒石酸酸性磷酸酶、c-Fos、基质金属蛋白酶9、组织蛋白酶K mRNA表达均高于空白组(P < 0.05),唑来膦酸微针组破骨细胞数量及抗酒石酸酸性磷酸酶、c-Fos、基质金属蛋白酶9、组织蛋白酶K mRNA表达均低于脂多糖组(P < 0.05)。表明在炎性状态下,载唑来膦酸可溶性微针可有效抑制破骨细胞的分化。
https://orcid.org/0009-0008-2244-1137 (张也)
中国组织工程研究杂志出版内容重点:生物材料;骨生物材料;口腔生物材料;纳米材料;缓释材料;材料相容性;组织工程
中图分类号: