Chinese Journal of Tissue Engineering Research ›› 2014, Vol. 18 ›› Issue (15): 2427-2433.doi: 10.3969/j.issn.2095-4344.2014.15.022
Previous Articles Next Articles
Vascularization for tissue engineering organs: research progress and application prospect
Zheng Xing-long 1, 2, Xiang Jun-xi 1, 2, Li Jian-hui 2, 3, Lv Yi 1, 2
- 1 Department of Hepatobiliary Surgery, First Affiliated Hospital of Xi’an Jiaotong University, Xi’an 710061, Shaanxi Province, China; 2 Research Institute of Advanced Surgical Technology and Engineering, Xi’an Jiaotong University, Xi’an 710061, Shaanxi Province, China; 3 Department of Surgical Oncology, Shaanxi Provincial People’s Hospital, Xi’an 710061, Shaanxi Province, China
-
Online:2014-04-09Published:2014-04-09 -
Contact:Lv Yi, Professor, Doctoral supervisor, Department of Hepatobiliary Surgery, First Affiliated Hospital of Xi’an Jiaotong University, Xi’an 710061, Shaanxi Province, China; Research Institute of Advanced Surgical Technology and Engineering, Xi’an Jiaotong University, Xi’an 710061, Shaanxi Province, China -
About author:Zheng Xing-long, Studying for master’s degree, Department of Hepatobiliary Surgery, First Affiliated Hospital of Xi’an Jiaotong University, Xi’an 710061, Shaanxi Province, China; Research Institute of Advanced Surgical Technology and Engineering, Xi’an Jiaotong University, Xi’an 710061, Shaanxi Province, China -
Supported by:Specialized Research Fund for the Doctoral Program of Higher Education, No. 20110201130009; International Cooperation Program of Science and Technology Development of Shaanxi Province, No. 2012KW-39-01
CLC Number:
Cite this article
Zheng Xing-long, Xiang Jun-xi, Li Jian-hui, Lv Yi. Vascularization for tissue engineering organs: research progress and application prospect[J]. Chinese Journal of Tissue Engineering Research, 2014, 18(15): 2427-2433.
share this article

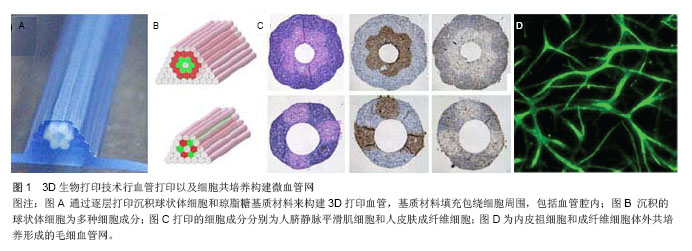
2.1 血管化在组织工程中的意义 体外构建的组织要在体内存活并发挥生物学功能,前提条件之一是能够获得充足的氧气和营养供应。然而,受体自发形成血管的速度很慢,仅限于每天十分之一微米,形成超过0.75 mm的完整血管需要几个星期时间[1]。而且,氧从血管到组织的弥散距离仅有200 μm[2],若缺少有效的血管网,体积超过2.0-3.0 mm3的组织植入体内后就无法获得足够营养,进行气体交换,排泄代谢产物[3]。从移植物表面到其深部,营养素及氧浓度呈现逐渐降低的过程,以致移植物中心可能出现坏死。因此,除外如皮肤、气管等对血供要求不高的组织,较厚的实质脏器如肝脏、肾脏等要实现体内的移植存活,构建充足有效的血管网系统是十分必要的。 然而,组织工程血管化仍面临诸多的难题。体外构建的血管主要是通过细胞共培养及复合生长因子的方式来实现的,且多数处于微血管网水平,无论从质量方面还是有效性方面均无法与体内形成的微血管网相媲美,这与血液中复杂的生物化学信号及血流的流体动力学影响有关[4]。要最终实现构建的组织运用于人体,所需的种子细胞要符合以下3点要求:①能够扩增一定数量的细胞数。②对受体免疫耐受。③尽量减少有创操作来获取细胞。另一个关键问题是如何将形成的毛细血管网与受体的大血管连接,形成有效动静脉结构。Tremblay等[5]将体外构建的含有微血管网的人造皮肤植入体内后发现移植物可在4 d内与受体的循环形成功能性连接,但是这种现象仅局限于相对较薄的组织,对于较厚的组织现尚无实验证明仅靠微血管网可以为移植物提供充足血供。Uygun等[6]给大鼠行左肾切除术,将大鼠再细胞化肝脏的门静脉和肝上下腔静脉分别与肾动脉和肾静脉连接,再细胞化肝脏在体内存活8 h,并可检测到白蛋白等反映肝脏合成功能的指标表达。但这种血管连接方式仅局限于实验阶段,要应用于临床需选择更为合适的移植部位和方式。 2.2 内皮细胞与血管化 2.2.1 内皮细胞的作用 体内所有的血管内壁均有内皮细胞附着,大血管的外层包有平滑肌细胞,其形态主要靠胶原和弹性蛋白等细胞外基质维持,微血管主要由内皮细胞组成。内皮细胞在体内具有多种重要的作用。它通过分泌促凝剂和纤维蛋白溶解成分维持血管内壁无血栓状态,通过活化纤维蛋白溶解酶原和尿激酶来平衡促凝和抗凝系统的相互作用。内皮细胞可以形成选择性渗透屏障,主动运输大分子物质通过血管壁。内皮细胞可以释放一些小分子物质作用于平滑肌细胞来调节血管张力,如释放一氧化氮和前列环素舒张血管,或是释放内皮缩血管肽收缩血管[7-8]。内皮细胞在血管壁黏附生长后,其相互作用所介导释放的细胞因子和基质蛋白对于血管的结构和功能有着重要的影响。内皮细胞由于具有选择性渗透屏障、防止血栓形成、调节血管压力和促进血管生成的特性[9],成为了血管化策略中备受关注的焦点。 2.2.2 内皮细胞的来源 不同组织来源的内皮细胞呈现出的生物学行为,在血管生成的潜能、血管张力和免疫耐受等方面存在着较大的差异,因此需要审慎地选择合适的种子细胞。 人脐静脉内皮细胞已经在体外血管化的研究中得到了广泛应用。它具有易获得、易体外提取、易扩增等优势,但是由其构建的血管稳定性较弱。Schechner等[10]和Zheng等[11]分别将人端粒酶逆转录酶和抗凋亡蛋白(Bcl-2)转染人脐静脉内皮细胞,试图增强其在体内的存活能力,并形成了类小动脉和小静脉,但是这些基因操作存在着致癌风险。 有研究者将人源的内皮细胞在胶原凝胶支架上培养,发现能自发形成毛细血管样结构。Levenberg等[12]利用成熟的内皮细胞和胚胎成纤维细胞在多孔的可降解支架上构建了工程化的骨骼肌组织,体内植入后成功存活。然而应用成熟的内皮细胞存在以下问题:①需要有创的分离过程。②相对较低的增殖能力。③单次活检较难取得有效数量的细胞。④体外培养过程中内皮细胞易受污染而影响细胞的表型和功能[13-14]。 胚胎干细胞具有干细胞分化的特性受到研究者们的关注,但出于伦理考虑和对其分化机制的不了解限制了临床应用。 内皮祖细胞是一类具有成熟内皮细胞特性的成体干细胞,其表面具有CD133,CD34和VEGFR-2三种特异性标志物[15-16]。内皮祖细胞主要存在于骨髓中,并能够释放到外周血。根据内皮祖细胞基本特征的差异,可将其分为两个亚群:早期内皮祖细胞(循环血管生成细胞)和晚期内皮祖细胞(内皮集落生成细胞)[17]。这两种细胞在组织内皮化的过程中均扮演重要角色。而且,已经证明早期内皮祖细胞可以通过分泌血管生成因子促进血管生成。晚期内皮祖细胞具有较高的增殖率,在新生血管的形成过程中扮演了直接的作用[18-19]。Finkenzeller等[17]研究证实晚期内皮祖细胞具有部分人脐静脉内皮细胞的能力,可以诱导形成基本的毛细血管和诱导萌发形成管腔样结构,而且这些细胞在体外具有同成熟内皮细胞一样的血管源性特征。近来,有研究证实单独将晚期内皮祖细胞植入体内并不能形成稳定的血管结构[20],但是如果将它同其他细胞共植入,如肌细胞,可以形成稳定的血管结构,并且可与受体循环形成功能性的连接[21],这提示了细胞共培养的重要作用。 2.2.3 内皮细胞共培养 研究发现内皮细胞需要与其他细胞(如周细胞、成纤维细胞等)共培养才能形成稳定的、具有功能的血管,单一的内皮细胞培养并不能形成成熟的血管或会较快退化。早期实验中研究者希望通过受体的血管系统原位萌发小血管,向植入的生物支架爬附来实现植入支架的血管化,但这种现象更多是出于受体对移植物的炎症反应。新生的血管主要是用来维持炎性细胞的趋化和代谢所需。由于这些血管缺乏维持血管结构的成分,易被白细胞侵蚀而失去血管形态。当炎症反应减弱后,血管开始退化,血流量减少,内皮细胞开始凋亡,只留下基底膜,可以作为将来再细胞化的空支架[22]。内皮细胞与成纤维细胞的细胞间接触及其产生的细胞外基质的相互作用,以及角蛋白细胞产生的血管内皮生长因子可以诱导产生毛细血管网结构[23]。Chen等[24]用人脐静脉内皮细胞和内皮祖细胞在体外分别与不同浓度的成纤维细胞共培养,形成毛细血管网,体内植入后发现仅四五天就能与受体形成功能性的血管连接,而且高浓度的成纤维细胞组较低浓度组构建的血管网更加完善。同样,血管平滑肌细胞也是重要的共培养细胞。Levenberg等[12]用人脐静脉内皮细胞与肌细胞、成纤维细胞共培养构建血管化的骨骼肌组织,其中,成纤维细胞促进内皮细胞形成管腔样结构,肌细胞在血管周围生长增殖以维持血管形态。Koike等[25]将间充质干细胞与内皮细胞共培养,间充质干细胞可以促进细胞外基质的分泌和稳定血管结构,形成的毛细血管存在分支样结构,并在体内发挥功能长达1年。这些实验结果均提示内皮细胞与其他细胞的共培养是促进血管化的有效途径。 2.3 血管化策略 基于种子细胞、支架材料和细胞共培养这3个组织工程的基本要素,出现了多种实现血管化的策略。其实,多数研究并非是单纯采用一种策略促进血管化的进程,更多的是联合几种不同的策略,彼此协同,以实现组织的血管化。 2.3.1 基于生长因子的策略 运用生长因子促进移植物内新生血管形成是最常用的策略。血管生长因子是诱发新生血管强有力的始动因子。它能激活并刺激内皮细胞沿其浓度梯度迁移生长,并且能够促进细胞聚集、血管形成及成熟。直接调节血管形成的血管生长因子包括:血管内皮生长因子、碱性成纤维细胞生长因子和肝细胞生长因子;间接调节的血管生长因子包括:血小板衍生生长因子、转化生长因子β和血管生成素[26]。为了避免生长因子局部的高浓度和保证其长时间维持一定浓度的释放,研究者通过包被生物可降解材料来实现生长因子的缓释过程,最大程度地模拟生理过程。Karal-Y?lmaz等[27]用聚乳酸-羟基乙酸共聚物包被的血管内皮生长因子纳米微粒放入含有人脐静脉内皮细胞的培养系统,测得血管内皮生长因子长期稳定的释放及人脐静脉内皮细胞的显著增殖和迁移。另一种策略是用基因修饰的手段转染细胞使其过表达血管生长因子。Geiger将转染了聚乳酸-羟基乙酸共聚物基因表达质粒的间充质干细胞分别与转染空质粒的间充质干细胞和单独使用聚乳酸-羟基乙酸共聚物的实验组作比较,发现前者在血管生成方面有着显著的优势。然而,单一的生长因子并不能有效诱导形成成熟的血管,可能会导致血管的瘘、出血等,且不同的生长因子在血管形成过程中的作用及作用时点不同,如血小板衍生生长因子会导致血管的去稳定性[28],血管生成素1可以促进内皮细胞的增殖及防止血管瘘的发生[29],因此除了添加周细胞等以产生细胞外支架稳定新血管外,联合序贯多种生长因子也是十分重要的[30]。Sun等[31]联合使用血管内皮生长因子、胰岛素样生长因子和趋化生长因子CXCL12在水凝胶支架上模拟新生血管的长入,其结果显示联合使用多种生长因子组在血管的数量和质量上均优于单独使用血管内皮生长因子组。 2.3.2 基于支架的策略 除了为细胞提供合适的定植环境,支架本身也可以促进工程化组织及器官的血管化进程。支架的结构和力学性能在促进体内血管生成和诱导受体微血管渗入方面扮演了十分重要的角色。细胞在平面培养体系中很容易去分化、丧失功能并且凋亡,这是因为细胞失去了细胞外基质分泌的调节因子、细胞间联系和复杂的信号转导,正常的生存微环境遭到破坏。因此,建立工程组织及器官的前提是需要提供一个三维的组织培养体系。 供三维培养的生物支架对材料的结构及性能有着特殊的要求:①具有良好的生物相容性和组织相容性。②材料具有三维立体多孔管道结构,合适的孔隙大小和孔隙率,以适应细胞集落生长、增殖的空间需求,为新陈代谢提供通道和空间,为预血管化和血管生成创造条件。③具有良好的生物可降解性和一定的力学性能,降解速度与细胞增殖速度匹配,降解产物无毒且不引起炎症反应。 无论是天然生物支架还是人工支架,它们都能为细胞的定植提供合适的3D细胞外基质,与2D培养相比,具有更加仿真的生物学结构。常用的人工高分子材料主要有:聚乳酸-羟基乙酸共聚物(Poly(Lactic-co-Glycolic Acid),PLGA)、聚乙酰内酯(poly-N-P-viny-benzyl-D-lactomide,PVLA)、聚ε-己内酯乙烷基乙烯基磷酸盐共聚物(poly(ε-caprolactone-co-ethyl ethylene phosphate),PCLEEP)、聚己酸内酯(polycaprolact one PCL)、聚-β-羟基丁酸(Poly-β-hydroxybutyric acid,PHB)等。采用高分子材料制成的人工支架,具有优良的机械性能、生物降解性可控、可加工性、成本低廉等优点,可使细胞聚集成三维状态,机械性能支撑良好,为细胞间输送营养物质和代谢产物的提供足够的空间。但细胞难以对其形成特异性黏附,其酸性降解产物也不利于细胞生长,且容易刺激局部组织产生炎症反应,具有一定的免疫原性,生物相容性不够理想。聚乳酸-羟基乙酸共聚物是目前研究和应用最广泛的可降解人工合成高分子材料,其结构以及亲、疏水性可通过两者含量的比例进行调节,从而决定支架材料降解速率,在体内最终代谢产物为CO2和H2O。Levenberg 等[32]利用可降解的PLLA/PLGA支架成功在体外将人源的胚胎干细胞分化为内皮细胞,并构建了毛细血管网,他还利用同样的支架构建了血管化的骨骼肌组织[12]。天然生物支架材料主要有胶原、壳聚糖、透明质酸、层黏连蛋白、丝素蛋白、海藻酸盐等,大多属于细胞外基质成分。这些材料普遍具有无毒、生物相容性良好、可参与组织的代谢过程等优势,但利用其制作的支架材料结构稳定性和机械性能较差,可加工性欠缺,这在一定程度上限制了天然生物材料的应用。胶原是一种比较常用天然的高分子材料,采用浸泡、高温、酸碱水解等多种方法从动物肌腱、韧带、骨骼等中提炼而来。它是一种良好的表面活性剂,生物可降解性良好,抗原性弱,组织相容性好,但其水溶液成凝胶状难以成型。Colette等曾用胶原制成的泡沫材料用于肝细胞培养。壳聚糖属于氨基多糖,是一种天然高分子聚合物,且价格低廉,物理性能良好,降解速度适中。水解后形成氨基葡萄糖,可被人体吸收,无免疫原性及毒性。在作为神经、肌腱、骨骼等器官的修复材料以及作为培养肾脏、肝脏等器官的支架材料的研究中都表现出较好的应用前景。Elcin等在构建人工肝脏时采用了壳聚糖作为支架材料,并将生长有肝细胞的壳聚糖材料移植于大鼠腹股沟内,结果发现经表皮生长因子诱导形成新生血管后,移植肝细胞存活时间大于2周,且形成了具有一定功能的类肝组织。 此外,通过综合高分子材料及天然生物材料的优缺点,将几种基质材料以适当的比例混合配比,最大限度的优化支架的生物相容性及力学性能,然后运用3D打印技术,将这些基质成分精确定位打印,构建出具有良好的孔隙率及高度仿真的支架结构。更有研究者利用3D打印技术个性化定制的优势,根据基质材料的不同特性(如降解速率不同或在不同温度条件下发生固态到液态的转换等),在打印支架的内部预留有微血管网结构,以便更快地实现血管化目标(图1)。David等运用3D生物打印技术,用40% Pluronic F127(EO-PO型聚醚) 来打印血管网络及塑型,GelMA(明胶丙烯酸甲酯)来承载及封装细胞,首先在常温下将Pluronic F127和GelMA生物墨水逐层打印,然后将整个结构冷却至4℃以使其中的Pluronic F127成分液化,留下相互连接的通道可提供所需的血管网络,最后在成型的血管网络中注射人脐静脉内皮细胞悬液以完成血管网络的内皮化。利用3D打印的方式构建微血管网,在一定程度上实现了高精确度的微观结构,但是仍无法与天然的血管网结构相比拟。 除外上述支架,另一种热点策略就是在运用脱细胞技术获得三维立体的细胞外基质支架的基础上,在支架上种植血管化相关的细胞或相应的实质细胞,联合生物反应器动态培养,从而构建血管化及功能化的组织器官。这种策略的明显优势是脱细胞支架材料保留了天然的血管网络基质结构,为动态组织培养和再血管化提供了极大的便利。同时,其所保留的细胞外基质成分由细胞生命活动的分泌产物组成,又产于构成细胞生存和功能表达的微环境,是细胞与生物体重要的组成成分,也为组织、器官提供力学支持和功能行使的途径,其中含有的各种生长因子对组织细胞生长、增殖起到促进作用,是一种天然的支架材料。2008年麻省总医院的 Ott研究小组首次报道了建立大鼠心脏脱细胞支架并构建体外组织工程心脏的研究[33],树立了组织工程领域脱细胞构建组织器官的里程碑。此后又陆续成功建立了肺脏[34]、肝脏等实质器官的脱细胞支架[6],并在此基础上构建了具有一定功能的组织工程器官,这不仅为构建组织工程器官开辟了新思路,同时也为血管化研究提供了新的策略。 2.3.3 体内预血管化 体内预血管化是指将未血管化或只含有细胞外基质的移植物植入体内富血供的区域,并与动静脉连接,靠受体细胞及微环境来实现移植物血管网的构建,最后将移植物从富血供区取出并重新植入到预定位置。与前两种策略相比,体内预血管化可以瞬时跟预定位置的血管形成功能性的灌注,但同时也存在几个问题:①需要几个星期才能实现最初的血管化,期间移植物要靠自然形成的血管维持组织的存活。②需要有植入、移除、再植入的过程。③需要对最初移植处的一段血管进行外科操作。这一策略已成功应用于气管、骨、骨骼肌等组织构建中,而且其应用领域已从小动物模型扩展到羊等大动物,并通过血管造影和CT三维重建实时监测血管化进程。Tanaka等[35]和Polykandriotis等[36]分别在动物模型中利用动静脉分流环预血管化皮肤和骨组织,取得了良好的效果。为了尽可能缩短最初移植期间移植物乏血供的时间,可通过对移植物支架进行生物化学的修饰或复合生长因子,以原位刺激血管的发生或细胞增殖。 2.3.4 诱导多能干细胞诱导分化 诱导多能干细胞是利用现代生物学技术使已经成熟的体细胞返回到胚胎干细胞的阶段。2006年,日本京都大学Shinya Yamanaka等利用Oct3/4,Sox2,c-Myc和Klf4这4种转录因子基因克隆入病毒载体,然后引入小鼠成纤维细胞,通过基因重新编程,获得在形态、增殖及分化潜能等方面与胚胎干细胞相似的细胞,即诱导多能干细胞。2007年,该小组又利用人成纤维细胞,通过相似的过程,同样获得诱导多能干细胞。这些研究成果为干细胞研究提供了新的思路。诱导多能干细胞可以取材于患者的成熟体细胞,来源广泛,同时避免伦理问题,并且具有较强的多向分化潜能和可自体移植等优点,被认为是最具临床应用前景的干细胞。 目前已经有研究报道运用诱导多能干细胞重建脱细胞心脏并实现再生心脏的电生理活动和自发收缩[37],以及运用诱导多能干细胞分化获得的角蛋白细胞和表皮成纤维细胞构建3D皮肤来治疗皮肤病[38]。诱导多能干细胞不仅在构建工程化组织领域发挥越来越核心的作用,而且在血管化研究方面也日益展现出令人期待的潜能。Samuel等[39]利用人诱导多能干细胞分化而来的内皮细胞在小鼠体内构建了稳定、具有功能性的血管网,且时间长达280 d;与此同时,该小组利用人诱导多能干细胞分化来的内皮前体细胞和间质前体细胞在小鼠体内构建了相同的血管网结构。这一结果证实了人自体的诱导多能干细胞分化的血管前体细胞可以有效地在体内构建稳定的血管结构,也为诱导多能干细胞促进组织工程血管化和治疗血管性疾病提供了有力的依据。Takebe等[40]将诱导多能干细胞分化而来的肝内胚层细胞与人脐静脉内皮细胞和间充质干细胞体外共培养,形成类器官样的肝胚组织,植入裸鼠头部后意外的发现这些细胞自发的形了三维的类肝样组织,且仅在48 h内就与受体形成功能性连接,其中间充质干细胞提供了支撑结构,人脐静脉内皮细胞衍生出疏松的血管网,这样的微环境进一步促进了肝内胚层细胞向肝细胞的分化成熟。形成的肝胚组织可以发挥正常的白蛋白分泌、药物代谢等肝脏功能,将其移植于肠系膜后可以逆转药物诱导的肝衰竭。鉴于脱细胞支架并不能很好的解决与受体血管连接的问题,相比之下,通过诱导多能干细胞联合其他干细胞诱导分化,自发形成与受体有血管连接的类器官有望成为未来组织工程血管化研究的新策略[41]。 "
| [1]Jain RK, Au P, Tam J,et al.Engineering vascularized tissue.Nat Biotechnol. 2005;23(7):821-823. [2]Kannan RY, Salacinski HJ, Sales K,et al.The roles of tissue engineering and vascularisation in the development of micro- vascular networks: a review.Biomaterials. 2005;26(14):1857- 1875. [3]Shieh SJ, Vacanti JP.State-of-the-art tissue engineering: from tissue engineering to organ building.Surgery. 2005;137(1): 1-7. [4]Borges J, Mueller MC, Padron NT,et al.Engineered adipose tissue supplied by functional microvessels.Tissue Eng. 2003; 9(6):1263-1270. [5]Tremblay PL, Hudon V, Berthod F,et al.Inosculation of tissue-engineered capillaries with the host's vasculature in a reconstructed skin transplanted on mice.Am J Transplant. 2005;5(5):1002-1010. [6]Uygun BE, Soto-Gutierrez A, Yagi H,et al.Organ reengineering through development of a transplantable recellularized liver graft using decellularized liver matrix.Nat Med. 2010;16(7):814-820. [7]Cunningham KS, Gotlieb AI.The role of shear stress in the pathogenesis of atherosclerosis.Lab Invest. 2005;85(1): 9-23. [8]Li YS, Haga JH, Chien S.Molecular basis of the effects of shear stress on vascular endothelial cells.J Biomech. 2005; 38(10):1949-1971. [9]Novosel EC, Kleinhans C, Kluger PJ.Vascularization is the key challenge in tissue engineering.Adv Drug Deliv Rev. 2011;63(4-5):300-311. [10]Schechner JS, Nath AK, Zheng L,et al.In vivo formation of complex microvessels lined by human endothelial cells in an immunodeficient mouse.Proc Natl Acad Sci U S A. 2000; 97(16):9191-9196. [11]Zheng L, Dengler TJ, Kluger MS,et al.Cytoprotection of human umbilical vein endothelial cells against apoptosis and CTL-mediated lysis provided by caspase-resistant Bcl-2 without alterations in growth or activation responses.J Immunol. 2000;164(9):4665-4671. [12]Levenberg S, Rouwkema J, Macdonald M,et al.Engineering vascularized skeletal muscle tissue.Nat Biotechnol. 2005; 23(7):879-884. [13]Brey EM, Greisler HP.Telomerase expression in somatic cells.Lancet. 2005;365(9477):2068-2069. [14]Torensma R.Blood vessels engineered from human cells.Lancet. 2005;366(9489):892-893. [15]Asahara T, Murohara T, Sullivan A,et al.Isolation of putative progenitor endothelial cells for angiogenesis.Science. 1997; 275(5302):964-967. [16]Hristov M, Erl W, Weber PC.Endothelial progenitor cells: mobilization, differentiation, and homing.Arterioscler Thromb Vasc Biol. 2003;23(7):1185-1189. [17]Finkenzeller G, Torio-Padron N, Momeni A,et al.In vitro angiogenesis properties of endothelial progenitor cells: a promising tool for vascularization of ex vivo engineered tissues.Tissue Eng. 2007;13(7):1413-1420. [18]Hur J, Yoon CH, Kim HS,et al.Characterization of two types of endothelial progenitor cells and their different contributions to neovasculogenesis.Arterioscler Thromb Vasc Biol. 2004;24(2): 288-293. [19]Schatteman GC, Dunnwald M, Jiao C.Biology of bone marrow-derived endothelial cell precursors.Am J Physiol Heart Circ Physiol. 2007;292(1):H1-18. [20]Finkenzeller G, Graner S, Kirkpatrick CJ,et al.Impaired in vivo vasculogenic potential of endothelial progenitor cells in comparison to human umbilical vein endothelial cells in a spheroid-based implantation model.Cell Prolif. 2009;42(4): 498-505. [21]Au P, Daheron LM, Duda DG,et al.Differential in vivo potential of endothelial progenitor cells from human umbilical cord blood and adult peripheral blood to form functional long-lasting vessels.Blood. 2008;111(3):1302-1305. [22]Baffert F, Le T, Sennino B,et al.Cellular changes in normal blood capillaries undergoing regression after inhibition of VEGF signaling.Am J Physiol Heart Circ Physiol. 2006; 290(2):H547-559. [23]Black AF, Berthod F, L'heureux N,et al.In vitro reconstruction of a human capillary-like network in a tissue-engineered skin equivalent.FASEB J. 1998;12(13):1331-1340. [24]Chen X, Aledia AS, Popson SA,et al.Rapid anastomosis of endothelial progenitor cell-derived vessels with host vasculature is promoted by a high density of cotransplanted fibroblasts.Tissue Eng Part A. 2010;16(2):585-594. [25]Koike N, Fukumura D, Gralla O,et al.Tissue engineering: creation of long-lasting blood vessels.Nature. 2004;428 (6979):138-139. [26]Nomi M, Miyake H, Sugita Y,et al.Role of growth factors and endothelial cells in therapeutic angiogenesis and tissue engineering.Curr Stem Cell Res Ther. 2006;1(3):333-343. [27]Karal-Y?lmaz O, Serhatl? M, Baysal K,et al.Preparation and in vitro characterization of vascular endothelial growth factor (VEGF)-loaded poly(D,L-lactic-co-glycolic acid) microspheres using a double emulsion/solvent evaporation technique.J Microencapsul. 2011;28(1):46-54. [28]Andrae J, Gallini R, Betsholtz C.Role of platelet-derived growth factors in physiology and medicine.Genes Dev. 2008;22(10):1276-1312. [29]Perets A, Baruch Y, Weisbuch F,et al.Enhancing the vascularization of three-dimensional porous alginate scaffolds by incorporating controlled release basic fibroblast growth factor microspheres.J Biomed Mater Res A. 2003;65(4):489- 497. [30]Zisch AH, Lutolf MP, Hubbell JA.Biopolymeric delivery matrices for angiogenic growth factors.Cardiovasc Pathol. 2003;12(6):295-310. [31]Sun G, Shen YI, Kusuma S,et al.Functional neovascularization of biodegradable dextran hydrogels with multiple angiogenic growth factors.Biomaterials. 2011;32(1): 95-106. [32]Levenberg S, Golub JS, Amit M,et al. Endothelial cells derived from human embryonic stem cells.Proc Natl Acad Sci U S A. 2002;99(7):4391-4396. [33]Ott HC, Matthiesen TS, Goh SK,et al.Perfusion-decellularized matrix: using nature's platform to engineer a bioartificial heart. Nat Med. 2008;14(2):213-221. [34]Ott HC, Clippinger B, Conrad C,et al.Regeneration and orthotopic transplantation of a bioartificial lung.Nat Med. 2010; 16(8):927-933. [35]Tanaka Y, Tsutsumi A, Crowe DM,et al.Generation of an autologous tissue (matrix) flap by combining an arteriovenous shunt loop with artificial skin in rats: preliminary report.Br J Plast Surg. 2000;53(1):51-57. [36]Polykandriotis E, Arkudas A, Beier JP,et al.Intrinsic axial vascularization of an osteoconductive bone matrix by means of an arteriovenous vascular bundle.Plast Reconstr Surg. 2007; 120(4):855-868. [37]Lu TY, Lin B, Kim J,et al.Repopulation of decellularized mouse heart with human induced pluripotent stem cell-derived cardiovascular progenitor cells.Nat Commun. 2013;4:2307. [38]Itoh M, Umegaki-Arao N, Guo Z,et al.Generation of 3D skin equivalents fully reconstituted from human induced pluripotent stem cells (iPSCs).PLoS One. 2013;8(10):e77673. [39]Samuel R, Daheron L, Liao S,et al.Generation of functionally competent and durable engineered blood vessels from human induced pluripotent stem cells.Proc Natl Acad Sci U S A. 2013;110(31):12774-12779. [40]Takebe T, Sekine K, Enomura M,et al.Vascularized and functional human liver from an iPSC-derived organ bud transplant.Nature. 2013;499(7459):481-484. [41]Willenbring H, Soto-Gutierrez A.Transplantable liver organoids made from only three ingredients.Cell Stem Cell. 2013;13(2):139-140. |
| [1] | Pu Rui, Chen Ziyang, Yuan Lingyan. Characteristics and effects of exosomes from different cell sources in cardioprotection [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 1-. |
| [2] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [3] | Zeng Yanhua, Hao Yanlei. In vitro culture and purification of Schwann cells: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1135-1141. |
| [4] | Jiang Xin, Qiao Liangwei, Sun Dong, Li Ming, Fang Jun, Qu Qingshan. Expression of long chain non-coding RNA PGM5-AS1 in serum of renal transplant patients and its regulation of human glomerular endothelial cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 741-745. |
| [5] | Xu Dongzi, Zhang Ting, Ouyang Zhaolian. The global competitive situation of cardiac tissue engineering based on patent analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 807-812. |
| [6] | Wu Zijian, Hu Zhaoduan, Xie Youqiong, Wang Feng, Li Jia, Li Bocun, Cai Guowei, Peng Rui. Three-dimensional printing technology and bone tissue engineering research: literature metrology and visual analysis of research hotspots [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 564-569. |
| [7] | Chang Wenliao, Zhao Jie, Sun Xiaoliang, Wang Kun, Wu Guofeng, Zhou Jian, Li Shuxiang, Sun Han. Material selection, theoretical design and biomimetic function of artificial periosteum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 600-606. |
| [8] | Liu Fei, Cui Yutao, Liu He. Advantages and problems of local antibiotic delivery system in the treatment of osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 614-620. |
| [9] | Li Xiaozhuang, Duan Hao, Wang Weizhou, Tang Zhihong, Wang Yanghao, He Fei. Application of bone tissue engineering materials in the treatment of bone defect diseases in vivo [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 626-631. |
| [10] | Zhang Zhenkun, Li Zhe, Li Ya, Wang Yingying, Wang Yaping, Zhou Xinkui, Ma Shanshan, Guan Fangxia. Application of alginate based hydrogels/dressings in wound healing: sustained, dynamic and sequential release [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 638-643. |
| [11] | Chen Jiana, Qiu Yanling, Nie Minhai, Liu Xuqian. Tissue engineering scaffolds in repairing oral and maxillofacial soft tissue defects [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 644-650. |
| [12] | Xing Hao, Zhang Yonghong, Wang Dong. Advantages and disadvantages of repairing large-segment bone defect [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 426-430. |
| [13] | Jiang Tao, Ma Lei, Li Zhiqiang, Shou Xi, Duan Mingjun, Wu Shuo, Ma Chuang, Wei Qin. Platelet-derived growth factor BB induces bone marrow mesenchymal stem cells to differentiate into vascular endothelial cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(25): 3937-3942. |
| [14] | Liu Chang, Li Datong, Liu Yuan, Kong Lingbo, Guo Rui, Yang Lixue, Hao Dingjun, He Baorong. Poor efficacy after vertebral augmentation surgery of acute symptomatic thoracolumbar osteoporotic compression fracture: relationship with bone cement, bone mineral density, and adjacent fractures [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3510-3516. |
| [15] | Chen Siqi, Xian Debin, Xu Rongsheng, Qin Zhongjie, Zhang Lei, Xia Delin. Effects of bone marrow mesenchymal stem cells and human umbilical vein endothelial cells combined with hydroxyapatite-tricalcium phosphate scaffolds on early angiogenesis in skull defect repair in rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3458-3465. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||