Chinese Journal of Tissue Engineering Research ›› 2023, Vol. 27 ›› Issue (21): 3382-3390.doi: 10.12307/2023.458
Previous Articles Next Articles
Potential of collagen peptide to improve skin and the countermeasures to improve its bioavailability
Bai Lei1, 2, Wang Yang1, 2, Tian Xiaojing1, 2, Wang Wenhang1, 2
- 1College of Food Science and Technology, Tianjin University of Science and Technology, Tianjin 300457, China; 2Research & Development Center of Collagen Products, Xingjia Biotechnology Co., Ltd., Tianjin 300457, China
-
Received:2022-06-27Accepted:2022-07-30Online:2023-07-28Published:2022-11-24 -
Contact:Wang Wenhang, MD, Researcher, College of Food Science and Technology, Tianjin University of Science and Technology, Tianjin 300457, China; Research & Development Center of Collagen Products, Xingjia Biotechnology Co., Ltd., Tianjin 300457, China -
About author:Bai Lei, Master candidate, College of Food Science and Technology, Tianjin University of Science and Technology, Tianjin 300457, China; Research & Development Center of Collagen Products, Xingjia Biotechnology Co., Ltd., Tianjin 300457, China -
Supported by:General Program of National Natural Science Foundation of China, No. 32172249 (to WWH); Tianjin Synthetic Biotechnology Innovation Capability Improvement Action Special Program, No. TSBICIP-KJGG-004 (to WWH)
CLC Number:
Cite this article
Bai Lei, Wang Yang, Tian Xiaojing, Wang Wenhang. Potential of collagen peptide to improve skin and the countermeasures to improve its bioavailability[J]. Chinese Journal of Tissue Engineering Research, 2023, 27(21): 3382-3390.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
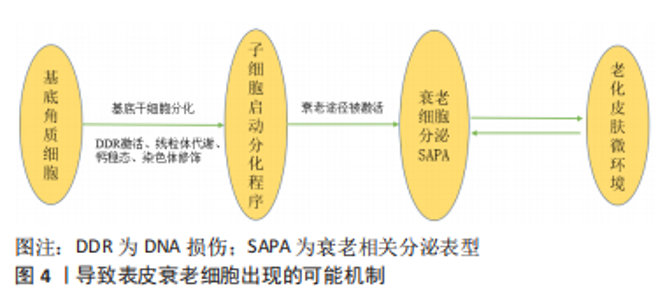
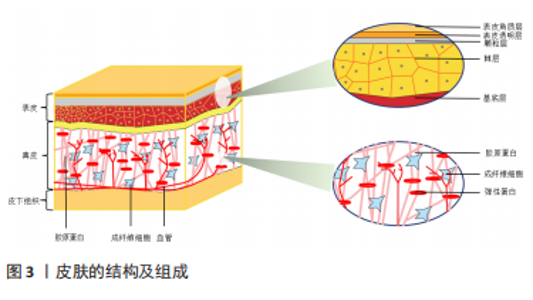
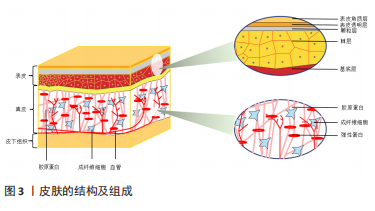
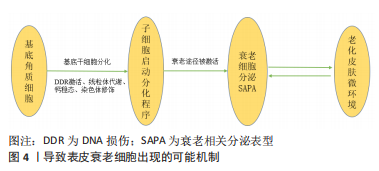
表皮作为最外层屏障,由基底层、棘层、颗粒层和角质层组成;胶原蛋白、弹性蛋白和透明质酸构成了真皮的基本成分,赋予皮肤结构、弹性和紧致度;而由脂肪细胞和较大的淋巴管和血管组成的皮下组织建立了皮肤与身体下层组织(如肌肉和骨骼)之间的联系,为组织提供保护、维持机械完整性并支持皮肤内血管和神经信号的传导。Ⅰ型胶原蛋白是皮肤、骨骼、肌腱和其他非软骨组织的主要蛋白成分[3],在年轻人群的皮肤中可达到80%[10]。其他类型的胶原蛋白含量相对较低,也发挥着提高胶原纤维直径和性质的作用[11]。儿童的皮肤以Ⅲ型胶原为主,它是一种纤维较少、富有弹性的胶原,随着年龄增长,Ⅲ型胶原逐渐被Ⅰ型胶原取代。 生理年龄的增加、生存环境的变化以及工作生活压力均会诱导皮肤表皮增厚,并导致细胞外基质(extracellular matrix,ECM)化合物水平降低,从而导致皮肤功能障碍,即老化,表现为弹性下降、粗糙干燥、皱纹形成和下垂[12]。皮肤老化可分为内在老化和外在老化。遗传变异、机体代谢和激素水平都可引起皮肤内在老化,使胶原纤维增厚、缩短、Ⅰ型胶原丧失,胶原蛋白类型比例发生改变。据估计,随着年龄的增长,机体补充胶原蛋白的能力每年降低1.5%[10]。外在老化主要由不良环境因素导致,例如:紫外线会导致皮肤粗糙干燥,皱纹多且深,主要表现为出现可见的血管、色素沉着和皮肤弹性下降[13];同时,真皮表皮交界处变平,皮肤完整性丧失和皱纹增多,黑色素细胞功能失调,色素沉着发生改变。表皮细胞的衰老受多种因素的影响,包括活性氧(reactive oxygen species,ROS)介导的DNA损伤(DNA damage response,DDR)、线粒体代谢、钙稳态和染色体修饰等[14-15],见图4。"
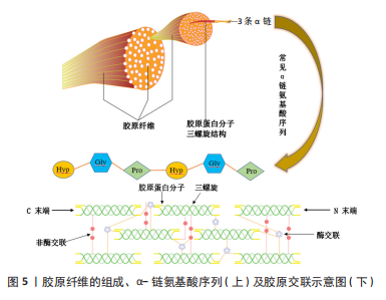
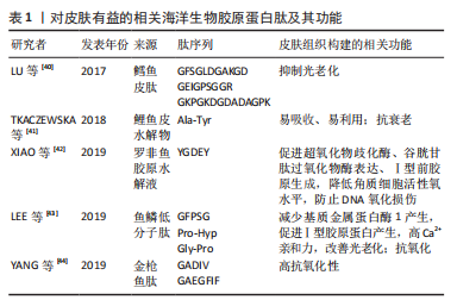
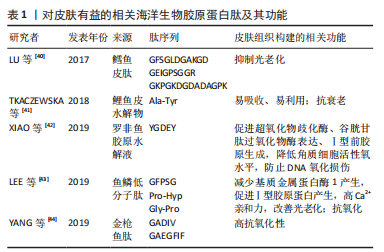
在光老化发生时,大量的活性氧会诱导分子破坏,从而使分子丧失生物学功能[16],活性氧增多也会导致表皮增生、跨细胞失水、Ca2+内流以及细胞外基质降解,同时激活丝裂原活化蛋白激酶(mitogen activated protein kinase,MAPK)——位于细胞膜上的丝氨酸/苏氨酸蛋白激酶受体,将细胞外信号传输到细胞质和细胞核中,与细胞增殖、凋亡调控和炎症反应等多种生命活动有关,如抑制胶原合成并提高基质金属蛋白酶(matrix metalloproteinases,MMPs)活性[17]。 细胞衰老是一个复杂的、动态的和高度营养化的过程[18],均衡饮食和摄入功能性因子可消除皮肤中由于自然衰老、紫外线引起的自由基,从而维持肌肤正常代谢、延缓皮肤老化。 2.2 胶原蛋白肽的组成与来源 胶原蛋白肽是由天然胶原蛋白或明胶水解而成的小分子生物活性肽。胶原蛋白由3条α链组成,形成三股螺旋结构,螺旋的长度以及非螺旋部分的大小和性质因类型而异,具有一定的机械强度和保湿作用。胶原蛋白分子通过共价交联形成胶原纤维,见图5。"
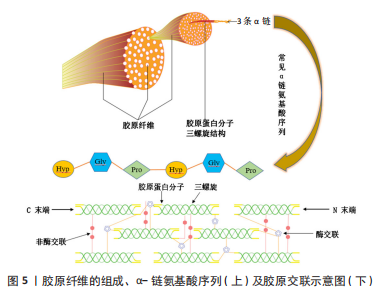
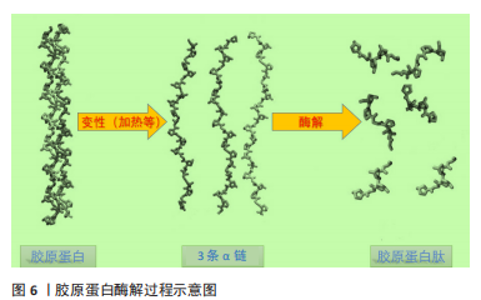
纤维型胶原蛋白(即能够形成纤维的胶原蛋白)包括Ⅰ,Ⅱ,Ⅲ,Ⅴ和Ⅺ型胶原蛋白,其α链由螺旋结构域、N端肽和C端肽组成,约占总胶原蛋白的90%,而非纤维胶原蛋白中的α链则包括三螺旋和非三螺旋结构域。胶原蛋白家族多样性主要由几种氨基酸数目不同的α链所决定。Ⅰ型胶原主要由2种类型的α链[2条α1(Ⅰ)和一条α2(Ⅰ)]构成,作为支架支撑皮肤结构。而Ⅲ型为含有3条α1链的同源三聚体,常与Ⅰ型胶原紧密结合形成富含Ⅰ型胶原的杂化胶原纤维,以增加组织的柔韧性和扩张性。胶原蛋白是由Gly-X-Y氨基酸重复序列形成的螺旋结构域,其中X常为Pro,Y常为Hyp,Gly-Pro-Hyp等标志性肽段常用于护肤研究。胶原蛋白合成中,存在转录翻译和胞内转译后修饰,后者包括前胶原α链的合成、羟基化、糖基化和交联。除重复序列外,每条α链的螺旋端部都有一个通常由赖氨酸及羟赖氨酸组成的非螺旋末端肽,该末端肽在前胶原链转换为胶原蛋白过程中被切除,其结构域有助于分子间相互作用并利于正常的纤维组装。胶原蛋白肽的不同氨基酸功能各异,Gly可以增加谷胱甘肽的水平来延长人体寿命,降低同型半胱氨酸水平[8], 同时在α链重复序列中的高含量和作为最小氨基酸使其成为克服空间位阻形成超螺旋的关键;Pro则利于身体形成新的蛋白 (包括胶原蛋白、皮肤和肠内壁)帮助身体愈合,胶原蛋白合成前体的三维链也主要是由Gly和Pro组成;Hyp是胶原蛋白的特征氨基酸,其与羟基形成的链间氢键有利于胶原超螺旋结构的维持。 胶原蛋白通常以酶解的方式水解形成肽段,见图6。"
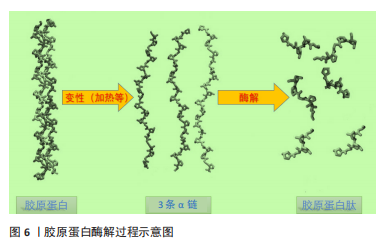
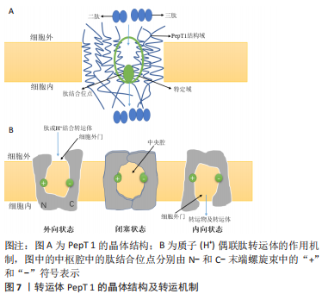
SULEIVYS等[19]利用生物信息学方法对5种不同动物来源(牛、猪、鸡、鳟鱼和鲑鱼)的胶原蛋白进行分类分析,发现相关物种之间具有较多相同序列,这表明胶原蛋白肽不仅限于一种或者几种来源,而且提供了不同来源胶原互换使用的可能性。此外,有研究表明胶原蛋白水解物在血浆中发挥作用的是以Pro-Hyp为主的二肽和一些三肽(Pro-Hyp-Gly、Gly-Pro-Hyp)形式[20]。 因此Pro-Hyp可能不是惟一的功能性肽成分,可选择特定肽段含量高的胶原蛋白肽制备原料或方法以提高产品护肤效果。 2.3 胶原蛋白肽吸收途径 胶原蛋白肽可通过口服参与人体代谢,经胃肠道消化吸收或经皮渗透进入皮肤真皮层,从而对皮肤产生积极作用。 2.3.1 肠道吸收机制 肠道高度折叠的特殊刷状缘膜为人体代谢活动提供巨大的表面积。胶原蛋白肽经口服后在胃肠道的各种酶如胰蛋白酶、胃蛋白酶、糜蛋白酶或微生物的作用下进行降解[21],随后通过PepT 1介导的渗透、紧密连接的细胞旁转运、胞吞作用或被动跨细胞扩散通过小肠上皮细胞到达血液[22],其中肽的生物利用度可能部分取决于其在肠膜中的蛋白酶抗性及肽的疏水性、电荷、大小、分子质量、氨基酸序列和稳定性[23]。 胶原蛋白肽可以通过主动吸收进入血液。PepT1是一种高容量、低亲和力的载体,依靠H+电化学梯度将肽从肠腔驱动到肠上皮细胞中[24-25],以类似口袋的识别方法输送生物活性肽,见图7A。PepT 1优先结合各种二肽和三肽(Pro-Hyp和Gly-Pro-Hyp也通过PepT 1转运体吸收)[26],但不能转载四肽及以上的肽,通过H+/Na+交换器维持的质子梯度和膜电位决定吸收的方向和速率[27],见图7B。可通过改变胶原蛋白肽疏水性增加其与PepT 1亲和力,提高透过率。研究发现人或者小鼠口服胶原蛋白肽后其血液中的Pro-Hyp水平较高[20],部分原因是胶原蛋白中Pro-Hyp序列的数量较高,该结果表明Pro-Hyp可被视为一种不可消化的肽,因为超过75%的Pro-Hyp在体外与人血清反应后会在血液中保留24 h[28]。"
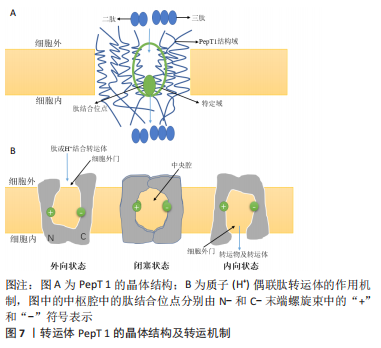
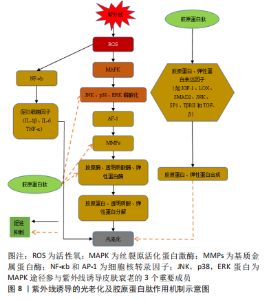
胞吞作用是一种需能的跨细胞转运途径,长链肽主要通过此途径运输。由于肽在被细胞内化之前,需要通过疏水相互作用与上皮细胞的顶端脂质膜表面相互作用,导致胞吞作用更倾向于疏水性肽。 胶原蛋白肽也可通过被动运输进入人体,比如细胞旁途径,其与能量无关,与肠道透过率和肽的分子大小相关。较高的吸收率可能产生更高生物活性作用,这可能也是低分子肽有更高生物利用度的原因。细胞旁途径作为寡肽主要运输方式,倾向于亲水性、带负电的低分子肽段,而对于正电肽段则具有选择性[29-30]。另一种被动运输方式称为跨细胞扩散,倾向于疏水性肽,其转运主要包括3个过程:被动摄取到细胞中、细胞内转运和基底外侧分泌。但通过此途径参与生物活性肽运输的介质尚未确定。成功转运的生物活性肽可能会被细胞质肽酶和血液肽酶部分水解为较小的肽片段或氨基酸[20,27]。 明胶和肽形式的14C标记的Pro-Hyp能够在人和鼠尿液中检测到[26,31],这表明Pro-Hyp的吸收和排泄是完整的,但其却以微摩尔范围内的浓度转运到血流和皮肤中[22],相较于摄入量,可供吸收并有益于皮肤的含量很低,同时完整透过肠上皮的少量二肽和三肽也可能在静脉循环中被血浆肽酶降解,从而降低其到达皮肤的有效浓度。ALCOCK等[32-33]研究表明在服用20 g明胶或水解胶原蛋白的志愿者血浆中存在相似的Gly峰值浓度,并且在总血浆氨基酸利用率方面无明显差异。因此需要对相同来源的胶原蛋白经不同水解方式后的可消化性进行比较,以保证最大限度地将胶原蛋白肽吸收到循环中,而研究口服肽的血浆浓度和动力学对于评估膳食肽的生物活性至关重要。上述研究表明,目前生物活性肽的口服生物利用度较低,水解物面临生理挑战和检测血浆中肽所需的高灵敏度和特异性分析挑战,可应用质谱和肽组学来提高检测生物环境中复杂水解产物释放的单个肽的能力[34]。 2.3.2 经皮吸收机制 天然胶原蛋白与人皮肤胶原蛋白结构相似,生物相容性较好。胶原蛋白肽经皮主要通过角质层、毛囊、汗管及皮脂腺4条途径吸收而不进入体循环,其中后3者常被称为旁路途径。角质层经皮途径又可分为2种[35]:①细胞间途径:通常脂溶性、非极性物质易通过此途径扩散,但细胞间隙的脂质会产生阻力;②跨细胞途径:直接穿过角质细胞和细胞间隙。经皮吸收和转运可能发生在角质层、活表皮(由除角质层外的其他表皮层组成),甚至在皮肤层更深处扩散。角质层结构致密的扁平无核角质细胞和细胞间脂质是经皮吸收的主要阻力,胶原蛋白肽需到达真皮层中才能刺激成纤维细胞,恢复皮肤弹性,或活性成分向基底层进一步扩散达到美白效果,可通过改变有序排列的角质层脂质双分子层结构,作用于皮肤角质层细胞内蛋白质产生水化通道,促进物质在角质层扩散;增加物质在皮肤中的溶解度或可逆地改变皮肤屏障功能使物质的透皮吸收率增加[36]。已死亡的扁平无核角质细胞的细胞膜是致密的交联网状蛋白架构,胞内大量微丝角蛋白和丝蛋白整齐排列,对化学物质扩散产生阻碍,分子可以根据其物理化学特性通过不同的途径渗透穿过表皮层。一般水溶性和极性物质容易从角质细胞经皮渗透,疏水性化合物优先通过细胞间途径渗透,而可溶性分子则利用跨细胞途径[37]。皮肤附属器(毛囊、汗管和皮脂腺)是化妆品经皮吸收的一条途径,大分子物质及离子型物质难以通过富含类脂的角质层,可经该途径进入皮肤。 2.4 对皮肤健康的促进作用 胶原蛋白肽具有抗氧化、促进细胞增殖和趋化等多种生物学功能。胶原蛋白肽含有大量酪氨酸残基,可与黑色素竞争结合位点,具有美白效果。此外,紫外线引起的Ca2+上升会引发线粒体膜电位下降,从而导致细胞内各种炎症因子和凋亡因子的表达。活性氧促进细胞内Ca2+离子浓度的上升,而Ca2+增加细胞内一系列酶反应促进活性氧的产生,胶原蛋白肽则具有清除活性氧的能力,可抑制信号转导并恢复超氧化物歧化酶(superoxide dismutase,SOD)、过氧化氢酶(catalase,CAT)和谷胱甘肽过氧化物酶(glutathione peroxidase,GSH-Px)活性,降低丙二醛含量[7],抑制MAPK/AP-1信号,减少了基质金属蛋白酶的形成和活性,从而减少了皮肤中胶原的降解、弹性纤维异常等。同时胶原蛋白肽通过增加转化生长因子β及其受体的表达以及减少抑制性Smad来恢复转化生长因子β/Smad信号转导,激活胶原合成。WATANABE-KAMIYAMA等[31]通过对大鼠喂食14C标记的Pro或Gly-Pro-Hyp,在大鼠的皮肤中出现了高放射性且保持时间高达14 d,证明了与胶原蛋白肽相关的特定肽段的血液和皮肤的高保持率,为其在皮肤中发挥作用提供了理论依据。同时,彭志兰[38]利用牡蛎源胶原蛋白肽涂抹光老化小鼠皮肤,发现不同剂量对小鼠皮肤有着不同程度的改善效果,利用蛋白质印记分析证明了胶原蛋白肽经皮给药能够抑制光老化引起的MAPK级联信号通路中的JNK,p38,ERK蛋白(MAPK途径中参与紫外线诱导皮肤衰老的3个重要成员)的磷酸化,而其磷酸化会激活细胞核的转录因子例如激活子蛋白1和核转录因子κB,调控相关基因的表达而出现皮肤健康问题,见图8。"
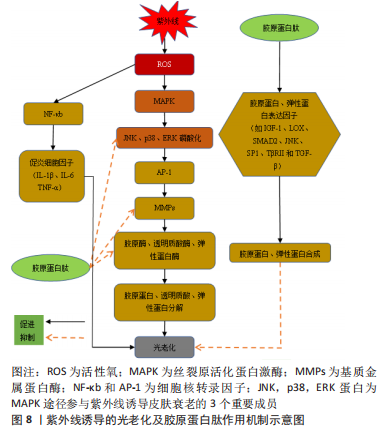

2.5 提高胶原蛋白肽生物利用度的措施 如何提高胶原蛋白肽的生物利用度是目前胶原蛋白护肤领域一个亟待解决的问题。低分子质量胶原蛋白肽的较多氨基酸残基暴露,可能与其较强吸湿保湿性能有关,同时胶原蛋白肽联合抗氧化物质及胶原合成相关酶的辅助因子或通过载体递送的方式增加胶原蛋白肽的口服利用,能够提高人体皮肤胶原合成效率。 2.5.1 选择适宜的分子质量 低分子质量胶原蛋白肽能以一种或多种方式通过肠上皮转运,意味着更小的物理阻力和更多的氨基酸残基暴露,能够更加有效地进入人体表现出更高的生物活性。LI等[45]利用3种重要海洋鱼类软骨胶原制备了39种胶原蛋白水解物,探究了水解物的平均分子质量(0.64 kD≤MW≤ 257.19 kD)与肽功能的关系,结果表明抗氧化能力与胶原蛋白水解物的分子质量呈负相关。LIANG等[46]将罗非鱼胶原蛋白进行模拟胃肠消化,发现平均分子质量为436.8 Da的胶原蛋白肽具有最高的抗氧化活性。 YU等[47]通过让健康女性志愿者口服不同来源明胶、明胶水解物和低分子质量明胶水解物,对受试者肘静脉血浆中的游离Hyp以及Pro-Hyp、Hyp-Gly浓度进行检测,结果表明摄入明胶后血浆中食物源性含Hyp肽(尤其是小肽)的水平不会以分子质量依赖性方式增加,这表明低分子质量肽具有更好的人体吸收和分布性,但过低分子质量不会有更多益处,同时,不同来源肽的适宜分子质量有待探究。对于混合来源的胶原蛋白肽的分子质量与其抗氧化性能,ZAMORANO-APODACA等[48]探究了5个分子质量的不同鱼类混合副产物胶原蛋白水解物,证明了低分子质量肽段具有高还原力和羟基自由基清除活性。生产技术与低分子质量胶原蛋白肽生产有关,HONG等[49]研究表明经α-淀粉酶预处理可增强木瓜蛋白酶水解的低分子质量胶原蛋白肽的产量,因此今后可考虑从酶解方法及所用酶方面制备低分子活性肽(如碱性蛋白酶为内切酶可在短时间内水解胶原蛋白),并从酶切位点出发开发新型酶。 胶原蛋白肽的另一个特点是呈剂量依赖性,SHIGEMURA等[50]通过让志愿者服用不同剂量的鳕鱼皮胶原蛋白水解物发现,30.8 mg/kg以下的剂量对人体无健康作用,153.8 mg/kg和384.6 mg/kg的剂量可导致血液中游离Hyp和肽结合形式的Hyp含量升高。对于不同来源的胶原蛋白,其主要功能肽存在差异,因此可在其分子质量以及氨基酸组成基础上进行最佳使用剂量的研究。在经皮途径中,彭志兰[38]利用牡蛎源胶原蛋白肽证明了低分子质量胶原蛋白肽相较于高分子质量有更好的护肤效果。 2.5.2 联合其他物质应用 联合抗氧化物质:维生素E能够将自由基还原成过氧化物,其主要形式是α-生育酚,可失去质子转化为不反应的自由基达到抗氧化作用。人体试验证明维生素E可作为内源防御系统中谷胱甘肽过氧化物酶的吸收物来激活抗氧化,益于过氧化氢酶、谷胱甘肽过氧化物酶催化H2O2(脂质过氧化的主要触发器)还原为水,从而防止污染物诱导的皮肤炎症和胶原蛋白降解,此效果适用于口服和外用[8]。维生素C则能促进前胶原mRNA的转录和稳定,促进角质形成细胞分化和皮肤屏障功能,提供电子消除潜在自由基[39],作为Pro和赖氨酸羟化酶的辅助因子促进多肽链的羟基化,并稳定胶原纤维。在成纤维细胞核DNA翻译时,维生素C催化未成熟氨基酸基团将O和H连接到多肽链来稳定细胞外基质。胶原和维生素C同时使用能够防止固有氧化应激诱导的皮肤萎缩,两者具有协同作用效果并减少氧化的维生素E[51]。例如彭志兰[38]利用胶原蛋白肽协同维生素C证明了其对小鼠皮肤更高的保健作用。此外碧萝芷也被建议与维生素E和C协同作用增加内源性抗氧化酶系统。研究表明相较于单独使用一种微量营养素,维生素E和C联用能更有效地保护人体免受户外刺激[8],能够作为胶原蛋白肽产品的添加剂来提高护肤效果。 多酚能增加老化皮肤中的胶原蛋白和弹性蛋白,并作为抗氧化剂防止光老化,为皮肤提供双重保护;而番茄红素是一种高度不饱和烃,掺入基于磷脂的媒介物中可成功溶解和稳定制剂中的类胡萝卜素,局部施用后沉积在皮肤上具抗氧化活性,与胶原蛋白肽联用都能够增强护肤效果[9]。 联合酶辅因子:铜可作为赖氨酰氧化酶促进皮肤胶原纤维交联的辅助因子[52];锌能激活胶原蛋白合成所必需的蛋白质来提高胶原合成水平,而锰这种鲜为人知的矿物质可刺激酶的产生,作为前胶原的生物合成中肽基半乳糖羟赖氨酰葡萄糖基转移酶的辅助因子来促进糖基化过程,影响所形成的胶原纤维直径并降低胶原蛋白对胶原酶的易感性,对Pro的产生有重要作用[9]。人类有8种谷胱甘肽过氧化物酶,其中5种含有作为辅助因子的硒,硫氧还蛋白还原酶和谷胱甘肽过氧化物酶都是含硒半胱氨酸的黄酮酶,添加硒可提高其活性。因此基于酶辅因子对皮肤胶原蛋白生成的促进作用和抗氧化性能,可考虑在胶原蛋白肽产品中添加多种酶辅因子来提高胶原蛋白肽和酶辅因子之间的协同护肤作用[53-58]。几种护肤常用抗氧化物质及酶辅因子如表2。"

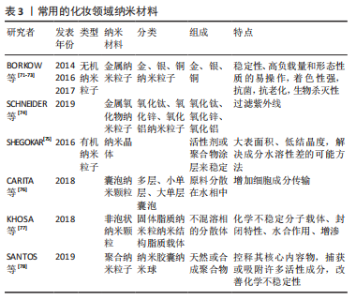
联合弹性蛋白:胶原蛋白肽联合弹性蛋白口服可提高动物皮肤胶原蛋白和弹性蛋白的含量,显著上调透明质酸和Hyp的表达,降低基质金属蛋白酶3、白细胞介素1α的表达,此外,联合使用还可显著增加胰岛素样生长因子1、LOX、SMAD2、JNK、SP1、TβRⅡ和转化生长因子β 等7种胶原和弹性蛋白合成相关因子的表达[59]。例如源自弹性蛋白的序列为GLPY和GPGGVGAL的肽可抑制活性氧的上调、Ca2+内流、胶原和弹性蛋白分解,前者对由基质金属蛋白酶12下调和Ⅰ型胶原mRNA表达上调引起的细胞外基质降解表现出更强的抑制作用,而后者对Ca2+内流表现出更高的抑制作用并在胃肠中保持完整[60],因此可开发更多作为抗光老化潜在成分且能够提高胶原蛋白肽生物利用度的弹性蛋白特定肽段。 2.5.3 载体递送 纳米颗粒的表面可被修饰成亲水性或亲脂性[61],从而增强胶原蛋白肽在体内的稳定性,增加其循环半衰期,可使其以有效浓度到达靶组织[62],此方法只适用于少数口服递送的肽,但目前常以胶原类化妆品中充当载体给药的形式增加皮肤的渗透性。因此可以探索由天然生物聚合物组成的新材料用以递送胶原蛋白肽,如多糖、蛋白质甚至脂质,同时在载体功能验证中应充分考虑化合物在胃肠道中的稳定性、易于穿透肠道黏液层、增强细胞摄取和打开细胞连接[63]。各种多功能递送系统,包括基于脂质和多糖的颗粒、无机颗粒和合成的多功能颗粒,实现了治疗性肽的有效口服递送[64],此方法适用于口服和经皮吸收。 2.5.4 口服与外用结合的新趋势 D-半乳糖诱导衰老的小鼠实验验证了胶原蛋白肽经皮吸收的吸湿保湿性能[65]。除此之外,外界刺激能够导致肠道微生物组成改变,使其产生神经递质(多巴胺、血清素、γ-氨基丁酸和乙酰胆碱),通过肠上皮到达血液调节皮肤功能,如丁酸盐可以通过增加胰岛素样生长因子信号刺激成纤维细胞合成胶原蛋白;细菌代谢物可以改变褪黑素的合成和上皮细胞中的皮肤屏障功能。 应用模拟人体消化条件的静态和动态消化模型正在成为评估肽的人体吸收(即消化率、生物利用度)的宝贵工具,例如将消化模型与肠细胞培养相结合,以模拟上皮转运及验证作为消化混合物获得的肽和氨基酸的肠道生物活性[66]。而胶原蛋白肽可以调节肠道微生物的整体组成,如WANG等[67]利用鳕鱼皮胶原蛋白肽喂食小鼠证明了胶原蛋白肽可改变小鼠的肠道菌群组成,可作为进一步开发相关代谢疾病辅助治疗的潜在药物。 通过胶原蛋白肽的口服和经皮吸收的有效结合[9],同时保证均衡的饮食以达到身体的胶原蛋白代谢平衡,能够有效提高胶原蛋白肽的护肤作用,对于光老化和机体老化引起皮肤亚健康有积极作用。此外,将来自动物副产品转化为高附加值胶原蛋白肽护肤产品具有经济效益和可再生性,促进了食品和化妆品行业的发展,符合绿色发展方式。 2.6 提高胶原蛋白肽经皮吸收的措施 渗透性是经皮吸收的主要问题,主要与物质的高分子质量、亲水性和表皮的固有物理屏障有关,可通过修饰胶原蛋白肽来增加其经皮渗透,棕榈酸能极大增加天然蛋白质对皮肤的渗透性,对多肽的渗透率增加上百倍,可作为化妆品的优良渗透剂[68]。如五肽(KTTKS)对Ⅰ型和Ⅲ型胶原蛋白及纤连蛋白具有特定刺激作用,而棕榈酸酯残基具有驱动亲脂性增加的作用,其衍生物(pal-KTTKS)稳定性提高并增强了其经皮渗透性[69],因此今后可采用生物信息学等方法对生物活性肽进行序列的分析和设计。 短多肽因其分子质量低且表皮层对其阻碍降低,可以渗透到皮肤的更深层,在皮肤深层的保湿性能非常高。除此之外,使用化学渗透促进剂(例如脂肪酸、醇和二醇、表面活性剂和纳米载体)或通过应用物理方法[70](例如电穿孔、超声导入、离子电渗疗法和微针)也能提高胶原蛋白经皮渗透性。值得一提的是,纳米材料因其微小尺寸以及大的表面积与体积比能够增强材料的分散性并改善产品的质地[61],所以可用来增强胶原蛋白肽产品的渗透性、稳定性及控制活性成分的释放以及作为活性剂来克服化妆品的常见局限性。纳米材料既可以作为外用载体又可作为活性成分,但其长期使用可能存在潜在毒性,但新材料的开发逐渐克服了这一缺点,并还具有一定的生物活性和抗菌性[71-78],可将其分为有机和无机2类,见表3。"
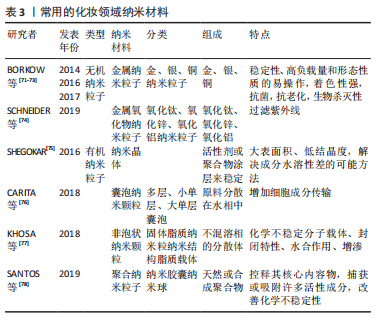

除纳米材料外,在微成型技术合成溶解胶原微针中优化各种工艺参数,如生物聚合物的质量/体积比、微针高度、压降和固化持续时间,提高了微针的皮肤穿透能力[79]。由于微针具有微创和无痛特性克服了部分技术所引起的疼痛等问题而被广泛使用[80]。此外,可以通过改变构成微乳液的多种聚合物的浓度来改善微乳液的增溶能力以此增强胶原蛋白肽的经皮渗透[81]。 载体给药能有效增加皮肤的渗透性。如透明质酸因其独特的黏弹性、生物相容性、生物降解性及非免疫原性而对皮肤有诸多益处[82],能够极大地增加皮肤的吸湿保水性,虽其局部的外源应用可能会引起炎症,但因其较好的护肤效果而在化妆品行业应用广泛,可考虑将其作为胶原蛋白局部应用的渗透载体来提高胶原蛋白到达真皮的效率并在皮肤中发挥抗皱、水合和组织再生等作用。"

| [1] HOLWERDA AM, VAN LOON LJ. The impact of collagen protein ingestion on musculoskeletal connective tissue remodeling: a narrative review. Nutr Rev. 2022;80(6):1497-1514. [2] SORUSHANOVA A, DELGADO LM, WU Z, et al. The collagen suprafamily: From biosynthesis to advanced biomaterial development. Adv Mater. 2019;31(1):1801651. [3] SATO K. Food for skin health: collagen peptides. Ency Food Chem. 2019. doi: 10.1016/B978-0-08-100596-5.21733-2. [4] Kim DU, Chung HC, Choi J, et al. Oral intake of low-molecular-weight collagen peptide improves hydration, elasticity, and wrinkling in human skin: a randomized, double-blind, placebo-controlled study. Nutrients. 2018;10(7):826. [5] 艾丽奇.鳕鱼皮胶原蛋白肽的抗皮肤光老化功效及其作用机制研究[D].广州:华南理工大学,2020. [6] 王晴.罗非鱼皮胶原蛋白延缓小鼠皮肤自然衰老作用研究[D].镇江:江苏大学,2017. [7] BANG J, JIN YJ, CHOUNG SY. Low molecular polypeptide from oyster hydrolysate recovers photoaging in SKH-1 hairless mice. Toxicol Appl Pharm. 2019;386:114844. [8] WOODBY B, PENTA K, PECORELLI A, et al. Skin health from the inside out. Annu Rev Food Sci T. 2020;11:235-254. [9] FARIA-SILVA C, ASCENSO A, COSTA AM, et al. Feeding the skin: a new trend in food and cosmetics convergence. Trends Food Sci Tech. 2020;95:21-32. [10] SIBILLA S, GODFREY M, BREWER S, et al. An overview of the beneficial effects of hydrolysed collagen as a nutraceutical on skin properties: scientific background and clinical studies. Open Nutr J. 2015;8(1):29-42. [11] REST M, GARRONE R. Collagen family of proteins. FASEB J. 1991;5(13): 2814-2823. [12] ICHIHASHI M, ANDO H, YOSHIDA M, et al. Photoaging of the skin. Anti-Aging Med. 2009;6(6):46-59. [13] FITSIOU E, PULIDO T, CAMPISI J, et al. Cellular senescence and the senescence-associated secretory phenotype as drivers of skin photoaging. J Invest Dermatol. 2021;141(4):1119-1126. [14] WANG A S, OLIVER D. Biomarkers of cellular senescence and skin aging. Front Genet. 2018;9:247. [15] HO CY, DREESEN O. Faces of cellular senescence in skin aging. Mech Ageing Dev. 2021;198:111525-111525. [16] MCCABE MC, HILL RC, CALDERONE K, et al. Alterations in extracellular matrix composition during aging and photoaging of the skin. Matrix Biology Plus. 2020;8:100041. [17] SCHWARTZ E, CRUICKSHANK FA, CHRISTENSEN C, et al. Collagen alterations in chronically sun-damaged human skin. Photochem Photobiol. 2010;58(6):841-844. [18] VAN, DEURSEN, JAN, M. The role of senescent cells in ageing. Nature. 2014;509.7501:439-446. [19] SULEIVYS M, GUZMÁN F, VALENCIA P, et al. Collagen as a source of bioactive peptides: a bioinformatics approach. Electron J Biotechn. 2020;48:101-108. [20] YAZAK M, ITO Y, YAMADA M, et al. Oral ingestion of collagen hydrolysate leads to the transportation of highly concentrated Gly-Pro-Hyp and its hydrolyzed form of pro-Hyp into the bloodstream and skin. J Agr Food Chem. 2017;65(11):2315-2322. [21] SULTAN S, HUMA N, BUTT MS, et al. Therapeutic potential of dairy bioactive peptides: a contemporary perspective. Crit Rev Food Sci. 2018;58(1):105-115. [22] XU Q, HONG H, WU J, et al. Bioavailability of bioactive peptides derived from food proteins across the intestinal epithelial membrane: a review. Trends Food Sci Tech. 2019;86:399-411. [23] TANAKA M, HONG SM, AKIYAMA S, et al. Visualized absorption of anti-atherosclerotic dipeptide, Trp-His, in Sprague-Dawley rats by LC-MS and MALDI-MS imaging analyses. Mol Nutr Food Res. 2015;59(8):1541-1549. [24] HANNELORE D, TAMARA Z. Taste and move:glucose and peptide transporters in the gastrointestinal tract.. Exp Physiol. 2015;100(12): 1441-1450. [25] XU F, ZHANG J, WANG Z, et al. Absorption and metabolism of peptide wdhhapqlr derived from rapeseed protein and inhibition of HUVEC apoptosis under oxidative stress. J Agr Food Chem. 2018;66(20):5178-5189. [26] AITO-INOUE M, LACKEYRAM D, FAN MZ, et al. Transport of a tripeptide, Gly-Pro-Hyp, across the porcine intestinal brush-border membrane. J Pept Sci. 2007;13(7):468-474. [27] MINER-WILLIAMS WM, STEVENS BR, MOUGHAN PJ. Are intact peptides absorbed from the healthy gut in the adult human? Nutr Res Rev. 2014; 27(2):308-329. [28] GENOVESE L, CORBO A, SIBILLA S. An Insight into the changes in skin texture and properties following dietary intervention with a nutricosmeceutical containing a blend of collagen bioactive peptides and antioxidants. Skin Pharmacol Phys. 2017;30(3):146. [29] ALUKO RE. Antihypertensive peptides from food proteins. Annu Rev Food Sci T. 2015;6:235-262. [30] MATSUI T. Are peptides absorbable compounds? J Agr Food Chem. 2018;66(2):393-394. [31] WATANABE-KAMIYAMA M, SHIMIZU M, KAMIYAMA S, et al. Absorption and effectiveness of orally administered low molecular weight collagen hydrolysate in rats. J Agr Food Chem. 2010;58(2):835-841. [32] ALCOCK RD, SHAW GC, TEE N, et al. Plasma amino acid concentrations after the ingestion of dairy and collagen proteins, in healthy active males. Front Nutr. 2019;6:163. [33] LIS DM, BAAR K. Effects of different vitamin-c enriched collagen derivatives on collagen synthesis. Int J Sport Nutr Exe. 2019;29.5:526-531. [34] ABEER MM, TRAJKOVIC S, BRAYDEN DJ. Measuring the oral bioavailability of protein hydrolysates derived from food sources: a critical review of current bioassays. Biomed Pharmacother. 2021;144: 112275. [35] 化璟琳,谢莹莹,徐鹤然,等.胶原蛋白肽分析方法及透皮吸收特征[J].中国组织工程研究,2021,25(34):5544-5551. [36] 杨铭,姚婷,钟绮婷,等.促渗透技术在化妆品中应用的综述[J].广东化工,2021,48(22):123-124. [37] HATTA I. Chapter 42-Structural Aspects of Stratum Corneum. Cosmetic Sci Tech. 2017;699-709. doi:10.1016/B978-0-12-802005-0.00042-2. [38] 彭志兰.牡蛎蛋白源抗皮肤光老化活性肽的分离纯化、鉴定及其作用机理研究[D].湛江:广东海洋大学,2021. [39] ANNA C, KANIA EM, LICIA G, et al. Daily oral supplementation with collagen peptides combined with vitamins and other bioactive compounds improves skin elasticity and has a beneficial effect on joint and general wellbeing. Nutr Res. 2018;57:97-108. [40] LU J, HOU H, FAN Y, et al. Identification of MMP-1 inhibitory peptides from cod skin gelatin hydrolysates and the inhibition mechanism by MAPK signaling pathway. J Funct Foods. 2017;33:251-260. [41] TKACZEWSKA J, BUKOWSKI M, MAK P. Identification of antioxidant peptides in enzymatic hydrolysates of carp (Cyprinus carpio) skin gelatin. Molecules. 2018;24(1):97. [42] XIAO Z, LIANG P, CHEN J, et al. A peptide YGDEY from tilapia gelatin hydrolysates inhibits UVB‐mediated skin photoaging by regulating MMP‐1 and MMP‐9 expression in HaCaT cells. Photochem Photobiol. 2019;95(6):1424-1432. [43] LEE HJ, JANG HL, AHN DK, et al. Orally administered collagen peptide protects against UVB-induced skin aging through the absorption of dipeptide forms, Gly-Pro and Pro-Hyp. Biosci Biotech Bioch. 2019; 83(6):1146-1156. [44] YANG XR, ZHAO YQ, QIU YT, et al. Preparation and characterization of gelatin and antioxidant peptides from gelatin hydrolysate of skipjack tuna (Katsuwonus pelamis) bone stimulated by in vitro gastrointestinal digestion. Mar Drugs. 2019;17(2):78. [45] LI Z, WANG B, CHI C, et al. Influence of average molecular weight on antioxidant and functional properties of cartilage collagen hydrolysates from Sphyrna lewini, Dasyatis akjei and Raja porosa. Food Res Int. 2013; 51(1):283-293. [46] LIANG Q, LIN W, HE Y, et al. Hydrolysis kinetics and antioxidant activity of collagen under simulated gastrointestinal digestion. J Funct Foods. 2014;11:493-499. [47] YU I, NAKATOGAWA M, SHIMIZU A, et al. Comparison of gelatin and low-molecular weight gelatin hydrolysate ingestion on hydroxyproline (Hyp), Pro-Hyp and Hyp-Gly concentrations in human blood. Food Chem. 2021;369:130869. [48] ZAMORANO-APODACA JC, GARCÍA-SIFUENTES CO, CARVAJAL-MILLÁN E, et al. Biological and functional properties of peptide fractions obtained from collagen hydrolysate derived from mixed by-products of different fish species. Food Chem. 2020;331:127350. [49] HONG H, FAN H, ROY BC, et al. Amylase enhances production of low molecular weight collagen peptides from the skin of Spent Hen, Bovine, Porcine, and Tilapia. Food Chem. 2021;352:129355. [50] SHIGEMURA Y, KUBOMURA D, SATO Y, et al. Dose-dependent changes in the levels of free and peptide forms of hydroxyproline in human plasma after collagen hydrolysate ingestion. Food Chem. 2014;159(15):328-332. [51] SHIBUYA S, OZAWA Y, TODA T, et al. Collagen peptide and vitamin C additively attenuate age-related skin atrophy in Sod1-deficient mice. Biosci Biotech Bioch. 2014;78(7):1212-1220. [52] PEARSON K. Nutraceuticals and skin health: key benefits and protective properties. J Aesthetic Nursing. 2018;7(Sup1):35-40. [53] KROL ES, KRAMER-STICKLAND KA, LIEBLER DC. Photoprotective actions of topically applied vitamin E. Drug Metab Rev. 2000;32(3-4):413-420. [54] SAUERMANN K, JASPERS S, KOOP U, et al. Topically applied vitamin C increases the density of dermal papillae in aged human skin. BMC Dermatology. 2004;4(1):1-6. [55] MARINI A, GRETHER-BECK S, JAENICKE T, et al. Pycnogenol® effects on skin elasticity and hydration coincide with increased gene expressions of collagen type I and hyaluronic acid synthase in women. Skin Pharmacol Phys. 2012;25(2):86-92. [56] Sticozzi C, Belmonte G, Cervellati F, et al. Resveratrol protects SR-B1 levels in keratinocytes exposed to cigarette smoke. Free Radical Bio Med. 2014;69:50-57. [57] SOUYOUL SA, SAUSSY KP, LUPO MP. Nutraceuticals: a review. Dermatol Ther. 2018;8(1):5-16. [58] ZOIDIS E, SEREMELIS I, KONTOPOULOS N, et al. Selenium-dependent antioxidant enzymes: actions and properties of selenoproteins. Antioxidants. 2018;7(5):66. [59] ZHANG Z, ZHU H, ZHENG Y, et al. The effects and mechanism of collagen peptide and elastin peptide on skin aging induced by D-galactose combined with ultraviolet radiation. J Photochem Photobiol B. 2020;210(8):111964. [60] LIU Y, SU G, WANG S, et al. A highly absorbable peptide GLPY derived from elastin protect fibroblasts against UV damage via suppressing Ca2+ influx and ameliorating the loss of collagen and elastin. J Funct Foods. 2019;61:103487. [61] SALVIONI L, MORELLI L, OCHOA E, et al. The emerging role of nanotechnology in skincare. Adv Colloid Interfac. 2021;293:102437. [62] GUPTA S, JAIN A, CHAKRABORTY M, et al. Oral delivery of therapeutic proteins and peptides: a review on recent developments. Drug Deliv. 2013;20(6):237-246. [63] CHAI J, JIANG P, WANG P, et al. Intelligent delivery systems for bioactive compounds in foods: Physicochemical and physiological conditions, absorption mechanisms, obstacles and responsive strategies. Trends Food Sci Tech. 2018;78:144-154. [64] HAN Y, GAO Z, CHEN L, et al. Multifunctional oral delivery systems for enhanced bioavailability of therapeutic peptides/proteins. Acta Pharm Sin B. 2019;9(5):902-922. [65] 李幸.鳕鱼皮胶原肽保湿护肤效果的研究[D].青岛:中国海洋大学, 2014. [66] GIROMINI C, CHELI F, REBUCCI R, et al. Invited review:dairy proteins and bioactive peptides: modeling digestion and the intestinal barrier. J Dairy Sci. 2019;102(2):929-942. [67] WANG S, LV Z, ZHAO W, et al. Collagen peptide from Walleye pollock skin attenuated obesity and modulated gut microbiota in high-fat diet-fed mice. J Funct Foods. 2020;74:104194. [68] DOMINIK I, EILEEN J, MARC H, et al. Activation of TGF-β: a gateway to skin rejuvenation. H&PC Today. 2015;10:1-6. [69] CHOI YL, PARK EJ, KIM E, et al. Dermal stability and in vitro skin permeation of collagen pentapeptides (KTTKS and palmitoyl-KTTKS). Biomol Ther. 2014;22(4):321. [70] CHEUNG K, DAS DB. Microneedles for drug delivery:trends and progress. Drug Deliv. 2016;23(7):2338-2354. [71] BORKOW G. Using copper to improve the well-being of the skin. Cur Chem Biol. 2014;8(2):89-102. [72] CAO M, LI J, TANG J, et al. Gold nanomaterials in consumer cosmetics nanoproducts: analyses, characterization, and dermal safety assessment. Small. 2016;12(39):5488-5496. [73] SALVIONI L, GALBIATI E, COLLICO V, et al. Negatively charged silver nanoparticles with potent antibacterial activity and reduced toxicity for pharmaceutical preparations. Int J Nanomed. 2017;12:2517. [74] SCHNEIDER SL, LIM HW. A review of inorganic UV filters zinc oxide and titanium dioxide. Photodermatol Photo. 2019;35(6):442-446. [75] SHEGOKAR R. What nanocrystals can offer to cosmetic and dermal formulations. Nanobiomaterials in galenic formulations and cosmetics. 2016. doi: 10.1016/B978-0-323-42868-2.00004-8. [76] CARITA AC, ELOY JO, CHORILLI M, et al. Recent advances and perspectives in liposomes for cutaneous drug delivery. Curr Med Chem. 2018;25(5):606-635. [77] KHOSA A, REDDI S, SAHA RN. Nanostructured lipid carriers for site-specific drug delivery. Biomed Pharmacother. 2018;103:598-613. [78] SANTOS AC, MORAIS F, SIMÕES A, et al. Nanotechnology for the development of new cosmetic formulations. Expert Opin Drug Del. 2019;16(4):313-330. [79] ADITYA A, KIM B, KOYANI RD, et al. Kinetics of collagen microneedle drug delivery system. J Drug Deliv Sci Tec. 2019;52:618-623. [80] MONIZ T, LIMA S, REIS S. Marine polymeric microneedles for transdermal drug delivery. Carbohyd Polym. 2021;266:118098. [81] SZUMAŁA P, JUNGNICKEL C, KOZŁOWSKA-TYLINGO K, et al. Transdermal transport of collagen and hyaluronic acid using water in oil microemulsion. Int J Pharmaceut. 2019;572:118738. [82] ZHU J, TANG X, JIA Y, et al. Applications and delivery mechanisms of hyaluronic acid used for topical/transdermal delivery – A review. Int J Pharmaceut. 2020;578:119127. |
| [1] | Zhan Yuanbo, Liu Xinpeng, Xu Wenxia, Miao Nan, Mu Sen, Zhang Ruimin, Li Ying. Expression of histone deacetylase 9 in bone marrow mesenchymal stem cells during senescence [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(30): 4762-4766. |
| [2] | Wang Jiawei, Liu Ye. Motor coordination: evolution of theoretical model and quantitative method [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(20): 3256-3264. |
| [3] | Hua Jinglin, Xie Yingying, Xu Heran, Zhang Xiaona, Wang Min. Analysis methods and transdermal absorption of collagen peptides [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(34): 5544-5551. |
| [4] | You Bin, Huang Xiuzhu, Lin Yu, Huang Xi. Changes in bone morphology, bone mineral density and bone metabolism in different parts of natural aging rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(26): 4118-4122. |
| [5] | Chen Yongjia, Li Yanlin, Liu Dejian, He Yinghong, Yang Xiao. Sustained-release effect and clinical application of thermosensitive gels [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(34): 5428-5433. |
| [6] | Guo Enhui, Xu Zitong, Liang Yize, Zhou Liang, Lu Zhaoxiang, You Liang, Xia Yujun. Properties of a novel photocrosslinked fish collagen peptide-hyaluronic acid hydrogel [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(28): 4518-4525. |
| [7] | Luo Jianchun, Guo Qi, Zhang Min, Zhong Meng, Wan Shengli, Zhang Jingqing. Intestinal absorption characteristics of curcumin hydroxypropyl-beta-cyclodextrin in rats: an analysis using one-way perfusion method [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(6): 957-962. |
| [8] | Tan Jun, Ding Wei, Li Gao-feng, Li Bo, Qin Xiao-dong. Distribution characteristics of epidermal stem cells after treatment with fractional CO2 laser in a model of skin photoaging [J]. Chinese Journal of Tissue Engineering Research, 2013, 17(6): 1075-1080. |
| [9] | Zhou Xiang-jun, Ye Cai-guo, Yang Guang-li, Liu Lin-sheng. Protective action of salvianolic acid B on skin photoaging in mice [J]. Chinese Journal of Tissue Engineering Research, 2013, 17(2): 275-279. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||