Chinese Journal of Tissue Engineering Research ›› 2021, Vol. 25 ›› Issue (29): 4721-4727.doi: 10.12307/2021.175
Previous Articles Next Articles
Reopening the fused suture provides a new idea for maxillary expansion
Zhang Mingjin, Zhou Yanheng, Liu Dawei
- Department of Orthodontics, Peking University School of Stomatology, Beijing 100081, China
-
Received:2020-10-26Revised:2020-10-29Accepted:2020-12-12Online:2021-10-18Published:2021-07-22 -
Contact:Zhou Yanheng, MD, Professor, Chief physician, Department of Orthodontics, Peking University School of Stomatology, Beijing 100081, China Liu Dawei, MD, Associate professor, Associate chief physician, Department of Orthodontics, Peking University School of Stomatology, Beijing 100081, China -
About author:Zhang Mingjin, Department of Orthodontics, Peking University School of Stomatology, Beijing 100081, China -
Supported by:the National Natural Science Foundation of China (General Programs), No. 6207023221 (to ZYH) and 81970909 (to LDW); the New Clinical Technology and Therapy Project of Peking University School of Stomatology, No. PKUSSNCT-20A07 (to LDW)
CLC Number:
Cite this article
Zhang Mingjin, Zhou Yanheng, Liu Dawei. Reopening the fused suture provides a new idea for maxillary expansion[J]. Chinese Journal of Tissue Engineering Research, 2021, 25(29): 4721-4727.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
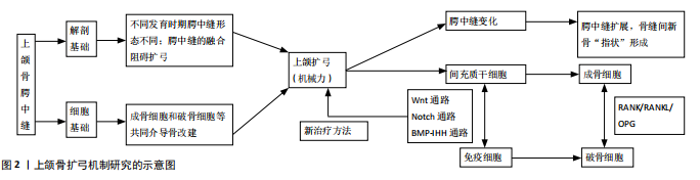
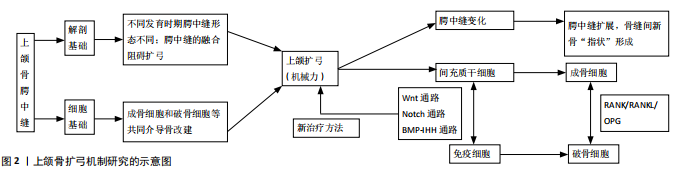
2.1 上颌骨扩弓的临床进展概况 2.1.1 上颌骨扩弓适应证 上颌横向发育不足(maxillary transverse deficiency, MTD)是临床常见的错牙合 畸形,临床上表现为腭盖高拱、单侧或双侧后牙反牙合 、牙列不齐等[1]。上颌扩弓可以打开腭中缝,从而扩大上颌骨和上牙弓宽度,是解决上颌横向发育不足的临床有效手段。同时有研究表明,上颌骨扩弓可以增加鼻咽气道的空间,增宽鼻腔基底宽度,从而减少鼻气道阻力,增加上呼吸道通气量,用于治疗阻塞性睡眠呼吸暂停综合征[2]。 2.1.2 上颌骨扩弓方法进展 临床上目前常用矫治方法包括上颌快速扩弓、上颌慢速扩弓、外科辅助上颌快速扩弓、种植体支抗辅助上颌快速扩弓以及反复交替式上颌快速扩缩弓,有学者对不同扩弓方法的起源、技术简介、临床应用优缺点也进行了综述[3]。 上颌快速扩弓及上颌慢速扩弓一般适用于生长发育期的儿童,通过施加横向的矫治力,可以打开腭中缝,随着骨缝扩宽,期间会有新骨形成,通过骨沉积的方式使上颌骨扩宽。二者主要不同在于加力的不同,后者更慢、更小。生长发育期过后,随着年龄增长,治疗更多地导致牙的颊向倾斜,而非腭中缝的变化。 外科辅助上颌快速扩弓主要适用于骨骼完全成熟、骨缝完全闭合的严重上颌发育不足,它被看作是正畸治疗和牵引成骨的结合疗法,在提供了牙弓间隙的同时,减小了上颌横向发育不足的复发[4];但其也存在手术创伤大、感染、神经血管损伤等并发症的风险。 种植体支抗辅助上颌快速扩弓是将支抗种植体植入腭部基骨作为支抗,使矫形力直接作用于基骨,配合螺旋扩弓器,牵张骨缝促进新骨沉积,增加骨量从而实现上颌横向扩宽,适用于成人上颌横向发育不足[3]。该种方法的应用扩大了临床上颌骨扩弓的适应证范围,但对于年龄较大的成年患者仍有治疗失败的可能。贾海潮等[5]设计并研究个性化微螺钉辅助上颌快速扩弓成年患者腭中缝扩开的成功率为88.9%;CHOI等[6]研究腭中缝扩开成功率89.96%。 反复交替式上颌快速扩缩弓是2005年由LIOU等学者引入,原理类似于拔牙时颊舌向松解牙齿[7],通过“交替扩缩”最大程度松解并激活环上颌骨周围骨缝,刺激颌骨自身生长,从而增加上颌骨向前的生长量。临床上配合前方牵引主要用于治疗早期安氏Ⅲ类错牙合畸形患者,用于提高前方牵引效 果[8]。 2.2 上颌骨扩弓的基础 2.2.1 上颌骨扩弓的解剖学基础——骨缝形态与发育 骨缝是指脊椎动物头骨的纤维关节,由两侧骨端以及其间的从胚胎间质发育而来的纤维结缔组织构成[9]。骨缝不仅仅是骨与骨之间的连接,也是骨祖细胞增殖、分化并在成骨前沿发挥作用的主要位点。 骨缝对于扩弓的影响主要体现在两方面,首先,大多数骨缝会随着生长发育而发生不同程度的融合,其形态也会发生特征性改变,从而对扩弓产生阻碍,影响临床扩弓方法的选择。 有学者认为扩弓的阻力主要来自上颌骨周围骨缝(包括颧颌缝、颧颞缝、翼腭缝等),而腭中缝是其中最重要的区域之一[10];GRUNHEID等[11]学者研究发现相比于上颌骨周围骨缝,腭中缝的融合对于上颌快速扩弓的疗效影响更大,结果符合这一观点;临床上也多采用腭中缝成熟水平辅助判断预估上颌骨扩弓后的开展情况[12]。腭中缝是上颌骨腭突和腭骨水平部之间融合线,它的融合或开展是影响上颌骨扩弓的重要因素。不同生长发育时期腭中缝形态变异巨大,与生理年龄并无明确的直接联系,而明确腭中缝发展阶段对于临床治疗又至关重要,所以判断腭中缝融合程度的手段和指标也越来越多。 ANGELIERI等[13]根据CBCT拍摄的从鼻腔到口腔的中央横断面将腭中缝融合程度分为5个阶段:A阶段,腭中缝几乎是一条高密度直线影像,没有或者几乎没有结合;B阶段,腭中缝形态不规则,表现为扇贝型的高密度线状影像,也可能出现2条平行邻近的扇形高密度线状影,中间有低密度阴影分隔;C阶段,腭中缝表现为2条平行邻近的扇形高密度线状影,中间被上颌骨和腭骨内的低密度阴影分隔,此时骨缝可为直线或为不规则形态;D阶段,腭中缝由后至前出现融合,腭骨内骨缝不可见,但上颌骨内融合尚未发生;E阶段,上颌骨内腭中缝也开始融合,即至少部分上颌骨内骨缝不可见。随着骨缝融合程度的增加,扩弓的阻力也随之增加。高璐等[14]观察研究中国人群腭中缝形态特点并在Angelieri分类基础上改进,将其分为5期;也有不同学者通过CBCT测量上颌区域和硬腭区域腭中缝密度[15]、或者腭中缝密度比(即腭中缝及上颌骨腭突平均灰度值与软腭平均灰度值的差值之比)评估腭中缝的成熟阶段[11]。 腭中缝的成骨过程开始于骨缝边缘的骨以及在骨缝间隙中的岛状物细胞组织和钙化结构,随着边缘骨的形成和成熟,其形成了许多由结缔组织分隔的邻近扇形区域;同时,骨缝间的交指结合增加,融合从后至前,皮质骨吸收,松质骨形成[13];SAVOLDI等[15]研究发现不同区域骨缝的生长并非同步。 骨缝对于扩弓的第二个影响主要体现在施加于骨缝上的机械应力可以调节腭中缝的成骨过程及颅面骨生长,而上颌扩弓正是利用了这一点。PRIYADARSHINI等[16]发现骨缝所承受的机械应力可以调节骨缝生长,同一骨缝也具有不同的应力分布模式,从而导致差异性的骨改建。WU等[17]学者发现扩展的骨缝间新骨呈“手指状”形成,不同方向的力会影响新骨形成和上颌骨移动方向;扩张力会导致骨骼的形成,而收缩力会导致这些指状骨骼的断裂。 2.2.2 上颌骨扩弓的细胞生物学基础 膜内成骨和软骨内骨化是脊椎动物骨骼发育中调节骨形成的两种方式,其中颅面骨的形成主要通过膜内成骨完成的[9],扩弓而施加在骨缝间的机械应力会刺激骨的重塑,力可以诱导间充质干细胞分化为成骨细胞,同时破骨细胞成熟活化。一般情况下,破骨细胞凋亡后骨吸收被抑制,骨的形成占据主导,当达到新的平衡时,骨改建完成[18]。 骨改建的过程主要分为4个阶段:激活、吸收、逆转、形成,其中最重要的有两个问题:该过程如何被激活,以及成骨破骨的平衡如何保持,这均需要成骨细胞、破骨细胞等多种细胞的共同参与和调节。 上颌骨扩弓中,GUERRERO等[19]研究发现施加于腭中缝的机械应力会激活成骨样细胞,同时上调成骨细胞和破骨细胞标志物的表达,从而增加新骨形成,并且在不同的机械应力下成骨细胞和破骨细胞的分布不同,该研究也从细胞学角度解释了不同种类的机械应力刺激使腭中缝处骨形成或骨吸收结果不同的原因。 成骨细胞来源于间充质干细胞,有研究表明机械应力具有激活骨间充质干细胞中ERK1/2-Runx2细胞内途径的能力,从而介导其分化为成骨细胞[20],即在拉伸应力的作用下,Runx2以及Ⅰ型胶原mRNA上调,骨膜细胞表达出成骨表型,腭中缝处在拉伸应力作用下成骨前体细胞分化成成骨细胞。CAPRIOGLIO等[20]对3例扩弓患者的病例报告中发现新形成的骨和矿化的骨基质不仅出现在骨边缘处,同时骨缝中心也有矿化过程。WU等[17]发现扩展的骨缝间形成指状突起的新骨表面有纺锤形成骨细胞连续覆盖,以上研究均说明了扩弓的成骨机制可能是由于机械应力激活间充质干细胞或成骨前体细胞的细胞通路,进而产生成骨细胞发挥成骨效应。 破骨细胞来源于单核造血髓系细胞,其前体和成熟细胞表面高度表达核因子κB受体活化因子(receptor activator of nuclear factor-kappa B,RANK),破骨细胞形成和功能均受到巨噬细胞集落刺激因子和核因子κB受体激活因子配体 (receptor activator of nuclear factor kappa-B ligand,RANKL)的调节,这些是破骨细胞形成必需的细胞因子,可以由多种细胞表达,包括成骨细胞、成软骨细胞、B细胞和T细胞等。骨保护素来自肿瘤坏死因子受体家族,是RANKL的可溶性竞争抗体,以高亲和力与RANKL结合并抑制其对RANK的作 用[21]。RANK和RANKL结合后,可激活肿瘤坏死因子受体相关因子家族(TNF receptor–associated factor,TRAFs),RANK/TRAF可以通过多种信号通路调节破骨细胞的形成活化,包括核因子κB和MAPK等。也有研究发现肿瘤坏死因子α 和其他细胞因子在某些特定情况下也有可能诱导破骨细胞的形成,但是尚不能完全替代RANKL[22]。目前认为RANKL对破骨细胞的调节起重要作用,而其机制复杂,受到成骨细胞、免疫细胞及其分泌的多种细胞因子调控,这也提示了上颌骨扩弓骨重建中多种细胞通过不同细胞因子之间的相互作用机制。 不同类型的机械力会对破骨细胞形成影响不同,体外实验中,压应力会加速破骨细胞的生成[23],而周期性的拉应力和低强度高频震动会抑制破骨细胞的生成[24],生理负荷下高强度的应力会促进破骨细胞融合激活[25];体内研究表明,正畸牙齿移动过程中施加于牙周膜的应力应变和牙周组织内破骨细胞的分布有直接关系,在压应力区域破骨细胞数量最多,而在拉应力区域破骨细胞数量最少。 腭中缝扩张、牵张成骨、正畸牙齿移动都运用了机械应力来调节骨的改建。尽管腭中缝扩张和牵张成骨都可以通过类似扩张的机械力引导骨形成,但是两者机制并不相同。对于后者,施加牵张力前需要一段潜伏期,在这段时间内骨痂逐渐形成[26],在此基础上牵张形成新骨,本质上是急性炎症反应;而扩弓的过程中腭中缝在施加机械力时,并不需要潜伏期,本质上更近似于成骨细胞和破骨细胞等对机械力的生物学反应。 正畸治疗牙齿移动中,正畸矫治器施加到牙齿的力通过牙周膜传递到牙槽骨,从而导致骨的沉积或吸收,最终牙齿移动。牙周膜间充质干细胞在这一过程起关键作用,它可以感受机械刺激而分化出不同类型细胞,HUANG等[27]研究发现正畸牙齿移动时当张力超过一定程度,牙周膜干细胞会更倾向于分化为破骨细胞,而短期压应力的施加可促进牙周膜干细胞的成骨分化,长期压应力抑制成骨、促进破骨细胞生成。而腭中缝区域并不存在牙周膜,上颌扩弓时其作用由骨缝间充质干细胞所代替,机械应力会对骨缝间充质干细胞的分化产生调节作用从而产生效果。 2.3 上颌骨扩弓的机制研究进展 2.3.1 间充质干细胞参与扩弓骨形成 骨髓来源的间充质干细胞是成骨细胞、软骨细胞、脂肪细胞等间质细胞的常见前体细胞,间充质干细胞可分化为成骨细胞,诱导形成骨膜和成骨位点,从而修复损伤形成新骨。有研究表明颅面骨缝间的间充质干细胞对骨缝融合和新骨形成等有重要作用,同时颅面骨骨缝又为干细胞提供了有利的生长微环境[28]。成骨的范围主要邻近骨缝周围或者位于颅面骨的外表面,骨髓腔内也有新骨形成,但是形成量较小[29]。即扩弓过程中,骨缝不仅是成骨的主要位点,骨缝的存在还有利于间充质干细胞的生长,如此才能更好地获得骨缝处新骨的形成,达到上颌骨扩弓的效果。骨缝间质中的Gli1+细胞被鉴定为颅面部骨骼干细胞,骨祖细胞分泌的IHH调节骨缝间的间充质干细胞分化为成骨细胞,除此之外,Axin2+以及Prx+标记的间充质细胞被认定为对于颅面骨发育、稳态维持、损伤修复有重要作用,用于标记骨缝间充质干细胞[30]。 骨缝间充质干细胞除了可以分化为成骨细胞促进新骨形成之外,还可以调节破骨细胞的分化影响扩弓过程中骨的改建。GUO等[31]研究发现骨前体细胞表达具有活性的骨形态发生蛋白,同时分泌IHH激活骨缝间充质干细胞,骨形态发生蛋白介导的IHH信号通路和RANKL具有协同作用,共同促进破骨细胞的分化激活,从而平衡成骨和破骨细胞活性;而ABE等[32]实验发现间充质干细胞可能通过促进骨保护素的产生,抑制破骨细胞的形成。破骨细胞可能通过开展骨缝来诱导骨缝间充质干细胞迁移至骨缺损区域,进而促进新骨的形成;若破骨细胞活性受损,间充质干细胞的迁移也会受到阻碍,从而影响骨再生能力。 有研究表明间充质干细胞分泌外泌体可以促进其成骨分化,以及成骨细胞的增殖和迁移[33],同时已经分化为成骨表型的间充质干细胞可以以正反馈调节机制刺激其他间充质干细胞向相同表型分化[34];成骨细胞也可以通过外泌体激活Wnt通路,进而促进间充质干细胞的成骨分化[35-38];QIN 等[39]研究发现间充质干细胞释放的细胞外囊泡可以通过成骨细胞的胞吞作用介导成骨基因的表达,从而促进间充质干细胞的成骨分化。另一种细胞外囊泡类型——凋亡小体可以由破骨细胞在其生命周期末凋亡时分裂形成,MA等[40]研究发现成熟破骨细胞源性的凋亡小体可以激活RANKL反向信号传导而促进成骨细胞分化;LIU等[41]研究发现间充质干细胞可以通过吞噬外源性凋亡小体,激活WNT/β-catenin通路支持间充质干细胞的稳态,从而减少骨质流失。间充质干细胞还可以通过分泌细胞外囊泡、细胞因子(例如转化生长因子β)等来调节巨噬细胞极化从而减轻炎症,介导组织修复及骨改建[42-44]。以上研究说明细胞外囊泡系统在上颌骨扩弓中可能起到的重要作用,间充质干细胞可通过不同细胞外囊泡类型介导的机制发生成骨分化达到扩弓的目的。 在扩弓的过程中,不同的机械刺激对间充质干细胞的成骨分化也会产生影响。研究发现循环拉伸的机械刺激可诱导Notch信号传导,从而促进间充质干细胞的成骨分化,此外流体剪切应力可以增加间充质干细胞的成骨潜力[45];LI等[46]研究发现在大鼠模型中,机械张力作用下,ROCK调节TAZ核移位进一步结合下游通路的Runx2,从而促进骨缝间充质干细胞的成骨分化;而FRANK等[47]发现频繁的机械应力会抑制间充质干细胞的增殖而不影响其多能性。 2.3.2 免疫细胞参与扩弓骨形成 免疫细胞可以通过作用于破骨细胞的形成激活影响扩弓过程中的骨形成。许多活化的免疫细胞,包括B淋巴细胞和T淋巴细胞、单核细胞、树突状细胞等可以分泌RANKL[48],被认为是刺激破骨细胞形成的潜在因素。这些细胞还可以产生多种促炎或抗炎细胞因子影响RANK-RANKL信号通路进而影响骨改建的过程。一方面,细胞因子肿瘤坏死因子α、白细胞介素1、白细胞介素3、白细胞介素6、 白细胞介素7、白细胞介素11、白细胞介素15和白细胞介素17通过促进破骨细胞的分化激活或通过成骨细胞诱导RANKL表达来增强骨丢失;另一方面,白细胞介素4、白细胞介素5、白细胞介素10、白细胞介素12、白细胞介素13、 白细胞介素18、干扰素α和干扰素β等可直接或间接地阻断RANKL信号从而抑制破骨细胞形成[49]。干扰素γ对于破骨细胞形成具有双面作用,有研究认为它可以通过快速降解TRAF6抑制RANKL信号抑制破骨细胞形成,而有些研究发现干扰素γ在不依赖RANKL信号通路的T细胞过度活化或炎症条件下对于破骨细胞形成有重要作用[50]。 T细胞虽然也表达RANKL,但是一般认为其属于抗破骨细胞,而其中Th17亚群不产生抑制RANKL信号传导的干扰素γ,但分泌大量白细胞介素17,表达促炎因子肿瘤坏死因子α等,RANKL表达增强,诱导破骨细胞形成,白细胞介素17还可诱导基质降解酶合成,导致骨的降解吸收;Treg群通过细胞直接接触以及分泌白细胞介素4、白细胞介素10、转化生长因子β等抗炎细胞因子方式抑制破骨细胞形成,从而减少骨吸收[49];BOZEC等[51]研究表明Treg群还可以通过CTLA-4结合前体破骨细胞表面的CD80/86介导抑制破骨细胞分化,诱导其凋亡;而LI等[50]发现上颌快速扩弓过程中Th1及Th17和他们分泌的细胞因子促进破骨细胞生成,而Treg亚群通过抑制Th1及Th17细胞功能减少破骨细胞生成,促进腭中缝区域新骨形成。由此可见,T细胞对破骨细胞的作用主要取决于表达的正调节和负调节因子之间的平衡。 除外T细胞,巨噬细胞在机械负荷诱导的骨改建和牙齿运动中起着至关重要的作用。巨噬细胞根据环境条件可以极化成不同的表型从而行使不同功能,其中M1型巨噬细胞通过产生诱导型一氧化氮合酶和肿瘤坏死因子α等细胞因子加剧炎症,而M2型通过产生抗炎因子如Arg-1和白细胞介素10等促进组织愈合[52]。HE等[53]研究发现M1型巨噬细胞的极化以及M1/M2型巨噬细胞比例的增加促进了牙槽骨吸收,从而加速正畸牙齿移动;而巨噬细胞和破骨细胞被认为是髓样祖细胞竞争分化的结果,二者之间存在着调节机制,具体表现为M1型巨噬细胞相关的细胞因子,例如肿瘤坏死因子α、白细胞介素6、白细胞介素1β可以诱导破骨细胞生成,而M2型巨噬细胞相关的细胞因子会抑制破骨细胞形成[54-55]。 巨噬细胞也可以对间充质干细胞产生调节作用,CD169+巨噬细胞可以通过提高支持造血干细胞因子的表达直接调节骨髓间充质干细胞,巨噬细胞的消耗也会导致骨髓间充质干细胞成骨表达下降[56];JIN等[57]实验证明了M2型巨噬细胞可以增强间充质干细胞的成骨分化,诱导骨再生;而巨噬细胞的耗竭会减少间充质干细胞的分化从而减少的骨形成。 由此可见,间充质干细胞和免疫细胞之间的互相作用在骨再生中十分重要。骨髓间充质干细胞可以通过介入核因子κB信号或分泌白细胞介素1R的拮抗剂来抑制巨噬细胞,而产生白细胞介素1β的单核细胞又可以介导促进间充质干细胞的转化生长因子β的分泌。间充质干细胞不仅可以募集单核巨噬细胞,诱导控制M2型巨噬细胞的极化,还会受到单核巨噬细胞的负反馈调节,分化为成骨细胞,从而支持组织再生[56]。 2.3.3 生长发育与上颌骨扩弓 生长发育的过程中,颅面骨发育以膜内成骨为主要生长方式,其中骨缝作为成骨的重要位点,需要有充足的成骨相关细胞募集至成骨前沿,同时骨缝间细胞需要维持未分化状态[9]。成骨前体细胞分化为成骨细胞,分泌细胞外基质蛋白,同时启动矿化,形成新骨,从而增大骨体积。如果颅骨骨缝融合过早或者其间骨增长过多,则会导致颅缝早闭等。腭中缝融合一直被认为是上颌骨扩弓治疗在成人中进行的阻碍之一[13],是否能通过在生长发育结束前抑制骨缝融合,或者重新打开已经融合的骨缝,使得成人的上颌骨重新获得“生长潜力”,再配合机械力的施加,从而达到与生长发育期上颌骨扩弓相同的疗效,这就给上颌骨横向发育不足治疗提供了新方向。 颅骨骨缝间融合机制的研究进展及颅缝早闭的新兴治疗方法,也为上颌骨扩弓治疗思路增添了可能性。近年来关于颅缝早闭的治疗方法进展趋向于制造相关致病基因学修饰小鼠模型,进行颅缝早闭遗传分子机制及基因或细胞治疗,通过抑制不同细胞通路逆转颅缝早闭的发生。其中,颅骨骨缝间融合受到许多基因及信号通路调节[58],包括成纤维细胞生长因子受体(FGFR1、FGFR2、FGFR3),转化生长因子β信号通路受体(TGFBR1、TGFBR2),HH信号通路配体IHH,骨形态发生蛋白信号通路转录因子MSX、EFNB1等都会影响颅面骨缝的闭合[59];XU等[60]研究发现诱导FGFR2基因激活会在成人阶段通过提高间充质干细胞成骨分化和增殖来增加骨形成;TWIST1对于头面骨形成时期间充质干细胞的早期迁移和存活必不可少[61]。同样,腭骨的生长发育也受到一些信号的调节,其中,LEVI等[62]研究发现在硬腭的生长发育中IHH信号上调从而促进成骨;XU等[63]研究发现FGF8信号可能会抑制间质细胞成骨分化,从而影响腭骨形成。 在颅缝早闭的治疗方法进展方面,有学者利用抗癌药物或纯化可溶性FGFR2相关药物等在小鼠模型中抑制FGFR的信号传导通路(即RAS-ERK途径),从而逆转颅缝早闭的情 况[64-65];多个研究表明酪氨酸激酶抑制剂在动物模型实验中对颅底、面中部骨缝进一步融合有抑制作用[66]。这对上颌骨扩弓治疗方法具有提示作用,可以通过调节不同细胞通路来抑制骨缝的融合,从而促进上颌骨开展。同时,骨缝的生长发育可能与对机械应力有反应的细胞信号通路有关,机械力可能会激活信号通路并改变骨缝中成骨基因的表达。SOH 等[67]研究发现循环应力相比于连续的静态力更能引起骨缝成骨反应;BARRETO等[68]研究发现骨缝过早融合可能和异常的机械环境有关,同时通过激活JNK3和WNT2的MAPK相关非经典WNT信号通路,可以加速融合骨缝处的成骨,循环拉伸可以增加MAPK磷酸化水平,增加的水平随着拉应力施加的频率增加而提高[69]。这也提示若上颌骨扩弓时采用循环应力可能相较于静态力更能促进骨缝间骨的形成。上颌骨扩弓机制研究的示意图见图2。 "
| [1] 吕晨星,杨柳,陈璐璐,等. 支抗种植体辅助上颌快速扩弓的研究进展[J].中华口腔医学杂志,2019,54(11):778-782. [2] MCNAMARA JA JR, LIONE R, FRANCHI L, et al. The role of rapid maxillary expansion in the promotion of oral and general health. Prog Orthod. 2015;16:33. [3] 李鑫.五种腭中缝扩展技术的临床应用[J].临床口腔医学杂志,2019, 35(12):757-759. [4] STARCH-JENSEN T, BLÆHR TL. Transverse Expansion and Stability after Segmental Le Fort I Osteotomy versus Surgically Assisted Rapid Maxillary Expansion: a Systematic Review. J Oral Maxillofac Res. 2016; 7(4):e1. [5] 贾海潮,庄丽,张楠,等.个性化微螺钉辅助上颌快速扩弓器的设计及应用研究[J].中华口腔正畸学杂志,2020,27(1):4-8. [6] CHOI SH, SHI KK, CHA JY, et al. Nonsurgical miniscrew-assisted rapid maxillary expansion results in acceptable stability in young adults. Angle Orthod. 2016;86(5):713-720. [7] BÜYÜKÇAVUŞ MH. Alternate Rapid Maxillary Expansion and Constriction (Alt-RAMEC) protocol: A Comprehensive Literature Review.Turk J Orthod. 2019;32(1):47-51. [8] 冯光耀, 邹冰爽, 曾祥龙, 等.上颌牙弓反复快速扩缩配合较轻前方牵引力矫治安氏Ⅲ错(牙合)的临床疗效分析[J].中华口腔正畸学杂志,2017,24(4):217-220. [9] AL-REKABI Z, CUNNINGHAM ML, SNIADECKI NJ. Cell Mechanics of Craniosynostosis. ACS Biomater Sci Eng. 2017;3(11):2733-2743. [10] ABO SAMRA D, HADAD R. Midpalatal suture: evaluation of the morphological maturation stages via bone density. Prog Orthod. 2018; 19(1):29. [11] GRÜNHEID T, LARSON CE, LARSON BE. Midpalatal suture density ratio: A novel predictor of skeletal response to rapid maxillary expansion.Am J Orthod Dentofacial Orthop. 2017;151(2):267-276. [12] SAYAR G, KıLıNÇ DD. Rapid maxillary expansion outcomes according to midpalatal suture maturation levels. Prog Orthod. 2019;20(1):27. [13] ANGELIERI F, CEVIDANES LH, FRANCHI L,et al. Midpalatal suture maturation: classification method for individual assessment before rapid maxillary expansion. Am J Orthod Dentofacial Orthop. 2013; 144(5):759-769. [14] 高璐,谷岩.中国人群腭中缝生长发育形态特点分期与其相应生理年龄分布的初步研究[J].中华口腔正畸学杂志,2020,27(2):61-6. [15] SAVOLDI F, XU B, TSOI JKH,et al. Anatomical and mechanical properties of swine midpalatal suture in the premaxillary, maxillary, and palatine region. Scientific Reports. 2018;8(1):7073. [16] PRIYADARSHINI J, MAHESH CM, CHANDRASHEKAR BS,et al. Stress and displacement patterns in the craniofacial skeleton with rapid maxillary expansion-a finite element method study. Prog Orthod. 2017;18(1):17. [17] WU BH, KOU XX, ZHANG C,et al. Stretch force guides finger-like pattern of bone formation in suture. PloS one. 2017;12(5):e0177159. [18] CHENG Y, LV C, LI T, et al. Palatal expansion and relapse in rats: A histologic and immunohistochemical study. Am J Orthod Dentofacial Orthop. 2020;157(6):783-791. [19] GUERRERO JA, SILVA RS, DE ABREU LIMA IL,et al. Maxillary suture expansion: A mouse model to explore the molecular effects of mechanically-induced bone remodeling. J Biomech. 2020;108:109880. [20] CAPRIOGLIO A, FASTUCA R, ZECCA PA, et al. Cellular Midpalatal Suture Changes after Rapid Maxillary Expansion in Growing Subjects: A Case Report. Int J Mol Sci. 2017;18(3):615. [21] BOYCE BF. Advances in the regulation of osteoclasts and osteoclast functions. J Dent Res. 2013;92(10):860-867. [22] ONO T, NAKASHIMA T. Recent advances in osteoclast biology.Histochem Cell Biol. 2018;149(4):325-341. [23] HAYAKAWA T, YOSHIMURA Y, KIKUIRI T,et al. Optimal compressive force accelerates osteoclastogenesis in RAW264.7 cells. Mol Med Rep. 2015;12(4):5879-5885. [24] WU SH, ZHONG ZM, CHEN JT. Low-magnitude high-frequency vibration inhibits RANKL-induced osteoclast differentiation of RAW264.7 cells. Int J Med Sci. 2012;9(9):801-807. [25] XU XY, GUO C, YAN YX,et al. Differential effects of mechanical strain on osteoclastogenesis and osteoclast-related gene expression in RAW264.7 cells. Mol Med Rep. 2012;6(2):409-415. [26] WINTERS R,TATUM SA.Craniofacial distraction osteogenesis.Facial Plast Surg Clin North Am. 2014;22(4):653-664. [27] HUANG H, YANG R, ZHOU YH. Mechanobiology of Periodontal Ligament Stem Cells in Orthodontic Tooth Movement. Stem Cells Int. 2018;2018:6531216. [28] ZHAO H, FENG J, HO TV, et al. The suture provides a niche for mesenchymal stem cells of craniofacial bones. Nat Cell Biol. 2015;17(4):386-396. [29] MARUYAMA T, JEONG J, SHEU TJ,et al. Stem cells of the suture mesenchyme in craniofacial bone development, repair and regeneration. Nat Commun. 2016;7:10526. [30] WILK K, YEH SA, MORTENSEN LJ, et al. Postnatal calvarial skeletal stem cells expressing prx1 reside exclusively in the calvarial sutures and are required for bone regeneration. Stem cell reports. 2017;8(4):933-946. [31] GUO Y, YUAN Y, WU L, et al. BMP-IHH-mediated interplay between mesenchymal stem cells and osteoclasts supports calvarial bone homeostasis and repair. Bone Res. 2018;6:30. [32] ABE T, SUMI K, KUNIMATSU R, et al. The effect of mesenchymal stem cells on osteoclast precursor cell differentiation. J Oral Sci. 2019;61(1): 30-35. [33] ZHAO P, XIAO L, PENG J, et al. Exosomes derived from bone marrow mesenchymal stem cells improve osteoporosis through promoting osteoblast proliferation via MAPK pathway. Eur Rev Med Pharmacol Sci. 2018;22(12):3962-3970. [34] MASAOUTIS C, THEOCHARIS S. The Role of Exosomes in Bone Remodeling: Implications for Bone Physiology and Disease. Disease Markers. 2019;2019:9417914. [35] QI X, ZHANG J, YUAN H,et al. Exosomes Secreted by Human-Induced Pluripotent Stem Cell-Derived Mesenchymal Stem Cells Repair Critical-Sized Bone Defects through Enhanced Angiogenesis and Osteogenesis in Osteoporotic Rats. Int J Biol Sci. 2016;12(7):836-849. [36] ZHANG J, LIU X, LI H,et al. Exosomes/tricalcium phosphate combination scaffolds can enhance bone regeneration by activating the PI3K/Akt signaling pathway. Stem Cell Res Ther. 2016;7(1):136. [37] CUI Y, LUAN J, LI H,et al. Exosomes derived from mineralizing osteoblasts promote ST2 cell osteogenic differentiation by alteration of microRNA expression. FEBS letters. 2016;590(1):185-192. [38] QIN Y, SUN R, WU C,et al. Exosome: A Novel Approach to Stimulate Bone Regeneration through Regulation of Osteogenesis and Angiogenesis. Int J Mol Sci. 2016;17(5):712. [39] QIN Y, WANG L, GAO Z,et al. Bone marrow stromal/stem cell-derived extracellular vesicles regulate osteoblast activity and differentiation in vitro and promote bone regeneration in vivo. Sci Rep. 2016;6:21961. [40] MA Q, LIANG M, WU Y, et al. Mature osteoclast-derived apoptotic bodies promote osteogenic differentiation via RANKL-mediated reverse signaling. J Biol Chem. 2019;294(29):11240-11247. [41] LIU D, KOU X,CHEN C,et al.Circulating apoptotic bodies maintain mesenchymal stem cell homeostasis and ameliorate osteopenia via transferring multiple cellular factors. Cell Res. 2018;28(9):918-933. [42] HE D, LIU F, CUI S, et al. Mechanical load-induced H(2)S production by periodontal ligament stem cells activates M1 macrophages to promote bone remodeling and tooth movement via STAT1. Stem Cell Res Ther. 2020;11(1):112. [43] HE X, DONG Z, CAO Y, et al. MSC-Derived Exosome Promotes M2 Polarization and Enhances Cutaneous Wound Healing. Stem Cells Int. 2019;2019:7132708. [44] QIU X, LIU S, ZHANG H,et al. Mesenchymal stem cells and extracellular matrix scaffold promote muscle regeneration by synergistically regulating macrophage polarization toward the M2 phenotype. Stem Cell Res Ther. 2018;9(1):88. [45] VINING KH, MOONEY DJ. Mechanical forces direct stem cell behaviour in development and regeneration. Nat Rev Mol Cell Biol. 2017;18(12):728-742. [46] LI W, ZHAO J, WANG J,et al. ROCK-TAZ signaling axis regulates mechanical tension-induced osteogenic differentiation of rat cranial sagittal suture mesenchymal stem cells.J Cell Physiol. 2020;235(9): 5972-5984. [47] FRANK V, KAUFMANN S, WRIGHT R, et al. Frequent mechanical stress suppresses proliferation of mesenchymal stem cells from human bone marrow without loss of multipotency. Scientific reports. 2016;6:24264. [48] FIERRO FA, NOLTA JA, ADAMOPOULOS IE. Concise Review: Stem Cells in Osteoimmunology. Stem cells (Dayton, Ohio). 2017;35(6):1461-1467. [49] OKAMOTO K, NAKASHIMA T, SHINOHARA M,et al. Osteoimmunology: The Conceptual Framework Unifying the Immune and Skeletal Systems. Physiol Rev. 2017;97(4):1295-1349. [50] LI J, YU TT, YAN HC, et al. T cells participate in bone remodeling during the rapid palatal expansion. FASEB J. 2020;34(11):15327-15337. [51] BOZEC A, ZAISS MM, KAGWIRIA R, et al. T cell costimulation molecules CD80/86 inhibit osteoclast differentiation by inducing the IDO/tryptophan pathway. Sci Transl Med. 2014;6(235):235ra60. [52] GORDON S,MARTINEZ FO.Alternative activation of macrophages: mechanism and functions. Immunity. 2010;32(5):593-604. [53] HE D, KOU X, YANG R,et al. M1-like Macrophage Polarization Promotes Orthodontic Tooth Movement. J Dent Res. 2015;94(9):1286-1294. [54] HE D, KOU X, LUO Q,et al. Enhanced M1/M2 macrophage ratio promotes orthodontic root resorption. J Dent Res. 2015;94(1):129-139. [55] YANG D, WAN Y. Molecular determinants for the polarization of macrophage and osteoclast. Semin Immunopathol. 2019;41(5):551-563. [56] LE BLANC K, MOUGIAKAKOS D. Multipotent mesenchymal stromal cells and the innate immune system. Nat Rev Immunol. 2012;12(5):383-396. [57] JIN SS, HE DQ, LUO D,et al. A Biomimetic Hierarchical Nanointerface Orchestrates Macrophage Polarization and Mesenchymal Stem Cell Recruitment To Promote Endogenous Bone Regeneration. ACS nano. 2019;13(6):6581-6595. [58] 李国清, 寇瑶, 程铭津,等. 颅缝早闭症与FGF信号通路[J].组织工程与重建外科杂志,2017,13(4):215-219. [59] JOHNSON D, WILKIE AOM. Craniosynostosis. Eur J Hum Genet. 2011; 19(4):369-376. [60] XU W, LUO F, WANG Q,et al. Inducible Activation of FGFR2 in Adult Mice Promotes Bone Formation After Bone Marrow Ablation.J Bone Miner Res. 2017;32(11):2194-2206. [61] YILMAZ E, MIHCI E, NUR B,et al. Recent Advances in Craniosynostosis. Pediatr Neurol. 2019;99:7-15. [62] LEVI B, JAMES AW, NELSON ER,et al. Role of Indian hedgehog signaling in palatal osteogenesis. Plast Reconstr Surg. 2011;127(3):1182-1190. [63] XU J, HUANG Z, WANG W, et al. FGF8 Signaling Alters the Osteogenic Cell Fate in the Hard Palate. J Dent Res. 2018;97(5):589-596. [64] MORITA J, NAKAMURA M, KOBAYASHI Y, et al. Soluble form of FGFR2 with S252W partially prevents craniosynostosis of the apert mouse model. Dev Dyn. 2014;243(4):560-567. [65] YOKOTA M, KOBAYASHI Y, MORITA J,et al. Therapeutic effect of nanogel-based delivery of soluble FGFR2 with S252W mutation on craniosynostosis. PloS one. 2014;9(7):e101693. [66] RACHWALSKI M,KHONSARI RH,PATERNOSTER G.Current Approaches in the Development of Molecular and Pharmacological Therapies in Craniosynostosis Utilizing Animal Models. Mol Syndromol. 2019; 10(1-2):115-123. [67] SOH SH, RAFFERTY K, HERRING S. Cyclic loading effects on craniofacial strain and sutural growth in pigs. Am J Orthod Dentofacial Orthop. 2018;154(2):270-282. [68] BARRETO S,GONZÁLEZ-VÁZQUEZ A,A RC,et al. Identification of stiffness-induced signalling mechanisms in cells from patent and fused sutures associated with craniosynostosis. Sci Rep. 2017;7(1):11494. [69] HSU HJ, LEE CF, LOCKE A,et al. Stretch-induced stress fiber remodeling and the activations of JNK and ERK depend on mechanical strain rate, but not FAK. PloS one. 2010;5(8):e12470. (责任编辑:WZH,ZN,ZH) |
| [1] | Pu Rui, Chen Ziyang, Yuan Lingyan. Characteristics and effects of exosomes from different cell sources in cardioprotection [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 1-. |
| [2] | Lin Qingfan, Xie Yixin, Chen Wanqing, Ye Zhenzhong, Chen Youfang. Human placenta-derived mesenchymal stem cell conditioned medium can upregulate BeWo cell viability and zonula occludens expression under hypoxia [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 4970-4975. |
| [3] | Zhang Shangpu, Ju Xiaodong, Song Hengyi, Dong Zhi, Wang Chen, Sun Guodong. Arthroscopic suture bridge technique with suture anchor in the treatment of acromioclavicular dislocation [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1417-1422. |
| [4] | Hou Jingying, Yu Menglei, Guo Tianzhu, Long Huibao, Wu Hao. Hypoxia preconditioning promotes bone marrow mesenchymal stem cells survival and vascularization through the activation of HIF-1α/MALAT1/VEGFA pathway [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 985-990. |
| [5] | Shi Yangyang, Qin Yingfei, Wu Fuling, He Xiao, Zhang Xuejing. Pretreatment of placental mesenchymal stem cells to prevent bronchiolitis in mice [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 991-995. |
| [6] | Liang Xueqi, Guo Lijiao, Chen Hejie, Wu Jie, Sun Yaqi, Xing Zhikun, Zou Hailiang, Chen Xueling, Wu Xiangwei. Alveolar echinococcosis protoscolices inhibits the differentiation of bone marrow mesenchymal stem cells into fibroblasts [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 996-1001. |
| [7] | Fan Quanbao, Luo Huina, Wang Bingyun, Chen Shengfeng, Cui Lianxu, Jiang Wenkang, Zhao Mingming, Wang Jingjing, Luo Dongzhang, Chen Zhisheng, Bai Yinshan, Liu Canying, Zhang Hui. Biological characteristics of canine adipose-derived mesenchymal stem cells cultured in hypoxia [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1002-1007. |
| [8] | Geng Yao, Yin Zhiliang, Li Xingping, Xiao Dongqin, Hou Weiguang. Role of hsa-miRNA-223-3p in regulating osteogenic differentiation of human bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1008-1013. |
| [9] | Lun Zhigang, Jin Jing, Wang Tianyan, Li Aimin. Effect of peroxiredoxin 6 on proliferation and differentiation of bone marrow mesenchymal stem cells into neural lineage in vitro [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1014-1018. |
| [10] | Zhu Xuefen, Huang Cheng, Ding Jian, Dai Yongping, Liu Yuanbing, Le Lixiang, Wang Liangliang, Yang Jiandong. Mechanism of bone marrow mesenchymal stem cells differentiation into functional neurons induced by glial cell line derived neurotrophic factor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1019-1025. |
| [11] | Duan Liyun, Cao Xiaocang. Human placenta mesenchymal stem cells-derived extracellular vesicles regulate collagen deposition in intestinal mucosa of mice with colitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1026-1031. |
| [12] | Pei Lili, Sun Guicai, Wang Di. Salvianolic acid B inhibits oxidative damage of bone marrow mesenchymal stem cells and promotes differentiation into cardiomyocytes [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1032-1036. |
| [13] | Wang Xianyao, Guan Yalin, Liu Zhongshan. Strategies for improving the therapeutic efficacy of mesenchymal stem cells in the treatment of nonhealing wounds [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1081-1087. |
| [14] | Wang Shiqi, Zhang Jinsheng. Effects of Chinese medicine on proliferation, differentiation and aging of bone marrow mesenchymal stem cells regulating ischemia-hypoxia microenvironment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1129-1134. |
| [15] | Kong Desheng, He Jingjing, Feng Baofeng, Guo Ruiyun, Asiamah Ernest Amponsah, Lü Fei, Zhang Shuhan, Zhang Xiaolin, Ma Jun, Cui Huixian. Efficacy of mesenchymal stem cells in the spinal cord injury of large animal models: a meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1142-1148. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||