Chinese Journal of Tissue Engineering Research ›› 2020, Vol. 24 ›› Issue (21): 3363-3371.doi: 10.3969/j.issn.2095-4344.2662
Previous Articles Next Articles
Research and application of tissue optical clearing technique
Tian Ting1, Yang Zhaoyang2, 3, Li Xiaoguang1, 2, 3
- 1Beijing Key Laboratory of Biomaterials and Neural Regeneration, School of Biological and Medical Engineering; 2Department of Neurobiology, School of Basic Medical Sciences, Capital Medical University; 3Beijing International Science and Technology Cooperation Base of Biomaterials and Neural Regeneration, Beijing Biomedical Engineering High-tech Innovation Center
-
Received:2019-09-03Revised:2019-09-05Accepted:2019-10-24Online:2020-07-28Published:2020-04-17 -
Contact:Li Xiaoguang, MD, Professor, Beijing Key Laboratory of Biomaterials and Neural Regeneration, School of Biological and Medical Engineering, Beihang University, Beijing 100083, China; Department of Neurobiology, School of Basic Medical Sciences, Capital Medical University, Beijing 100069, China; Beijing International Science and Technology Cooperation Base of Biomaterials and Neural Regeneration, Beijing Biomedical Engineering High-tech Innovation Center, Beihang University, Beijing 100083, China -
About author:Tian Ting, Doctoral candidate, Beijing Key Laboratory of Biomaterials and Neural Regeneration, School of Biological and Medical Engineering, Beihang University, Beijing 100083, China -
Supported by:the National Natural Science Foundation of China, No. 31730030 and 31650001, 31670988 and 31971279, and 31970970; National Key Research and Development Project, No. 2017YFC1104001 and 2017YFC1104002; 2018 Annual Science and Technology Plan Key Project of Beijing Municipal Education Commission, No. KZ201810025030
CLC Number:
Cite this article
Tian Ting, Yang Zhaoyang, Li Xiaoguang. Research and application of tissue optical clearing technique[J]. Chinese Journal of Tissue Engineering Research, 2020, 24(21): 3363-3371.
share this article
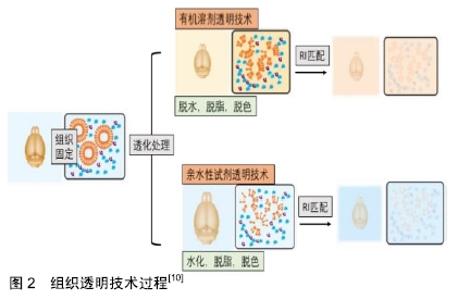
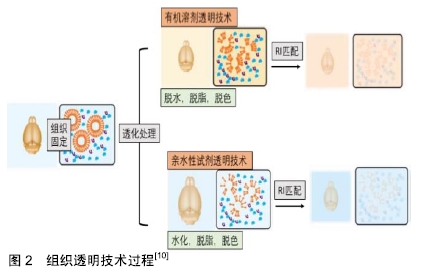
2.1 组织透明技术原理及过程 生物组织的不透明性是由不同光学特性的非均质成分造成的,如折射率(RI)和光吸收率,大多数生物组织由高折射率的散射粒子,如脂质、蛋白、髓鞘,弹性纤维,以及低折射率的周围介质,如细胞间质液和细胞质共同组成的。由于每种成分具有不同的折射率,这种非均质物质结构会使入射光发生散射,限制了光学成像深度[9]。此外,内源性色素如血红素、核黄素、黑色素和脂褐素的光吸收也会使光传播衰减[10]。因此改变组织非均质成分的光学特性,降低光散射和光吸收是增加组织成像深度的关键。1个世纪前,SPALTEHOLZ[11]首次引入3D组织标本的透明原理,在此研究基础上,GENINA等[12]将组织浸入光学透明剂中平衡折射率,使组织变得更加透明,进一步增加了成像深度。 随着光学显微镜的发展和普及,以及数据采集和存储技术的进步,组织透明技术使全器官甚至全身成像成为可能,近年来研究人员开发出一系列组织透明技术(见表1),所有透明技术都致力于平衡组织折射率,以减少光散射的不均一性。 "
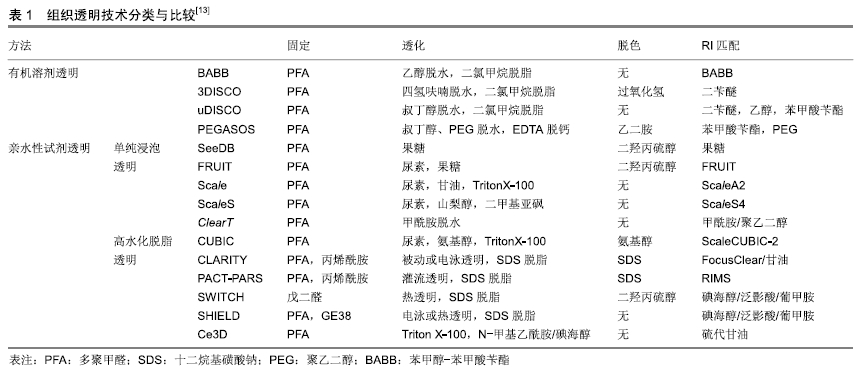

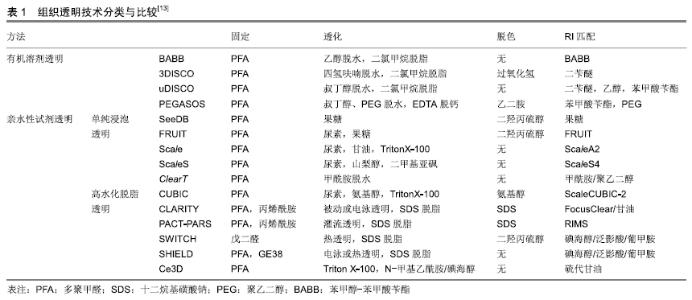
2.2 组织透明技术分类 目前组织透明技术主要分为两类:有机溶剂透明技术和亲水性试剂透明技术(见表1)。 2.2.1 有机溶剂透明 有机溶剂透明技术主要是应用含有高折射率介质的光学透明剂取代组织中水分和脂质来平衡组织折射率,使组织达到光学透明。透明方案包括2个步骤:①脱水/脱脂;②光学透明剂浸透。高折射率介质与水不混溶,因此需要应用有机溶剂进行组织脱水,脂质是光散射的主要来源,脂质双分子层决定细胞膜的通透性,因此,组织脱水后必须进行脱脂处理,以促进光学透明剂向深层组织渗透。 SPALTEHOLTZ[11]首次应用有机溶剂透明组织样本,制作出光学透明器官,推动了解剖学的发展进程。DODT小组[14]在此基础上进行改良,采用乙醇脱水,BABB脱脂,透明完整小鼠胚胎和新生小鼠大脑,结合光片显微成像技术,对完整海马进行三维图像,获得了CA1神经元树突树和树突棘在细胞分辨率水平的三维图像。但是,苯甲醇-苯甲酸苄酯(BABB)透明最大的缺陷是乙醇脱水会导致内源性荧光蛋白淬灭,为了解决这一问题,ERTüRK小组[15]应用四氢呋喃孵育代替乙醇脱水,保护绿色荧光蛋白(GFP)信号,同时应用二苄醚(DBE)替代BABB以提高透明效率,开发出基于四氢呋喃和DBE的新型透明方案3DISCO。3DISCO能够快速透明多种器官组织,包括小鼠大脑,肺脏,肿瘤及人类胚胎等[16-18],并有效延长了绿色荧光蛋白的表达时间。为了充分保存内源性荧光蛋白,RENIER团队[19]结合3DISCO透明,建立了一种全组织包埋免疫标记的三维成像技术iDISCO,应用免疫标记实现目的蛋白的可视化。iDISCO通过组织脱水脱脂,增加抗体渗透性,能够对小鼠胚胎及成年小鼠组织(如肾脏,大脑)进行可视化三维免疫标记,结合AAV2病毒示踪,iDISCO展示了视神经损伤后神经退变及再生的三维成像。虽然3DISCO能够保护内源性荧光蛋白,但是DBE的降解产物如过氧化物或醛类物质,会对荧光蛋白产生有害干扰,荧光蛋白信号仅能维持几天,为了克服这一缺陷,Dodt引入抗氧化剂没食子酸丙酯抑制DBE降解产物的积累,设计出sDISCO透明方案,高效透明组织样本的同时,有效保存透明样品的荧光信号和组织结构,结合STED,树突棘结构清晰可见[20]。 为了更有效地保存内源性荧光蛋白,ERTüRK小组开发出一种基于DPE的透明技术uDISCO,可以高效透明啮齿类动物及临床人类标本[21],有效保存荧光蛋白信号长达数月,结合显微成像技术,uDISCO能够完成小鼠全身血管生成的三维成像,此外,uDISCO可以与多种标记技术兼容,如病毒示踪和免疫染色[21]。但是对于绿色荧光蛋白表达水平较低的样品,uDISCO保存荧光蛋白信号的能力并不理想。朱丹课题组在uDISCO基础上,调整试剂pH值,推出改良透明方案a-uDISCO[22],能够更好地保留绿色荧光蛋白荧光,并且以高质量成像展示了整个小鼠大脑神经元网络,a-uDISCO是绿色荧光蛋白低表达样品成像的优先选择。为了增强荧光蛋白信号强度,CAI等[23]随即开发出一种基于纳米体的全身免疫标记技术vDISCO,纳米体标记显著提高了荧光染料对大型组织的标记效率,使荧光信号强度增强100倍,因此能够对透明小鼠进行从头到脚的光学成像和亚细胞水平的量化分析。结合光片显微,ERTüRK团队首次构建出成年小鼠神经元全身投射图,并揭示了急性中枢神经系统损伤后远端神经末梢的投射变化和炎症过程。虽然uDISCO能够透明大部分小鼠器官,但是对肝脏、脾脏等器官以及硬组织的透明效果欠佳,为了提高全身透明效率,赵瑚团队开发出一种基于聚乙二醇(PEG)的新型全组织透明技术PEGASOS[24],通过脱钙,脱色,脱水,脱脂等优化处理,该透明技术首次实现了对动物软、硬组织的同时透明化,包括骨骼、牙齿、大脑、肌肉等,结合Thy1-EGFP转基因小鼠,赵瑚团队对完整脊柱进行三维成像,展示了脊髓神经纤维走行以及DRG与脊髓的连接关系。 基于有机溶剂的透明技术在透明动力学上具有一定的优势,能快速高效透明多种类型组织样本。但是有机溶剂透明会导致样本大幅度皱缩,对组织结构和蛋白具有潜在的破坏性;此外有机溶剂具有一定的毒性和腐蚀性,需要特殊防护,并且需要特殊物镜进行成像,限制了其广泛应用。 2.2.2 亲水性试剂透明 由于有机溶剂透明存在一定的局限性,许多研究人员开始寻求基于亲水性试剂的透明方案。目前,亲水性试剂透明主要包括2种:单纯浸泡透明和高水化脱脂透明。 (1)单纯浸泡透明:是指将样本放置在含高折射率介质的水溶液中孵育,在渗透压驱动下逐渐完成透明。在水溶性溶剂中,尿素分子(相对分子质量60,分子半径0.22 nm)是最具渗透性的分子之一,由于其具有供氢基团和受体基团,因此具有较强水化能力[10]。基于尿素的透明技术Scale[25],能够在保存荧光蛋白的前提下,透明小鼠胚胎及大脑组织切片(约3 mm厚),结合双光子显微镜,Scale能够对新生小鼠大脑皮质进行三维成像,皮质V/VI层锥体神经元及其树突网络结构清晰可见,甚至能观察到单个树突棘结构。但是Scale透明速率缓慢,并且会导致组织膨胀和某些蛋白丢失。为了克服这些缺陷,HAMA小组[26]开发出一种基于尿素和山梨醇的透明方案ScaleS,能快速透明小鼠大脑半球而不引起明显的组织变形,同时组织超微结构保存良好,透明样本可以在透明试剂中稳定保存1年。应用ScaleS,HAMA展示了阿尔茨海默病模型中Aβ淀粉样斑块的3D网络结构,并对单个斑块进行了多维度追踪。基于果糖的透明方案SeeDB[27],能在几天内透明成年小鼠大脑半球,并且对内源性荧光蛋白和亲脂性神经示踪剂有较好的兼容性,透明过程样本体积无明显改变。结合双光子显微镜,SeeDB展示了小鼠嗅球中僧帽细胞的完整连接图以及树突连接模式的多样性,为研究编码气味的神经元提供了解剖基础。然而,饱和果糖溶液黏度较高,不利于制备、操作和清洗,并且易产生气泡,极大限制了成像过程中样品的移动。为了解决这一问题,HOU等[28]设计出基于果糖和尿素的透明技术FRUIT,能够透明成年兔的全脑,同时兼容EYFP及亲脂性示踪剂DiI。但是基于果糖的透明技术(如SeeDB、FRUIT)会使样本发生美拉德褐变反应,即使添加还原剂也不能完全避免,因此透明样本不能长期保存。 单纯浸泡透明方法简单,易于操作,经济可行,并且与多种荧光蛋白和亲脂性染料兼容,但是由于没有去除组织中脂质成分,透明效果欠佳,透明速率较低,不适合大样本透明。 (2)高水化脱脂透明:由于高折射率介质分子体积较大,不易在组织内扩散,因此,组织脱脂是提高组织渗透性和透明效率的关键。 洗涤剂能够有效去除脂质,所有CLARITY相关的透明技术都是基于洗涤剂的脱脂作用,水凝胶包埋为组织提供物理框架支持,与蛋白质、核酸等生物分子形成共价连接,使细胞结构和分子信息得到有效保存。但是洗涤剂分子量较大,在组织中渗透缓慢,因此需要提高洗涤剂在组织内的扩散动力学,实现深层组织充分脱脂。为此,DEISSEROTH团队首先引入基于电泳的组织透明技术ETC-CLARITY[29],电泳组织透明(ETC)促进洗涤剂十二烷基磺酸钠(SDS)向深层组织主动扩散,有效去除脂质,加快成年小鼠大脑的透明速度,而组织分子信息和精细结构如膜定位蛋白,突触等保存完好。应用CLARITY透明技术,CHUNG等[29]实现了对成年小鼠完整大脑的三维免疫标记成像。结合CLARITY和免疫标记,SARITAS等[30]在三维水平评估了饮食钾限制对肾小管长度和增殖的影响,为肾小管可以快速适应饮食提供了理论依据。为了简化电泳系统,缩短样本处理时间,杜浩小组建立非循环电泳系统,并开发出改良透明技术PRE-CLARITY和离心-膨胀染色技术(CEx染色)[31],能够更快、更充分地透明和标记完整小鼠大脑。ETC虽然可以快速组织透明进度,但是可能会因样品加热导致组织降解,被动CLARITY可以避免这种风险[32],但是透明速度缓慢,不适合大样本或全身透明。为了温和快速的透明整个生物体,TREWEEK等[33]开发出PACT-PARS透明技术,在优化透明试剂的基础上,通过持续心脏压力灌注取代ETC驱动,促进全身透明和免疫标记,同时应用新型折射率匹配试剂RIMS优化成像质量。PACT-PARS可以在两三天内透明大部分组织器官,一两周内透明小鼠大脑,并且与内源性荧光蛋白,免疫标记以及单分子RNA原位杂交有良好的兼容性,能够获取透明组织内高分辨率的细胞及亚细胞结构信息。应用PACT-PARS,DABROWSKA等[34]研究癫痫发作时海马到双侧运动皮质的神经回路激活情况,揭示了癫痫传播路径及逆行性遗忘可能的机制。为了增加骨透明度,GRADINARU开发出Bone CLARITY,用于透明小鼠全骨,结合LSFM,能够快速、全面地展示完整骨组织的生物学过程[35]。为了降低透明成本,ROZA小组在原始CLARITY基础上,进行优化改良,设计出一种简单廉价的被动透明方案inCLARITY,对外周神经和完整DRG进行免疫标记和透明,inCLARITY与多种逆性神经示踪剂兼容,如荧光金(FG),Dil等,适合用于研究外周神经系统损伤及修复过程中神经纤维的变化规律[36]。 基于戊二醛的透明技术SWITCH,通过缓冲液切换,将组织转化为耐热和耐化学的凝胶混合物,便于多轮免疫标记,应用SDS高温脱脂,可以快速透明组织,而组织结构、生物分子和抗原性不受损伤。该技术不需要灌注,也不需要任何特殊设备或试剂,因此适用于动物和人类样本。利用SWITCH,MURRAY等[37]对人类皮质进行蛋白表达谱分析,并研究了小鼠大脑神经纤维通路的几何结构。为了更好地保存关键分子信息,PARK等[38]建立了SHIELD技术,通过环氧化物交联增强核酸和蛋白质三级结构的稳定性,能够在充分保存荧光蛋白、抗原和转录本的情况下快速透明组织。结合SHIELD,Park检测了小鼠树突棘的形态结构和病毒标记神经元的分子特征以及靶向投射,同时展示了人类活检组织和脑细胞的三维分子表型。 基于尿素的高水化作用以及多元醇的脱脂脱色功能,UEDA小组开发出鸡尾酒透明方案CUBIC,可以透明完整幼鼠和成年小鼠全身,结合光片显微镜,能够在单细胞分辨率下对全身或全器官进行快速三维成像[39]。CUBIC也适用于多种器官的三维免疫标记成像,HASEGAWA等[40]应用CUBIC对小鼠肾脏进行透明和免疫标记,体积成像结果显示肾缺血-再灌注损伤后交感神经会发生失神经支配,并且会持续28 d,提示慢性肾病进展过程中交感神经持续异常,CUBIC-透明肾为肾脏研究提供了全面、宏观的视角。为了提高全身透明效率,UEDA小组对1 600种亲水性试剂进行综合筛选、分析,得到更新的鸡尾酒配方CUBIC-2,通过优化脱脂、脱色、脱钙和折射率匹配环节,CUBIC-2能够有效透明小鼠全身以及灵长类动物组织,包括狨猴大脑和人类组织样本>10 cm3 [41]。结合转基因小鼠,CUBIC-2完成了多重神经元标记的全脑成像,有助于在全脑水平对椎体神经元、多巴胺能神经元、星形胶质细胞、少突胶质细胞等进行表达及分布比较。基于尿素和氨基糖的透明方法UbasM,在维持高效透明能力的同时,能够保护荧光基团发射及细胞膜的完整性,与亲脂性染料兼容,结合单光子显微镜,可对厘米尺度的样品进行三维成像[42]。专门为人类组织研发的透明技术OPTIClear,能有效透明新鲜和甲醛固定石蜡包埋的人类脑组织(5 mm厚),对超微结构保存良好,并且与多种荧光染料和亲脂性染料兼容,结合亲脂性染料示踪,OPTIClear可对人类脑组织神经元投射和树突棘结构进行高分辨率三维成像[43]。 GERNER团队最近研发出一种新型透明增强3D技术Ce3D[44],该技术应用N-甲基乙酰胺和碘海醇的混合液孵育组织,同时加入Triton X-100脱脂以提高透明效率。Ce3D能够在不脱钙的情况下快速透明整个股骨以及脑、肺、肾、肝、淋巴结等小鼠组织,同时有效保护多种报告蛋白和有机荧光基团,维持细胞形态,并对组织有较高的免疫标记能力。应用Ce3D技术,GERNER小组对致密淋巴组织的细胞表型进行精确定量分析,使用优化算法对细胞进行三维体积分割,并对人体活检样本进行了强劲的免疫染色、透明和成像。此外,Ce3D与RNA转录本检测兼容,Ce3D抗体染色结合RNAscope技术,能够对大体积组织中的RNA转录本进行高质量检测[45]。通过与其他透明方法比较,Bossolani发现Ce3D是完整肠段三维成像的首透明除方案,对于解析整个消化道内神经-免疫-血管交互网络中不同亚型细胞的分布提供了有力的工具,有助于更好的理解胃肠道疾病的病理生理变化过程[46]。 2.3 组织透明成像技术 目前显微成像技术正在以惊人的速度发展,这些显微成像技术包括共聚焦显微镜、双光子显微镜,光片显微镜和光学相干断层扫描等[47-48]。其中双光子显微镜最适合用于非透明组织的深部成像。然而组织透明技术去除了光散射造成的穿透限制,这将意味着成像深度不再受样本的限制,而是受物镜的限制,目前应用于透明组织光学成像技术主要包括以下几种: 2.3.1 共聚焦和双光子显微镜成像 组织透明成像的主要限制因素是物镜工作距离,而不是光的穿透,因此大轴向行程的立式显微镜对于适应较长工作距离的物镜和较厚样品是必不可少的。目前大多数显微镜制造商都推出了超长工作距离(>5 mm)和高NA(>0.9)的物镜,所以共聚焦显微镜和双光子显微镜都可以用于透明样品成像。对于多种染料标记的样品,共聚焦成像会产生更好的信噪比,因为单光子激发效率较高,交叉激发可能性低,此外,由于激光之间的快速切换(无需调谐),可以更快地获得多色共聚焦图像。双光子显微镜在进行较厚组织Z轴扫描时,能够防止焦平面以外的区域发生光漂白作用,此外应用近红外光作为激发光源,具有更强的组织穿透能力,因为即使透明样本也会存在一定程度的短波散射[49]。然而,双光子和共聚焦成像技术最主要的局限在于成像速度,激光扫描是一个耗时缓慢的过程。使用20X/1.0NA物镜扫描整个体积为1 000 mm3的小鼠大脑,即便以相对较快的扫描频率1 hz进行扫描,也需要将近50 d[50]。因此,对于透明组织,双光子和共聚焦成像只适用于较小区域的高分辨率成像。 2.3.2 光学投影断层成像 光学投影断层成像通过收集样品不同角度的透射投影图像,重建样本三维信息,能够对厘米尺度的样本进行快速明场和荧光的三维成像,是大体积生物标本成像的理想选择之一[51]。目前光学投影断层成像已广泛应用于神经科学领域,研究胚胎发育及全脑神经网络连接等。结合组织透明技术,光学投影断层成像成功检测了多种组织类型样本,包括发育中的小鼠胚胎、异种移植瘤组织、小鼠整个心脏、肾脏、大脑半球以及白色脂肪组织[52-53]。最近,BAN等[54]开发出无需组织标记的光学投影断层成像(LF-OPT),LF-OPT采用衰减对比度进行成像,因此无需任何荧光或染料标记即可实现对普通胚胎的三维成像,扩大了光学投影断层成像的应用范围。 2.3.3 光片显微镜成像 组织透明成像技术推动了光片显微镜的再发展[9],光片显微镜应用激光光束从侧面激发荧光样品,并通过垂直CCD来获取检测成像,由于激发与检测路径是分离的,且单个x-y平面图像在一次扫描中获得(无需线扫描),所以可以将光漂白和光学损伤降低到最低。相机读取速度以及焦平面移动速度是采样时间的主要限制因素,LSFM结合sCMOS相机,拍摄速度高达100帧,因此LSFM能够实现大体积样本的高速、高信噪比成像[32,55]。这些优点满足了系统生物学的研究要求,诸多实验将光片显微镜用于全器官成像,包括对动物胚胎发育的时空监测[56],鱼和苍蝇全脑神经活动的功能成像[57],或者小鼠全脑成像[58]。综上所述,LSFM是以高通量方式获取透明组织3D成像的最佳途径之一。 2.4 组织透明技术在生物医学研究领域的应用 组织透明化技术的发展使大型生物样本变得透明,为生物组织结构的三维可视化打开了大门,并为进一步探索人类疾病的复杂性提供了崭新的平台,近年来组织透明技术在生物医学研究领域得到了广泛应用。 2.4.1 组织透明技术在神经科学中的应用 神经科学一直是生命科学研究的热点,研究神经系统在健康和疾病中的功能连接,对于揭示神经精神疾病的发病机制至关重要的,为了明确神经元的结构和功能连接,需要对整个大脑和脊髓中的神经元及突触投射进行成像和追踪[59]。BRADKE结合3DISCO与光片显微镜和双光子显微镜,识别、追踪和评估慢性脊髓损伤后的轴突再生,确定了轴突再生能力及再生轴突轨迹,有助于解释轴突再生机制,同时定量测定了脊髓损伤后神经胶质的活动反应[60]。研究者应用CLARITY,让整个大脑变得“透明”,结合Thy1-EYFP小鼠,展示了大脑神经元远距离投射、局部电路连接、细胞关系、亚细胞结构、蛋白质复合物、核酸和神经递质的成像,同时对成年小鼠完整大脑进行多轮免疫标记和原位杂交检测[29]。MURAKAMI等[61]应用CUBIC-X透明小鼠大脑,在亚细胞分辨率下对整个小鼠大脑进行无缝成像,并构建出基于点的小鼠大脑方位图,反映出小鼠全脑发育的不均匀性,揭示了出生后发育过程中大脑视觉和体感皮质区域细胞数目明显下降以及可能的机制,组织透明技术能够让人们更清晰地理解大脑解剖结构、神经通路及其功能之间的关系。 2.4.2 组织透明技术在骨骼系统的应用 骨骼系统为机体提供物理支持并保护内部器官免受外部身体压力[62],不同类型骨骼具有特定的生理过程,对于机体的发展和生存至关重要,如造血细胞的增长,骨骼的生长和重塑[63]。骨组织透明技术能够更清晰地显示完整骨组织的生物学过程,骨由硬组织(矿物)和软组织(骨髓)共同构成,结构极为复杂,因此骨组织透明具有一定的挑战性。大多数骨组织采用有机溶剂透明[64-65],由于未涉及矿物质去除,只能获得约200 μm的成像深度。ACAR等[66]应用改良BABB透明方法制备出透明的小鼠胫骨,并对骨髓腔内造血干细胞进行三维成像,揭示了造血干细胞的空间生态分布。但是BABB透明会破坏内源性荧光蛋白,不适合荧光报告鼠,GRADINARU利用Bone CLARITY,制备出透明的小鼠全骨,结合光片显微镜使成像深度达到1.5 mm,同时保持原有tdTomato荧光和较高的信噪比,应用该技术,GRADINARU绘制出Sox9+骨祖细胞的三维空间分布图,有助于对小鼠骨祖细胞进行可视化和定量化分 析[67]。利用PEGASOS,晶典制备出高度透明的小鼠长骨,并对骨髓腔中的神经网络进行三维成像,绘制出不同模式的神经分布图[24]。 2.4.3 组织透明技术在肿瘤系统的应用 单个细胞的随机和增殖事件会破坏体内平衡,导致致命疾病的发生,如癌症转移[68]。为了在癌症转移早期阶段检测和量化稀疏分布的转移细胞,有必要在全身检测转移细胞并可视化单个肿瘤的微环境,TAINAKA团队通过9个癌细胞系对13个小鼠模型进行研究,应用CUBIC透明技术处理标本,结合光片荧光显微镜和共聚焦显微镜,在单细胞分辨率水平上对转移性癌症进展进行时空定量分析[18]。CUBIC成像分析能够区分不同血源性转移模式,如富血管生长和协同生长,并且发现上皮-间质转化不仅促进细胞外渗,而且促进细胞在转移部位的存活。此外,TAINAKA还研究了转化生长因子b信号在肺转移中的作用,并应用体内系统评价了抗癌药物对肿瘤转移的治疗效果[18]。CUBIC透明及成像技术为分析全身癌症的转移、生长和发展提供了良好的平台,为研究目前无法治愈的转移性疾病提供技术基础。 2.4.4 组织透明技术在胚胎发育领域的应用 准确绘制人类胚胎的细胞和分子图谱对于理解正常和病理条件下的器官发生机制至关重要。ALAIN小组将36个人类胚胎和妊娠6-14周的胎儿进行全组织包埋免疫标记染色,结合3DISCO透化技术和光片显微镜成像,构建出怀孕前3个月人类胚胎周围神经、肌肉、血管、心肺和泌尿生殖系统的三维图像[17]。ALAIN发现成年样的皮肤神经支配模式是在妊娠头3个月结束前建立的,神经分支显示出重要的个体内和个体间的变异,此外,男性和女性生殖道的不同血管化与性别决定相关[17],这项工作为绘制人类胚胎细胞和分子图谱铺平了道路,为研究生理和病理条件下调控人类胚胎发育的分子机制开辟新途径。KOLESOVá等[69]应用CUBIC技术透明Cx40:绿色荧光蛋白小鼠胚胎心脏,研究冠状动脉发育,结合共聚焦显微镜和Micro-CT,绘制出E16.5小鼠冠状动脉三维解剖图,展示了间隔动脉的发育细节,有助于提高对冠状动脉异常疾病的了解。 "

| [1] ISOSAKA T, MATSUO T, YAMAGUCHI T, et al. Htr2a-Expressing Cells in the Central Amygdala Control the Hierarchy between Innate and Learned Fear. Cell. 2015;163(5):1153-1164. [2] PICHAT J, IGLESIAS JE, YOUSRY T, et al. A Survey of Methods for 3D Histology Reconstruction. Med Image Anal. 2018;46:73-105. [3] RAGAN T, KADIRI LR, VENKATARAJU KU,et al. Serial two-photon tomography for automated ex vivo mouse brain imaging. Nat Methods. 2012;9(3):255-258. [4] DENK W, STRICKLER JH, WEBB WW.Two-photon laser scanning fluorescence microscopy. Science. 1990;248(4951):73-76. [5] HILLMAN EMC, VOLETI V, LI W, et al. Light-Sheet Microscopy in Neuroscience. Annu Rev Neurosci. 2019;42:295-313. [6] ZHU D, LARIN KV, LUO Q, et al. Recent progress in tissue optical clearing. Laser Photon Rev. 2013;7(5):732-757. [7] WENNER M. The most transparent research. Nat Med. 2009;15(10): 1106-1109. [8] SDOBNOV AY, DARVIN ME, GENINA EA, et al. Recent progress in tissue optical clearing for spectroscopic application. Spectrochim Acta A Mol Biomol Spectrosc. 2018;197(6):216-229. [9] SUSAKI EA, UEDA HR. Whole-body and Whole-Organ Clearing and Imaging Techniques with Single-Cell Resolution: Toward Organism-Level Systems Biology in Mammals. Cell Chem Biol. 2016; 23(1):137-157. [10] TAINAKA K, KUNO A, KUBOTA SI, et al. Chemical Principles in Tissue Clearing and Staining Protocols for Whole-Body Cell Profiling. Annu Rev Cell Dev Biol. 2016;32(6):713-741. [11] SPALTEHOLZ W. Uber das Durchsichtigmachen von menschlichen und tierischen Praparaten. (S Hierzel). 1914. [12] GENINA EA, BASHKATOV AN, TUCHIN VV. Tissue optical immersion clearing. Expert Rev Med Devices. 2010;7(6):825-842. [13] RICHARDSON DS, LICHTMAN JW. SnapShot: Tissue Clearing. Cell. 2017;171(2):496-e1. [14] DODT HU, LEISCHNER U, SCHIERLOH A, et al. Ultramicroscopy: three-dimensional visualization of neuronal networks in the whole mouse brain. Nat Methods. 2007;4(4):331-336. [15] ERTURK A, BECKER K, JAHRLING N,et al. Three-dimensional imaging of solvent-cleared organs using 3DISCO. Nat Protoc. 2012; 7(11):1983-1995. [16] YANG L, FEUCHTINGER A, MOLLER W, et al. Three-Dimensional Quantitative Co-Mapping of Pulmonary Morphology and Nanoparticle Distribution with Cellular Resolution in Nondissected Murine Lungs. ACS Nano. 2019;13(2):1029-1041. [17] BELLE M, GODEFROY D, COULY G, et al. Tridimensional Visualization and Analysis of Early Human Development. Cell. 2017; 169(1):161-73 e12. [18] KUBOTA SI, TAKAHASHI K, NISHIDA J,et al. Whole-Body Profiling of Cancer Metastasis with Single-Cell Resolution. Cell Rep. 2017;20(1): 236-250. [19] RENIER N, WU Z, SIMON DJ, et al. iDISCO: a simple, rapid method to immunolabel large tissue samples for volume imaging. Cell. 2014; 159(4):896-910. [20] HAHN C, BECKER K, SAGHAFI S, et al. High resolution imaging of fluorescent whole mouse brains using stabilised organic media (sDISCO). J Biophotonics.2019;12(8):e201800368. [21] PAN C, CAI R, QUACQUARELLI FP, et al. Shrinkage-mediated imaging of entire organs and organisms using uDISCO. Nat Methods. 2016; 13(10):859-867. [22] LI Y, XU J, WAN P, et al. Optimization of GFP Fluorescence Preservation by a Modified uDISCO Clearing Protocol. Front Neuroanat.2018;12:67. [23] CAI R, PAN C, GHASEMIGHARAGOZ A, et al. Panoptic imaging of transparent mice reveals whole-body neuronal projections and skull-meninges connections. Nat Neurosci. 2019;22(2):317-327. [24] JING D, ZHANG S, LUO W, et al. Tissue clearing of both hard and soft tissue organs with the PEGASOS method. Cell Res. 2018;28(8): 803-818. [25] HAMA H, KUROKAWA H, KAWANO H,et al.Scale: a chemical approach for fluorescence imaging and reconstruction of transparent mouse brain. Nat Neurosci. 2011;14(11):1481-1488. [26] HAMA H, HIOKI H, NAMIKI K, et al. ScaleS: an optical clearing palette for biological imaging. Nat Neurosci. 2015;18(10):1518-1529. [27] KE MT, FUJIMOTO S, IMAI T. SeeDB: a simple and morphology- preserving optical clearing agent for neuronal circuit reconstruction. Nat Neurosci. 2013;16(8):1154-1161. [28] HOU B, ZHANG D, ZHAO S,et al. Scalable and DiI-compatible optical clearance of the mammalian brain. Front Neuroanat. 2015;9:19. [29] CHUNG K, WALLACE J, KIM SY, et al. Structural and molecular interrogation of intact biological systems. Nature. 2013;497(7449): 332-337. [30] SARITAS T, PUELLES VG, SU XT, et al. Optical Clearing in the Kidney Reveals Potassium-Mediated Tubule Remodeling.Cell Rep. 2018; 25(10):2668-75 e3. [31] DU H, HOU P, WANG L, et al. Modified CLARITY Achieving Faster and Better Intact Mouse Brain Clearing and Immunostaining.Sci Rep. 2019; 9(1):10571. [32] TOMER R, YE L, HSUEH B, et al. Advanced CLARITY for rapid and high-resolution imaging of intact tissues. Nat Protoc. 2014;9(7): 1682-1697. [33] TREWEEK JB, CHAN KY, FLYTZANIS NC, et al. Whole-body tissue stabilization and selective extractions via tissue-hydrogel hybrids for high-resolution intact circuit mapping and phenotyping.Nat Protoc. 2015;10(11):1860-1896. [34] DABROWSKA N, JOSHI S, WILLIAMSON J,et al. Parallel pathways of seizure generalization. Brain. 2019;142(8):2336-2351. [35] GREENBAUM A, CHAN KY, DOBREVA T, et al. Bone CLARITY: Clearing, imaging, and computational analysis of osteoprogenitors within intact bone marrow. Sci Transl Med. 2017;9(387). pii: eaah6518. [36] BERNAL L, CISNEROS E, GARCIA-MAGRO N,et al. Immunostaining in whole-mount lipid-cleared peripheral nerves and dorsal root ganglia after neuropathy in mice. Sci Rep. 2019;9(1):8374. [37] MURRAY E, CHO JH, GOODWIN D, et al. Simple, Scalable Proteomic Imaging for High-Dimensional Profiling of Intact Systems. Cell. 2015; 163(6):1500-1514. [38] PARK YG, SOHN CH, CHEN R,et al. Protection of tissue physicochemical properties using polyfunctional crosslinkers. Nat Biotechnol. 2018;168(6):129-136 [39] SUSAKI EA, TAINAKA K, PERRIN D, et al. Whole-brain imaging with single-cell resolution using chemical cocktails and computational analysis. Cell. 2014;157(3):726-739. [40] HASEGAWA S, SUSAKI EA, TANAKA T, et al. Comprehensive three-dimensional analysis (CUBIC-kidney) visualizes abnormal renal sympathetic nerves after ischemia/reperfusion injury. Kidney Int. 2019; 96(1):129-138. [41] TAINAKA K, MURAKAMI TC, SUSAKI EA, et al. Chemical Landscape for Tissue Clearing Based on Hydrophilic Reagents. Cell Rep. 2018;2 4(8):2196-210 e9. [42] CHEN L, LI G, LI Y, et al. UbasM: An effective balanced optical clearing method for intact biomedical imaging. Sci Rep. 2017;7(1):12218. [43] LAI HM, LIU AKL, NG HHM,et al. Next generation histology methods for three-dimensional imaging of fresh and archival human brain tissues. Nat Commun. 2018;9(1):1066. [44] LI W, GERMAIN RN, GERNER MY. Multiplex, quantitative cellular analysis in large tissue volumes with clearing-enhanced 3D microscopy (Ce3D). Proc Natl Acad Sci U S A. 2017;114(35):E7321- E7330. [45] LI W, GERMAIN RN, GERNER MY. High-dimensional cell-level analysis of tissues with Ce3D multiplex volume imaging. Nat Protoc. 2019;14(6):1708-1033. [46] BOSSOLANI GDP, PINTELON I, DETREZ JD, et al. Comparative analysis reveals Ce3D as optimal clearing method for in toto imaging of the mouse intestine. Neurogastroenterol Motil. 2019;31(5):e13560. [47] MERTZ J. Optical sectioning microscopy with planar or structured illumination. Nat Methods. 2011;8(10):811-819. [48] LI X, YU B, SUN Q, et al. Generation of a whole-brain atlas for the cholinergic system and mesoscopic projectome analysis of basal forebrain cholinergic neurons. Proc Natl Acad Sci U S A. 2018;115(2): 415-420. [49] COMBS CA, SMIRNOV A, CHESS D, et al. Optimizing multiphoton fluorescence microscopy light collection from living tissue by noncontact total emission detection (epiTED). J Microsc. 2011;241(2): 153-161. [50] RICHARDSON DS, LICHTMAN JW. Clarifying Tissue Clearing. Cell. 2015;162(2):246-257. [51] SHARPE J, AHLGREN U, PERRY P, et al. Optical projection tomography as a tool for 3D microscopy and gene expression studies. Science. 2002;296(5567):541-545. [52] ANDERSON GA, WONG MD, YANG J, et al. 3D imaging, registration, and analysis of the early mouse embryonic vasculature. Dev Dyn. 2013;242(5):527-538. [53] ZENG W, PIRZGALSKA RM, PEREIRA MM,et al. Sympathetic neuro-adipose connections mediate leptin-driven lipolysis. Cell. 2015; 163(1):84-94. [54] BAN S, CHO NH, MIN E, et al. Label-free optical projection tomography for quantitative three-dimensional anatomy of mouse embryo. J Biophotonics. 2019;12(7):e201800481. [55] KELLER PJ, AHRENS MB. Visualizing whole-brain activity and development at the single-cell level using light-sheet microscopy. Neuron. 2015;85(3):462-483. [56] WU Y, WAWRZUSIN P, SENSENEY J, et al. Spatially isotropic four-dimensional imaging with dual-view plane illumination microscopy. Nat Biotechnol. 2013;31(11):1032-1038. [57] LERNER TN, SHILYANSKY C, DAVIDSON TJ, et al. Intact-Brain Analyses Reveal Distinct Information Carried by SNc Dopamine Subcircuits. Cell. 2015;162(3):635-647. [58] TAINAKA K, KUBOTA SI, SUYAMA TQ, et al. Whole-body imaging with single-cell resolution by tissue decolorization. Cell. 2014;159(4): 911-924. [59] MANO T, ALBANESE A, DODT HU, et al. Whole-Brain Analysis of Cells and Circuits by Tissue Clearing and Light-Sheet Microscopy. J Neurosci. 2018;38(44):9330-9337. [60] ERTURK A, MAUCH CP, HELLAL F, et al. Three-dimensional imaging of the unsectioned adult spinal cord to assess axon regeneration and glial responses after injury. Nat Med. 2011;18(1):166-171. [61] MURAKAMI TC, MANO T, SAIKAWA S, et al. A three-dimensional single-cell-resolution whole-brain atlas using CUBIC-X expansion microscopy and tissue clearing. Nat Neurosci. 2018;21(4):625-637. [62] LONG F. Building strong bones: molecular regulation of the osteoblast lineage. Nat Rev Mol Cell Biol. 2011;13(1):27-38. [63] KLAG KA, HORTON WA. Advances in treatment of achondroplasia and osteoarthritis. Hum Mol Genet. 2016;25(R1):R2-8. [64] BERKE IM, MIOLA JP, DAVID MA, et al. Seeing through Musculoskeletal Tissues: Improving In Situ Imaging of Bone and the Lacunar Canalicular System through Optical Clearing. PLoS One. 2016;11(3):e0150268. [65] NEU CP, NOVAK T, GILLILAND KF,et al. Optical clearing in collagen- and proteoglycan-rich osteochondral tissues. Osteoarthritis Cartilage. 2015;23(3):405-413. [66] ACAR M, KOCHERLAKOTA KS, MURPHY MM, et al. Deep imaging of bone marrow shows non-dividing stem cells are mainly perisinusoidal. Nature. 2015;526(7571):126-130. [67] GREENBAUM A, CHAN KY, DOBREVA T, et al. Bone CLARITY: Clearing, imaging, and computational analysis of osteoprogenitors within intact bone marrow. Sci Transl Med. 2017;9(387):68-82. [68] SAADATPOUR Z, REZAEI A, EBRAHIMNEJAD H, et al. Imaging techniques: new avenues in cancer gene and cell therapy. Cancer Gene Ther. 2017;24(1):1-5. [69] KOLESOVÁ H, BARTOŠ M, HSIEH WC, et al. Novel approaches to study coronary vasculature development in mice. Developmental Dynamics. 2018;247(8):1018-1027. [70] LEE E,CHOI J, JO Y,et al.ACT-PRESTO: Rapid and consistent tissue clearing and labeling method for 3-dimensional (3D) imaging. Sci Rep. 2016;6:18631. [71] YANG B, TREWEEK JB, KULKARNI RP,et al.Single-cell phenotyping within transparent intact tissue through whole-body clearing. Cell. 2014;158(4):945-958. [72] WANG K, MILKIE DE, SAXENA A, et al. Rapid adaptive optical recovery of optimal resolution over large volumes. Nat Methods. 2014;11(6):625-628. |
| [1] | Liu Jinwei, Chen Yunzhen, Wan Chunyou. Changes of osteogenic growth factors in the broken end of bone nonunion under stress [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(23): 3619-3624. |
| [2] | Zhang Liang, Ma Xiaoyan, Wang Jiahong. Regulatory mechanism of Shenshuai Yin on cell apoptosis in the kidney of chronic renal failure rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(23): 3672-3677. |
| [3] | Lu Jie, Li Xue, Wang Lu, Fan Jia, Zhang Yeting, Lu Xiaobin, Yuan Qiongjia. Effects of different-intensity swimming exercises on spatial learning and memory ability and the expression of Orexin A in the rat cerebellum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(23): 3697-3703. |
| [4] | Yang Xinhua, Yan Yindi, Luo Xuguang, Yang Yanping, Li Hairong, Cui Huilin, Cao Ximei. Bmal1 and Clock regulate the development and differentiation of skeletal muscle [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(20): 3130-3137. |
| [5] | Wang Jing, Wu Jiangbo. Irisin mediates protective effects on failing heart via integrin alpha V receptors [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(20): 3219-3225. |
| [6] | He Fan, Xiong Xiuli, Shan Xianfeng, Zhang Shutong, Hu Jian, Wang Xuejin. Guided bone regeneration in a small animal model of critical size craniofacial bone defects [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(20): 3226-3231. |
| [7] | Li Shang, Huang Xiang, Chen Ming, Lei Mingxing, Cheng Shi, Zhang Licheng, Yin Pengbin, Tang Peifu. Semaphorin 3A is expected to be a new target for the repair of skeletal muscle injury [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(20): 3232-3238. |
| [8] | Lin Haiqi, Chen Liang, Tang Lu, Weng Xiquan, Lin Wentao. Significance of urinary proteomics assessing pathological changes in the body [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(20): 3259-3266. |
| [9] | Han Lei, Liu Haiying, Zhang Hao. Numerical analysis of the mechanical behaviors of cartilage in various levels of osteoarthritis in a gait cycle [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(18): 2810-2815. |
| [10] | Hu Wandong, He Jialin, Zhang Longsheng, Liao Wenbo. Differential proteomics study of patients with sternal ossification of the ligamentum flavum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(17): 2625-2629. |
| [11] | Zhu Shiqiang, Xu Jianfeng, Hei Xiaoyan, Chen Yundong, Tian Xinbao, Zhang Jinchen, Lin Ruizhu. Effect of internal heat-type acupuncture needle therapy on the expression of type I collagen, matrix metalloproteinase-3 and osteopontin in the subchondral bone of rabbit knee osteoarthritis model [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(17): 2636-2642. |
| [12] | Ailimaierdan·Ainiwaer, Wang Ling, Gu Li, Dilidaer•Taxifulati, Wang Shan, Yin Hongbin. Effect of transforming growth factor-beta3 on the proliferation and osteogenic capability of osteoblasts [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(17): 2664-2669. |
| [13] | Huang Yunmei, Feng Fangfang, Chen Wenlie, Lu Xiaodong, Lin Ruhui, Li Zuanfang, Huang Meiya, Tan Chunjiang, Li Xihai, Li Xiaodong. Anti-inflammatory and anti-swelling effects of Tougu Xiaotong Capsule in rat models of early osteoarthritis with synovial edema [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(17): 2697-2702. |
| [14] | Zhang Shuang, Tan Rui, Wang Chunxiao, Wu Fengyu, Guo Hongyu. MicroRNAs for assessing the motion control of human skeletal muscles [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(17): 2755-2760. |
| [15] | Zhang Yunqing, Wang Jian, Yang Chunhua, Li Cong. Effects of miR-335-5p on proliferation and apoptosis of osteoarthritic chondrocytes by targeting programmed cell death 5 [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(14): 2142-2147. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||