Chinese Journal of Tissue Engineering Research ›› 2020, Vol. 24 ›› Issue (11): 1756-1761.doi: 10.3969/j.issn.2095-4344.2046
Previous Articles Next Articles
Cerebral organoids culture and application in central nervous system diseases
Fan Wenjuan1, 2, Chen Xudong1, Deng Jinbo2, 3
- 1Luohe Medical College, Luohe 462002, Henan Province, China; 2College of Life Science, Henan University, Kaifeng 475004, Henan Province, China; 3Henan Academy of Population and Family Planning Science and Technology, Key Laboratory of Birth Defect Prevention of National Health and Health Commission, Zhengzhou 450002, Henan Province, China
-
Received:2019-07-13Revised:2019-07-15Accepted:2019-09-02Online:2020-04-18Published:2020-02-29 -
Contact:Fan Wenjuan, Luohe Medical College, Luohe 462002, Henan Province, China; College of Life Science, Henan University, Kaifeng 475004, Henan Province, China -
About author:Fan Wenjuan, MD, Lecturer, Luohe Medical College, Luohe 462002, Henan Province, China; College of Life Science, Henan University, Kaifeng 475004, Henan Province, China -
Supported by:the Doctor Launch Fund of Luohe Medical College, No. 2019-DF-01; a grant from Science and Technology Department of Henan Province, No. 182102310083
CLC Number:
Cite this article
Fan Wenjuan, Chen Xudong, Deng Jinbo. Cerebral organoids culture and application in central nervous system diseases[J]. Chinese Journal of Tissue Engineering Research, 2020, 24(11): 1756-1761.
share this article
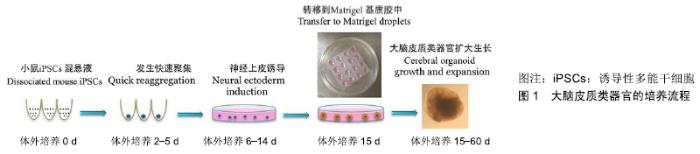
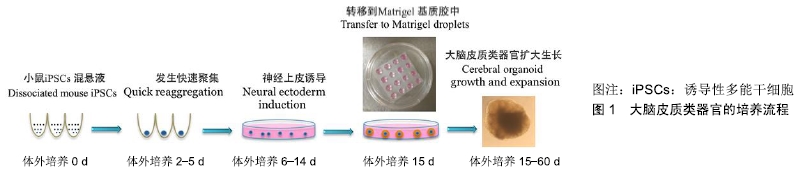
2.1 大脑皮质类器官培养现状 大脑组织是人体发育最复杂的结构,许多人类大脑疾病难以在动物体内重现,因此建立大脑发育的体外模型具有非常重要的研究价值。 利用胚胎干细胞或诱导性多能干细胞培养大脑类器官,YOSHIKI SASAI课题组和LANCASTER课题组分别做了开创性的工作[2]。EIRAKU等[3-4]最早报道了一种“胚状体样聚集体的快速再聚集无血清悬浮培养法(SFEBq培养法) ”。在没有添加外部信号因子的情况下,利用该法培养可促使胚胎干细胞以自组织发育的模式自发形成视杯或极化的大脑皮质;随后LANCASTER等[2]研究方案为大脑类器官的建立方法迈上了一个新的台阶。与SFEBq培养法不同的是,在神经外胚层初始发育之后,拟胚体被嵌入到细胞外基质胶中,这就为神经上皮的生长提供了空间支持,使神经上皮扩展出更大的神经上皮芽,为大脑皮质类器官的生成提供了发育基础[2]。在这种条件下,神经上皮自发发育成不同的大脑区域,包括视网膜、背侧皮层、腹侧前脑、中脑、脉络丛和海马等类器官结构。以后的大脑类器官培养方案均参考了这种胚胎干细胞自我组织的方法,但可以通过添加特异性诱导信号分子来模拟大脑发育的内源性模式,以此更有效地驱动神经上皮细胞向某一特定区域的脑组织分化。 在作者以往的研究中,通过添加细胞因子Noggin和胰岛素样生长因子1,有效地促进了神经上皮的发生以及前脑的分化[13]。培养时首先将消化成单细胞的诱导性多能干细胞按照一定的细胞密度在低黏附U形底的96孔板内悬浮培养,诱导性多能干细胞在20-30 min内即可发生快速聚集,待诱导性多能干细胞形成拟胚体后对其进行神经上皮诱导,神经上皮芽长出后将其嵌入Matrigel基质胶做的悬滴(Matrigel droplets)中。基质胶为神经上皮的生长提供了支撑,保证了神经上皮的连续性生长。利用微型平板摇床低速摇动培养以便为类器官的生长提供更多的营养支持。经过2个月左右的扩大生长期,即可形成大脑皮质类器官,见图1。 "

结合国内外相关文献[2-4,14-15],在体外利用多能干细胞培养大脑类器官的方法可以简单概括为以下几点:①适当的起始细胞群:一定数量的胚胎干细胞或诱导性多能干细胞可在低黏附培养板中发生快速聚集,这对于拟胚体的形成是非常重要的。②一定量的生长因子:虽然多能干细胞可以发生自发组织形成神经前体,但适时添加生长因子或神经诱导信号分子有利于维持大脑类器官的长期生长。例如LANCASTER等[2]的培养方案中添加了ROCK抑制剂以改善胚胎干细胞的存活率,加入不同浓度的碱性成纤维细胞生长因子来影响胚胎干细胞的增殖及分化能力。MOU等[15]先用双SMAD抑制剂(阻断转化生长因子β信号传导通路)处理人诱导性多能干细胞以抑制中胚层和内胚层的形成,在初级神经前体形成阶段加入GSK抑制剂、重组WNT3A蛋白和SMAD抑制剂等来减少类器官内部细胞的死亡。③合适的细胞外基质:细胞外基质不但为类器官的产生提供了足够的营养和空间支持,其主要成分——层粘连蛋白可以促进刚性神经上皮的形成,也就是有助于形成连续的神经上皮。 2.2 大脑皮质类器官的形成机制 2.2.1 多能干细胞的自我重组(Self-organization)作用 (1)多能干细胞具有自我构建成复杂组织结构的能力:适当条件下,像胚胎干细胞或诱导性多能干细胞这一类的多能干细胞具有自发发育成某些原始结构的趋势。通过采取一些措施去除抑制多能干细胞分化的因素,可以使多能干细胞聚集成团,生成拟胚体。拟胚体与发育早期的胚胎组织类似,是一个多种细胞混杂的、排列无序且具有3个胚层结构的多细胞聚合体结构。聚合体中各种细胞分泌各自的生长因子和分化因子,此时可通过改变培养条件,促使这些干细胞团向某一特定的细胞谱系进行分化。多能干细胞的自我重组不需要外部生物材料的支撑。EIRAKU等[3]报道胚胎干细胞通过无血清悬浮培养可以自发形成皮质样结构,这种人工皮质不仅具有神经细胞和神经胶质细胞等成分,还形成了简单的皮质片层化结构,在边缘层甚至出现了Cajal-Retzius细胞。该研究小组于2011年又发现胚胎干细胞经过快速聚集后,局部细胞层经历组织力学的变化,会内陷形成视杯,从无规则的细胞聚集体自发分化形成高度有序的、具有明显分层的视网膜结构[4]。此后,陆续又有包括甲状腺[16],胰腺[17],肺等其他类器官利用多能干细胞在三维培养条件下自我构建的报道[18],进一步证明了胚胎干细胞或诱导性多能干细胞具有自发产生功能性多细胞结构的先天能力。 (2)多能干细胞自我构建过程中的黏合力作用:对取自脊椎动物胚胎期不同组织的细胞混合培养,发现来自同一组织的细胞总是能够重新聚集在一起,提示同一类型的细胞间具有较强的相互作用力[19];进一步的研究认为,具有较强相互作用或相互张力的细胞向拟胚体内部迁移,而具有较弱相互作用的细胞则向外部迁移[20]。这样,根据细胞张力的强弱,在体外培养的拟胚体会自发分化出具有不同细胞类型的分层结构。 (3)三维支架与组织及器官的重塑:Matrigel基底膜基质是一种常见的三维细胞外基质,包含粘连蛋白、胶原蛋白、生长因子和金属蛋白酶等生物活性成分。Matrigel通过基底膜配体提供支架和组织特异性的生化因子,增强了细胞的附着和细胞与细胞之间的相互作用能力,为干细胞衍生的类器官提供了一个动态的生长发育的微环境[21]。有研究报道,将人胚胎干细胞包埋入细胞外基质蛋白凝胶中,人胚胎干细胞由于与细胞外基质的相互作用,可以自发分化成上皮并形成具有极化结构的空腔,类似于活体大脑中的脑室[22],这也是许多含空腔的类器官发生的基础。 2.2.2 大脑类器官发生中的神经诱导及基因调控 胚胎发育早期,原肠形成内、中、外3个胚层的组织结构。内胚层(Endoderm)发育为呼吸和消化系统,中胚层(Mesoderm)发育成真皮、骨骼、肌肉和心血管系统等,外胚层(Ectoderm)发育成表皮、神经组织、眼晶状体等结构[23]。三胚层的建立规划了动物器官系统发育的原基,具有产生原始器官结构的潜能,此后胚胎祖细胞逐渐分化为终末分化细胞,最终发育成高度特异化的器官系统。 神经外胚层的形成受多个基因的调控。目前的研究表明,有3类诱导信号对神经系统的发育起着诱导作用。第一类信号是BMP的抑制物,包括Chordin、Noggin和Folliststin,主要起抑制BMP4的作用,使外胚层发育成为神经外胚层[24-25];第二类信号是能够诱导神经管前端部分(脑)产生Wnt抑制物Dickkopf[26]、Frzb[27]、胰岛素样生长因子等[28],这些信号分子的作用相似,均是通过抑Wnt信号通路诱导头部结构的产生;第三类信号是能够诱导神经管后部结构(脊髓)产生Wnt、BMP、FGF和RA等[29]。Wnt参与神经管后部结构的形成,抑制Wnt的信号转导途径,头部结构就会向神经管的后端推进。FGF的作用是促进细胞对Wnt信号转导作出反应。RA在脊索中胚层中也有一个浓度梯度,与Wnt一样,从后端往前端递减,浓度高时促进神经管后部结构的形成。 在没有这些抑制剂的情况下,仅依靠较少的类器官培养基培养也可以产生广泛的大脑区域的神经细胞类型[2],然而使用双重SMAD和Wnt抑制可以更有效地促进大脑类器官的神经分化[3,15],这些大脑类器官形成具有特征性的神经细胞生发中心和皮质区域。总之,大脑类器官的培养要先促使胚胎干细胞或诱导性多能干细胞自发分化为具有胚胎3个胚层细胞结构的拟胚体,再通过在培养体系中加入特异性的神经信号分子作为诱导剂,进一步产生大脑组织特异性的类器官[30-32]。 2.3 大脑类器官在神经系统发育与疾病方面的应用 2.3.1 模拟大脑皮质的早期发育 大脑类器官可以重现人类神经发育的多个方面。现有的研究已经证明,大脑类器官具有正常皮质所有的板层结构,其内的神经细胞也可以表达在正常皮质板层中所出现的特定神经元的标志蛋白,在细胞类型上也表现出多样性和可重复 性[2-3,15,32]。利用RNA测序的研究表明,体外培养6个月的大脑类器官可以鉴定出包括神经上皮祖细胞、放射状胶质细胞、星形胶质细胞、神经元系细胞、富含前脑标记的细胞以及视网膜特异性细胞等10种不同的细胞群[32]。 大脑类器官可用来模拟人类大脑特定的结构特征或功能。在正常发育中的大脑皮质,包含2个主要的神经元群体,即兴奋性谷氨酸能神经元和抑制性γ-氨基丁酸能中间神经元[33]。兴奋性神经元主要由背侧前脑祖细胞产生,而抑制性γ-氨基丁酸能神经元由腹侧前脑祖细胞产生[23]。为了形成完整的神经元回路,中间神经元需要从它们的腹侧进入远处的背侧皮质区域。这个远程切向迁移是由许多信号传导途径控制的。数以亿计的神经元组成复杂的神经网络,这就使得研究神经回路的发生途径变得更加困难。BAGLEY等[34]通过将指向背侧和腹侧前脑的类器官进行融合,产生了背腹侧前脑轴,从而允许γ-氨基丁酸能中间神经元在腹侧和背侧前脑组织之间迁移,这提示可以利用融合类器官的方法,重现人类皮质环路的发育过程。 大脑类器官还可用来研究特定基因在大脑皮质发育中所起的作用。以往在研究大脑胚胎发育的分子机制时,通常会使用一些经过基因修饰的动物来研究特定基因的作用,例如某种基因敲除或敲入的小鼠。为产生研究所需要的基因类型,往往需要首先产生携带多个突变等位基因的突变品系小鼠,还要经过繁琐的传代育种,才能筛选出所需要的基因组合。与小鼠相比,将基因改变引入多能干细胞比较容易,特别是CRISPR/Cas9技术的出现使其可以直接在多能干细胞基因组中产生精确的突变[35],还可以对相同的细胞进行多重修饰,这使得在多能干细胞中可以容易地组合多个等位基因,例如floxed等位基因、cre重组酶转基因和荧光报道基因等。因此,利用多能干细胞衍生的大脑类器官研究特定基因在大脑皮质发育的特定阶段所起的作用也更加方便。 2.3.2 建立神经系统疾病模型 尽管神经系统疾病的动物模型在研究疾病发生的病理机制方面至关重要,但是有许多独特的人类认知行为的疾病如自闭症、小头畸形等多基因遗传病难以在动物体内重现。因此,利用来源这些患者自身的诱导性多能干细胞制备脑组织类器官,成为研究这些特殊疾病发病机制的新工具。目前多能干细胞衍生的大脑类器官建立的疾病模型主要涉及以下几种。 (1)小头畸形(Microcephaly,MCPH)与Zika病毒:常染色体隐性原发性小头畸形是一种大脑发育缺陷,其特征为在出生时头围减小并伴有不同程度的智力障碍。在小头畸形患者中,由于在胚胎神经发生期间产生的大脑皮质神经元数量减少,脑部大小减小到其原始体积的几乎1/3。有16个基因与小头畸形有关,其中大部分基因编码在有丝分裂进程中发挥作用的中心体蛋白。在这些小头畸形相关基因中,CDK5RAP2是围绕中心体的微管组织,具有调节有丝分裂纺锤体定位、不对称中心体的遗传、中心粒复制、DNA损伤信号传导等多种功 能[35-36]。CDK5RAP2已经显示影响神经祖细胞增殖的作用,但在CDK5RAP2基因突变小鼠并没有表现出严重降低脑容量的表型,表明小头畸形的发病过程很难在动物模型中重现。LANCASTER等[2]从CDK5RAP2基因突变的小头畸形患者获诱导性多能干细胞,然后将其培养为脑组织类器官,与正常对照组相比,小头畸形患者脑组织类器官神经上皮增殖率下降,并显示过早的神经分化,若在患者来源的诱导性多能干细胞中过表达突变体基因CDK5RAP2,可观察到扩大的神经上皮,这表明缺乏CDK5RAP2基因活性的神经祖细胞很早就停止增殖并开始分化,导致形成体积较小的脑组织表型, 美洲最近爆发的Zika病毒(ZIKV)也突出了类器官建模的潜在用途。尽管有研究表明ZIKV流行病与先天性小头症病例增加之间存在相关性,但没有直接的实验证据表明ZIKV感染会导致小头畸形出生缺陷,而脑类器官的建立有助于证明ZIKV感染与神经祖细胞的选择性靶向破坏之间的因果关系。使用ZIKV感染人诱导性多能干细胞衍生的脑类器官,几个不同的研究小组均发现类器官体积减小,神经祖细胞和分化的神经元数量显著减少,细胞死亡率增加[37-39]。DANG等[38]使用人胚胎干细胞来源的脑类器官来研究ZIKV的致病性,发现ZIKV感染祖细胞是由于先天性免疫受体Toll样受体3基因的上调导致神经分化紊乱和细胞死亡增加。这些研究表明体外培养的脑类器官在ZIKV感染的致病性模型中的应用价值。 (2)自闭症谱系障碍(Autism spectrum disorder,ASD):自闭症谱系障碍是一种以语言障碍、社交沟通困难和重复行为为特征的大脑发育的复杂疾病,病理学改变最明显的是前额叶皮质。自闭症谱系障碍大脑发育的改变导致皮质结构紊乱,从而影响到可能导致自闭症行为的神经元网络发育。大多数自闭症谱系障碍病例都是特发性的,因此自闭症的确切遗传原因尚不清楚。MARIANI等[40]使用来自特发性自闭症谱系障碍患者的诱导性多能干细胞衍生的脑组织类器官来模拟早期自闭症谱系障碍的神经发育改变,生成的脑组织类器官具有常见的大头表型。基因组分析揭示了参与细胞增殖、神经元分化和突触组装的基因上调,表现出细胞周期加速和γ-氨基丁酸能抑制性神经元的过度产生;利用RNA干扰揭示了FOXG1及其下游基因是造成自闭症谱系障碍衍生脑类器官中表型异常的原因[40]。 (3)神经退行性疾病:神经退行性疾病是一类常见的以神经系统功能和结构逐步丧失和萎缩为特征的疾病,其发病机制目前还不明确,但利用大脑类器官建立神经退行性疾病模型研究其发病机制和发病过程成为一种新型的研究方法。由于大多数神经退行性疾病首先出现在老年期,作为一类迟发性疾病,研究其发病早期细胞的功能活动,有助于疾病的早期诊断、预防与开发有效的治疗药物。目前已经建立阿尔茨海默病与帕金森病大脑类器官模型,相关研究主要集中在检测与疾病相关的已知病理标记物的发生[41-42]。研究表明,阿尔茨海默病患者衍生的类器官能够重演阿尔茨海默病关键的病理学特征,如淀粉样蛋白β斑块和神经原纤维缠结的聚 集[43]。同样,来源于帕金森病患者的人诱导性多能干细胞产生的中脑样类器官不但表达人中脑特征性标记的不同神经元细胞层,还能检测到具有电生理活性的功能性中脑多巴胺能神经元和多巴胺神经递质的产生[42]。 利用中枢神经系统类器官建立的神经系统疾病模型是探究人类神经发育疾病潜在病因的一个有力的工具,也为评估进展和筛选治疗药物提供了新的机会。 "

| [1] CLEVERS H. Modeling Development and Disease with Organoids. Cell. 2016;165(7):1586-1597. [2] LANCASTER MA, RENNER M, MARTIN CA, et al. Cerebral organoids model human brain development and microcephaly. Nature. 2013;501 (7467):373-379. [3] EIRAKU M, WATANABE K, MATSUO-TAKASAKI M, et al. Self-organized formation of polarized cortical tissues from ESCs and its active manipulation by extrinsic signals. Cell Stem Cell. 2008;3(5): 519-532. [4] EIRAKU M, TAKATA N, ISHIBASHI H, et al. Self-organizing optic-cup morphogenesis in three-dimensional culture. Nature. 2011;472(7341): 51-56. [5] CHEUNG C, BERNARDO AS, PEDERSEN RA, et al. Directed differentiation of embryonic origin-specific vascular smooth muscle subtypes from human pluripotent stem cells. Nat Protoc. 2014;9(4): 929-938. [6] TAKEBE T, SEKINE K, ENOMURA M, et al. Vascularized and functional human liver from an iPSC-derived organ bud transplant. Nature. 2013;499(7459):481-484. [7] TAKASATO M, ER PX, CHIU HS, et al. Kidney organoids from human iPS cells contain multiple lineages and model human nephrogenesis. Nature. 2015;526(7574):564-568. [8] RAY K. Development: Modelling human stomach development with gastric organoids. Nat Rev Gastroenterol Hepatol. 2017;14(2):68. [9] FORSTER R, CHIBA K, SCHAEFFER L, et al. Human intestinal tissue with adult stem cell properties derived from pluripotent stem cells. Stem Cell Reports. 2014;2(6):838-852. [10] THOMSON JA, ITSKOVITZ-ELDOR J, SHAPIRO SS, et al. Embryonic stem cell lines derived from human blastocysts. Science. 1998; 282 (5391):1145-1147. [11] TAKAHASHI K, TANABE K, OHNUKI M, et al. Induction of pluripotent stem cells from adult human fibroblasts by defined factors. Cell. 2007; 131(5):861-872. [12] TAKAHASHI K, YAMANAKA S. Induction of pluripotent stem cells from mouse embryonic and adult fibroblast cultures by defined factors. Cell. 2006;126(4):663-676. [13] 范文娟,王倩,孙仪征,等.起源于小鼠诱导性多能干细胞的大脑皮质类器官的建立及其生物学特性[J].解剖学报,2017,48(4): 387-396. [14] BERSHTEYN M, KRIEGSTEIN AR. Cerebral organoids in a dish: progress and prospects. Cell. 2013;155(1):19-20. [15] MOU H, VINARSKY V, TATA PR, et al. Dual SMAD Signaling Inhibition Enables Long-Term Expansion of Diverse Epithelial Basal Cells. Cell Stem Cell. 2016;19(2):217-231. [16] ANTONICA F, KASPRZYK DF, SCHIAVO AA, et al. Generation of Functional Thyroid Tissue Using 3D-Based Culture of Embryonic Stem Cells. Methods Mol Biol. 2017;1597:85-95. [17] LEE J, SUGIYAMA T, LIU Y, et al. Expansion and conversion of human pancreatic ductal cells into insulin-secreting endocrine cells. Elife. 2013;2:e00940. [18] CHOI J, IICH E, LEE JH. Organogenesis of adult lung in a dish: Differentiation, disease and therapy. Dev Biol. 2016;420(2):278-286. [19] VASIOUKHIN V, BAUER C, YIN M, et al. Directed actin polymerization is the driving force for epithelial cell-cell adhesion. Cell. 2000;100(2): 209-219. [20] ADAMS CL, CHEN YT, SMITH SJ, et al. Mechanisms of epithelial cell-cell adhesion and cell compaction revealed by high-resolution tracking of E-cadherin-green fluorescent protein. J Cell Biol. 1998; 142(4):1105-1119. [21] BENTON G, ARNAOUTOVA I, GEORGE J, et al. Matrigel: from discovery and ECM mimicry to assays and models for cancer research. Adv Drug Deliv Rev. 2014;79-80:3-18. [22] TANIGUCHI K, SHAO Y, TOWNSHEND RF, et al. Lumen Formation Is an Intrinsic Property of Isolated Human Pluripotent Stem Cells. Stem Cell Reports. 2015;5(6):954-962. [23] 刘厚奇,蔡文琴. 医学发育生物学[M].北京:科学出版社, 2012:177-199. [24] MCMAHON JA, TAKADA S, ZIMMERMAN LB, et al. Noggin-mediated antagonism of BMP signaling is required for growth and patterning of the neural tube and somite. Genes Dev. 1998;12(10):1438-1452. [25] BIER E, DE ROBERTIS EM, EMBRYO DEVELOPMENT. BMP gradients: A paradigm for morphogen-mediated developmental patterning. Science. 2015;348(6242):aaa5838. [26] CHAE WJ, EHRLICH AK, CHAN PY, et al. The Wnt Antagonist Dickkopf-1 Promotes Pathological Type 2 Cell-Mediated Inflammation. Immunity. 2016;44(2):246-258. [27] GUO Y, XIE J, RUBIN E, et al. Frzb, a secreted Wnt antagonist, decreases growth and invasiveness of fibrosarcoma cells associated with inhibition of Met signaling. Cancer Res. 2008;68(9):3350-3360. [28] WANG JY, DEL VALLE L, GORDON J, et al. Activation of the IGF-IR system contributes to malignant growth of human and mouse medulloblastomas. Oncogene. 2001;20(29):3857-3868. [29] APPEL B, EISEN JS. Retinoids run rampant: multiple roles during spinal cord and motor neuron development. Neuron. 2003;40(3):461-464. [30] MASON JO, PRICE DJ. Building brains in a dish: Prospects for growing cerebral organoids from stem cells. Neuroscience. 2016;334: 105-118. [31] KELAVA I, LANCASTER MA. Stem Cell Models of Human Brain Development. Cell Stem Cell. 2016;18(6):736-748. [32] LANCASTER MA, CORSINI NS, WOLFINGER S, et al. Guided self-organization and cortical plate formation in human brain organoids. Nat Biotechnol. 2017;35(7):659-666. [33] MATSUI A, JARVIE BC, ROBINSON BG, et al. Separate GABA afferents to dopamine neurons mediate acute action of opioids, development of tolerance, and expression of withdrawal. Neuron. 2014;82(6):1346-1356. [34] BAGLEY JA, REUMANN D, BIAN S, et al. Fused cerebral organoids model interactions between brain regions. Nat Methods. 2017;14(7): 743-751. [35] DOUDNA JA, CHARPENTIER E. Genome editing. The new frontier of genome engineering with CRISPR-Cas9. Science. 2014;346(6213): 1258096. [36] ISSA L, KRAEMER N, RICKERT CH, et al. CDK5RAP2 expression during murine and human brain development correlates with pathology in primary autosomal recessive microcephaly. Cereb Cortex. 2013; 23(9):2245-2260. [37] GARCEZ PP, LOIOLA EC, MADEIRO DA COSTA R, et al. Zika virus impairs growth in human neurospheres and brain organoids. Science. 2016;352(6287):816-818. [38] DANG J, TIWARI SK, LICHINCHI G, et al. Zika Virus Depletes Neural Progenitors in Human Cerebral Organoids through Activation of the Innate Immune Receptor TLR3. Cell Stem Cell. 2016;19(2):258-265. [39] GABRIEL E, RAMANI A, KAROW U, et al. Recent Zika Virus Isolates Induce Premature Differentiation of Neural Progenitors in Human Brain Organoids. Cell Stem Cell. 2017;20(3):397-406. [40] MARIANI J, COPPOLA G, ZHANG P, et al. FOXG1-Dependent Dysregulation of GABA/Glutamate Neuron Differentiation in Autism Spectrum Disorders. Cell. 2015;162(2):375-390. [41] CHANG KH, LEE-CHEN GJ, HUANG CC, et al. Modeling Alzheimer's Disease by Induced Pluripotent Stem Cells Carrying APP D678H Mutation. Mol Neurobiol. 2019;56(6):3972-3983. [42] LOPES FM, BRISTOT IJ, DA MOTTA LL, et al. Mimicking Parkinson's Disease in a Dish: Merits and Pitfalls of the Most Commonly used Dopaminergic In Vitro Models. Neuromolecular Med. 2017;19(2-3): 241-255. [43] ROBBINS JP, PRICE J. Human induced pluripotent stem cells as a research tool in Alzheimer's disease. Psychol Med. 2017;47(15): 2587-2592. [44] LANCASTER MA, KNOBLICH JA. Generation of cerebral organoids from human pluripotent stem cells. Nat Protoc. 2014;9(10):2329-2340. [45] GIANDOMENICO SL, LANCASTER MA. Probing human brain evolution and development in organoids. Curr Opin Cell Biol. 2017;44:36-43. |
| [1] | Luo Lin, Song Naiqing, Huang Jin, Zou Xiaodong. Review and prospect of international research on preschool children’s movement development assessment: a CiteSpace-based visual analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1270-1276. |
| [2] | Xie Wenjia, Xia Tianjiao, Zhou Qingyun, Liu Yujia, Gu Xiaoping. Role of microglia-mediated neuronal injury in neurodegenerative diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1109-1115. |
| [3] | Jiao Hui, Zhang Yining, Song Yuqing, Lin Yu, Wang Xiuli. Advances in research and application of breast cancer organoids [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1122-1128. |
| [4] | Pan Qile, Zhang Hong, Zhou Huikang, Cai Guang. Comparison of the Greulich-Pyle method, the CHN method and the China 05 method for assessing bone age in children and adolescents [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 662-667. |
| [5] | Zhang Yu, Feng Shuo, Yang Zhi, Zhang Ye, Sun Jianning, An Lun, Chen Xiangyang. Three-dimensional gait of patients with developmental dysplasia of hip undergoing total hip arthroplasty with high hip center [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 350-355. |
| [6] | Lin Tianye, Yang Peng, Xiong Binglang, He Xiaoming, Yan Xinhao, Zhang Jin, He Wei, Wei Qiushi . Comparison of preoperative three-dimensional reconstruction simulation and intraoperative drawing of femoral osteotomy to measure rotation angle in vitro [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(21): 3349-3353. |
| [7] | Pan Xuan, Zhao Meng, Zhang Xiumei, Zhao Jie, Zhai Yunkai. Research and application of biological three-dimensional printing technology in the field of precision medicine: analysis of Chinese and English literature [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(21): 3382-3389. |
| [8] | Liu Yongyu, Xu Jingli, Lin Tianye, Wu Feng, Shen Chulong, Xiong Binglang, Zou Qizhao, Lai Qizhong, Zhang Qingwen . Medium-and long-term follow-up of Salter pelvic osteotomy and implant fixation for children with developmental hip dislocation [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(15): 2380-2384. |
| [9] | Zhang Nianjun, Liu Xiaofang, Zhou Guanming, Su Yao, Hong Shi. Three-dimensional-printing assisted total hip arthroplasty for individualized treatment of adult developmental dysplasia of the hip [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(12): 1820-1825. |
| [10] | Fan Qingtao, Du Yun, Zhou Lei . Analysis of development trends of global three-dimensional bio-printing technology based on patent information [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(12): 1891-1897. |
| [11] | Long Qian, Guan Xiaoyan, Wang Qian, Hu Huan, Liu Jianguo. Transcriptome sequencing technology and its application in oral diseases, dental implants and regeneration [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(11): 1791-1798. |
| [12] | Wang Hongshu, Han Shen, Liu Zu, Li Xiaofang, Zhong Chongbin, Li Lifeng, Li Yaxiong, Jiang Lihong. Transcription factor NKX2-5: molecular structure and biological function in regulating cardiovascular precursor cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(1): 108-115. |
| [13] | Lin Wang, Wang Yingying, Lin Weimin, Xu Shenggui, Huang Qilong, Guo Weizhong, Lin Chengshou. Development and biomechanical study of a new sternoclavicular hook plate [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(9): 1395-1399. |
| [14] | Cao Xuhan, Bai Zixing, Sun Chengyi, Li Yanle, Sun Weidong. Application of robot in orthopedic surgery: reliability and room for improvement [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(9): 1416-1421. |
| [15] | Lin Ming, Pan Jinyong, Zhang Huirong. Knockout of NIPBL gene down-regulates the abilities of proliferation and osteogenic differentiation in mouse bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(7): 1002-1008. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||