Chinese Journal of Tissue Engineering Research ›› 2021, Vol. 25 ›› Issue (11): 1791-1798.doi: 10.3969/j.issn.2095-4344.3077
Previous Articles Next Articles
Transcriptome sequencing technology and its application in oral diseases, dental implants and regeneration
Long Qian1, 2, Guan Xiaoyan1, 2, Wang Qian2, Hu Huan2, Liu Jianguo1, 2
- 1Affiliated Stomatological Hospital of Zunyi Medical University, Zunyi 563099, Guizhou Province, China; 2Key Laboratory of Oral Disease Research of Guizhou Colleges and Universities and Key Laboratory of Oral Disease Research of Zunyi, Zunyi 563006, Guizhou Province, China
-
Received:2020-04-23Revised:2020-04-26Accepted:2020-05-28Online:2021-04-18Published:2020-12-22 -
Contact:Guan Xiaoyan, Associate professor, Affiliated Stomatological Hospital of Zunyi Medical University, Zunyi 563099, Guizhou Province, China; Key Laboratory of Oral Disease Research of Guizhou Colleges and Universities and Key Laboratory of Oral Disease Research of Zunyi, Zunyi 563006, Guizhou Province, China Liu Jianguo, Professor, Affiliated Stomatological Hospital of Zunyi Medical University, Zunyi 563099, Guizhou Province, China; Key Laboratory of Oral Disease Research of Guizhou Colleges and Universities and Key Laboratory of Oral Disease Research of Zunyi, Zunyi 563006, Guizhou Province, China -
About author:Long Qian, Master, Physician, Affiliated Stomatological Hospital of Zunyi Medical University, Zunyi 563099, Guizhou Province, China; Key Laboratory of Oral Disease Research of Guizhou Colleges and Universities and Key Laboratory of Oral Disease Research of Zunyi, Zunyi 563006, Guizhou Province, China -
Supported by:Development Project of Youth Science and Technology Talents of Department of Education of Guizhou Province, No. KY[2017]200 (to GXY); Science and Technology Joint Funds of Zunyi Science and Technology Bureau & Zunyi Medical University, No. 2016 (42) (to GXY); Science and Technology Joint Funds of Zunyi Science and Technology Bureau & Zunyi Medical University & Affiliated Hospital of Stomatology of Zunyi Medical University, No. (2018) 239 (to GXY); Special Subsidy Project for Academic New Seedling Cultivation and Innovation Exploration of Zunyi Medical University in 2018, No. [2017] 5733-024 (to GXY)
CLC Number:
Cite this article
Long Qian, Guan Xiaoyan, Wang Qian, Hu Huan, Liu Jianguo. Transcriptome sequencing technology and its application in oral diseases, dental implants and regeneration[J]. Chinese Journal of Tissue Engineering Research, 2021, 25(11): 1791-1798.
share this article
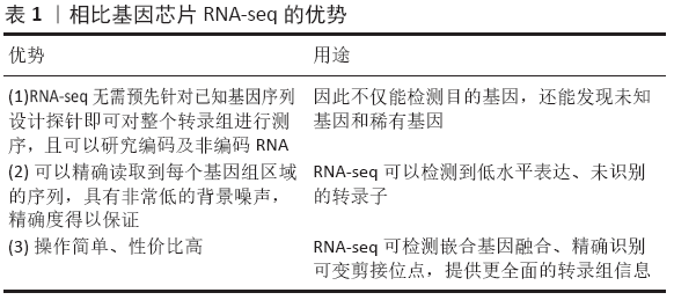
2.1 转录组测序技术 转录组测序技术最早可追溯至1983年COSTANZO等提出的表达序列标签技术雏形,经过几十年发展,该技术已经衍生出众多测序方法,其中RNA-seq凭借其自身优势,成为目前在科学研究中应用最多的转录组测序技术。在口腔医学方面,RNA-seq最开始应用于癌症的研究,后在各分支学科研究中流行起来。 目前应用较多的转录组测序技术有2种:基于测序技术的转录组测序技术和基于杂交技术的微阵列技术[3]。基于测序技术的转录组测序技术包括表达序列标签技术(expression sequence tags,EST)、基因表达系列分析技术(serial analysis of gene expression,SAGE)、RNA-seq、单分子实时测序技术(single molecule real time sequencing,SMRT-seq)和Oxford Nanopore 纳米孔单分子测序技术等[4]。表达序列标签技术和基因表达系列分析技术是最早出现的转录组测序方法。表达序列标签技术的测序长度是150-500 bp,通量低;从cDNA片段的3’-端或者5’-端特定序列开始测序,具有盲目性;高、中丰度基因的表达序列标签技术有一定的冗余性,增加测序成本[5]。基因表达系列分析技术是将转录本转化成9-14 bp大小的标签,且多个标签串联,测序通量得到提高;一个文库可以测定几十万个短标签,测序深度得以提升。但是,也正因为标签太短,很难唯一注释到转录本。为了提高测序精度,研究者加长测序标签至21 bp[6],但是到目前为止,仍有近一半的标签未能进行注释。因此,RNA-seq技术顺势而生。 RNA-seq技术核心思想是边合成边测序或边连接边测序,提高了测序通量,降低了测序成本,快速准确地获得基因组编码序列[7];与表达序列标签技术、基因表达系列分析技术相比较,具有精度高、通量大、动态检测范围广且价格低的优点。但是RNA-seq技术也有着自身局限,即通量高的读长短,读长长的通量低[8]。为了解决这一难题,SMRT-seq和Oxford Nanopore出现[9-10],该技术直接对原始模板进行检测,实现了长读长、单分子测序,测序速度快,通量高,但也正因为是单分子测序,只要其中一个分子检测错误,实验结果的准确性将会大打折扣。也就是说,相比RNA-seq,SMRT-seq和Oxford Nanopore的测序精度有待提高。基于杂交技术的微阵列技术即基因芯片,也称为DNA芯片,理论基础来源于Southern 提出的杂交测序理论,即把预先设计好的基因探针集成在基片(玻片、尼龙膜等)上,然后与经过荧光标记的样本进行杂交,形成互补链,通过显微镜检测杂交信号,以实现对样本的数据分析[11]。基因芯片技术可以利用多个基片在短时间内同时研究不同样本中上万个基因,检测效率高。但是由于基片不能重复使用,并且需要预先设计探针,因此检测费用昂贵,且只能针对已知序列基因进行检测分析[12]。相比基因芯片,RNA-seq具有显著优势[13](表1),因此RNA-seq目前已广泛应用于生物学、医学基础研究、临床疾病分子诊断等各个生命科学领域。 2.2 RNA-seq在口腔医学领域的应用 RNA-seq技术最早应用于酿酒酵母、玉米和拟南芥等的研究[14-16],由于其独特优势,深受广大研究者青睐。在口腔医学领域,RNA-seq技术最开始被用于鳞癌的研究,后逐渐在口腔干细胞、牙体、牙周、修复和正畸领域相关研究中普及,刷新了人们对口腔领域的认知。 2.2.1 口腔鳞状细胞癌(oral squamous cell carcinoma,OSCC) 口腔鳞状细胞癌是最常见的头颈部癌,具有发病率高、侵袭性强、易转移的特点,现有筛查手段效果有限,治疗方式破坏性强,且预后差,因此对口腔癌早期诊断、治疗和预后评估的研究一直处于热门。RNA-seq技术从分子水平探究口腔癌的刺激因素、诊断治疗以及预后影响,以期降低口腔鳞状细胞癌发病率、提高治愈率。 目前,针对口腔鳞状细胞癌易感因素的研究众多,但是易感因素的种类及其作用的分子机制并不明确。ZAMMIT等[17]利用RNA-seq技术研究口腔鳞状细胞癌与烟草和HPV的关系,结果显示,烟草因其可改变细胞TP53转录、mTOR信号转导和线粒体功能而成为口腔鳞状细胞癌危险因素,但HPV感染与口腔鳞状细胞癌的相关性并不高,这一结论与WATLING等[18]和GHANTOUSA等[19]研究一致。然而,有学者表示HPV感染亦是口腔鳞状细胞癌的一个重要危险因素[20-21],但是,目前的研究并没有充分证据证明两者之间的关系。分子和遗传的研究证据表明,癌症的发生、发展与体细胞特定基因突变的积累有关。ZHANG 等[22]利用RNA-seq成功筛选了70 000多个与肿瘤相关的突变基因,并鉴定出6个口腔鳞状细胞癌特异性突变基因,包括ANKRA2、GTF2H5、STOML1、NUP37、PPP1R26和TAF1L;而且还发现TGFBR2在口腔鳞状细胞癌中有5种选择性剪接缺陷形式,通过这些剪接缺陷形式,癌细胞可以逃避转化生长因子β信号通路调节的抗肿瘤作用。GOERTZEN等[23]利用RNA-seq研究并发现机体通过上调促炎基因表达从而增加癌细胞的细胞分裂,其中肿瘤坏死因子α是促进口腔鳞状细胞癌发展的重要启动子。该研究中,上调的促炎基因主要包含C-X-C基序的细胞因子,如CXCL1、CXCL3、CXCL2和CXCL10,这些因子已被XIA等[24]和LEE等[25]证明参与调控口腔鳞状细胞癌进程;研究同时还发现上调的基质金属蛋白酶1、基质金属蛋白酶9、基质金属蛋白酶14、LAMB3和成纤维细胞生长因子2等浸润相关基因显著增加肿瘤的侵袭性[26-27]。ZHANG等[28]利用RNA-seq分析了舌鳞状细胞癌的基因表达,发现有7个基因表达差异性显著,其中FOLR1、NKX3-1、TFF3和PIGR显著下调,NEFL、基质金属蛋白酶13、HMGA2显著上调。在这些基因中,基质金属蛋白酶13、HMGA2已被证明能显著增加口腔鳞癌的侵袭和转移[29-30];TFF3曾在乳腺癌、前列腺癌、胃癌等癌组织中被发现[31-33],在口腔鳞癌中的发现属首次,其所扮演的角色有待探究。YAO等[34]的研究发现MALAT1在口腔鳞状细胞癌中过表达,KTN1-AS1、LINC00460和RP5-894A10.6这3个基因可能是口腔鳞状细胞癌患者准确预测疾病预后的生物标志物。MISHRA等[35]利用RNA-seq探究口腔鳞状细胞癌相关基因表达情况,结果表明,细胞黏附分子PCDH18的高表达降低了口腔鳞状细胞癌的总体存活率,提示PCDH18是该癌的潜在负性预后因子。 目前的研究发现诸多与口腔鳞状细胞癌发生、发展和预后评估相关的基因,但是并没有明确哪些基因与口腔鳞状细胞癌高度有关,也没有说明这些基因间是否存在协同或者拮抗作用,更没有提出针对这些基因的靶向治疗方案,未来的研究可以针对已发现基因进行更为深入的探索,亦可转向基因间的相互作用以及如何控制基因改变的研究,以找到评估和治疗口腔鳞状细胞癌的靶向基因。 2.2.2 牙周炎 牙周炎是由菌斑生物膜引起的牙周支持组织的感染性破坏性疾病,如若治疗不及时,随着病变发展,最终可导致牙齿丧失。目前,牙周炎的检测指标少,治疗方式单一,治愈后也容易复发,不能从根本治疗牙周炎。因此,需要找到更为有效的检测手段和治疗方式,避免因检测不及时和治疗不当所带来的严重后果。 早在2008年,DEMMER等[36]便对牙周炎患者牙龈组织转录组进行研究,为牙周炎病理生物学的研究奠定基础。2012年,DAVANIAN等[37]首次使用RNA-Seq对牙周炎患者牙龈组织中基因表达进行定量综合定位,确立了牙周炎炎性标志物白细胞介素1β、白细胞介素6、白细胞介素8、肿瘤坏死因子α、RANTES和MCP-1,在此之前也曾被报道过[38]。口腔是一个复杂的微环境,细菌种类成百上千,微生物与牙周病之间是否存在某些联系,尚未有确切的说法。SOLBIATI等[39]从转录水平研究发现微生物群落的失衡与牙周病间存在某种关系,但是并没有明确指出其中的缘由。DURAN-PINEDO等[40]从转录水平研究口腔微生物代谢情况表明,细菌脂多糖、鞭毛和铁的获取是导致牙周炎的主要原因。后来的研究表明牙龈卟啉单胞菌的脂多糖可以影响人牙周膜成纤维细胞,但是它们之间的关系一直没有明确。WU等[41]通过RNA-seq技术对牙龈卟啉单胞菌的致病机制进行研究,结果表明牙龈卟啉单胞菌脂多糖能够促使人牙周膜成纤维细胞分泌白细胞介素6、白细胞介素8、MCP-1、基质金属蛋白酶1、基质金属蛋白酶3等炎性因子对牙周组织进行破坏,且得到qRT-PCR的验证。 研究者们利用RNA-seq技术优势对牙周炎基因改变进行研究,试图寻找牙周炎治疗的靶向基因。KIM等[42]对10例健康人和牙周炎患者的牙龈组织进行RNA-Seq深度测序,基因差异表达分析显示牙周炎组织中存在400个上调基因和62个下调基因。前10位上调基因分别是CSF3、MAFA、CR2、GLDC、SAA1、LBP、MME、基质金属蛋白酶3、MME-AS1和SAA4,富集到防御/免疫蛋白、受体、蛋白酶和信号分子途径;前10位下调的基因是SERPINA12、MT4、H19、KRT2、DSC1、PSORS1C2、KRT27、LCE3C、AQ5和LCE6A,富集到细胞骨架蛋白和结构蛋白。LUNDMARK等[43]采用空间转录组学方法,即结合RNA-Seq测序和组织学分析,对牙周炎患者牙龈组织中的基因表达进行了定量和定位。研究结果揭示了基因表达簇在上皮、结缔组织的发育区和未发育区表达一致,其中,IGLL5、SSR4、MZB1和XBP1是4个表达上调幅度最高的基因。有研究表明牙周病的发生与维生素D缺乏有关[44],但具体机制尚可未知,LORENZO等[45]通过体外实验和动物实验试图探索其机制。体外实验用非活性维生素D处理人牙龈上皮细胞,检测发现牙龈上皮细胞表达2个25-羟化酶(CYP27A1和CYP2R1)和1-α羟化酶,使维生素D同时转化为25(OH)D3和1,25(OH)2D3,抑制牙龈单胞菌的生长;利用RNA序列技术检测1,25(OH)2D3作用于牙龈上皮细胞后的总mRNA序列,测序结果显示经1,25(OH)2 D3处理后,牙龈促炎因子白细胞介素1α表达水平降低。而动物实验显示在饮食中缺乏维生素D的小鼠口腔内观察到牙龈炎症和牙槽骨缺失,与对照组相比,差异显著;小鼠局部应用维生素D3和1,25(OH)2D3可抑制小鼠牙龈促炎因子白细胞介素1α的表达。总的来说,牙龈上皮细胞可以将非活性维生素D原位转化为活性形式,活化的维生素D在体内外均能增强牙龈上皮细胞抵抗牙周病原菌侵袭的活性,抑制炎症反应,支持了维生素D可以直接应用于牙龈预防或治疗牙周病的假设。LIU等[46]利用RNA-seq对慢性牙周炎中的单核细胞进行了研究,结果发现慢性牙周炎患者外周血单核细胞的吞噬功能、细胞因子生成和细胞凋亡是慢性牙周炎发病的重要机制,这对研究慢性牙周炎病因和治疗起到指导意义。SHUSTERMAN等[47]则通过RNA-seq明确PF4、PPBP、CXCL5 这3个基因可能是造成牙周炎遗传的基因座,为研究牙周炎的遗传倾向提供基础。 目前大量研究对牙周炎的生物标志物、基因变化和微生物群的作用进行探索,除了明确牙周炎的炎性标志物外,并没有清楚阐述基因间的相互作用,同时缺乏足够的证据证明上述基因的改变一定会导致牙周炎。而且牙周炎的疾病分类众多,不同类别的牙周炎之间基因改变是否有区别也是值得商榷的。因此,还需对牙周炎进行更为深入的研究。 2.2.3 牙体牙髓病 龋病是牙体硬组织的慢性、进行性、不可逆性疾病,发展到一定程度,则导致牙髓疾病。虽然目前大量研究明确了牙体牙髓病的发生、发展,并对治疗作出指导,但是临床上仍然有许多尚未解决的难题,因此,需要从新的方向进行研究,期以找到解决问题的方法。 儿童早期龋病发病率高,进展快,治疗费用昂贵,且对儿童来说治疗过程相当痛苦。有研究表明在患有儿童早期龋病的儿童口腔生物膜中,白色念珠菌常与变形链球菌大量共存。白色念珠菌是口腔中常见的机会真菌,可与某些链球菌相互作用后在黏膜表面形成生物膜,导致口腔黏膜感染。但是白色念珠菌并不能直接与变异链球菌进行良好的黏附,也不能独立定植于牙面,然而在蔗糖存在下,变形链球菌和白色念珠菌之间的共黏附显著增加,SZTAJER等[48]利用扫描电镜、气相色谱-质谱和转录组的分析结果均证实这一观点。然而,两者是如何相互作用从而刺激变形链球菌发挥更大的致龋性仍然不清楚。HE等[49]用RNA-seq对变异链球菌单种生物膜和变异链球菌混合白色念珠菌双种生物膜中富集的mRNA进行转录组分析,分析了白色念珠菌的存在对变形链球菌整个转录组的影响。结果表明,白色念珠菌显著改变双种生物膜中变形链球菌的基因表达,促进碳水化合物代谢,增加了变形链球菌对底物的利用率。ELLEPOLA等[50]采用转录组学分析结合蛋白质组学方法试图揭示白色念珠菌与变异链球菌在双种生物膜中共培养时的分子途径。研究表明,白色念珠菌的糖代谢和蛋白质相关基因显著增强,主要包括糖转运、有氧呼吸、丙酮酸分解和乙醛酸循环;进一步分析发现,变形链球菌的GtfB能与白色念珠菌细胞表面特异结合,促进两者的共黏附,从而将蔗糖分解成葡萄糖和果糖,而葡萄糖和果糖又很容易被白色念珠菌代谢。以上研究表明,在蔗糖存在时,白色念珠菌与变形链球菌的GtfB特异结合,增加了两者在生物膜上的黏附性,并通过改变相关基因促进糖代谢,加速龋齿形成。 CHO等[51]利用RNA-seq测定人牙髓细胞暴露于低毒性浓度的三甘醇二甲基丙烯酸酯的基因表达改变,结果证实,即使是低毒性浓度的树脂单体,牙髓细胞基因表达也会随着时间发生变化,其中HMOX1、OSGIN1、SMN2、SRXN1 AKR1C1、SPP1、TOMM40L是随时间推移高度上调的基因,WRAP53和CCL2是随时间变化高度下调的基因,该研究提示树脂会刺激牙髓发生炎症反应,临床治疗时需考虑这一因素。ZENG等[52]利用RNA-seq初步探究变异链球菌经蔗糖和果糖处理后的转录组的变化,研究指出,蔗糖和其他碳水化合物对变异链球菌这种机会致病菌的生理和遗传产生深远影响,不仅阻碍能量代谢和促进产酸,而且可能通过侧向基因转移影响应激耐受、细胞间通讯和细菌进化。SENEVIRATNE等[53]利用RNA-Seq分析粪肠球菌生物膜形成机制和耐药性分析,为控制粪肠球菌感染和预防根管治疗失败提供理论依据,从而提高根管治疗成功率。 目前针对牙体牙髓病在转录组的研究较少,主要集中在白色念珠菌与变异链球菌的关系、牙体牙髓病的治疗上。但龋病和牙髓病是多因素相互作用导致的,且患病部位不同,病情严重程度不同,致病菌亦有所区别,若想探究清楚龋病、牙髓病的致病因素和基因改变,不能一概而论,应对其进行分类后研究。而且,针对牙髓病的治疗方式有限且疗效不甚理想,未来的研究可以着重于牙髓病的治疗上,以指导临床工作。 2.2.4 牙再生工程 牙再生工程是口腔医学领域当下最热门研究。人牙髓干细胞的成牙本质/成骨分化是牙髓再生的关键因素。2014年KEISHI等[54]对干细胞基牙再生的研究进展进行综述,探讨了诱导多能干细胞进行干细胞基牙再生的可能性,使得牙再生技术得以广泛传播。 哺乳动物的牙齿是通过神经嵴来源的中胚层和靠近中胚层的6-8层外胚层相互作用形成,先前的研究表明牙髓干细胞是一种在成人牙齿中保持再生能力的干细胞群。目前的研究均使用间充质干细胞的表面标志物来笼统标记所有干细胞,因此人们认为牙髓干细胞表达间充质干细胞表面标志物,如CD44、CD45、CD73、CD90、CD146、CD29和Stro-115。实际上,并不是所有的干细胞都能表达间充质干细胞表面标记物。因此,找到牙髓干细胞特异性表面标记物对未来的研究有着重大指导意义。MACRIN等[55]通过RNA-seq和qPCR分析确认蛋白Barx1是牙髓干细胞的标记物,同时利用RNA-seq和蛋白质组学综合分析发现在快速老化的牙髓干细胞中,转化生长因子β和细胞骨架蛋白表达上调。通过该研究,可以预测和阻止牙髓干细胞的老化,对牙再生研究和指导临床治疗都是有益的。牙髓干细胞是有再生能力的干细胞,但是其成牙本质/成骨分化机制尚不明确。Stathmin是牙髓干细胞中一种重要的可溶性微管辅助蛋白,通过螯合和传递参与Shh/Gli、Wnt/β-catenin、核因子κB等成骨相关信号通路,但Stathmin在牙髓干细胞成牙本质/成骨分化中的调控机制并不清楚。ZHANG等[56]利用RNA-seq技术探讨Stathmin影响牙髓干细胞增殖和成牙本质细胞/成骨细胞分化的机制,首次揭示Stathmin蛋白通过Wnt/β-catenin通路参与调控牙髓干细胞增殖和成牙本质细胞/成骨细胞分化。研究同时筛选出3 000多个与Stathmin水平变化相关的蛋白,为进一步探索Stathmin在细胞生物学特性各个方面的调控机制提供了可能。此次研究为进一步研究牙髓干细胞的成牙本质/成骨分化机制提供了理论依据,并为Stathmin能否作为牙髓组织临床修复的关键基因提供证据,为牙髓组织工程提供了新的思路。 TAO等[57]之前的体外实验显示Krüppel-样因子4(KLF4)可以促进小鼠牙乳头细胞和人牙髓细胞的成牙本质分化,但其机制尚不清楚。现该团队利用RNA-seq测序技术检测Klf4与牙本质形成的关系,结果表明Klf4通过调节转化生长因子β信号通路及与组蛋白乙酰化的相互作用促进成牙本质细胞分化和牙本质形成。以往研究表明抗转化生长因子β信号传导参与调控牙齿形态,而Smad7是转化生长因子β的通用拮抗剂,但是Smad7在牙齿发育中的确切作用尚不清楚。LIU等[58]在发育中的小鼠磨牙里发现Smad7在牙齿上皮细胞中的表达水平较高,而Smad7缺乏将使上皮细胞增殖能力严重受损,导致过小牙的形成。RNA序列分析显示Smad7主要通过抑制牙上皮细胞发育过程中转化生长因子β信号传导来发挥对细胞增殖的积极调节作用,并强调Smad7在控制牙齿大小中的正调节作用。WNT10a是Wnt/β-catenin途径中的配体,最近有证据表明WNT10a突变的患者牙齿呈典型的牛牙样牙特征[59-61],表明Wnt10a与牙根形态发育之间存在联系,但是究竟是上皮细胞还是间充质细胞的Wnt10a控制根分叉的形成尚不清楚。YU等[62]通过动物实验进行研究,首次揭示上皮细胞中的Wnt10a是根分叉形成的关键。该实验利用RNA-seq证明上皮细胞的Wnt10a可以控制邻近间充质细胞组织增殖,从而控制牙根形成,同时还在病变牙中检测到Wnt4,说明Wnt4可能参与调控根分叉病变,但具体机制尚不清楚。Wnt10a在上皮间质相互作用的研究刷新了人们对牙根发育的认知,将有助于牙根再生的生物工程。尽管目前有多种来源的干细胞可供利用,但获得这些干细胞涉及侵入性操作,可能很难或成本高昂,而且数量有限。牙髓干细胞是一种多能干细胞,存在于脱落牙髓的深处。为了研究牙髓干细胞的特性,对牙髓干细胞进行了一系列的存活、衰老、永生化和基因表达研究,发现经人类端粒酶反转录酶处理的牙髓干细胞神经元具有与非永生化牙髓干细胞相同的形态学和电生理特性,用人类端粒酶反转录酶处理后72 h内的牙齿仍可以提取到牙髓干细胞并用于体外研究。LU等[63]鉴定多生牙干细胞(SNTSCs)的基本特征和基因表达谱,并与正常牙髓干细胞进行比较。RNA-seq结果显示多生牙干细胞与牙髓干细胞之间存在差异表达基因,且基因表达模式不同,多生牙干细胞增殖率和迁移率均显著高于牙髓干细胞。该研究揭示了多生牙干细胞可能具有较大的细胞分化潜能。 虽然有研究认为lncRNAs、circRNAs和miRNAs参与了牙周膜干细胞成骨分化过程,但关于它们的潜在关联和功能的研究还不多见。竞争性内源RNAs(ceRNAs)通过竞争miRNA反应元件打破miRNA和靶基因之间的平衡,从而调节生理和病理过程,这些ceRNAs包括各种类型的RNA,如lncRNAs、circRNAs、mRNAs等。为了充分了解ceRNA对牙周膜干细胞成骨分化的影响,研究lncRNA/circRNA-miRNA竞争性调控网络至关重要。GU等[64]利用RNA-seq技术研究鉴定了牙周膜干细胞成骨分化过程中lncRNAs、circRNAs和mRNAs的差异表达。通过GO和KEGG通路分析,整合了lncRNAs、circRNAs、miRNAs和mRNAs的ceRNA网络,并探讨其成骨调控机制。研究表明,特异性lncRNAs和circRNAs可能作为ceRNAs促进牙周膜干细胞成骨分化和牙周再生。 目前的研究主要集中在牙髓干细胞表面标志物和其成骨/成牙本质调控因子、牙冠大小和牙根发育调控因素、牙髓干细胞保存、多生牙干细胞再生能力和牙周膜干细胞成骨分化,试图阐述干细胞对于牙再生的作用机制;但是牙再生涉及牙冠、牙根、牙周组织的再生,每一部分涉及的因素都很多。目前的研究结果只是牙再生工程的冰山一角,仍需要大量的研究作为理论支撑以实现牙再生,未来若牙再生工程成功,在口腔医学界将引起不小的轰动。 2.2.5 正畸、种植 纵观目前正畸的基础研究,正畸牙移动的分子生物学研究大多集中在mRNA,对ncRNA的研究鲜见报道,而ncRNA已被证明在癌症、老年痴呆症和牙周炎等疾病的病原学中发挥着重要作用,那在正畸牙移动过程中扮演什么角色呢?HUANG等[65]首次利用转录组测序技术对正畸牙中牙周膜干细胞的mRNA和长非编码RNA(lncRNA)进行测序,并用qRT-PCR验证结果,研究除发现519个与细胞外基质组织、胶原纤维组织和细胞对缺氧反应有关的差异表达的mRNAs外,还发现90个差异显著的lncRNAs,其中72个上调表达,18个下调表达,参与基因转录的调控、转录后调控、剪接以及表观遗传调控和印记等。该研究初步探索了lncRNA在正畸牙运动中的潜在作用,使得正畸学研究进入新领域。在未来,lncRNA很可能被用于调节牙齿运动,以达到治疗目的,如加速正畸治疗、预防正畸诱导的牙根吸收等。PROFF等[2]发表文章及HUANG等[65]的研究让人们第一次注意到正畸学中被忽视的lncRNA。HUANG等[65]对牙周膜干细胞机械压缩过程中差异表达lncRNA可能功能的初步研究,极大的扩展了人们对牙齿运动规律的认识,为未来正畸研究奠定了基础,同时也为正畸医师提供新的治疗方向和诊疗辅助手段。 骨皮质切开是促进正畸牙齿移动的一种常用技术,可在无皮瓣反射的情况下诱发局部牙槽骨改建,加速牙齿移动,且不会对患者造成过大创伤[66-67]。然而,骨皮质切开术加速正畸牙移动的潜在机制仍不清楚,通过分析大鼠牙齿移动模型的差异转录组,探讨了骨皮质切开后牙槽组织重塑的机制。骨皮质切开组和未行骨皮质切开组的总mRNA中有399个基因统计学差异显著,选择11个基因进行qRT-PCR验证,结果一致。11个基因中包括Rasgrp2, Rasprp4, Prkcb和Pak2等,这4个基因编码关于Ras信号的4种蛋白,可加速破骨细胞生成,在骨皮质切开组中高表达,因此可以证明骨皮质切开术通过Ras信号通路介导的破骨细胞生成加速正畸牙移动[68]。 牙齿缺失是临床常见疾病,随着社会经济的发展,越来越多的人选择种植牙修复缺失牙,但是种植后的成功率受到许多因素影响,如何提高种植成功率是目前面临的一大难题。临床中发现吸烟是导致种植术失败的重要危险因素,但是其机制并不明确。THALJI等[69]在吸烟和非吸烟患者口腔中植入种植体,1周后提取植入物中的RNA进行全基因组微阵列检测,发现在骨结合的早期种植体贴壁细胞基因表达谱没有差异,表明骨结合早期吸烟者和非吸烟者的种植黏附细胞相似,提示未来若研究吸烟是否是牙种植失败的原因,应将观察时间延长,至少超过2周。CHOA等[70]通过转录组学层面发现初级纤毛对成骨细胞在骨-种植体界面感知应变相关的机械刺激至关重要。CALCIOLARI等[71]认为转录组学技术正在成为发现骨形成和骨结合分子机制的强大工具,用于识别特定的信号通路,而这些通路则成为以后治疗的靶向目标。目前对于正畸、种植转录组学研究较少,正畸牙齿移动机制和种植牙骨结合失败的原因仍不清楚,还需要大量研究进行探索。"

| [1] IRWANDI RA, VACHARAKSA A. The role of microRNA in periodontal tissue: A review of the literature. Arch Oral Biol. 2016;72:66-74. [2] PROFF P, KIRSCHNECK C. The fascinating world of Non-Coding RNA and how It may help to unravel the mysteries of tooth movement regulation. Eur J Orthod. 2019;41(4):343-345. [3] 史硕博, 陈涛, 赵学明. 转录组学平台技术及其在代谢工程中的应用[J]. 生物工程学报,2010,26(9):1187-1198. [4] MAXAM AM, GILBERT W. A new method for sequencing DNA. Proc Natl Acad Sci U S A. 1977;74(2):560-564. [5] SULIEMAN AA, HUSSEIN MM, Salem SA. Analysis of Expressed Sequence Tags (EST) in Date Palm. Methods Mol Biol. 2017;1638: 283-313. [6] WAHL MB, HEINZMANN U, IMAI K. LongSAGE analysis significantly improves genome annotation: identifications of novel genes and alternative transcripts in the mouse. Bioinformatics. 2005;21: 1393-1400. [7] GOODWIN S, MCPHERSON JD, MCCOMBIE WR. Coming of age: ten years of next-generation sequencing technology. Nat Rev Genet. 2016; 17(6):333-351. [8] CHOWDHURY HA, BHATTACHARYYA DK, KALITA JK. Differential expression analysis of RNA-seq reads: overview, taxonomy and tools. Trans Comput Biol Bioinform. 2020;17(2):566-586. [9] SIMON A, ADAM A, JORIS RV, et al. Single molecule real-time (SMRT) sequencing comesof age: applications and utilities for medicaldiagnostics. Nucleic Acids Res. 2018;46(5):2159-2168. [10] LU H, GIORDANO F, NING Z. Oxford Nanopore MinION Sequencing and Genome Assembly. Genomics Proteomics Bioinformatics. 2016; 14(5):265-279. [11] GU Q, SIVANANDAM TM, KIM C. Signal stability of Cy3 and Cy5 on antibody microarrays. Proteome Sci. 2006;4:21. [12] BOLÓN-CANEDO V, ALONSO-BETANZOS A, LÓPEZ-DE-ULLIBARRI I,et al. Challenges and Future Trends for Microarray Analysis. Methods Mol Biol. 2019;1986:283-293. [13] STARK R , GRZELAK M, HADFIELD J. RNA sequencing: the teenage years. Nat Rev Genet. 2019;20(11):631-656. [14] EMRICH SJ, BARBAZUK WB, LI L, et al. Gene discovery and annotation using LCM-454 transcriptome sequencing. Genome Res. 2007;17(1): 69-73. [15] LISTER R, O’MALLEY RC, TONTI-FILIPPINI J, et al. Highly integrated single-base resolution maps of the epigenome in Arabidopsis. Cell. 2008;133(3):523-536. [16] NAGALAKSHMI U, WANG Z, WAERN K, et al. The transcriptional landscape of the yeast genome defined by RNA sequencing. Science. 2008; 320(5881):1344-1349. [17] ZAMMIT AP, SINHA R, COOPER CL, et al. Examining the contribution of smoking and HPV towards the etiology of oral cavity squamous cell carcinoma using high-throughput sequencing: A prospective observational study. PLoS One. 2018;13(10):e0205406. [18] WATLING DW, GOWN AM, COLTRERA MD. Overexpression of p53 in head and neck cancer. Head Neck. 1992;14(6):437-444. [19] GHANTOUSA Y, BAHOUTHB Z, ABU EI. Clinical and genetic signatures of local recurrence in oral squamous cell carcinoma. Arch Oral Biol. 2018;95:141-148. [20] HÜBBERS CU, AKGÜL B. HPV and cancer of the oral cavity. Virulence. 2015;6(3):244-248. [21] JIANG S, DONG Y. Human papillomavirus and oral squamous cell carcinoma: A review of HPV-positive oral squamous cell carcinoma and possible strategies for future.Curr Probl Cancer. 2017;41(5): 323-327. [22] ZHANG Q, ZHANG J, JIN H, et al. Whole transcriptome sequencing identifies tumor-specific mutations in human oral squamous cell carcinoma. BMC Medical Genetics. 2013;6:28. [23] GOERTZEN C, MAHDI H, LALIBERTE C, et al. Oral inflammation promotes oral squamous cell carcinoma invasion. Oncotarget. 2018;9(49): 29047-29064. [24] XIA J, WANG J, CHEN N, et al. Expressions of CXCR7/ligands may be involved in oral carcinogenesis.J Mol Histol. 2011;42(2):175-180. [25] LEE CH, SYU SH, LIU KJ, et al. Interleukin-1 beta transactivates epidermal growth factor receptor via the CXCL1-CXCR2 axis in oral cancer. Oncotarget. 2015;6:38866-38880. [26] JIMENEZ L, JAYAKAR SK, OW TJ, et al. Mechanisms of invasion in gead and neck cancer. Arch Pathol Lab Med. 2015;139(11):1334-1348. [27] HASE T, KAWASHIRI S, TANAKA A, et al. Fibroblast Growth factor-2 accelerates invasion of oral squamous cell carcinoma. Oral science international. 2006;3(1):1-9. [28] ZHANG HX, SHENG O, DENG LC, et al. Genome-wide gene expression profiling of tongue squamous cell carcinoma by RNA-seq. Clin Oral Investig. 2018;22(1):209-216. [29] YANG B, GAO J, RAO Z, et al. Clinicopathological significance and prognostic value of MMP-13 expression in colorectal cancer. Scand J Clin Lab Invest. 2012;72(6):501-505. [30] ZHAO XP, ZHANG H, JIAO JY, et al. Overexpression of HMGA2 promotes tongue cancer metastasis through EMT pathway. J Transl Med. 2016;14: 26. [31] MAY FE, WESTLEY BR. TFF3 is a valuable predictive biomarker of endocrine response in metastatic breast cancer. Endocr Relat Cancer. 2015;22(3):465-479. [32] TERRY S, NICOLAIEW N, BASSET V, et al. Clinical value of ERG, TFF3, and SPINK1 for molecular subtyping of prostate cancer. Cancer. 2015; 121(9):1422–1430. [33] GU J, ZHENG L, ZHANG L, et al. TFF3 and HER2 expression and their correlation with survival in gastric cancer.Tumour Biol. 2015;36(4): 3001-3007. [34] YAO Y, XINYUAN C, SHUAI L, et al. Circulating long noncoding RNAs as biomarkers for predicting head and neck squamous cell carcinoma. Cell Physiol Biochem. 2018;50(4):1429-1440. [35] MISHRA A, SRIRAM H, CHANDARANA P, et al. Decreased expression of cell adhesion genes in cancer stem-like cells isolated from primary oral squamous cell carcinomas. Tumour Biol. 2018;40(5): 1010428318780859. [36] DEMMER RT, BEHLE JH, WOLF DL, et al. Transcriptomes in healthy and diseased gingival tissues. J Periodontol. 2008;79(11):2112-2124. [37] DAVANIAN H, STRANNEHEIM H, BAGE T, et al. Gene Expression Profiles in Paired Gingival Biopsies from Periodontitis-Affected and Healthy Tissues Revealed by Massively Parallel Sequencing. PLoS One. 2012; 7(9): e46440. [38] PRADEEP AR, DAISY H, HADGE P, et al. Correlation of gingival crevicular fluid interleukin-18 and monocyte chemoattractant protein-1 levels in periodontal health and disease. J Periodontol. 2009;80(9):1454-1461. [39] SOLBIATI J, FRIAS-LOPEZ J. Metatranscriptome of the Oral Microbiome in Health and Disease. J Dent Res. 2018;97(5):492-500. [40] DURAN-PINEDO AE, CHEN T, TELES R, et al. Community-wide transcriptome of the oral microbiome in subjects with and without periodontitis. ISME J. 2014;8(8):1659-1672. [41] WU X, ZHANG G, FENG XQ , et al. Transcriptome analysis of human periodontal ligament fibroblasts exposed to porphyromonas gingivalis LPS. Arch Oral Biol. 2020;110:104632. [42] KIM YG , KIM M, KANG JH, et al. Transcriptome sequencing of gingival biopsies from chronic periodontitis patients reveals novel gene expression and splicing patterns. Hum Genomics. 2016;10(1):28. [43] LUNDMARK A, GERASIMCIK N , BÅGE T, et al. Gene expression profling of periodontitis-afected gingival tissue by spatial transcriptomics. Sci Rep. 2018;8(1):9370. [44] LAKY M, BERTL K, HARIRIAN H, et al. Serum levels of 25-hydroxyvitamin D are associated with periodontal disease. Clin Oral Investig. 2017; 21(5):1553-1558. [45] LORENZO PM , WILLAM R , MOBASWAR HC, et al. Activation of Vitamin D in the gingival epithelium and its role in gingival inflammation and alveolar bone loss.J Periodontal Res. 2019;54(4):444-452. [46] LIU YZ, MANEY P, PURI J, et al. RNA-sequencing study of peripheral blood monocytes in chronic periodontitis. Gene. 2016;581(2): 152-160. [47] SHUSTERMAN A, MUNZ M, RICHTER G, et al. The PF4/PPBP/CXCL5 gene cluster is associated with periodontitis. J Dent Res. 2017;96(8):945-952. [48] SZTAJER H , SZAFRANSKI SP, TOMASCH J, et al. Cross-feeding and interkingdom communication in dual-species biofilms of Streptococcus mutans and Candida albicans.ISME J. 2014;8(11):2256-2271. [49] HE JZ, KIM D, ZHOU XD, et al. RNA-seq reveals enhanced sugar metabolism in streptococcus mutans co-cultured with candida albicans within mixed-species biofilms. Front Microbiol. 2017;8:1036. [50] ELLEPOLA K, TRUONG T, LIU Y, et al. Multi-omics analyses reveal synergistic carbohydrate metabolism in streptococcus mutans-candida albicans mixed-species biofilms. Infect Immun. 2019;87(10):e00339-19. [51] Cho SG, Lee JW, Heo JS, et al. Gene expression change in human dental pulp cells exposed to a low-level toxic concentration of triethylene glycol dimethacrylate: an RNA-seq analysis.Basic Clin Pharmacol Toxicol. 2014;115(3):282-290. [52] ZENG L, BURNE RA. Sucrose-and Fructose-Specific effects on the transcriptome of streptococcus mutans, as determined by RNA Sequencing. Appl Environ Microbiol. 2015;82(1):146-156. [53] SENEVIRATNE CJ, SURIVANARAYANAN T, SWARUP S, et al. Transcriptomics analysis reveals putative genes involved in biofilm formation and biofilm-associated drug resistance of enterococcus faecalis. J Endod. 2017; 43(6):949-955. [54] KEISHI O , MIKA KS, NAOKI F, et al. Stem cell sources for tooth regeneration: current status and future prospects. Front Physiol. 2014;5:36. [55] MACRIN D, ALGHADEER A, ZHAO YT, et al. Metabolism as an early predictor of DPSCs aging. Sci Rep. 2019;9(1):2195. [56] ZHANG XY, NING TT, WANG H, et al. Stathmin regulates the proliferation and odontoblastic/osteogenic differentiation of human dental pulp stem cells through Wnt/β-catenin signaling pathway.J Proteomics. 2019;202:103364. [57] TAO HH, LIN H, SUN ZY, et al. Klf4 Promotes dentinogenesis and odontoblastic differentiation via modulation of TGF‐β signaling pathway and interaction with histone Acetylation. J Bone Miner Res. 2019;34(8):1502-1516 [58] LIU Z, CHEN T, BAI D, et al. Smad7 Regulates Dental Epithelial Proliferation during Tooth Development.J Dent Res. 2019;98(12):1376-1385. [59] XU M, HORRELL J, SNITOW M, et al. WNT10A mutation causes ectodermal dysplasia by impairing progenitor cell proliferation and KLF4-mediated differentiation. Nat Commun. 2017;8:15397. [60] YANG J, WANG SK, CHOI M, et al. Taurodontism, variations in tooth number, and misshapened crowns in Wnt10a null mice and human kindreds. Mol Genet Genomic Med. 2015;3(1):40-58. [61] YU M, LIU Y, LIU H, et al. Distinct impacts of bi-allelic WNT10A mutations on the permanent and primary dentitions in odonto-onycho-dermal dysplasia. Am J Med Genet A. 2019;179(1):57-64. [62] YU M, LIU Y, WANG Y, et al. Epithelial Wnt10a is essential for tooth root furcation morphogenesis.J Dent Res. 2020;99(3):311-319. [63] LU X , LIU SF, WANG HH, et al. A biological study of supernumerary teeth derived dental pulp stem cells based on RNA-seq analysisInt Endod J. 2019;52(6):819-828. [64] GU XG, LI MY, JIN Y, et al. Identification and integrated analysis of differentially expressed lncRNAs and circRNAs reveal the potential ceRNA networks during PDLSC osteogenic differentiation. BMC Genet. 2017;18(1):100. [65] HUANG YP, ZHANG YY, LI XB, et al. The long non-coding RNA landscape of periodontal ligament stem cells subjected to compressive force. Eur J Orthod. 2019;41(4):333-342. [66] KIM SJ, MOON SU, KANG SG, et al. Effects of low-level laser therapy after corticision on tooth movement and paradental remodeling.Lasers Surg Med. 2009;41(7):524-533. [67] KIM SJ, PARK YG, KANG SG. Effects of corticision on paradental remodeling in orthodontic tooth movement. Angle Orthod. 2009;79(2): 284-291. [68] ZHANG D, SUN B, ZHAO X, et al. Effect of corticision on orthodontic tooth movement in a rat model as assessed by RNA sequencing.J Mol Histol. 2017;48(3):199-208. [69] THALJI G, COOPER LF. Gene expression profiles of early implant adherent cells in smokers and non-smokers. J Oral Implantol. 2015; 41(6):640-645. [70] CHOA YD, KIMC PJ, KIM HG, et al. Transcriptome and methylome analysis of periodontitis and peri-implantitis with tobacco use. Gene. 2019;727: 144258. [71] CALCIOLARI E, DONOS N. The use of omics profiling to improve outcomes of bone regeneration and osseointegration. How far are we from personalized medicine in dentistry? J Proteomics. 2018;188:85-96. [72] WANG Z, GERSTEIN M, SNYDER M. RNA-Seq: a revolutionary tool for transcriptomics. Nat Rev Genet. 2009;10(1):57-63. |
| [1] | Zhang Mi, Wu Saixuan, Dong Ming, Lu Ying, Niu Weidong. Expression of interleukin-24 in a mouse model of periapical periodontitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 679-684. |
| [2] | Zhang Bin, Sun Lihua, Zhang Junhua, Liu Yusan, Cui Caiyun. A modified flap immediate implant is beneficial to soft tissue reconstruction in maxillary aesthetic area [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 707-712. |
| [3] | Zhang Guomei, Zhu Jun, Hu Yang, Jiao Hongwei. Stress of three-dimensional finite element models of E-MAX porcelain inlay [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 537-541. |
| [4] | Yang Junhui, Luo Jinli, Yuan Xiaoping. Effects of human growth hormone on proliferation and osteogenic differentiation of human periodontal ligament stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(25): 3956-3961. |
| [5] | Liu Jianyou, Jia Zhongwei, Niu Jiawei, Cao Xinjie, Zhang Dong, Wei Jie. A new method for measuring the anteversion angle of the femoral neck by constructing the three-dimensional digital model of the femur [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(24): 3779-3783. |
| [6] | Li Xinping, Cui Qiuju, Zeng Shuguang, Ran Gaoying, Zhang Zhaoqiang, Liu Xianwen, Fang Wei, Xu Shuaimei. Effect of modification of β-tricalcium phosphate/chitosan hydrogel on growth and mineralization of dental pulp stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3493-3499. |
| [7] | He Fan, Xiong Xiuli, Shan Xianfeng, Zhang Shutong, Hu Jian, Wang Xuejin. Guided bone regeneration in a small animal model of critical size craniofacial bone defects [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(20): 3226-3231. |
| [8] | Mu Yufeng, Wei Lina, Wu Yong, Shao Anliang, Chen Liang, Qu Shuxin, Xu Liming. Development and evaluation of alpha-galactosyl antigen-deficient rabbit model [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(2): 281-285. |
| [9] | Li Rong, Zuo Enjun. Gingival retraction: application profiles and hot spotlights [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(2): 322-328. |
| [10] | Liu Yan, Gao Xiang, Zhao Xiaoxia, Chen Qingyu, Gao Junwu. Effects of conditioned medium of human periodontal ligament stem cells on proliferation and osteogenic differentiation of inflammatory tissue-derived human periodontal ligament stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(13): 2005-2010. |
| [11] | Guan Weiwei, Gu Yu, Guan Xiaoyan, Wu Jiayuan, Bai Guohui, Tian Yuan, Liu Jianguo. Transgenic tomato vaccine expressing chimeric protein PAcA/CTB can immunize rats through gastrointestinal absorption [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(11): 1712-1716. |
| [12] | Ren Chunmei, Liu Yufang, Xu Nuo, Shao Miaomiao, He Jianya, Li Xiaojie. Non-coding RNAs in human dental pulp stem cells: regulations and mechanisms [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(7): 1130-1137. |
| [13] | Feng Xiaoxia, Hou Weiwei, Jin Xiaoting, Wang Xinhua. Construction of periodontal biomimetic membrane with electrospun poly(lactic-co-glycolic acid) nanofibers and electrosprayed chitosan microspheres [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(4): 511-516. |
| [14] | Zhang Suping, Sun Ling, Wan Dingming, Cao Weijie, Li Li, Liu Changfeng, Liu Yufeng, Wang Dao, Guo Rong, Jiang Zhongxing, Xie Xinsheng. Effectiveness of unrelated peripheral blood stem cell transplantation in the treatment of severe aplastic anemia [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(31): 4994-5001. |
| [15] |
Xiang Haidong, Cheng Dongmei, Guo Han, Gao Qi .
Changes in the proliferation and angiogenesis of human dental pulp stem cells after treated with prostaglandin E1 combined with basic fibroblast growth factor [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(25): 4006-4011. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||