Chinese Journal of Tissue Engineering Research ›› 2018, Vol. 22 ›› Issue (3): 456-463.doi: 10.3969/j.issn.2095-4344.0047
Previous Articles Next Articles
AxiaLif application in lumbosacral vertebral fusion
Shu Xiao-lin, Song Xi-zheng
- Department of Spine Surgery, First Affiliated Hospital, University of South China, Hengyang 421001, Hunan Province, China
-
Online:2018-01-28Published:2018-01-28 -
Contact:Song Xi-zheng, M.D., Chief physician, Associate professor, Department of Spine Surgery, First Affiliated Hospital, University of South China, Hengyang 421001, Hunan Province, China -
About author:Shu Xiao-lin, Studying for master’s degree, Department of Spine Surgery, First Affiliated Hospital, University of South China, Hengyang 421001, Hunan Province, China -
Supported by:the National Natural Science Foundation of China, No. 81272055
CLC Number:
Cite this article
Shu Xiao-lin, Song Xi-zheng. AxiaLif application in lumbosacral vertebral fusion[J]. Chinese Journal of Tissue Engineering Research, 2018, 22(3): 456-463.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
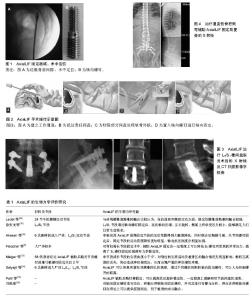
2.1 传统的腰骶椎融合手术方式及特点 2.1.1 腰椎前路椎间融合在腰骶椎融合术中的应用1933年Burns最早将腰椎前路椎间融合应用于临床对腰椎滑脱的治疗[12],1986年Crock等运用腰椎前路椎间融合的方法对盘源性腰痛治疗[13]。它经腹膜后入路的方法,通过各种分离方式,抵达主动脉分叉处即L5/S1椎间隙位置[14],直接彻底切除椎间盘,通过前路Cage植骨固定更好的恢复腰骶椎的矢状位平衡,恢复了椎间孔的高度,使受压的神经根得到充分减压,同时腰椎前路椎间融合也为脊柱前柱提供更好的力学稳定性,提高了植骨区的融合率[3-4,15]。但术中也存在一些问题,术中对髂血管、内脏神经、腹腔脏器、前纵韧带等损伤,术后出现腹胀、肠道瘘、逆行射精等并发症也不容忽视[16-17]。 2.1.2 腰椎后路椎间融合在腰骶椎融合术中的应用1953年CIoward[18]最早将腰椎后路椎间融合技术用于治疗椎间盘退变引起的下腰部疼痛,并取得良好的临床效果,奠定了该技术在临床应用的基础,在植骨区域可以完成360°植骨,后路重要的神经血管较前路少,在一定程度上降低了前路手术并发的大血管损伤、男性逆行射精的风险,使之在临床治疗中得到推广。但是该项技术在术中完成Cage置入时,对神经根及硬膜的牵拉较多、时间较长,从而也增加了神经损伤、脑脊液外漏、硬膜纤维化等风险[19]。而腰椎后路椎间融合置入椎间隙的Cage由于受到神经根和硬脊膜的限制,所以其体积较腰椎前路椎间融合的Cage小,可能会降低植骨区的关节融合率[20]。 2.1.3 椎间孔腰椎间融合在腰骶椎融合术中的应用1983年Harms介绍了椎间孔腰椎间融合技术,它主要是通过切除一侧关节突关节暴露椎间隙的后外侧,完成椎间盘切除及节段的植骨融合,最大程度减少了对神经根和硬膜的牵拉,减少了神经损伤、脑脊液外漏等风险。但植骨区的关节融合率较前路手术低。 2.1.4 极外侧入路椎间融合在腰骶椎融合术中的应用极外侧入路椎间融合于2001年Pimenta[21]首次报道在内镜下经极外侧入路腰椎间合术,是传统中的微创手术。但在L5/S1节段运用该技术时,由于双侧髂嵴的遮挡,故不能抵达责任节段进行手术操作,所以极外侧入路椎间融合技术只能使用L5/S1或L4/5以上节段进行操作。而主要的并发症是生殖股神经及腰丛等重要神经损伤。 2.1.5 腰椎斜向微创椎间融合和经椎间盘镜下腰椎间融合在腰骶椎融合术中的应用 2012年Silvestre等[22]提出了腰椎斜向微创椎间融合术式,它不经过腰大肌,而是通过血管和腰大肌之间的天然的解剖间隙,来完成椎间减压、植骨融合的手术操作。它与前路和后路手术方式相比,明显降低了对大血管、腹腔脏器、脊柱后柱等结构的破坏的风险。但也存在比较严重的并发症,据国外学者Kubota等[23]报道1例腰椎斜向微创椎间融合术后患者并发输尿管损伤,出现尿液外漏。予以经皮肾造瘘及广谱抗生素治疗,患者症状基本得到控制。输尿管损伤非常罕见,其损伤主要的原因是有限的手术操作视野,给术者暴露带来挑战;其次是解剖位置关系,输尿管位于腹膜后与腰大肌之间的狭小间隙中,且被脂肪组织包裹,前侧有较多的血管组织,其位置非常接近腹膜,由于其解剖位置的特殊性,故在操作时需细心,才能降低对其损伤的风险。随着脊柱内镜技术的发展,Yeung[24]提出了经椎间盘镜下腰椎间融合术式,是在脊柱内镜下辅助下进行椎间盘切除植骨术。该技术是在局麻下进行操作,可经皮侧方入路或者后方入路进行手术,切除责任节段的椎间盘后,处理相邻椎体的上下终板,放入Cage植骨融合,该手术对血管肌肉组织损伤小,减压彻底,为术后提供即可稳定性,一定程度上能够满足患者的需求。由于在内镜辅助下置入椎间的融合器较传统开放手术放置的Cage小,所以提供脊柱前柱的力学稳定性较传统的腰椎前路椎间融合、腰椎后路椎间融合术较差。由于视野较小,操作时对神经牵拉,术后神经水肿或神经损伤可能发生。在内镜下操作要熟悉脊柱侧方或后方解剖学结构,所以学习曲线较长,这对初学者是一大技术性挑战。 2.1.6 微创椎间孔入路减压植骨内固定术式 (minimally invasive transforaminal lumbarinterbody fusion,MIS-TLIF)在腰骶椎融合术中的应用 2003年Foley等[25]提出了MIS-TLIF,具有术中出血少、下地时间早、住院时间短、术后恢复快等优势,一般单侧进行该术式较常见,如责任节段双侧存在狭窄或突出,需进行减压时,该项技术本身难度较大、操作起来较困难,增加了工作量和时间。在双节段减压操作时,为了简化手术操作程序,在症状明显侧行MIS-TLIF,而在对侧经椎板入路行小开窗术。随着脊柱微创技术的发展,有学者行单侧MIS-TLIF手术,采用单侧固定的方法治疗单侧神经根症状为主的腰椎退行性疾病[26]。据Chen等[27]报道单侧椎弓根钉与单Cage联合固定同样具有相似的生物力学稳定性。Suk等[28]认为单边固定的生物力学研究显示,单侧椎弓根螺钉仅能提供双侧椎弓根螺钉一半的力学强度,并存在明显的轴向旋转活动,在加压时可能造成双侧不平衡而出现侧凸的可能。因此MIS-TILF术式在临床应用方面也存在一些限制,有待进一步探索。 综上所述,传统的腰椎前路椎间融合、腰椎后路椎间融合开放手术及极外侧入路椎间融合、椎间孔腰椎间融合、MIS-TILF、腰椎斜向微创椎间融合、经椎间盘镜下腰椎间融合微创手术,虽然对责任节段减压彻底,但由于传统的开放手术切口较大、对肌肉、神经、血管等重要的解剖结构损伤较多,同时对软组织的持续牵拉,造成软组织缺血、挛缩等伴随的并发症影响术后的愈合,而近年来形成的脊柱微创手术虽然对脊柱正常组织损伤较小,术后恢复较快,但由于其力学稳定性较传统的开放手术稍差、学习曲线较长,这无疑对许多刚入门医生是一项技术性挑战。所以为了减少传统手术对机体的损伤,提高术后的恢复水平,需对腰骶椎融合手术需进一步探索和不断改良。 2.2 AxiaLIF在腰骶椎融合术中的应用 2004年Cragg[5]创造性的提出AxiaLIF,其在尾骨右侧旁切开2-4 cm手术切口,通过钝性分离进入骶骨前直肠后的间隙,在C臂机透视之下,沿脊柱纵轴方向建立S1、L5骨性通道,完成L5/S1椎间盘切除与植骨固定,见图1。这一术式创造性解决了不损伤脊柱前方、后方、侧方重要结构这一难题,也不进入腹腔脏器,同时也保留了前后纵韧带、纤维环等关键的解剖学结构,避免了肌肉、神经及血管等软组织由于长时间或过度牵拉造成不可逆性缺血、挛缩、神经功能减退等问题,为患者术后病情良好恢复打下坚实基础。AaxiLIF可以单独使用也可以联合其他微创及开放手术联合使用[10-11]。真正达到微创的目的,是一种可选择的替代的融合固定手术。 AxiaLIF的生物力学评价:AxiaLIF经骶骨前直肠后间隙,轴向融合腰骶椎,手术方式新颖、微创,受到广泛脊柱外科医生们的青睐。据此,国内外学者对该项技术进行生物力学研究,见表1。Ledet等[29]对24节牛的腰椎运动节段进行生物力学分析,与传统腰椎前路椎间融合比较认为,在抗前屈和侧屈运动方面,稳定性腰椎前路椎间融合较强。AxiaLIF在抗旋转稳定性较钉棒固定系统稍差。国内学者对AxiaLIF进行有限元分析,L5/S1节段通过轴向螺钉固定后,在抗轴向压缩、左右旋转、侧屈上所承受压力较小,能够满足人们日常生活需 求[30]。Erakn等[31]对6具成人尸体L4-S1运动节段进行AxiaLIF的生物力学分析,得知在L4、L5节段上,在抗轴向旋转、屈伸稳定性方面,与辅助后路关节突螺钉及椎弓根螺钉无明显差异,效果相当,在抗侧屈运动稳定性较辅助后路钉棒固定稍差。而在L5、S1节段上,抗轴向旋转和侧屈运动上,AxiaLIF和辅助后路钉棒固定效果不相上下,但是在抗前后屈伸方面上,单纯AxiaLIF的力学稳定性较联合使用后路双侧关节突螺钉或双侧椎弓根螺钉薄弱。Akesen等[32]用6具新鲜的成人尸体,对L5/S1运动节段进行AxiaLIF的生物力学分析,AxiaLIF技术保护了脊柱周围的重要的组织结构,得出结论,单独应用AxiaLIF使得固定节段的运动范围得到大幅度降低,同时联合后路椎弓根、关节突螺钉固定后,固定节段的运动范围降低更加明显,轴向抗压刚度亦明显加强,特别是前屈、后伸、侧弯方面的运动范围较小最为明显,很大程度上提高植区的融合成功率。Fiescher 等[8]用人尸体标本分别对单纯后路椎弓根螺钉固定组、前路植骨联合后路椎弓根螺钉固定组、髂骨螺钉联合椎弓根螺钉固定组、AxiaLIF的轴向螺钉联合椎弓根螺钉固定组中对S1螺钉所受的应力进行生物力学研究,研究结果示在AxiaLIF的轴向螺钉联合椎弓根螺钉固定组中,固定节段的运动所受到的限制强度最大,同时在该组实验中,对S1螺钉进行力学测试,S1螺钉所受到的张力最小,因此对脊柱需长节段固定术中,辅助AxiaLIF固定,在一定程度上可以降低S1螺钉所受到的异常应力,提高了S1螺钉固定的强度和力学稳定性。脊柱的正常的生理曲度对维持脊柱的正常活动及生物力学具有重要作用。有学者对58例患者经过AxiaLIF辅助后路关节突螺钉或椎弓根螺钉固定术后2年[33],进行回顾性分析得知,58例患者术后脊柱的单节段或长节段的生理曲度增加或丢失都小于5°,并且在植骨区域获得成功融合。并得出结论,单节段或长节段的生理曲度小于5°,对脊柱的生理活动及植骨区的融合情况无明显影响。椎间孔高度的丢失,势必造成神经根受压,从而出现严重的神经根性疼痛。Marawar等[34]用6具新鲜的成人尸体对其L4/L5、L5/S1节段进行AxiaLIF固定后,分别测量了L4/L5、L5/S1双侧椎间孔的高度。测试结果表明,经轴向螺钉固定后,L4/L5双侧椎间孔的高度较术前增加了12%,L5/S1双侧椎间孔的高度较处理前增加了17%,AxiaLIF可以恢复和增加双侧椎间孔的高度,通过不同螺纹间距的轴向固定螺钉,可以人为控制撑开的距离,在尸体标本研究中,每旋转一圈螺钉,平均撑开2 mm,二至三圈可以撑开到最大高度。Patil等[35]研究表明,AxiaLIF辅助后路钉棒固定,可以提高其抗旋转稳定性,在维持正常的椎间隙高度方面亦发挥重要作用,一定程度上缓解相邻节段间盘的退变。国内学者研究并验证AxiaLIF联合后路椎弓根螺钉固定,稳定性更好,并提高植骨融合率[10]。由于单纯应用AxiaLIF效果欠佳,通常需联合后路钉棒固定,操作较繁琐,2017年国内学者刘栋梁[36]对轴向固定螺钉进行改良,研制出带刺轴向固定螺钉,并对其进行有限元分析,得出该带刺轴向螺钉在理论上可以提供坚强固定,利于植骨的成功融合,并能够满足人体各方面的生理需求。 2.3 AxiaLIF的手术操作 患者术前24 h进行清洁灌肠,在连续硬膜外麻醉后,患者取俯卧位,气垫垫高腹部,常规消毒铺巾。在尾骨尖旁右侧约1 cm处,做一1.5 cm长横行手术切口,逐层切开皮肤,手指钝性分离皮下脂肪、韧带等软组织,然后进入骶骨前直肠后间隙。用不同直径的钝性套头插入切口内,用C型臂反复进行正侧位的透视,确保钝头分离器贴紧骶骨腹面向头端缓慢轻移。当分离器到达S1、S2连接部的椎体腹侧前缘时,通过钝头分离器套筒插入导针并捶入骶骨,再沿导针依次用6,8,10 mm扩张套管扩张骶骨前软组织,最后将 10 mm扩张器与套管一起置入并捶入骶骨中。建立了一个10 mm的骨性工作通道。然后将9 mm骨钻沿工作通道进入S1椎体,到达L5/S1椎间隙后退出骨钻置入旋转刀头至L5/S1间隙,在透视下刮除髓核及上下软骨终板,刮除完毕后利用特制的刷形收集器,将椎间盘及软骨终板碎片取出。椎间盘处理完毕后,利用特殊的植骨器将植骨材料置入到L5/S1间隙内,再用7.5 mm骨钻在透视下钻入L5椎体至L5上终板下缘,约椎体2/3高度处,经工作通道再次放入导针,取出套管。换上另一个专用于放置轴向融合器的套管,经工作通道沿导针置入合适长度的轴向融合器,L5/S1椎间隙被撑开,高度恢复。如果是行L4-S1双节段固定,需要2枚轴向融合器,用同样的方法处理L4/L5椎间盘和钻入L4椎体,此时须先沿导针拧入L4、L5的轴向融合器,直至轴向融合器近端接近L5下终板,再拧入L5、S1的轴向融合器,并与L4、L5的轴向融合器在L5/S1椎间隙对接。完成后退出工作套管与导向器,缝合皮肤切口,放置引流管。如需要增强抗旋转稳定性的话,可予以后路经双侧椎弓根螺钉或关节突螺钉固定。手术操作示意图见图2。 2.4 AxiaLIF在腰椎间盘退变性疾病中的临床应用 2.4.1 AxiaLIF在腰椎间盘突出、腰椎滑脱中的临床应用 近年来,微创脊柱外科迅猛发展,对传统的脊柱融合手术理念提出新的挑战,AxiaLIF技术在脊柱外科微创领域掀起研究热潮,临床应用地位显著提高。国外学者研究表明,AxiaLIF已经成功运用到治疗腰椎间盘退变性疾病及腰椎滑脱(Ⅱ度以下)方面,并取得非常好的融合固定临床疗效[7]。Aryan等[7]对35例患者因腰椎间盘退变、腰椎滑脱、峡部裂性滑脱引起的腰背部及下肢放射疼痛,用AxiaLIF技术进行手术治疗,其中有23例患者辅助后路双侧椎弓根螺钉固定。在术后平均17.5个月随访中,32(91%)例术后患者行影像学检查表明在手术节段(L5/S1)植骨区已完全成功融合。Tobler等[37]对26例腰椎间盘退变性疾病患者进行术后2年的前瞻性研究,所有患者都进行AxiaLIF辅助后路双侧椎弓根螺钉固定。其中1个节段(L5/S1)的手术有17例,2个节段(L4-S1)9例,在术后1年的随访结果中有22例患者已经成功融合,2年的随访中,达到23例患者手术节段已完全融合。其中1例患者并发假性关节形成,并未引起明显的临床症状,术后经过后外侧植骨融合翻修,已完全融合。Tobler等[38]对156例腰椎间盘退变疾病患者的L5/S1节段经过AxiaLIF术后2年进行回顾性分析,术后下腰部疼痛目测类比评分、ODI较术前明显改善,影像学研究表明94%的患者获得成功融合。国内学者宋西正等[10]运用AxiaLIF联合脊柱内镜对腰椎间盘突出患者进行手术治疗,术中出血平均80 mL,手术时间平均130 min,术后下腰部及双下肢疼痛较术前明显减轻,术后6个月随访,融合率84.4%,而12个月后融合率为100%。Gerszten等[39]对26例腰椎滑脱(Ⅱ度以下)的患者采用AxiaLIF辅助后路双侧椎弓根螺钉固定方法进行临床疗效研究,近50%的患者的到良好复位效果,术后予以佩戴脊柱支具1个月,增加制动效果。所有患者的轴向疼痛较术前降低66%,在2年的随访中,所有患者都得到完全融合。因此,AxiaLIF不仅在腰椎间盘退变性突出疾病中具有微创、融合率高的临床效果,在治疗退变性腰椎滑脱方面也具有一定的优势,见图3。 2.4.2 AxiaLIF在脊柱长节段固定中的临床应用 在脊柱畸形治疗中,通常需进行矫形手术来治疗,而矫形手术固定节段较长,大部分的固定延长至L5-S1节段,在长节段的钉棒固定之下,使的腰骶部生物力学环境发生改变,在异常应力的刺激之下,加剧了L5/S1椎间盘退变的速度。随之带来的L5/S1节段的腰椎间盘退变性疾病、腰椎滑脱、远端固定螺钉松动等并发症也越来越明显。为了降低L5/S1节段退变的风险,通常需对该节段进行辅助融合手术。Anand等[40]对28例退变性脊柱侧患者进行回顾性研究,在长节段固定辅助AxiaLIF后使得融合节段平面增加,一般可以增加二至三个节段。在后来22个月随访中,所有固定节段得到完全骨性融合,且未发生严重的并发症。Issack等[41]对9例成年脊柱侧弯患者进行随访,联合AxiaLIF术的患者融合节段从T10椎体平面增加到T3椎体水平,与单独长节段相比,明显增加了融合平面。有学者对58例患者经过AxiaLIF辅助后路关节突螺钉或椎弓根螺钉固定术后2年,进行回顾性分析得知,58例患者术后脊柱的单节段或长节段的生理曲度增加或丢失都小于5°,并且在植骨区域获得成功融合。在缓解S1螺钉张力、保护S1螺钉稳定性方面具有重要作 用[33]。总之,AxiaLIF在长节段辅助固定方面是可行、安全的,可获得满意的临床效果,见图4。 2.5 AxiaLIF的并发症及预防措施 每一种手术方式都有其优缺点,因此其带来的并发症也是客观存在的。常见的并发症有直肠损伤、骶骨前血肿、直肠瘘、内置物下沉、假关节炎形成、骶骨骨折、髂血管损伤、浅表感染、盆腔感染、败血症等,而最常见的主要是直肠损伤和直肠瘘。Botolin等[42]报道1例AxiaLIF术后出现高位直肠损伤,术后行骨盆CT检查被证实,予以广谱抗生素治疗,病情得到控制。Mazur等[43]报道1例患者在行AxiaLIF术后并发直肠瘘,为了控制病情进一步发展,他们对该患者进行直肠造瘘术同时进行广谱抗感染治疗,病情逐渐好转,直至完全恢复。因此,为了尽量降低直肠损伤,术前应该仔细询问病史,是否有大肠手术史、盆腔手术史,术前应该充分完善骨盆、下腹部相关影像学检查等,如存在盆腔炎症、盆腔手术史、盆腔组织粘连等应视为该手术禁忌证。AxiaLIF术后假性关节炎形成也是备受关注的焦点,通常以L4/5、L5/S1双节段融合后多见。Issack等[41]对L4/L5、L5/S1双节段融合术后的患者进行回顾性分析,发现假关节炎形成的概率较单节段术后的概率高。因此他们建议在操作过程中适当切除髓核及对椎体终板处理是非常重要的,它可以增加融合率,减少假关节炎的形成。Hofsetter等[44]对38例AxiaLIF术后26个月进行随访,部分患者由于轴向螺钉的下沉,导致腰椎单节段的生理曲度丢失。其中5例术后患者进行二次翻修手术治疗。因此他们建议再完成AxiaLIF术后辅助后路钉棒固定,可以明显降低轴向螺钉下沉的概率。Marchi等[45]对27例患者进行术后2年的随访,主要并发症包括轴向螺钉断裂(15%)、螺钉远近端分离(11%)、轴向螺钉穿透上终板(24%)。Patil等[35]对68例患者术后进行系统性回顾性分析,得知2例患者并发直肠穿孔、6例患者出现假关节、4例患者出现浅表感染、2例盆腔血肿形成、2例骶骨骨折。他们发现针对浅表感染,可通过广谱抗生素得到控制,同时骶尾部作横形切口比纵型切口能够更好降低感染风险。为了预防术后骨盆血肿形成,术前应常规行盆腔MRI检查,评估直肠后方与骶骨前间隙之间的组织厚度,如置钉通道存在广泛的血管等软组织,应视为AxiaLIF术的禁忌证。如术后盆腔血肿已形成,血肿体积不大,可自行吸收,如体积较大或存在继发性出血,仍需行手术干预。另外,选择适当的置钉骨性通道是预防骶骨骨折的关键,置钉位置太靠前,容易造成椎体前缘骨皮质骨折,置钉位置过的靠后,容易造成神经根损伤,所以置钉位置的选择也是手术时考虑的重点。"
| [1] Gerszten PC, Tobler WD, Nasca RJ. Retrospective analysis of L5-S1 axial lumbar interbody fusion (AxiaLIF): a comparison with and without the use of recombinant human bone morphogenetic protein-2. Spine J. 2011;11:1027-1032.[2] Vibert BT, Sliva CD, Herkowitz HN. Treatment of instability and spondylolisthesis: surgical versus nonsurgical treatment. Clin Orthop Relat Res. 2006;443:222-227.[3] Chen D, Fay LA, Lok J, et al. Increasing neuroforaminal volume by anterior interbody distraction in degenerative lumbar spine. Spine (Phila Pa 1976). 1995;20:74-79.[4] Vamvanij V, Ferrara LA, Hai Y, et al. Quantitative changes in spinal canal dimensions using interbody distraction for spondylolisthesis. Spine (Phila Pa 1976). 2001;26:E13-E18.[5] Cragg A,Carl A,Casteneda F. New percutaneous access method for minimally invasive anterior lumbosacral surgery.J Spinal Disord Tech. 2004;17(1): 21-28.[6] Marotta N, Cosar M, Pimenta L, et al. A novel minimally invasiveresacral approach and instrumentation technique for anterior L5-S1,intervertehral discectomy and fusion. Neurosurg Focus. 2006;20(1):E9.[7] Aryan HE, Newman CB, Gold JJ, et al. Percutaneous axial lumbar interbody fusion (AxiaLIF) of the L5-S1 segment: initial clinical and radiographic experience. Minim Invasive Neurosurg. 2008;51(4):225-230.[8] Fleischer GD, Kim YJ, Ferrara LA, et al. Biomechanical analysis ofsacral screw strain and range of motion in long posterior spinal fixation constructs:effects of lumbosacral fixation strategies in reducing sacral screw strains. Spine. 2012;37(3): 163-169.[9] 戎利民,董健文,刘斌,等. 轴向椎体间融合术微创治疗腰骶椎失稳症[J]. 中华显微外科杂志,2009,32(1):15-18.[10] 宋西正,王文军,薛静波,等. 经骶前间隙轴向椎间融合联合内窥镜下后入路椎间盘摘除治疗腰骶椎退行性疾病[J]. 中国脊柱脊髓杂志,2013,23(9):778-782.[11] 宋西正. 经骶前间隙轴向椎间融合术联合显微内窥镜下后入路椎间盘摘除治疗腰骶椎退行性疾病[A]. 中国中西医结合学会脊柱医学专业委员会、《中国骨伤》杂志.中国中西医结合学会脊柱医学专业委员会第五届学术年会暨第二届专业委员会换届选举会议论文集[C].中国中西医结合学会脊柱医学专业委员会、《中国骨伤》杂志,2012.[12] Burns BH. An operation for spondylolisthesis.Lancet. 1933;1: 1233.[13] Vamvanij V, Ferrara LA, Hai Y, et al. Quantitative changes in spinal canal dimensions using interbody distraction for spondylolisthesis. Spine (Phila Pa 1976). 2001;26: E13-E18.[14] Fantini GA, Pappou IP, Girardi FP, et al. Major vascular injury during anterior lumbar spinal surgery: incidence, risk factors, and management. Spine (Phila Pa1976). 2007;32: 2751-2758.[15] Hsieh PC, Koski TR, O’Shaughnessy BA, et al. Anterior lumbar interbody fusion in comparison with transforaminal lumbar interbody fusion: implications for the restoration of foraminal height, local disc angle, lumbar lordosis, and sagittal balance. J Neurosurg Spine. 2007;7:379-386.[16] Fantini GA, Pappou IP, Girardi FP, et al. Major vascular injury during anterior lumbar spinal surgery: incidence, risk factors, and management. Spine (Phila Pa 1976). 2007;32: 2751-2758.[17] Sasso RC, Kenneth Burkus J, LeHuec JC. Retrograde ejaculation after anterior lumbar interbody fusion: transperitoneal versus retroperitoneal exposure. Spine (Phila Pa 1976). 2003;28: 1023-1026.[18] Cloward RB.The treatment of ruptured lumbar intervertebral discs by vertebral body fusion: indications, operative technique, after care. J Neurosurg. 1953;10:154-168.[19] Jutte PC, Castelein RM. Complications of pedicle screws in lumbar and lumbosacral fusions in 105 consecutive primary operations. Eur Spine J. 2002;11(6):594-598.[20] DiPaola CP, Molinari RW. Posterior lumbar interbody fusion. J Am Acad Orthop Surg. 2008;16:130-139.[21] Pimenta L. Lateral endoscopic transpsoas retroperitoneal approach for lumbar spine surgery. VIII Brazilian Spine Society Meeting.[22] Silvestre C, Mac-Thiong JM, Hilmi R, et al. Complications and morbidities of mini-open anterior retroperitoneal lumbar interbody fusion: oblique lumbar interbody fusion in 179 patients. Asian Spine J. 2012; 6(2): 89-97.[23] Kubota G, Orita S, Umimura T, et al. Insidious intraoperative ureteral injury as a complication in oblique lumbar interbody fusion surgery: a case report. BMC Res Notes. 2017;10:193.[24] Yeung AT. The evolution of percutaneous spinal endoscopy and discectomy: state of the art.Mt Sinai J Med. 2000;67: 327-332.[25] Foley KT, Holly LT, Schwender JD. Minimally invasive lumbar fusion. Spine. 2003;28(15S):S26-S35.[26] Xue H, Tu Y, Cai M. Comparison of unilateral versus bilateral instrumented transforaminal lumbar interbody fusion in degenerative lumbar diseases. The Spine J. 2012;12(3): 209-215.[27] Chen HH, Cheung HH, Wang WK, et al. Biomechanical analysis of unilateral fixation with interbody cages. Spine. 2005;30(4): E92-E96. [28] Suk KS, Lee HM, Kim NH, et al. Unilateral versus bilateral pedicle screw fixation in lumbar spinal fusion. Spine. 2000;25(14): 1843-1847.[29] Ledet EH, Tymeson MP, Salerno S, et al. Biomechanical evaluation of a novel lumbosacral axial fixation device. J Biomech Eng. 2005;127(6): 929-933.[30] 徐宏光,杨晓明,吴天亮,等.经皮前路腰骶融合螺钉的有限元分析[J].中华医学杂志, 2010, 90(3): 153-156.[31] Erkan S, Wu C, Mehbod AA, et al. Biomechanical evaluation of a new AxiaLIF technique for two-level lumbar fusion. Eur Spine J.2009;18(6):807-814.[32] Akesen B, Wu C, Mehbod AA, et al. Biomechanical evaluation of paracoccygealtranssacral fixation. J Spinal Disord Tech. 2008;21(1):39-44.[33] 戎利民,董健文,刘斌,等. 轴向椎体间融合术微创治疗腰骶椎失稳症[J]. 中华显微外科杂志, 2009, 32(1): 15-18.[34] Marawar S, Ordway N, Jung J, et al. Changes in neuroforaminal height with 2 level axial presacral lumbar interbody fusion at L4-S1. J Spine Surg. 2014.[35] Patil SS, Lindley EM, Patel VV, et al. Clinical and radiological outcomes of axial lumbar interbody fusion. Orthopedics. 2010;33(12):883.[36] 刘栋梁.腰骶椎带刺内锁轴向融合内固定的有限元分析[D].南华大学,2017.[37] Tobler WD, Ferrara LA. The presacral retroperitoneal approach for axial lumbar interbody fusion: a prospective study of clinical outcomes, complications and fusion rates at a follow-up of two years in 26 patients. J Bone Joint Surg Br. 2011; 93: 955-960.[38] Tobler WD, Gerszten PC, Bradley WD, et al. Minimally invasive axial presacral L5-S1 interbody fusion: two-year clinical and radiographic outcomes. Spine (Phila Pa 1976). 2011;36:E1296-E1301.[39] Gerszten PC, Tobler W, Raley TJ, et al. Axial presacral lumbar interbody fusion and percutaneous posterior fixation for stabilization of lumbosacral isthmic spondylolisthesis. J Spinal Disord Tech. 2012;25:E36-E40.[40] Anand N, Baron EM, Thaiyananthan G, et al. Minimally invasive multilevel percutaneous correction and fusion for adult lumbar degenerative scoliosis: a technique and feasibility study. J Spinal Disord Tech. 2008;21:459-467.[41] Issack PS, Boachie-Adjei O. Axial lumbosacral interbody fusion appears safe as a method to obtain lumbosacral arthrodesis distal to long fusion constructs. HSS J. 2012;8: 116-121.[42] Botolin S, Agudelo J, Dwyer A, et al. High rectal injury during trans-1 axial lumbar interbody fusion L5-S1 fixation: a case report. Spine (Phila Pa 1976). 2010;35:E144-E148.[43] Mazur MD, Duhon BS, Schmidt MH, et al. Rectal perforation after AxiaLIF instrumentation: case report and review of the literature. Spine J. 2013;13:e29-e34.[44] Hofstetter CP, Shin B, Tsiouris AJ, et al. Radiographic and clinical outcome after 1- and 2-level transsacral axial interbody fusion. Clinical article. J Neurosurg Spine. 2013;19: 454-463.[45] Marchi L, Oliveira L, Coutinho E, et al. Results and complications after 2-level axial lumbar interbody fusion with a minimum 2-year follow-up. Clinical article. J Neurosurg Spine. 2012;17:187-192.[46] 邱贵兴. 以人为本,发展骨科[J]. 中华外科杂志, 2009, 47(1): 4-6. |
| [1] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [2] | Yao Rubin, Wang Shiyong, Yang Kaishun. Minimally invasive transforaminal lumbar interbody fusion for treatment of single-segment lumbar spinal stenosis improves lumbar-pelvic balance [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1387-1392. |
| [3] | Zeng Yanhua, Hao Yanlei. In vitro culture and purification of Schwann cells: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1135-1141. |
| [4] | Zhang Lei, Ma Li, Fu Shijie, Zhou Xin, Yu Lin, Guo Xiaoguang. Arthroscopic treatment of greater tuberosity avulsion fractures with anterior shoulder dislocation using the double-row suture anchor technique [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(6): 895-900. |
| [5] | Song Chengjie, Chang Hengrui, Shi Mingxin, Meng Xianzhong. Research progress in biomechanical stability of lateral lumbar interbody fusion [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(6): 923-928. |
| [6] | Kong Lingbao, Lü Xin. Effect of implant selection and approach on support in the operation of posterolateral tibial plateau fractures [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(6): 942-947. |
| [7] | Xu Dongzi, Zhang Ting, Ouyang Zhaolian. The global competitive situation of cardiac tissue engineering based on patent analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 807-812. |
| [8] | Wu Zijian, Hu Zhaoduan, Xie Youqiong, Wang Feng, Li Jia, Li Bocun, Cai Guowei, Peng Rui. Three-dimensional printing technology and bone tissue engineering research: literature metrology and visual analysis of research hotspots [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 564-569. |
| [9] | Chang Wenliao, Zhao Jie, Sun Xiaoliang, Wang Kun, Wu Guofeng, Zhou Jian, Li Shuxiang, Sun Han. Material selection, theoretical design and biomimetic function of artificial periosteum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 600-606. |
| [10] | Liu Fei, Cui Yutao, Liu He. Advantages and problems of local antibiotic delivery system in the treatment of osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 614-620. |
| [11] | Li Xiaozhuang, Duan Hao, Wang Weizhou, Tang Zhihong, Wang Yanghao, He Fei. Application of bone tissue engineering materials in the treatment of bone defect diseases in vivo [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 626-631. |
| [12] | Zhang Zhenkun, Li Zhe, Li Ya, Wang Yingying, Wang Yaping, Zhou Xinkui, Ma Shanshan, Guan Fangxia. Application of alginate based hydrogels/dressings in wound healing: sustained, dynamic and sequential release [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 638-643. |
| [13] | Chen Jiana, Qiu Yanling, Nie Minhai, Liu Xuqian. Tissue engineering scaffolds in repairing oral and maxillofacial soft tissue defects [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 644-650. |
| [14] | Song Kaikai, Zhang Kai, Jia Long. Microenvironment and repair methods of peripheral nervous system injury [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 651-656. |
| [15] | Liang Yan, Zhao Yongfei, Zhu Zhenqi, Liu Haiying, Mao Keya. Minimally invasive transforaminal lumbar interbody fusion in the treatment of sciatic scoliosis caused by lumbar disc herniation: a 2-year follow-up of coronal and sagittal balance [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 409-413. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||