Chinese Journal of Tissue Engineering Research ›› 2013, Vol. 17 ›› Issue (8): 1513-1520.doi: 10.3969/j.issn.2095-4344.2013.08.029
Synthetic dressing for the treatment of skin Ⅱ degree burns
Wang Qing-hua, Su Qiu-mei
- Second District of Department of General Surgery, Hainan General Hospital, Haikou 570311, Hainan Province, China
-
Received:2012-08-17Revised:2013-01-31Online:2013-02-19Published:2013-03-23 -
About author:Wang Qing-hua, Associate chief nurse, Second District of Department of General Surgery, Hainan General Hospital, Haikou 570311, Hainan Province, China wangqinghua.1974@yahoo.com.cn
CLC Number:
Cite this article
Wang Qing-hua, Su Qiu-mei. Synthetic dressing for the treatment of skin Ⅱ degree burns[J]. Chinese Journal of Tissue Engineering Research, 2013, 17(8): 1513-1520.
share this article
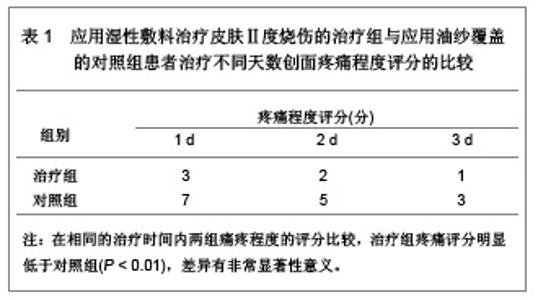
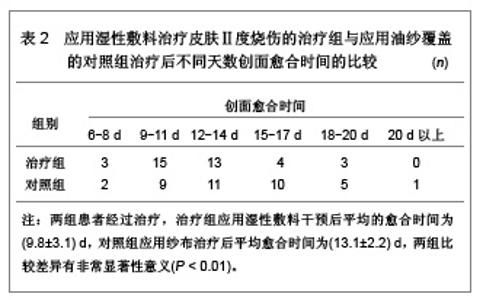
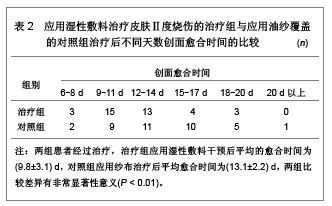
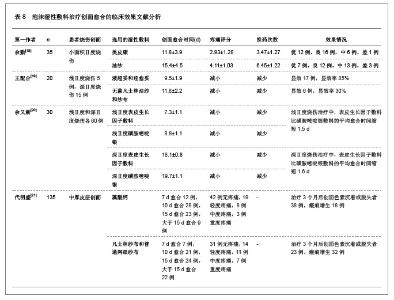
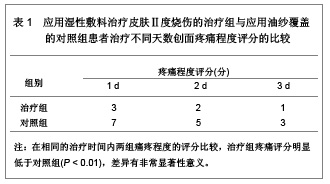
1 湿性敷料治疗皮肤Ⅱ度烧伤的病例分析 对象:选择海南省人民医院门诊接受治疗的38例皮肤Ⅱ度烧伤患者,男18例,女20例,年龄5-53岁,平均年龄39.5岁。其中合并糖尿病的患者有3例,创面部分有深Ⅱ度烧伤患者5例,最小创面约4 cm×3 cm,最大创面约25 cm×18 cm。为了使创面统一标准、可比性强,所有患者设自身对照法,即所选患者均有2处以上伤口,一处伤口标记作为治疗组,另一处伤口标记作为对照组,两组伤口面积和深度大致相等。 治疗方法:研究中湿性敷料选用瑞典墨尼克公司提供的银离子湿性敷料。治疗组处理:用生理盐水清洁创面后,剪去破损的游离表皮,直接在皮肤破损处覆盖湿性敷料,外加绷带或宽胶布固定。第3天打开创面,抽出直径>2 cm的水泡,并剪去浮松的表皮,继续给予湿性敷料覆盖包扎。对照组处理:用生理盐水清洁创面后外覆Ⅲ型安尔碘纱布,两三天抽出直径>2 cm的水泡,覆盖凡士林油纱,外加无菌纱布包扎。 观察指标:①在烧伤治疗后第6天开始观察创面愈合情况,1次/d,其中创面的愈合标准是出现上皮化,观察两组处理后的创面愈合时间[2]。②根据目测类比评分法作为疼痛的评分标准:0分为无痛;1-3分患者有较微的疼痛,患者能忍受;4-6分患者疼痛并影响睡眠,尚能忍受;7-10分患者有渐强烈的疼痛,难于忍受。观察两组方法处理后,不同时间创面的疼痛程度,并给予评分,比较两种治疗方法对创面疼痛的影响。 统计学分析:所有数据采用SPSS 10.0统计学软件进行分析,计量数据以x(_)±s表示,采用t 检验,P < 0.05为差异有显著性意义;P < 0.01为差异有非常显著性意义。 治疗结果评价:治疗和对照创面治疗后疼痛程度评分的比较,见表1。治疗和对照治疗后不同天数创面愈合患者数的比较,见表2。"

2 湿性敷料的种类以及促进烧伤创面愈合的机制 2.1 湿性敷料的种类 湿性敷料按照材料的不同可以分为几种[3]:①水凝胶类湿性敷料。可以水化伤口、软化痂皮、自溶清创。②藻酸盐类湿性敷料:吸收大量渗液,轻微止血消炎。③银离子类湿性敷料:具有杀菌抗感染、吸收渗液的作用。④泡沫类湿性敷料:阻止肉芽过度生长,促进上皮化。⑤水胶体类湿性敷料:可以调理伤口,刺激肉芽组织的生长。⑥美盐湿性敷料:能吸收大量渗液,消炎消肿,还具有抑菌、杀菌和洁净伤口的作用。 2.2 湿性敷料的临床应用指征 湿性敷料的临床应用指征包括以下几种:①创面有黑痂时可以选水凝胶类湿性敷料,起到保湿作用。②创面有腐肉时,可以选水凝胶敷料+美盐敷料。③创面有腐肉并伴有感染时,可以选银离子类湿性敷料。④创面有腔洞伴大量渗液时,可以选用美盐、藻酸盐、亲水纤维或银离子类湿性敷料。⑤创面有肉芽全层伤口时,可以选水凝胶类湿性敷料填充或者用美盐敷料。⑥创面有肉芽水肿时,可以选用美盐湿性敷料。⑦创面有肉芽过长时,可以选用银离子或泡沫类湿性敷料。 2.3 湿性敷料促进烧伤创面愈合的理论基础 湿性敷料促进烧伤创面愈合的理论基础有伤口湿性环境愈合理论、渗液滋养理论、自溶清创理论、微创或无创理论以及减少瘢痕形成理论[4]。 伤口湿性环境愈合理论:伤口湿性环境即适度湿润、低氧或无氧环境以及微酸环境和自溶清创的愈合环境下,对创面的愈合有促进作用。适度湿润环境可以促进生长因子释放,刺激细胞增殖,促进生长因子受体与生长因子结合,促进免疫细胞活性及其功能增强,加快表皮细胞迁移的速度。低氧或无氧环境可以刺激巨噬细胞释放生长因子,氧梯度刺激毛细胞血管生长,并且在低氧状态时,成纤维细胞的生长最为理想。皮肤是弱酸性,是理想的伤口愈合环境,封闭的伤口环境呈弱酸性,即pH值在6.4±0.5,开放伤口的pH值大于7.1,胶原是基本的构建蛋白,是肉芽组织的主要成分,成纤维细胞需要在酸性环境中才能产生胶原。 渗液滋养理论:在封闭的伤口渗液中富含电介质、营养物质、炎症介质、白细胞、蛋白消化酶和生长因子等,可以防止伤口干燥。渗液在愈合的伤口中还可以刺激细胞增殖、蛋白消化酶以非活性形式出现,在愈合不良的伤口中,渗液作用相反,含有大量炎症递质和活性蛋白消化酶。渗液还可以帮助组织修复细胞移动,提供细胞代谢所需的营养,协助生长因子和免疫因子扩散,帮助分解坏死或受损组织。在未感染的伤口渗透液能促进成纤维细胞、内皮细胞、角质细胞的生长,除渗透液过多或者感染需要清除外,否则均给予妥善的处理。以往的观点认为所有渗液都是无用的,渗液的增多是由于细菌量增加或明显感染造成的,用过的敷料毫无作用,需要更多的敷料来处理渗液,这些都是错误的。 自溶清创理论:应用湿性敷料水化伤口,软化坏死的痂皮,渗液中含有吞噬细胞及嗜中性粒细胞产生的溶解素能溶解坏死组织,伤口内自身酶也使失活组织液化,每次更换敷料去除坏死组织,保持伤口洁净,此过程称为自溶性清创。"


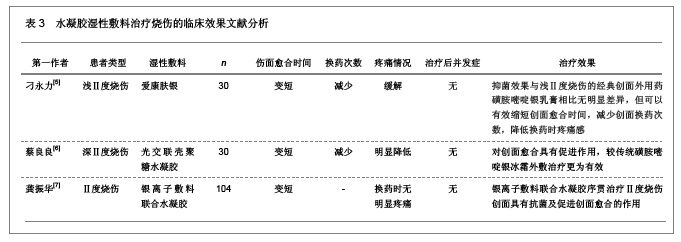
3 临床应用不同湿性敷料治疗烧伤创面的效果及特点 3.1 应用水凝胶湿性敷料的特点及治疗烧伤的效果 水凝胶类湿性敷料是在可以渗透的材料上使用水凝胶,水凝胶是一种含有大量水分的亲水性网状高子溶胀体,引入一部分疏水基团和亲水残基,亲水残基与水分子结合,将水分子连接在网状内部,而疏水残基遇水交联聚合物。由胶原、明胶、透明质酸以及纤维蛋白等天然高分子材料形成的,其含水量可达到96%,材料表面光滑,具有良好的生物相容性,可以保持创面的湿润环境,与接触的组织可以发生水合作用,同时吸收伤口的渗出物,由于水凝胶材料的温度只有 5 ℃,可以起到温和的冷却作用,减少治疗后疼痛和炎症反应,水凝胶为高含水量的亲水性聚氨酯聚合物,自动调节伤口的湿润度,有少量吸收渗液的能力,容易去除。水凝胶湿性敷料的半透明设计可以观察到伤口的愈合情况,水凝胶湿性敷料治疗烧伤的临床效果文献分析,见表3。"

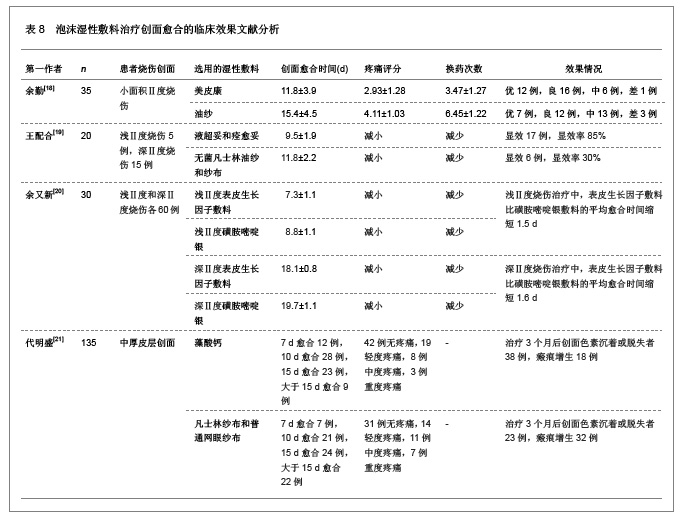
饶志高等[8]为了解决水凝胶敷料吸收创面渗液能力较差的问题,以免经常更换敷料,研制出一种高吸水性的水凝胶敷料,同时制作放射性动物烧伤模型,在所制备的凝胶敷料中掺入血管内皮生长因子,研究其在放射性烧伤治疗中的作用。材料分别选取其中的1种或2种,以不同的浓度和质量比单独或混合溶解,辐射交联,制备水凝胶膜。观察不同条件下制备的水凝胶膜外观,检测其溶胀度、凝胶分数和抗张强度,寻找理想水凝胶膜伤口敷料制备方法。高能电子束照射大鼠臀部,总照射剂量为50 Gy,制作大鼠放射性烧伤动物模型,并将血管内皮生长因子掺入所制备的水凝胶膜中,对照组应用凡士林纱布敷料,分别覆盖烧伤面进行治疗。测量治疗过程中创面溃疡面积,计算溃疡愈合时间,并且在不同时间活体取材,应用苏木精伊红染色法观察治疗过程中放射性皮肤烧伤的病理学变化。 材料以浓度30%、40%溶解后,所制备的水凝胶膜有较好的透明度,气泡少,溶胀度较高,但其抗张强度低。在电子束照射剂量为45 kGy时,材料A和材料B质量比为25∶2所制备的水凝胶膜具有最高的溶胀度,并且具有较高的透明度,较好的凝胶分数以及适宜的抗张强度,而质量比为25∶6所制备的水凝胶膜具有十分理想的抗张强度、较高的溶胀度、较好的凝胶分数和透明度。在该凝胶敷料中掺入血管内皮生长因子后,相比较凡士林纱布敷料,该水凝胶敷料具有良好的放射性烧伤治疗效果。 3.2 应用藻酸盐湿性敷料的特点及治疗烧伤的效果 藻酸盐敷料是从海藻中提取出来的藻蛋白酸,是一种类似于纤维素的不能溶解的多糖,柔软的无纺织纤维,含有85%的天然藻酸盐纤维,15%的羟甲基纤维素钠。藻酸盐敷料类似凝胶并能被生物降解的藻朊,可与氯化钙反应制成蚕丝状细纤维,按一定顺序交织排列,加压后制成2 mm厚的藻酸盐敷料。在制作过程中被转换成钙盐,具有很强的吸收性,吸收率为自身质量的20倍,能有效控制渗出液,形成柔软、潮湿、类似凝胶的半固体物质,与渗液发生离子交换,将不溶性藻酸钙变为可溶性藻酸钠,同时释放钙离子,因此具有止血功能,延长敷料的使用时间,还可以在伤口表面形成一层比较稳定的网状结构,使伤口与外界隔绝,形成一个密闭的无氧环境,加速新生微血管增生,对维持湿润环境,提高表皮细胞的再生能力,加快表皮细胞移动,有利于血液凝固。 藻酸盐敷料具有以下特点:①透气性良好,无毒、无刺激、无抗原性。②具有机械压迫止血和促进凝血的功效。③可以减少创面水、盐与营养物质的丢失。④限制细菌在创面上生长繁殖。⑤使创面保持湿润环境,有利于上皮生长。⑥携带和使用方便。与传统敷料比较,藻酸盐敷料引起感染的机率较低,主要是由于其材料的密闭性好,隔绝与外界空气的接触,同时还可以促进局部血管增生,增加血液供应,使治疗效果有所提高,而且潮湿和微酸的内环境对中性粒细胞发挥作用有辅助作用,提高了局部的杀菌能力,使感染的发生率降低。 藻酸盐敷料的产品有褐藻酸钠敷料等。褐藻酸钠是褐藻类植物富含的一种天然创伤修复材料,在铜藻中含量为31%,在裙带菜中的含量为29%,海带中褐藻酸钠的含量在24%-26%。将褐藻洗净后,加入热碱水搅烂,用水稀释后,去除残渣后就可以得到一种分散均匀的溶解胶体,这种胶体就是褐藻酸钠。如果将胶体用酸处理,就会得到凝胶褐藻酸。褐藻酸钠和褐藻酸统称为褐藻胶。用其制作的凝胶膜片或海绵材料,可以用来保护创面和治疗烧伤和烫伤创面。褐藻胶还是安全有效的止血药,用褐藻胶制成的止血纱布,用于压迫和包扎大动脉出血,数分钟后就能有效止血。褐藻胶制成得各种药物,如止血粉、止血海绵等在外科中应用十分普遍。同时,褐藻酸钠还可以制成良好的血浆代用品,当大量失血、大面积烫伤等原因引起血液循环量降低,产生休克的危急状态时,可以用褐藻酸钠制成代血浆,补充血容量。 藻酸盐湿性敷料治疗烧伤的临床效果文献分析,见表4。"

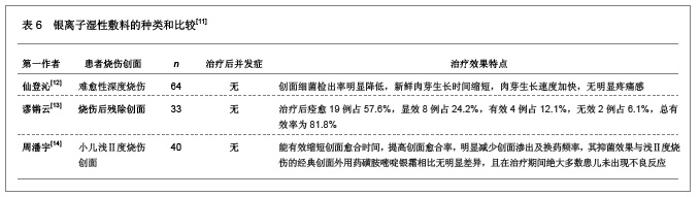
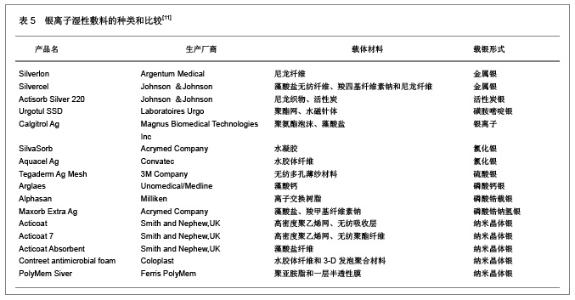
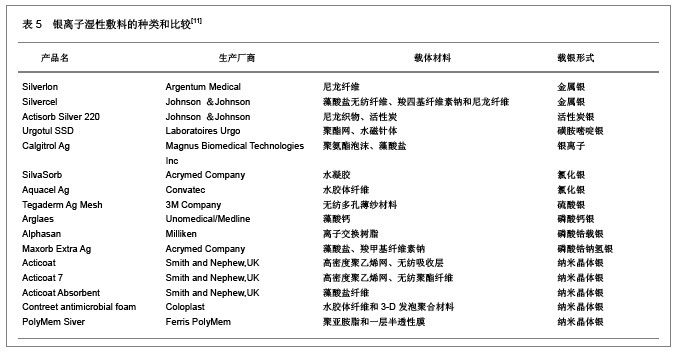
银离子湿性敷料具有独特的吸收性能,在吸收渗液的同时能够释放银离子来杀菌,纳米量级的银离子颗料可以避免银离子过度沉积,杀菌活性明显提高,明显优于传统的庆大霉素敷料,由于长期使用庆大霉素会出现耳毒性或肾毒性,因此建议不宜长期使用庆大霉素敷料。银离子敷料是基于重金属离子对细菌蛋白质的变性作用,因而具有广谱杀菌和很少产生耐药菌的特点,吸收能力较强且透气性能良好,能够促进伤口上皮组织的愈合。银离子敷料是在水胶体敷料的基础上添加含银化合物制成的,可以持续释放银离子,有效时间长达1周,吸收渗液的同时提供湿性愈合环境,适合于各种难愈合伤口局部感染的预防和治疗。银离子湿性敷料治疗烧伤的临床效果文献分析,见表6。"


3.4 应用泡沫湿性敷料特点及治疗烧伤的效果 泡沫湿性敷料的结构具有多孔性,对液体具有较大的吸收容量,对氧气和二氧化碳几乎能完全透过。合成原料有聚乙烯丁醛、聚氨基甲酸乙酯、聚氨酯、聚已烯醇等。其对伤口渗出液的处理是靠海绵型的水蒸汽转运和吸收机制来控制渗出物的。辅料可制成各种厚度,对创面具有良好的保护作用,保温、保湿能力较强,敷料材质轻,患者感觉较舒服。泡沫结构能够防止敷料与肉芽组织黏连,同时半通透性的膜体可以维持伤口的湿性愈合环境,防水和防菌。泡沫湿性敷料吸收渗液后快速膨胀可以使敷料与伤口底部良好的接触。中等孔径的泡沫具有良好的毛细管作用,独特的负压引流作用可以确保与创面的完全接触,快速引流,垂直吸收,将渗液紧锁在固定区域,不会浸渍周围皮肤。泡沫湿性敷料最长可以使用5-7 d的时间,主要用于各种伤口愈合阶段的中等渗出,表浅无感染的伤口。泡沫湿性敷料治疗创面愈合的临床效果文献分析,见表7。"


3.5 其他湿性敷料 纳米氧化硅是一种表面呈微孔的新型生物材料,应用化学的阴阳粒子交换法进入纳米氧化硅的微孔中,再使用低温脱水、高温稳定等工艺制成纳米级的抗菌谱广、无毒、高效、持久透气性好的烧烫伤敷料,纳米氧化硅具有较强皮肤渗透性及抗菌性,可以有效预防和消除创面感染的发生,促进创面愈合。纳米抗菌敷料不仅在烧伤的治疗中有良好的疗效,在其他慢性溃疡及感染伤口治疗方面也有效果。纳米敷料的杀菌机理是能透过细菌细胞膜来阻断呼吸酶,并通过银离子的缓释后与带阴电荷的菌体蛋白质结合。使其变性沉淀,导致基酶活性受抑制,抑制烧伤创面过多的基质金属蛋白酶。使纳米敷料具有广谱的杀菌和抗菌作用,而且不易产生耐药性。但是纳米敷料由于其成本价格较高,大面积使用仍然受到限制。此外,纳米抗菌敷料的生物学机制还有待于深入研究。"


5 小结 理想的湿性敷料在临床应用时需要具备以下优点:①有类似于皮肤的水分蒸发率。②保持伤口生理环境,防止干燥。③有利于坏死组织的脱落、清除、保持伤口基底洁净,减少感染的危险。④吸收过多的渗液,有利于引流除臭。⑤保持伤口温度在28-32 ℃;有良好的顺应性,易揭除,不伤肉芽,无痛。⑥免除微生物的入侵,起到屏障作用。⑦减少热量、蛋白质、电解质经伤口丢失。 创面的修复过程是十分复杂的,与许多因素的相互作用有关,如局部组织的营养、微环境、生长因子含量、微循环、低氧条件、感染等[22]。近年来,创面的愈合与低氧湿润环境的研究倍受学术界的关注,目前创面的湿性愈合理论已被临床广泛应用,湿性敷料能够加速创面愈合和促进组织生长提供理想的微环境[23-25]。有利于创面的炎症扩散消退,缓解疼痛,使渗出物的含量减少,有纤维蛋白膜的出现,细菌生长减少[26]。微循环保持低氧的状态,可以刺激新生的毛细血管生长以及肉芽组织生长和上皮移行[27]。银离子湿性敷料的创面接触层为一层软聚硅酮黏胶,使伤口保持一个适度湿润的环境,司肤泰克层可以确保更换敷料的无创性,可轻柔的从皮肤处揭开却不会产生皮肤表层的脱落,从而造成的良好的湿性环境能够促进创面的愈合。 临床治疗中观察湿性敷料的应用效果,证实湿性敷料在Ⅱ度烧伤创面,有伤口愈合时间缩短,疼痛减轻,能用于身体的任何部位,提高了患者的舒适度,从而提高患者生活质量的优点。因此,尽管湿性愈合敷料单价较高,成为影响使用障碍的因素,但从伤口愈合全过程及患者的舒适度方面进行成本效益计算,经过有关资料分析[28],患者总费用没有增加,文章中介绍的患者均在门诊治疗,与住院治疗费用相比也明显减少。 作者贡献:王清华进行实验设计、实施、评估、资料收集和成文,王清华对实验进行审校并对文章负责。 利益冲突:课题未涉及任何厂家及相关雇主或其他经济组织直接或间接的经济或利益的赞助。 伦理要求:实验获得所在单位的伦理委员会批注,符合伦理学标准。 作者声明:文章为原创作品,数据准确,内容不涉及泄密,无一稿两投,无抄袭,无内容剽窃,无作者署名争议,无与他人课题以及专利技术的争执,内容真实,文责自负。"

| [1] Winter GD.Formation of the scab and the rate of epithelisation of superficial wounds in the skin of the young domestic pig.1962.J Wound Care.1995;4(8):366-367.[2] 李东,张杰,牛星焘,等.密闭湿润环境与创面愈合[J].实用美容整形外科杂志,2000,11(3):142-145.[3] 杨晓静,范红.湿性伤口愈合的护理体会[J].实用医技杂志,2004, 11(8): 1490-1491. [4] 湿性敷料.Mepilex美皮康产品介绍[DB/OL].2013-01-31. http://www.mepiform.net.[5] 刁永力,王书军,陈濛.水凝胶敷料爱康肤银在浅Ⅱ度烧伤创面治疗中的应用[J].东南大学学报(医学版),2012,31(6):729-731. [6] 蔡良良,吕国忠,陈敬华,等.光交联壳聚糖水凝胶膜治疗深Ⅱ度烧伤创面的临床研究[J].中华损伤与修复杂志(电子版),2010,5(1): 27-29. [7] 龚振华,姚建,季建峰,等.银离子敷料联合水凝胶对Ⅱ度烧伤创面愈合的作用[J].中国组织工程研究与临床康复,2009,13(42): 8373-8376. [8] 饶志高.新型高溶胀性水凝胶膜的研制及其治疗放射性烧伤的实验研究[D].浙江:苏州大学,2008:4-6. [9] 叶溱,陈炯.藻酸盐敷料在烧伤供皮区创面的应用[J].浙江医学, 2001,23(4):248-249. [10] 黄国宝,张磊,张科验,等.藻酸盐敷料应用于难愈性烧伤创面随机对照[J].中国组织工程研究与临床康复,2010,14(34): 6355-6358. [11] 焦展,安胜军,温昕,等.载银敷料研究现状与展望[J].中华创伤杂志,2009,25(10):958-960. [12] 仙登沁,赵海,王运平,等.银离子敷料联合水胶体密闭法治疗难愈性深度烧伤创面[J].武警医学,2012,23(11):952-954. [13] 廖锵云,吴晓健,容咏新,等.纳米晶体银敷料治疗烧伤后残余创面的效果评价[J].中国当代医药,2012,19(26):66-67. [14] 周潘宇,夏照帆,贲道锋,等.爱康肤银离子敷料在小儿浅Ⅱ度烧伤创面的临床应用[J].第二军医大学学报,2011,32(12): 1321-1323. [15] 张金梅,刘静,李恒,等.泡沫敷料用于伤口肉芽组织水肿创面换药的效果观察[J].护士进修杂志,2012,27(1):63-64. [16] 吕文魁,秦纹,孙奇.重组人表皮生长因子联合软聚硅酮泡沫敷料治疗糖尿病足的疗效观察[J].新疆医学,2010,40(10):8-10.[17] 石晓敏,周琴,吴庆芳.泡沫银敷料治疗小儿面部烫伤创面的临床体会[J].全科护理,2012,10(5):408-409. [18] 余勤,王金凤,毛洪梅,等.美皮康超薄型敷料与油纱在小面积Ⅱ度烧伤换药中的效果比较[J].西部医学,2011,23(3):563-565. [19] 王配合,杨建民,张轶,等.液超妥与痊愈妥复合敷料治疗Ⅱ度烧伤创面的效果观察[J].临床误诊误治,2011,24(6):17-18. [20] 余又新,陈旭林,汪昌荣.表皮生长因子敷料和磺胺嘧啶银治疗小面积Ⅱ度烧伤疗效比较[J].安徽医学,1999,20(6):48. [21] 代明盛,王李云,沈华强.湿性敷料与干性敷料在中厚供皮区上应用的对比研究[J].实用医学杂志,2011,27(1):58-60. [22] 吴祖煌,刘敏,王煜,等.湿性敷料促进供皮区创面愈合的临床研究[J].中国实用美容整形外科杂志,2004,15(5):251-252. [23] 付小兵,王德文.创伤修复基础[M].北京:人民军医出版社,1999: 173-177. [24] 付小兵,王德文.现代创伤修复学[M].北京:人民军医出版社,1999: 245-248. [25] 田建广,夏照帆.创面敷料的研究进展[J].解放军医学杂志,2003, 28(5):470-471. [26] Chen WY, Rogers AA, Lydon MJ.Characterization of biologic properties of wound fluid collected during early stages of wound healing.J Invest Dermatol.1992;99(5):559-564.[27] 孟凡慧,王丽华,王嘉茹,等.湿性敷料在切口裂开护理中的效果观察[J].现代护理,2005,11(6):424-426.[28] 黄漫容,叶新梅,陈利芬,等.湿性愈合敷料治疗压疮的效果观察与成本效益分析[J].现代临床护理,2005,4(6):10-12. |
| [1] | Liu Yang, Liu Donghui , Xu Lei, Zhan Xu, Sun Haobo, Kang Kai. Role and trend of stimuli-responsive injectable hydrogels in precise myocardial infarction therapy [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(8): 2072-2080. |
| [2] | Wang Zheng, Cheng Ji, Yu Jinlong, Liu Wenhong, Wang Zhaohong, Zhou Luxing. Progress and future perspectives on the application of hydrogel materials in stroke therapy [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(8): 2081-2090. |
| [3] | Guo Yuchao, Ni Qianwei, Yin Chen, Jigeer·Saiyilihan, Gao Zhan . Quaternized chitosan hemostatic materials: synthesis, mechanism, and application [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(8): 2091-2100. |
| [4] | Liu Hongjie, Mu Qiuju, Shen Yuxue, Liang Fei, Zhu Lili. Metal organic framework/carboxymethyl chitosan-oxidized sodium alginate/platelet-rich plasma hydrogel promotes healing of diabetic infected wounds [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(8): 1929-1939. |
| [5] | Zhou Hongli, Wang Xiaolong, Guo Rui, Yao Xuanxuan, Guo Ru, Zhou Xiongtao, He Xiangyi. Fabrication and characterization of nanohydroxyapatite/sodium alginate/polycaprolactone/alendronate scaffold [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(8): 1962-1970. |
| [6] |
Dong Chunyang, Zhou Tianen, Mo Mengxue, Lyu Wenquan, Gao Ming, Zhu Ruikai, Gao Zhiwei.
Action mechanism of metformin combined with Eomecon chionantha Hance dressing in treatment of deep second-degree burn wounds#br#
#br#
[J]. Chinese Journal of Tissue Engineering Research, 2026, 30(8): 2001-2013.
|
| [7] | Pan Hongfei, Zhuang Zhenbing, Xu Baiyun, Yang Zhangyang, Lin Kairui, Zhan Bingqing, Lan Jinghan, Gao Heng, Zhang Nanbo, Lin Jiayu. Inhibitory effects of different concentrations of auranofin on M1 macrophage function and its therapeutic potential in diabetic wound healing [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(6): 1390-1397. |
| [8] | Peng Zhiwei, Chen Lei, Tong Lei. Luteolin promotes wound healing in diabetic mice: roles and mechanisms [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(6): 1398-1406. |
| [9] | Li Haojing, Wang Xin, Song Chenglin, Zhang Shengnan, Chen Yunxin. Therapeutic efficacy of extracorporeal shock wave therapy in the upper trapezius muscle area combined with exercise control training in patients with chronic non-specific neck pain [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(5): 1162-1170. |
| [10] | Liu Xinyue, Li Chunnian, Li Yizhuo, Xu Shifang. Regeneration and repair of oral alveolar bone defects [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(5): 1247-1259. |
| [11] | Yu Shiyu, Yu Sutong, Xu Yang, Zhen Xiangyan, Han Fengxuan. Advances in research and application of tissue engineering therapeutic strategies in oral submucous fibrosis [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(4): 936-948. |
| [12] | Li Hanyue, Li Yini, Xiang Linmei, Li Sen. Effects of resistance exercise therapy on pain and function in patients with cervical spondylotic radiculopathy: a meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(4): 987-996. |
| [13] | Zhou Feng, Fu Pengfei, Qian Yufan, Xu Pingcheng, Guo Jiongjiong, Zhang Lei. Correlation between spinal sagittal imbalance and knee joint parameters detected by whole-body EOS imaging [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(3): 596-603. |
| [14] | Yang Hu, Zheng Yu, Jia Chengming, Wang Tong, Zhang Guangfei, Ji Yaoyao. Immune microenvironment regulates bone regeneration [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(3): 701-710. |
| [15] | Yang Peng, Xu Chenghan, Zhou Yingjie, Chai Xubin, Zhuo Hanjie, Li Lin, Shi Jinyu. A meta-analysis of risk factors for residual back pain after vertebral augmentation for osteoporotic vertebral compression fractures [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(3): 731-739. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||