Chinese Journal of Tissue Engineering Research ›› 2017, Vol. 21 ›› Issue (26): 4252-4257.doi: 10.3969/j.issn.2095-4344.2017.26.026
Previous Articles Next Articles
Application and prospect of dextran as a new medical dressing
- 1Plastic Surgery Hospital, Chinese Academy of Medical Sciences, Beijing 100000, China; 2Beijing Bohui Ruijin Biological Technology Limited Company, Beijing 100000, China
-
Received:2017-05-03Online:2017-09-18Published:2017-09-28 -
Contact:Pan Bo, M.D., Associate chief physician, Plastic Surgery Hospital, Chinese Academy of Medical Sciences, Beijing 100000, China -
About author:Wang Xiao-lin, Studying for master’s degree, Plastic Surgery Hospital, Chinese Academy of Medical Sciences, Beijing 100000, China -
Supported by:the National High-tech Research and Development Program of China (863 Program), No. 2015AA033602
CLC Number:
Cite this article
Wang Xiao-lin, Zhao Bao, Pan Bo.
share this article
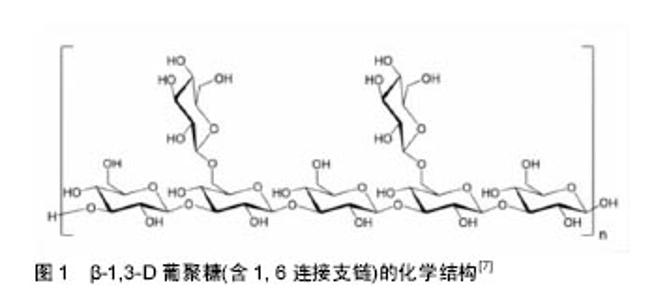
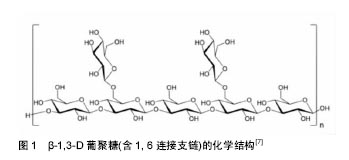
2.1 葡聚糖促进伤口愈合的相关生理功能 葡聚糖是一种细胞壁多糖,存在于酵母、真菌(包括蘑菇)、细菌、谷物等[6]。葡聚糖结构是以葡萄糖为单元,单元之间以糖苷键链接,且根据糖苷键的不同分为α-葡聚糖和β-葡聚糖,其中以β-葡聚糖最具有生理活性。有研究发现β-葡聚糖诸多理化性质及生理功能均与其分子结构密切相关,要合理解释β-葡聚糖这些性质并有效加以开发利用,就必需首先弄清其分子结构。关于β-葡聚糖分子结构,国外学者很早就开始研究。现已知它是D葡萄糖以β-1→4和β-1→3糖苷键连接而成线性多糖(图1)[7]。这两种糖苷键比例大致为7∶3,但其确切比例不同学者研究结论略有不同,这与研究中所采用提取条件、温度及分析方法有关。"

在20世纪40年代,Pillager博士首次发现并报道酵母细胞壁中有一种物质β-葡聚糖具有提高免疫力的作用。从20世纪70年代后,越来越多的科学工作者对β-葡聚糖的生理功能进行了深入研究,发现其在抗肿瘤、保护心肌、创伤愈合以及抗凝血方面都有重要的作用[8]。其中促进创伤愈合作用、调节免疫、抗凝血与β-葡聚糖可作为新敷料息息相关。 国内外的许多研究都证明了β-葡聚糖能够促进伤口愈合。在Yamamoto 和Kimura的实验研究中发现从绣球菌中提纯的β-葡聚糖能够促进糖尿病小鼠的伤口愈合[9],证明了β-葡聚糖在促进伤口愈合过程中起到一定作用。而Hisao等[10]的组织病理学研究也提示β-葡聚糖会促进小鼠皮肤的愈合。Choi等[11]实验将从眼虫中分离的β-葡聚糖作用于小鼠碱烧伤模型,发现β-葡聚糖特别是结合了透明质酸会促进上皮愈合并抑制炎症反应,此实验再次证明了β-葡聚糖的促进伤口愈合作用。针对β-葡聚糖的这种促进伤口愈合的作用有许多学者进行了深入的探究,发现其通过多方面作用促进伤口的愈合。①曾经有文献报道β-葡聚糖能增加巨噬细胞在创伤区域的渗入、促进肉芽生长、胶原沉积以及增强伤口的抗拉强度[12];②另有研究发现在人的成纤维细胞表面有一种特殊的葡聚糖受体,它与相应的葡聚糖配体结合后,能够调节成纤维细胞的功能[13];③Wei等[14]研究发现β-葡聚糖能够刺激神经营养因子3、血小板衍生生长因子A、血小板衍生生长因子B、成纤维细胞生长因子、转化生长因子以及血管内皮生长因子等在成纤维细胞中的表达。以上实验研究不仅从直观效果上证明了β-葡聚糖确实存在促进伤口愈合的作用,甚至还从分子机制上进一步进行了论证。 另一方面,根据临床经验得知减少创面感染概率也会促进创面愈合,所以β-葡聚糖在调节免疫方面的作用可在一定程度上减少创面感染,这又是β-葡聚糖可以作为新型医用敷料的一个依据。有实验证明β-葡聚糖能解除抗肿瘤药物对机体免疫力的抑制作用,从而印证了其具有免疫活性[15]。Zykova等[16]在对糖尿病足溃疡的治疗研究中也发现β-葡聚糖作为免疫诱导剂可以加速皮肤愈合。另有实验甚至发现β-葡聚糖可通过与巨噬细胞和嗜中性粒细胞、淋巴细胞表面多糖受体结合,影响细胞信息传递过程,从而影响免疫细胞基因表达和淋巴细胞功能,达到调节免疫作用[17]。以上及其他大量实验研究共同证明了β-葡聚糖具有激活巨噬细胞、树突状细胞和单核细胞,诱导一氧化氮合成,调控与免疫反应相关的细胞信号传递,降低电离辐射对机体免疫力的损伤,促进免疫球蛋白合成等免疫活性[18]。 研究还发现葡聚糖具有抗凝血作用。曾经有研究为了寻找肝素的替代品,合成了多种结构确定的多糖硫酸盐,经过测试β-葡聚糖硫酸盐表现出了显著的抗凝血活性[19]。实验对其构效关系、相对分子质量等方面进行研究,发现硫酸盐的模式以及多糖的基本结构是葡聚糖抗凝效果的决定因素,即葡聚糖依靠于自身独特的结构,特定地干扰凝血过程的不同阶段。虽然葡聚糖具有抗凝血功能,但是这种生理功能对于伤口愈合的作用还是未知的,需要进一步研究证明。 2.2 葡聚糖的高分子优势 葡聚糖自身所特有的高分子优势也为其作为新型医用敷料提供了新依据。葡聚糖和其他药用高分子材料相比具有以下优点[20]:第一,葡聚糖的水溶性好,油/水分配系数接近1,吸收性好。这样就可以吸收大量的伤口渗液,使敷料更换的时间间隔较长,次数较少,减少护理时间,降低总体护理费用;同时能够有效保留伤口渗液,提供伤口愈合所需的湿润环境。毛珺等[21]观察高吸型壳聚糖敷料的创面止血及促愈合效果。实验取清洁级SD大鼠40只,制作背部深Ⅱ度烫伤创面,随机分为2组,实验组创面局部以高吸型壳聚糖敷料包扎,对照组以凡士林纱布包扎,修复后7,14,21 d实验组的未愈合创面面积均低于对照组(P < 0.05)。修复后21 d,对照组上皮修复较好,有少许淋巴细胞浸润,可见痂皮;实验组上皮修复良好,可见完整新生鳞状上皮层,无炎症细胞浸润;结果表明,高吸型壳聚糖敷料具有良好的创面止血和促创面愈合效果,发现吸水性较好的高吸型壳聚糖敷料能够吸收大量渗液,避免伤口处的组织液外渗以及频繁进行伤口敷料的更换。葡聚糖较好的吸水性特点可成为其作为新型医用敷料的一个很重要的特性。第二,葡聚糖具有生物可降解性,敷料使用后变为医用垃圾不会对环境造成污染,具有环保性。第三,抗原性小,会减少排异反应和炎症反应,有利于伤口的恢复。第四,葡聚糖分子结构中含有大量的羟基,适合于与其他物质发生反应,形成高分子挂接药物或者交联形成微球等。这个优势可以使葡聚糖跟其他高分子相结合进行优劣互补。第五,具有安全性,葡聚糖在临床上已经被用作代血浆[22],其作为医用敷料具有很高的安全性。第六,葡聚糖的分子质量可控且分布窄,市场可提供分子质量分级的葡聚糖,这为葡聚糖敷料的市场化提供了有利的条件。上述葡聚糖具有的优势以及其无毒副作用、无耐药性、无污染的特点都证明了葡聚糖作为新型医用敷料具有很好的临床前景[23]。 2.3 葡聚糖与其他高分子、大分子结合作为医用敷料的相关研究 葡聚糖与其他高分子相结合也为其作为新型敷料提供了更为广阔的前景。最近就有实验将葡聚糖与聚乙烯醇相结合研制成具有葡聚糖微结构的聚乙烯醇凝胶敷料[24]。将葡聚糖与聚乙烯醇结合,可以做到优势互补,使医用敷料更加理想化。在聚乙烯醇的宏观凝胶网络中嵌入葡聚糖微凝胶,把微凝胶的快速响应性与大凝胶的高机械强度有效的结合在一起。聚乙烯醇宏观凝胶的高机械强度可保持敷料形状的完整性,不会破碎,对外界起到屏障作用,抑制病菌入侵感染。实验比较了不给药组纱布、聚乙烯醇凝胶、聚乙烯醇/葡聚糖复合凝胶和Dex/PVA BHMs凝胶(包埋了苯妥英钠的具有葡聚糖微结构的聚乙烯醇凝胶)包扎后10 d内伤口愈合效果。结果显示采用纱布包扎的伤口10 d内仅结痂,并没有出现明显缩小、愈合的现象,而聚乙烯醇/葡聚糖复合凝胶伤口愈合效果比纱布及单纯聚乙烯醇的效果都好。该实验充分证明葡聚糖可以与其他高分子结合来作为医用敷料促进伤口的愈合。而且该实验还在聚乙烯醇/葡聚糖复合凝胶的基础上包埋了苯妥英钠药物,实验结果显示其对于大鼠背部烧伤处伤口不仅无损伤破坏作用,而且促进伤口愈合,显著提高了愈合效果。许多研究也发现在新型医用敷料的材料上负载各种药物和生长因子,不仅可有效控制药物释放,同时还达到促进伤口愈合及治疗作用[1]。所以在制备以葡聚糖为原料的医用敷料的时候也可以包埋药物,来达到更快速地促进伤口愈合。 有实验对葡聚糖与透明质酸相结合作为医用敷料进行了研究[7],即将葡聚糖和透明质酸通过接枝反应形成葡聚糖接枝透明质酸海绵敷料。两者结合后一方面可以克服自身单独的缺点,另一方面又能促进创伤修复,来达到葡聚糖接枝透明质酸可以作为医用敷料的目的。该研究中通过小鼠创伤修复实验,表明葡聚糖、葡聚糖接枝透明质酸都能够通过刺激巨噬细胞分泌白细胞介素1和白细胞介素6,刺激成纤维细胞增殖以及促进透明质酸、胶原和胶原酶合成,从而促进创伤修复。作为医用敷料不仅需要其有促进伤口愈合的效果,而且其毒性、降解性等方面也是考虑作为医用敷料的重点。因此,该实验中除了证明葡聚糖接枝透明质酸对创伤修复的直接作用,还对其降解性、细胞毒性及组织相容性做了相关研究,这些研究结论都为葡聚糖接枝透明质酸做为新型医用敷料提供了可能。通过降解实验,发现葡聚糖接枝透明质酸能够克服葡聚糖难以降解和透明质酸过快降解的缺点,并且集合了两者的生物活性功能。通过细胞毒性实验检测出葡聚糖接枝透明质酸材料在20 g/L质量浓度范围内没有细胞毒性。通过细胞黏附实验得出成纤维细胞可以在葡聚糖接枝透明质酸薄膜上生长,说明材料具有良好的细胞生物相容性,能够与细胞发生相互作用。通过动物模型实验发现葡聚糖和透明质酸结合可促进伤口愈合,同时其细胞毒性、生物相容性以及可降解性实验进一步证明葡聚糖接枝透明质酸作为医用敷料的可行性。 除了葡聚糖与聚乙烯醇、透明质酸相结合形成新型材料外,Kim等[25]研究还将葡聚糖与聚羟基乙酸结合形成一种新型聚合物膜(BG/PLGA)。该研究在显微镜下观察发现葡聚糖/聚羟基乙酸能够增加细胞反应、加快细胞增殖。而且在动物模型实验中,葡聚糖/聚羟基乙酸与聚羟基乙酸相比,增加了伤口周围细胞之间的相互作用,加快了细胞增殖及血管再生,有促进伤口愈合的效果。聚羟基乙酸已经被美国FDA批准为医用高分子材料,并且以其机械性能好,可塑性强的优势改善了葡聚糖支架的机械强度。 魏婷婷[26]将明胶和β-葡聚糖以不同比例混合制得骨架,考察成纤维细胞在这些骨架中的附着与繁殖,从而证明明胶和β-葡聚糖复合物可以促进伤口愈合。该实验的研究基础是,一方面明胶作为创伤敷料和具有黏附性、吸收性的外科用衬垫广泛应用于医学治疗中;胶原及其降解物在创伤修复、骨折愈合以及胚胎形成过程中可能作为体内成纤维细胞的引诱剂;在生物学性质上,明胶无抗原性,能活化巨噬细胞,具有很好的止血作用。另一方面它能表现出抗菌性、抗病毒性和抗凝作用以及促进伤口愈合的活性。动物实验表明,细胞性明胶/(1-3),(1-6)-β-葡聚糖聚合生物人造皮肤促进了全厚皮肤创伤的表皮再生,即有促进创伤愈合的效果。明胶和葡聚糖组成的多孔骨架具有互联多孔结构和足以支撑成纤维细胞和角化细胞生长的孔径。细胞的附着和繁殖随着明胶含量的增加而增强,吸水量随β-葡聚糖的增加而增加。综上所述,由明胶和β-葡聚糖制得的人造皮肤确实可以有效地促进伤口愈合。 葡聚糖与聚乙烯醇、透明质酸、聚羟基乙酸以及明胶结合形成的新型聚合物在以上实验研究中都论证了其可作为医用敷料的可能。与高分子、大分子结合形成新的聚合物给以葡聚糖为原料制备新型医用敷料提供了新的思路,使葡聚糖在新型医用敷料方面的前景更加广阔。 2.4 葡聚糖在组织工程材料及药物载体中的应用 葡聚糖在组织工程材料方面的应用大多是以葡聚糖水凝胶的形式进行。葡聚糖作为理想的组织工程材料的基础是其水凝胶网络中含有大量的水分,且具有良好的生物相容性和可降解性,并具有与生物组织相似的理化性质。肖飞等[27]研究以甲基丙烯酰基修饰的葡聚糖与N-异丙基丙烯酰胺共聚制备水凝胶,利用红外光谱表征了单体和凝胶结构,并对凝胶进行了细胞培养和脱附研究,结果发现该凝胶具有良好的温度敏感性和细胞相容性,可通过控制温度变化,实现细胞从凝胶表面自动脱附,保护了细胞的功能完整性。 近年来葡聚糖以其水凝胶的形式在药物输送与药物释放方面的应用研究发展很快。周四元等[28]研究将葡聚糖与强的松龙结合形成不同分子质量的强的松 龙-葡聚糖,研究表明不同分子质量地塞米松-葡聚糖连接物均具有一定的结肠靶向释药特异性。研究还有一重要发现:葡聚糖的骨架结构对葡聚糖-糖皮质激素连接物的结肠靶向释药也有极其重要的作用,如果葡聚糖的骨架结构被破坏,则糖皮质激素-葡聚糖连接物的结肠靶向释药特性消失。在葡聚糖作为药物载体的研究中发现,葡聚糖具有大量活泼的羟基,很容易对其进行改性,而且来源丰富,价格低廉;此外葡聚糖可在体内被葡萄糖苷酶降解,降解后的产物对身体无毒无害,是一种生物可降解性和生物相容性都较好的材料[29]。 2.5 葡聚糖提取及制备工艺 尽管葡聚糖本身具有很多优势以及在医用敷料方面的良好应用前景。但从原料葡聚糖到生产出以葡聚糖为原料的新型医用敷料还有很长的路要走。首先要面临的就是葡聚糖的提取。关于β-葡聚糖的提取分离纯化技术很多,包括热水提取、溶剂提取、酶法提取、碱水提取等。多种比较容易操作的葡聚糖获取方法,使得制备以葡聚糖为原料的新型医用敷料成为可能。 选用超滤膜法对β-葡聚糖进行浓缩处理[30],目的是通过超滤膜浓缩纯化β-葡聚糖替代或补充传统工艺,降低其运行费用,减少有效成分流失。实验使用科氏卷式超滤膜分离系统在进料流速70 L/min,压力为0.3-0.5 MPa,温度为35-55 ℃,料液浓缩10倍的范围内,对料液中的有效成分实现100%的截留,实验最后使用超滤膜法浓缩β-葡聚糖10倍后进入喷雾干燥工艺。与蒸发浓缩的方式相比,喷雾干燥工艺具有环保、节能、不破坏营养成分的优点。实验结果表明使用相对分子质量为10 000的超滤膜对β-葡聚糖进行浓缩脱水是可行的。 近些年,中空纤维液流场流分离技术因其分离效果好,中空纤维造价便宜,装置简单易于操作,已被视为分离高分子物质和粒子物质的好方法[31]。实验设计了一种简单易操作的中空纤维液流场流分离装置,实现了高分子葡聚糖的获取。原料是将蓝色葡聚糖(相对分子质量为2 000 000)溶解在蒸馏水中制备葡聚糖溶液。然后安装好中空纤维液流场流分离装置,用泵通以乙醇液或甲醇液润湿纤维并赶走空气,最后将葡聚糖溶液放入该装置中。实验结果表明,在不同的入口流速下,给予足够的液流交汇时间和外场强度,葡聚糖能得到很好的保留。 葡聚糖提取及制备工艺已使葡聚糖成功应用于制药工业和保健品等。一些欧美国家甚至实现了葡聚糖的产业化,这将为以葡聚糖为原料的医用敷料市场化提供了可能,满足了进一步生产出以葡聚糖为原料的新型医用敷料的前提。 目前市场上的医用新型敷料分为薄膜类、水凝胶类、泡沫类等,见表1。"

| [1]王震云.医用伤口敷料的研制与临床应用[J].中华护理杂志, 2006,41(1) :87-88.[2]杜天乐,刘东林,景春晖,等. 创伤敷料对促进创面愈合的研究进展[J]. 医学综述,2015,21(6):969-971.[3]吴健,郑裕东,刘向阳,等.医用敷料产业发展现状及前景分析与探讨[J].新材料产业,2011(10):70-76.[4]张世庆,鲁景艳,章金刚.医用敷料进展及产品安全有效性研究简述[J].中国药物警戒,2012,9(5):299-302.[5]王冰洋,牛广明,杜华,等.不同敷料在糖尿病足溃疡伤口治疗中的研究与应用[J].中国组织工程研究,2016,20(34):5155-5162.[6]Du B, Bian Z, Xu B.Skin health promotion effects of natural beta-glucan derived from cereals and microorganisms: a review.Phytother Res. 2014;28(2):159-166.[7]陈鹏. 葡聚糖接枝透明质酸共聚物作为皮肤敷料的研究[D].广州:暨南大学,2013.[8]周瑞瑞,刘爱军,刘建国,等.beta葡聚糖的药理作用研究进展[J].药学实践杂志,2009,27(6):401-403.[9]Yamamoto K, Kimura T.Orally and topically administered Sparassis crispa (Hanabiratake) improved healing of skin wounds in mice with streptozotocin-induced diabetes.Biosci Biotechnol Biochem. 2013;77(6):1303-1305.[10]Hsiao CM, Wu YS, Nan FH,et al. Immunomodulator 'mushroom beta glucan' induces Wnt/β catenin signalling and improves wound recovery in tilapia and rat skin: a histopathological study. Int Wound J. 2016;13(6):1116-1128.[11]Choi JA, Oh TH, Choi JS,et al. Impact of β-1,3-glucan isolated from Euglena gracilis on corneal epithelial cell migration and on wound healing in a rat alkali burn model. Curr Eye Res. 2013;38(12):1207-1213.[12]Huang MH, Yang MC. Evaluation of glucan/poly(vinyl alcohol) blend wound dressing using rat models. Int J Pharm. 2008; 346(1-2):38-46.[13]Kougias P, Wei D, Rice PJ, et al. Normal human fibroblasts express pattern recognition receptors for fungal (1-->3)-beta-D-glucans. Infect Immun. 2001;69(6):3933-3938.[14]Wei D, Williams D, Browder W. Activation of AP-1 and SP1 correlates with wound growth factor gene expression in glucan-treated human fibroblasts. Int Immunopharmacol. 2002;2(8):1163-1172.[15]董靓儿,黄一帆,李进伟. 燕麦β-葡聚糖水凝胶溶胀性研究[J]. 粮食与油脂,2014(10):29-32.[16]Zykova SN, Balandina KA, Vorokhobina NV, et al. Macrophage stimulating agent soluble yeast β-1,3/1,6-glucan as a topical treatment of diabetic foot and leg ulcers: A randomized, double blind, placebo-controlled phase II study. J Diabetes Investig. 2014;5(4):392-399.[17]王晓玲,杨海龙,刘高强,等. 食药用菌β-葡聚糖的结构、构效关系及其药理作用[J]. 食用菌学报,2014(1):35-41.[18]吴昊,张建法.β-葡聚糖免疫调节作用的研究进展[J].细胞与分子免疫学杂志,2014,30(1):97-100.[19]Wang ZM, Li L, Li B, et al. Anticoagulant property of a semi-synthesized sodium beta-1,4-glucan sulfate. Yao Xue Xue Bao. 2006;41(4):323-327.[20]赵乃才,张克义.临床药物不良反应大典[M].沈阳:辽宁科学技术出版社,1998:91-97.[21]毛珺,周应山,吴庭,等.高吸型壳聚糖敷料的创面止血及促愈合效果[J].中国组织工程研究,2016,20(16):2391-2396.[22]宋少云,廖威. 葡聚糖的研究进展[J]. 中山大学学报:自然科学版, 2005, 44(s2):229-232.[23]徐智鹏,胡骏鹏,周小辉. 酵母细胞壁多糖的作用及其成分检测方法[J]. 中国饲料,2015(11):40-42.[24]钱琴. 葡聚糖微结构的聚乙烯醇凝胶敷料的制备[D]. 合肥:合肥工业大学,2010.[25]Kim HL, Lee JH, Lee MH, et al. Evaluation of electrospun (1,3)-(1,6)-β-D-glucans/biodegradable polymer as artificial skin for full-thickness wound healing.Tissue Eng Part A. 2012;18(21-22):2315-2322.[26]魏婷婷. 明胶/(1→3),(1→6)-β-葡聚糖聚合生物人造皮肤[J].明胶科学与技术,2004,24(4):199-206.[27]肖飞,邢蕊峰,董晶,等.温度敏感葡聚糖凝胶的合成及其细胞相容性研究[J].功能材料,2007,38(增刊):1835-1838.[28]周四元,梅其炳,周瑾,等.不同分子质量强的松龙-葡聚糖连接物的体外靶向释药[J].第四军医大学学报,2003,24(17): 1551-1553.[29]孙继红,温丽利,吴雁,等.葡聚糖-聚乳酸接枝共聚物的合成及其药物载体输送系统[J].北京工业大学学报,2013,39(8): 1269-1274.[30]张鹏.超滤膜分离浓缩β-葡聚糖实验研究[J].甘肃科技,2010, 26(18):44-45.[31]秦泉,Battu Serge,Cardot Philippe.一种新的中空纤维液流场流分离装置及其对葡聚糖保留行为的研究[J].四川师范大学学报:自然科学版,2010,33(5):664-667. |
| [1] | Yao Xiaoling, Peng Jiancheng, Xu Yuerong, Yang Zhidong, Zhang Shuncong. Variable-angle zero-notch anterior interbody fusion system in the treatment of cervical spondylotic myelopathy: 30-month follow-up [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1377-1382. |
| [2] | Zhang Jinglin, Leng Min, Zhu Boheng, Wang Hong. Mechanism and application of stem cell-derived exosomes in promoting diabetic wound healing [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1113-1118. |
| [3] | An Weizheng, He Xiao, Ren Shuai, Liu Jianyu. Potential of muscle-derived stem cells in peripheral nerve regeneration [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1130-1136. |
| [4] | Li Weiming, Xu Qingwen, Li Yijun, Sun Yanbo, Cui Jin, Xu Pengyuan . Deep seawater promotes wound healing in diabetic mice by activating PI3K/Akt pathway [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 724-729. |
| [5] | He Yunying, Li Lingjie, Zhang Shuqi, Li Yuzhou, Yang Sheng, Ji Ping. Method of constructing cell spheroids based on agarose and polyacrylic molds [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 553-559. |
| [6] | He Guanyu, Xu Baoshan, Du Lilong, Zhang Tongxing, Huo Zhenxin, Shen Li. Biomimetic orientated microchannel annulus fibrosus scaffold constructed by silk fibroin [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 560-566. |
| [7] | Chen Xiaoxu, Luo Yaxin, Bi Haoran, Yang Kun. Preparation and application of acellular scaffold in tissue engineering and regenerative medicine [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 591-596. |
| [8] | Kang Kunlong, Wang Xintao. Research hotspot of biological scaffold materials promoting osteogenic differentiation of bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 597-603. |
| [9] | Shen Jiahua, Fu Yong. Application of graphene-based nanomaterials in stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 604-609. |
| [10] | Zhang Tong, Cai Jinchi, Yuan Zhifa, Zhao Haiyan, Han Xingwen, Wang Wenji. Hyaluronic acid-based composite hydrogel in cartilage injury caused by osteoarthritis: application and mechanism [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 617-625. |
| [11] | Li Hui, Chen Lianglong. Application and characteristics of bone graft materials in the treatment of spinal tuberculosis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 626-630. |
| [12] | Gao Cangjian, Yang Zhen, Liu Shuyun, Li Hao, Fu Liwei, Zhao Tianyuan, Chen Wei, Liao Zhiyao, Li Pinxue, Sui Xiang, Guo Quanyi. Electrospinning for rotator cuff repair [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 637-642. |
| [13] | Guan Jian, Jia Yanfei, Zhang Baoxin , Zhao Guozhong. Application of 4D bioprinting in tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(3): 446-455. |
| [14] | Liu Jiali, Suo Hairui, Yang Han, Wang Ling, Xu Mingen. Influence of lay-down angles on mechanical properties of three-dimensional printed polycaprolactone scaffolds [J]. Chinese Journal of Tissue Engineering Research, 2022, 10(16): 2612-2617. |
| [15] | Huang Bo, Chen Mingxue, Peng Liqing, Luo Xujiang, Li Huo, Wang Hao, Tian Qinyu, Lu Xiaobo, Liu Shuyun, Guo Quanyi . Fabrication and biocompatibility of injectable gelatin-methacryloyl/cartilage-derived matrix particles composite hydrogel scaffold [J]. Chinese Journal of Tissue Engineering Research, 2022, 10(16): 2600-2606. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||