Chinese Journal of Tissue Engineering Research ›› 2013, Vol. 17 ›› Issue (29): 5379-5386.doi: 10.3969/j.issn.2095-4344.2013.29.018
Previous Articles Next Articles
Structural characteristics and advantages of a self-assembling peptide nanofiber scaffold
Yuan Liang-liang, Liang Peng
- Department of Neurosurgery, the First Affiliated Hospital of Harbin Medical University, Harbin 150001, Heilongjiang Province, China
-
Received:2013-02-04Revised:2013-03-31Online:2013-07-22Published:2013-07-22 -
Contact:Liang Peng, Professor, Doctoral supervisor, Department of Neurosurgery, the First Affiliated Hospital of Harbin Medical University, Harbin 150001, Heilongjiang Province, China liangpengd@yahoo.cn -
About author:Yuan Liang-liang★, Studying for master’s degree, Department of Neurosurgery, the First Affiliated Hospital of Harbin Medical University, Heilongjiang Province, China erallo@163.com
CLC Number:
Cite this article
Yuan Liang-liang, Liang Peng . Structural characteristics and advantages of a self-assembling peptide nanofiber scaffold[J]. Chinese Journal of Tissue Engineering Research, 2013, 17(29): 5379-5386.
share this article
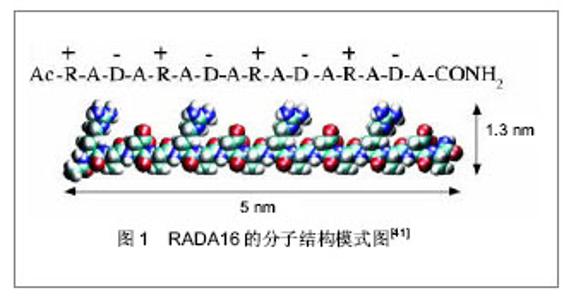
2.1 纳米纤维支架的自组装 自组装是小分子自发聚集形成具有一定连结和空间构象更大一级结构的过程。生物界中广泛存在自组装过程,从最简单的原核生物内到最复杂的生物体内普遍存在。不少天然存在的多肽、DNA、RNA、酶、蛋白,乃至病毒等都可以自发形成高度组织化、信息化和功能化的复杂结构。20年前生物起源的组分(如氨基酸和核苷酸)通常不被认为是组织工程的构建组分,随着生物技术、基因工程技术、材料工程技术和化学技术的发展,传统观念发生了急剧的转变。自从1993年存在于天然zuotin蛋白中的EAK16-Ⅱ(EAEAKAKAEAEAKAKA)被发现以来,基于自组装多肽体系的纳米材料设计获得了人们越来越多的关注,其中的离子互补型多肽近年来得到了较为广泛深入的研究。EAK16-Ⅱ属于离子互补型多肽,亲水残基和疏水残基交替出现,在培养基或生理盐水条件下形成三维纳米基质[8]。RADA16-I (RADARADARADARADA)是通过这一原则设计合成的多肽,见图1。"
在过去15年中借助天然氨基酸和核苷酸人工合成的多肽(通常将10-50个氨基酸组成的肽称为多肽)、脂肽、DNA成为组织工程材料,标志着组织工程在生物材料方面取得了巨大的突破和进展[5-6]。生物界广泛存在的分子级别自组装所形成的组合体往往具有独特的生物功能,自组装多肽的研究重点是仿照自然界的自组装过程设计出化学上互补、结构上相容的同时具备独特功能的多肽。分子自组装已经被公认为是制造涵盖一系列广泛而独特应用的新材料的重要路线[1]。 当前,纳米纤维支架的制备通常有3种技术:静电纺丝技术、相态分离技术和自组装技术[5]。借助多肽间的自组装,自组装多肽可在液态离子环境或水溶液中自组装形成3D结构。自组装多肽多以粉末的状态保存于-20 ℃冷冻干燥的条件,粉末溶解的过程即为多肽自组装的过程。由于多肽易受细菌降解,通常应用无菌纯化水溶解或肽溶液用0.2 μmol滤膜过滤。对于含半胱氨酸、蛋甲硫氨酸或色氨酸的多肽,脱氧缓冲剂对其溶解必不可少,因为这种多肽易在空气中氧化。溶液肽远比冻干形式不稳定,溶液应为中性pH值,-20 ℃保存。多肽自组装形成多肽水凝胶的分子内部和分子间主要作用途径包括:①多肽分子可逆的共价键形成。②多肽分子的金属与配体结合。③分子内部的氢键。④静电相互作用(含电荷)。⑤静电相互作用(含偶极子)。⑥疏水的相互作用。⑦芳香族的π重叠效应及电荷转移。⑧范德华力。借助上述8种作用方式,自主装多肽可以在一定条件下自发形成稳定的结构[4]。通常一个氨基酸由一个中心碳原子组成,它由4个其他基团包围:氨基、羰基、羟基和侧链,任何多肽链的关键连接均为由一个氨基酸的氨基与另一氨基酸缩合形成的肽键,某些侧链含有影响肽键形成的功能团。 多肽经离子触发可自组装成为纳米凝胶支架材料,形成与细胞外微环境相似的立体网状结构,可以构建类似体内正常的细胞外环境,区别于通常用于细胞培养的2D环境(培养皿、培养板、培养瓶等),同时又因其表面积大和多孔的特性,形成了细胞和基质间独特的接触,这种支架材料具有以下特点:①肽序列基本单位易于设计修改,可获得特异生物学活性的双亲分子,具有良好的表面活性。②形成水凝胶,类似体内微环境的3D纳米级结构,表面积和体积比大,含水量大,具有良好的结构相容性,利于细胞的黏附、增殖、分化、迁移。③不易引起毒副反应及免疫反应。④生物降解性好,即可自行降解,降解产物为氨基酸,可作为生物体营养物质的来源。⑤黏弹性好,与脊髓的物理强度相近,便于移植,可注射到靶位点[4]。以上的特点使得自组装多肽支架材料成为了一种具有良好应用前景的支架材料,逐步被应用于神经组织工程中,并且取得了理想的效果。当前,已经设计并且合成了多种不同结构的自组装多肽纳米纤维支架材料,并在生物组织工程中得到广泛的应用。例如,来源于层粘连Protein-Ⅰ的YIGSR多肽片断以及来源于Ⅳ型胶原的TAGSCLRKFSTM多肽片断,两者都具有促内皮细胞附着、生长的功能。Genové等[20]通过固相多肽合成法合成了包含活性多肽片断的自组装多肽水凝胶,在此种支架材料中培养内皮细胞时内皮细胞的分化得以促进。由于在神经系统中神经细胞与细胞外微环境紧密接触,神经细胞活性受基质的直接影响,上述优点使多肽自组装三维支架凝胶作为神经干细胞培养的支架,为神经细胞的黏附、增殖、迁移和分化提供良好的细胞外基质,为组织工程中细胞在体外的研究创造稳定的类似体内的3D微环境。作为一种新型的组织工程基质材料,自组装多肽纳米纤维支架可以为神经细胞生长和细胞功能提供优良的纳米级基质[3]。纳米自组装多肽的研究是纳米技术发展中重要的一环,已成为当前组织工程和再生医学中的研究热点。 2.2 自组装多肽的结构特点和设计策略[9-21] 早期神经组织工程材料主要是高分子聚合材料和生物高分子聚合物等,虽然这些材料都可为神经细胞黏附提供支架,对脊髓损伤修复有一定的促进作用,但由于它们通常存在细胞-材料界面不相容的问题,并且在降解过程中会产生有害的酸性物质,加之它们的生物学活性较低,因而没有在神经组织工程中取得良好的效果。第2代材料的改进之处包括在上述材料之中加入了生物活性成分,将活性成分固定于支架材料的表面对其进行修饰。虽然进行了一系列的尝试,并且在一定的程度上提高了支架材料的生物活性和细胞-界面的相容特性,但存在的问题在于包裹于支架内部有活性的生物分子位点不能得到充分暴露,限制其活性作用的发挥,由于多肽表面加入活性位点的过程复杂繁琐,并且连接于多肽之上的活性位点数量有限,此外,此类生物支架仍存在生物活性低及降解产物的生物毒性问题,因而第2代支架材料也未能在神经组织工程领域中得到广泛应用。 近年来一些研究发现多肽经离子触发可自组装成为纳米凝胶支架材料,形成与细胞外微环境相似的立体网状结构。双亲多肽是一类简单的人工设计修饰的自组装多肽,由天然氨基酸合成,分子横断面直径小于10 nm,自发组装成具有规则结构的多肽水凝胶,含水量99%,内部孔隙在5-200 nm。它们大多拥有疏水的尾部和亲水的头部。在通常的N-C型多肽序列中大多数多肽疏水部在N端,亲水部在C端。这类多肽的结构和化学特性都和多肽表面活性位点相关。多肽在水溶液中能够形成具有良好秩序的纳米结构,包括多肽双分子层、纳米管、纳米棒、纳米囊和微粒等。自组装多肽材料显示了对环境条件的敏感性,如pH值、温度、离子强度、离子种类、细胞培养介质和光等都可以诱导其发生自组装或改变其状态。多肽RADA16-I(分子式Ac(RADA)4CONH2)是人工设计合成的多肽,它在一定条件下可自组装形成具有β-折叠结构的纳米纤维材料,这种纤维材料可以促进细胞生长、损伤组织修复等,见图2。"
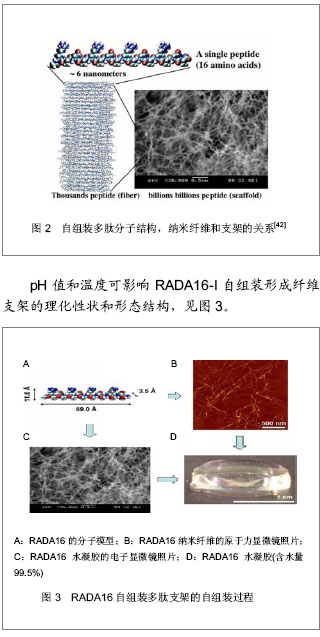

当多肽暴露于pH值为1.0-4.0的环境时可自组装形成典型的β-折叠状结构并形成相当长度的纳米纤维。双亲多肽的尾部通常由3-9个无极性的氨基酸(G,A,V,I,L,P,F)组成,这些氨基酸的大小、形状和疏水性各不相同,使得多肽特性不同。多肽的尾部也可以由12-16个碳的酰基链组成,或者由酰基链和无极性氨基酸共同组成。一条或多条碳水化合物和亲水多肽序列相连形成的分子类别称为脂肽。这类分子的亲水头部可以由带正电荷的氨基酸(H,K,R)或带负电荷的氨基酸(D,E)或者两者兼有所构成。通常情况下尾部越长多肽的溶解性越差。另一方面,随着尾部长度的减小,多肽的溶解度增加,多肽聚集的趋势减小。但尾部长度的减小可通过增加主链中疏水氨基酸或酰基支链获得补偿,将多肽溶解性维持在正常范围。此外,影响自组装多肽亲水性的除了多肽尾部长度外还有其分子横断面的直径。多肽不溶的主要问题是形成二级结构,这在有多重疏水残基的肽中更显著,残基Ala,Cys,Ile,Leu,Met,Phe和Val将全增加多肽的溶解难度。盐会促进二级结构形成,先在无菌蒸馏水或去离子水中溶解多肽,如需要增加溶解率可用声处理。溶解仍有问题,加少量稀乙酸(10%)或氨水会便于溶解。这些方法不溶的多肽,需要DMF、脲、guanidiniam chloride或acetonitnle来溶解,这些溶剂可能某些实验有不良反应,设计多肽时应该注意到这点。自组装多肽的带电基团在多肽中的位置还可以影响多肽功能,在多肽链中的位置不同导致多肽的功能也不尽相同。多肽长度则取决于多肽序列和多肽尾部的选择。多肽序列和酰基不同结构可导致自组装过程中多肽之间相互作用和自组装多肽纳米纤维支架结构上的差异。 孙丽娟等[8]研究了氨基酸序列和组装时间对多肽二级结构和自组装形成纳米结构的影响。非结晶区序列插入RADA16-1后,R1(n-RADARADAGGASRA DARADA-c)和R2(n-RADARADAGPGGYRADARA DA-c)形成的长度仅达200nm的短纳米纤维和球状纳米结构。随着时间的延长,R1和R2形成的β-折叠的含量升高,纤维变长变宽,R1形成数量少但长达几十微米的纤维,R2形成约1 μm但数量多的纤维。通过改变这些条件可以达到控制自组装形成的纳米结构的目的。 多肽特定的残端或侧链基团可使其在自组装后具备特定的功能。脯氨酸残端和其他氨基酸相比具有刚性构象,这在发卡结构、α-螺旋的开端和β-折叠的边缘很常见。由于这种优点,脯氨酸被应用在自组装多肽分子的内部折叠。利用脯氨酸制造具有发卡结构的多肽,Schneider等[7]在这方面做了大量工作,这类自组装多肽被用于药物控释和细胞培养,通常还具有一定的抗菌活性。此外,生物功能基团(如生物素、细胞黏附肽RGDS)应用在多肽中,这些生物活性基团的应用可导致多肽的新功能,在自组装多肽领域有广阔的应用空间。自然界的生物大分子(如蛋白质)中包含一些最具有活性的小分子多肽,这些多肽决定了生物大分子的功能,通过对这些小分子功能多肽进行特别地修饰,使其能够借助静电、疏水键等分子间的作用力,自发地形成规则的结构,形成有功能的多肽支架,新形成的纳米纤维支架不仅具备原生物大分子的生物学功能,而且由于结构的紧凑使其生物学活性有所提高。修饰后的自组装多肽由于其出色功能和生物相容性,已作为优良的纳米材料应用于药物控释、基因传递、稳固膜蛋白、3D细胞培养和组织工程中等领域[1]。 2.3 自组装多肽纳米纤维支架在神经组织工程中的应用[24-31] 随着生物技术、基因工程、材料技术和合成技术的发展,研究人员希望通过体外模拟组织的再生来修复损伤组织,研究难点在于寻找合适的基质支持材料。目前常用的基质材料如透明质酸、壳聚糖、胶原衍生物及纤维蛋白等,虽具备一定促进细胞黏附、生长和分化的作用,但与细胞外微环境的纳米结构仍有一定差异,而且其稳定细胞外微环境和调控细胞生物活性的能力较低,这已成为制约组织工程发展的难点问题。 在神经系统中神经细胞或胶质细胞的变性,或者任何神经组织的细胞外基质的改变都会导致多种临床病变。神经组织修复是一项令人畏惧的挑战,因 为几乎所有神经损伤都会导致不可逆的神经功能缺失[5]。组织工程是目前研究神经损伤修复的一个重要手段,方法是将神经干细胞接种于适宜生物材料中,随后移植至受损神经组织,修复损伤的神经组织。神经组织工程的目标是借助生物工具(正常的基因工程细胞和细胞外微环境类似物)设计出生物材料支架,对损伤神经组织进行有效地修复。神经细胞在体内包被、浸润、生长于细胞外微环境中,细胞外微环境中含有大量层粘连蛋白,可为神经细胞的黏附、生长、迁移和分化提供构架支撑和活性调节,并使神经前体细胞向神经元分化,增强神经元黏附和引导神经轴突生长。来自细胞外微环境的生物信号对神经细胞的存活和功能起到关键作用。Matson等[2]证实了自组装多肽对细胞间信号传导的有效性和可靠性。 Yang等[17]研究了纳米纤维支架对神经干细胞的影响,结果显示无方向性的纳米纤维(150-350 nm)不仅可以支持神经干细胞黏附,而且可以促进神经干细胞分化。他们将这一发现归因于纳米纤维的无序性和表面积体积比高。Yang等又进一步研究了均衡有序的纳米纤维在组织工程中的表现,结果显示神经干细胞在结构规则的纳米纤维支架上生长较好,轴突沿有序的纳米纤维方向伸长。体外实验的满意结果让研究人员进而开始支架在体内实验。Tysseling- Mattiace等[25]将含有IKVAV自组装多肽的两亲性分子在一定离子条件下使其自组装成三维纳米纤维,并将其注入脊髓损伤动物模型,实验结果表明自组装多肽可抑制神经胶质瘢痕的形成,促进少突胶质细胞增殖,并使神经元轴突延伸,有利于损伤脊髓的再生修复。 Semino等[23]设计了一种自组装多肽支架,研 究3D细胞培养和细胞捕获,他们将海马和齿状回的薄层切片贴附于自组装纳米纤维支架表面培养,在接触面神经干细胞和神经祖细胞发生迁移并被纤维支架捕获。培养1周以后,迁移进支架的细胞深度为400-500 μm。被捕获的细胞用于新的培养并获得满意结果,作者将结果归因于自组装多肽类似体内细胞外微环境的结构。实验还为神经祖细胞的体外分离培养提供了一种新的方法。Guo等[22]则从绿色荧光蛋白转基因小鼠中分离出神经祖细胞和许旺细胞,并将两种细胞在自组装多肽支架共培养后注入脊髓背侧柱横断小鼠动物模型,研究证实自组装多肽支架可促进神经元细胞、毛细血管和轴突的生长。"

| [1] Zhao X,Pan F,Xu H, et al. Molecular self-assembly and applications of designer peptide amphiphiles.Chem Soc Rev. 2010;39(9):3480-3498. [2] Matson JB,Stupp SI.Self-assembling peptide scaffolds for regenerative medicine.Chem Commun.2012;48:26-33. [3] Li WJ,Tuan RS. Fabrication and application of nanofibrous scaffolds in tissue engineering. Curr Protoc Cell Biol. 2009; Chapter 25:Unit 25.2. [4] Wang B, Shao Z. Application of self-assembling peptide nanofiber scaffold in nerve tissue engineering.Zhongguo Xiu Fu Chong Jian Wai Ke Za Zhi. 2009;23(7):861-863. [5] Vasita R,Katti DS. Nanofibers and their applications in tissue engineering. Int J Nanomed.2006;1(1): 15-30. [6] Dagdas YS,Tombuloglu A,Tekinay AB,et al.Interfiber interactions alter the stiffness of gels formed by supramolecular self-assembled nanofibers.Soft Matter. 2011; 7:3524-3532. [7] Schneider JP,Pochan DJ,Ozbas B,et al.Responsive Hydrogels From the Intermolecular Folding and Self-Assembly of a Designed Peptide. J Am Chem Soc. 2002; 124:15030-15037. [8] 孙丽娟,赵晓军.氨基酸序列和时间对短肽纳米纤维形成的影响[J].生物医学工程学杂志, 2009,26(6):1276-1280. [9] Jackson AR,Yuan TY,Huang CY,et al. Effect of compression and anisotropy on the diffusion of glucose in annulus fibrosus.Spine (Phila Pa 1976) .2008;33(1):1-7. [10] Cormier AR,Ruiz-Orta C,Alamo RG,et al.Solid state self-assembly mechanism of RADA16-I designer peptide. Biomacromolecules. 2012;13(6):1794-1804. [11] Sun L,Zhao X.A self-assembling peptide RADA16-I integrated with spider fibroin uncrystalline motifs.Int J Nanomedicine. 2012;7:571-580. [12] Cheng L,Englander O,Paravastu A,et al.An effective continuum approach for modeling non-equilibrium structural evolution of protein nanofiber networks. J Chem Phys.2011; 135(5):055102. [13] Ye Z,Zhang H,Luo H,et al.Temperature and pH effects on bio- physical and morphological properties of self-assembling peptide.RADA16-I.J Pept Sci.2008;14:152-162. [14] Mata A,Hsu L,Capito R,et al. Micropatterning of bioactive self-assembling gels. Soft Matter.2009;5:1228-1236. [15] Navarro-Alvarez N,Soto-Gutierrez A,Rivas-Carrillo JD,et al. Self-Assembling Peptide Nanofiber as a Novel Culture System for Isolated Porcine Hepatocytes. Cell Transplantation. 2006;(15): 921-927. [16] Zhang S,Gelain F,Zhao X.Designer self-assembling peptide nanofiber scaffolds for 3D tissue cell cultures. Semin Cancer Biol.2005;15(5):413-420. [17] Yang SH,Wu CC,Shih TT,et al. Three-dimensional culture of human nucleus pulposus cells in fibrin clot: comparisons on cellular proliferation and matrix synthesis with cells in alginate. Artif Organs.2008;32(1): 70-73. [18] 黄任平, 宋纯, 张增岭, 等. 3D自组装肽纳米纤维支架对胰岛细胞分泌功能的影响[J].中国组织工程研究与临床康复,2011, 15(42): 7863-7867. [19] Wang B,Wu Y,Shao Z,et al.Functionalized self-assembling peptide nanofiber hydrogel as a scaffold for rabbit nucleus pulposus cells.J Biomed Mater Res A. 2012;100(3):646-653. [20] Genové E,Shen C,Zhang S,et al. The effect of functionalized self-assembling peptide scaffolds on human aortic endothelial cell function. Biomaterials. 2005; 26(16): 3341-3351. [21] Mi K,Wang G,Liu Z,et al.Influence of a Self-Assembling Peptide,RADA16,Compared with Collagen I and Matrigel on the Malignant Phenotype of Human Breast-Cancer Cells in 3D Cultures and in vivo. Macromol Biosci. 2009;9: 437-443. [22] Guo J,Su H,Zeng Y,et al.Reknitting the injured spinal cord by self-assembling peptide nanofiber scaffold. Nanomedicine. 2007;3(4):311-321. [23] Semino CE,Kasahara J,Hayashi Y,et al. Entrapment of migrating hippocampal neural cells in three-dimensional peptide nanofiber scaffold.Tissue Eng.2004;(10):643-655. [24] Holmes TC,Lacelle SD,Su X,et al.Extensive neurite outgrowth and active synapse formation on self- assembling peptide scaffolds.Proc Natl Acad Sci U S A.2009;97(12): 6728-6733. [25] Tysseling-Mattiace VM,Sahni V,Niece KL,et al. Self-assembling nanofibers inhibit glial scar formation and promote axon elongation after spinal cord injury. J Neurosci. 2008;28(14):3814-3823. [26] Moradi F,Bahktiari M,Joghataei MT,et al. BD PuraMatrix peptide hydrogel as a culture system for human fetal Schwann cells in spinal cord regeneration. J Neurosci Res.2012;90(12):2335-2348. [27] Leung GK,Wang YC,Wu W.Peptide nanofiber scaffold for brain tissue reconstruction. Methods Enzymol.2012; 508: 177-190. [28] Liedmann A,Rolfs A,Frech MJ.Cultivation of human neural progenitor cells in a 3-dimensional self-assembling peptide hydrogel.J Vis Exp.2012;(59):e3830. [29] Cunha C,Panseri S,Villa O,et al. 3D culture of adult mouse neural stem cells within functionalized self-assembling peptide scaffolds. Int J Nanomedicine. 2011;6:943-55. [30] Cigognini D,Satta A,Colleoni B,et al.Evaluation of early and late effects into the acute spinal cord injury of an injectable functionalized self-assembling scaffold. PLoS One. 2011; 6(5):e19782. [31] Matson JB,Newcomb CJ,Bitton R,et al.Nanostructure-templated control of drug release from peptide amphiphile nanofiber gels. Soft Matter.2012;8(13):3586-3595. [32] Kim JH,Jung Y,Kim BS,et al.Stem cell recruitment and angiogenesis of neuropeptide substance P coupled with self-assembling peptide nanofiber in a mouse hind limb ischemia model.Biomaterials.2013;34(6):1657-1668. [33] Wang T,Zhong X,Wang S,et al. Molecular Mechanisms of RADA16-1 Peptide on Fast Stop Bleeding in Rat Models.Int J Mol Sci.2012;13(11):15279-15290. [34] Guo HD,Cui GH,Yang JJ,et al.Sustained delivery of VEGF from designer self-assembling peptides improves cardiac function after myocardial infarction. Biochem Biophys Res Commun. 2012;424(1):105-111. [35] Chen K,Sahoo S,He P,et al.A hybrid silk/RADA-based fibrous scaffold with triple hierarchy for ligament regeneration.Tissue Eng Part A.2012;18(13-14):1399-1409.
[36] Liu J,Zhang L,Yang Z,et al.Controlled release of paclitaxel from a self-assembling peptide hydrogel formed in situ and antitumor study in vitro. Int J Nanomedicine. 2011;6: 2143-2153. [37] Liu X,Wang X,Horii A,et al.In vivo studies on angiogenic activity of two designer self-assembling peptide scaffold hydrogels in the chicken embryo chorioallantoic membrane. Nanoscale. 2012;4(8):2720-2727. [38] Nishimura A,Hayakawa T,Yamamoto Y,et al.Controlled release of insulin from self-assembling nanofiber hydrogel, PuraMatrix™: application for the subcutaneous injection in rats. Eur J Pharm Sci.2012;45(1-2):1-7. [39] Kohgo T,Yamada Y,Ito K,et al. Bone regeneration with self-assembling peptide nanofiber scaffolds in tissue engineering for osseointegration of dental implants.. Int J Periodontics Restorative Dent.2011;31(4):e9-16. [40] Allen P,Melero-Martin J,Bischoff J,et al.Type I collagen, fibrin and PuraMatrix matrices provide permissive environments for human endothelial and mesenchymal progenitor cells to form neovascular networks. J Tissue Eng Regen Med. 2011;5(4): e74-86. [41] Yokoi H, Kinoshita T,Zhang S.Dynamic reassembly of peptide RADA16 nanofiber scaffold. Proc Natl Acad Sci USA.2005; 102(24):8414-8419. [42] Schneider A, Garlick JA, Egles C.Self- assembling peptide nanofiber scaffolds accelerate wound healing.PLoS One. 2008;3(1):e1410. |
| [1] | Li Xuanze, Shu Liping, Chen Jiao, Sun Yu, Zou Qiang, Wang Weiyu, Liu Jun, Yang Long, Ma Minxian, Ye Chuan. Preparation of sodium alginate-hydroxyapatite-polyethylene glycol composite hydrogel scaffold and its biocompatibility [J]. Chinese Journal of Tissue Engineering Research, 2019, 23(26): 4230-4236. |
| [2] | He Xue-feng, Xiong Ai-bing. Application and research progress of three-dimensional printing in the field of orthopaedics [J]. Chinese Journal of Tissue Engineering Research, 2017, 21(3): 428-432. |
| [3] | Zhang Bao-hua, Qiu Fu-cheng, Dong Ci1, Han Rui, Zhang Yong-zhi, Liu Hui-miao,Xie Bing-chuan, Zhang Li-na, Wang Wen-ting, Wang Yan-yong, Zhang Zhen-qing, Gu Ping,Yan Bao-yong. Neural stem cell transplantation for central nervous system diseases via the cerebrospinal fluid [J]. Chinese Journal of Tissue Engineering Research, 2014, 18(6): 974-978. |
| [4] | Nie De-zhi, Wan Ying, Ben Liang, Wang Ying-jun, Liu Xiang-zhu, Wang Li-hui, Li Chao, Zhang Shi-dong. Stem cell tumorigenicity in Balb/c nude mice [J]. Chinese Journal of Tissue Engineering Research, 2014, 18(6): 888-893. |
| [5] | Wu Yue-kui, Wang Shang-wu, Ma Jian-hua, Yi Bo, Gao Bing-bing, Qin Jia-zhen, Yang Zhi-jun, Dai Yi-wu. Umbilical cord blood neural stem cells for obsolete spinal cord injury [J]. Chinese Journal of Tissue Engineering Research, 2014, 18(41): 6678-6683. |
| [6] | Li Hui-li, Du Cheng-fen, Zheng Hong-mei, Hou Ping-zhi, Wang Yun, Xiang Zi-jun, Lv Gui-li, Li Meng, Yu Hai-qin, Chen Shan-shan. Bone marrow mesenchymal stem cells for repair of spinal cord injury: how to promote axonal regeneration? [J]. Chinese Journal of Tissue Engineering Research, 2014, 18(41): 6703-6707. |
| [7] | Liu Bai-yan, Yu Yue, Yi Jian, Chen Xue-mei, Cai Guang-xian. Culture and biological characteristics of neural stem cells from caveolin-1 knockout embryonic mice [J]. Chinese Journal of Tissue Engineering Research, 2014, 18(23): 3739-3744. |
| [8] | Lu Feng, Zhang Hong-tu, Ma Shu-you. Drug release characteristics of gatifloxacin-poly sebacic anhydride local controlled release system [J]. Chinese Journal of Tissue Engineering Research, 2013, 17(29): 5351-5356. |
| [9] | Xian Yuan-fang, Wang Wen-ting, Yu Wei, Tu Li-hui, Wang Sheng-hai, Zou Cheng, Min Xiao-feng. Preparation of gelatin-magnetic micro-capsules by condensation method [J]. Chinese Journal of Tissue Engineering Research, 2013, 17(29): 5357-5363. |
| [10] | Ma Yong-fu, Liu Yang, Guo Jun-tang, Zhang Tao, Liang Chao-yang. Degradable properties of biodegradable composite stents in the trachea [J]. Chinese Journal of Tissue Engineering Research, 2013, 17(29): 5371-5378. |
| [11] | Li Wen-cheng. Antibiotic bone cement and renovation after artificial joint replacement [J]. Chinese Journal of Tissue Engineering Research, 2013, 17(29): 5409-5414. |
| [12] | Zhan Liu, Xie Shu-juan, Pan Wei-hong. Three-dimensional finite element analysis of prosthesis stress variation [J]. Chinese Journal of Tissue Engineering Research, 2013, 17(29): 5403-5408. |
| [13] | Yao Jin-feng, Zhang Xiao-wei, Zhou Qi, Zheng Cang-shang, Liang Zhi-gang, Bao Chong-yun. Ectopic bone formation in adipose-derived mesenchymal stem cell-seeded osteoinductive calcium phosphate scaffolds [J]. Chinese Journal of Tissue Engineering Research, 2013, 17(29): 5261-5268. |
| [14] | Ye Peng, Tian Ren-yuan, Huang Wen-liang, Ma Li-kun, Deng Jiang. Silk fibroin/chitosan/nano hydroxyapatite complicated scaffolds for bone tissue engineering [J]. Chinese Journal of Tissue Engineering Research, 2013, 17(29): 5269-5274. |
| [15] | Yin Xiao-peng, Xu Hui-fen, He Hui-yu. Comparison of the biocompatibility of three kinds of antigen-extracted xenogeneic cancellous bone matrices [J]. Chinese Journal of Tissue Engineering Research, 2013, 17(29): 5275-5281. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||