Chinese Journal of Tissue Engineering Research ›› 2019, Vol. 23 ›› Issue (14): 2279-2284.doi: 10.3969/j.issn.2095-4344.1639
Previous Articles Next Articles
Research progress of myocardial scaffolds in the treatment of myocardial infarction
Zhao Liang1, 2, Qiu Xiaona3, 4, Li Xiafei2
- 1College of Engineering, Peking University, Beijing 100871, China; 2College of Life Sciences and Technology, Xinxiang Medical University, Xinxiang 453003, Henan Province, China; 3Central Laboratory, Datong Third People’s Hospital, Datong 037008, Shanxi Province, China; 4First Clinical College, Shanxi Medical University, Taiyuan 030001, Shanxi Province, China
-
Received:2018-10-15 -
Contact:Zhao Liang, College of Engineering, Peking University, Beijing 100871, China; College of Life Sciences and Technology, Xinxiang Medical University, Xinxiang 453003, Henan Province, China -
About author:Zhao Liang, MD, Master’s supervisor, College of Engineering, Peking University, Beijing 100871, China; College of Life Sciences and Technology, Xinxiang Medical University, Xinxiang 453003, Henan Province, China -
Supported by:the Second University Life Science League Project, No. SKYLS017 (to ZL); the Key Research Project of Higher Education in Henan Province, No.17A180034 (to ZL)
CLC Number:
Cite this article
Zhao Liang, Qiu Xiaona, Li Xiafei. Research progress of myocardial scaffolds in the treatment of myocardial infarction[J]. Chinese Journal of Tissue Engineering Research, 2019, 23(14): 2279-2284.
share this article
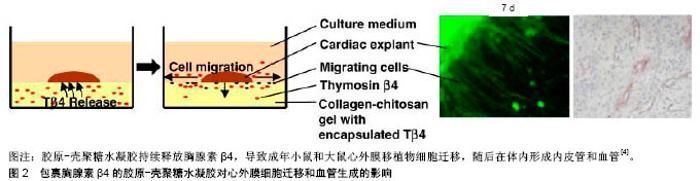
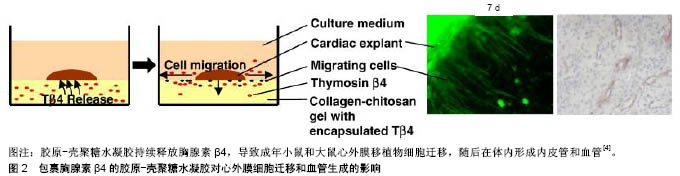
2.1 天然生物材料 2.1.1 胶原/Matrigel 胶原是一种天然生物材料,是细胞外基质的主要成分,起到连接细胞和组织的作用,被广泛用于各类组织工程的研究中。应用液态胶原制备的支架具有很好的弹性,可促进细胞之间的整合。在中国,有学者首次以液态胶原为支架复合Matrigel,证明了以液态胶原为支架构建的心肌组织是一种较好的生物材料。为探讨胶原生物材料的组成和交联如何影响其物理性质,Davidenko等[1]对由胶原蛋白、明胶(部分变性胶原蛋白)和50%胶原-50%明胶混合物制成的支架进行比较,结果表明无论使用何种成分的支架,用于交叉连接胶原蛋白支架的碳二酰亚胺含量减少了10倍,游离胺组(主要是胶原赖氨酸残基)含量显著增加(几乎4倍),而不影响所合成支架的力学性能和稳定性,导致了类似于原生细胞对胶原支架的附着。研究表明,碳二酰亚胺浓度变化提供了一种简单的方法来调节支架材料的物理和生物特性。 2.1.2 纤维蛋白 纤维蛋白是天然的生物多聚体,可促进伤口愈合和组织再生,具有很好的生物相容性。纤维蛋白凝胶由纤维蛋白原与凝血酶相互作用生成,被广泛应用于骨、软骨、心肌组织等领域。有学者首次将纤维蛋白凝胶与骨骼肌成肌细胞复合注射到大鼠心肌梗死部位,5周后的结果提示,大鼠心肌梗死面积减少且有新生血管的生成。近期Tang等[2]使用喷雾系统(一种双腔注射器)使富含血小板的血浆和含钙介质通过原位聚合形成血小板纤维蛋白凝胶,以微创的方式涂撒在心脏表面,研究表明这种血小板纤维蛋白凝胶可释放生长因子,减弱不良的左心室重塑,抑制心肌细胞凋亡,促进了心肌修复,减轻了心肌梗死后的心脏功能障碍。 2.1.3 壳聚糖 壳聚糖作为一种天然的线性多糖,能够模仿细胞外基质,可携带多种生长因子,其水凝胶作为支架蛋白已被广泛应用于骨、软骨、皮肤、心血管、神经及角膜组织等组织工程。Xu等[3]运用温敏性壳聚糖水凝胶黏附间充质干细胞注射到小鼠梗死心肌内,进而对植入的间充质干细胞存活进行了评估,结果表明壳聚糖水凝胶在缺血性心脏中增加了移植物的大小和细胞保留,促进了间充质干细胞分化为心肌细胞,增加了间充质干细胞对新生血管形成的影响。此外,壳聚糖水凝胶增强了间充质干细胞对心肌梗死区心脏功能和血流动力学的改善,提示壳聚糖水凝胶是一种合适的材料,可以将间充质干细胞输送到梗死的心肌。同样,有研究将胚胎干细胞与温敏性壳聚糖水凝胶支架结合,同样表明壳聚糖水凝胶使细胞留存率增高,心脏功能得到改善。Chiu等[4]研发了一种将胸腺素β4(一种43氨基酸的肽,诱导对血管稳定所必需的内皮细胞和平滑肌细胞分化,保护心脏)封装起来的壳聚糖水凝胶,使胸腺素β4在28 d内被控制释放,引起局部和长期效果。与壳聚糖水凝胶相比,控制释放胸腺素β4的壳聚糖复合水凝胶,能够促进心外膜细胞迁移和血管生成,见图2。 2.1.4 透明质酸 透明质酸由Meyer等首次在牛眼玻璃体中提取、分离、纯化得到的,广泛分布于各种脊椎动物的细胞间质中,具有良好的生物相容性及可降解性,被广泛应用于众多领域。有研究通过大鼠心肌梗死模型实验得出,注射低分子质量的丙烯酸透明质酸交联凝胶可促进细胞的增殖和血管生成。天然的透明质酸易降解,但可通过化学修饰来稳定其物理性质,且可与其他心机支架材料复合使用,取长补短,发挥更大的优势。 2.1.5 脱细胞心肌材料 心肌再生的成功临床应用,将取决于建立生理组织结构的能力及植入后即刻的移植灌注。天然人心脏基质提供了生理微结构和宏观结构、细胞外基质及可灌注的分层血管床,作为组织工程心肌的基础支架。Guyette等[5]基于脱细胞处理办法获得了具有生物相容性的人脱细胞心脏支架,保存了细胞外基质成分、结构和可灌注的冠状血管。然后将由非转基因人诱导的多能干细胞衍生的心肌细胞填充心脏基质,产生三维的人工心脏组织,证明了天然心脏细胞外基质支架可维持基质成分和结构,以支持人类诱导多能干细胞衍生的心肌细胞接种和植入,成功实现功能复杂的人类心肌样组织构建。Sánchez等[6]制备了脱细胞的人工心脏支架,保持其三维结构和血管,并重新种植细胞。结果显示,去除细胞后保留了三维心脏宏观和微观结构,天然血管网络处于可灌注状态。脱细胞的人工心脏支架了促进干细胞向心肌细胞的分化,并将存在的心肌细胞组织成新生的肌肉,显示电耦合。这些发现为制造人类心脏移植或治疗心血管疾病奠定了基础。 2.2 人工合成材料 目前常用的人工合成材料有聚酯类材料及纳米材料,纳米材料又有纳米纤维、纳米粒子、纳米管、纳米晶体等,其中又以碳纳米管研究最为热点。该类材料的降解速度和强度可调节,易构建高孔隙率三维支架,但材料本身对细胞亲和力弱,往往需要引入适量能促进细胞黏附和增殖的活性基团、生长因子或黏附因子等[7]。 2.2.1 聚酯类合成材料 聚癸二酸甘油酯是一种生物可降解的高分子聚合体,有良好的组织相容性和生物降解性。聚癸二酸甘油酯支架机械性能与机体软组织相似,依从性好,以表面侵蚀方式降解,不伴有膨胀、变形和周围炎症反应,纤维变性轻,与多种细胞相容性好。多数研究者注重以聚癸二酸甘油酯为基质研发心肌补片,向梗死区输送健康心肌细胞,但聚癸二酸甘油酯基质的硬度与天然心肌组织不相配。Engelmayr等[8]利用微加工技术在聚癸二酸甘油酯中制造出一种类似手风琴的的蜂窝组织结构,这种结构能产生多孔的、弹性的三维支架,具有可控制的刚度和各向异性,克服了之前支架的结构机械限制,促进与心脏细胞一致的移植物形成,使其机械性质更接近原生心肌。Boothe等[9]在平面聚丙烯酰胺水凝胶表面,从1-25 kPa培养了新生大鼠心室肌细胞,发现以9 kPa弹性模量水凝胶培养的心肌细胞与原生心肌相似,具有最长的动作电位持续时间。此外研究表明,基质硬度对培养的新生大鼠心肌细胞动作电位长度和钙通量有显著影响,这些结果可解释在心肌梗死后心脏缺血区细胞外基质弹性模量变化引起的心肌细胞功能差异。Marsano等[10]研究了一种三维弹性体支架的初始刚度-高孔聚脂(甘油塞巴酸酯)-在灌注8 d的心肌细胞功能组装上的效果,研究结果表明工程心脏结构的收缩功能与支架低抗压刚度呈正相关。Castellano等[11]利用电纺丝技术制备了聚(3-羟基丁酸)、聚(e-己内酯)、蚕丝、聚乳酸、聚酰胺支架,通过与非交联胶原膜控制材料在体内外免疫应答及心脏功能等方面进行对比。结果显示,聚(3-羟基丁酸)和聚(e-己内酯)聚合物可最大限度地促进间充质干细胞、心肌细胞和心肌成纤维细胞的黏附和生长。将支架植入梗死大鼠心脏时,胶原膜、聚(e-己内酯)和聚(3-羟基丁酸)都降低了负重构,但只有聚(3-羟基丁酸)诱导了显著的血管生成,表明聚(3-羟基丁酸)是心脏修复的优越基质。但不同的聚乳酸和聚合L-酪氨酸是目前报道的唯一被用作支架材料的聚合材料,在临床试验中取得了令人鼓舞的结果[12]。 2.2.2 纳米材料 碳纳米管由日本的Iijima博士于1991年发现,属于富勒烯家族,单个石墨烯片产生单壁碳纳米管,而多个石墨烯片组成多壁碳纳米管[13]。碳纳米管以SP2杂化方式形成独特的六角形碳原子结构单位,具有良好的弹性、热稳定性、耐酸碱性及导电性。2010年,有学者发现碳纳米管具有潜在致癌作用,可能是由于巨噬细胞吞噬碳纳米管释放氧自由基导致炎症反应。2011年,有研究发现多壁碳纳米管对孕鼠有严重的胎盘毒性,随后的几年里,研究人员致力于将碳纳米管与其他生物材料结合使用来降低碳纳米管的生物毒性。 2.3 复合材料 心肌细胞由于其独特的自主收缩性及导电性,要求制备心肌支架的材料除具有一般支架材料的性能外,还要有可伸性、弹性性能及导电性能。因此,组织工程心肌支架材料的要求是多样性的。 目前已有大量的天然生物材料和合成聚合物被用来制作心脏组织支架,但每一种都有各自的优缺点。天然生物材料具有良好的组织细胞相容性、免疫原性及可降解性,但机械强度不够;合成聚合材料虽然具有更强的强度,但存在生物材料对细胞亲和力较差、相容性不高等缺点。因此越来越多的研究者将目光投向了2种材料结合所形成的复合材料,理论上可取长补短,创造了无数新颖的支架设计。目前有薄膜沉积、网孔、粉体、微珠、水凝胶、纳米模式、烧结、电纺、编织、3D打印、冻干、化学和UV交联、相分离等方式制备复合材料[14]。其中通过调整静电纺丝设备的参数及对静电纺丝设备的简单改进,能制备多层纳米纤维及具有一定取向度的纳米纤维[15],使得采用静电纺丝技术制备纳米纤维成为目前研究的热点。3D打印技术是目前最前沿的制作工艺技术,3D打印指的是利用人体解剖结构的影像学数据进行重建,将数据输入3D打印机中打印出结构模型,能够更加精准地制作复杂精细的生物3D结构,在打印材料中可添加其他生物、化学因子,使细胞可控地分布于支架中,能更有效地促进功能组织的再生。目前该打印技术已在牙科、颌面、肌肉和骨骼领域积累了成功经验[16]。已有研究表明,复合材料可能是最好的3D打印类似细胞外基质支架材料[17-19],但在心脏组织工程方面尚处于研究当中。3D打印与其负载的材料密切相关,目前人们通过对凝胶材料的变性以实现更好的性能,如在明胶的细胞结合域RGD(Arg-Gly-Asp)序列上引入甲基丙烯酸酯分子侧基,形成甲基丙烯酸酯明胶。此外,甲基丙烯酸酯明胶/聚乙二醇二丙烯酸酯/海藻酸钠、胶原/海藻酸钠、琼脂/聚乙二醇、海藻酸钠/聚丙烯酰胺、海藻酸钠/甲基纤维素等也都被用于3D生物打印研究。 Efraim等[20]利用天然生物材料的生物活性和心脏细胞外基质的独特结构,研发了一种基于溶解的脱细胞猪心脏细胞外基质与天然生物材料京尼平或壳聚糖复合形成的可注射性支架。在研究中,用天然材料京尼平和壳聚糖对猪心脏细胞外基质进行了脱胶处理,保存了细胞外基质的重要成分,如胶原蛋白Ⅰ、Ⅲ和葡萄糖胺聚糖。组织学分析结果表明,壳聚糖浓度越高,细胞的吸收和凝胶降解能力越强。既表明了凝胶成分微调的重要性,也表明了以猪心脏细胞外基质为基础的凝胶复合天然生物材料具有巨大的治疗意义。有研究表明,只要简单地在材料上创建纳米级的表面形貌,细胞存活率就会显著增加[21]。 Martins等[22]应用碳纳米纤维作为掺杂材料,开发了一种高导电的壳聚糖基复合材料。以壳聚糖为基础,通过沉淀制备壳聚糖/碳复合材料支架,支架具有完全连通的高度孔隙,且碳纳米纤维在壳聚糖基质中均匀分布,将支架植入新生大鼠心脏细胞,经过14 d的培养,整个结构体的支架孔充满了细胞。与壳聚糖支架细胞相比,壳聚糖/碳结构中细胞的代谢活性显著提高同时,也导致了肌肉收缩和电耦合的心脏特异性基因表达增加,研究表明将碳纳米纤维掺入多孔壳聚糖支架,可提高心肌组织结构的性能,增强细胞间电信号的传递。 陈焱等[23]利用静电纺丝技术制造出聚己内酯纳米纤维立体支架,接种小鼠诱导多能干细胞培养,探讨支架材料对小鼠诱导多能干细胞向心肌特异性分化的作用,结果表明心肌特异性蛋白cTnT、MLC2和MHC在分化后的诱导多能干细胞中均有不同程度的表达,证实了诱导多能干细胞在聚己内酯纳米纤维立体支架上可分化出心肌细胞,但所分化的心肌细胞不够成熟,可在分化过程中添加细胞因子或化学诱导剂,也可采用细胞外基质立体培养或延长培养时间来促细胞成熟。刘耀文 等[24]向聚乳酸溶液中加入不同比例多壁碳纳米管,采用静电纺丝技术成功制备出具有良好力学和导电性能的聚乳酸/碳纳米管复合纤维膜,通过观察心肌细胞在复合纤维膜上的生长行为发现,含3%多壁碳纳米管的支架表现出最佳的力学和导电性能,能够确保心肌细胞的动作电位迅速准确地通过纤维支架进行传导,展示出了较好的黏附性和生长能力,显示了多壁碳纳米管在心肌组织工程应用中具有重要意义。Ahadian等[25]利用双电泳的方法将具有导电性能的碳纳米管垂直排列在甲基丙烯酸酯水凝胶中,与原始的凝胶水凝胶和含有随机分布碳纳米管的凝胶水凝胶相比,凝胶状的碳纳米管水凝胶具有各向异性的电导率和优越的力学性能。在甲基丙烯酸酯水凝胶中,垂直排列碳纳米管上生长的骨骼肌细胞产生的功能性肌纤维,较在水凝胶中被随机分布的碳纳米管和水平排列的碳纳米管所培养的细胞数量要高;此外,由于垂直排列碳纳米管水凝胶的各向异性电导率,在沿排列碳纳米管的方向上施加电刺激后,肌原基因和蛋白表达增多。Sun等[26]将多壁碳纳米管加入胶原水凝胶,研究表明碳纳米管的加入对心肌细胞没有毒性,且增强了细胞的黏附和伸长;可显著改善细胞排列和组装,形成具有较强收缩能力的工程化心脏组织,基于碳纳米管/胶原水凝胶的心脏组织具有更好的功能,可改善细胞排列和心脏结构的性能。Martinelli等[27]研究表明,碳纳米管能够促进心肌细胞成熟。Liu等[28]通过静电纺丝制备了对齐的聚乳酸-乙醇酸共聚物/多壁碳纳米管纤维,提示其在心脏组织工程中具有很大的潜力。 "
| [1] Davidenko N,Schuster CF,Bax DV,et al.Control of crosslinking for tailoring collagen-based scaffolds stability and mechanics. Acta Biomaterialia.2015;25:131-142.[2] Tang J,Vandergriff A,Wang Z,et al.A Regenerative Cardiac Patch Formed by Spray Painting of Biomaterials onto the Heart. Tissue Eng Part C Methods.2017;23(3):146-155.[3] Xu B, Li Y, Deng B,et al.Chitosan hydrogel improves mesenchymal stem cell transplant survival and cardiac function following myocardial infarction in rats. Exp Ther Med.2017;13(2):588-594.[4] Chiu LL, Radisic M.Controlled release of thymosin beta4 using collagen-chitosan composite hydrogels promotes epicardial cell migration and angiogenesis. J Control Release. 2011;155(3):376-385.[5] Guyette JP,Charest JM,Mills RW,et al.Bioengineering Human Myocardium on Native Extracellular Matrix. Circ Res. 2016; 118(1):56-72.[6] Sánchez PL,Fernandez-Santos ME,Costanza S,et al. Acellular human heart matrix: A critical step toward whole heart grafts.Biomaterials.2015;61:279-289.[7] 方易冰,廖斌.心肌组织工程支架材料研究进展[J].中国修复重建外科杂志,2011,4(3):361-364.[8] Engelmayr GC Jr, Cheng M,Bettinger CJ, et al. Accordion-like honeycombs for tissue engineering of cardiac anisotropy. Nat Mater. 2008;7(12):1003-1010.[9] Boothe SD,Myers JD,Pok S,et al.The Effect of Substrate Stiffness on Cardiomyocyte Action Potentials. Cell Biochem Biophys.2016;74(4):527-535.[10] Marsano A,Maidhof R,Wan LQ,et al.Scaffold stiffness affects the contractile function of three-dimensional engineered cardiac constructs. Biotechnol Prog.2010;26(5):1382-1390.[11] Castellano D,Blanes M,Marco B,et al.A comparison of electrospun polymers reveals poly(3-hydroxybutyrate) fiber as a superior scaffold for cardiac repair.Stem Cells Dev. 2014; 23(13):1479-1490.[12] Soares JS,Moore JE Jr.Biomechanical Challenges to Polymeric Biodegradable Stents.Ann Biomed Eng. 2016; 44(2):560-579.[13] Kalbacova M,Broz A,Kong J,et al.Graphene substrates promote adherence of human osteoblasts and mesenchymal stromal cells.Carbon.2010;48(15):4323-4329.[14] Kaiser NJ,Coulombe KL.Physiologically inspired cardiac scaffolds for tailored in vivo function and heart regeneration. Biomed Mater.2015;10(3):034003.[15] Moheman A,Alam MS,Mohammad A,et al.Recent trends in electrospinning of polymer nanofibers and their applications in ultra thin layer chromatography. Adv Colloid Interface Sci. 2016;229:1-24.[16] Giannopoulos AA,Steigner ML,George E,et al.Cardiothoracic Applications of 3-dimensional Printing. J Thorac Imaging. 2016;31(5):253-272.[17] Inzana JA,Olvera D,Fuller SM,et al.3D printing of composite calcium phosphate and collagen scaffolds for bone regeneration. Biomaterials.2014;35(13):4026-4034.[18] Serra T,Planell JA,Navarro M.High-resolution PLA-based composite scaffolds via 3-D printing technology. Acta Biomater.2013;9(3):5521-5530.[19] 曹志强,孙吉鹏,李欣阳,等.3D打印组织工程支架的构建研究进展[J].解放军医药杂志,2016,28(11):1-5.[20] Efraim Y,Sarig H,Cohen Anavy N,et al.Biohybrid cardiac ECM-based hydrogels improve long term cardiac function post myocardial infarction.Acta Biomaterialia. 2017;50: 220-233.[21] Amezcua R,Shirolkar A,Fraze C,et al.Nanomaterials for Cardiac Myocyte Tissue Engineering. Nanomaterials (Basel, Switzerland).2016;6(7):133.[22] Martins AM, Eng G, Caridade SG,et al.Electrically conductive chitosan/carbon scaffolds for cardiac tissue engineering. Biomacromolecules.2014;15(2):635-643.[23] 陈焱,何顺舟,李晓莉,等.静电纺丝聚己内酯纳米纤维支架支持小鼠诱导多能干细胞表达心肌细胞标志物[J].基础医学与临床, 2016,36(4):86-91.[24] 刘耀文,王淑瑶,叶劲松,等.聚乳酸/碳纳米管导电复合纤维用于心肌组织工程的研究[J].化工新型材料, 2016,44(2):216-218.[25] Ahadian S,Ramón-Azcón J,Estili M,et al.Hybrid hydrogels containing vertically aligned carbon nanotubes with anisotropic electrical conductivity for muscle myofiber fabrication.Sci Rep. 2014;4:4271. [26] Sun H,Zhou J,Huang Z,et al. Carbon nanotube-incorporated collagen hydrogels improve cell alignment and the performance of cardiac constructs.Int J Nanomedicine. 2017; 12:3109-3120.[27] Martinelli V,Cellot G,Toma FM,et al.Carbon nanotubes promote growth and spontaneous electrical activity in cultured cardiac myocytes.Nano lett.2012;12(4):1831-1838.[28] Liu Y,Liang X,Wang S,et al. Electrospun Poly(lactic-co-glycolic acid)/Multiwalled Carbon Nanotube Nanofibers for Cardiac Tissue Engineering.J Biomater Tissue Eng. 2016;6(9):719-728. |
| [1] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [2] | Zeng Yanhua, Hao Yanlei. In vitro culture and purification of Schwann cells: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1135-1141. |
| [3] | Xu Dongzi, Zhang Ting, Ouyang Zhaolian. The global competitive situation of cardiac tissue engineering based on patent analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 807-812. |
| [4] | Wu Zijian, Hu Zhaoduan, Xie Youqiong, Wang Feng, Li Jia, Li Bocun, Cai Guowei, Peng Rui. Three-dimensional printing technology and bone tissue engineering research: literature metrology and visual analysis of research hotspots [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 564-569. |
| [5] | Chang Wenliao, Zhao Jie, Sun Xiaoliang, Wang Kun, Wu Guofeng, Zhou Jian, Li Shuxiang, Sun Han. Material selection, theoretical design and biomimetic function of artificial periosteum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 600-606. |
| [6] | Liu Fei, Cui Yutao, Liu He. Advantages and problems of local antibiotic delivery system in the treatment of osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 614-620. |
| [7] | Li Xiaozhuang, Duan Hao, Wang Weizhou, Tang Zhihong, Wang Yanghao, He Fei. Application of bone tissue engineering materials in the treatment of bone defect diseases in vivo [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 626-631. |
| [8] | Zhang Zhenkun, Li Zhe, Li Ya, Wang Yingying, Wang Yaping, Zhou Xinkui, Ma Shanshan, Guan Fangxia. Application of alginate based hydrogels/dressings in wound healing: sustained, dynamic and sequential release [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 638-643. |
| [9] | Chen Jiana, Qiu Yanling, Nie Minhai, Liu Xuqian. Tissue engineering scaffolds in repairing oral and maxillofacial soft tissue defects [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 644-650. |
| [10] | Xing Hao, Zhang Yonghong, Wang Dong. Advantages and disadvantages of repairing large-segment bone defect [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 426-430. |
| [11] | Chen Siqi, Xian Debin, Xu Rongsheng, Qin Zhongjie, Zhang Lei, Xia Delin. Effects of bone marrow mesenchymal stem cells and human umbilical vein endothelial cells combined with hydroxyapatite-tricalcium phosphate scaffolds on early angiogenesis in skull defect repair in rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3458-3465. |
| [12] | Wang Hao, Chen Mingxue, Li Junkang, Luo Xujiang, Peng Liqing, Li Huo, Huang Bo, Tian Guangzhao, Liu Shuyun, Sui Xiang, Huang Jingxiang, Guo Quanyi, Lu Xiaobo. Decellularized porcine skin matrix for tissue-engineered meniscus scaffold [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3473-3478. |
| [13] | Mo Jianling, He Shaoru, Feng Bowen, Jian Minqiao, Zhang Xiaohui, Liu Caisheng, Liang Yijing, Liu Yumei, Chen Liang, Zhou Haiyu, Liu Yanhui. Forming prevascularized cell sheets and the expression of angiogenesis-related factors [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3479-3486. |
| [14] | Liu Chang, Li Datong, Liu Yuan, Kong Lingbo, Guo Rui, Yang Lixue, Hao Dingjun, He Baorong. Poor efficacy after vertebral augmentation surgery of acute symptomatic thoracolumbar osteoporotic compression fracture: relationship with bone cement, bone mineral density, and adjacent fractures [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3510-3516. |
| [15] | Liu Liyong, Zhou Lei. Research and development status and development trend of hydrogel in tissue engineering based on patent information [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3527-3533. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||