Chinese Journal of Tissue Engineering Research
Digital technology in prosthodontics: impression, shade selection, material design and processing
Yu Jia-li, Nie Er-min, Jiang Rui, Zhang Chun-yuan, Huang Zhe-xun, Zhang Yu-hang, Lu Dun-lang
- Department of Stomatology, First Affiliated Hospital of Sun Yat-Sen University, Guangzhou 510080, Guangdong Province, China
-
Received:2018-01-20Online:2018-08-08Published:2018-08-08 -
Contact:Nie Er-min, Attending physician, Department of Stomatology, First Affiliated Hospital of Sun Yat-Sen University, Guangzhou 510080, Guangdong Province, China -
About author:Yu Jia-li, Master, Department of Stomatology, First Affiliated Hospital of Sun Yat-Sen University, Guangzhou 510080, Guangdong Province, China -
Supported by:the Social Development Program of Guangdong Provincial Science and Technology Department, No. 2012B061700066
CLC Number:
Cite this article
Yu Jia-li, Nie Er-min, Jiang Rui, Zhang Chun-yuan, Huang Zhe-xun, Zhang Yu-hang, Lu Dun-lang. Digital technology in prosthodontics: impression, shade selection, material design and processing[J]. Chinese Journal of Tissue Engineering Research, doi: 10.3969/j.issn.2095-4344.0850.
share this article
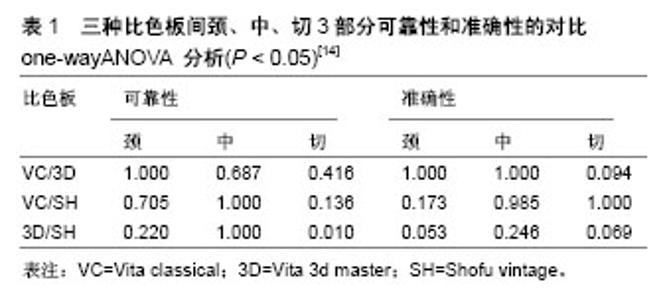
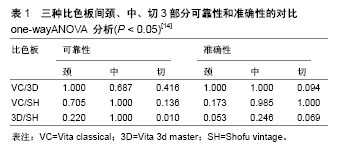
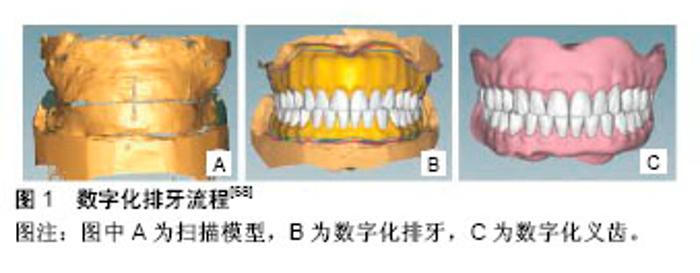
2.1 数字化数据采集 数字化数据采集在口腔修复领域主要包括数字化印模技术(获得口内软硬组织静态形态)和数字化比色技术(获得口内软硬组织以及颜面部色彩信息)等两个方面。 2.1.1 数字化印模技术 数字化印模是指将光学、电子技术及计算机图像识别和处理技术结合在一起,通过口内光学扫描,将获取的光学信号转换为计算机所能识别的电子信号,将实体物体转换为虚拟数字信息,从而获得三维数字模型[4]。目前临床上常用的数字化印模方法分为直接法和间接法。 直接法是通过扫描仪探头直接对牙齿和牙周软硬组织进行近距离扫描并获取数据,然后在计算机上将数据转换为数字化模型,其过程省略了制取印模和灌注模型等步骤,可减少患者口内获取印模时产生的不适感,并能减少印模过程中或翻制超硬石膏模型过程中人为因素所产生的误差,提高了修复操作的效率和精度,它是目前最常使用的方法。直接法主要有非接触式机械扫描和接触式机械扫描[5]。激光扫描是一种非接触式扫描方式,激光探头探测物体或实体模型的完整信息,通过光学感受器将捕捉到的光学信号转换为计算机所能识别的数字化信息,通过处理转换成三维虚拟数字化结构图,它具有速度快、精度高及重建后图像清晰和使用范围广等优点。目前临床上常用的光学扫描方法有云纹相移法、投影光栅直接分析法、莫尔条纹法、数字散斑相关测量法等,临床上常用的有Cerec、iTero、E4D等系统。接触式机械扫描是扫描仪探头直接接触被扫描物体表面进行扫描,选取牙体或石膏模型表面关键点及相应数值作为参考点,将数值输入到计算机进行图像处理,从而获得三维图像,这种扫描方式精度较高,但操作技术较为复杂,且可导致具有弹性的物体表面产生形变。该方法不适用于具有高弹性表面的物体,且相对于光学扫描时间和费用上较高。 间接法是通过扫描临床获取的藻酸盐或硅橡胶印模或石膏模型来获得三维数据,然后通过电脑传输给技工而制作修复体。该方法无论在患者口内获取印模或在转换为超硬石膏阳模的过程中都存在人为因素的干扰,比如调印模材料时操作方法不当或调配比例不当出现气泡,在制取印模时托盘未就位、印模材料未充分覆盖基牙或种植基台及印模材料超过硬化时间等、在灌注石膏模型过程中出现膨胀及气泡等现象,降低了模型的精确度,从而产生一些误差。该方法是在直接法的基础上多了取印模或灌注石膏模型的过程,该过程会增加误差率并增加制作修复体的成本,在未来该方法将被淘汰。 目前临床上有众多学者针对不同的印模方法进行了对照研究。谢轶伦等[6]对5例患者分别进行传统印模法取模及口内扫描技术行数字化印模,最后得出口内直接数字化技术精确性及可重复性高。对于口腔固定修复体,边缘密合性至关重要,与修复体的远期效果有关,边缘密合性差可引起继发龋、牙本质过敏、牙周病等问题,其中印模的质量对修复体边缘密合性高低很关键[7]。国外也有学者对需要烤瓷金属全冠修复的患者分别进行数字化印模和传统印模,实验结果得出相对于传统印模,数字化印模技术修复冠边缘间隙及内冠和预备体间隙较小,临床上可接受[8-9]。在可摘局部义齿方面,目前仅适用于制作肯氏Ⅲ类可摘局部义齿,对于其他类型的牙列缺损或牙列缺失患者,因需制取功能性印模,目前暂不适用[10]。目前比较常用的数字化扫描仪有:LavaTMC.O. S,TRIOS,iTero,CEREC AC Omnicam,CEREC AC Bluecam,E4D等[11]。经大量实验研究与临床应用证明这些扫描仪各有不同的特点,例如CRREC AC Omnicam、TRIOS和iTero系统无需喷雾涂敷,既方便了操作,又提高了精确性;CEREC AC Bluecam、CRREC AC Omnicam和E4D系统有椅旁铣削系统,使数字化修复实现一次性就诊;CEREC AC Bluecam系统拥有防抖系统,提高了扫描的准确性;CEREC AC Omnicam系统的进步在于其真彩三维图像,使医患医技沟通更便捷;LavaTMC.O.S系统具有最小的扫描头,便于在口腔狭小的空间应用符合临床的使用需求[12]。 2.1.2 数字化比色技术 随着材料学的不断发展及人们对美学效果的不断追求,比色在口腔修复操作环节中越来越被大家所重视,其能决定该修复成功与否,尤其是前牙区修复。如果色彩选择不当,会造成修复效果不理想,修复体返工,会对医生和患者造成经济和时间上的浪费。目前临床上常用的比色方法有比色板比色、比色仪比色及使用数码相机拍照等方法。传统的比色方法是目测法,需要借助比色板,该方法操作相对简单,没有经济支出,但易受周围环境、操作者熟练程度等影响,有时需配合使用数码相机进行色彩信息记录。目前临床常用的比色板为VITA3D比色板。随着科技的不断发展及患者对美观要求逐渐提高,口腔数字化比色技术被广泛应用到临床,同时数字比色仪以其快速、量化、客观、准确的优点被多数口腔临床医师所接受。采用数码相机进行色彩采集和传递是比色板比色和比色仪比色的辅助色彩采集手段,对于特殊颜色牙齿(氟斑牙、四环素牙及釉质发育不全等)及特殊牙体形态进行临床补偿,使技工更能清楚了解临床医生所传递过来的信息,使修复体的颜色和形态更能够为患者接受,该方法简单、快捷、经济。但数码相机采集颜色受到多种因素的制约,比如背景颜色、背景灯光及摄影者的技术等因素的影响,往往造成色彩失真。 数字比色技术是通过电脑将比色和配色过程合理配置,通过导入的数据分析得出被测牙的色调、明度、彩度,最后为修复体制作提供瓷粉的配方。数字比色仪器根据测色原理主要分为分光光度计、色度计、数字成像系统3个类型,分光光度计是目前最准确、最灵敏、最有用的数字比色仪器之一[13]。张新媛等[14]通过体外模型来评估分光光度计型比色仪的可靠性和准确性,其对Vita classical、Vita 3d master和Shofu vintage 比色板的测试结果具有更高的可靠性,与对照天然牙更接近,同时患者满意度高,虽然比色过程繁琐一些,但得到的比色结果具有更实用的价值(表1)。另有学者的研究表明相对于传统目测法,数字比色技术更准确,可重复性更高,最终的修复效果使得患者更加满意[15]。"
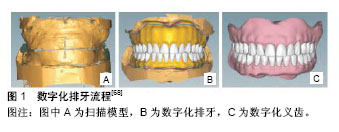
目前临床上较多采用比色板比色,成本低、速度快,对于特殊颜色的患者多配合使用数码相机进行补偿,但对于年轻医师往往因为经验不足,对于色彩的信息捕捉和传递有误差,应多加培训。比色仪比色的结果较为准确,是临床医生较好的选择,但需要临床医生进行专门训练及相关色彩知识的培训,且对于牙体颜色较特殊的患者,在临床上也需要配合使用数码相机和比色板。 2.2 数字化数据传递 传统的信息传递过程是临床医生在获得实体模型及色彩记录后,通过在修复体加工设计单上填写相应的设计方案及患者的临床要求,传递给修复体制作单位,来完成数据信息的传递,该方法在信息传递过程中容易造成部分有效信息的丢失。目前临床医生可通过电子邮件、微信及数据存储媒介等将临床医生获得的临床信息、设计要求、患者的主观要求等客观的传递给义齿制作单位,这样可有效减少信息传递误差,提高修复体设计及制作的效率和精度,提高患者满意度。 2.3 数字化修复体设计和制作 2.3.1 数字化修复体设计 数字化设计即计算机辅助设计(computer aided design,CAD)是一个综合性的复杂过程,把计算、绘图、通讯、管理等结合在一起合理应用的一种现代化技术,也是口腔修复CAD/计算机辅助制作(computer aided manufacturing,CAM)流程中的中间环节,口腔医师将扫描数据导入计算机通过其强大的计算能力和图文处理功能来设计及修改修复体,极大提高了临床中各种修复体设计效率,避免了传统手工制作中的一些误差,节省了大量人力和时间,同时利用数字化设计系统对修复设计相关数据进行自动化计算,也提高了修复体制作质量[1]。CAD完成需要以下2个步骤:①将形状不规则的图形信息通过计算机软件依据关键点数据,创建曲线,进而形成曲面并转化为数字化曲面数据;②通过特殊软件将收集到的不规则几何图像信息数据进行修改设计,获得理想的三维虚拟修复效果[2-3]。目前,口腔CAD技术已被应用于牙体缺损固定修复(冠修复),包括冠的内表面、外表面以及冠内外表面结合部分的设计,该技术较为成熟,且多数系统带有标准牙数据并以此为参考进行设计。冠内表面的设计是在预备体或种植体表面数据上增加黏结剂厚度,内外表面结合处为颈缘线结合处。修复体咬合面设计目前还是CAD系统亟待解决的难题,因为良好咬合关系是在动态咬合过程中建立的,而现有的CAD计算机软件还无法完全模拟口腔咀嚼活动,目前需借助中间媒介建立视频咬合架[16-17]。另外CAD在牙列缺损的可摘局部义齿修复及在全口义齿制作方面也有较大进展,提高了患者修复重建的效率与精确度[18-19]。 2.3.2 数字化修复体制作 CAD完成后,将三维虚拟模型通过数字化加工技术转换为实体物体或修复体。目前临床上常用且比较成熟的加工技术有CAM技术和3D打印技术。 CAM是指将计算机设计的三维虚拟修复体,通过小型精密数控铣床或激光成型机转换为预期的修复体产品[20]。目前的临床研究多将CAM和CAD两个环节结合在一起,称为CAD/CAM,也就是在完成CAD数字化虚拟模型构建后,采用快速成型技术进行快速制造[21]。数控铣床加工有磨削、激光成型和电火花蚀刻等方法。临床上较常用磨削法,该方法费时且消耗刀具,材料浪费较为严重;激光成型机主要应用于光敏树脂,适用范围较窄;电火花技术要先加工石墨电极,步骤较为复杂。通过磨削法获得的修复体精度受到数字印模技术及机械加工技术的影响,相对于传统的修复体制作精度有所提高。临床上可用的CAD/CAM修复材料有陶瓷类、树脂类及金属类。陶瓷类包括长石类可切削陶瓷、玻璃陶瓷、氧化铝陶瓷及氧化锆陶瓷等,主要应用于全冠、固定桥、嵌体及贴面等修复体,强度和美观性根据每种陶瓷的成分和加工方式不同有差异,可根据临床需求进行选择。树脂类是一种颗粒增强型复合材料,为可切削复合树脂,临床上常用的有Paradigm MZ100树脂、DC-tell复合树脂及VITA CAD-Temp复合树脂等,该类材料具有一定的强度,美观性能好,可用于临时冠桥、咬合重建、种植导板等方面。金属类可切削材料主要是纯钛,该材料具有良好的力学性能和生物相容性,可用于冠桥修复及可摘义齿的金属支架等方面。目前临床上常用的CAD/CAM牙科系统有Cerec系统、Duret系统、Dux系统、Procera CAD-CAM系统、Digident系统、DCS系统及CICERO系统等。 3D打印技术是一种快速成型技术,其原理是先由电脑构建出三维数字模型,将模型分割成众多层面,通过3D打印机逐层打印堆积,最终形成实体模型[21-23]。3D打印技术具有精度好、效率高、无需机械加工和模具及节约材料的优点,而且该方法几乎能打印出任何形状的物体,特别是对于形状特殊的几何模型或物体,在医学领域可应用到口腔科(义齿制作、赝附体制作、种植导板及教学模具制作等)、耳鼻喉科、心血管外科、法医学、骨科以及组织工程学等[24-37]。相对于CAD/CAM技术“减法”的磨削原理,3D打印是依靠“加法”原理,将材料粉末层层叠加在一起,最终完成修复体的制作,目前常用4种方法,有3D喷印、光固化立体印刷、选择性激光烧结和熔融沉积成型及生物打印技术[38-42]。3D喷印又称为3D印刷技术,是指将打印的每一层通过喷涂液态黏结剂的方法层层打印叠加而成,该技术主要用于金属和陶瓷粉末的打印,可用于全瓷修复体和种植外科导板[43-44];光固化立体印刷采用液体状态的光敏树脂作为原料,是将获得的三维数字模型通过分层离散软件进行分离,通过数控平台将可调控的紫外光照射液态光敏树脂,并使扫描区的树脂逐点逐层固化,最终完成修复体的制作,该技术的细节重现效果较好、精度高,但所使用材料受限,临床上用于临时冠桥、种植导板、活动义齿及咬合重建等方面[43,45];选择性激光烧结是利用高强度激光束产生高温融化粉末形成一层固态薄层,然后逐层烧结并融合,完成修复体制作,该方法获得试件强度高、精度好,且选用的材料为热塑性材料,材料涵盖范围广,应用领域较广,可用于金属冠桥基底、种植体、活动义齿金属支架及用于防龋和磨损的涂层材料等[41,45-46];熔融沉积成型是将热塑性材料加热到一定温度成为半液体状态,然后操作平台喷头按照计算机预先设定喷射轨迹进行喷涂,材料迅速冷却凝固,层层叠加形成实体,该技术选用的材料多为热塑性树脂材料,可用于制作种植导板、临时冠桥及咬合重建等,成本较低,精度低[43,47]。生物打印技术包括生物材料支架打印及生物细胞直接打印两种方式,生物支架打印是将可吸收降解的生物材料聚集形成细胞生长所需的体内环境,为细胞的生长、繁殖及新陈代谢等提供生命支持,而生物细胞直接打印是指将生物细胞通过水凝胶及纤维蛋白原液等基质材料直接打印成高浓度的细胞结构模型,该方法是目前医学研究的前沿和难点,对于打印生物材料和细胞的选择及存活率还有待研究[40]。随着3D打印技术的高速发展,对于可打印材料需求也越来越大,特别是医用材料,目前医学类可打印材料根据成分不同分为:金属类、陶瓷类、树脂类、生物高分子材料及生物细胞等。金属类可打印材料要求纯度高、球形度好、颗粒分布窄、氧含量低等,目前临床上应用较多的为纯钛、钛合金、钴铬合金和镍钛记忆合金等,主要用于种植体、烤瓷金属基底冠及活动义齿支架等[48-53];陶瓷类是未来临床制作修复体的趋势,该材料具有耐高温、强度和硬度高、化学稳定和生物相容性好及耐腐蚀等优点,但陶瓷直接快速成型工艺尚未成熟[23,26,50,54-55];树脂类是一种由特定波长的紫外光照射引起聚合反应的复合基质材料,该材料为液态,具有强度高、耐高温、可塑性好及易抛光等优点,可用于临时冠桥、个性托盘、咬合重建及种植导板等方面[50,56-58];生物高分子材料是目前研究的热点和前沿,该材料具有良好的生物相容性,可用于人造颌骨、人造骨粉骨膜等,应用前景广阔,生物细胞是先用实验室培养的细胞作为介质以水机溶胶为黏合剂,逐层叠加后形成各种组织和器官,该技术目前已被应用于临床,成功率较高[40,59-65]。 随着CAD/CAM和3D打印技术及材料学的不断发展,其应用领域将会不断扩展,应用效果越来越好,给患者和医生带来福音。王峥[66]的研究将固定义齿修复患者76例随机等分为试验组和对照组,试验组接受口腔固定义齿数字化修复,对照组接受口腔传统固定义齿修复,最后试验组术后龋病、牙周病、楔状缺损、黏膜疾病发生率低于对照组,其护理要求有所降低,说明口腔固定义齿数字化技术有利于提高患者的口腔卫生情况,改善患者牙周健康,对于口腔健康护理是一个飞跃的提升,值得在临床上推广,并且在口腔护理工作当中有着前瞻性的研究空间和使用空间。过去可摘局部义齿制作方面的数字化实现有一定难度,由于每个患者缺失牙齿位置不同,结构复杂,同时缺乏活动义齿的专用设计软件,使得制作难度显著增加,随着3D打印技术的引入,实现了所谓的“加法”,能够快速制作任意复杂结构的模型,与CAD/CAM技术联合后现在可制作出结构精细的可摘局部义齿支架。黄丽娟等[67]应用CAD/CAM与3D打印技术制作出了可摘局部义齿支架,同时对义齿就位情况及软硬组织的适合性等临床效果进行评价,最后制作的义齿外形完整,大部分能顺利就位,同时义齿的固位力和稳定性良好,卡环和支托与基牙接触密合,基托的高点经过调磨后患者试戴舒服,说明到目前为止CAD/CAM和3D打印技术可用于可摘局部义齿支架制作,具有良好的应用前景。关于全口义齿的数字化制作有关报道较少,姚江武[68]报道了1例上下颌各残根经根管治疗的无牙颌患者, 通过传统取模,哥特式弓记录轨迹,面弓转移咬合记录,上咬合架, 扫描模型,利用软件排牙及虚拟咬合运动,最后戴入患者口内,其固位和稳定性良好,患者满意,该制作过程简单,人工费用降低,将是今后全口义齿制作的方向,但有一些问题需要改进如功能性印模制取,哥特式弓记录和面弓使用尚未数字化等(图1)。"
| [1] 刘一帆,郑秀丽,王伟娜,等.数字化设计技术在口腔修复中的应用[J].实用口腔医学杂志,2017,33(1):129-133.[2] 聂二民,徐会勇,姜瑞,等.采用CAD/CAM技术构建上颌中切牙的标准测试模型[J].中国组织工程研究,2015,19(51):8253-8258.[3] Alghazzawi Tariq F.Advancements in CAD/CAM technology: Options for practical implementation.J Prosthodont Res.2016; 60(2):72-84.[4] Mandelli F,Ferrini F,Gastaldi G,et al.Improvement of a Digital Impression with Conventional Materials:Overcoming Intraoral Scanner Limitations.Int J Prosthodont.2017;30(4):373-376. [5] 刘一帆,郑秀丽,于海,等.数字化印模技术在口腔修复中的应用[J].实用口腔医学杂志,2016,32(6):879-885.[6] 谢轶伦,沈刚.全口牙列口内扫描的精确性与可重复性分析[J].上海口腔医学,2016,25(5):593-599.[7] 包旭东,高学军.椅旁CAD/CAM数字化修复[J].中国实用口腔科杂志,2016,9(6):321-325.[8] Su TS,Sun J.Comparison of marginal and internal fit of 3-unit ceramic fixed dental prostheses made with eitheraconventionalordigitalimpression.J Prosthet Dent. 2016; 116(3):362-367.[9] Rai R,Kumar SA,Prabhu R,et al.Evaluation of marginal and internal gaps of metal ceramiccrowns obtained from conventional impressions and casting techniques with those obtained fromdigitaltechniques.Indian J Dent Res. 2017;28(3): 291-297. [10] [Kattadiyil MT,Mursic Z,AlRumaih H,et al.Intraoral scanning of hard and soft tissues for partial removable dental prosthesis fabrication.J Prosthet Dent.2014;112(03):444-448.[11] 陆亚倩,胡建.数字化印模技术修复应用的研究进展[J].口腔生物医学,2016,7(4):211-216.[12] 朱国慧,孙迎春,高平.口腔数字化印模精度的研究与进展[J].口腔颌面修复学杂志,2017,18(2):125-128.[13] 雷畅,蒋滔.数字比色技术的临床应用[J].国际口腔医学杂志, 2013,40(2):212-215. [14] 张新媛,吴效民.体外模型评估Cyrstaleye比色仪的可靠性和准确性[J].口腔颌面修复学杂志,2012,13(4):232-235.[15] Alshiddi IF, Richards LC.Intraoral scanning of hard and soft tissues for partial removable dental prosthesis fabrication. Aust Dent J.2015;60(2):176-181.[16] Stavness IK,Hannam AG,Tobias DL,et al.Simulation ofdentalcollisions and occlusal dynamics in the virtual environment.J Oral Rehabil.2016;43(4):269-278.[17] Solaberrieta E,Garmendia A,Minguez R,et al. Virtualfacebowtechnique.J Prosthet Dent. 2015;114(6):751-755.[18] Al-Fouzan AF,Al-Mejrad LA,Albarrag AM.Adherence of Candidatocomplete denturesurfaces in vitro: A comparison of conventionalandCAD/CAMcompletedentures.J Adv Prosthodont.2017;9(5):402-408.[19] Hassan B,Greven M,Wismeijer D.Integrating 3D facial scanning in a digital workflow toCAD/CAM design and fabricatecompletedentures for immediate total mouth rehabilitation.J Adv Prosthodont.2017;9(5):381-386.[20] 赵昕,战德松.CAD/CAM系统及可切削材料在口腔修复的应用现状[J].中国实用口腔科杂志,2013,6(6):331-337. [21] Barazanchi A,Li KC,Al-Amleh B,et al.AdditiveTechnology: Update on Current Materials and Applications in Dentistry.J Prosthodont.2017;26(2):156-163.[22] Barazanchi A,Li KC,Al-Amleh B,etal.AdditiveTechnology: Update on Current Materials and Applications in Dentistry.J Prosthodont.2017;26(2):156-163.[23] 肖凌浩,高平,孙迎春.3D打印技术及其在口腔修复学领域的应用[J].口腔颌面修复学杂志,2015,16(6):359-362.[24] Sun YC,Li R,Zhou YS,et al.Application and outlook ofthree-dimensional printingin prosthetic dentistry.Zhonghua Kou Qiang Yi Xue Za Zhi.2017;52(6):381-385. [25] 黄俊辉,刘桂,姚志刚,等.3D打印技术在口腔颌面修复中的应用[J].中华口腔医学研究杂志(电子版),2015,9(3):252-255.[26] 何雪锋,熊爱兵.3D打印技术在整形外科的研究及应用进展[J].中国组织工程研究,2017,21(3):428-432.[27] Vermeulen N,Haddow G,Seymour T,et al.3Dbioprint me: a socioethical view of bioprinting human organs and tissues.J Med Ethics.2017;43(9):618-624. [28] Zheng SN,Yao QQ,Mao FY,et al.Application of 3D printing rapid prototyping-assisted percutaneous fixation in the treatment of intertrochanteric fracture.Exp Ther Med. 2017; 14(4):3644-3650.[29] Velasco I,Vahdani S,Ramos H. Low-cost Method for Obtaining Medical Rapid Prototyping Using Desktop 3D printing: A Novel Technique for Mandibular Reconstruction Planning.J Clin Exp Dent.2017;9(9):e1103-e1108.[30] Wang X.Intelligent freeform manufacturing ofcomplex organs. Artificial Organs.2012;36(11):951-961.[31] McMenamin PG,Quayle MR,McHenry CR,et al.Theproduction of anatomical teaching resources using three-dimensional (3D) printing technology.AnatSci Educ.2014;7(6):479-486.[32] Goyanes A,Buanz AB,Basit AW,et al. Fused-filament 3D printing (3DP) for fabrication of tablets. Int J Pharm. 2014; 476(1-2):88-92.[33] Schmauss D,Haeberle S,Hagl C,et al.Three-dimensional printing in cardiac surgery and interventionalcardiology:a single-centre experience.Eur J Cardiothorac Surg. 2015; 47(6):1044-1052.[34] Liu YF,Zhang PY,Zhang QF,et al.Digital design and fabrication of simulation model for measuring orthodontic force. Biomed Mater Eng.2014;24(6):2265-2271.[35] Silberstein JL,Maddox MM,Dorsey P,et al.Physical models of renal malignancies using standard cross-sectional imaging and 3-dimensional printers: a pilot study.Urology. 2014;84(2): 268-272.[36] Lim CG,Campbell D,Clucas DM.Rapid prototyping technology in orbital floor reconstruction: application in three patients.Craniomaxillofac Trauma Reconstr. 2014;7(2): 143-146.[37] Banks J.Adding value in additive manufacturing: researchers in the United Kingdom and Europe look to 3D printing for customization.IEEE Pulse.2013;4(6):22-26.[38] 张文燕.3D打印医学未来[J].中国医院院长,2013,12(12):60-62.[39] 王强.3D打印“小时代”[J].印刷工业,2013,8(7):76-77.[40] 杨道朋,夏旭.3D打印生物材料研究及其临床应用优势[J].中国组织工程研究,2017,21(18):2927-2933.[41] Torabi K,Farjood E,Hamedani S.Rapid Prototyping Technologies and their Applications in Prosthodontics,a Review of Literature.J Dent (Shiraz).2015;16(1):1-9.[42] 贺超良,汤朝晖,田华雨,等.3D打印技术制备生物医用高分子材料的研究进展[J].高分子学报,2013,57(6):722-732.[43] 陈小冬,邢文忠.快速成型技术及其在口腔修复中的应用[J].中国实用口腔科杂志,2013,6(6):326-330.[44] 程蕙娟,吴丹,孙健.三维打印技术制作上颌全口义齿基托蜡型的初步研究[J].口腔材料器械杂志,2014,23(1):23-26.[45] Giacomo GD,Silva J,Martines R,et al.Computer-designed selectivelasersinteringsurgical guide and immediate loading dental implants with definitive prosthesis in edentulous patient: A preliminary method.Eur J Dent.2014;8(1):100-106. [46] Biland?i? MD,Wollgarten S,Stollenwerk J,et al. Glass- ceramiccoating material for the CO2 laserbasedsintering of thin films as caries and erosion protection.Dent Mater.2017; 33(9):995-1003.[47] 刘洋子健,夏春蕾,张均,等.熔融沉积成型3D打印技术应用进展及展望[J].工程塑料应用,2017,45(3):130-133.[48] 任玲,杨柯.医用金属的生物功能化——医用金属材料发展的新思路[J].中国材料进展,2014,33(2):125-128. [49] Chanchareonsook N,Tideman H,Lee S,et al.Mandibular reconstruction with a bioactive-coated cementless Ti6Al4V modular endoprosthesisin Macacafascicularis.Int J Oral Maxillofac Surg.2014;43(6):758-768.[50] 杜宇雷,孙菲菲,原光,等.3D打印材料的发展现状[J].徐州工程学院学报(自然科学版),2014,29(1):20-24. [51] Venkatesh KV,Nandini VV.Direct Metal Laser Sintering: A Digitised Metal Casting Technology.J Indian Prosthodont Soc. 2013;13(4):389-392.[52] 刘洁,迟帅,许谨,等.制作方法对钴铬合金金瓷结合性能的影响[J].华西口腔医学杂志,2014,32(2):115-118.[53] Revilla León M,Klemm IM,García-Arranz J,et al. 3DMetalPrinting-Additive ManufacturingTechnologies for Frameworks of Implant-Borne Fixed Dental Prosthesis.Eur J Prosthodont Restor Dent.2017;25(3):143-147.[54] Sun J,Zhang FQ.The application of rapid prototyping in prosthodontics.J Prosthodont.2012;21(8):641-644[55] Feilden E,Ferraro C,Zhang Q,et al.3D Printing Bioinspired Ceramic Composites.Sci Rep.2017;7(1):13759. [56] 牛茂,许在俊,李月.基于三维打印技术制作可摘局部义齿支架树脂熔模的适合性研究[J].重庆医学,2015,44(9):1235-1238. [57] Sun Y,Chen H,Li H,et al.Clinical evaluation of final impressions fromthree-dimensionalprinted custom trays.Sci Rep.2017;7(1):14958.[58] Hochman JB,Kraut J,Kazmerik K,et al.Generation ofa3D printed temporal bone model with internal fidelity and validation of the mechanical construct.Otolaryngol Head Neck Surg.2014;150(3):448-454.[59] 陈扬,蓝涛,钱文斌.3D打印技术在修复骨缺损中的应用研究[J].生物骨科材料与临床研究,2014,11(1):29-30,34.[60] Vijayavenkataraman S,Fuh JYH,Lu WF.3D printing and 3DBioprinting in Pediatrics.Bioengineering (Basel). 2017; 4(3):63.[61] Yi HG,Lee H,Cho DW.3D Printingof Organs-On-Chips. Bioengineering (Basel).2017;4(1):10.[62] Zadpoor AA,Malda J.Additive Manufacturing of Biomaterials, Tissues, and Organs.Ann Biomed Eng.2017;45(1):1-11.[63] Jang J.3DBioprinting and In Vitro Cardiovascular Tissue Modeling.Bioengineering (Basel).2017;4(3):71.[64] 石静,钟玉敏.组织工程中3D生物打印技术的应用[J].中国组织工程研究,2014,18(2):271-276.[65] 马新芳,张静莹.骨组织工程支架材料的研究现状与应用前景[J].中国组织工程研究,2014,18(30):4895-4899.[66] 王峥.数字化设计在固定义齿手术患者中的应用[J].护理实践与研究,2016,13(23):58-59.[67] 黄丽娟,景双林,聂蓉蓉,等.3D打印技术制作可摘局部义齿支架的临床应用[J].南京医科大学学报(自然科学版), 2016,36(10): 1259-1262.[68] 姚江武.数字化口腔修复(20)——数字化全口覆盖义齿的临床应用(附病例报告)[J].临床口腔医学志,2016,32(10):630-633. |
| [1] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [2] | Zeng Yanhua, Hao Yanlei. In vitro culture and purification of Schwann cells: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1135-1141. |
| [3] | Xu Dongzi, Zhang Ting, Ouyang Zhaolian. The global competitive situation of cardiac tissue engineering based on patent analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 807-812. |
| [4] | Wu Zijian, Hu Zhaoduan, Xie Youqiong, Wang Feng, Li Jia, Li Bocun, Cai Guowei, Peng Rui. Three-dimensional printing technology and bone tissue engineering research: literature metrology and visual analysis of research hotspots [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 564-569. |
| [5] | Chang Wenliao, Zhao Jie, Sun Xiaoliang, Wang Kun, Wu Guofeng, Zhou Jian, Li Shuxiang, Sun Han. Material selection, theoretical design and biomimetic function of artificial periosteum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 600-606. |
| [6] | Liu Fei, Cui Yutao, Liu He. Advantages and problems of local antibiotic delivery system in the treatment of osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 614-620. |
| [7] | Li Xiaozhuang, Duan Hao, Wang Weizhou, Tang Zhihong, Wang Yanghao, He Fei. Application of bone tissue engineering materials in the treatment of bone defect diseases in vivo [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 626-631. |
| [8] | Zhang Zhenkun, Li Zhe, Li Ya, Wang Yingying, Wang Yaping, Zhou Xinkui, Ma Shanshan, Guan Fangxia. Application of alginate based hydrogels/dressings in wound healing: sustained, dynamic and sequential release [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 638-643. |
| [9] | Chen Jiana, Qiu Yanling, Nie Minhai, Liu Xuqian. Tissue engineering scaffolds in repairing oral and maxillofacial soft tissue defects [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 644-650. |
| [10] | Xing Hao, Zhang Yonghong, Wang Dong. Advantages and disadvantages of repairing large-segment bone defect [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 426-430. |
| [11] | Chen Siqi, Xian Debin, Xu Rongsheng, Qin Zhongjie, Zhang Lei, Xia Delin. Effects of bone marrow mesenchymal stem cells and human umbilical vein endothelial cells combined with hydroxyapatite-tricalcium phosphate scaffolds on early angiogenesis in skull defect repair in rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3458-3465. |
| [12] | Wang Hao, Chen Mingxue, Li Junkang, Luo Xujiang, Peng Liqing, Li Huo, Huang Bo, Tian Guangzhao, Liu Shuyun, Sui Xiang, Huang Jingxiang, Guo Quanyi, Lu Xiaobo. Decellularized porcine skin matrix for tissue-engineered meniscus scaffold [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3473-3478. |
| [13] | Mo Jianling, He Shaoru, Feng Bowen, Jian Minqiao, Zhang Xiaohui, Liu Caisheng, Liang Yijing, Liu Yumei, Chen Liang, Zhou Haiyu, Liu Yanhui. Forming prevascularized cell sheets and the expression of angiogenesis-related factors [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3479-3486. |
| [14] | Liu Chang, Li Datong, Liu Yuan, Kong Lingbo, Guo Rui, Yang Lixue, Hao Dingjun, He Baorong. Poor efficacy after vertebral augmentation surgery of acute symptomatic thoracolumbar osteoporotic compression fracture: relationship with bone cement, bone mineral density, and adjacent fractures [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3510-3516. |
| [15] | Liu Liyong, Zhou Lei. Research and development status and development trend of hydrogel in tissue engineering based on patent information [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3527-3533. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||