Chinese Journal of Tissue Engineering Research
Previous Articles Next Articles
Development of surface treatments for medical magnesium alloys
Zhang Yong-qiang1, 2, Zhao Jian-ning1, 3, Bao Ni-rong1, 3
- 1Orthopedic Department, Nanjing General Hospital of Nanjing Military Region, Nanjing 210000, Jiangsu Province, China; 2School of Medicine, Southeast University, Nanjing 210000, Jiangsu Province, China; 3School of Medicine, Nanjing University, Nanjing 210000, Jiangsu Province, China
-
Received:2017-12-14Online:2018-08-08Published:2018-08-08 -
Contact:Bao Ni-rong, M.D., Associate chief physician, Orthopedic Department, Nanjing General Hospital of Nanjing Military Region, Nanjing 210000, Jiangsu Province, China; School of Medicine, Nanjing University, Nanjing 210000, Jiangsu Province, China -
About author:Zhang Yong-qiang, Master candidate, Orthopedic Department, Nanjing General Hospital of Nanjing Military Region, Nanjing 210000, Jiangsu Province, China; School of Medicine, Southeast University, Nanjing 210000, Jiangsu Province, China -
Supported by:the National Natural Science Foundation of China, No. 81572111, 81000814; the Science and Technology Project of Jiangsu Province, No. BK20161385
CLC Number:
Cite this article
Zhang Yong-qiang, Zhao Jian-ning, Bao Ni-rong. Development of surface treatments for medical magnesium alloys[J]. Chinese Journal of Tissue Engineering Research, doi: 10.3969/j.issn.2095-4344.0731.
share this article
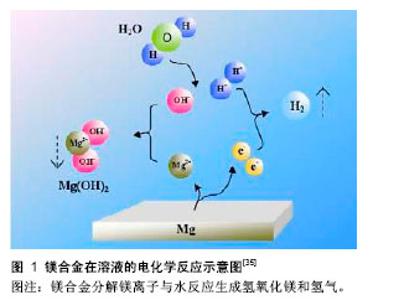
2.2 纳入资料的研究结果特征 表面处理技术不仅可以降低内置物的降解速度,还可以改变金属表面的生物相容性[4]。常用的医用镁合金的表面处理方式有:①表面涂层覆盖;②表面结构改性;③其他方式[5]。其中用于涂层的材料有很多,包括:生物活性陶瓷、高分子聚合物、化学转化膜、金属镀层及阳极氧化膜等[5]。表面结构改性技术包括:离子注入、激光表面熔融和表面纳米结晶;而表面涂层覆盖可分为:电化学法、微弧氧化、化学转化和高分子涂层。 2.2.1 表面涂层覆盖 电化学处理法:是常用的保护阴极金属的方法。磷酸钙是骨组织中的主要无机成分,是镁合金的常见涂层,具有良好的生物相容性、生物活性、骨诱导性和无毒性[6],并且可以提高镁金属的抗腐蚀性[7],故而羟基磷灰石是最常用的涂层。羟基磷灰石是天然矿物质形式的钙磷灰石,常常被作为生物活性陶瓷用于合金涂层的研究。龚沛等[8]在纯镁材料上沉积一层仿生羟基磷灰石,实验证明涂层后的骨支架可以加速骨愈合。有研究在镁基金属上制备羟基磷灰石涂层后发现金属的腐蚀速率可以通过羟基磷灰石进行调控,并且腐蚀形式变为均匀腐蚀。同时,有研究在AZ91D上制备了具有降解性能的均匀羟基磷灰石涂层,发现合金腐蚀速率得到了改善[5]。与其他磷酸钙涂层相比,在Mg合金上沉积二水磷酸氢钙涂层更容易,而且在浸入NaOH溶液2 h后可以转化成均匀的羟基磷灰石[9]。有研究在AZ31合金上制备了由二水磷酸氢钙和β-磷酸三钙组成的涂层,结果合金的生物腐蚀性——特别是耐点腐蚀性得到了提高[10]。陶瓷涂层也是电化学方法制备的,虽然金属的陶瓷涂层可以有效降低其降解速率,但是陶瓷涂层为惰性涂层,其不可降解性也是研究的重要问题。此外,电镀金属也是常用的涂层之一。杨等通过电沉积法生产Al-AZ91D,铝涂层附着力和硬度良好,且金属耐腐蚀性得到提高[11]。 微弧氧化:又称微等离子氧化,是一种依靠弧光放电产生的瞬时高温高压作用,生长基体金属氧化物涂层的技术,现广泛应用在镁金属的耐腐蚀研究中。该工艺过程容易控制,操作简单,处理效率高,对环境无污染。微弧氧化形成的膜层具有优异的耐磨和耐蚀性能[12]。微弧氧化是减轻镁合金腐蚀的有效手段。有研究在纯镁的表面制备了微弧氧化涂层,涂层厚且密实,可以很好地保护镁基体,提高其耐蚀性能[13]。另外,理想状态下,可降解金属的腐蚀速率与腐蚀形式应与体内骨骼的生长过程相适应。曲立杰研究指出超声微弧氧化处理的金属降解速率高于微弧氧化-电沉积金属以及单纯微弧氧化的金属,但是在整个实验种植的24周内,超声微弧氧化种植体保持着均匀缓慢的降解,为细胞生长、增殖以及骨矿化提供了良好的空间,以保持腐蚀产物缓慢的被代谢[14]。 微弧氧化涂料的优点是稳定、坚硬的、耐磨以及耐腐蚀,但其缺点是脆性高。虽然微弧氧化技术在镁合金体外实验中具有良好的抗腐蚀性及生物安全性,然而其体内实验以及持久的抗腐蚀性却很少报道,并且微弧氧化涂层中的主要成分MgO不能诱导磷灰石的形成。虽然近年来有关微弧氧化的报道层出不穷,但始终没有得到大规模的应用。日后微弧氧化的研究将会向着多层复合叠加的方向(如微弧氧化膜层+有机涂层)发展[15]。 化学转化(氟转化、稀土转化):化学转化涂层即通过化学转化的方法在合金表面形成一层能显著降低镁合金腐蚀速率的钝化层。目前,研究较多的化学转化膜有稀土转化膜、氟化物转化膜等。 氟化处理是常用的化学转化方法之一。氟不仅在人类的饮食中是必需的,而且还具有刺激成骨细胞增殖和增加松质骨中新矿物质沉积的优点。Drynda等[16]通过两步法在镁钙合金上制造了氟化物涂层,实验样品显示出良好的机械性能,降低了腐蚀速率并且对血管细胞有着良好的生物相容性。Yan等通过在不同时间段将AZ31B浸没在氢氟酸溶液中制备氟化物涂层,而后在模拟体液中浸渍45 d,发现涂层样品保持机械完整性,并显示出比裸合金具有更好的耐腐蚀性[17-18]。颜廷亭[18]研究还指出,氟转化处理后的镁合金起先具有良好的耐腐蚀性,浸泡60 d后腐蚀速率开始加速,这种滞后的腐蚀行为可以更好的符合组织生长趋势,在组织愈合前,材料能够缓慢降解或者不降解,以保证足够的力学性能及生物学性能,当组织愈合后,材料应开始快速降解,以免继续留存在体内,阻碍自体组织的正常生长或造成局部炎症。 另外,稀土转化层也是目前研究的热点。稀土转化涂层能够有效提高AZ3IB镁合金在生理盐水与模拟体液溶液中的耐蚀性能,并且提高AZ31B镁合金的抗凝血性能[18]。虽然化学转化膜有着良好的抗腐蚀性和生物相容性,但化学转化膜也有着自身的缺陷:化学转化膜较薄,极易造成损害,故而导致其应用显著受限。 高分子涂层:高分子涂层主要是有机涂层,为了防止金属基材在环境下的腐蚀,有机涂层必须是均匀无孔的,和基体有良好的结合力,且具有一定的自修复能力[19]。医用金属研究中常用的高分子涂层有聚乳酸、壳聚糖等。聚乳酸是一种可以完全降解的植物性高分子材料,其可被人体完全吸收,同时还具有良好的生物安全性,现已在临床中开始使用[20]。镁基金属聚乳酸涂层现已有大量报道。有研究证明了聚乳酸在模拟体液中改善微弧氧化处理的AZ31 Mg合金的耐腐蚀性[21]。有研究已经生产了丙交酯乙交酯共聚物涂层的Mg-6Zn镁合金,涂层后的金属耐腐蚀性得到了大大提高,细胞附着力也有所增加[22]。 聚乙烯亚胺也是高分子涂层之一。有研究报道了在AZ91D镁合金上制备聚乙烯亚胺、聚苯乙烯磺酸盐和 8-羟基喹啉组成的防腐逐层涂层的研究,发现其具有较好的成骨诱导性[23]。 壳聚糖涂层在镁合金表面的研究目前才刚开始。壳聚糖涂层是无毒的,并且可以作为组织愈合过程中细胞的黏合剂,还可增强金属的耐腐蚀性[24]。有研究研究了壳聚糖对Mg-Ca合金的表面改性作用,成功减缓了其在模拟体液中的腐蚀速率[25]。有研究了在体外条件下微弧氧化后涂覆有壳聚糖的Mg-Zn-Ca合金的腐蚀速率,结果显示防腐蚀速率显著改善[26-27]。同样,有研究将微弧氧化处理后的合金用壳聚糖和聚苯乙烯逐层涂层,结果证明了WE43-Mg合金的耐腐蚀性明显增强[22]。但是,由于壳聚糖涂层的耐磨性较差,仍需日后进一步实验研究。 许多报道已经证明,Ⅰ型胶原蛋白有利于骨细胞的增殖和黏附[27]。因此,Wang等[28]研究了聚乳酸/羟基磷灰石/胶原蛋白复合涂层在AZ31Mg合金上的耐腐蚀性和生物相容性,发现天然聚合物如胶原蛋白降解太快,耐腐蚀效果并不明显。 此外,血清白蛋白涂层也已有研究。有研究发现在AZ91镁合金上的牛血清白蛋白涂层降低了阴极电流,提高了合金在模拟体液内的耐腐蚀性[25]。 2.2.2 表面结构改性 离子注入(金属注入镀层、喷涂):是一种提高镁合金耐腐蚀性的有效方法,最早将离子注入技术应用于镁合金表面处理是在1984年,此后离子注入法得到长期的发展。Tian等已经将氮离子注入AZ31B镁合金,发现合金耐腐蚀性得到显着提高。有研究将钽离子注入AZ31,并观察到合金的耐腐蚀性得到了最大化提高[9]。离子注入技术在提高材料耐蚀性方面的优点主要在于:①生成分布均匀的新表层;②在表面改性的同时能保持合金本身的性质不变;③消除了改性涂层与合金之间的附着问题[29]。镁合金通过热喷铝还能消除镁合金基体与涂层之间的孔隙,起到封闭保护层的作用[9]。 激光表面熔融:激光表面处理技术具有传统工艺无可比拟的优势:能源清洁、经济、非接触加工、对基体热影响小和便于自动控制等。目前来说,激光表面处理在提高镁合金表面耐蚀、耐磨性能,延长材料的使用寿命等方面发挥的作用越来越明显。激光表面熔融可有效提高合金表面性能,如耐磨性,耐腐蚀性和生物相容性等。唐荻研究指出,镁合金经激光表面处理后,耐腐蚀性能得到微小的提高;而经激光表面+碱热复合处理后,其在模拟体液溶液中腐蚀速率明显降低,均比未行处理的合金以及单用激光处理的合金低[30]。 表面纳米结晶:由塑性变形引起的表面纳米结晶化同样是表面改性措施之一。Ho等[31]已经发现,在模拟体液中,激光冲击强化后的纳米结构将Mg-Ca合金的抗腐蚀性提高100倍。就目前来说,虽然表面纳米技术抗腐蚀性较好,但仍然缺乏进一步的研究进行证明。高正源等在AZ31表面磁控溅射单层纳米Al2O3涂层,用电化学工作站和摩擦磨损实验研究了涂层的耐蚀和耐磨性能,结果表明,磁控溅射单层纳米Al2O3涂层显著地改善了镁合金的耐腐蚀和耐磨损性能[32]。还有研究证实,纳米材料具有很好的抗菌作用[33]。 其他方法(碱热处理、快速凝固、挤压态及溶胶-凝胶法):除了上述常用的两大方面的表面处理方法之外,还存在其他的一些措施,如碱热处理、快速凝固、溶胶-凝胶涂层等。碱热处理即是将钱合金样品在80 ℃条件下在氢氧化钠溶液中浸泡12 h,然后再将样品在500 ℃下热处理12 h。将样品在氢氧化钠溶液浸泡之后,会在基体表面形成一层致密的氢氧化镁钝化层,经过热处理之后,致密的氢氧化镁钝化层会转变为致密氧化镁涂层。在腐蚀过程中,氧化镁钝化层将阻止腐蚀液对基体的腐烛,显著降低腐蚀速率。有研究将纯镁进行热处理后,经模拟体液浸泡发现处理后的材料抗蚀性显著提高[9]。苏颖超研究发现,将具有复合膜层结构的钙磷化学转化膜通过碱热处理转化为羟基磷灰石膜层后覆盖在镁合金上,结果表明,镁合金耐腐蚀性能不仅得到了提高,而且还表现出较好的生物矿化能力[3]。通过热轧、挤压等变形加工处理可以使得镁合金材料的晶粒尺寸得到细化,张佳[34]发现挤压态的JDBM合金在模拟体液中的降解速度从0.25 mm/年降低到了0.14 mm/年,析氢速度也有所降低。此外,硅烷基溶胶-凝胶涂层也被广泛用作于医用镁合金上的抗腐蚀研究和生物相容性涂层制备。快速凝固则可以减少合金中有害物质的掺入,且合金表面更均匀化,还能生成保护性的玻璃体膜,减缓其腐蚀速率。 2.2.3 腐蚀机制与生物安全性 镁合金的腐蚀方式包括电化学腐蚀、应力腐蚀以及点腐蚀,因其在含水溶液中生成 Mg(OH)2,故而耐腐蚀性差,其腐蚀原理见图1[35]。表面处理后的镁合金可以引起相应的腐蚀方式的改变。另外,生物安全性也是医用镁合金的重点。研究表明未处理的纯镁有明显的溶血作用,而经过表面改性提高其耐腐蚀性后,无溶血作用;有研究表明,镁合金降解过程中巨噬细胞吞噬颗粒和炎性组织增生轻微[36]。因此,镁作为生物材料,具有较好的生物安全性基础。由于镁金属本身具有一定的生物安全性,因而为了改变其降解速率采取的表面处理方式也必须拥有较好的生物安全性。 表面涂层覆盖:包括电化学转化的无机膜以及高分子聚合物的有机膜。高分子有机涂层的优点在于可以较易地在化学,物理和机械性能上进行改性,由于其降解速率取决于涂层分子量的大小,因此这类聚合物膜层常被用于控制镁合金的初始降解速率[25]。对于化学转化膜,羟基磷灰石涂层以及二水磷酸氢钙涂层等可以在金属表面形成惰性屏障,提高了对点腐蚀的耐性[9]。而化学转化主要是在基体表面形成一层金属氧化物的钝化层,最常用的就是氟化处理及稀土转化,其钝化层可增加腐蚀电阻,降低腐蚀电流,从而达到抗腐蚀作用[18]。另外,微弧氧化后的镁合金点腐蚀电位提高,且其高频容抗弧半径显著增大,从而降低镁合金的腐蚀溶解反应,起到抗腐蚀的作用[37]。 对于涂层覆盖方面,硅烷基涂层被广泛用作镁合金的生物安全性涂层[25]。实验指出,处理后的镁基材料,其浸提液对内皮细胞的毒性在1,3,5 d均显示为1级,符合生物材料的细胞毒性的要求[38]。再如丙交酯乙交酯共聚物、胶原蛋白涂层、天然聚合物等一些生物高分子,其涂层本身就具有生物安全性,用于涂层覆盖时可以有效的发挥自身特性。电化学试验结果表明,羟基磷灰石膜层不仅可以提高镁合金基体的耐蚀性能,而且还表现出较好的生物矿化能力。此外氟化处理是提高镁合金耐腐蚀性非常有效的方法,大量研究指出氟化层不仅具有很好的生物安全性,还可以有效促进骨的生长分化;体外降解实验表明少量镁粉及氟化镁粉的加入可以提高复合材料的生物活性。而对于微弧氧化后金属的生物相容性却存在争议,有研究者指出微弧氧化中的主要成分MgO不能诱导磷灰石形成,因此生物相容性不是很好,但另有研究者报道其制备的微弧氧化/聚左旋乳酸复合涂层,观察到良好的血液相容性[9]。再者,稀土元素的转化涂层可以显著的提高镁基合金的抗凝血能力。AZ3IB镁合金经氧化锰转化处理后,其溶血性能得到了有效的改善,电镀锌处理后在模拟体液溶液中浸泡表面会不断沉积磷酸钙,也一定程度上表明涂层增加了金属的生物活性[18]。 表面结构处理及其他方法:除了涂层覆盖的方法,结构改性通过改变基体金属表面结构来达到抗腐蚀效果。离子注入法使得材料改性层与基体之间呈渐变的方式,可以有效地降低腐蚀电流,从而改善降解速率。激光表面熔融可使金属表面发生二次相溶解,使细晶界析出,进而有利于Mg(OH)2膜的固定和保留,从而提高了耐腐蚀性[9],而表面纳米结晶处理的合金其腐蚀速率与结晶球的大小有关。经碱热处理后的镁合金具有更好的钝化现象,且其点腐蚀电位得到提高,从而降低腐蚀速率[3]。 对于表面结构处理的镁基金属来说,由于其并未添加过多外源性物质,因此其生物安全性主要取决的合金本身的性质。有研究报道,激光表面熔融可有效提高表面性能以及生物相容性[9]。在等离子体处理后,有报道称其对细胞的黏附,增殖和分化的行为有积极的影响[39]。还有,通过MTT检测和细胞形态分析得知,经碱热处理后的Mg-Zn-Sr合金其细胞毒性为0级,且表面处理后对细胞的活性略有提高。 "
| [1] Gepreel AH, Niinomi M. Biocompatibility of Ti-alloys for long-term implantation. J Mech Behav Biomed. 2013;20(4):407-415. [2] 王艳娜.生物医用AZ31B镁合金表面改性及性能研究[D].沈阳:沈阳建筑大学,2011.[3] 苏颖超.镁合金及复合材料表面钙磷膜层的制备与腐蚀降解行为研究[D].长春:吉林大学,2016.[4] Neděla O, Slepi?ka P, Švor?ík V, et al. Surface Modification of Polymer Substrates for Biomedical Applications. Materials. 2017; 10(10):1115.[5] 齐峥嵘.微弧氧化表面处理的ZK60镁合金在大鼠体内的降解行为及生物相容性研究[D].北京:中国人民解放军军医进修学院,2013.[6] Xu L, Pan F, Yu G, et al. In vitro and in vivo evaluation of the surface bioactivity of a calcium phosphate coated magnesium alloy. Biomaterials. 2009;30(8):1512-1523. [7] Surmeneva MA, Tyurin AI, Mukhametkaliyev TM, et al. Enhancement of the mechanical properties of AZ31 magnesium alloy via nanostructured hydroxyapatite thin films fabricated via radio-frequency magnetron sputtering. J Mech Behav Biomed. 2015;46:127-136.[8] 龚沛,王欣宇,郭洁.仿生法制备纯镁/羟基磷灰石复合涂层的研究[J].生物骨科材料与临床研究,2008,5(4):39-42.[9] 林锐,刘朝辉,王飞,等.镁合金表面改性技术现状研究[J].表面技术, 2016,45(4):124-131. [10] Li X, Liu X, Wu S, et al. Design of Magnesium Alloys with Controllable Degradation for Biomedical Implants: from Bulk to Surface. Acta Biomater. 2016;45:2-30.[11] Walker J, Shadanbaz S, Kirkland NT, et al. Magnesium alloys: Predicting in vivo corrosion with in vitro immersion testing. J Biomed Mater Res B. 2012;100B(4):1134-1141.[12] Marques IS, Alfaro MF, Cruz NC, et al. Tribocorrosion behavior of biofunctional titanium oxide films produced by micro-arc oxidation: synergism and mechanisms. J Mech Behav Biomed. 2016;60:8.[13] Echever R, Monica, Galvis O, et al. Osseointegration improvement by plasma electrolytic oxidation of modified titanium alloys surfaces. J Mater Sci-Mater M. 2015;26(2):72.[14] 曲立杰.镁合金表面超声微弧氧化生物涂层的组织结构与性能[D].哈尔滨:哈尔滨工业大学,2015.[15] 慕伟意,李争显,杜继红,等.镁合金的应用及其表面处理研究进展[J].表面技术,2011,40(2):86-91.[16] Drynda A, Hassel T, Bach FW, et al. In vitro and in vivo corrosion properties of new iron–manganese alloys designed for cardiovascular applications. J Biomed Mater Res B. 2015;103(3): 649-660.[17] Martinez Sanchez AH, Luthringer BJ, Feyerabend F, et al. Mg and Mg alloys: how comparable are in vitro and in vivo corrosion rates? A review. Acta Biomater. 2015;13:16-31.[18] 颜廷亭.AZ31B镁合金的生物医用表面改性研究[D].南京:南京理工大学, 2010.[19] Yeung KWK, Wong KHM. Biodegradable metallic materials for orthopaedic implantations: a review. IOS Press. 2012. [20] Jain A, Kunduru KR, Basu A, et al. Injectable formulations of poly(lactic acid) and its copolymers in clinical use. Adv Drug Deliver Rev. 2016;107:213. [21] Golshirazi A, Kharaziha M, Golozar M. Polyethylenimine/Kappa Carrageenan: Micro-arc Oxidation Coating for Passivation of Magnesium Alloy. Carbohyd Polym. 2017;167:185.[22] Xu G, Shen X, Dai L, et al. Reduced bacteria adhesion on octenidine loaded mesoporous silica nanoparticles coating on titanium substrates. Mat Sci Eng C. 2017;70:386-395.[23] Ostrowski N, Lee B, Enick N, et al. Corrosion protection and improved cytocompatibility of biodegradable polymeric layer-by-layer coatings on AZ31 magnesium alloys. Acta Biomater. 2013;9(10): 8704-8713.[24] 曾荣昌,刘丽君,骆凯捷,等.AZ31镁合金表面层层组装PSS/GS膜的体外耐蚀与抗菌性能(英文)[J].中国有色金属学报(英文版),2015,25(12): 4028-4039.[25] Agarwal S, Curtin J, Duffy B, et al. Biodegradable magnesium alloys for orthopaedic applications: a review on corrosion, biocompatibility and surface modifications. Mat Sci Eng C-Mater. 2016;68:948.[26] Lu Y, Wan P, Zhang B, et al. Research on the corrosion resistance and formation of double-layer calcium phosphate coating on AZ31 obtained at varied temperatures. Mat Sci Eng C. 2014;43(43): 264-271.[27] Qiao X, Russell S J, Yang X, et al. Compositional and in Vitro Evaluation of Nonwoven Type I Collagen/Poly-dl-lactic Acid Scaffolds for Bone Regeneration. J Funct Biomater. 2015;6(3):667-686.[28] Wang ZL, Yan YH, Tao W, et al. Poly (L-lactic acid)/Hydroxyapatite/ Collagen Composite Coatings on AZ31 Magnesium Alloy for Biomedical Application. P I Mech Eng H. 2013;227(10):1094.[29] 张春怀.医用镁合金的腐蚀行为及高分子修饰研究[D].天津:天津大学, 2007.[30] 唐荻.激光+碱热处理的医用Mg--4.0Zn--1.5Sr合金的降解及生物相容性研究[D].沈阳:东北大学,2014.[31] Ho YH, Vora HD, Dahotre NB. Laser surface modification of AZ31B Mg alloy for bio-wettability. J Biomater Appl. 2015;29(7):915-928.[32] 高正源,潘复生,汤爱涛,等.AZ31镁合金表面纳米A12O3涂层的耐蚀耐磨性能研究[J].功能材料,2013,44(8):1069-1072.[33] Vimbela GV, Ngo SM, Fraze C, et al. Anti bacterial properties and toxicity from metallic nanomaterials. Int J Nanomed. 2017;12: 3941-3965.[34] 张佳.新型Mg-Nd-Zn-Zr合金在模拟体液中的降解行为研究[D].上海:上海交通大学,2010.[35] 张晶.Mg-Zn-Zr合金的表面处理及其内外腐蚀降解性能研究[D].天津:天津理工大学,2014.[36] 谢兴文,黄晋,李宁,等.镁及镁合金植入体在骨科临床中的应用与进展[J].中国组织工程研究,2012,16(39):7317-7321.[37] 钱琳灵.表面处理对医用镁合金降解性能的影响研究[D].南京:东南大学,2016.[38] 龚才华.表面有机改性镁基生物材料的制备及生物相容性研究[D].重庆:重庆大学,2016.[39] Zhao S, Chen Y, Liu B, et al. A Dual-task Design of Corrosion-controlling and Osteo-compatible Hexamethylenediaminetetrakis-(methylene phosphonic acid) (HDTMPA) Coating on Magnesium for Biodegradable Bone Implants Application. J Biomed Mater Res A. 2015;103(5):1640-1652.[40] 彭友霖,周丽丽,周艳红.镁合金作为生物医用植入材料的临床应用[J].中国组织工程研究,2011,15(42):7923-7926. |
| [1] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [2] | Zeng Yanhua, Hao Yanlei. In vitro culture and purification of Schwann cells: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1135-1141. |
| [3] | Xu Dongzi, Zhang Ting, Ouyang Zhaolian. The global competitive situation of cardiac tissue engineering based on patent analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 807-812. |
| [4] | Wu Zijian, Hu Zhaoduan, Xie Youqiong, Wang Feng, Li Jia, Li Bocun, Cai Guowei, Peng Rui. Three-dimensional printing technology and bone tissue engineering research: literature metrology and visual analysis of research hotspots [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 564-569. |
| [5] | Chang Wenliao, Zhao Jie, Sun Xiaoliang, Wang Kun, Wu Guofeng, Zhou Jian, Li Shuxiang, Sun Han. Material selection, theoretical design and biomimetic function of artificial periosteum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 600-606. |
| [6] | Liu Fei, Cui Yutao, Liu He. Advantages and problems of local antibiotic delivery system in the treatment of osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 614-620. |
| [7] | Li Xiaozhuang, Duan Hao, Wang Weizhou, Tang Zhihong, Wang Yanghao, He Fei. Application of bone tissue engineering materials in the treatment of bone defect diseases in vivo [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 626-631. |
| [8] | Zhang Zhenkun, Li Zhe, Li Ya, Wang Yingying, Wang Yaping, Zhou Xinkui, Ma Shanshan, Guan Fangxia. Application of alginate based hydrogels/dressings in wound healing: sustained, dynamic and sequential release [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 638-643. |
| [9] | Chen Jiana, Qiu Yanling, Nie Minhai, Liu Xuqian. Tissue engineering scaffolds in repairing oral and maxillofacial soft tissue defects [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 644-650. |
| [10] | Xing Hao, Zhang Yonghong, Wang Dong. Advantages and disadvantages of repairing large-segment bone defect [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 426-430. |
| [11] | Chen Siqi, Xian Debin, Xu Rongsheng, Qin Zhongjie, Zhang Lei, Xia Delin. Effects of bone marrow mesenchymal stem cells and human umbilical vein endothelial cells combined with hydroxyapatite-tricalcium phosphate scaffolds on early angiogenesis in skull defect repair in rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3458-3465. |
| [12] | Wang Hao, Chen Mingxue, Li Junkang, Luo Xujiang, Peng Liqing, Li Huo, Huang Bo, Tian Guangzhao, Liu Shuyun, Sui Xiang, Huang Jingxiang, Guo Quanyi, Lu Xiaobo. Decellularized porcine skin matrix for tissue-engineered meniscus scaffold [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3473-3478. |
| [13] | Mo Jianling, He Shaoru, Feng Bowen, Jian Minqiao, Zhang Xiaohui, Liu Caisheng, Liang Yijing, Liu Yumei, Chen Liang, Zhou Haiyu, Liu Yanhui. Forming prevascularized cell sheets and the expression of angiogenesis-related factors [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3479-3486. |
| [14] | Liu Chang, Li Datong, Liu Yuan, Kong Lingbo, Guo Rui, Yang Lixue, Hao Dingjun, He Baorong. Poor efficacy after vertebral augmentation surgery of acute symptomatic thoracolumbar osteoporotic compression fracture: relationship with bone cement, bone mineral density, and adjacent fractures [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3510-3516. |
| [15] | Liu Liyong, Zhou Lei. Research and development status and development trend of hydrogel in tissue engineering based on patent information [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3527-3533. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||

