Chinese Journal of Tissue Engineering Research ›› 2018, Vol. 22 ›› Issue (32): 5234-5240.doi: 10.3969/j.issn.2095-4344.0558
Previous Articles Next Articles
Research advance, bottlenecks and challenges of microarray of micro organs
Yang Peng-cheng, Qi Yan, Zhang Dong-hui
- College of Life Science, Hubei University, Wuhan 430062, Hubei Province, China
-
Received:2018-06-05Online:2018-11-18Published:2018-11-18 -
Contact:Zhang Dong-hui, PhD, Professor, College of Life Science, Hubei University, Wuhan 430062, Hubei Province, China -
About author:Yang Peng-cheng, College of Life Science, Hubei University, Wuhan 430062, Hubei Province, China Qi Yan, College of Life Science, Hubei University, Wuhan 430062, Hubei Province, China Yang Peng-cheng and Qi Yan contributed equally to this work.
CLC Number:
Cite this article
Yang Peng-cheng, Qi Yan, Zhang Dong-hui. Research advance, bottlenecks and challenges of microarray of micro organs[J]. Chinese Journal of Tissue Engineering Research, 2018, 22(32): 5234-5240.
share this article
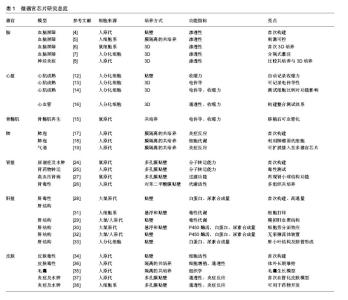
2.1 总述 在2004年, Andersson等[1]就首次介绍了搭建用于构建细胞模块、控制细胞、组织形态和作为生物反应器的微流控设备,称为“微器官组织芯片”。经过10余年的发展,已开发出针对多种不同组织、器官的微器官组织芯片,用于模拟相应的器官的不同生理活动。 不同的微器官芯片往往由不同的微尺度制备工艺集成,最常使用的方法有硬光刻、软光刻和3D打印。其中,硬光刻和软光刻精度高,但操作工艺复杂、对材料和技术要求高;3D打印操作相对容易却难以达到微米级的精确度。在制作微器官组织芯片的过程中,这些技术往往联合应用,以体现各自的优势。2017年Beauchamp等[2]制作出了有史以来最小的3D打印微流控装置。这种微型芯片能在小于100 μm的尺寸下起作用,为3D打印微流控装置的大规模生产提供了条件。 微器官组织芯片涉及4个关键元件,分别为微流控组件、活细胞组织组件、用于刺激或药物投放的组件和用于读出结果的传感组件。微流控组件是指利用微流控将目的细胞送达指定位置的组件,也包括在培养过程中培养液的输入,以及废液的排出系统。通常,该组件具有小型化、集成化和自动化的特点。活细胞组织组件是指将特定细胞类型在2D或3D情况下进行空间上的规范排布的组件,通常通过添加生物相容性材料(例如水凝胶)来防止机械损伤和塑造三维排布。虽然与2D情况相比,3D的组织结构可以更好地模拟体内情况,但是由于技术和成本以及细胞外基质的组装以及脉管的预设和形成的限制,器官组织芯片中活细胞组件仍以2D培养居多。第三是用于刺激或药物投放的组件。一方面,对于某些特定组织,物理或化学信号刺激是模拟体内微环境的必要条件,该刺激可以促进微组织成熟和功能化(例如电刺激可以帮助心肌组织成熟[3]);另一方面,不同的信号刺激可以来源于不同药品的添加,用于药物筛选。最后是用于读出结果的传感组件,该传感组件既可以是嵌入式的传感输出组件,也可以是基于透明芯片的可视化功能评价体系。前者读数快,但需要解决传感组件的生物相容性问题;后者相对记录复杂,但可分析系数增加。由于微器官组织芯片的主要用途是基于疾病模型的药物筛选,目前进行研发的微器官也多集中在和重大疾病相关的重要组织器官,例如:脑、心脏、肾脏、肝脏等等。 2.2 微型脑组织芯片 大脑作为人体中枢神经的所在历来是药物筛选和毒性测试的重要靶器官。血脑屏障(BBB)由于其独特的选择性通透性,使得脑组织内环境保持相对稳定,维持中枢系统的正常生理功能,成为了药物检测研究的重中之重。 早在2012年,Yeon等[4]首次发表了关于脑微血管系统渗透性测定的微器官组织芯片装置。该装置利用聚二甲基硅氧烷预设两个平行的,有微孔连接的高度为 25 μm的管道,通过控制不同管道中液体的流速,在微孔处产生压力差。而微孔处则是人类脐带血管内皮细胞培养层,在用星形胶质细胞条件培养基与血管内皮细胞培养基分别培养2 h后发现,星形胶质细胞条件培养基的存在降低了血管内皮细胞培养层的渗透性。 随后,2013年Griep等[5]发表了另外一个微型脑组织芯片模型。该模型将人脑微血管内皮细胞系细胞培养在多孔聚碳酸酯(PC)膜上形成屏障,通过测试电阻的方式来测定屏障的通透能力,发现加入炎性蛋白肿瘤坏死因子α后,通透性下降。 2015年,Kim等[6]将小鼠bEnd3内皮细胞在3D打印的微管中培养以模拟血脑屏障。荧光标记的葡聚糖通透实验证明了该微器官芯片的功能,甘露醇测定进一步表征了渗透性及其随时间恢复的特性。同年的9月,Brown等团队[7]通过软光刻将单个完整的神经-血管单元重现在微组织器官芯片上。该芯片分为3层,分别为一个入口通道血管腔层,脑室层和脑灌注通道层。芯片中使用的细胞来源于诱导多能细胞干细胞(hiPSC)分化而来的功能性神经元细胞。该研究发现:谷氨酸盐会增加渗透性,而抗坏血酸具有降低渗透性的功能;33 ℃的冷休克会引起血脑屏障的选择性屏蔽能力降低。 2016年,Herland等工作组[8]使用软光刻法在单个方形微通道内产生圆柱形胶原凝胶管,并且在凝胶管壁内嵌入星形胶质细胞,通过在凝胶管腔内顺序播种周细胞和内皮细胞来建立多种细胞类型协同的血脑屏障微组织三维模型。该研究发现:内皮细胞的完整性依赖星形细胞和周细胞的存在。相对于简单的二维培养,这种三维多细胞类型微组织培养,能够产生和体内血脑屏障类似的功能性炎症刺激反应。这可以帮助研究在炎症条件下,血脑屏障对不同药物通透性的变化情况,从而防止产生未预期的不良反应。 而在未来的研究中,更多细胞类型的加入(包括人类免疫细胞,如嗜中性粒细胞,胶质细胞和单核细胞以及人类皮质神经元等等),无疑会使微型脑组织器官芯片具有更多的可测试的功能,用于研究神经炎症、其他神经系统疾病、免疫相关神经疾病,以及帮助筛查有可能产生中枢系统毒性的新药。 2.3 微型横纹肌组织芯片 心肌和骨骼肌都属于横纹肌。心肌是心脏的主要组成部分,而心脏是人体存活的必要器官。骨骼肌约占人总体质量的40%[9],是人体重要的运动器官。对于横纹肌来讲,一方面,要具有收缩性;另一方面,该收缩受神经及电信号调控,需达到收缩的一致性。研究药物处理对横纹肌的影响对于帮助开发更有效和更安全的药物有重要意义。检测横纹肌的功能,可以通过测定肌肉组织的体外收缩性来完成。常用的两种方法:第1种方法是Uehata等[10]的测量法,直接将手术取得的横纹肌肌肉条悬挂在收缩力传感器上测量,这需要测量较大的力;第2种方法是Jacot等[11]开发的,利用横纹肌细胞收缩距离的变化来模拟计算细胞的收缩力,该方法可用来测量单个肌细胞,但是得到的收缩力数值是相对数值,并不是绝对数值。 2012年,Grosberg等[12]利用二甲基硅氧烷(PDMS)制成带有表面纹理的弹性薄膜,并将新生大鼠心肌细胞种于膜上,形成肌肉薄膜(MTF)。伴随心肌细胞收缩,该肌肉薄膜可向一侧发生卷曲。通过测定肌肉薄膜的卷曲程度,可以分析种植在聚二甲基硅氧烷膜上的不同细胞收缩能力大小的差异。该实验体系既适用于单一肌肉薄膜的测定,也适用于基于高通量的自动化多控板测定。同年5月,Ma等[13]利用标准光刻和软光刻相结合,将微电极整合在了微肌肉芯片内。通过测试两电极之间微肌肉束的导电能力来评价肌肉细胞的功能。 随后,2013年,Zhang等[14]利用水凝胶系统在聚二甲基硅氧烷模具内制作自组装的心肌组织片。值得一提的是,该工作中用到的心肌细胞来源于人胚胎干细胞分化得到的功能性心肌。该三维组织工程人心肌组织片得到了高达25.1 cm/s的动作电位传导速度,并具有 11.8 mN/mm2的收缩应力。和二维培养相比,3D培养更利于hESC-CM的成熟。并且,分化体系的副产物,成纤维细胞和血管内皮细胞能够帮助心肌细胞进一步成熟。同一实验室,2014年Juhas等[15]利用类似的培养体系,体外形成三维骨骼肌微肌肉束,移植入小鼠体内后呈现骨骼肌相应功能,并能够血管化。2016年,Zhang等[16]应用了3D打印技术制成了同时整合了心肌和血管系统的微器官组织芯片。该模型先利用血管内皮细胞形成血管网,再将心肌细胞接种于血管网的间隙中,该血管-心肌微器官组织芯片为心血管相关药物提供了可能的筛选平台。 2.4 微型肺组织芯片 近10年来,科学家们已设计出多种基于微流控的、用于研究肺的生理学功能的肺组织器官芯片,其中有些甚至可以用作呼吸辅助装置或者氧合器。第一个设计出微型肺芯片的是Huh等[17]工作组,他们利用软光刻成型技术制作了一个分为上下两个腔室的微型芯片,人肺泡上皮细胞和肺微血管内皮细胞分别培养于上腔室和下腔室中,上下两腔室被10 μm厚、附有细胞外基质的带微孔聚二甲基硅氧烷膜隔开。 为了模拟真实肺泡结构——形成肺泡-毛细血管的类似气-液界面,在细胞附着在聚二甲基硅氧烷膜之后,下部腔室通以培养基使两种细胞生长汇集,上部腔室通以空气诱导细胞分化,形成气液界面。同时,由于聚二甲基硅氧烷膜具有弹性,Huh等[17]在上层气相腔室中构建中空室,进行循环真空抽吸来模拟人体肺中隔膜收缩导致的肺泡的扩张、收缩与肺泡-肺泡毛细血管屏障的变形。利用该装置,Huh等[17]进行了炎症损伤、纳米毒理学、肺水肿等研究,验证了其仿生能力,并首次说明了生理机械力对白细胞介素2诱导的肺泡毛细血管屏障通透性的增加,存在不良影响。2015年,Stucki及其同 事[18]报道了另一种微型肺组织器官芯片,该模型使用来自患者的原代人肺泡上皮细胞与内皮细胞共培养,并首次使用三维立体的扩张方式来取代单向弹性膜扩张来模拟呼吸。随后,Blume等[19]开发了一种新型的气道上皮细胞三维体外培养模型,直接将带有原代支气管上皮细胞的插入式细胞培养器(Transwell®)整合到微流体培养系统中,利用系统能不断地交换体液和介质的特性,来模拟肺间质流动,从而达到在更接近体内的环境中研究上皮屏障反应的目的。这套微流控系统利用带有可渗透过滤器的支架作为单一组织培养室,并将多个培养室联合起来,使其集成性提高,更容易和其他(如皮肤,肠,肝或肾)微器官组织芯片联用。在微型肺组织器官芯片中,在通过微流控系统来模拟肺部气-液界面和呼吸扩张的同时,还能向肺泡及附着的毛细血管施加压力并提供剪切流动剖面[20],进而更真实的模拟肺部环境。肺组织器官芯片同样还用于研发具有临床应用潜力的可植入呼吸辅助装置,例如Kniazeva等[21]和Hoganson等[22]基于堆叠微通道网络与超薄气体交换膜设计出了小型微流体人造肺和可植入的动态肺辅助装置。Rochow 等[23]同样也利用堆叠微通道网络设计出了一种微型氧合器,可通过脐带血管灌注到胚胎中,以支持呼吸功能不全的新生儿。鉴于流体参数的精确控制以及组织界面的成功建模,微流体平台在呼吸系统病理生理学研究中的应用将越来越广泛。 2.5 微型肾组织器官芯片 肾脏的主要功能是产生尿液,一方面,肾脏的滤过功能帮助排出代谢废物和毒素;另一方面保留水分,对蛋白、糖类及无机盐进行重吸收,以调节人体的电解质平衡及酸碱平衡。在药物筛选中,很多药物具有很高的肝肾毒性,会对肾脏的滤过功能产生不可逆的损伤。研制微型肾组织器官芯片对于药物的毒性筛查有重要的意义。 有效培养肾小管细胞对体外模拟肾功能极为重要,而微流控系统一方面可以真实模拟肾小管细胞生长所依赖的流体环境,另一方面还可以提供多孔膜支撑,以利于细胞极性的形成。Jang等[24]2010年首次介绍了一种用于培养小鼠肾脏内髓集合管细胞的多层微流控装置用于模拟小鼠的肾滤过系统。该装置由聚二甲基硅氧烷制成的上下2个小室组成,上室具有通道,其间通以流体来模拟尿腔,下室用以培养细胞,两室之间用多孔膜相隔。该装置通过提供一个仿生环境,增强了小鼠肾脏内髓集合管细胞的极性、帮助其细胞骨架重组,帮助其在激素刺激下的分子转运。2013年,该工作组利用同样的微流控装置培养人原代肾上皮细胞制备人微型肾组织器官芯片[25],除了显示出更强的白蛋白转运、葡萄糖再吸收等能力外,利用该装置还测量出更接近体内的顺铂毒性和Pgp流出转运蛋白活性。在2015年Ilka Maschmeyer及其研究团队[26]设计并制造的四器官芯片联通系统中,也有微型肾组织器官芯片。该系统分为6个腔室,2个作为排泄液体的储存器,另外4个作为肝脏、小肠、肾脏、皮肤组织的培养室。系统中血液流回路和排泄流回路分别由单独的微量泵控制,且在肾近端小管培养室中重叠。该系统不仅重建了肾近端小管屏障模型,还首次实现了4个组织持续28d内环境可重复的共培养,构建的系统能够支持候选药物微流体ADME(吸收、分布、代谢、排泄)分析和剂量可重复的全身毒性实验。2016年Zhou等[27]为研究高血压肾病所设计的肾小球芯片模型也采用了类似的上下室结构:上室提供灌注流产生机械力,下室通废液,中间以多孔膜相隔,多孔膜上端培养小鼠肾小球内皮细胞,下端培养小鼠足细胞。不同的是,他们将4个相同的细胞培养室相连形成一个单元来模拟肾小球毛细血管环网络结构。同一芯片上又集成了4个肾小球单元以便提高实验效率。 2.6 微型肝组织器官芯片 肝脏是人体重要的解毒器官,对于药物的药代动力学和毒性测试有着重要的意义;并且,如何能够在体外培养成体肝脏细胞并保持其活性一直是困扰肝细胞相关研究的瓶颈。早在2006年,Kane等[28]设计出最原始的肝组织器官芯片,由64个(8×8)微流体孔构成的阵列组成,孔内共培养有大鼠肝细胞和3T3-J2成纤维细胞,实现了培养基和气道的分离。该芯片内培养的大鼠肝细胞具有连续、稳定合成白蛋白与代谢的能力。相比该工作,Lee等[29]2007年设计的微型肝组织器官芯片模拟条件更接近于体内生理条件。该芯片主体分为细胞培养室和流体通道,二者由类内皮细胞屏障隔开。该屏障由有机硅蚀刻而成,一方面浓缩培养室中的细胞;另一方面将培养室和流体通道隔开,减少对流的同时,允许物质扩散运输,从而达到模拟肝血窦功能的目的。在该装置中,大鼠与人的肝细胞在无细胞外基质涂层的情况下存活了7 d,且通过代谢介导的肝毒性双氯芬酸实验说明其具有代谢毒性物质的功能。 Lee等[30]2013年设计的一种三维微型肝组织芯片则是用于研究肝细胞和肝星状细胞(HSCs)的相互作用。该芯片由两个腔室构成,一个室表面平坦,用于培养大鼠肝星状细胞,另一个室具有凹孔,用于培养大鼠肝细胞球体。两种细胞接种到培养室后,以连接管相连,在渗透泵的作用下,培养基连续从肝星状细胞培养室流向肝细胞培养室。共培养的肝细胞球体相比于单培养球体,流出液中白蛋白和尿素的含量更高,说明肝星状细胞有助于肝细胞球体的维持。Bhise等[31]2016年先利用聚二甲基硅氧烷微孔共培养HepG2/C3A细胞形成球体,以更好的模拟体内肝小叶中肝细胞状态,再将球体以7×7的阵列生物打印到芯片中的中心细胞培养室中,培养室通过流体通道与出入口相连。以流出液中白蛋"
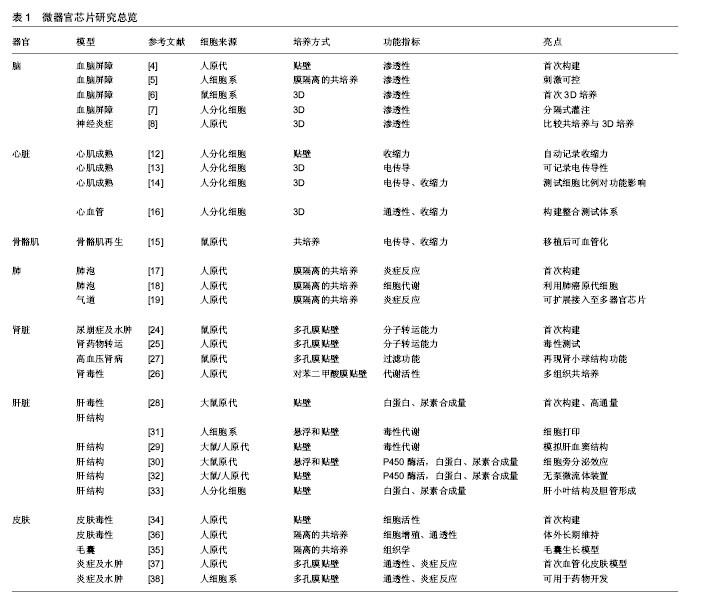
白、转铁蛋白、铜蓝蛋白等生物标志物含量作为检测指标,结果不仅证明该芯片在应对APAP治疗时的结果类似于动物和体外模型,可被用于药物毒性分析,还证明经30 d的培养后,细胞球体仍保持较高的活性[32]。截至目前,最新设计出的微型肝组织芯片则通过开发无泵微流体灌注平台实现了人肝细胞样细胞的高效分化,以及可扩展的肝小叶芯片实现人肝细胞的稳定培养和周边组织(胆汁小管网络)的形成[33]。 2.7 微型皮肤芯片 鉴于皮肤移植相对于其他器官移植要简单易行,以及皮肤本身平面化的特征。皮肤的微器官芯片在研究如何促进血管化的基础上,更增加微器官复杂度,着眼于探索制作功能和正常皮肤更类似的微器官。 O’Neill等[34]在2008年构建了首个培养人类表皮角化细胞(HEK)的四通道微流控装置。装置最底层为 50 mm×75 mm的载玻片,使用Ⅰ型鼠尾胶原在载玻片上构建平行条带,进而选择性黏附、扩增不同通道中的HEK,模拟多孔板中的培养物阵列;再在胶原条带上放 置软光刻而成的PDMS细胞培养通道,4个通道以不同流速灌注细胞,72 h培养后,培养基灌注速率0.025- 0.4 μL/min时,细胞可维93.0%-99.6%的存活率。2013年,Atac团队[35]开发的灌注平台将培养有青少年包皮组织及下层支撑组织和男性头皮毛囊的Transwell分别插入平台中,以微通道将两者相连,并通过内置微型泵驱动平台内介质流动。实验结果证明,与静态培养相比,灌注培养延长了皮肤等效物的培养周期、提高了毛发纤维的伸长率。同年Ilka Wagner等[36]通过利用类似的微流控设备再次证明,灌注培养可延长市售的皮肤等效物的培养周期与更有效的开展药物研究。2015年,Abaci等[37]设计的皮肤芯片可持续培养人成纤维细胞与角质形成细胞共培养形成的人体皮肤等效物,该芯片分为3层,最底层PDMS两侧均有培养基储存器,两者以微流体通道相连,最上层PDMS有培养孔,其中可插入培养有人皮肤等效物的Transwell,上下两层以聚碳酸酯多孔膜相隔。人皮肤等效物底层与多孔膜接触,顶层直接与空气接触;整个芯片置于一个摇摆平台上,利用平台的循环摇摆合适的介质流速;该芯片不仅可以持续3周稳定培养人皮肤等效物用作药物测试,还建立起了数学模型以助于更好的评估药物扩散和分配速率,从而获得更佳的测试结果;Wufuer等[38]2016年开发了由表皮、真皮、血管层3层组成的人体皮肤模型,该芯片包含3个PDMS层和2个用以分隔的聚酯多孔膜,上层膜上表面培养人表皮角质形成细胞,下表面和下层膜上表面培养成纤维细胞,下层膜下表面则培养内皮细胞,培养3 d使3种细胞汇合。该模型成功模拟了皮肤炎症与水肿模型,从而更有针对性的开展透皮药物治疗与皮肤损伤修复。"
| [1] Andersson H, van den Berg A.Microfabrication and microfluidics for tissue engineering: state of the art and future opportunities. Lab Chip. 2004;4(2):98-103 [2] Beauchamp MJ, Nordin GP, Woolley AT. Moving from millifluidic to truly microfluidic sub-100-μm cross-section 3D printed devices. Anal. Bioanal. Chem.Anal Bioanal Chem. 2017; 409(18):4311-4319.[3] Sun X, Nunes SS. Maturation of Human Stem Cell-derived Cardiomyocytes in Biowires Using Electrical Stimulation. J Vis Exp. 2017;(123). [4] Yeon JH, Na D, Choi K,et al. Reliable permeability assay system in a microfluidic device mimicking cerebral vasculatures. Biomed. Microdevices. Biomed Microdevices. 2012;14(6): 1141-1148.[5] Griep LM, Wolbers F, de Wagenaar B,et al.BBB on chip: microfluidic platform to mechanically and biochemically modulate blood-brain barrier function. Biomed Microdevices. 2013;15(1):145-150.[6] Kim JA, Kim HN, Im SK, Chung S,et al.Collagen-based brain microvasculature model in vitro using three-dimensional printed template. Biomicrofluidics. 2015;9(2):024115.[7] Brown JA, Pensabene V, Markov DA, et al. Recreating blood-brain barrier physiology and structure on chip: A novel neurovascular microfluidic bioreactor.Biomicrofluidics. 2015; 9(5):054124.[8] Herland A, van der Meer AD, FitzGerald EA, et al.Distinct Contributions of Astrocytes and Pericytes to Neuroinflammation Identified in a 3D Human Blood-Brain Barrier on a Chip. PLoS One. 2016;11(3):e0150360.[9] Fox EL,Bowers RW,Foss ML.The physiological basis for exercise and sport.1993.[10] Uehata M, Ishizaki T, Satoh H, et al. Calcium sensitization of smooth muscle mediated by a Rho-associated protein kinase in hypertension.Nature. Nature. 1997;389(6654):990-994.[11] Jacot JG, McCulloch AD, Omens JH. Substrate stiffness affects the functional maturation of neonatal rat ventricular myocytes. Biophys. J. Biophys J. 2008;95(7):3479-3487.[12] Grosberg A, Nesmith AP, Goss JA, et al.Muscle on a chip: in vitro contractility assays for smooth and striated muscle. J Pharmacol Toxicol Methods. 2012 ;65(3):126-135.[13] Ma Z, Liu Q, Liu H, et al. Laser-patterned stem-cell bridges in a cardiac muscle model for on-chip electrical conductivity analyses. Lab Chip. 2012;12(3):566-573.[14] Zhang D, Shadrin IY, Lam J, et al. Tissue-engineered cardiac patch for advanced functional maturation of human ESC-derived cardiomyocytes. Biomaterials. 2013;34(23): 5813-5820.[15] Juhas M, Engelmayr GC Jr, Fontanella AN, et al.Biomimetic engineered muscle with capacity for vascular integration and functional maturation in vivo. Proc Natl Acad Sci U S A. 2014; 111(15):5508-5513.[16] Zhang YS, Arneri A, Bersini S, et al.Bioprinting 3D microfibrous scaffolds for engineering endothelialized myocardium and heart-on-a-chip. Biomaterials. 2016;110:45-59.[17] Huh D, Matthews BD, Mammoto A, et al.Reconstituting organ-level lung functions on a chip. Science. 2010;328(5986): 1662-1668.[18] Stucki AO, Stucki JD, Hall SR, et al.A lung-on-a-chip array with an integrated bio-inspired respiration mechanism. Lab Chip. 2015;15(5):1302-1310.[19] Blume C, Reale R, Held M, et al.Temporal Monitoring of Differentiated Human Airway Epithelial Cells Using Microfluidics. PLoS One.2015 ;10(10):e0139872.[20] Schilders KA, Eenjes E, van Riet S, et al.Regeneration of the lung: Lung stem cells and the development of lung mimicking devices. Respir Res.2016;17:44. [21] Kniazeva T, Hsiao JC, Charest JL,et al.A microfluidic respiratory assist device with high gas permeance for artificial lung applications. Biomed Microdevices. 2011;13(2):315-323. [22] Hoganson DM, Pryor HI 2nd, Bassett EK, et al.Lung assist device technology with physiologic blood flow developed on a tissue engineered scaffold platform. Lab Chip.2011;11(4): 700-777. [23] Rochow N, Manan A, Wu WI, et al.An integrated array of microfluidic oxygenators as a neonatal lung assist device: in vitro characterization and in vivo demonstration.Artif Organs. 2014;38(10):856-866.[24] Jang KJ, Suh KY. A multi-layer microfluidic device for efficient culture and analysis of renal tubular cells. Lab Chip. 2010; 10(1):36-42.[25] Jang KJ, Mehr AP, Hamilton GA,et al.Human kidney proximal tubule-on-a-chip for drug transport and nephrotoxicity assessment. Integr Biol (Camb). 2013;5(9):1119-1129. [26] Maschmeyer I, Lorenz AK, Schimek K, et al.A four-organ-chip for interconnected long-term co-culture of human intestine, liver, skin and kidney equivalents. Lab Chip. 2015;15(12):2688-2699.[27] Zhou M, Zhang X, Wen X, et al.Development of a Functional Glomerulus at the Organ Level on a Chip to Mimic Hypertensive Nephropathy. Sci Rep. 2016;6:31771.[28] Kane BJ, Zinner MJ, Yarmush ML, et al.Liver-Specific Functional Studies in a Microfluidic Array of Primary Mammalian Hepatocytes. Anal Chem. 2006;78(13):4291-4298.[29] Lee PJ, Hung PJ, Lee LP et al.An artificial liver sinusoid with a microfluidic endothelial-like barrier for primary hepatocyte culture. Biotechnol Bioeng. 2007;97(5):1340-1346.[30] Lee SA, No da Y, Kang E, et al.Spheroid-based three-dimensional liver-on-a-chip to investigate hepatocyte- hepatic stellate cell interactions and flow effects. Lab Chip. 2013;13(18):3529-3537. [31] Bhise NS, Manoharan V, Massa S,et al.A liver-on-a-chip platform with bioprinted hepatic spheroids. Biofabrication. 2016;8(1):014101. [32] Ong LJY, Chong LH, Jin L, et al.A pump-free microfluidic 3D perfusion platform for the efficient differentiation of human hepatocyte-like cells. Biotechnol Bioeng. 2017;114(10): 2360-2370. [33] Banaeiyan AA, Theobald J, Paukštyte J,et al.Design and fabrication of a scalable liver-lobule-on-a-chip microphysiological platform. Biofabrication. 2017 ;9(1):015014.[34] O'Neill AT, Monteiro-Riviere NA, Walker GM,et al.Characterization of microfluidic human epidermal keratinocyte culture. Cytotechnology. 2008;56(3):197-207. [35] Ataç B, Wagner I, Horland R, et al.Skin and hair on-a-chip: in vitro skin models versus ex vivo tissue maintenance with dynamic perfusion. Lab Chip. 2013;13(18):3555-3561. [36] Ilka Wagner, Beren Atac, Gerd Lindner ,et al.Skin and hair-on-a-chip: Hair and skin assembly versus native skin maintenance in a chip-based perfusion system. BMC Proc. 2013;7:P93.[37] Abaci HE,Gledhill K,Guo Z,AM,et al.Pumpless microfluidic platform for drug testing on human skin equivalents. Lab Chip.2015;15(3):882-888. [38] Wufuer M,Lee G,Hur W,et al.Skin-on-a-chip model simulating inflammation, edema and drug-based treatment.Sci Rep.2016; 6:37471. |
| [1] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [2] | Zeng Yanhua, Hao Yanlei. In vitro culture and purification of Schwann cells: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1135-1141. |
| [3] | Xu Dongzi, Zhang Ting, Ouyang Zhaolian. The global competitive situation of cardiac tissue engineering based on patent analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 807-812. |
| [4] | Wu Zijian, Hu Zhaoduan, Xie Youqiong, Wang Feng, Li Jia, Li Bocun, Cai Guowei, Peng Rui. Three-dimensional printing technology and bone tissue engineering research: literature metrology and visual analysis of research hotspots [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 564-569. |
| [5] | Chang Wenliao, Zhao Jie, Sun Xiaoliang, Wang Kun, Wu Guofeng, Zhou Jian, Li Shuxiang, Sun Han. Material selection, theoretical design and biomimetic function of artificial periosteum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 600-606. |
| [6] | Liu Fei, Cui Yutao, Liu He. Advantages and problems of local antibiotic delivery system in the treatment of osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 614-620. |
| [7] | Li Xiaozhuang, Duan Hao, Wang Weizhou, Tang Zhihong, Wang Yanghao, He Fei. Application of bone tissue engineering materials in the treatment of bone defect diseases in vivo [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 626-631. |
| [8] | Zhang Zhenkun, Li Zhe, Li Ya, Wang Yingying, Wang Yaping, Zhou Xinkui, Ma Shanshan, Guan Fangxia. Application of alginate based hydrogels/dressings in wound healing: sustained, dynamic and sequential release [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 638-643. |
| [9] | Chen Jiana, Qiu Yanling, Nie Minhai, Liu Xuqian. Tissue engineering scaffolds in repairing oral and maxillofacial soft tissue defects [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 644-650. |
| [10] | Xing Hao, Zhang Yonghong, Wang Dong. Advantages and disadvantages of repairing large-segment bone defect [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 426-430. |
| [11] | Chen Siqi, Xian Debin, Xu Rongsheng, Qin Zhongjie, Zhang Lei, Xia Delin. Effects of bone marrow mesenchymal stem cells and human umbilical vein endothelial cells combined with hydroxyapatite-tricalcium phosphate scaffolds on early angiogenesis in skull defect repair in rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3458-3465. |
| [12] | Wang Hao, Chen Mingxue, Li Junkang, Luo Xujiang, Peng Liqing, Li Huo, Huang Bo, Tian Guangzhao, Liu Shuyun, Sui Xiang, Huang Jingxiang, Guo Quanyi, Lu Xiaobo. Decellularized porcine skin matrix for tissue-engineered meniscus scaffold [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3473-3478. |
| [13] | Mo Jianling, He Shaoru, Feng Bowen, Jian Minqiao, Zhang Xiaohui, Liu Caisheng, Liang Yijing, Liu Yumei, Chen Liang, Zhou Haiyu, Liu Yanhui. Forming prevascularized cell sheets and the expression of angiogenesis-related factors [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3479-3486. |
| [14] | Liu Chang, Li Datong, Liu Yuan, Kong Lingbo, Guo Rui, Yang Lixue, Hao Dingjun, He Baorong. Poor efficacy after vertebral augmentation surgery of acute symptomatic thoracolumbar osteoporotic compression fracture: relationship with bone cement, bone mineral density, and adjacent fractures [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3510-3516. |
| [15] | Liu Liyong, Zhou Lei. Research and development status and development trend of hydrogel in tissue engineering based on patent information [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3527-3533. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||