Chinese Journal of Tissue Engineering Research ›› 2018, Vol. 22 ›› Issue (6): 971-978.doi: 10.3969/j.issn.2095-4344.0077
Previous Articles Next Articles
Application of hydroxyapatite functional graded biomaterials in human hard tissue replacement
- 1Department of Stomatology, Affiliated Hospital of Binzhou Medical University, Binzhou 256603 Shandong Province, China; 2Liaocheng Veteran Hospital, Liaocheng 252000, Shandong Province, China
-
Received:2017-09-01Online:2018-02-28Published:2018-02-28 -
Contact:Wang Qing-shan, Professor, Master’s supervisor, Department of Stomatology, Affiliated Hospital of Binzhou Medical University, Binzhou 256603 Shandong Province, China -
About author:Wei Wei, Studying for master’s degree, Department of Stomatology, Affiliated Hospital of Binzhou Medical University, Binzhou 256603 Shandong Province, China -
Supported by:the Medical and Health Science and Technology Development Plan of Shandong Province, No. 2013WS0308; the Natural Science Foundation of Shandong Province, No. ZR2013HM044
CLC Number:
Cite this article
Wei Wei, Shu Jing-ai, Wang Jing, Zheng Li-xia, Li Lu, Wang Qing-shan. Application of hydroxyapatite functional graded biomaterials in human hard tissue replacement[J]. Chinese Journal of Tissue Engineering Research, 2018, 22(6): 971-978.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
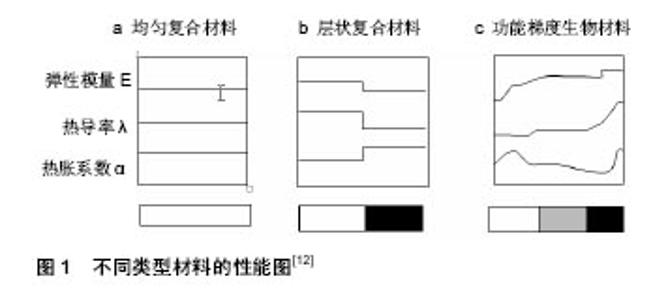
2.1 硬组织替代与羟基磷灰石功能梯度生物材料 人体硬组织结构主要包括牙齿和骨骼,这些组织中除含有一部分有机成分(如胶原)和水外,大部分以无机盐如羟基磷灰石结晶的形式存在。人工合成的羟基磷灰石具有良好的骨传导性,能刺激新骨生长,并与人体骨组织形成牢固的化学键性结合,而且不引起任何局部或系统的毒性及炎症,也不会出现异物反应。硬组织替代除要求有良好的生物学性能外,还必须有足够的力学强度。功能梯度复合材料采用先进的材料复合技术,使材料的组成、结构等由一侧向另一侧呈连续变化,从而使其性能也呈梯度变化[10]。据此,功能梯度生物材料的设计思路为:中心层为金属、高强度陶瓷或高分子材料,作为力学承载区,以承担人体的各种运动载荷;中间层为过渡层,随着梯度层数的增多,相邻层间组分含量的差异减小,层间界面的相容性提高,不同热膨胀系数可减小产生的残余应力,因而各层间的结合更加紧密,力学性能也得以提高;表层为羟基磷灰石等生物活性材料,由于该类材料的中的钙、磷离子可与生物体液中的钙、磷进行交换,构成离子通道,多孔结构引导新生骨组织在空隙表面生长,从而有利于成骨细胞沉积,引导新骨形成,实现材料与生物骨组织间产生紧密的骨性结合,而且不会引起排异、积水、腐蚀、炎症等。 功能梯度复合材料是一种全新的材料,它既解决了复合材料的界面应力问题,同时又保持了材料的复合特性。由于功能梯度复合材料中过渡层的组元成分呈梯度变化,所以其热应力性能也是逐渐变化的,这与均匀复合材料和常规的层状复合材料有着本质上的区别[11]。图1为不同类型材料的性能示意图[12],分别显示了均匀复合材料、层状复合材料和功能梯度复合材料的弹性模量E、热导率λ、热膨胀系数α及成分在厚度方向上的变化。常规复合材料的性能参数在界面处发生突变,而功能梯度复合材料具有连续变化的热力学性能[13],这种连续的变化在缓和热应力型金属/陶瓷功能梯度复合材料中得到了充分体现。国内外学者在功能梯度复合材料成分设计理论的基础上,提出了成分分布模型,如Wakashima等[14]采用幂函数来描述材料的成分分布f(x)):f(x)=(x/d)p×f(s),公式中x代表层数,即由内向外分别为1、2、3…n,d为梯度总层数;f(s)为常数,若表面为单一材料,则f(s)=100%;p为梯度指数。通过数值改变,f(x)曲线的形状相应改变;适当改变p值可以满足成分设计要求,从而得到热应力缓和、力学和生物学性能最优的功能梯度复合材料。"
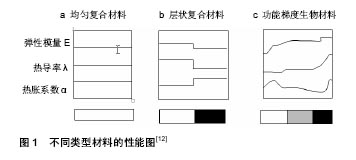
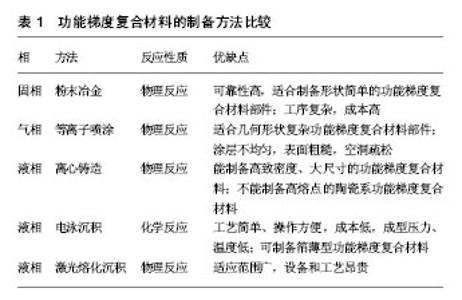
功能梯度生物材料用于硬组织替代主要有陶瓷基、金属基、聚合物基功能梯度复合材料[15]。氧化锆陶瓷基和金属基功能梯度复合材料具有较高的机械强度和硬度、良好的力学性能及易加工性和稳定性等,被广泛应用于医学硬组织修复[16]。聚合物基功能梯度复合材料主要成分包括聚乙烯和聚丙烯,是现今功能复合材料研究的前沿领域,具有质轻、无毒性、较强的抗冲击和抗摩擦性等优点,主要用于人工关节的替换[17-18]。 2.2 功能梯度生物材料的制备方法 材料制备是功能梯度生物材料的核心,通过设计不同的梯度层数、中心层厚度、梯度指数来获得最佳梯度组成的结构模型,从而采用适当方法制备出符合临床要求的功能梯度复合材料。近年来研究和应用较多的制备方法有粉末冶金、等离子喷涂、离心铸造、电泳沉积等[19],见表1。"

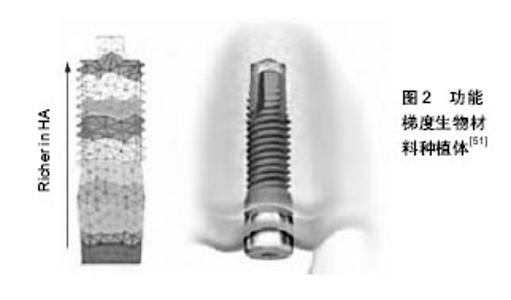
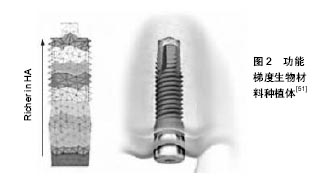
2.2.1 粉末冶金 粉末冶金法是将原始粉末按设计的不同配比均匀混合后,以梯度分布方式变化的规律进行逐层堆积,压制成所需形状形成生坯,最后通过常压烧结、热压烧结、等静压烧结等方式合成热应力缓和的功能梯度材料,可用于金属基或陶瓷基羟基磷灰石功能梯度复合材料的制备[20]。粉末冶金法具有设备简单、易于操作、成本低、可控制粉末粒度、烧结温度等优点,是目前最常用的梯度功能材料的制备方法。已有应用该方法制备出钛基生物陶瓷材料的报道[21]。Fuji等[22]使用粉末冶金法制成了钛基纳米羟基磷灰石生物梯度材料和钛基氧化钇稳定四方相氧化锆生物梯度功能材料,并测得其具有较好的抗剪切强度、断裂韧性、维氏硬度及抗弯强度。粉末冶金方法制备的多孔梯度功能材料层与层之间梯度变化连续性较差,不能完全消除界面间的应力分布且空隙不连通,影响了组织液流通和纤维组织的生长,因此,如何实现组分间梯度变化是粉末冶金研究的重点。 2.2.2 等离子喷涂法 等离子喷涂发展于20世纪50年代[23],目前已成为制备生物涂层最广泛的技术,并得到越来越多的材料学家的重视。等离子喷涂是将不同配比粉末材料作为原料送入设备中,通过等离子流使粉末加速、融化或部分融化,在冲击力的作用下将不同组合比例的粉末分层叠加喷射到基材表面,形成功能梯度复合材料[6]。该方法由于其焰流温度较高,可熔化几乎所有高熔点和高硬度材料,因此适用于陶瓷-金属系功能梯度材料的制作,如钛基羟基磷灰石或钛基氧化锆陶瓷功能梯度生物材料。与其他喷涂方法相比[7],该法得到的功能梯度复合材料涂层致密性好,稳定性及结晶性显著提高,并在一定程度上克服了陶瓷的脆性,耐磨性及韧性显著增强。但由于单一涂层与金属基体间热膨胀系数匹配性差,界面间热应力大且界面结合主要为机械结合,因而容易导致涂层出现裂纹及剥落。通过优化工艺参数、改进喷涂方式和材料配比等,能够显著提高钛基与羟基磷灰石涂层的结合强度[24-25]。Baino等[26]采用等离子喷涂法,通过对涂层孔隙率、结合强度、相对耐磨性检测分析,验证了硅灰石作为涂层材料可与基体间形成均匀、连续的界面,提高结合强度,减少涂层孔隙、裂纹等。鲍雨梅等[27]采用等离子喷涂技术制备成以钛合金为基底含30%氧化锆的羟基磷灰石生物陶瓷复合涂层功能梯度复合材料,观察发现羟基磷灰石涂层表面覆盖着针片状晶粒,其结构致密、均匀,截面以无规则细小的气孔为主,ZrO2中间过渡层分别与羟基磷灰石涂层、基体结合界面实现良好的机械结合。 2.2.3 离心铸造法 离心铸造法是将不同合金金属液放入高速旋转铸件中,在离心作用下金属液充填铸件并凝固,形成强化相呈梯度发布的功能材料的方法[28]。其基本原理是离心力产生质点偏倚,强化相质点与液态金属熔体之间产生密度差,通过控制加工时间、颗粒尺寸、转速、温度来制备高致密度的功能梯度材料。该方法生产效率高,成本低,设备简单。其缺点是合金金属液体间必须有密度差,因此难以制备出高熔点的陶瓷系梯度材料,一般仅适用于圆筒类铸件。El-Hadad等[29]采用离心铸造法制备了铝基氧化锆功能梯度材料,结果显示不同的材料耐磨性与离心力大小有关,通过控制氧化锆及合金铝颗粒的取向和体积分数可增强其耐磨性。 2.2.4 电泳沉积技术 电泳电沉积是利用电泳动现象,在低温条件下使金属、陶瓷、有机涂料等胶体颗粒在电极表面沉积形成沉积层,得到功能梯度材料的化学制备方法[30]。电沉积法作为低温液相制备技术,由于设备简单、操作方便等优点适用于制备薄膜型功能梯度材料。国外学者采用电泳法制备梯度功能材料的实验较多,如Huang等[31]采用电泳电沉积将纳米羟基磷灰石作为涂层附着于金属钛的表面,内层为致密的纯氧化钛,中间为羟基磷灰石/TiO2混合过渡层,外层为纯羟基磷灰石层,制备出以纯钛为基体,表面为纯多孔纳米羟基磷灰石的梯度功能材料,使其既有优异的机械性能,又具有良好的生物学性能。Salahi等[32]采用电泳电沉积成功制备了AL2O3/ZrO2梯度功能材料,由于中间成分的梯度变化,消除了材料间宏观界面,提高了涂层间结合强度,且具有良好的耐腐蚀性及抗热冲击性能。 2.2.5 激光熔化沉积技术 激光熔化沉积技术是一种新型制备梯度功能材料的技术,它融合了传统粉末冶金法及激光熔覆技术的优点,采用计算机逐点连续添加原理,通过高功率激光熔化同步输送原材料,逐层堆积,并由计算机辅助设计模型,最终得到高性能梯度复合材料及试件[33]。该技术集材料设计、制备、成形智能化于一体,代表了未来的发展方向。目前采用该方法已制备出性价比更高的试件,Li等[34]通过激光熔化沉积技术制备Ti/SiC功能梯度复合材料, 用扫描电子显微镜、显微硬度计、磨损试验机等对激光熔覆层组织及性能进行观察和分析,结果表明Ti/SiC功能梯度复合材料硬度、耐磨性及耐蚀性明显增强,显示出激光熔化沉积在制备梯度复合结构上的优势。随着3D打印技术的发展,相信不久的将来,激光熔化沉积将打印出表面为羟基磷灰石的临床所需硬组织替代物或种植体。 2.3 功能梯度生物材料的性能评价 功能梯度生物材料硬组织替代物制备后必须对其性能进行评价,达到植入物各项性能要求后才能应用于临床。功能梯度生物材料的性能评价是指在一定条件下,对试件各种性能进行测试,根据性能评价结果判断试件是否满足硬组织替代的设计要求,从而筛选出最优化的材料配比和成分分 布[35-36]。根据临床对硬组织替代材料的要求,结合功能梯度生物材料的性能特征,功能梯度生物材料的性能评价主要对力学性能及生物学性能进行测试,包括断裂韧性、耐磨性、抗弯强度、黏结强度及生物学特性5个方面。 2.3.1 断裂韧性 是材料抵抗裂纹扩展断裂的性能,是材料抵抗脆性破坏的韧性参数。通常采用压痕法对其进行性能表征。Genga等[37]成功制备了氧化锆基氧化铝梯度功能材料,内层为纯的氧化锆粉体,中间层为氧化铝与氧化锆粉体梯度混合层,外层为纯的氧化铝粉体,功能梯度复合材料从内层到外侧随氧化铝含量的增加其硬度、断裂韧性和颗粒尺寸量相应增强并呈一定的梯度变化,在氧化铝含量占总体积分数90%时,其硬度高达17.65 GPa。实验结果表明,梯度层的存在增强了材料的断裂韧性。Askari等[38]采用电泳沉积与热等静压技术相结合,SiC作为中间层,在氩气中,从室温经过2 h缓慢升至1 800 ℃成功制备了Al2O3/SiC/ZrO2梯度功能材料。疲劳测试结果显示外层含有SiC的硬度远大于内层断裂韧性,通过结果对比表明SiC提高外层压应力。 2.3.2 耐磨性 耐磨性是指材料的磨损性能,耐磨性几乎与材料的所有性能都有关系。人体关节在承受各种负荷时会产生磨损,因此材料的耐磨性是制备耐磨材料的首要问题[39]。Radhika[40]研究不同Cu含量对Al-Si12Cu/Al2O3功能梯度复合材料耐磨性的影响时,发现Cu的加入降低了功能梯度复合材料的摩擦系数,且随着Cu含量的增加,Al-Si12Cu/Al2O3功能梯度复合材料的耐磨性能先增加后降低,表明通过设计多元梯度过渡层可实现成分和性能上的逐渐过渡,提高材料的抗摩擦、磨损等性能。Ji等[41]利用磁控溅射技术和等离子体增强化学气相沉积及阴极电弧离子镀技术,在硬质合金表面沉积了Cr、TiAl、TiAlN、Cr/TiAl/TiAlN结构的梯度过渡类金刚石涂层,经试验测试300圈时磨损直径为0.203 1 mm,有效提高了硬质合金的耐磨性能,说明梯度层可在提高材料硬度,增加抗磨损能力。 2.3.3 抗弯强度 抗弯强度指材料受外力时抵抗弯曲不断裂的能力。一般测试试件的三点或四点弯曲强度,加力至试样断裂,利用公式计算出数值。Yang等[42]以生物相容性优良的FeCrAl纤维增强羟基磷灰石并同时采用功能梯度材料的梯度层递进缓和残余应力,在 1 050 ℃的条件下制备羟基磷灰石/FeCrAl纤维功能梯度材料,采用扫描电子显微镜、投射电子显微镜和X射线衍射手段对制备的样品进行表征,测试结果表明,FeCrAl纤维增加促使复合材料断裂韧性得到提高,且随纤维加入,羟基磷灰石与FeCrAl结合更紧密。 2.3.4 黏结强度 黏结强度是在同种物质内部相邻各部分之间的相互吸引力,用试验机对试件各梯度层施加垂直向力时致粘结面分离或破碎的最大力值,根据公式计算黏结强度。杜菲菲[43]采用射频磁控溅射法在Ti-6Al-4V基板上沉积了钛层及镍钛层制备了TiN/Ti多层膜,利用X射线衍射仪、扫描电子显微镜、显微硬度仪和划痕仪测量分析了硬度及薄膜与基体之间的结合力,结果表明与单层镍钛薄膜相比,多层镍钛薄膜的硬度显著提高,当Ti/N=30层时,薄膜与基体的界面结合强度达73 N。 2.3.5 生物特性 主要测验材料的生物相容性、生物活性。生物相容性是材料植入人体后与人体相容程度,是否会对人体组织造成毒害作用,包括血液相容性和组织相容性;生物活性是指引导正常细胞发生生理功能的能力,从而使生物材料与机体骨组织产生化学键合。研究发现,纳米羟基磷灰石生物陶瓷与组织之间具有良好的生物相容性、优良的骨结合、骨诱导、骨传导性。Lin等[44]研究发现,羟基磷灰石可与胶原蛋白复合制备成功能梯度生物材料,比单纯的羟基磷灰石功能梯度复合材料表现出更好的生物相容性及更为显著的骨结合和诱导能力。 2.4 功能梯度生物材料在人工牙根中的应用 凭借优异的力学性能和生物相容性,医用钛及钛合金成为人工牙根植入的基本材料[45]。但由于纯钛和钛合金都是生物惰性金属[46],其结构和成分与骨组织差异大,不易与骨组织形成良好的界面结合,导致种植体稳定性差且负重所需时间较长,存在种植体周围炎、种植体松动等问题。另外由于种植体-牙龈边缘处容易形成灰色线,尤其在上颌前牙区则会严重影响美观[47-48]。相比纯钛,氧化锆有较高的断裂韧性和弯曲强度,生物相容性和美观性均优于同期观察的钛种植体,但也存在生物活性差的缺陷。纳米羟基磷灰石在成分、结构、形态上与骨和牙组织的磷灰石相似,具有良好的生物活性和化学稳定性,能与骨组织形成紧密的化学结合,可诱导骨形成,但不足的是纳米羟基磷灰石强度低、脆性大,达不到种植体所需要的机械强度,在临床应用中受到限制。国内外对牙种植体材料的研究表明,单一的牙种植体材料无法同时具备优良的生物相容性、生物活性和力学性能[49]。为了提高牙种植体的生物相容性和力学性能,学者们试图将纳米羟基磷灰石作为涂层材料应用于种植体表面。但是,种植牙植入后因结合强度较低易发生涂层的溶解、吸收和脱落,崩解的涂层可激发吞噬细胞反应引起快速骨吸收。 种植牙植入后,种植体与周围软硬组织的结合界面直接关系到种植体的稳定性是种植成功的关键[50]。功能梯度生物材料作为新一代人工牙根植入材料,具有特殊的组成结构,如图2所示[51],中心层为高强度金属或陶瓷基,中间为过渡层,表层为纯生物活性材料,从而既充分发挥了各材料的性能优势又使各组分间产生牢固的机械结合和化学结合,有望解决涂层脱落、种植体稳定性差等问题[5]。 Hedia等[52]在钛表面涂覆羟基磷灰石及胶原质制备钛基功能梯度生物材料,外层为疏松多孔的羟基磷灰石及胶原质,中间层逐渐梯度过渡,中心为致密的氧化钛,发现其与下颌骨的皮质骨、松质骨紧密接触,大幅度降低了皮质骨和松质骨的最大应力。Lin等[44,53]用约4年的时间实验观察钛-羟基磷灰石功能梯度复合材料对下颌骨骨组织的影响,发现钛基多孔纳米羟基磷灰石功能梯度材料能够促进成骨细胞的粘附及生长,具有良好的生物诱导活性、生物相容性和骨传导性。丁元圣[54]研究含氟羟基磷灰石涂层钛合金及钛合金正畸微种植体植入后,骨结合状况及对种植体周围炎发生、发展的影响,将两者分别植入白兔两侧下颌前磨牙区颊侧牙槽骨,应用电镜观察种植体周围骨结合的状态,显示含氟羟基磷灰石涂层的骨组织相容性较好,对种植体周围炎能起到一定的抑制作用。周立伟等[55]应用纳米羟基磷灰石/聚醚醚酮仿生种植材料在150 N垂直加载条件下,观察种植体周围骨皮质及骨松质的应力分布,发现纳米羟基磷灰石/聚醚醚酮材料更有利于将种植体所受载荷以应力的形式传递到周围骨组织中去,有利于保持骨结合面的长期稳定。 上述研究表明,种植体表面羟基磷灰石的应用,能够显著提高骨结合强度,而梯度技术则避免了表层羟基磷灰石的脱落。应用3D打印技术在计算机控制下,根据CAD模型,利用激光熔化沉积技术逐层沉积直接制造出种植体应为今后的发展方向。采用该方法可将20- 60 µm厚度的金属薄层结合在一起制备出形态复杂多样、空隙结构呈梯度变化的种植体,由于其强度更接近密质骨,也称为等弹性种植体[56]。 2.5 功能梯度生物材料在骨组织中的应用 骨组织是由松质骨和密质骨组成的一种结缔组织,具有致密而坚硬的特点,有较小缺损时具有自我修复能力,但骨组织较大缺损如创伤、骨骼疾病或骨肿瘤切除等原因却无法通过骨再生和自我修复来达到恢复其相应生理功能的效 果[57-58]。组织工程学的发展为骨缺损的修复提供了新的选择。目前临床应用较为广泛的骨缺损替代材料主要为生物金属材料如钛、钛合金、316L不锈钢,Co-Cr-Mo合金和生物陶瓷如含氟羟基磷灰石、β-磷酸三钙生物陶瓷等[59]。金属材料具有良好的力学性能但缺乏良好的生物相容性,生物陶瓷材料生物相容性好,但不能承受较大的组织负荷。为弥补缺陷通常在金属合金的表面涂覆纳米羟基磷灰石来改善其生物活性,但由于金属与纳米羟基磷灰石之间成分和热膨胀系数差别较大,因而其结合强度较低。 有学者提出理想的骨修复支架应具有骨结合性、骨传导性和骨诱导性、生物相容性,以及良好的力学性能、一定的生物降解性、高孔隙率且相互连通[60]。金属/生物陶瓷功能梯度材料凭借其良好的骨界面结合、材料间的密切结合等优点在硬组织替代中具有广阔的发展前景。其制备方法包括等离子喷涂法、粉末冶金、自蔓延高温合成、电泳沉积、3D打印技术等[61]。有研究采用等离子喷涂法制备生物活性玻璃/纳米羟基磷灰石功能梯度复合材料,表现出良好的生物活性和高耐磨性,在沉积相下显现出致密、均匀一致的涂层,在骨整合过程中植入物有良好的稳定性和较低降解性[62]。程瑶等[63]制备未掺杂纳米结构羟基磷灰石与多元掺杂纳米结构羟基磷灰石,将其放入小鼠成骨前体细胞中对比两者对成骨前体细胞增殖和分化的影响,发现多元掺杂纳米结构羟基磷灰石更有利于成骨细胞矿化。3D打印技术以快速、高精度、高强度、个性化的优势在医学领域尤其是人工骨制造中的应用越来越广泛。张钰[64]基于熔融沉积成型原理,利用3D打印装置在最优打印条件下制造出塑料聚醚醚酮仿生人工骨,突破了其只能用注塑和激光烧结制造的局限,通过建立3D打印模型可获得成形质量良好、满足技术要求的聚醚醚酮仿生人工骨。 "
| [1]Li L,Zhang D.Dynamic analysis of rotating axially FG tapered beams based on a new rigid-flexible coupled dynamic model using the B-spline method.Compos Struct.2015;124:357-367.[2]Papia E,Jimbo R,Chrcanovic BR,et al.Surface structure and mechanical properties of impaction-modified Y-TZP.Dent Mater.2014;30(8):808-816. [3]Chao SC,Wang MJ,Pai NS,et al.Preparation and characterization of gelatin–hydroxyapatite composite microspheres for hard tissue repair.Mater Sci Eng C Mater Biol Appl.2015;57:113-122.[4]新野正之,平井敏雄,渡边龙三.倾斜机能材料-宇宙机用超耐热材料应用[J].日本复合材料学会志,1987,13(6):257-264.[5]Xuereb M,Camilleri J,Attard NJ.Systematic review of current dental implant coating materials and novel coating techniques.Int J Prosthodont.2015;28(1):51-59.[6]Hanane MA,Khalid EB,Rhali B.Geometrically Non-Linear Free Vibration of Fully Clamped FGM Skew Plates Using Homogenization Technique.Adv Mater Res.2015;1105: 370-380. [7]Bai X,More K,Rouleau CM,et al.functionally graded hydroxyapatite coatings doped with antibacterial components.Acta Biomaterial.2010;6(6):2264-2273.[8]Bykov YV,Egorov SV,Eremeev AG,et al.Temperature profile optimization for microwave sintering of bulk Ni–Al2O3 functionally graded materials.J Mater Proc Technol.2014; 214(2):210-216.[9]Duarte Campos DF,Vogt M,Lindner M,et al.Two-photon laser scanning microscopy as a useful tool for imaging and evaluating macrophage-, IL-4 activated macrophage‐and osteoclast‐based In Vitro degradation of beta-tricalcium phosphate bone substitute material.Microsc Res Tech. 2014;77(2):143-152. [10]Helal WMK,Shi DY.FE Analysis of Functionally Graded Material Plate during Debonding Case with Different Boundary Conditions.Key Eng Mater.2015;627:57-60. [11]Ramu I,Mohanty SC.Buckling Analysis of Rectangular Functionally Graded Material Plates under Uniaxial and Biaxial Compression Load.Procedia Eng.2014;86:748-757. [12]高晓菊,王伯芊,贾平斌,等.功能梯度材料的制备技术及其研发现状[J].材料导报,2014,28(1):31-36.[13]Jin ZH,Paulino GH.Transient thermal stress analysis of an edge crack in a functionally graded material.Int J Fract. 2001;107(1):73-98.[14]Wakashima K,Hirano T,Niino M.Functionally Gradient Materials(Fgm)Architecture: A New Type of Ceramic-Metal Assemblage Designed for Hot Structural Components.Proc. of the ESA Symp. on Space Applications of Advanced Structural Materials (ESA SP-303),ESTEC-ESA,1990.[15]张勇.功能梯度材料制备方法的研究现状[J].热加工工艺, 2012, 41(18):14-16.[16]Pompe W,Worch H,Epple M,et al.Functionally graded materials for biomedical applications.Mater Sci Eng A. 2003;362(1):40-60. [17]Ai Z,Xiang Z,Li Y,et al.Conversion of monkey fibroblasts to transplantable telencephalic neuroepithelial stem cells. Biomaterials.2016;77:53-65. [18]Bahraminasab M,Sahari BB,Edwards KL,et al.Material tailoring of the femoral component in a total knee replacement to reduce the problem of aseptic loosening. Mater Design.2013;52(7):441-451. [19]Sola A,Bellucci D,Cannillo V.Functionally graded materials for orthopedic applications–an update on design and manufacturing.Biotechnol Adv.2016;34(5):504-531.[20]Xu L,Zhang F,Yue X,et al.Advance on Al2O3 Particulates Reinforced Aluminum Metal Matrix Composites (Al-MMCs) Manufactured by the Power Metallurgy (PM) Methods- Improved PM Techniques.MATEC Web of Conferences. 2016;67:06098. [21]Arifin A,Sulong AB,Muhamad N,et al.Material processing of hydroxyapatite and titanium alloy (HA/Ti) composite as implant materials using powder metallurgy: a review.Mater Design.2014;55:165-175. [22]Fuji T,Tohgo K,Araki H,et al.Fabrication and strength evaluation of biocompatible ceramic-metal composite material.J Solid Mech MaterEng.2010;4(11):1699-1699. [23]Koch D,Mauer G,Vaßen R.Manufacturing of Composite Coatings by Atmospheric Plasma Spraying Using Different Feed-Stock Materials as YSZ and MoSi2.J Therm Spray Technol.2017:1-9.[24]Levingstone TJ,Barron N,Ardhaoui M,et al.Application of response surface methodology in the design of functionally graded plasma sprayed hydroxyapatite coatings.Surf Coat Technol.2017;313: 307-318.[25]Pakseresht AH,Javadi AH,Ghasali E,et al.Evaluation of hot corrosion behavior of plasma sprayed thermal barrier coatings with graded intermediate layer and double ceramic top layer.Surf Coat Technol.2016;288:36-45.[26]Baino F,Vitale-Brovarone C.Wollastonite containing bio-ceramic coatings on alumina substrates: Design considerations and mechanical model.Ceram Int. 2015;41(9): 11464-11470.[27]鲍雨梅,徐哲玉,马龙,金志伟.氧化锆增强HA涂层的制备及其磨损性能[J].中国陶瓷,2016,58(4):58-63.[28]Radhika N,Raghu R.Development of functionally graded aluminium composites using centrifugal casting and influence of reinforcements on mechanical and wear properties.Trans Nonferrous Met Soc China. 2016;26(4):905-916. [29]El-Hadad S,Sato H,Watanabe Y.Wear of Al/Al 3 Zr functionally graded materials fabricated by centrifugal solid-particle method. J Mater Proc Technol.2010;210(15):2245-2251.[30]Abdel Hamid Z,El-Etre AY,Fareed M.Performance of Ni-Cu/ZrO2 nano-composite coatings fabricated by electrodeposition technique.Anti-Corrosion Methods Mater. 2017;64(3):315-325.[31]Huang J,Ni Y,Wang Z.Preparation of hydroxyapatite functionally gradient coating on titanium substrate using a combination of electrophoretic deposition and reaction bonding process.Surf Coat Technol.2010;204(21):3387-3392.[32]Salahi E,Esfahani H,Mobasherpour I,et al.Sintering behavior and mechanical properties of alumina/zirconia multilayers composite via nano-powder processing.Ceram Int.2014;40(2): 2717-2722.[33]Salonitis K,D’Alvise L,Schoinochoritis B,et al.Additive manufacturing and post-processing simulation: laser cladding followed by high speed machining.Int J Adv Manuf Technol. 2016;9(85):2401-2411. [34]Li SN,Xiong HP,Li N,et al.Mechanical properties and formation mechanism of Ti/SiC system gradient materials fabricated by in-situ reaction laser cladding.Ceram Int. 2017; 43(1):961-967.[35]Verma G.Functionally Graded Materials.Res J Eng Technol. 2016;7(4):182.[36]Rego BV,Sacks MS.A functionally graded material model for the transmural stress distribution of the aortic valve leaflet.J Biomech.2017;54:88-95.[37]Genga RM,Akdogan G,Polese C,et al.Abrasion wear, thermal shock and impact resistance of WC-cemented carbides produced by PECS and LPS.Int J Refract Metals Hard Mater. 2015;49:133-142. [38]Askari E,Mehrali M,Metselaar IH,et al.Fabrication and mechanical properties of AL2O3/SiC/ZrO2 functionally graded material by electrophoretic deposition.J Mech Behav Biomed Mater. 2012;12:144-150.[39]张波,郭艾.磨损颗粒引发假体周围骨溶解的机制及药物治疗进展[J].中国骨质疏松杂志,2007,13(8):596-599.[40]Radhika N. Mechanical Properties and Abrasive Wear Behaviour of Functionally Graded Al-Si12Cu/Al2O3 Metal Matrix Composite.Trans Indian Ins Metals. 2017;70(1):145-157. [41]Ji X, Xu Z,He L,et al.Effects of Different Inter layers on the Adhesion and Wear Resistance of Diamond-like-carbon Coatings.Vacuum.2013;50(6):1-6.[42]Yang H,Li J,Fang H,et al.Synthesis,characterization and biological activity in vitro of FeCrAl (f)/HA asymmetrical biological functionally gradient materials.J Cent South Univ.2014;21(2):447-453.[43]杜菲菲.反应溅射TiN梯度薄膜及其力学性能研究[D].东北大学,2014.[44]Lin D,Li Q,Li W,et al.Bone remodeling induced by dental implants of functionally graded material.Biomed Mater Res B Appl Biomater.2010;92(2):430-438.[45]Dang Y,Zhang L,Song W,et al.In vivo osseointegration of Ti implants with a strontium-containing nanotubular coating.Int J Nanomedicine.2016;11:1003-1011. [46]Siddiqi A,Kieser JA,De Silva RK,et al.Soft and Hard Tissue Response to Zirconia versus Titanium One‐Piece Implants Placed in Alveolar and Palatal Sites: A Randomized Control Trial.Clin Implant Dent Relat Res.2015;17(3):483-496.[47]Wittneben JG,Buser D,Salvi GE,et al.Complication and Failure Rates with Implant‐Supported Fixed Dental Prostheses and Single Crowns: A 10‐Year Retrospective Study.Clin Implant Dent Relat Res. 2014;16(3):356-364.[48]van Velzen FJ,Ofec R,Schulten EA,et al.10‐year survival rate and the incidence of peri‐implant disease of 374 titanium dental implants with a SLA surface: a prospective cohort study in 177 fully and partially edentulous patients.Clin Oral Implants Res.2015;26(10):1121-1128. [49]Xuereb M,Camilleri J,Attard NJ.Systematic review of current dental implant coating materials and novel coating techniques. Int J Prosthodont.2015;28(1):51-59.[50]Chrcanovic BR,Kisch J,Albrektsson T,et al.Factors influencing early dental implant failures. J Dent Res. 2016;95(9):995-1002.[51]Sadollah A,Bahreininejad A.Optimum gradient material for a functionally graded dental implant using metaheuristic algorithms.J Mech Behav Biomed Mater. 2011;4(7):1384-1395.[52]Hedia HS,Aldousari SM,Abdellatif AK,et al.A new design of cemented stem using functionally graded materials(FGM).Biomed Mater Eng.2014;24(3):1575-1588. [53]Raza MR,Sulong AB,Muhamad N,et al.Effects of binder system and processing parameters on formability of porous Ti/HA composite through powder injection molding.Adv Mater Res.2015;87:386-392.[54]丁元圣.含氟羟基磷灰石涂层(FHA)钛合金正畸微种植体对骨结合界面周围炎症的影响[D].佳木斯大学,2015.[55]周立伟,陈向深,乔永刚,等.纳米羟基磷灰石/聚醚醚酮复合种植体受力的三维有限元分析[J].口腔医学研究, 2016,32(4):391-394.[56]Xu W,Brandt M,Sun S,et al.Additive manufacturing of strong and ductile Ti–6Al–4V by selective laser melting via in situ martensite decomposition.Acta Materialia.2015;85:74-84.[57]Sharma B,Varghese S.Progress in orthopedic biomaterials and drug delivery.Drug Deliv Transl Res.2016;6(2):75-76.[58]Nam J,Do WS,Stinner DJ,et al.The Highest-Impact Combat Orthopedic and Extremity Injury Articles in the Past 70 Years: A Citation Analysis.J Spec Oper Med.2017;17(1):55-66.[59]Lin X,Yang S,Lai K,et al.Orthopedic implant biomaterials with both osteogenic and anti-infection capacities and associated in vivo evaluation methods.Nanomedicine. 2017;13(1):123-142.[60]Raphel J,Holodniy M,Goodman SB,et al.Multifunctional coatings to simultaneously promote osseointegration and prevent infection of orthopaedic implants.Biomaterials. 2016;84:301-314.[61]Tuchinskiy L.Processes for Making Functionally Graded Materials and Products Produced by These Processes: U.S. Patent Application 14/279,707[P]. 2014-5-16.[62]Bolelli G,Bellucci D,Cannillo V,et al.Comparison between suspension plasma sprayed and high velocity suspension flame sprayed bioactive coatings. Surfand Coat Technol. 2015;280:232-249.[63]程瑶,王铭,王星星,等.仿骨成分多元掺杂羟基磷灰石体外成骨性能研究[J].无机材料学报,2016,31(12):1341-1346.[64]张钰.聚醚醚酮仿生人工骨3D打印热力学仿真及实验研究[D].吉林大学,2014. |
| [1] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [2] | Zeng Yanhua, Hao Yanlei. In vitro culture and purification of Schwann cells: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1135-1141. |
| [3] | Xu Dongzi, Zhang Ting, Ouyang Zhaolian. The global competitive situation of cardiac tissue engineering based on patent analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 807-812. |
| [4] | Liu Jiangfeng. Nano-hydroxyapatite/polyamide 66 composite filling combined with locking plate in the treatment of fibrous dysplasia of femoral bone [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 542-547. |
| [5] | Wu Zijian, Hu Zhaoduan, Xie Youqiong, Wang Feng, Li Jia, Li Bocun, Cai Guowei, Peng Rui. Three-dimensional printing technology and bone tissue engineering research: literature metrology and visual analysis of research hotspots [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 564-569. |
| [6] | Chang Wenliao, Zhao Jie, Sun Xiaoliang, Wang Kun, Wu Guofeng, Zhou Jian, Li Shuxiang, Sun Han. Material selection, theoretical design and biomimetic function of artificial periosteum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 600-606. |
| [7] | Liu Fei, Cui Yutao, Liu He. Advantages and problems of local antibiotic delivery system in the treatment of osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 614-620. |
| [8] | Li Xiaozhuang, Duan Hao, Wang Weizhou, Tang Zhihong, Wang Yanghao, He Fei. Application of bone tissue engineering materials in the treatment of bone defect diseases in vivo [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 626-631. |
| [9] | Zhang Zhenkun, Li Zhe, Li Ya, Wang Yingying, Wang Yaping, Zhou Xinkui, Ma Shanshan, Guan Fangxia. Application of alginate based hydrogels/dressings in wound healing: sustained, dynamic and sequential release [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 638-643. |
| [10] | Chen Jiana, Qiu Yanling, Nie Minhai, Liu Xuqian. Tissue engineering scaffolds in repairing oral and maxillofacial soft tissue defects [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 644-650. |
| [11] | Xing Hao, Zhang Yonghong, Wang Dong. Advantages and disadvantages of repairing large-segment bone defect [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 426-430. |
| [12] | Chen Siqi, Xian Debin, Xu Rongsheng, Qin Zhongjie, Zhang Lei, Xia Delin. Effects of bone marrow mesenchymal stem cells and human umbilical vein endothelial cells combined with hydroxyapatite-tricalcium phosphate scaffolds on early angiogenesis in skull defect repair in rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3458-3465. |
| [13] | Wang Hao, Chen Mingxue, Li Junkang, Luo Xujiang, Peng Liqing, Li Huo, Huang Bo, Tian Guangzhao, Liu Shuyun, Sui Xiang, Huang Jingxiang, Guo Quanyi, Lu Xiaobo. Decellularized porcine skin matrix for tissue-engineered meniscus scaffold [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3473-3478. |
| [14] | Mo Jianling, He Shaoru, Feng Bowen, Jian Minqiao, Zhang Xiaohui, Liu Caisheng, Liang Yijing, Liu Yumei, Chen Liang, Zhou Haiyu, Liu Yanhui. Forming prevascularized cell sheets and the expression of angiogenesis-related factors [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3479-3486. |
| [15] | Liu Chang, Li Datong, Liu Yuan, Kong Lingbo, Guo Rui, Yang Lixue, Hao Dingjun, He Baorong. Poor efficacy after vertebral augmentation surgery of acute symptomatic thoracolumbar osteoporotic compression fracture: relationship with bone cement, bone mineral density, and adjacent fractures [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3510-3516. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||