Chinese Journal of Tissue Engineering Research ›› 2024, Vol. 28 ›› Issue (27): 4390-4396.doi: 10.12307/2024.545
Previous Articles Next Articles
Mechanism by which exercise improves inhibitory control and drug craving in methamphetamine abstinent patients
Liao Shuaixiong1, Deng Kai2, Bai Nan1, Yang Wenliang1, Wang Feng1, Hao Zongji3, Li Xueying1
- 1Department of Physical Education (Sports College), Inner Mongolia University of Science and Technology, Baotou 014010, Inner Mongolia Autonomous Region, China; 2Mianyang Xiyuan School, Mianyang 621013, Sichuan Province, China; 3Chongqing Liangjiang Yucai Middle School, Chongqing 401121, China
-
Received:2023-10-11Accepted:2023-11-07Online:2024-09-28Published:2024-01-29 -
Contact:Li Xueying, Master, Department of Physical Education (Sports College), Inner Mongolia University of Science and Technology, Baotou 014010, Inner Mongolia Autonomous Region, China -
About author:Liao Shuaixiong, Master, Lecturer, Department of Physical Education (Sports College), Inner Mongolia University of Science and Technology, Baotou 014010, Inner Mongolia Autonomous Region, China
CLC Number:
Cite this article
Liao Shuaixiong, Deng Kai, Bai Nan, Yang Wenliang, Wang Feng, Hao Zongji, Li Xueying. Mechanism by which exercise improves inhibitory control and drug craving in methamphetamine abstinent patients[J]. Chinese Journal of Tissue Engineering Research, 2024, 28(27): 4390-4396.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks

2.1.1 急性运动对甲基苯丙胺戒断者抑制控制的影响 纳入的4篇急性运动对甲基苯丙胺戒断者抑制控制干预的研究中[14-17],运动干预方式主要以功率自行车为主的有氧运动(3篇)[14-15,17],高强度间歇训练(1篇)[16];单次干预时长均为30 min。4篇研究均报道了运动干预强度[14-17],其中明确了低强度为40%-50%最大心率、中等强度为65%-75%最大心率和55%-75%最大心率、中高强度为75%-95%最大心率、高强度为85%-95%最大心率。现有研究主要采用Go/No Go测试、Stroop测试和相关脑电位等来评估急性运动对甲基苯丙胺戒断者抑制控制的影响效果。WANG等[14]、王艳秋等[15]和YIN等[16]的研究均论证了中等强度有氧运动和中高强度的间歇训练都可显著改善甲基苯丙胺戒断者的抑制功能,并促进其Go/No Go测试和Stroop测试反应时间的缩短和准确性的提高。WANG等[17]在研究中横向对比了低、中、高,不同运动强度对甲基苯丙胺戒断者抑制能力的影响,研究指出相较于低强度和高强度,中等强度有氧运动在Go/No Go测试中反应时最短[(333.96±31.47) ms]、准确性最高[(99.91±0.29)%]、NoGo-N2波幅最大[(?2.72±0.38) μV]。YIN等[16]的研究也观察到中等强度有氧运动(太极拳)对甲基苯丙胺戒断者抑制控制能力的改善,但要指出的是,YIN等[16]研究发现相比于中等强度有氧运动,中高强度的间歇训练在改善甲基苯丙胺戒断者抑制控制准确性方面的效果更好(P < 0.001)。 2.1.2 长期运动对甲基苯丙胺戒断者抑制控制的影响 纳入的3篇长期运动对甲基苯丙胺戒断者抑制控制功能的干预研究中[18-20],运动干预方式为有氧运动,采用的运动形式主要为功率自行车和康复操。干预周期为10-12周;干预频次为每周两三次;单次运动干预时长均为30 min。以上3篇研究均对运动干预强度进行了报道[18-20],其中2篇研究只采用了中等强度(65%-75%最大心率) [18,20],1篇研究采用了中等强度(65%-75%最大心率)和高强度(76%-85%最大心率) [19]。现有研究主要采用Go/No Go测试、功能性近红外成像(fNIRS)、Stroop测试和EEG脑电数据分析来评估长期运动改善甲基苯丙胺戒断者抑制控制功能的效果。 WANG等[18]和CHEN等[19]研究均指出,每周3次,每次30 min,持续12周中等强度的有氧功率自行车运动均能够有效改善甲基苯丙胺戒断者的抑制功能,表现为Go/No Go和Stroop测试中反应时的缩短和准确性的提升;相比与中等强度,持续的高强度有氧功率自行车运动并不能在甲基苯丙胺戒断者的抑制控制上产生有益影响。与WANG等[18]的研究不同,陈一凡等[20]采用每周2次,每次30 min,持续10周的中等强度功率自行车和康复操运动,探究以上两种不同运动形式对甲基苯丙胺戒断者抑制功能的影响。研究并未在功率自行车组上观察到实验前、后Stroop测试的显著性变化(P > 0.05),但在康复操组上检测到实验后Stroop效应显著小于实验前(校正前P=0.005,校正后P=0.020),且康复操组在实验后测时大脑右侧腹外侧前额叶氧合血红蛋白浓度与功率自行车组相比呈现显著降低趋势(P=0.052)。功率自行车和康复操均属于有氧运动,且运动干预强度、时间、频率和周期都相同,但两者在对甲基苯丙胺戒断者抑制控制功能的改善效果上存在差异。分析其原因可能在于,相比功率自行车运动,康复操更加灵活多变,更能够调动甲基苯丙胺戒断者对运动的兴趣,这进一步强化了运动所带来的欣快感,因此后者带来的改善效果在一定程度上优于前者。是否还存在其他原因导致以上差异的出现,其内在机制有待进一步探讨。此外,研究也提示对于长期运动干预而言,中等强度有氧功率自行车运动在改善甲基苯丙胺戒断者抑制控制上存在最低的运动频率,即每周3次的运动干预才能有效发挥功率自行车的改善效益。 2.1.3 对运动改善甲基苯丙胺戒断者抑制控制的评述 文章全面总结和系统分析了运动与甲基苯丙胺戒断者抑制控制的关系,对甲基苯丙胺戒断者抑制控制能力的改善,建议急性运动采用30 min以上的中等强度有氧运动或中高强度间歇运动进行干预。对于长期运动而言,采用干预周期10-12周,单次干预时长不低于30 min,每周干预频次两三次的中等强度有氧操课练习或全身性的综合练习;若采用有氧功率自行车运动,建议增加每周练习次数,且以不低于每周3次为宜。 2.2 运动对甲基苯丙胺戒断者药物渴求的影响 药物渴求是毒品滥用者对过去体验过的精神活性物质效应的一种难以抑制的渴望[21]。吸毒者个体对毒品的心理渴求是导致其戒断后产生强迫觅药行为直至复吸的重要动因之一[13]。因此,要从根本上戒断毒品,降低吸毒者的药物渴求是关键。在探究运动对甲基苯丙胺戒断者药物渴求影响的13篇文献中[19,22-33],6篇采用急性运动干预方式[22-27],7篇采用长期运动干预方式[19,28-33],见表2,3。"

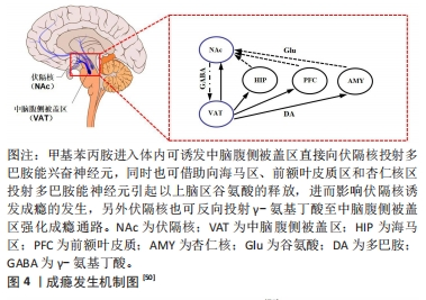
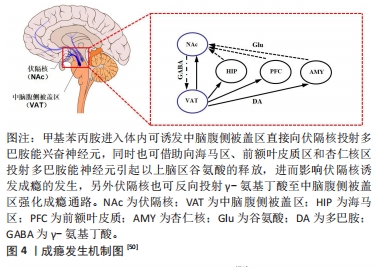
2.2.1 急性运动对甲基苯丙胺戒断者药物渴求的影响 纳入的6篇急性运动对甲基苯丙胺戒断者药物渴求的研究中[22-27],运动干预方式包含有氧运动(3篇)[22,24,27]、抗阻运动(1篇)[26]、舞蹈(1篇)[23]、VR自行车运动(1篇)[25];单次干预时长为10 min(1篇)[25]、20 min(1篇)[22]、30 min(1篇)[24]、35 min(2篇)[23,27]和40 min(1篇)[26];其中5篇报道了运动干预强度[22-24,26-27],4篇指出中等有氧运动强度为65%-75%最大心率、高强度有氧运动为75%-85%最大心率[22-24,27],1篇明确抗阻运动低强度为30%-35% 1RM、中等强度为55%-60% 1RM、高强度为75%-80% 1RM[26]。现有研究主要采用视觉模拟评分表、药物线索反应测试和功能性近红外成像等评估急性运动对甲基苯丙胺戒断者药物渴求的影响效果。 龚丹等[22]、ZHOU等[23]和CHEN等[24]的研究均论证了中等强度有氧运动可显著改善甲基苯丙胺戒断者药物渴求,表现为与药物渴求相关的视觉模拟评分显著降低。QI等[25]研究指出仅10 min虚拟现实竞技自行车运动就可显著降低甲基苯丙胺戒断者对药物的渴求,且观察到运动干预前,在药物相关和中性线索下,被试双侧背外侧前额叶皮质和眶前叶皮质呈现激活态势;而运动干预后药物相关线索并没有引起被试双侧背外侧前额叶皮质和左侧眶前叶皮质的激活。由此可见,急性虚拟现实竞技自行车运动减少了与甲基苯丙胺戒断者大脑激活相关线索诱导的渴求。另外,虚拟现实竞技自行车运动后,被试背外侧前额叶皮质和眶前叶皮质的血流动力学反应显著降低(P < 0.05)、前额叶皮质和运动皮质之间的功能连接增加(P < 0.05)。彭波等[26]的研究发现,中等强度的抗阻训练对甲基苯丙胺戒断者药物渴求的改善效果最佳。与ZHOU等[23]的研究结果不同,陈一凡等[27]在研究中虽也采用单次运动时长为35 min的有氧运动,但仅观察到高强度有氧运动对甲基苯丙胺戒断者药物渴求的改善效益,而中等强度有氧运动的改善效果并不显著。进一步分析发现,两者所采取的有氧运动形式不同,ZHOU等[23]要求被试在跑步机上完成有氧运动,而陈一凡等[27]则要求被试在功率自行车上进行,这可能造成两者研究结果出现差异。另外,陈一凡等[27]研究纳入的被试均为男性,而ZHOU等[23]的被试均为女性,两者性别上的差异可能也是导致其结果出现差异的原因。以上研究结果提示,急性有氧运动运用于甲基苯丙胺成瘾者的药物戒断,应注重其运动方式的选择和患者性别的差异。 2.2.2 长期运动对甲基苯丙胺戒断者药物渴求的影响 纳入的7篇长期运动对甲基苯丙胺戒断者药物渴求的研究中[19,28-33],运动干预方式包括有氧运动(4篇)[19,28,31,33]、抗阻运动(1篇)[29]、有氧联合抗阻运动(2篇)[30,32];干预周期为8-24周,单次干预时长为10-60 min;干预频次为3-5次/周;6篇研究报道了运动干预强度[19,28-30,32-33],其中5篇包含中等强度[19,28-30,33],2篇包含高强度[19,33],1篇采用递增负荷强度[32]。现有研究主要采用视觉模拟评分表、苯丙胺渴求量表、药物渴求度问卷和脑电检测来评估长期运动对甲基苯丙胺戒断者药物渴求的改善效果。 王东石等[28]、李可峰等[29]和李松洋[30]研究表明中等强度有氧运动、中等强度抗阻训练和中等强度有氧联合抗阻训练均能够对甲基苯丙胺戒断者的药物渴求产生显著改善效益。ZHANG等[31]研究指出每周5次、每次50 min,持续24周的太极拳运动不仅能够有效降低甲基苯丙胺戒断者的药物渴求,还对患者平衡控制能力、心理健康和特质焦虑等方面存在改善效果,提升了患者的整体健康感。WANG等[32]研究发现持续8周的递增负荷有氧联合抗阻训练对甲基苯丙胺戒断者药物渴求和身体炎症有明显的改善作用,表现为运动后被试视觉模拟评分表和苯丙胺渴求量表得分均显著降低(P < 0.001),且体内白细胞介素6、肿瘤坏死因子α和白细胞介素1β水平也均呈现显著降低态势。赵琦等[33]和CHEN等[19]采用有氧功率自行车的运动形式,对比了中等和高强度有氧运动对甲基苯丙胺戒断者药物渴求的影响。前者在研究中观察到中等和高强度的有氧运动均可显著降低戒断者的药物渴求,而后者在研究中仅观察到高强度有氧运动的改善效益,中等强度有氧运动的改善效果并不显著。进一步分析发现,两者的单次运动干预时长不同,且对于高强度的衡量标准存在差异。赵琦等[33]实验单次运动时长为40 min,高强度定义为80%-85%最大心率,而CHEN等[19]实验单次运动时长为30 min,高强度定义为76%-85%最大心率,以上差异的出现可能是导致实验结果不相一致的原因。 2.2.3 对运动改善甲基苯丙胺戒断者药物渴求的评述 文章对运动与甲基苯丙胺戒断者药物渴求的关系进行了系统梳理和分析,对甲基苯丙胺戒断者药物渴求的的改善,建议急性运动采用运动时长10-40 min,中等强度(65%-75%最大心率)有氧运动或中等强度(55%-60% 1RM)抗阻力运动进行干预,对于男性戒断人群而言运动强度可适当偏高,但尽量控制在85%最大心率以内。长期运动干预建议采用运动周期8-24周,单次运动时长10-60 min,每周运动频次3-5次的中、高强度功率自行车、跳绳、慢跑、太极拳和器械抗阻力练习等方式进行干预。 2.3 甲基苯丙胺成瘾及改善机制 2.3.1 成瘾机制 中脑——边缘多巴胺系统介导成瘾发生的生理学机制:多巴胺作为大脑奖赏机制中的关键性神经递质,与药物成瘾紧密相关。众所周知,大脑存在4条多巴胺作用通路,即黑质-纹状体与结节-漏斗通路、中脑-边缘与中脑-皮质通路。其中,中脑-边缘通路是参与奖赏的核心,可调控机体的成瘾行为[34]。具体而言,由中脑腹侧被盖区多巴胺能神经元投射到边缘系统的伏隔核、杏仁核和下丘脑的弓状核以及中脑导水管周围灰质等区域,以上脑区神经递质的相互协调,是大脑产生奖赏效应的基础[35]。体内多巴胺在正常情况下被储存于神经末梢突触前膜的囊泡中,当其被释放入突触间隙后,可与突触后膜的相关受体结合产生生理效应。同时释放出的多巴胺又能被突触前膜上的多巴胺转运体重摄取,使其浓度维持在适宜水平[36]。突触前膜对多巴胺的释放和重摄取处于动态平衡,这为多巴胺参与机体各类生理活动,产生生理效应提供了保障。甲基苯丙胺经吸食进入体内会使奖赏区域中的多巴胺神经系统和多巴胺神经元上的痕量胺相关受体被过度激活,其结果会导致与药物渴求相关奖赏通路中的多巴胺释放被促进而回收被抑制[37-38]。具体来说,甲基苯丙胺进入体内可与多巴胺转运体结合进入突触前膜加快前膜内多巴胺的释放,同时,又与单胺类转运体结合抑制多巴胺的重摄取,最终造成神经末梢内多巴胺的耗竭[39]。以上结果在对甲基苯丙胺成瘾大鼠的研究中得到证实[40]。此外,甲基苯丙胺进入机体引起多巴胺神经元兴奋,导致被投射区多巴胺分泌量的增加,这也进一步打破了原有脑区神经递质的平衡,从而致使其他神经递质,如5-羟色胺、γ氨基丁酸和谷氨酸等分泌量的变化,这些神经递质的变化也被证实与药物成瘾和相关病理表现存在关联[41-42]。 伏隔核谷氨酸信号通路介导成瘾发生的分子机制:谷氨酸是一种多功能氨基酸,不仅参与机体的消化和免疫还与大脑健康紧密相关。谷氨酸作为大脑最主要的兴奋性神经递质,其多存在于大脑皮质、杏仁核和海马等区域,且投射兴奋纤维到伏隔核和中脑腹侧被盖区等脑区,独立于中脑——边缘多巴胺系统参与到药物的奖赏过程中[43]。众所周知,与药物成瘾相关的奖赏系统主要涉及大脑的伏隔核区。研究证实,存在于伏隔核中的谷氨酸信号通路是调控戒断后机体再次寻求药物的关键,其机制在于该区域含有大量的谷氨酸能神经突触,通过影响中型多棘神经元并受细胞和分子改变的控制实现对药物成瘾的应答[44]。另外,研究发现可卡因持续给药后,伏隔核内神经元对谷氨酸系统的刺激反应性降低,改变了谷氨酸受体亚型和剪接变异体的表达,最终促进了伏隔核区谷氨酸的释放[45]。此外,在急性甲基苯丙胺重复给药动物模型中也观察到大脑伏隔核区谷氨酸的过度释放现象[46]。进一步分析发现,以上现象的机制在于成瘾性药物摄入,打破了谷氨酸Ⅰ型转运体在体内的动态平衡,而该转运体主要负责对细胞外谷氨酸的重吸收[47]。过多的谷氨酸释放会导致神经元的过度激活,进而对大脑特定脑区造成不可逆的永久性损伤,这也可能是药物成瘾者在戒断后频繁复吸的原因。 谷氨酸除独立的参与到药物奖赏外,还可通过介导多巴胺实现机体对药物成瘾的依赖。具体而言,中脑腹侧被盖区中的多巴胺神经元接受来自脑桥大脑脚、下丘脑和内侧前额叶皮质等脑区的兴奋性谷氨酸投射,刺激中脑腹侧被盖区谷氨酸受体,可调节伏隔核和前额叶皮质部位多巴胺的释放[43]。以上部位多巴胺释放量的增加会对大脑海马和纹状体区域谷氨酸代谢产生影响,其结果是导致以上脑区细胞外谷氨酸含量增加,并进一步激活谷氨酸离子受体,致使细胞内钙离子含量递增,而钙离子则可引起钙离子依赖的磷酸酯酶、蛋白酶和相关内切酶过度活化,继而对细胞形态及其遗传物质造成损伤,最终影响相关脑区的功能,导致药物成瘾[48-49]。此外,过度活化的谷氨酸离子受体也可通过增加体内一氧化氮的形式介导甲基苯丙胺神经毒性的发生[48]。 有研究全面总结了成瘾的发生机制[50],见图4。"

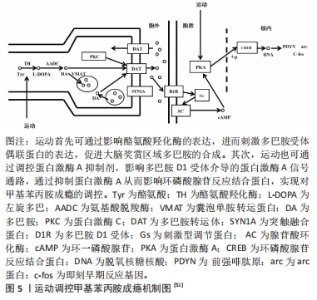
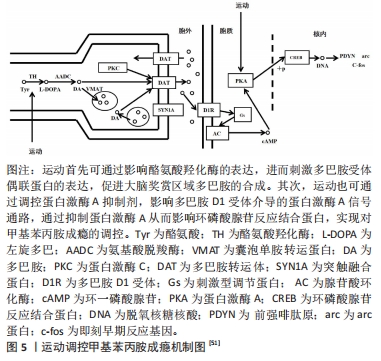
运动干预能够通过促进腹侧背盖区酪氨酸羟化酶的表达,进而刺激多巴胺受体偶联蛋白的表达,实现对大脑相关奖赏区域多巴胺合成的促进。GREENWOOD等[52]对344只成年雄性Fischer大鼠进行了研究,将大鼠随机分为2组,一组为运动组,实验期间进行自愿转轮运动,另一组为对照组,实验共持续6周[52];研究观察到6周的自愿转轮运动,改变了大鼠中脑边缘奖赏通路中与奖赏和多巴胺能神经传递相关的基因转录水平。具体而言,与对照组大鼠相比,运动组大鼠中脑腹侧被盖区的酪氨酸羟化酶mRNA水平显著升高(P < 0.002),伏隔核阿片受体基因表达增加(P < 0.04),伏隔核尾侧KOR基因表达增加(P < 0.02)。相关研究证实阿片受体的激活可以促进伏隔核中多巴胺的释放,自愿运动后大鼠伏隔核中阿片受体基因表达和多巴胺合成量的增加最终会增强伏隔核中多巴胺的神经传递[53]。以上研究结果提示,运动诱发的这种改变在某种意义上起到了与甲基苯丙胺类似的作用,减缓了药物戒断初期由于患者体内多巴胺急剧减少而出现的戒断综合征。 另外,甲基苯丙胺经吸食进入体内可通过血脑屏障,促使对应脑区囊泡内多巴胺释放,使胞外多巴胺浓度急剧增长。胞外多巴胺与细胞膜中多巴胺D1受体结合通过环磷酸腺苷→蛋白激酶A→环磷酸腺苷反应结合蛋白途径,最终影响核内DNA转录,导致药物成瘾发生[54]。运动则可有效调控以上过程,具体而言,运动能够通过调控蛋白激酶A抑制剂,影响多巴胺D1受体介导的蛋白激酶A信号通路,通过抑制蛋白激酶A从而影响环磷酸腺苷反应结合蛋白,最终减少戒断者的觅药行为[55]。此外,运动也可通过影响多巴胺D2/D3受体,实现对药物成瘾的调控,LEE等[56]证实多巴胺D2/D3受体可用性与甲基苯丙胺戒断者自我报告的用药冲动呈负相关。动物研究中也观察到运动干预增加了大鼠大脑纹状体多巴胺D2/D3受体可利用率,有效降低了甲基苯丙胺成瘾小鼠对药物的渴求[52,57]。 运动调节谷氨酸影响药物成瘾的分子机制:谷氨酸能系统信号传递的改变与药物成瘾者的觅药行为和复吸渴求存在关联[58]。众所周知,成瘾性药物进入体内会打破机体谷氨酸内环境的稳态,致使胶质细胞谷氨酸转运体水平下调,增加机体对药物相关刺激的敏感性[59]。运动能够使机体的谷氨酸水平恢复正常,保护因长期吸毒导致的药物对谷氨酸受体的过度刺激[60]。REAL等[61]研究证实,大鼠在强迫跑步机运动后,大脑纹状体代谢型谷氨酸受体2/3基因表达量增加,同时谷氨酸受体突触可塑性也发生了改变,这直接导致大鼠脑内谷氨酸能系统信号传导被抑制,最终表现为药物易感性降低。运动也可通过影响大脑红核区细胞c-fos基因表达,激活谷氨酸神经元亚群的形式实现对药物成瘾的调控[62]。大脑红核区主要由两部分组成,即背外侧小细胞部分和背外侧大细胞部分,其中背外侧小细胞部分中的大多数神经元是γ-氨基丁酸,而背外侧大细胞部分则主要是谷氨酸能神经元[63]。背外侧大细胞部分谷氨酸神经元投射到中脑腹侧被盖区并与该区域多巴胺神经元形成突触[64]。运动可激活背外侧大细胞部分中的谷氨酸神经元亚群,产生奖赏效应,实现对药物渴求的改善。如HE等[62]将8-16周龄C57B/6小鼠进行为期10 d,2 h/d的自由转轮运动,观察到在实验过程中阻断小鼠大脑红核至中脑腹侧被盖区谷氨酸途径,会终止运动的奖赏效应,但通过运动或直接刺激该通路可显著减少小鼠在可卡因自我给药期间的药物摄入量,并减少在戒断期间对药物的渴求。此外,KATSIDONI等[65]的研究还证实,运动在激活投射到中脑腹侧被盖区的背外侧大细胞部分谷氨酸神经元后,在功能上也增强了该区域多巴胺神经元的活性,这可能介导了戒断后期机体对药物渴求的抑制。"

| [1] LAPPIN SFM. Methamphetamine use and future risk for Parkinson’s disease: evidence and clinical implications. Drug Alcohol Depen. 2018;187(6):46-63. [2] 苏乐乐,田甜,赤艳,等.甲基苯丙胺依赖所致认知障碍的治疗进展[J].中国药物滥用防治杂志,2022,28(2):146-150. [3] 《2019年世界毒品问题报告》:全球3500万人患有药物滥用障碍仅七分之一的人获得治疗[EB/OL]. [2023-09-06]. https://news.un.org/zh/story/2019/06/1037091. [4] VOLKOW ND, MORALES M. The brain on drugs: from reward to addiction. Cell. 2015;162(4):712-725. [5] 王坤,张庭然,罗炯.甲基苯丙胺成瘾者抑制控制损伤的可逆性:有氧运动的改善机制及应用研究进展[J].体育科学,2021,41(4):88-97. [6] 杨孟,超金鹏,王德,等.运动改善注意缺陷多动障碍儿童执行功能和注意力的研究进展[J].体育科学,2022,42(5):77-87. [7] ZHOU Y, STUBBS RJ, FINLAYSON G. A neurocognitive perspective on the relationship between exercise and reward: implications for weight management and drug addiction. Appetite. 2023;182(46):125-132. [8] KAO S, BAUMGARTNER N, NAGY C, et al. Acute effects of aerobic exercise on conflict suppression,response inhibition,and processing efficiency underlying inhibitory control processes: an ERP and SFT study. Psychophysiology. 2022;(32):57-73. [9] ELLINGSEN MM, CLAUSEN T, JOHANNESEN SL, et al. Effects of acute exercise on drug craving in adults with poly-substance use disorder. A randomized controlled trial. Ment Health Phys Activ. 2021;21(100423):142-157. [10] KOHLEROVA M Z, FISEROVA Z, PAV M. Physical activity habits and their effects on quality of life in patients with addiction: data from the Czech Republic. Curr Psychol. 2023;17(6):63-81. [11] 容浩,刘佳宁,刘旭东,等.有氧运动改善甲基苯丙胺成瘾者执行控制能力的脑机制研究[J].体育学刊,2019,26(3):138-144. [12] 董贵俊,罗仁苹,唐泽坤,等.乒乓球运动干预甲基苯丙胺成瘾者脑激活及认知功能研究[J].中国体育科技,2021,57(6):16-22. [13] 顾庆,盛蕾,马小铭.毒品成瘾者运动戒毒方法与康复效果研究进展[J].体育与科学,2019,40(6):37-45. [14] WANG D, ZHOU C, CHANG Y. Acute exercise ameliorates craving and inhibitory deficits in methamphetamine: an ERP study. Physiol Behav. 2015;147(1):38-46. [15] 王艳秋,施大庆,赵敏,等.有氧运动对改善甲基苯丙胺类成瘾者抑制能力的研究——来自ERP的证据[J].中国运动医学杂志,2015,34(3):297-302. [16] YIN Y, YANG S, XIAO K, et al. Comparison of the acute effects of Tai chi versus high-intensity interval training on inhibitory control in individuals with substance use disorder. Front Psychol. 2022;13(941719):142-158. [17] WANG D, ZHOU C, ZHAO M, et al. Dose-response relationships between exercise intensity, cravings, and inhibitory control in methamphetamine dependence: an ERPs study. Drug Alcohol Depen. 2016;161(4):331-339. [18] WANG D, ZHU T, ZHOU C, et al. Aerobic exercise training ameliorates craving and inhibitory control in methamphetamine dependencies: a randomized controlled trial and event-related potential study. Psychol Sport Exerc. 2017;30(3):82-90. [19] CHEN Y, LIU T, ZHOU C. Effects of 12-week aerobic exercise on cue-induced drug craving in methamphetamine-dependent patients and the moderation effect of working memory. Ment Health Phys Activ. 2021;21(100420):253-265. [20] 陈一凡,蒋丰,王姁如,等.不同运动方式对女性甲基苯丙胺成瘾者冲突抑制能力的影响:一项近红外功能成像研究[J].中国运动医学杂志,2022,41(12):933-940. [21] MORPHETT K, CARTER A, HALL W, et al. Framing tobacco dependence as a “brain disease”: implications for policy and practice. Nicotine Tob Res. 2017;19(7):48-62. [22] 龚丹,覃丽平,朱婷,等.短时有氧运动对甲基苯丙胺依赖者渴求度、情绪状态及神经递质的影响[J].中国体育科技,2019,55(5):56-64. [23] ZHOU Y, FINLAYSON G, LIU X, et al. Effects of acute dance and aerobic exercise on drug craving and food reward in women with methamphetamine dependence. Med Sci Sport Exer. 2021; 53(11):2245-2253. [24] CHEN Y, WANG X, ZHOU C. Effects of different exercise patterns on drug craving in female methamphetamine-dependent patients: evidence from behavior and fNIRS. Ment Health Phys Activ. 2023;25(100534):175-184. [25] QI L, TIAN Z, YUE Y, et al. Effects of acute exercise on craving and cortical hemodynamics under drug-cue exposure in MA-dependent individuals. Neurosci Lett. 2022;781(136672):46-59. [26] 彭波,陈佳尘,苏锐,等.抗阻运动对甲基苯丙胺类毒品依赖者心理渴求及诱发因素的影响及其剂量效应[J].中国运动医学杂志,2021,40(1):46-54. [27] 陈一凡,周宇,王家宽,等.急性有氧运动强度影响甲基苯丙胺戒断者药物渴求度的认知调节作用[J].中国药物依赖性杂志,2019,28(5):371-378. [28] 王东石,朱婷.有氧运动对甲基苯丙胺类依赖者体适能、渴求度及情绪状态的作用[J].体育科学,2017,37(7):50-59. [29] 李可峰,闫前,丁荔洁,等.中等强度抗阻训练对甲基苯丙胺成瘾者脑功能连接的影响[J].体育科学,2021,41(3):25-33. [30] 李松洋.有氧运动联合抗阻训练对甲基苯丙胺成瘾者身心康复影响的研究[J].中国药物依赖性杂志,2022,31(3):188-193. [31] ZHANG Z, ZHU D. Effect of taijiquan exercise on rehabilitation of male amphetamine-type addicts. Evid-based Compl Alt. 2020;2020(5):214-227. [32] WANG J, LU C, ZHENG L, et al. Peripheral inflammatory biomarkers of methamphetamine withdrawal patients based on the neuro-inflammation hypothesis: the possible improvement effect of exercise. Front Psychiatry. 2021;12(795073):179-192. [33] 赵琦,刘佳宁,陆颖之,等.长期有氧运动改善甲基苯丙胺成瘾者对毒品的渴求——来自alpha波的证据[J].中国运动医学杂志,2020,39(10):804-809. [34] ROSEN L G, NINGLEI S, WALTER R, et al. Molecular and neuronal plasticity mechanisms in the amygdala-prefrontal cortical circuit: implications for opiate addiction memory formation. Front Neurosci-switz. 2015;9(3):63-74. [35] KROLL SL, HULKA LM, KEXEL A, et al. Plasma endocannabinoids in cocaine dependence and their relation to cerebral metabotropic glutamate receptor 5 density. Transl Psychiat. 2023;13(1):325-331. [36] 刘溪,代振凤,蒲小平.甲基苯丙胺成瘾机制进展[J].中国新药杂志,2017,26(21):2541-2545. [37] LIN M, SAMBO D, KHOSHBOUEI H, et al. Methamphetamine regulation of firing activity of dopamine neurons. J Neurosci. 2016;36(40):10376-10391. [38] MINER NB, ELMORE JS, BAUMANN MH, et al. Trace amine-associated receptor 1 regulation of methamphetamine-induced neurotoxicity. Neurotoxicology. 2017;57(13):26-35. [39] SØRENSEN G, RICKHAG M, LEO D, et al. Disruption of the PDZ domain-binding motif of the dopamine transporter uniquely alters nanoscale distribution, dopamine homeostasis, and reward motivation. J Biol Chem. 2021;297(6):101361-101374. [40] O’DELL SJ, GALVEZ BA, BALL AJ, et al. Running wheel exercise ameliorates methamphetamine-induced damage to dopamine and serotonin terminals. Synapse. 2012;66(1):71-80. [41] MCFADDEN LM, REBECCA C, TAMEE L, et al. Behavioral and serotonergic changes in the frontal cortex following methamphetamine self-administration. Int J Neuropsychoph. 2018(8):8-17. [42] LOMINAC KD, QUADIR SG, BARRETT HM, et al. Prefrontal glutamate correlates of methamphetamine sensitization and preference. Eur J Neurosci. 2016;43(5):689-702. [43] 李媛媛,李娟,杨根梦,等.甲基苯丙胺神经毒性作用及机制的研究进展[J].昆明医科大学学报,2021,42(2):5-8. [44] PUIG S, XUE X, SALISBURY R, et al. Circadian rhythm disruptions associated with opioid use disorder in synaptic proteomes of human dorsolateral prefrontal cortex and nucleus accumbens. Mol Psychiatr. 2023;32(5):28-36. [45] CHURCHILL L, SWANSON CJ, URBINA M, et al. Repeated cocaine alters glutamate receptor subunit levels in the nucleus accumbens and ventral tegmental area of rats that develop behavioral sensitization. J Neurochem, 1999;72(6):2397-2403. [46] MISHRA D, PENA-BRAVO JI, LEONG KC, et al. Methamphetamine self-administration modulates glutamate neurophysiology. Brain Struct Funct. 2017;222(5):2031-2039. [47] 李彦霖,朱莉,陈娇,等.甲基苯丙胺成瘾机制概述[J].中国药物滥用防治杂志,2023, 29(2):181-187. [48] FARIA AC, CARMO H, CARVALHO F, et al. Drinking to death: Hyponatraemia induced by synthetic phenethylamines. Drug Alcohol Depen. 2020;212(2):108045-108051. [49] LIANG M, ZHU L, WANG R, et al. Methamphetamine exposure in adolescent impairs memory of mice in adulthood accompanied by changes in neuroplasticity in the dorsal hippocampus. Front Cell Neurosci. 2022;16(1):892757-892765. [50] 吕宸,傅柯荃,汪洋,等.甲基苯丙胺成瘾机制及中草药治疗[J].时珍国医国药,2019, 30(9):2226-2228. [51] 廖帅雄.不同运动模式对甲基苯丙胺戒毒者药物戒断的效果对比及最佳运动模式的肠道菌群变化研究[D].重庆:西南大学.2020. [52] GREENWOOD BN, FOLEY TE, LE TV, et al. Long-term voluntary wheel running is rewarding and produces plasticity in the mesolimbic reward pathway. Behav Brain Res. 2011;217(2):354-362. [53] RETZLAFF CL, ROTHWELL PE. Characterization and mu opioid receptor sensitivity of neuropeptide Y interneurons in the mouse nucleus accumbens. Neuropharmacology. 2022; 218(3):109212-109219. [54] CÓRDOBA-GRUESO WS, MATTEY-MORA PP, CHEN C, et al. The association between exercise and prescription opioid misuse: a scoping review. Exp Clin Psychopharm. 2023;63(7):52-65. [55] CATALFIO AM, FETTERLY TL, NIETO AM, et al. Cocaine-induced sensitization and glutamate plasticity in the nucleus accumbens core: effects of sex. Biol Sex Differ. 2023;14(1):41-53. [56] LEE B, LONDON ED, POLDRACK RA, et al. Striatal dopamine d2/d3 receptor availability is reduced in methamphetamine dependence and is linked to impulsivity. J Neurosci. 2009; 29(47):14734-14740. [57] BAUER EE, BUHR TJ, REED CH, et al. Exercise-induced adaptations to the mouse striatal adenosine system. Neural Plast. 2020;2020:5859098. [58] BALDASSARRI SR, ASCH RH, HILLMER AT, et al. Nicotine use and metabotropic glutamate receptor 5 in individuals with major depressive and posttraumatic stress disorders. Chronic Stress. 2023;7(2):1994190694. [59] MONGI-BRAGATO B, AVALOS M P, GUZMÁN A S, et al. Endogenous enkephalin is necessary for cocaine-induced alteration in glutamate transmission within the nucleus accumbens. Eur J Neurosci. 2021;53(5):1441-1449. [60] 柯钰婷,周文华.运动干预药物依赖的神经生物学机制研究进展[J].中国药理学与毒理学杂志,2015,29(4):599-606. [61] REAL CC, FERREIRA AF, HERNANDES MS, et al. Exercise-induced plasticity of AMPA-type glutamate receptor subunits in the rat brain. Brain Res. 2010;13(63):63-71. [62] HE Y, MADEO G, LIANG Y, et al. A red nucleus-VTA glutamate pathway underlies exercise reward and the therapeutic effect of exercise on cocaine use. Sci Adv. 2022;8(35):1440-1451. [63] MARTINEZ-LOPEZ JE, MORENO-BRAVO JA, MADRIGAL MP, et al. Red nucleus and rubrospinal tract disorganization in the absence of Pou4f1. Front Neuroanat. 2015;9(6):8-17. [64] MORRIS R, VALLESTER KK, NEWTON SS, et al. The differential contributions of the parvocellular and the magnocellular subdivisions of the red nucleus to skilled reaching in the rat. Neuroscience. 2015;295(3):48-57. [65] KATSIDONI V, TZATZARAKIS M N, KARZI V, et al. Differential effects of chronic voluntary wheel-running on morphine induced brain stimulation reward, motor activity and striatal dopaminergic activity. Behav Brain Res. 2020;394(1):112831-112839. |
| [1] | Zhong Jun, Wang Wen. Network meta-analysis of different anatomical repair strategies to improve chronic lateral ankle instability [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(9): 1470-1476. |
| [2] | Wu Jing, Yao Yingce, Yang Xiaowei, Xue Boshi, Zhao Jianbin, Yang Chen, Luan Tianfeng, Zhou Zhipeng. Intervention of muscle strength training combined with neuromuscular electrical stimulation on lower limb function and biomechanical changes in patients with patellofemoral pain [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(9): 1365-1371. |
| [3] | Weng Rui, Lin Dongxin, Guo Haiwei, Zhang Wensheng, Song Yuke, Lin Hongheng, Li Wenchao, Ye Linqiang. Abnormal types of intervertebral disc structure and related mechanical loading with biomechanical factors [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(9): 1436-1442. |
| [4] | Chen Zhiling, Huang Xuecheng, Pan Min, Huang Ying, Wu Yuntian. Evaluation of the relationship between neck and shoulder pain and scalene muscles based on shear wave elastography [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(8): 1265-1270. |
| [5] | Wei Juan, Li Ting, Huan Mengting, Xie Ying, Xie Zhouyu, Wei Qingbo, Wu Yunchuan. Mechanism by which static exercise improves insulin resistance in skeletal muscle of type 2 diabetes [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(8): 1271-1276. |
| [6] | Lou Guo, Zhang Yan, Fu Changxi. Role of endothelial nitric oxide synthase in exercise preconditioning-induced improvement of myocardial ischemia-reperfusion injury [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(8): 1283-1288. |
| [7] | Cheng Jie, Wang Jihong, Zhang Pei. Functional exercise for tendon adhesion in a model of deep flexor tendon II injury of the third toe [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(8): 1161-1167. |
| [8] | Wang Ji, Zhang Min, Li Wenbo, Yang Zhongya, Zhang Long. Effect of aerobic exercise on glycolipid metabolism, skeletal muscle inflammation and autophagy in type 2 diabetic rats [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(8): 1200-1205. |
| [9] | Ruan Rong, Lou Xujia, Jin Qiguan, Zhang Libing, Xu Shang, Hu Yulong. Effect of resveratrol on gluconeogenesis in exercise-induced fatigue rats [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(8): 1229-1234. |
| [10] | Yang Yifeng, Huang Jian, Ye Nan, Wang Lin. Ischemia-reperfusion injury in total knee arthroplasty [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(6): 955-960. |
| [11] | Liu Zhiyang, Fu Zeting, Xia Yu, Ding Haili. The role of BMAL1 and MyoD in exercise-induced skeletal muscle damage [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 510-515. |
| [12] | Zhu Xiaofeng, Chen Weiwei, Huang Jian. Effects of maternal high-fat diet and exercise intervention on insulin sensitivity and the hypothalamic arcuate nucleus in male offspring mice [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 556-561. |
| [13] | Wang Shijie, Wen Dengtai, Wang Jingfeng, Gao Yinghui. Mammalian target of rapamycin in relation to exercise, high fat/high salt diet, and aging [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 574-580. |
| [14] | Yan Binghan, Li Zhichao, Su Hui, Xue Haipeng, Xu Zhanwang, Tan Guoqing. Mechanisms of traditional Chinese medicine monomers in the treatment of osteoarthritis by targeting autophagy [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 627-632. |
| [15] | Zhang Jinpu, Wang Junli, Zhang Siqi, Chen Jiahao, Yang Qiushi. Effectiveness of exercise interventions for fibromyalgia syndrome: a Meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(32): 5210-5216. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||