Chinese Journal of Tissue Engineering Research ›› 2024, Vol. 28 ›› Issue (11): 1756-1761.doi: 10.12307/2024.276
Previous Articles Next Articles
Progress in the treatment of knee osteoarthritis with monomer and compound Chinese medicine
Mo Jian1, Ye Sentao2, Zhang Xiaoyun1
- 1Ruikang Hospital, Guangxi University of Chinese Medicine, Nanning 530011, Guangxi Zhuang Autonomous Region, China; 2Graduate School, Guangxi University of Traditional Chinese Medicine, Nanning 530000, Guangxi Zhuang Autonomous Region, China
-
Received:2022-11-07Accepted:2023-04-10Online:2024-04-18Published:2023-07-27 -
Contact:Zhang Xiaoyun, MD, Master’s supervisor, Associate chief physician, Ruikang Hospital, Guangxi University of Chinese Medicine, Nanning 530011, Guangxi Zhuang Autonomous Region, China -
About author:Mo Jian, Master, Associate chief physician, Master’s supervisor, Ruikang Hospital, Guangxi University of Chinese Medicine, Nanning 530011, Guangxi Zhuang Autonomous Region, China
CLC Number:
Cite this article
Mo Jian, Ye Sentao, Zhang Xiaoyun. Progress in the treatment of knee osteoarthritis with monomer and compound Chinese medicine[J]. Chinese Journal of Tissue Engineering Research, 2024, 28(11): 1756-1761.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks

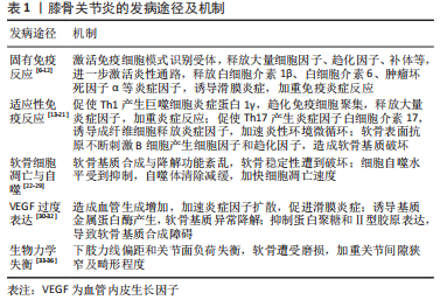
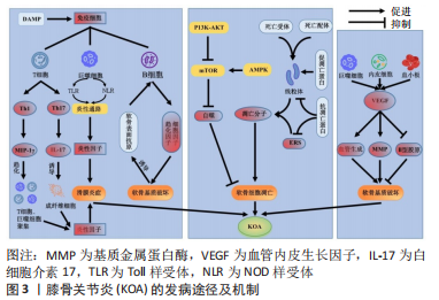
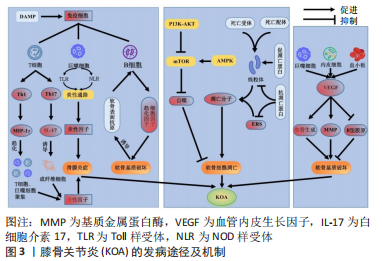
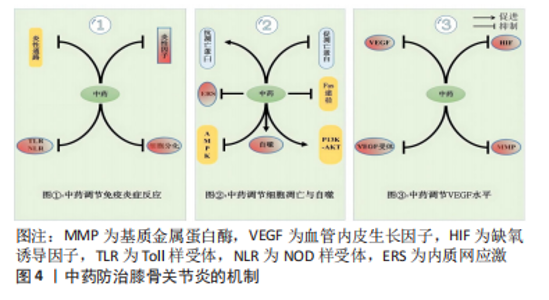
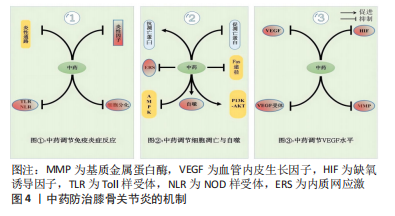
2.1.1 免疫反应在膝骨关节炎发病中的作用机制 (1)固有免疫:传统观点认为,膝骨关节炎只是一种涉及膝关节的退行性变疾病,但随着研究深入,越来越多的学者发现滑膜炎症与膝骨关节炎发病密切相关[6]。研究认为,慢性炎症参与了膝骨关节炎的发生发展,其中固有免疫反应和适应性免疫反应在这个过程中发挥着重要作用[7]。固有免疫反应是由巨噬细胞、单核细胞和中性粒细胞等主要免疫细胞识别、清除体内病原体的过程[8]。创伤或肥胖因素导致关节面负荷失衡,产生并释放损伤相关分子模式,进而被免疫细胞表面的模式识别受体识别,如Toll样受体(Toll-like receptor,TLR)和NOD样受体(Nod-like receptor,NLR),启动下游信号级联反应,进而释放大量细胞因子、趋化因子及补体。炎症因子的大量分泌打破软骨降解与修复的平衡,造成软骨的损伤,受损的软骨可进一步诱导肿瘤坏死因子α和白细胞介素1β等炎症因子大量产生,进一步加速滑膜组织的纤维样变及加重滑膜炎症,并形成恶性循环[9-10]。研究发现,膝骨关节炎炎性滑膜组织主要存在巨噬细胞、T细胞和B细胞等免疫细胞浸润[11]。SUN等[12]发现创伤和肥胖可上调炎症因子表达。在关节腔内创伤后,滑膜组织发现了大量M1型巨噬细胞表达,产生并释放的损伤相关分子模式被巨噬细胞表面的TLR识别,进一步激活核转录因子κb(Nuclear transcription factor kappa B,NF-κB)通路并上调炎症因子白细胞介素1β和白细胞介素6表达,加速炎性微环境形成;另外,高脂肪饮食促使M1型巨噬细胞表达增加,并加快了滑膜炎症的进展;最后在关节局部注射氯膦酸盐脂质体消耗巨噬细胞后,滑膜炎症和软骨损伤得到改善。综上,巨噬细胞介导的固有免疫反应加快了膝骨关节炎病变进展。创伤可诱导M1型巨噬细胞的过多表达并激活炎性通路释放大量炎症因子,进而加重滑膜炎症;而肥胖会造成滑膜组织结构紊乱,趋化促炎M1型巨噬细胞在滑膜和脂肪垫组织中聚集,导致炎性环境形成,加重滑膜炎症产生与发展。 (2)适应性免疫:适应性免疫又称获得性免疫,主要包括T细胞介导的细胞免疫和B细胞介导的体液免疫。成熟的T细胞按抗原类型可分为CD4+ T细胞与CD8+ T细胞,其中Th1、Th2、Th9、Th17、Treg等细胞亚群与膝骨关节炎病理密切相关。研究发现在膝骨关节炎患者滑膜组织和髌下脂肪垫存在大量T细胞浸润,CD4+ T细胞是主要的浸润细胞类型。在一项对小鼠十字韧带切除诱导膝骨关节炎的实验中发现,实验组滑膜在造模第30天后存在大量的CD4+ T细胞浸润,同时可检测到巨噬细胞炎症蛋白1γ和干扰素γ的表达增加;在对小鼠CD4+ T细胞进行敲除后,观察到巨噬细胞炎症蛋白1γ表达减少,软骨退化变慢。综上,CD4+ T细胞通过诱导巨噬细胞炎症蛋白1γ的表达对软骨退化产生重要影响,其可能的机制是CD4+ T细胞在干扰素γ的作用下分化为Th1细胞,Th1细胞选择性产生巨噬细胞炎症蛋白1γ,作为趋化因子诱导CD4+ T细胞、CD8+ T细胞、巨噬细胞等聚集并释放大量炎症因子,加重免疫炎症反应[13-14]。另外,CD4+ T细胞可在炎性微环境影响下分化成Th17细胞并进一步分泌产生炎症因子白细胞介素17,进而诱导成纤维细胞释放白细胞介素1β和肿瘤坏死因子α等炎症因子,加速炎性环境形成和循环;白细胞介素17在这种特定的炎性环境中会协同肿瘤坏死因子α共同作用,上调基质金属蛋白酶(matrix metalloproteinases,MMPs)的表达,引发软骨基质的降解破坏,造成严重的关节损伤[15-16]。WANG等[17]研究进一步证实了注射白细胞介素17能够诱导兔膝骨关节炎发生,且伴随MMP-1、MMP-3和MMP-13的表达增加。此外,一项研究通过应用拮抗白细胞介素17A的方法证实可有效减轻鼠膝骨关节炎炎症反应和减少MMP-13的表达[18]。综上,T细胞可通过分化成不同细胞类型参与介导膝骨关节炎的发生发展。 体液免疫反应是机体在受到抗原刺激后,B淋巴细胞分化增殖产生免疫球蛋白形成免疫应答的过程[19]。研究认为,当软骨出现退行性变时,软骨细胞外基质的屏障作用消失,关节软骨表面的特定抗原会诱导自身免疫反应,并产生细胞因子、趋化因子,在这些因子的刺激下可造成软骨基质进一步破坏,致使软骨表面抗原反复暴露于免疫系统中,加剧自身免疫反应[20]。SHIOKAWA等[21]研究证实B细胞的激活是在抗原刺激下产生的,说明抗原驱动B淋巴细胞并介导体液免疫反应在膝骨关节炎进展中发挥重要作用。 因此,作者认为T细胞通过诱导分化成多种细胞亚群参与介导免疫炎症反应,同时诱导软骨基质降解的关键酶MMP表达,造成软骨破坏;而B细胞介导的体液免疫会诱发机体产生特定的细胞因子和趋化因子,使关节软骨表面抗原诱发自身免疫反应,导致膝骨关节炎的发生发展。但目前对于膝骨关节炎发病机制中的免疫机制尚未明确,进一步深入研究抗软骨细胞膜蛋白抗体和抗软骨介导层蛋白抗体等免疫指标,可为进一步揭示膝骨关节炎免疫机制及对应治疗提供新依据。 2.1.2 软骨细胞自噬与凋亡在膝骨关节炎发病中的作用机制 细胞凋亡是指由基因控制的细胞程序性死亡过程。作为关节软骨中唯一的细胞类型,软骨细胞在维持关节软骨稳定性上发挥重要作用。软骨细胞的过度凋亡,会造成细胞外基质功能失衡及软骨损伤,加重关节软骨的退行性变进程[22]。线粒体途径是细胞凋亡的重要途径之一,研究表明DNA损伤、细胞缺氧和细胞生长因子缺失等因素可导致促凋亡蛋白激活,增加线粒体外膜通透性并释放凋亡因子,促进凋亡复合体形成,进一步激活下游Caspase-9和Caspase-3,致使DNA断裂并促进凋亡小体形成,最终导致软骨细胞凋亡[23]。此外,炎性因素会诱导死亡配体与死亡受体结合,进一步激活Caspase-8和Bid以增加线粒体通透性,加速细胞色素c释放并激活启动Caspase 级联反应,造成软骨细胞凋亡;而抗凋亡蛋白通过阻断Caspase-9的活化,抑制Caspase级联反应,以减少软骨细胞凋亡。内质网是细胞内蛋白质合成与折叠、钙离子存储的场地,当机体细胞受到应激源刺激时,未折叠蛋白增多及钙离子失衡造成内质网的功能紊乱而引发内质网应激;内质网应激通过激活PERK-eIF2α-ATF4的通路表达,进一步增强C/EBP同源蛋白(C/EBP homologous protein,CHOP)转录,进而影响内质网腔内蛋白的折叠功能,激活Caspase3启动Caspase级联反应使细胞发生凋亡[24]。TAKADA等[25]应用硝普钠刺激软骨细胞后,检测到内质网应激相关mRNA及凋亡分子CHOP表达均增加,且出现明显软骨细胞凋亡现象;应用内质网应激抑制剂和敲除CHOP后,软骨细胞凋亡减少。上述研究表明内质网应激是诱发细胞凋亡的重要因素,通过抑制内质网应激所引起的信号通路及凋亡因子的表达,可进一步减少细胞凋亡带来的软骨破坏,进而达到防治膝骨关节炎的目的。 细胞自噬是一种降解细胞内老化或受损的细胞器和蛋白质造成细胞主动性死亡,防止细胞过度凋亡的重要保护机制[26]。低ATP水平状态下,AMP的水平变化造成AMPK激活,进而抑制哺乳动物雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR)活性诱导自噬的发生,以减少软骨细胞凋亡,延缓膝骨关节炎的进展[27]。在胰岛素样生长因子刺激下,磷脂酰肌醇3-激酶(phosphatidylinositol 3 kinase,PI3K)/蛋白激酶B(protein kinase B,AKT)信号分子通过诱导mTOR活化以抑制自噬起始分子ULK1的功能,进而减少自噬表达,加快软骨细胞凋亡[28]。 AKARAPHUTIPORN等[29]研究表明:白细胞介素1β和硝普钠刺激软骨细胞后,ERK、Akt、mTOR表达显著增加,软骨细胞自噬活性、自噬通量和自噬相关基因mRNA表达减少,软骨细胞凋亡数量增多;应用雷帕霉素抑制mTOR表达后,自噬标志物LC3-Ⅱ表达增加。因此,mTOR的活化抑制自噬表达,促进了软骨细胞的凋亡。通过直接靶向mTOR的调控和上游通路的调节可有效促进自噬表达,减少细胞凋亡以保护关节软骨,延缓膝骨关节炎发生发展。 综上,作者认为多途径诱导的细胞凋亡以及自噬共同影响了膝骨关节炎发生发展。其主要机制有:①促凋亡蛋白的异常激活增加了线粒体膜通透性,并释放大量凋亡因子和启动Caspase级联反应,导致细胞凋亡并造成软骨损伤;而抗凋亡蛋白通过阻断Caspase-9活化和抑制Caspase级联反应,发挥抗凋亡作用以保护关节软骨;②钙离子失衡导致内质网结构功能紊乱,引发内质网应激并激活PERK-eIF2α-ATF4通路及凋亡分子CHOP表达,诱导一系列软骨细胞凋亡发生;③外源性死亡配体-死亡受体结合并激活Caspase-8-Bid-线粒体途径,启动Caspase级联反应,促进细胞凋亡;④细胞自噬中心分子和关键蛋白TOR通过感受多种信号变化,调节自噬水平,对软骨细胞凋亡产生促进或抑制作用;在胰岛素样生长因子刺激下,PI3K/AKT促进mTOR表达,从而抑制自噬水平,加速细胞凋亡;AMPK则抑制mTOR表达,使自噬水平升高,软骨细胞凋亡得以保护,有效延缓细胞凋亡导致的软骨侵蚀进展。因此,通过调节线粒体功能、抑制内质网应激、调节外源性促凋亡途径、平衡抗凋亡蛋白与促凋亡蛋白表达和调节自噬水平,是有效减少软骨细胞凋亡的重要途径,对延缓膝骨关节炎发生发展产生重要作用。 2.1.3 VEGF在膝骨关节炎发病中的作用机制 VEGF是来源于血小板、巨噬细胞和内皮细胞等促血管生成的因子,通过刺激血管内皮细胞有丝分裂和诱导内皮细胞迁移促进血管生成,诱发滑膜炎症、软骨破坏及退化和骨赘形成的发生。大量研究表明,在膝骨关节炎患者的滑膜组织中存在VEGF的高表达,这表明VEGF是膝骨关节炎发生发展过程中的一个重要因素。研究发现,在炎性滑膜组织存在炎症因子白细胞介素1β的过度表达,而白细胞介素1β可使缺氧诱导因子表达增加,最终导致VEGF高表达[30]。VEGF可与内皮细胞受体VEGFR-2结合,刺激内皮细胞增殖,促进血管生成的同时伴随神经生长因子的表达以及感觉神经的生长,诱导疼痛发生;同时趋化大量炎症因子聚集,导致慢性炎症产生[31]。此外,VEGF还通过抑制蛋白聚糖和Ⅱ型胶原基因表达造成软骨基质合成障碍,并上调MMPs的表达造成软骨基质降解破坏,导致软骨损伤[32]。综上,作者认为VEGF可通过促进炎症发生、诱导血管生成及破坏软骨等途径参与膝骨关节炎的发生发展。因此,通过直接调控VEGF或间接调控VEGF相关信号通路及上下游靶点,可有效延缓膝骨关节炎进展。 2.1.4 生物力学失衡在膝骨关节炎发病中的作用机制 创伤和肥胖导致下肢力线改变、关节面负荷失衡,使软骨与软骨下骨降解与合成失衡,从而诱发膝骨关节炎病变[33-34]。下肢力线是指从股骨头中心出发经膝关节中心偏内侧至踝关节中心的连线,当下肢力线异常产生偏距,可造成膝关节内外侧间室负荷不均,关节面负荷失衡,加速软骨磨损;软骨的磨损进一步造成关节面受力不均,加大力线偏距,形成恶性循环。FUKAYA等[35]研究表明:重度膝骨关节炎患者的膝关节应力集中于内侧间室,关节软骨载荷量大,内侧半月板的损伤和退变趋势明显。甘浩然等[36]研究发现胫骨平台的不均匀沉降会引发内翻畸形,其原因可能是在创伤或肥胖因素影响下,胫骨平台内侧大于外侧的不均匀沉降加大了力线向内侧偏距,最终导致内翻畸形和关节间隙狭窄等病变。这表明关节畸形的产生不完全是软骨磨损造成的,胫骨平台损伤也会造成力线偏距,导致膝骨关节炎患者关节畸形的加重。因此,通过有效指导患者步态训练以纠正力线偏距及深入中药在改善软骨性能方面的研究,可为膝骨关节炎防治提供新思路。 2.2 中医学对膝骨关节炎发病机制的认知 中医学将膝骨关节炎归属“骨痹”范畴,《素问·痹证》有云:“风、寒、湿三气杂至,合而为痹也……以冬遇此者为骨痹”,风寒湿邪乘虚侵袭,邪气流注关节,气机郁滞痹阻阳气,经络不通,血脉凝滞。《素问·长刺节论》“病在骨,骨重不可举,骨髓酸痛,寒气至,名曰骨痹”,强调寒邪侵入骨髓,致筋骨疼痛、活动不利,称为骨痹。《诸病源候论·虚劳膝冷候》“肾弱髓虚,为风冷所搏故也。肾居下焦主腰脚,其气荣润骨?,今肾虚受风寒,故令膝冷也”,强调了肾虚受邪,肾虚而髓减,筋骨失养,则发为膝骨痹。国医大师薛伯寿认为膝骨关节炎的核心病机是肾虚,同时寒湿、血瘀和湿热等实邪夹杂而至,发为膝骨痹[37]。周仲瑛则认为肝肾亏虚、风寒湿邪、痰瘀痹阻为膝骨关节炎的基本病机,骨痹初起多因年老肾气渐衰,肝肾亏损导致,气血无以化生,筋骨失养,外感诸邪乘入机体、客于关节,气血运行失畅、脉络壅滞[38]。施杞教授则提倡“三期论治膝骨关节炎”,以急性期气滞血瘀、筋脉失畅,亚急性期气血不足、痰湿内蕴证,慢性期肝肾亏虚、精血不足为辨证思想,认为肝脾肾亏虚、筋骨失衡为膝骨关节炎发病之本,风寒湿外邪侵袭、痰瘀阻滞经络是重要的致病因素,气血失和、瘀阻经脉则贯穿本病始终[39]。因此,膝骨关节炎的发病主要受外邪入侵、肝肾亏虚、痰瘀痹阻和气血亏虚等因素影响,治疗上主要以补益肝肾、活血祛瘀、蠲痹通络为主,兼以祛风除湿、调和气血。 2.3 中药单体及复方治疗膝骨关节炎的机制研究 目前中药被广泛应用于膝骨关节炎治疗中,其作用机制主要集中在调节炎性细胞因子水平[40-49]、软骨细胞自噬与凋亡[50-55]、VEGF水平和改善软骨性能方面[56-62],见表2及图4。"


2.3.1 调节炎性细胞因子水平 因创伤或负荷失衡等导致局部炎症产生,激活白细胞介素1β、白细胞介素6和肿瘤坏死因子α等炎症因子大量释放,加重局部乃至全身免疫炎症反应,最终导致早期关节炎症及损伤的发生。此外,TLRs、NF-κB等信号通路均能与炎性小体协同促使炎症因子表达,加剧炎症反应[40]。随着中药调节炎性因子水平干预膝骨关节炎研究的不断深入,目前发现中药在调节炎症因子、细胞免疫应答方面发挥重要的作用。 姜黄素,是来源于姜黄根茎中的多酚类物质,具有抗炎、抗氧化和抗肿瘤等作用。研究表明姜黄素通过与TLR结合,调节NF-κB、MAPK和JAK/STAT等信号通路,使白细胞介素1β、白细胞介素6、白细胞介素17和肿瘤坏死因子α炎症因子表达降低,以减轻膝骨关节炎炎症反应[41]。红景天提取物通过增加骨保护素表达,竞争性结合RANKL以抑制RANK活性,进一步抑制NF-κB通路活性及下调肿瘤坏死因子α、白细胞介素1β和前列腺素E2表达,实现降低机体炎症水平目的[42]。LI等[43]研究表明,芒果苷和肉桂酸的联合应用可介导TLR4/PI3K/AKT/NFκB信号通路,抑制NLRP3炎症复合体形成与激活,减少炎症因子肿瘤坏死因子α、白细胞介素6和白细胞介素12释放,有效缓解滑膜炎症、软骨降解和骨侵蚀对膝骨关节炎的影响。张金锋等[44]研究表明,丹参酮通过抑制TLR4/Myd88/NF-κB 信号通路的激活,显著降低了白细胞介素1β、白细胞介素6和肿瘤坏死因子α炎症因子表达,有效改善关节软骨形态及功能,以延缓膝骨关节炎进展。WANG等[45]研究表明甘草素通过下调NF-κB、p38/ERK1/2表达,减少NLRP3炎症复合体形成,并降低白细胞介素6、肿瘤坏死因子α、白细胞介素8和白细胞介素1β表达,有效减轻了组织炎性损伤。研究表明人参皂苷Rg1可抑制PI3K/AKT信号传导,激活STAT蛋白促进抗炎因子表达,并调节Treg/Tfr细胞分化平衡,恢复抗炎因子和促炎因子平衡,减轻了免疫炎症损伤[46]。葛海雅等[47]研究表明,化湿定痛汤可抑制Ras/Raf/Mek/Erk信号通路表达,进而减少滑膜组织炎症因子释放,以减轻关节周围组织炎症对软骨及滑膜组织的影响。此外,研究表明黄芪-黄连组合可激活STAT6信号,诱导M2巨噬细胞和Th2细胞分化,使M1/M2巨噬细胞和Th1/Th2细胞再平衡,达到抑制炎症的目的[48]。研究发现,防己黄芪消肿方可抑制 M1 型巨噬细胞极化,调控 M1/M2 巨噬细胞分化再平衡,进而抑制促炎因子及MMP的表达,以减轻滑膜炎症和软骨破坏对膝骨关节炎发展的影响[49]。综上,作者认为通过介导炎性通路可有效抑制炎症因子表达,减轻炎症反应;或直接干预NOD样受体及TLRs相关通路可有效改善滑膜炎症;或调节细胞分化,平衡M1/M2巨噬细胞、Th1/Th2及Treg/Tfr细胞表达,是降低免疫炎症反应,有效延缓膝骨关节炎进展的可靠途径。 2.3.2 调节软骨细胞自噬与凋亡 软骨细胞维系着关节软骨的稳定及功能,凋亡与自噬的异常表达会造成软骨的破坏与损伤,是膝骨关节炎发生发展的重要因素之一。因此,通过中药单体或复方调节软骨细胞自噬与凋亡,是有效延缓软骨损伤的重要途径。研究发现青蒿素通过抑制PI3K/AKT/mTOR信号通路表达,上调自噬基因Beclin-1、ATG5、ATG7和LC3表达,进而激活线粒体自噬以减少细胞凋亡[50]。XU等[51]研究表明当归多糖可上调软骨细胞自噬蛋白LC3II、Beclin-1、ATG5及抗凋亡蛋白Bcl-2表达,并下调促凋亡蛋白Bax表达,进而减少细胞凋亡;同时激活ERK1/2信号通路,促进自噬表达,降低了细胞凋亡对膝骨关节炎的影响。槲皮素通过激活SIRT1/AMPK信号通路,内质网应激受到抑制,软骨细胞凋亡数量减少,膝骨关节炎软骨退化变慢[52]。崔宏勋等[53]研究表明壮骨活血汤可下调PERK/eIF2α表达,进一步抑制CHOP转录及内质网应激,并降低caspase 12表达,有效减少软骨细胞凋亡。陈俊等[54]发现独活寄生汤可调控PERK/Bip信号通路,抑制内质网应激,降低PERK、Bip、eIF-2α、ATF-4、GADD153、Caspase-9和Caspase-3表达,减少了软骨细胞凋亡。CHEN等[55]研究表明,经FasL诱导后的细胞凋亡数量增加,芍药苷通过降低Fas和caspase-3表达水平,并抑制Fas-FasL信号通路的激活,以发挥抗凋亡作用。综上表明,调节自噬水平、抑制内质网应激、调节线粒体功能、平衡抗凋亡蛋白/促凋亡蛋白的表达及调节外源性死亡途径是中医药干预细胞凋亡与自噬的重点途径,可有效延缓膝骨关节炎发生发展。 2.3.3 调控VEGF水平 正常关节软骨在抗血管生成因子和促血管生成因子协调作用下保持平衡,因而在软骨潮线以外的非钙化层内不含血管。膝骨关节炎患者滑膜组织存在VEGF过度表达,因此造成血管生成因子之间的失衡,进而引发了血管生成增加、细胞凋亡、软骨基质破坏等变化。因此,针对VEGF的中医药调控研究越来越受到重视。AO等[56]研究表明苦参碱可调节HIF-VEGF-Ang轴和抑制PI3K/AKT信号通路表达,使抗血管生成因子表达增加,血管生成受到抑制;同时降低白细胞介素1β、干扰素γ表达,有效减轻了滑膜炎症。CHO等[57]发现地肤草提取物可下调P13K/AKT/mTOR通路,抑制内皮细胞的增殖、迁移,进而影响VEGFR-2活性,血管生成及炎症扩散受到抑制,延缓了膝骨关节炎进展。GUAN等[58]发现八宝丹呈剂量依赖性下调VEGFA、VEGFR-2、MMP-2和MMP-9表达,使内皮细胞的迁移、增殖及血管生成均受到抑制,表明介导VEGFA/VEGFR-2通路对血管生成调控,能够减缓VEGF对软骨基质的影响,达到保护关节软骨的目的。许奇等[59]发现温经通络汤可抑制VEGF/VEGFR2/ERK1/2信号通路和ADAMTS4的蛋白表达,减少内皮细胞的存活、增殖和侵袭,进而减轻软骨基质降解和软骨破坏,以延缓膝骨关节炎发生发展。综上,中药调节VEGF水平以HIF-VEGF、P13K/AKT/mTOR和VEGFA/VEGFR-2为主要调节途径,通过抑制血管生成造成的炎症、软骨破坏等影响,或直接抑制MMPs表达以减轻软骨降解,是防治膝骨关节炎的重要思路。但基于巨噬细胞与VEGF之间的调控研究甚少,通过构建巨噬细胞-VEGF的联系,全面揭示VEGF的调控机制,将为构建膝骨关节炎防治体系提供更完善的理论。 2.3.4 改善软骨性能 因创伤或肥胖因素导致关节软骨及软骨下骨承受应力不均,关节结构失稳,导致软骨磨损及关节间隙狭窄,加速了软骨的变性和损伤,因此,通过改善膝骨关节炎患者软骨性能及纠正力线偏距是防治膝骨关节炎进展的重要思路。研究发现鹿茸提取物可上调软骨生长与再生相关因子,如软骨形成的关键转录因子Trps1、维护关节完整性的生长因子Bmp6和促进软骨再生的细胞通信网络因子Cyr61表达,进而促进软骨生长与再生,有效改善软骨及软骨下骨性能[60]。梁婷[61]发现桦木酸可上调Ⅱ型胶原、蛋白聚糖的表达,并有效恢复软骨及软骨下骨的弹性模量,其机制可能与桦木酸改善膝关节软骨及软骨下骨的生物力学性能相关。赵忠胜等[62]研究表明,荣筋拈痛汤可下调MMP-3、MMP-9的表达,并上调Ⅱ型胶原和聚集蛋白聚糖的表达,通过影响软骨基质分解和合成代谢,减少软骨基质中胶原、蛋白多糖的丢失,以延缓软骨基质降解,减轻软骨组织形态结构的破坏,达到防治膝骨关节炎的目的。目前关于中药改善软骨性能的作用机制研究不足,深入信号通路及相关靶点研究会为膝骨关节炎防治提供更精准的依据。 "

| [1] 陈卫衡.膝骨关节炎中医诊疗指南(2020年版)[J].中医正骨,2020,32(10):1-14. [2] WANG L, LU H, CHEN H, et al. Development of a model for predicting the 4-year risk of symptomatic knee osteoarthritis in China: a longitudinal cohort study. Arthritis Res Ther. 2021;23(1):65. [3] 张莹莹,李旭东,杨佳娟,等.中国40岁及以上人群骨关节炎患病率的Meta分析[J].中国循证医学杂志,2021,21(4):407-414. [4] WANG H, MA B. Healthcare and scientific treatment of knee osteoarthritis. Healthc Eng. 2022;2022:5919686. [5] JANG S, LEE K, JU JH. Recent updates of diagnosis, pathophysiology, and treatment on osteoarthritis of the knee. Int J Mol Sci. 2021;22(5):2619. [6] TERKAWI MA, EBATA T, YOKOTA S, et al. Low-grade inflammation in the pathogenesis of osteoarthritis: cellular and molecular mechanisms and strategies for future therapeutic intervention. Biomedicines. 2022;10(5):1109. [7] NEDUNCHEZHIYAN U, VARUGHESE I, SUN AR,et al . Obesity, inflammation, and immune system in osteoarthritis. Front Immunol. 2022;13:907750. [8] ESTRADA MCDERMOTT J, PEZZANITE L, GOODRICH L, et al. Role of innate immunity in initiation and progression of osteoarthritis, with emphasis on horses. Animals (Basel). 2021;11(11):3247. [9] LAMBERT C, ZAPPIA J, SANCHEZ C, et al. The damage-associated molecular patterns (DAMPs) as potential targets to treat osteoarthritis:perspectives from a review of the literature. Front Med (Lausanne). 2021;7:607186. [10] SANCHEZ-LOPEZ E, CORAS R, TORRES A, et al. Synovial inflammation in osteoarthritis progression. Nat Rev Rheumatol. 2022;18(5):258-275. [11] KIM-WANG SY, HOLT AG, MCGOWAN AM, et al. Immune cell profiles in synovial fluid after anterior cruciate ligament and meniscus injuries. Arthritis Res Ther. 2021; 23(1):280. [12] SUN AR, WU X, LIU B, et al. Pro-resolving lipid mediator ameliorates obesity induced osteoarthritis by regulating synovial macrophage polarisation. Sci Rep. 2019;9(1):426. [13] ALAM MS, OTSUKA S, WONG N, et al. TNF plays a crucial role in inflammation by signaling via T cell TNFR2. Proc Natl Acad Sci USA. 2021;118(50):e2109972118. [14] SHEN PC, WU CL, JOU IM, et al. T helper cells promote disease progression of osteoarthritis by inducing macrophage inflammatory protein-1γ. Osteoarthritis Cartilage. 2011;19(6):728-736. [15] FAUST HJ, ZHANG H, HAN J, et al. IL-17 and immunologically induced senescence regulate response to injury in osteoarthritis. Clin Invest. 2020;130(10):5493-5507. [16] KONGDANG P, CHOKCHAITAWEESUK C, TANGYUENYONG S, et al. Proinflammatory effects of IL-1β combined with IL-17A promoted cartilage degradation and suppressed genes associated with cartilage matrix synthesis in vitro. Molecules. 2019;24(20):3682. [17] WANG Z, ZHENG C, ZHONG Y, et al. Interleukin-17 can induce osteoarthritis in rabbit knee joints similar to hulth’s method. Biomed Res Int. 2017;2017:2091325. [18] SHUI XL, LIN W, MAO CW, et al. Blockade of IL-17 alleviated inflammation in rat arthritis and MMP-13 expression. Eur Rev Med Pharmacol Sci. 2017;21(10):2329-2337. [19] SUN L, WANG X, SAREDY J,et al. Innate-adaptive immunity interplay and redox regulation in immune response. Redox Biol. 2020;37:101759. [20] OMATA Y, FRECH M, SAITO T,et al . Inflammatory arthritis and bone metabolism regulated by type 2 innate and adaptive immunity. Int J Mol Sci. 2022;23(3):1104. [21] SHIOKAWA S, MATSUMOTO N, NISHIMURA J. Clonal analysis of B cells in the osteoarthritis synovium. Ann Rheum Dis. 2001;60(8):802-805. [22] SALUCCI S, FALCIERI E, BATTISTELLI M. Chondrocyte death involvement in osteoarthritis. Cell Tissue Res. 2022;389(2):159-170. [23] TIAN C, LIU Y, LI Z, et al. Mitochondria related cell death modalities and disease. Front Cell Dev Biol. 2022;10:832356. [24] DONG X, YANG C, LUO Y, et al. USP7 attenuates endoplasmic reticulum stress and NF-κB signaling to modulate chondrocyte proliferation, apoptosis, and inflammatory response under inflammation. Oxid Med Cell Longev. 2022;2022:1835900. [25] TAKADA K, HIROSE J, YAMABE S, et al. Endoplasmic reticulum stress mediates nitric oxide-induced chondrocyte apoptosis. Biomed Rep. 2013;1(2):315-319. [26] ZHANG SL, ZHANG KS, WANG JF, et al. Corresponding changes of autophagy-related genes and proteins in different stages of knee osteoarthritis: an animal model study. Orthop Surg. 2022;14(3):595-604. [27] LI C, LIN L, ZHANG L, et al. Long noncoding RNA p21 enhances autophagy to alleviate endothelial progenitor cells damage and promote endothelial repair in hypertension through SESN2/AMPK/TSC2 pathway. Pharmacol Res. 2021;173:105920. [28] CHEN Y, PAN X, ZHAO J, et al. Icariin alleviates osteoarthritis through PI3K/Akt/mTOR/ULK1 signaling pathway. Eur J Med Res. 2022;27(1):204. [29] AKARAPHUTIPORN E, SUNAGA T, BWALYA EC, et al. An insight into the role of apoptosis and autophagy in nitric oxide-Induced articularchondrocyte cell death. Cartilage. 2021; 13(2_suppl):826S-838S. [30] QIN Q, LIU Y, YANG Z, et al. Hypoxia-inducible factors signaling in osteogenesis and skeletal repair. Int J Mol Sci. 2022;23(19):11201. [31] MILLER B, SEWELL-LOFTIN MK. Mechanoregulation of vascular endothelial growth factor receptor 2 in angiogenesis. Front Cardiovasc Med. 2022;8:804934. [32] QIAN JJ, XU Q, XU WM, et al. Expression of VEGF-A signaling pathway in cartilage of ACLT-induced osteoarthritis mouse model. Orthop Surg Res. 2021;16(1):379. [33] LUNA M, GUSS JD, VASQUEZ-BOLANOS LS, et al. Obesity and load-induced posttraumatic osteoarthritis in the absence of fracture or surgical trauma. Orthop Res. 2021;39(5):1007-1016. [34] AL KHATIB F, GOUISSEM A, MBARKI R, et al. Biomechanical characteristics of the knee joint during gait in obese versus normal subjects. Int J Environ Res Public Health. 2022;19(2):989. [35] FUKAYA T, MUTSUZAKI H, AOYAMA T, et al . A simulation case study of knee joint compressive stress during the stance phase in severe knee osteoarthritis using finite element method. Medicina (Kaunas). 2021;57(6):550. [36] 甘浩然,程楷,赵文胜,等.膝骨关节炎中骨性力线改变的影像学及临床研究[J].实用骨科杂志,2019,25(8):709-712+723. [37] 肖战说.国医大师薛伯寿辨治膝骨关节炎经验及补肾壮骨方自噬相关机制研究[D].北京:中国中医科学院,2022. [38] 张硕.周仲瑛教授益肾通络法治疗膝骨关节炎的临床研究[D].南京:南京中医药大学,2016. [39] 李晓锋,侯炜,薛纯纯,等.施杞从三期论治膝骨关节炎临床经验撷英[J].上海中医药杂志,2021,55(8):25-28. [40] 章晓云,曾浩,李华南,等.痛风性关节炎的发病机制及中医药治疗研究进展[J].中国实验方剂学杂志,2022,28(11):256-267. [41] PENG Y, AO M, DONG B, et al . Anti-inflammatory effects of gurcumin in the inflammatory diseases: status, limitations and countermeasures. Drug Des Devel Ther. 2021;15:4503-4525. [42] MA Y, ZHANG J, YU H, et al. Traditional chinese medicine rhodiola sachalinensis borissova from baekdu mountain (RsBBM) for rheumatoid arthritis: therapeutic effect and underlying molecular mechanisms. Molecules. 2022;27(18):6058. [43] LI W, WANG K, LIU Y, et al. A novel drug combination of mangiferin and cinnamic acid alleviates rheumatoid arthritis by inhibiting TLR4/NFκB/NLRP3 activation-induced pyroptosis. Front Immunol. 2022;13:912933. [44] 张金锋,徐志龙,吴梦,等.丹参酮ⅡA通过抑制信号通路延缓膝骨关节炎大鼠软骨退变及抑制局部炎症的研究[J].中国药学杂志,2021,56(23):1918-1926. [45] WANG Z, XU G, LI Z, et al. NLRP3 inflammasome pharmacological inhibitors in glycyrrhiza for NLRP3-driven diseases treatment: extinguishing the fire of inflammation. Inflamm Res. 2022;15:409-422. [46] JIN J, ZHONG Y, LONG J, et al. Ginsenoside Rg1 relieves experimental colitis by regulating balanced differentiation of Tfh/Treg cells. Int Immunopharmacol. 2021;100:108133. [47] 葛海雅,李楠,张燕,等.基于Ras/Raf/Mek/Erk信号通路探讨化湿定痛汤减轻膝骨关节炎大鼠滑膜炎症的机制[J].中华中医药杂志,2022,37(8):4428-4432. [48] LI Z, MA D, WANG Y, et al. Astragali radix-coptis rhizoma herb pair attenuates atherosclerosis in apoe-/- mice by regulating the M1/M2 and Th1/Th2 immune balance and activating the STAT6 signaling pathway. Evid Based Complement Alternat Med. 2022;2022:7421265. [49] 危一飞,程桯,肖潇,等.防己黄芪消肿方调控滑膜巨噬细胞极化治疗膝骨关节炎滑膜炎[J].中国实验方剂学杂志,2022,28(13):112-122. [50] LI J, JIANG M, YU Z, et al. Artemisinin relieves osteoarthritis by activating mitochondrial autophagy through reducing TNFSF11 expression and inhibiting PI3K/AKT/mTOR signaling in cartilage. Cell Mol Biol Lett. 2022;27(1):62. [51] XU C, NI S, ZHUANG C, et al. Polysaccharide from angelica sinensis attenuates SNP-induced apoptosis in osteoarthritis chondrocytes by inducing autophagy via the ERK1/2 pathway. Arthritis Res Ther. 2021;23(1):47. [52] FENG K, CHEN Z, PENGCHENG L, et al. Quercetin attenuates oxidative stress-induced apoptosis via SIRT1/AMPK-mediated inhibition of ER stress in rat chondrocytes and prevents the progression of osteoarthritis in a rat model. Cell Physiol. 2019;234(10):18192-18205. [53] 崔宏勋,郑振雨,郭珈宜,等.壮骨活血汤介导内质网应激调控人软骨细胞凋亡防治膝关节骨性关节炎的机制[J].中华中医药杂志,2022,37(8):4814-4818. [54] 陈俊,吴广文,许惠凤,等.独活寄生汤干预膝骨关节炎模型大鼠软骨PERK/Bip信号通路的表达[J].中国组织工程研究,2018,22(28):4493-4500. [55] CHEN SQ, LIN JP, ZHENG QK, et al. Protective effects of paeoniflorin against FasL-induced apoptosis of intervertebral disc annulus fibrosus cells via Fas-FasL signalling pathway. Exp Ther Med. 2015;10(6):2351-2355. [56] AO L, GAO H, JIA L, et al. Matrine inhibits synovial angiogenesis in collagen-induced arthritis rats by regulating HIF-VEGF-Ang and inhibiting the PI3K/Akt signaling pathway. Mol Immunol. 2022;141:13-20. [57] CHO HD, KIM JH, PARK JK,et al. Kochia scoparia seed extract suppresses VEGF-induced angiogenesis via modulating VEGF receptor 2 and PI3K/AKT/mTOR pathways. Pharm Biol. 2019;57(1):684-693. [58] GUAN JH, CAO ZY, GUAN B, et al. Effect of babao dan on angiogenesis of gastric cancer in vitro by regulating VEGFA/VEGFR2 signaling pathway. Transl Cancer Res. 2021;10(2): 953-965. [59] 许奇,钱佳佳,许炜民,等.温经通络汤对膝骨关节炎模型小鼠VEGF/VEGFR2/ERK1/2信号通路的影响[J].中国实验方剂学杂志,2021,27(13):28-34. [60] GUAN M, PAN D, ZHANG M, et al . Deer antler extract potentially facilitates xiphoid cartilage growth and regeneration and prevents inflammatory susceptibility by regulating multiple functional genes. Orthop Surg Res. 2021;16(1):208. [61] 梁婷.桦木酸通过改善小鼠软骨及软骨下骨微纳力学性能缓解骨关节炎的研究[J].医用生物力学,2021,36(S1):38. [62] 赵忠胜,郑若曦,林洁,等.荣筋拈痛方调控软骨基质代谢防治膝骨关节炎[J].中国组织工程研究,2023,27(20):3195-3201. |
| [1] | Li Yongjie, Fu Shenyu, Xia Yuan, Zhang Dakuan, Liu Hongju. Correlation of knee extensor muscle strength and spatiotemporal gait parameters with peak knee flexion/adduction moment in female patients with knee osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(9): 1354-1358. |
| [2] | Du Changling, Shi Hui, Zhang Shoutao, Meng Tao, Liu Dong, Li Jian, Cao Heng, Xu Chuang. Efficacy and safety of different applications of tranexamic acid in high tibial osteotomy [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(9): 1409-1413. |
| [3] | Qi Xue, Li Jiahui, Zhu Yuanfeng, Yu Lu, Wang Peng. Abnormal modification of alpha-synuclein and its mechanism in Parkinson’s disease [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(8): 1301-1306. |
| [4] | Zhang Xiaoyun, Liu Hua, Chai Yuan, Chen Feng, Zeng Hao, Gao Zhengang, Huang Yourong. Effect of Yishen Gushu Formula on bone metabolic markers and clinical efficacyn in patients with osteoporosis of kidney deficiency and blood stasis type [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(8): 1155-1160. |
| [5] | Huang Xiarong, Hu Lizhi, Sun Guanghua, Peng Xinke, Liao Ying, Liao Yuan, Liu Jing, Yin Linwei, Zhong Peirui, Peng Ting, Zhou Jun, Qu Mengjian. Effect of electroacupuncture on the expression of P53 and P21 in articular cartilage and subchondral bone of aged rats with knee osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(8): 1174-1179. |
| [6] | Pan Xiaolong, Fan Feiyan, Ying Chunmiao, Liu Feixiang, Zhang Yunke. Effect and mechanism of traditional Chinese medicine on inhibiting the aging of mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(7): 1091-1098. |
| [7] | Zhang Zeyi, Yang Yimin, Li Wenyan, Zhang Meizhen. Effect of foot progression angle on lower extremity kinetics of knee osteoarthritis patients of different ages: a systematic review and meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(6): 968-975. |
| [8] | Shen Feiyan, Yao Jixiang, Su Shanshan, Zhao Zhongmin, Tang Weidong. Knockdown of circRNA WD repeat containing protein 1 inhibits proliferation and induces apoptosis of chondrocytes in knee osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 499-504. |
| [9] | Maisituremu·Heilili, Zhang Wanxia, Nijiati·Nuermuhanmode, Maimaitituxun·Tuerdi. Effect of intraarticular injection of different concentrations of ozone on condylar histology of rats with early temporomandibular joint osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 505-509. |
| [10] | Wei Yuanxun, Chen Feng, Lin Zonghan, Zhang Chi, Pan Chengzhen, Wei Zongbo. The mechanism of Notch signaling pathway in osteoporosis and its prevention and treatment with traditional Chinese medicine [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 587-593. |
| [11] | Liu Luxing, Di Mingyuan, Yang Qiang. Signaling pathways in the mechanism underlying active ingredients of Chinese medicine in the treatment of osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(4): 609-614. |
| [12] | Xie Peng, Zhang Jiang, Deng Xiaolei, Wei Bo, Hou Decai. A systematic review of mouse model construction for sarcopenia [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(2): 263-266. |
| [13] | Zhang Huizhen, Wu Wei, Luo Haitao. Medium to low intensity exercise interferes with the expression of LncRNA HOTAIR in chondrocytes in high-fat-fed mice with knee joint damage [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(11): 1684-1689. |
| [14] | Zeng Jiaxu, He Qi, Chen Bohao, Li Miao, Li Shaocong, Yang Junzheng, Pan Zhaofeng, Wang Haibin. An insight into the mechanism of iron overload in knee osteoarthritis under the theory of blood stasis [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(11): 1743-1748. |
| [15] | Xu Kangli, An Lanhua, Zhang Jinsheng, Du Xiaoyan, Yin Lele, Zhang Xixian. Research hotspots and frontiers of functional magnetic resonance imaging in treatment of ischemic stroke by traditional Chinese medicine [J]. Chinese Journal of Tissue Engineering Research, 2024, 28(11): 1789-1796. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||