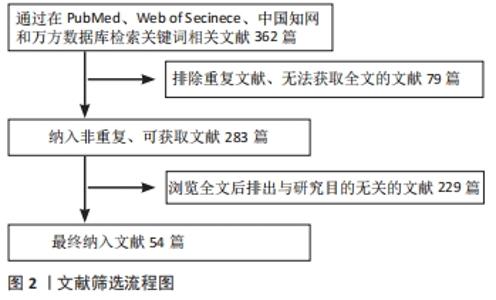
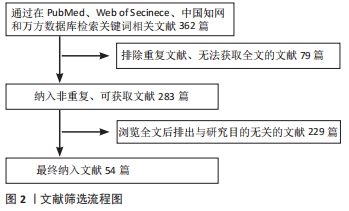
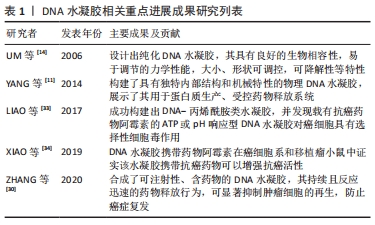
Chinese Journal of Tissue Engineering Research ›› 2022, Vol. 26 ›› Issue (27): 4379-4385.doi: 10.12307/2022.871
Previous Articles Next Articles
DNA hydrogel based on drug delivery and bone tissue engineering
Gao Zhao1, Zhao Yuhao1, He Yixiang1, Zhao Haiyan2, Wang Wenji2
- 1First Clinical Medical College of Lanzhou University, Lanzhou 730000, Gansu Province, China; 2Department of Orthopedics, First Hospital of Lanzhou University, Lanzhou 730000, Gansu Province, China
-
Received:2021-03-29Accepted:2021-05-08Online:2022-09-28Published:2022-03-12 -
Contact:Wang Wenji, Professor, Chief physician, Master’s supervisor, Department of Orthopedics, First Hospital of Lanzhou University, Lanzhou 730000, Gansu Province, China -
About author:Gao Zhao, Master candidate, First Clinical Medical College of Lanzhou University, Lanzhou 730000, Gansu Province, China -
Supported by:Fund Project of Lanzhou Talent Innovation and Entrepreneurship Project, No. 2020-RC-45 (to ZHY)
CLC Number:
Cite this article
Gao Zhao, Zhao Yuhao, He Yixiang, Zhao Haiyan, Wang Wenji. DNA hydrogel based on drug delivery and bone tissue engineering[J]. Chinese Journal of Tissue Engineering Research, 2022, 26(27): 4379-4385.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
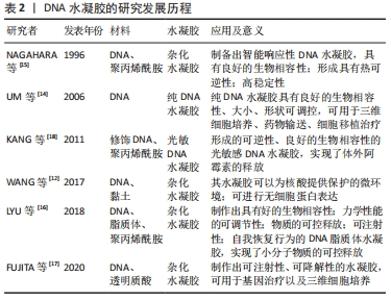
2.3 DNA水凝胶概述 DNA由脱氧核糖核酸组成的大分子聚合物。脱氧核苷酸由碱基、脱氧核糖和磷酸构成,其中碱基有4种:腺嘌呤(A)、鸟嘌呤(G)、胸腺嘧啶(T)和胞嘧啶(C)。DNA作为一种重要的遗传大分子,也是一种普通的结构材料,具有许多独特和迷人的特性,包括不可或缺的遗传功能、良好的生物相容性、精确的分子识别能力、可调的多功能和序列可编程性等特性。因此,DNA可以说既是完美的也是惟一的分子,能够连接生物和材料。DNA为创造新的生物响应性提供了关键和理想的前提条件,并开始日益成为构建水凝胶的不可替代和强大的基本单元[9-11]。由于合成DNA水凝胶需要大量DNA,需要消耗相关的高成本[12],目前,主要通过天然核酸提取及化学合成这2种方式获得形成DNA水凝胶的基础原料,并与核酸扩增手段相结合,包括变温扩增手段(如PCR)、等温扩增手段(如滚环扩增)以及非酶依赖的恒温链式杂交反应和DNA超级三明治结构等[13]。由DNA为支架构成的DNA水凝胶含水量可达到90%以上,通常由人工合成或天然提取的DNA作为原料,进行三维交联形成空间网络而成。由于DNA本身为生物大分子,形成水凝胶后将具有很好的生物相容性。而DNA所具有的智能响应性将使其有别于普通化学水凝胶,实现水凝胶的“智能化”,在药物载体、组织工程和智能器件等方面起重要作用。 2.4 不同类型的DNA水凝胶 DNA水凝胶则是一种依靠Wason-Crick碱基配对形成大规模可编程三维纳米DNA组分网络的自组装生物材料[14-15],其最早在1996年被NAGAHARA等[15]发现,随后UM等[14]通过将设计的支链DNA,相互交联形成纯化DNA水凝胶。许多学者将DNA与不同高分子材料(如聚丙烯酰胺、透明质酸、脂质体、胶原蛋白和海藻酸等)交联,形成杂化DNA水凝胶[12,14-18],主要发展历程见表2。"
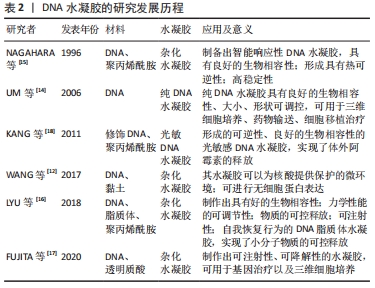
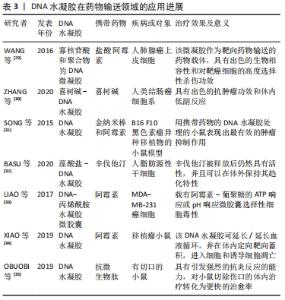
2.4.1 纯DNA水凝胶 将DNA本身交联,通过酶解、聚合、杂交和DNA基元的特异性结合形成水凝胶,称为纯DNA水凝胶。有研究设计和合成了分支DNA单体,该DNA单体的每个臂都有1个互补的黏性末端,其序列是回文的[14]。分支DNA单体的自组装与T4 DNA连接酶催化的反应相结合,形成了具有大规模三维结构的纯DNA水凝胶,它具有多种优点,包括:①由于其凝胶过程完全在生理条件下(无有机溶剂或高温),DNA凝胶可用于包裹活的哺乳动物细胞。②与质粒DNA不同,质粒DNA可能引起宿主免疫反应,DNA水凝胶由于其纯粹的合成性质,预计不具有免疫原性,具有良好的生物相容性。③DNA水凝胶的力学性能易于调节,在线性范围内,在给一定应力的条件下,交联的DNA分子维持现有的形状。④DNA水凝胶是一种机械性能易于调节的软材料。⑤DNA水凝胶的大小和形状可以精确控制。除了大小和形状外,它的形态和内部结构也有很大的变化,也可以根据分支DNA单体进行调节。⑥DNA水凝胶是可生物降解的,它们的降解性也应该依赖于分支DNA单体,因此可以通过分支DNA单体进行调节。 2.4.2 杂化DNA水凝胶 以DNA为支链的亲水聚合物链进行改性,然后通过交联这些支链形成杂化DNA水凝胶。其中DNA作为交联剂调节聚合物水凝胶的机械性能和响应性。DNA-聚合物杂化水凝胶的优点是减少了DNA含量,从而降低了材料成本,并且能够加入替代的功能基序以实现细胞黏附、水凝胶降解,或者用于动态调整机械性能的替代机制[19]。下文将着重介绍几种特殊类型杂化DNA水凝胶。 DNA聚合物水凝胶:值得注意的是,1996年,NAGAHARA等[15]通过将单链DNA接枝到聚丙烯酰胺链上,设计了第一个基于DNA的杂化水凝胶,其具有高膨胀性。利用寡核苷酸的互补碱基对进行杂交形成水凝胶具有以下特点:①由于互补寡核苷酸在室温下自发杂交,凝胶中固定的生物活性物质在水凝胶形成过程中将保持完好,没有任何副反应。②凝胶的形成是热可逆的。原则上,寡聚核苷酸的溶胀特性及其热响应性可以通过寡核苷酸的含量和碱基序列(组成和长度)来控制。虽然核酸碱基之间的一对氢键很弱,但特定序列氢键的总和能够制备一种新的具有高稳定性的水凝胶,就像在DNA的情况下所发现的那样[15]。有研究使用脂质体对用作交联剂的单链DNA进行修饰,然后将这种经DNA修饰的脂质体用于交联聚丙烯酰胺,得到DNA水凝胶[16]。CAI等[20]制备了一种DNA-聚丙烯酰胺杂化水凝胶,在这种水凝胶中,Hg2+激活了Hg2+特异的DNA酶,产生单链DNA,进而在2条发夹修饰的聚合物链之间引发杂交链式反应,从而在电极上诱导DNA-聚丙烯酰胺杂化水凝胶的形成。因DNA链需要直接与DNA交联剂相互作用来形成DNA水凝胶网络,需要在体系中加入高浓度的外源DNA。有研究将透明质酸与通过消化pUC118质粒与BSp1286I获得的DNA片段结合,通过杂交形成透明质酸DNA水凝胶。这种水凝胶容易被限制酶切开,并通过热变性分离,此属性还可能导致申请基因信息传递。因此,该材料具有生物和医疗应用的潜力[17]。 DNA黏土水凝胶:由于黏土水凝胶的独特结构,它为生物分子,特别是核酸提供了保护的微环境,进一步提高了生物响应反应的效率[21]。有研究利用黏土呈片状结构,在粒子的触发下,首先形成黏土水凝胶,随后,DNA通过静电作用连接到黏土水凝胶上,形成DNA-黏土水凝胶,或者通过DNA与黏土按一定比例结合,然后用离子刺激DNA-黏土水凝胶形成[12]。 基于特殊DNA结构的pH响应性DNA水凝胶:滚环扩增法(RCA)是一种高效、准确的等温扩增DNA的方法,利用滚环扩增法扩增DNA,通过合理设计模板序列,实现了滚环扩增法产物之间的分子间G-四链相互作用,并作为交联剂制备了功能化DNA水凝胶[22]。有研究设计了一种线形DNA,它包含1个双链,两端都有2个I-motif,由富含胞嘧啶的DNA序列形成的一种特殊的四链结构富含胞嘧啶的序列[23]。在pH值为8的条件下,这种线性DNA链可以先组装成双相。将pH值调为5后,富胞嘧啶序列倾向于形成分子间I-motif,使线性DNA分子连接在一起形成环状结构,形成DNA水凝胶。 酶响应性DNA水凝胶:DNA连接酶能将DNA片段与互补的黏性末端连接起来,并能修复带有3′-羟基和5′-磷酸末端的双链DNA上的缺口。NOLL等[24]通过酶切从质粒DNA中获得的线性双链DNA。水凝胶的形成是通过在酶连接过程中各个构建块之间形成共价键来实现的。通过用两种内切酶酶切质粒,产生2个带有黏性末端的线性双链DNA,其中包含自互补的回文序列,然后在连接酶的指导下形成DNA水凝胶。聚合酶如末端脱氧核苷酸转移酶催化dATP在引物的3′-OH末端重复加成,进而促进DNA自组装成水凝胶[25]。 光响应性DNA水凝胶:一种光调控所形成的DNA水凝胶,即光可控DNA水凝胶,主要是在紫外光或者自然光的刺激下,利用常规DNA序列经Watson-Crick碱基互补配对形成的DNA分支结构或多种功能核酸的特殊DNA序列形成的i-motif结构;T-A·T三螺旋结构、C-G·C+三螺旋结构及G-四链体结构等对光的敏感行为使水凝胶形成。DNA结构不易被光所影响,可在其中引入光敏基团,通过光敏基团的光诱导异构化引起DNA结构变化,进而导致水凝胶微观结构和宏观形态的变化。光可控DNA水凝胶形成主要包括2类,1类为偶氮苯结合的DNA被用作交联剂来形成水凝胶,这使得交联过程可以通过可见光和紫外光可逆地控制。在紫外光照射下,偶氮苯在反式和顺式之间发生异构化,决定了偶氮苯DNA与其互补链杂交的可能性[26]。基于此,有研究设计了一种新型的具有可逆光控制性的DNA交联聚合物杂化水凝胶[18]。这些水凝胶是通过在DNA交联剂中掺入偶氮苯基团来功能化的。该水凝胶是一种新型的可逆光调控水凝胶,并利用溶胶-凝胶转换来封装和释放不同的负载。偶氮化DNA交联剂不仅对水凝胶的构建至关重要,而且对水凝胶的光敏性、光控性等物理性能也具有重要意义。第2类为光热诱导DNA水凝胶形成。有研究实现了基于Y-DNA和接头DNA的光控DNA水凝胶形成[27],其中Y-DNA和接头DNA分别由3个和2个单链DNA组成的黏性末端具有互补的序列对的DNA。在光学控制方面,引入了一种C-DNA的单链DNA,存在Y-DNA的黏性互补末端,两端具有猝灭剂。在光激发猝灭剂后,热能在弛豫过程中被释放,Y-DNA从C-DNA解离并与接头-DNA连接形成DNA水凝胶。这一过程仅限于激发光的照射区域。DNA水凝胶的产量取决于光照强度,因此可以通过改变辐照方式灵活地控制其形状。 2.5 DNA水凝胶在药物释放方面的应用 传统给药往往需要频繁给药或大剂量给药才能达到治疗效果,它经常伴随全身不良反应,从而降低整体疗效和患者依从性。设计活性高效的载体,实现小分子和生物分子药物的可控给药是非常必要的。已经报道了广泛应用的载体,如无机纳米粒子、聚合物、蛋白质和脂质体,尽管它们的固有特性提高了治疗效果,但载体引起的免疫原性问题、非特异性凝集和难以生物降解性仍然是完全有效的障碍[28]。DNA微凝胶由于能够在其交联的多孔网络中封装不同种类的生物分子,无机纳米颗粒或小分子药物而被广泛用作控制药物输送的载体。近年来,DNA水凝胶系统已应用于药物输送[29-35],见表3。"
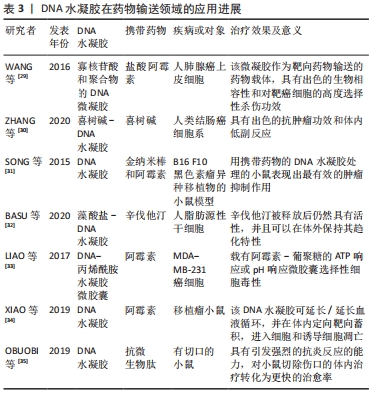

与传统载体不同,DNA水凝胶作为各种给药系统的载体具有很大的优势,它除了实现药物的原位包裹外,还可以建立与靶区的分子识别,提高细胞转染效率,保护生物分子有效载荷不被核酸酶或蛋白酶降解,减少非特异性分布,整合多种成分以实现协同治疗。这些诱人的优势极大地推动了核酸药物和功能蛋白的实际应用。因无机纳米粒子、小分子药物和功能性生物大分子都可以以一定的负载效率结合到DNA水凝胶的多孔网络中,它实现了一般治疗、免疫治疗和基因治疗的高性能传递系统。 2.5.1 DNA水凝胶用于疾病的一般治疗 DNA水凝胶可以对药物进行原位包裹,以及与靶区分子识别来实现一些疾病的治疗。现已有临床试验表明,DNA水凝胶可以作为辅助治疗传染病和癌症性的有效载体。KANG等[18]选择了一种抗癌药物阿霉素,以光可控水凝胶为载体,对荧光素分子进行包裹和释放,紫外线照射引发了大量药物快速释放到溶液中,再进行细胞活性研究。与未加水凝胶的细胞溶液相比,所有DNA水凝胶的细胞死亡率都增加了不到10%,这是由材料毒性和药物泄漏引起的;偶氮化DNA水凝胶在可见光下表现出与DNA水凝胶相似的形貌,表明偶氮部分对细胞活力的影响不大;然而,在紫外光照射下,偶氮化DNA水凝胶融化并释放负载的大量抗癌药物阿霉素,这反过来又导致了非常高的癌细胞死亡率(高约80%)。这些结果验证了偶氮化DNA水凝胶对紫外光的敏感光响应,释放了大量活性药物分子,从而抑制了细胞增殖。KIM等[36]研究了一种具有微流控智能DNA水凝胶及其在利用微流控设备高效释放蛋白质方面的应用,通过改变智能DNA水凝胶的大小来控制蛋白质的释放曲线。智能DNA水凝胶可以与天然酶中的DNA相互作用,它将进一步提供许多工具,以精确地操纵基于DNA的功能材料。SONG等[37]使用一种适体引发的恒温链式杂交反应成功合成多孔DNA水凝胶,用于循环肿瘤细胞的原位鉴定、释放以及活细胞分析。LYU等[16]报告了构建交联的响应性智能DNA水凝胶,实现功能性小分子有效载荷的控制释放。这些都表明,DNA水凝胶可以对药物实现原位包裹,并与药物分子进行特异性识别,保护药物免受体内各种酶的降解,实现了药物的靶向治疗。 2.5.2 DNA水凝胶用于免疫治疗 DNA水凝胶通过其加载免疫刺激序列的能力,已经显示出免疫治疗的许多优点。非甲基化的胞嘧啶-磷酸-鸟嘌呤二核苷酸(CpG DNA)是Toll样受体9的配体,与Toll样受体9结合后激活天然免疫系统。与功能DNA结构(非甲基化的CpG DNA)结合在一起,在免疫调控应用中是很有前途的材料,因为它在水凝胶和分析物之间引入了额外的界面。因此,CpG DNA可作为免疫治疗的佐剂用于治疗多种疾病[38]。目前,已有研究将CpG序列作为DNA水凝胶的功能成分,并将其应用于免疫调控领域。NISHIKAWA等[39]初步探索了将免疫刺激性CpG DNA自组装形成DNA水凝胶。证实CpG DNA水凝胶是一种有效的持续系统,可以将免疫刺激信号传递给Toll样受体9阳性的免疫细胞,并将嵌入型阿霉素传递给癌细胞,随后他们基于相似的原理合成了一种可注射的免疫调节DNA水凝胶用于抗原递送。在研究中,LEE等[40]利用Cas9/sgRNA的双链DNA精确编辑功能,设计了一种能够程序化释放PD-1适配子的DNA水凝胶,利用滚环扩增法的方法形成了DNA-适配子水凝胶,滚环扩增法产物包含适体的重复序列以及编码靶标或互补靶标序列的sgRNAs,通过内部位点交联形成水凝胶。水凝胶作用于Cas9/sgRNA后,在给药部位持续释放PD-1 DNA适配子,并通过增强免疫系统的激活发挥抗肿瘤作用,表明通过对DNA水凝胶的组成结构进行设计以及其携带药物的能力,未来在免疫治疗方面可能有广泛的应用前景。因此通过DNA精确设计的DNA水凝胶在抗癌免疫治疗方面具有很强的潜力。 2.5.3 DNA水凝胶用于基因治疗 基因治疗为通过将基因产物导入细胞来纠正疾病的病因,被认为是许多疾病的潜在候选者,如传染病、癌症和遗传疾病,但在其配方、给药方法和作用机制方面都存在许多障碍和问号。在这些问题中,基因转移系统因在临床试验中造成不良影响和低效而首当其冲。在关于基因治疗的研究中,有关水凝胶共聚物以及其他聚合物体系的应用逐年增加,聚合物系统是较新的系统,还没有被广泛使用,这解释了与临床试验的不同之处[41]。DNA微凝胶具有出色的生物相容性、生物降解性、结构和功能多样性,有利于基因传递,促进基因调控,提高生物安全性,因此有望成为基因传递的候选药物。近年来,已开发出多种基因加载的DNA水凝胶系统,用于基因调节。反义寡核苷酸可作为一种有效治疗癌症的潜在途径。然而,反义药物固有的不稳定性和低效的全身给药方式仍然是其临床应用的主要挑战。SARDONE等[42]通过一种新的合成反义单链寡核苷酸分子,通过靶向hnRNAs或mRNAs,干扰剪接、mRNA降解或抑制翻译,从而调节蛋白表达,最终导致靶蛋白表达的挽救或降低,来治疗一些无法治疗的疾病。有研究通过酶延伸法(滚动循环复制)自组装,生成复合核酸/焦磷酸镁海绵状微结构或DNA微长条,可显著提高核酸药物/载体的稳定性体内生物分布[43]。这些聚合物反义寡核苷酸系统可被设计成一种有效的手段,以显著低于传统合成载体的毒性,系统地向肿瘤细胞提供稳定和大量的反义寡核苷酸治疗药物,从而为临床翻译提供了一个治疗窗口。因此,DNA水凝胶作为反义核苷酸的承载系统,具有治疗癌症、传染病其他疾病的潜能。 2.6 DNA水凝胶在骨组织工程方面的应用 2.6.1 细胞培养 三维细胞培养通过提供与体内类似的微环境和对治疗药物的反应,在肿瘤生物学中发挥着不可估量的作用。由于水凝胶的三维结构以及其有高的机械强度、可控的形貌和良好的流变性能,与血液凝块和人工细胞外基质得许多方面类似[7],其高度膨胀的环境使营养物质和废物得以轻松运输,支持多种细胞类型的长期生存,而三维框架可以指导细胞相互作用和基质沉积。因此,合成水凝胶是三维培养人骨髓间充质干细胞的高度可控环境。包裹的人骨髓间充质干细胞呈现在一个“空白”的环境中,这个环境可以被严密地控制以诱导成骨反应。DNA水凝胶为细胞提供类似天然细胞外基质的三维环境。有研究制备了一种快速形成的超分子多肽-DNA水凝胶,并首次用于原位多层三维生物打印[44]。3D细胞打印被证明可以制造具有正常细胞功能的含有活细胞的结构。结合独特的生物相容性、渗透性和生物降解性,该水凝胶成为3D生物打印的理想生物材料,以生产用于组织工程应用的可设计3D结构。HOFFMAN等[45]在研究中,通过与未经处理的同种异体移植物对照相比,通过水凝胶为基础的骨膜将间充质干细胞移植到同种异体移植物表面,证明经骨膜修饰的同种异体移植物血管浸润和骨痂形成增加,促进了同种异体移植物的愈合。此外,使用骨膜移植的骨髓间充质干细胞也被证明直接有助于骨痂的形成,其间充质、软骨和编织骨的数量比未经处理的同种异体移植物更多。因此该DNA水凝胶可以用于携带骨髓间充质干细胞,通过促进骨痂的形成和诱导其分化来治疗骨缺损。 2.6.2 促进骨形成 基于DNA的水凝胶制剂除了可以注射并显示出受控的药物释放特性外,其还可以用与骨缺损的治疗[45-52],见表4。"


近年来,骨缺损的发生率增加,特别是在骨肿瘤切除的情况下,需要合适的骨移植和替代物。建立一个骨缺损替代模型在受控条件下的骨替代物和相关的修复过程[5]。有多种骨替代物可以用来替代骨丢失,但尽管进行了大量的研究,临床结果常并不令人满意。骨组织工程在骨增强、骨修复方面的应用日益突出,并有了新的发展前景。骨组织工程的目标是用创新的支架促进关键缺损处的骨形成,这种支架应具备生物相容性和生物可吸收[6]。DNA水凝胶的生物相容性、生物降解性、可注射性和多种功能化能力,可以将药理活性分子输送到骨组织,是骨组织工程应用的良好候选材料。有研究运用化学修饰的人血清白蛋白和合理设计的DNA制备多功能杂化DNA水凝胶[46],利用其在生理条件下通过DNA杂交快速凝胶化,自我愈合和注射的性质,以及特定负载和时空可控释放活性蛋白的可能性,把C2IN-C3lim-G205C突变体(来自肉毒杆菌的c2毒素的无毒部分-c3毒素-半胱氨酸代替205位甘氨酸的肉毒杆菌)运送到骨组织,有效减少了体外破骨细胞的形成和吸收活性,但不影响成骨细胞的分化和矿化。不仅为促进骨骼疾病的骨骼修复提供了一种很有前途的策略,而且也为局部骨质量的改善提供了一个很有前途的策略,例如,在紧邻骨植入物周围的地方。此外,在释放治疗蛋白后,这种水凝胶是可降解和无毒的,这对非侵入性治疗至关重要。有研究表明,纳米复合水凝胶通过递送骨髓间充质干细胞,用于覆盖从髋关节区域分离的同种异体骨,可以加快将同种异体骨移植整合到宿主组织中的过程。通过对未涂覆和涂覆的同种异体移植物的相比表明,设计的可注射纳米复合水凝胶可潜在地用作调节成骨药物释放或用作生物印刷油墨以及同种异体骨涂层的多功能平台[45]。在理想状态下,配制的水凝胶然后可以充当药物洗脱生物活性层,以增强同种异体骨的治疗功效。众所周知,地塞米松是体外诱导人骨髓间充质干细胞向成骨分化的有效、可靠的因子[47]。有研究成功设计了具有剪切力的DNA-硅酸盐纳米复合水凝胶,具有快速的自愈特性[48],通过将制备的水凝胶注射到大鼠颅骨缺损模型中进行体内初步研究,证实通过用水凝胶携带地塞米松到骨部位,在释放后仍保持其生物活性可刺激骨髓间充质干细胞细胞成骨分化,促进了骨缺损的愈合。 2.6.3 骨组织血管化 众所周知,移植骨缺乏血管被认为是骨组织工程方法应用于临床的主要挑战之一。同种异体移植的血管形成和新骨的形成对于同种异体移植物的存活和整合至关重要。通过促进植入后的快速血管形成以及鼓励内源宿主干细胞和祖细胞的募集,人们对增强用于骨骼重建的同种异体移植物的整合和功效的技术开发产生了极大的兴趣。通过实验表明FTY720(一种鞘氨醇-磷酸酯受体的选择性激动剂)可以增加同种异体移植组织部分内成熟的微血管网络生长,植入后仅6周,它就促进了明显的新骨形成,其压缩模量和极限抗拉强度在统计学上显著提高,其局部免疫反应和异物反应的调节也可能是FTY720促进同种异体植入的机制的一部分。这些结果支持这样的想法,即用FTY720之类的药理靶向治疗是促进新血管形成和增强骨愈合的令人兴奋的新方法。有研究表明,FTY720可以持续地从骨膜下和颅骨缺损植入物中的水凝胶涂层中释放出来,植入同种异体移植物在颅骨缺损植入8周后,可增加骨再生速率,移植物整合并在空隙中定向骨生长,从而提高了局部释放的速度,促进了骨的血管以及新骨的形成[53]。 成骨生长因子和血管生成生长因子是骨修复过程中的关键因子。将血管内皮生长因子和骨发生蛋白2植入工程组织构建物中,是促进成骨和血管化过程的有效途径。因此,利用其修复潜力的关键是设计一种多功能系统,以调节血管内皮生长因子和骨发生蛋白2的释放时间和持续时间,以模拟自然骨愈合的时间和持续时间组织再生中的细胞疗法引起了极大的热情。然而,许多试验的结果并不令人满意,这是由于缺乏适当的载体来控制细胞功能和生长因子的传递。而DNA水凝胶具有血管内皮生长因子和骨发生蛋白的高包封率和可控的时空释放的特性。DNA水凝胶不仅在体外表现出优越的生物活性,还通过可注射的水凝胶基质移植骨髓间充质干细胞微载体在体内诱导血管形成和异位骨形成[54]。有研究在大鼠颅骨缺损模型中评估了载药水凝胶的体内成骨潜能,发现DNA基纳米复合水凝胶可以作为骨再生的注射材料和治疗药物的缓释载体[48]。配制的具有机械弹性的DNA基纳米复合水凝胶作为一类可注射材料可以广泛应用于各种生物医学应用。"

| [1] VARAPRASAD K, RAGHAVENDRA GM, JAYARAMUDU T, et al. A mini review on hydrogels classification and recent developments in miscellaneous applications. Mater Sci Eng C Mater Biol Appl. 2017;79:958-971. [2] Tu Y, Chen N, Li C, et al. Advances in injectable self-healing biomedical hydrogels. Acta Biomater. 2019;90:1-20. [3] CHEN J, ZHU Y, LIU H, et al. Tailoring DNA self-assembly to build hydrogels. Top Curr Chem (Cham). 2020;378(2):32. [4] LIU Q, GE Z, MAO X, et al. Valency-controlled framework nucleic acid signal amplifiers. Angew Chem Int Ed Engl. 2018;57(24):7131-7135. [5] KLÜTER T, HASSAN R, RASCH A, et al. Ex vivoan bone defect model to evaluate bone substitutes and associated bone regeneration processes. Tissue Eng Part C Methods. 2020;26(1):56-65. [6] CELIKKIN N, MASTROGIACOMO S, JAROSZEWICZ J, et al. Gelatin methacrylate scaffold for bone tissue engineering:The influence of polymer concentration. J Biomed Mater Res A. 2018;106(1):201-209. [7] PEDERSEN SL, HUYNH TH, POSCHKO P, et al. Remotely Triggered Liquefaction of Hydrogel Materials. ACS Nano. 2020;14(7):9145-9155. [8] PAL P, NGUYEN Q, BENTON A, et al. Drug-loaded elastin-like polypeptide-collagen hydrogels with high modulus for bone tissue engineering. Macromol Biosci. 2019;19(9):e1900142. [9] PINHEIRO AV, HAN D, SHIH WM, et al. Challenges and opportunities for structural DNA nanotechnology. Nat Nanotechnol. 2011;6(12):763-772. [10] ROH YH, RUIZ RC, PENG S, et al. Engineering DNA-based functional materials. Chem Soc Rev. 2011;40(12):5730-5744. [11] YANG D, HARTMAN MR, DERRIEN TL, et al. DNA materials:bridging nanotechnology and biotechnology. Acc Chem Res. 2014;47(6):1902-1911. [12] WANG D, HU Y, LIU P, et al. Bioresponsive DNA hydrogels:beyond the conventional stimuli responsiveness. Acc Chem Res. 2017;50(4):733-739. [13] 马翾,张洋子,许文涛.功能核酸DNA水凝胶的制备与组装[J].生物技术进展,2019,9(6):554-562. [14] UM SH, LEE JB, PARK N, et al. Enzyme-catalysed assembly of DNA hydrogel. Nat Mater. 2006;5(10):797-801. [15] NAGAHARA TM. Hydrogel formation via hybridization of oligonucleotides derivatized in water-soluble vinyl polymers. Elsevier Science. 1996;4(2):111-127. [16] LYU D, CHEN S, GUO W. Liposome crosslinked polyacrylamide/DNA hydrogel:a smart controlled-release system for small molecular payloads. Small. 2018; 14(15):e1704039. [17] FUJITA S, HARA S, HOSONO A, et al. Hyaluronic Acid Hydrogel Crosslinked with Complementary DNAs. Advances in Polymer Technology. 2020;2020:1-7. [18] KANG H, LIU H, ZHANG X, et al. Photoresponsive DNA-cross-linked hydrogels for controllable release and cancer therapy. Langmuir. 2011;27(1):399-408. [19] BUSH J, HU CH, VENEZIANO R. Mechanical properties of DNA hydrogels:towards highly programmable biomaterials. Appl Sci. 2021;11(4):1885. [20] CAI W, XIE S, ZHANG J, et al. An electrochemical impedance biosensor for Hg(2+) detection based on DNA hydrogel by coupling with DNAzyme-assisted target recycling and hybridization chain reaction. Biosens Bioelectron. 2017;98:466-472. [21] YANG D, PENG S, HARTMAN MR, et al. Enhanced transcription and translation in clay hydrogel and implications for early life evolution. Sci Rep. 2013;3:3165. [22] HUANG Y, XU W, LIU G, et al. A pure DNA hydrogel with stable catalytic ability produced by one-step rolling circle amplification. Chem Commun (Camb). 2017; 53(21):3038-3041. [23] KAHN JS, Y HU, I WILLNER. Stimuli-responsive DNA-based hydrogels:from basic principles to applications. Acc Chem Res. 2017;50(4):680-690. [24] NOLL T, WENDERHOLD-REEB S, SCHONHERR H, et al. Pristine DNA Hydrogels from Biotechnologically Derived Plasmid DNA. Angew Chem Int Ed Engl. 2017; 56(39):12004-12008. [25] DENG S, YAN J, WANG F, et al. In situ terminus-regulated DNA hydrogelation for ultrasensitive on-chip microRNA assay. Biosens Bioelectron. 2019;137:263-270. [26] NAKASONE Y, OOI H, KAMIYA Y, et al. Dynamics of Inter-DNA Chain Interaction of Photoresponsive DNA. J Am Chem Soc. 2016;138(29):9001-9004. [27] SHIMOMURA S, NISHIMURA T, OGURA Y, et al. Photothermal fabrication of microscale patterned DNA hydrogels. R Soc Open Sci. 2018;5(2):171779. [28] MO F, JIANG K, ZHAO D, et al. DNA hydrogel-based gene editing and drug delivery systems. Adv Drug Deliv Rev. 2021;168:79-98. [29] WANG Y, YAN M, XU L, et al. Aptamer-functionalized DNA microgels: a strategy towards selective anticancer therapeutic systems. J Mater Chem B. 2016;4(32): 5446-5454. [30] ZHANG J, GUO Y, PAN G, et al. Injectable Drug-Conjugated DNA Hydrogel for Local Chemotherapy to Prevent Tumor Recurrence. ACS Appl Mater Interfaces. 2020;12(19):21441-21449. [31] SONG J, IM K, HWANG S, et al. DNA hydrogel delivery vehicle for light-triggered and synergistic cancer therapy. Nanoscale. 2015;7(21):9433-9437. [32] BASU S, PACELLI S, PAUL A. Self-healing DNA-based injectable hydrogels with reversible covalent linkages for controlled drug delivery. Acta Biomater. 2020; 105:159-169. [33] LIAO WC, LILIENTHAL S, KAHN JS, et al. pH- and ligand-induced release of loads from DNA-acrylamide hydrogel microcapsules. Chem Sci. 2017;8(5):3362-3373. [34] XIAO M, LAI W, WANG F, et al. Programming drug delivery kinetics for active burst release with DNA toehold switches. J Am Chem Soc. 2019;141(51):20354-20364. [35] OBUOBI S, TAY HK, TRAM NDT, et al. Facile and efficient encapsulation of antimicrobial peptides via crosslinked DNA nanostructures and their application in wound therapy. J Control Release. 2019;313:120-130. [36] KIM T, PARK S, LEE M, et al. DNA hydrogel microspheres and their potential applications for protein delivery and live cell monitoring. Biomicrofluidics. 2016; 10(3):034112. [37] SONG P, YE D, ZUO X, et al. DNA hydrogel with aptamer-toehold-based recognition, cloaking, and decloaking of circulating tumor cells for live cell analysis. Nano Lett. 2017;17(9):5193-5198. [38] UMEKI Y, SAITO M, KUSAMORI K, et al. Combined encapsulation of a tumor antigen and immune cells using a self-assembling immunostimulatory DNA hydrogel to enhance antigen-specific tumor immunity. J Control Release. 2018; 288:189-198. [39] NISHIKAWA M, OGAWA K, UMEKI Y, et al. Injectable, self-gelling, biodegradable, and immunomodulatory DNA hydrogel for antigen delivery. J Control Release. 2014;180:25-32. [40] LEE J, LE QV, YANG G, et al. Cas9-edited immune checkpoint blockade PD-1 DNA polyaptamer hydrogel for cancer immunotherapy. Biomaterials. 2019;218:119359. [41] KUSCU L, SEZER AD. Future prospects for gene delivery systems. Expert Opin Drug Deliv. 2017;14(10):1205-1215. [42] SARDONE V, ZHOU H, MUNTONI F, et al. Antisense oligonucleotide-based therapy for neuromuscular disease. Molecules. 2017;22(4):563. [43] ROH YH, LEE JB, SHOPSOWITZ KE, et al. Layer-by-layer assembled antisense DNA microsponge particles for efficient delivery of cancer therapeutics. ACS Nano. 2014;8(10):9767-9780. [44] LI C, FAULKNER-JONES A, DUN AR, et al. Rapid formation of a supramolecular polypeptide-DNA hydrogel for in situ three-dimensional multilayer bioprinting. Angewandte Chemie (International ed in English). 2015;54(13):3957-3961. [45] HOFFMAN MD, XIE C, ZHANG X, et al. The effect of mesenchymal stem cells delivered via hydrogel-based tissue engineered periosteum on bone allograft healing. Biomaterials. 2013;34(35):8887-8898. [46] GAČANIN J, KOVTUN A, FISCHER S, et al. Spatiotemporally Controlled Release of Rho-Inhibiting C3 Toxin from a Protein-DNA Hybrid Hydrogel for Targeted Inhibition of Osteoclast Formation and Activity. Adv Healthc Mater. 2017. doi:10.1002/adhm.201700392. [47] NUTTELMAN CR, TRIPODI MC, ANSETH KS. Dexamethasone-functionalized gels induce osteogenic differentiation of encapsulated hMSCs. J Biomed Mater Res A. 2006;76(1):83-195. [48] BASU S, PACELLI S, FENG Y, et al. Harnessing the noncovalent interactions of DNA backbone with 2D silicate nanodisks to fabricate injectable therapeutic hydrogels. ACS Nano. 2018;12(10):9866-9880. [49] LIU Y, ZHU Z, PEI X, et al. ZIF-8-modified multifunctional bone-adhesive hydrogels promoting angiogenesis and osteogenesis for bone regeneration. ACS Appl Mater Interfaces. 2020;12(33):36978-36995. [50] DADSETAN M, HEFFERAN TE, SZATKOWSKI JP, et al. Effect of hydrogel porosity on marrow stromal cell phenotypic expression. Biomaterials. 2008;29(14):2193-2202. [51] CELIKKIN N, MASTROGIACOMO S, JAROSZEWICZ J, et al. Gelatin methacrylate scaffold for bone tissue engineering: the influence of polymer concentration. J Biomed Mater Res A. 2018;106(1):201-209. [52] BENOIT DS, NUTTELMAN CR, COLLINS SD, et al. Synthesis and characterization of a fluvastatin-releasing hydrogel delivery system to modulate hMSC differentiation and function for bone regeneration. Biomaterials. 2006; 27(36):6102-6110. [53] PETRIE ARONIN CE, SHIN SJ, NADEN KB, et al. The enhancement of bone allograft incorporation by the local delivery of the sphingosine 1-phosphate receptor targeted drug FTY720. Biomaterials. 2010;31(25):6417-6424. [54] DASHTIMOGHADAM E, FAHIMIPOUR F, TONGAS N, et al. Microfluidic fabrication of microcarriers with sequential delivery of VEGF and BMP-2 for bone regeneration. Sci Rep. 2020;10(1):11764. |
| [1] | Xue Yadong, Zhou Xinshe, Pei Lijia, Meng Fanyu, Li Jian, Wang Jinzi . Reconstruction of Paprosky III type acetabular defect by autogenous iliac bone block combined with titanium plate: providing a strong initial fixation for the prosthesis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1424-1428. |
| [2] | Yao Xiaoling, Peng Jiancheng, Xu Yuerong, Yang Zhidong, Zhang Shuncong. Variable-angle zero-notch anterior interbody fusion system in the treatment of cervical spondylotic myelopathy: 30-month follow-up [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1377-1382. |
| [3] | Jiang Huanchang, Zhang Zhaofei, Liang De, Jiang Xiaobing, Yang Xiaodong, Liu Zhixiang. Comparison of advantages between unilateral multidirectional curved and straight vertebroplasty in the treatment of thoracolumbar osteoporotic vertebral compression fracture [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1407-1411. |
| [4] | Li Wei, Zhu Hanmin, Wang Xin, Gao Xue, Cui Jing, Liu Yuxin, Huang Shuming. Effect of Zuogui Wan on bone morphogenetic protein 2 signaling pathway in ovariectomized osteoporosis mice [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1173-1179. |
| [5] | Wang Jing, Xiong Shan, Cao Jin, Feng Linwei, Wang Xin. Role and mechanism of interleukin-3 in bone metabolism [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1260-1265. |
| [6] | Xiao Hao, Liu Jing, Zhou Jun. Research progress of pulsed electromagnetic field in the treatment of postmenopausal osteoporosis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1266-1271. |
| [7] | Wu Bingshuang, Wang Zhi, Tang Yi, Tang Xiaoyu, Li Qi. Anterior cruciate ligament reconstruction: from enthesis to tendon-to-bone healing [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1293-1298. |
| [8] | Tian Chuan, Zhu Xiangqing, Yang Zailing, Yan Donghai, Li Ye, Wang Yanying, Yang Yukun, He Jie, Lü Guanke, Cai Xuemin, Shu Liping, He Zhixu, Pan Xinghua. Bone marrow mesenchymal stem cells regulate ovarian aging in macaques [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 985-991. |
| [9] | Hu Wei, Xie Xingqi, Tu Guanjun. Exosomes derived from bone marrow mesenchymal stem cells improve the integrity of the blood-spinal cord barrier after spinal cord injury [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 992-998. |
| [10] | Gao Yujin, Peng Shuanglin, Ma Zhichao, Lu Shi, Cao Huayue, Wang Lang, Xiao Jingang. Osteogenic ability of adipose stem cells in diabetic osteoporosis mice [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 999-1004. |
| [11] | Wu Weiyue, Guo Xiaodong, Bao Chongyun. Application of engineered exosomes in bone repair and regeneration [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1102-1106. |
| [12] | Zhou Hongqin, Wu Dandan, Yang Kun, Liu Qi. Exosomes that deliver specific miRNAs can regulate osteogenesis and promote angiogenesis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1107-1112. |
| [13] | Hou Jingying, Guo Tianzhu, Yu Menglei, Long Huibao, Wu Hao. Hypoxia preconditioning targets and downregulates miR-195 and promotes bone marrow mesenchymal stem cell survival and pro-angiogenic potential by activating MALAT1 [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1005-1011. |
| [14] | Liang Xuezhen, Yang Xi, Li Jiacheng, Luo Di, Xu Bo, Li Gang. Bushen Huoxue capsule regulates osteogenic and adipogenic differentiation of rat bone marrow mesenchymal stem cells via Hedgehog signaling pathway [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1020-1026. |
| [15] | Cui Xing, Sun Xiaoqi, Zheng Wei, Ma Dexin. Huangqin Decoction regulates autophagy to intervene with intestinal acute graft-versus-host disease in mice [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1057-1062. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||