Chinese Journal of Tissue Engineering Research ›› 2023, Vol. 27 ›› Issue (1): 105-113.doi: 10.12307/2022.720
Previous Articles Next Articles
Application of concentrated growth factor and epidermal growth factor in the field of oral and maxillofacial soft and hard tissue injury repair
Liu Yunling1, 2, He Ruya1, 2, Nie Minhai1, 2, Li Tengyan1, 2, Liu Xuqian1, 2
- 1Department of Periodontics & Oral Mucosal Diseases, Affiliated Stomatology Hospital of Southwest Medical University, Luzhou 646000, Sichuan Province, China; 2Luzhou Key Laboratory of Oral & Maxillofacial Reconstruction and Regeneration, Southwest Medical University, Luzhou 646000, Sichuan Province, China
-
Received:2021-11-15Accepted:2021-12-20Online:2023-01-08Published:2022-06-06 -
Contact:Liu Xuqian, PhD, Associate professor, Department of Periodontics & Oral Mucosal Diseases, Affiliated Stomatology Hospital of Southwest Medical University, Luzhou 646000, Sichuan Province, China; Luzhou Key Laboratory of Oral & Maxillofacial Reconstruction and Regeneration, Southwest Medical University, Luzhou 646000, Sichuan Province, China -
About author:Liu Yunling, Master candidate, Department of Periodontics & Oral Mucosal Diseases, Affiliated Stomatology Hospital of Southwest Medical University, Luzhou 646000, Sichuan Province, China; Luzhou Key Laboratory of Oral & Maxillofacial Reconstruction and Regeneration, Southwest Medical University, Luzhou 646000, Sichuan Province, China -
Supported by:Science and Technology Planning Project of Sichuan Provincial Department of Science and Technology, No. 2020YJ0387 (to LXQ); Key Project of Science and Technology Strategic Cooperation between the People's Government of Luzhou of Sichuan Province and Southwest Medical University, No. 2019LZXNYDZ10 (to LXQ); Key Basic Application Project of Southwest Medical University, No. 2021ZKZD010 (to LXQ)
CLC Number:
Cite this article
Liu Yunling, He Ruya, Nie Minhai, Li Tengyan, Liu Xuqian. Application of concentrated growth factor and epidermal growth factor in the field of oral and maxillofacial soft and hard tissue injury repair[J]. Chinese Journal of Tissue Engineering Research, 2023, 27(1): 105-113.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
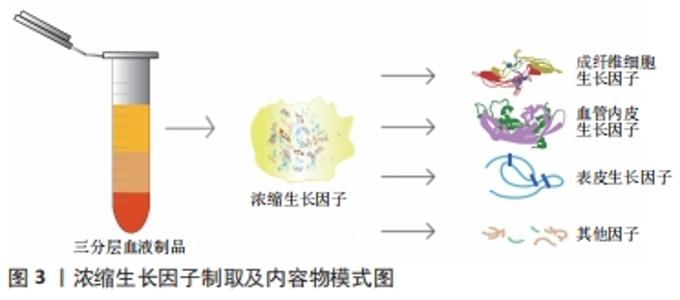
2.1 浓缩生长因子的组成及制取简述 浓缩生长因子是Sacco于2006年发现的第3代血小板制品,其中含有转化生长因子β1(transforming growth factor-β1,TGF-β1)及β2 (transforming growth factor-β2,TGF-β2)、表皮生长因子、血管内皮生长因子、血小板衍生生长因子(plateletderived growth factor,PDGF)、成纤维细胞生长因子(fibroblast growth factor,FGF)、胰岛素样生长因子(insulin-like growth factor,IGF)、基质金属蛋白酶(matrix metalloproteinase,MMP)等多种细胞生长因子。浓缩生长因子中还含有CD34+细胞,CD34抗原具有招募干细胞归巢至损伤部位的重要功能[1]。相较于前2代血小板制品富血小板血浆和富血小板纤维蛋白而言,浓缩生长因子通过差速离心获得,模拟天然凝血过程,形成更致密的纤维网络,对于血管内皮生长因子等生长因子的同期释放量更高,持续释放时间更长。各种生长因子之间协调作用,促进细胞增殖分化、基质改建、血管新生[2]。浓缩生长因子可制备成块状、膜状、颗粒状等多种形态以满足不同需求,具有制取方便、价格低廉等优点。且浓缩生长因子来自患者自体静脉血,不含外源性生物或化学添加剂,可避免免疫排斥及交叉感染等风险。广泛的研究证实浓缩生长因子在组织再生领域占据重要地位,是一种值得深入研究、应用的新型生物材料,见图3。"
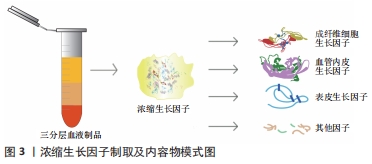
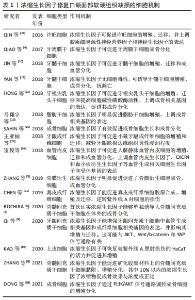
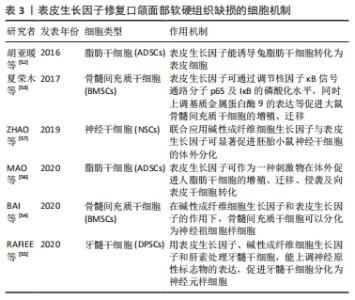
2.2 浓缩生长因子参与细胞水平修复口颌面部软硬组织缺损的机制 组织损伤的愈合由(出血性损伤包括止血过程)炎症反应期、增殖修复期、创面重塑期3个(或4个)相互重叠的过程组成。细胞通过生长因子的诱导进行增殖、迁移和分化等,从而促使愈合过程的发生发展,促进组织再生、修复[3]。组织细胞在正常生理状态下对生长因子的需求量小,当组织受损时,细胞表面暴露更多的生长因子受体以接纳更多的生长因子。浓缩生长因子可促进形成口颌面部软硬组织的多种细胞增殖分化,这是浓缩生长因子促进组织再生、修复的细胞基础。 2.2.1 牙周膜干细胞(periodontal ligament stem cells,PDLSCs) 牙周膜干细胞是存在于牙周膜中的一种具有多向分化潜能的种子细胞,其在牙周组织再生修复中具有重要作用。QIAO等[4]发现浓缩生长因子可促进牙周膜干细胞成骨分化,与rhPDGF-AB+rhTGF-β1培养体系相比,浓缩生长因子培养体系中细胞增殖和分化更强,说明浓缩生长因子中含更多种类促细胞增殖、生长和分化的生长因子。医师通过收集正畸减数拔牙或多生牙拔除等的离体牙牙周膜可提取牙周膜干细胞,患者接受度高。“自体牙周膜干细胞+自体浓缩生长因子提取物”或有机会应用于骨内阻生牙拔除后的颌骨缺损修复。 2.2.2 骨膜衍生细胞 车祸伤、恶性肿瘤根治术等常造成患者颌面部骨缺损,应用组织工程技术重建颌面部外形、恢复咀嚼及言语等功能成为研究热点。ZHANG等[5]研究发现浓缩生长因子明显促进骨膜衍生细胞的增殖行为及其碱性磷酸酶活性表达;上调骨膜衍生细胞中成骨相关因子——骨形态发生蛋白2、Ⅰ型胶原及骨钙蛋白等在蛋白和基因水平的表达。另外,浓缩生长因子促进骨膜衍生细胞中血管内皮生长因子和碱性成纤维细胞生长因子蛋白和基因水平的表达,提示浓缩生长因子促进了骨膜衍生细胞成血管分化。为改善患者生存质量,口颌面外科手术提倡“保存性”,尽量保留患者原有骨组织。在外伤骨折患者断端复位后在骨膜附近植入浓缩生长因子凝胶或可促进断端血供恢复及新骨形成。 2.2.3 骨髓间充质干细胞 传统的骨缺损治疗常需要植入骨或骨替代物,可能需要开辟第二术区,手术创伤大、术后反应重,而基于细胞的骨组织再生治疗已被广泛研究,其中“浓缩生长因子+骨髓间充质干细胞”模式更是被众研究者青睐。CHEN 等[6]发现骨髓间充质干细胞与浓缩生长因子共培养,可促进骨髓间充质干细胞的骨诱导活性,促进新骨形成,且浓缩生长因子刺激血管新生的效果优于胶原蛋白。ROCHIRA等[7]有同样发现,并首次证实浓缩生长因子单独应用能够诱导人骨髓间充质干细胞在体外的成骨分化。ZHANG等[8]的细胞实验和兔动物实验证实浓缩生长因子促进矿化胶原材料上的骨髓间充质干细胞黏附、增殖分化,其中10%以内的浓缩生长因子浓缩物促成骨效果与浓度呈正比。 2.2.4 牙龈间充质干细胞 牙龈间充质干细胞是存在于牙龈固有层的干细胞,具有抗炎、调节免疫的作用,在机体需要的情况下可以功能向分化为牙周膜细胞和成骨细胞等细胞。QI等[9]用浓缩生长因子处理牙龈间充质干细胞,结果显示浓缩生长因子能增强牙龈间充质干细胞的增殖与迁移;证实了浓缩生长因子可增强牙龈间充质干细胞中血管生成相关基因和成纤维细胞相关基因(纤维连接蛋白、Ⅰ型胶原、血管生成素1和血管内皮生长因子)的表达。而浓缩生长因子的刺激作用可能归因于AKT、Wnt/b-catenin和YAP信号通路的激活,与体外实验一起均证实浓缩生长因子能显著诱导YAP向细胞核的转运,增强增殖标志物Ki67和内皮细胞标志物CD31的表达。这些可能有助于创造促进细胞增殖、胶原沉积的促血管生成生化微环境。慢性牙周炎是口腔常见病,牙周手术中应用自体浓缩生长因子膜或能促进牙龈间充质干细胞增殖分化为成纤维细胞等,胶原合成增加,创口加速愈合。 2.2.5 牙髓干细胞 牙髓干细胞在牙髓的形成、损伤过程中发挥重要作用,可根据牙髓状况功能向分化为多种功能细胞,维持牙髓完整和牙体健康。JIN等[10]发现浓缩生长因子可促进牙髓干细胞的增殖、迁移和成血管分化。YAN 等[11]通过体外细胞实验和比格犬动物模型体内实验发现浓缩生长因子与牙髓干细胞有较好的相容性,无细胞毒性,可诱导牙髓干细胞增殖、成骨分化、抗凋亡。“活髓切断术+浓缩生长因子”不失为保存年轻恒牙牙髓活力、促进牙根继续发育的可能方法。 2.2.6 牙根尖乳头干细胞 牙根尖乳头干细胞位于根尖未发育完全的乳头组织中,具有多向分化潜能,是牙髓组织工程的细胞来源热点,其在牙髓的发育过程中起到种子细胞的作用。浓缩生长因子具有促进细胞增殖、诱导干细胞功能向分化的生物学作用。近年来,“浓缩生长因子+牙髓再生”被广泛研究。HONG等[12]设计相关实验证实了浓缩生长因子可促进牙根尖乳头干细胞的增殖、迁移和提高细胞碱性磷酸酶活性,上调成骨相关基因(碱性磷酸酶、骨涎蛋白、牙本质基质蛋白1和牙本质涎磷蛋白)的表达。浓缩生长因子有助于牙根尖乳头干细胞的成骨分化,未来研究者们还需探究“浓缩生长因子+牙根尖乳头干细胞”在牙髓再生、根尖周组织重建等领域的可能性。 2.2.7 脂肪干细胞 脂肪干细胞是从脂肪组织中分离出来的一种干细胞,具有多向分化的潜能,在组织修复中可发挥重要作用。浓缩生长因子在体外培养时可促进犬、大鼠、人源性脂肪干细胞增殖及成骨分化[2]。马翔宇等[13]研究浓缩生长因子对比格犬脂肪干细胞体外增殖和成骨分化的影响时发现浓缩生长因子明显促进脂肪干细胞增殖,同时经成骨诱导后浓缩生长因子促进碱性磷酸酶活性表达和 Ⅰ型胶原、Runt相关转录因子2等成骨相关基因的表达。脂肪干细胞易于提取,并可在浓缩生长因子诱导下增殖、成骨分化等特性为浓缩生长因子与脂肪干细胞联合应用于颌骨缺损的修复奠定了理论基础。HU等[14]用SD大鼠颅骨缺损模型证实了脂肪干细胞加浓缩生长因子联用修复口颌面部骨缺损的可能性。 2.2.8 成骨细胞 在对浓缩生长因子的相关研究中,成骨细胞是一个热门的研究靶点细胞。众多学者围绕骨缺损、骨再生对浓缩生长因子与成骨的相关性方面进行大量研究,尤其是在种植领域。SAHIN等[15]研究发现浓缩生长因子明显促进细胞增殖和碱性磷酸酶活性表达,提高骨钙蛋白表达水平,有效促进成骨细胞生长和成骨分化,提高种植的成功率。李欣等[16]还发现浓缩生长因子促进成骨细胞株中核心结合蛋白因子2和成骨细胞特异性转录因子基因的表达,促进成骨细胞株与钛片的生物相容性,这在种植应用中是很重要的发现。BORSANI等[17]通过实验发现浓缩生长因子能显著促进成骨细胞的增殖和分化,且与白藜芦醇共处理对保护成骨细胞免受双膦酸盐损害有积极作用。DONG等[18]发现浓缩生长因子浓缩物通过PI3K/AKT信号通路[phosphoinositide 3-kinase (PI3K)/serine-threonine kinase (AKT) pathway]调控成骨细胞的增殖分化。 2.2.9 角质形成细胞 角质形成细胞是表皮(或上皮)层中主要的细胞成分,当皮肤或黏膜损伤时,角质形成细胞可在生长因子等诱导下增殖并迁移到受损部位,填平创面,达到修复损伤的作用。用浓缩生长因子膜体外培养人角质形成细胞株,可促进其迁移、增殖,并重新形成上皮样结构[19]。表皮层(上皮层)作为皮肤(黏膜)直接暴露于外界的部分,尽快恢复其完整性能减少感染发生率。 2.2.10 成纤维细胞 真皮成纤维细胞:紫外线A是造成皮肤老化、损伤的重要原因。真皮成纤维细胞是皮肤真皮层主要的细胞之一,也是紫外线A损伤皮肤的主要作用靶点[19]。研究发现浓缩生长因子与真皮成纤维细胞具有良好的生物相容性,能促进其胶原合成、增殖及迁移,逆转紫外线A对真皮成纤维细胞的损伤,在体积分数5%浓缩生长因子中真皮成纤维细胞迁移率高于正常对照组细胞[20-21]。浓缩生长因子可抑制紫外线A对真皮成纤维细胞的老化、损伤效应,减缓皮肤因紫外线A造成的衰老进程;可提高光损伤细胞中超氧化物歧化酶活性,显著降低活性氧的含量。美容整形医师已将浓缩生长因子广泛运用于减少瘢痕、改善色素沉着、抗皱等。对口颌面部皮肤缺损的处理同样应考虑到美观因素,除牙种植术外,口颌面部存在外伤或肿瘤切除术等导致的累及皮肤全层的伤口时,可皮下植入浓缩生长因子膜后缝合创口,促进愈合。 牙龈成纤维细胞:是牙龈固有层的主要组成细胞,有收缩功能,在牙龈等黏膜组织损伤修复中发挥收缩、重塑创面的作用,研究发现浓缩生长因子可促进牙龈成纤维细胞的增殖、迁移等生物学行为。王亚楠等[22]通过动物实验发现浓缩生长因子膜可促进牙龈缺损的愈合,减轻缺损边缘组织炎性浸润程度,提高缺损愈合质量;组织学观察发现浓缩生长因子治疗后的新生组织以正角化为主,而明胶海绵覆盖治疗组愈合组织以不全角化为主;体外细胞实验发现浓缩生长因子促进小鼠牙龈成纤维细胞的增殖和迁移。 2.2.11 许旺细胞 许旺细胞是周围神经细胞中比较具有代表性的细胞,其在周围神经再生过程中发挥关键性作用。近年来有学者开始研究浓缩生长因子对许旺细胞生物学行为的影响,进而探讨浓缩生长因子对周围神经受损治疗的效果。QIN等[23]发现浓缩生长因子可促进许旺细胞的增殖,并上调许旺细胞中胶质细胞源性神经营养因子和神经生长因子的表达。另外,浓缩生长因子可促进许旺细胞的迁移,而整合素β1部分参与该过程。但浓缩生长因子促进许旺细胞增殖、迁移的最佳浓度仍存疑。 2.2.12 血管内皮细胞 血管内皮细胞的增殖、迁移、分化是血管生成过程中的必要生物学行为,浓缩生长因子、血管内皮细胞与血管再生的关系也被广泛研究。宦俊等[24]通过实验研究发现浓缩生长因子提取液可促进人脐静脉血管内皮细胞的增殖、迁移和成血管分化,同时浓缩生长因子上调人脐静脉血管内皮细胞中血管生成相关细胞生长因子和受体(血管内皮生长因子、趋化因子受体4、血小板衍生生长因子)基因的表达。 浓缩生长因子含有多种生长因子和CD34+细胞,可促进多种组织细胞生长、增殖、迁移和分化、抑制凋亡等生物学行为,在口颌面部软硬组织损伤修复中具有重要作用,是一种具有极大发展潜力的新型生物材料。干细胞、支架和生长因子是组织工程的3大要素。干细胞获取的难易程度、患者的可接受度、生物相容性等决定了组织工程的发展方向及临床应用前景。浓缩生长因子为三维网状结构,可充当组织再生的支架,同时富含多种生长因子,故受到组织工程研究者的青睐。学者们探究了浓缩生长因子对多种干细胞的生物学行为影响,被研究的干细胞主要来源于牙、牙周组织、骨组织、脂肪等。多数研究提示,浓缩生长因子可上调干细胞成骨相关基因的表达及成骨分化。其中,从脂肪组织获取脂肪干细胞具有创伤小、来源丰富及患者接受度高等优点。ZHANG等[8]的研究提到浓缩生长因子对骨髓间充质干细胞的促成骨效应呈剂量依赖性,但是否浓缩生长因子对其他干细胞的积极影响也与剂量相关,还需要大量的基础实验数据。除干细胞外,学者对成骨细胞、角质形成细胞、成纤维细胞、许旺细胞及血管内皮细胞的研究提示,浓缩生长因子也能诱导口颌面部损伤修复所需细胞的迁移、黏附、增殖、分化,促进血管生成和软硬组织形成,具体机制见表1。 "

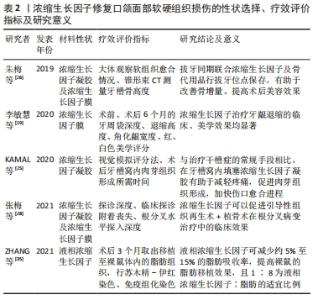
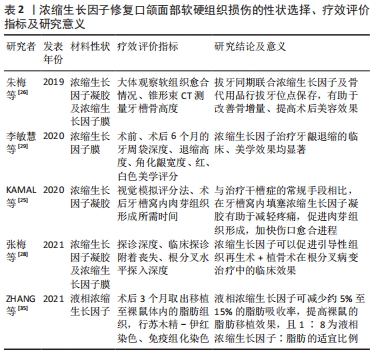
2.3 浓缩生长因子作用于口颌面部软硬组织损伤修复及再生 2.3.1 浓缩生长因子作用于口颌面部软组织损伤修复及再生 干槽症是下颌第3磨牙拔除后的常见并发症,传统治疗手段为彻底清创后以碘仿纱条填塞拔牙创口。清创后在拔牙窝中填入浓缩生长因子,治疗效果优于传统治疗手段,医师可观察到肉芽组织形成加快,患者也反馈疼痛有缓解[25]。对于锥形束CT提示术后创伤较大的下颌低位阻生牙拔除,临床医生可考虑预防性使用浓缩生长因子,减少术后患者发生干槽症的风险。拔牙同期采用浓缩生长因子联合骨代用品填充牙槽窝,可降低远期骨增量手术比例,有效保存牙槽嵴顶宽度,提高术后附着龈丰满度[26]。 赵军伟等[27]最先将自体浓缩生长因子与脱矿冻干骨联合应用,治疗骨下袋,这提示了临床即刻制取自体浓缩生长因子而后于手术中应用的可行性,且锥形束CT提示浓缩生长因子组术后牙周组织再生优于对照组。张梅等[28]将浓缩生长因子和BioGide胶原膜联合应用治疗牙周根分叉病变,BioGide胶原膜可延长浓缩生长因子膜的屏障时间,为种子细胞提供更长的爬行时间,改善牙周病变的治疗效果。在膜龈手术加用浓缩生长因子膜能改善牙龈退缩,术后评价为角化龈宽度增加、美学评分佳[29]。于文凤等[30]在冠向复位瓣修复牙龈退缩时联用腭侧自体结缔组织或修剪为适合填塞创口的载有浓缩生长因子凝胶的胶原海绵及自体浓缩生长因子膜,术后二者效果类似。填塞胶原海绵及浓缩生长因子膜能减少患者术后感染概率。尽管KORKMAZ等[31]的临床试验认为自体结缔组织移植物在辅助治疗牙龈退缩方面效果优于浓缩生长因子,自体结缔组织移植仍是最适合治疗牙龈退缩后牙根暴露问题的方式。但相较于自体结缔组织移植,浓缩生长因子具有创伤小、不需要开辟第二术区、患者接受度更高等优点[32]。抽取自体静脉血的感染风险远小于开辟第二术区取结缔组织的风险,因此应用浓缩生长因子治疗牙龈退缩有广阔发展前景。 任静等[33]对上颌前牙美学区种植术后6,12个月红白美学效果进行评分,应用浓缩生长因子组美学效果更好,软组织轮廓衔接更为自然。 国外有研究发现浓缩生长因子能提高脂肪移植的存活率和质量,向裸鼠体内植入脂肪组织时混入液相的浓缩生长因子可减少5%-15%的吸收率,目前认为,为提高脂肪组织的存活率,液相浓缩生长因子与自体脂肪较恰当的比例为1∶8[34-35]。这证明浓缩生长因子联合脂肪干细胞修复口颌面部软硬组织缺损是未来的研究热点,但二者联合应用的体积比、具体起效时间、可能的并发症等还需进一步探究。 口颌面部外伤、下颌阻生智齿拔除、腮腺恶性肿瘤根治术等易造成三叉神经和面神经等的损伤,付丽等[36]观察到浓缩生长因子有助于促进神经损伤的恢复。多数研究提示浓缩生长因子可促进真皮中的胶原和弹性纤维增加,减少面部皱纹,延缓皮肤衰老,促进创面愈合,促进白癜风外科治疗患者手术区域的色素恢复,萎缩性瘢痕修复,增强皮肤弹性[37]。能否在唇腭裂修复手术中皮瓣修复时辅助应用浓缩生长因子凝胶以减少出血,促进愈合,减少瘢痕形成,改善远期皮肤色泽,还需大量实验验证。 2.3.2 浓缩生长因子作用于口颌面部骨组织损伤修复及再生 依靠自体骨移植,骨粉填充,上颌窦提升术等技术的成熟,牙槽骨状况欠佳、牙周炎症的患者也得以行种植手术,改善口腔功能。此类种植手术,常辅助应用骨粉、自体浓缩生长因子、胶原膜等生物材料,以改善手术效果,改善术后植体的初期稳定性,保证植骨量的可估性,减轻患者疼痛症状、提高手术成功率。许军旗等[38]在患者牙周炎症期行即刻种植,用浓缩生长因子联合骨粉及引导骨再生技术有效抑制炎症反应,减轻患者疼痛程度。周海兰等[39]用3D钛网结合浓缩生长因子膜及BioGide双层膜行种植术,骨增量效果好。 KERANMU等[40]将浓缩生长因子应用于自体第三磨牙移植至第一、二磨牙,浓缩生长因子膜被放置在受区牙槽窝底部并包裹移植牙牙根,此举可改善植入牙的初期稳定性,缓解患者术后症状,提高远期自体牙移植成功率。在种植术中,浓缩生长因子膜紧贴创面深部放置,反折后可起到固定骨粉的作用;碎屑状浓缩生长因子膜可与骨粉混匀至黏稠混合物状态,填充骨缺损部分。但浓缩生长因子与骨粉混合的最适体积比还需进一步探究。颌骨囊肿切除术、恶性肿瘤根治术等常造成口颌面部软硬组织缺损。李勇等[41]发现混合浓缩生长因子、骨粉填充颌骨囊肿术后中、大型骨缺损区,可有效促进骨组织修复和软组织愈合。目前多是用影像学指标来评价浓缩生长因子对骨组织再生的作用,仍缺乏定量的生物力学评价指标,可通过动物实验填补该部分空白。有学者研究发现浓缩生长因子可改善药物相关性颌骨坏死患者的骨质疏松状况,但临床试验未显示统计学差异[42]。 近年来,多数病例报告或临床对照试验报道了浓缩生长因子在改善软硬组织再生、增加美学效果及促进伤口愈合、缓解患者疼痛症状等方面疗效显著[43-47]。学者们主要通过测量角化龈宽度变化、进行红、白色美学评分等评价浓缩生长因子对软组织损伤的修复效果,测量者的主观因素对软组织损伤修复测量结果有较大影响。应用佛罗里达探针系统或可改善对探诊深度、附着龈宽度等软组织评价指标的测量准确性。锥形束CT在口颌面部的广泛应用使得学者评价浓缩生长因子对骨组织损伤的修复效果相对客观。术前、术后1年的锥形束CT对比数据,结合探诊深度、临床探诊附着丧失、根分叉水平探入深度等数据的测定,可得出浓缩生长因子能改善口颌面部骨组织的损伤修复这一结论。同时,较多学者探索了通过脂肪组织移植填充口颌面部大面积缺损的可能性,而浓缩生长因子有望减少移植脂肪组织的吸收率,改善修复效果。浓缩生长因子修复口颌面部软硬组织损伤的研究见表2。 "
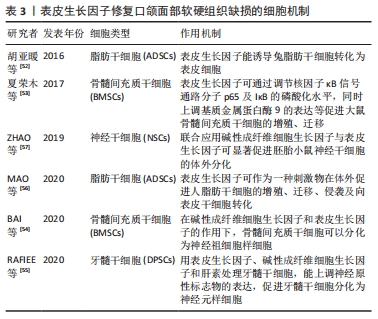
2.4 重组人表皮生长因子的来源及生物学特性 有学者在一项关于小鼠唾液腺内神经生长因子的研究中发现,在某种跨膜前体蛋白(相对分子质量为130 000)的裂解过程中可以产生一种具有促进表皮细胞增殖功能的物质,首次提出了表皮生长因子的概念。在进一步的研究中发现,表皮生长因子是一种相对分子质量为6 000,由53个氨基酸残基、3对稳定的二硫键构成的蛋白多肽链。而它的受体(表皮生长因子受体)是一种由胞内的激酶结构域及胞外结构域共同组成的糖蛋白,在机体的多种细胞(如上皮细胞、成纤维细胞、平滑肌细胞等)表面均有表达。表皮生长因子受体在大多数文献中用表皮生长因子表示,也可称其为HER1或ErbB1,和其他的ErbB受体(HER2/ErbB2/Neu、HER3/ErbB3以及HER4或ErbB4)一样,都属于表皮生长因子受体酪氨酸激酶家族[48]。 生理状况下,表皮生长因子与相关的表皮生长因子受体进行特异性识别后调控各种细胞的增殖分化,促进血管新生,刺激核酸及胶原蛋白等物质的合成,加速机体的新陈代谢及生长发育进程。在病理情况下,当机体对表皮生长因子受体及其下级信号通路调控失衡,或者出现表皮生长因子相关基因的过表达或突变,都将导致或加速局部组织器官的癌变。目前临床上,主要采用酪氨酸激酶抑制剂和抗表皮生长因子受体的单克隆抗体来设计肺癌、胃癌、乳腺癌和白血病等多种相关癌症的靶向治疗方案[49]。 研究表明,人体内可自行合成分泌表皮生长因子,在多种器官(颌下腺、肝脏、十二指肠等)和体液(诸如尿液、唾液、乳汁、血清和精液等)中均可检测到它不同程度的表达。人体内的表皮生长因子被发现与动物体内的表皮生长因子具有高达70%的同源性。在哺乳动物整个生长发育的过程中,表皮生长因子可以被不断地合成与分泌,但随着年龄的增加,自体可产生的表皮生长因子量会随之下降,可直接从生物体内被检测或提取出来的有活性的表皮生长因子量也越来越低。故目前临床上使用的表皮生长因子大多数是通过基因工程提取而来的各种类型的重组人表皮细胞生长因子[50]。 2.5 表皮生长因子参与细胞水平修复口颌面部软硬组织缺损的机制 目前的学术研究成果提示表皮生长因子在神经再生方面有很大发展空间。利用干细胞的多向分化潜能,诱导神经组织再生,为修复因退行性疾病或肿瘤切除而破坏的神经组织提供了可能。有学者分别报道了在表皮生长因子及碱性成纤维细胞生长因子的诱导下,牙周膜干细胞、骨髓间充质干细胞、牙髓干细胞、神经元干细胞等分化为神经元样细胞[51]。同时,胡亚暖等[52]的报道证实表皮生长因子可促进脂肪干细胞分化为表皮细胞,这为拓展表皮生长因子在口颌面部软组织缺损中的临床应用范围打下了基础。 2.5.1 骨髓间充质干细胞 夏荣木等[53]通过CCK-8法、克隆形成实验、Transwell小室等检测表皮生长因子对骨髓间充质干细胞增殖、迁移能力的影响,发现表皮生长因子可通过调节核因子κB信号通路分子p65及IκB的磷酸化水平,同时上调基质金属蛋白酶9的表达等促进大鼠骨髓间充质干细胞的增殖、迁移。BAI等[54]的体外实验证实在碱性成纤维细胞生长因子和表皮生长因子的作用下,骨髓间充质干细胞可以分化为神经祖细胞样细胞。学者们可将经碱性成纤维细胞生长因子和表皮生长因子处理的骨髓间充质干细胞应用于神经损伤的修复领域纳入研究范围。 2.5.2 牙髓干细胞 RAFIEE等[55]发现用表皮生长因子、碱性成纤维细胞生长因子和肝素处理牙髓干细胞,能上调神经原性标志物的表达,促进神经元样细胞的产生,促进牙髓干细胞分化为神经元样细胞。但表皮生长因子促进牙髓神经再生的分子机制还需进一步研究。 2.5.3 脂肪干细胞 脂肪干细胞具有良好的自我增殖和多谱系分化潜能,可以分化为脂肪细胞、成骨细胞、内皮细胞和表皮细胞等组织细胞。胡亚暖等[52]分别以不同浓度的表皮生长因子溶液诱导兔脂肪干细胞向表皮细胞分化,通过检测CK-19和整合素β的表达,认为表皮生长因子能诱导兔脂肪干细胞转化为表皮细胞,且10 ng/mL为最佳浓度。MAO等[56]在上调或下调人永生化角质形成细胞中表皮生长因子的表达后,通过将脂肪干细胞与修饰过的人永生化角质形成细胞共培养,探索细胞活力、迁移以及CK19和整合素β表达的变化。其研究得出与胡亚暖相似结论,肯定了表皮生长因子在应用脂肪干细胞治疗皮肤创伤修复中具有良好应用前景。 2.5.4 神经干细胞 神经损伤的修复需要神经元干细胞诱导神经元修复,促进神经轴突的生长以重建神经元网络。有学者从胚胎小鼠的前脑中分离出神经干细胞,并联合应用碱性成纤维细胞生长因子与表皮生长因子对神经干细胞进行体外分化[57],探究其促进神经损伤修复的分子机制,发现二者在促进神经元分化方面作用显著。 以上对表皮生长因子在细胞水平修复口颌面部软组织缺损研究提示,表皮生长因子的干预可促进骨髓间充质干细胞、脂肪干细胞等增殖、新生血管形成和基质分泌;表皮生长因子可诱导骨髓间充质干细胞、牙髓干细胞向神经元样细胞分化。口颌面部软硬组织缺损时,应用表皮生长因子或对上皮缺损、神经损伤的修复都有益。 表皮生长因子在调节干细胞生长、增殖和分化过程中发挥重要作用。其中,表皮生长因子对干细胞的促分化作用主要集中在分化为表皮细胞和神经元样细胞两方面。对兔脂肪干细胞和人脂肪干细胞的体外研究都提示表皮生长因子可促进脂肪干细胞向表皮细胞分化。表皮细胞的形成是恢复上皮完整性的前提,“表皮生长因子+脂肪干细胞”或有希望加速口颌面部软组织损伤修复进程,降低创面感染概率。表皮生长因子还可促进骨髓间充质干细胞、牙髓干细胞分化为神经元样细胞。其中,车祸、创伤等造成的口颌面部深在损伤常存在骨折、骨断端暴露及神经损伤等,局部应用表皮生长因子对术后神经功能的恢复可能有积极作用。另外,动物实验提示表皮生长因子可诱导骨髓间充质干细胞的增殖、迁移,即未来应用“表皮生长因子+骨髓间充质干细胞”有同时改善口颌面部骨组织和神经组织损伤修复效果的可能性。 文章汇总描述了表皮生长因子修复口颌面部软硬组织缺损的细胞机制[52-57],见表3。 "

2.6 表皮生长因子修复口颌面部软组织缺损的临床应用 口腔黏膜的完整性在抵御细菌入侵、防止机体感染方面具有重要生物学意义。复发性阿弗他溃疡是最常见的口腔溃疡,病情严重者愈后留有瘢痕。目前临床常对症应用止痛、消炎杀菌、促进组织愈合、补充维生素的药物。研究表明,在口腔黏膜溃疡的病理过程中,内源性表皮生长因子及其相关受体的表达量下降,上皮细胞的增殖活性会受到抑制,延长局部溃疡面的愈合时间。基于此,一些学者开展了利用外源性表皮生长因子相关制剂来进行针对性治疗口腔溃疡的研究。有学者通过回顾性研究发现,以有效浓度为30 μg/g的复方外用重组人表皮生长因子凝胶治疗溃疡、手术创伤、烧伤和瘢痕等多种皮损,均有较好的疗效[58]。郭磊等[59]学者针对复发性阿弗他溃疡的治疗,进行了重组人表皮生长因子溶液联合半导体激光的疗效研究,研究结果提示,二者联合使用的观察组较单纯使用重组人表皮生长因子外用溶液的对照组效果更佳,患者自觉疼痛消失变快、溃疡愈合所需时间缩短、短期内溃疡复发率更低。 VISWANATHAN等[60]的随机对照试验证实应用重组人表皮生长因子能促进人糖尿病足溃疡处胶原合成增加,愈合时间缩短。基于黏膜与皮肤的基本组织学结构层次较为相似,重组人表皮生长因子对糖尿病足溃疡愈合的促进作用一定程度上也提示了重组人表皮生长因子在口腔黏膜溃疡修复领域的远大前景。有研究认为,从犬脂肪组织中分离培养扩增得到间充质干细胞,并注射至狗口腔溃疡处,有助于加速溃疡愈合[61]。这可能是因为间充质干细胞可分化为内皮细胞和表皮细胞等,协同作用修复溃疡创面。重组人表皮生长因子作为单一生长因子制剂,其促进创面愈合的作用有限,通过运载体给药等形式将重组人表皮生长因子与其他药物结合使用,可拓宽药物起效途径。 "

| [1] RODELLA LF, FAVERO G, BONINSEGNA R, et al. Growth factors, CD34 positive cells, and fibrin network analysis in concentrated growth factors fraction. Microsc Res Tech. 2011;74(8):772-777. [2] HU Y, JIANG Y, WANG M, et al. Concentrated growth factor enhanced fat graft survival: a comparative study. Dermatol Surg. 2018;44(7):976-984. [3] BRISSETT AE, HOM DB. The effects of tissue sealants, platelet gels, and growth factors on wound healing. Curr Opin Otolaryngol Head Neck Surg. 2003;11(4):245-250. [4] QIAO J, AN N. Effect of concentrated growth factors on function and Wnt3a expression of human periodontal ligament cells in vitro. Platelets. 2017;28(3):281-286. [5] ZHANG L, AI H. Concentrated growth factor promotes proliferation, osteogenic differentiation, and angiogenic potential of rabbit periosteum-derived cells in vitro. J Orthop Surg Res. 2019;14(1):146. [6] CHEN X, WANG J, YU L, et al. Effect of concentrated growth factor (CGF) on the promotion of osteogenesis in bone marrow stromal cells (BMSC) in vivo. Sci Rep. 2018;8(1):5876. [7] ROCHIRA A, SICULELLA L, DAMIANO F, et al. Concentrated growth factors (CGF) induce osteogenic differentiation in human bone marrow stem cells. Biology (Basel). 2020;9(11):370. [8] ZHANG Y, LIU K, YAN M, et al. Effect of concentrated growth factor combined with mineralized collagen material on the adhesion, proliferation, and osteogenic differentiation of bone marrow mesenchymal stem cells and the osteogenic effect in vivo. Zhongguo Xiu Fu Chong Jian Wai Ke Za Zhi. 2021;35(3):295-302. [9] QI L, LIU L, HU Y, et al. Concentrated growth factor promotes gingival regeneration through the AKT/Wnt/β-catenin and YAP signaling pathways. Artif Cell Nanomed B. 2020;48(1):920-993. [10] JIN R, SONG G, CHAI J, et al. Effects of concentrated growth factor onproliferation, migration, and differentiation of human dental pulp stem cells in vitro. J Tissue Eng. 2018;9:2041731418817505. [11] YAN QF, DOU L, HUAN J, et al. The effect of concentrate growth factors on the survival, proliferation and differentiation of human dental pulp cells. Sichuan Da Xue Xue Bao (Yi Xue Ban). 2018;49(5):716-719. [12] HONG S, CHEN W, JIANG B. A comparative evaluation of concentrated growth factor and platelet-rich fibrin on the proliferation, migration, and differentiation of human stem cells of the apical papilla. J Endod. 2018;44(6):977-983. [13] 马翔宇,丁俐丹,唐世俊,等.自体浓缩生长因子对比格犬脂肪干细胞体外增殖及成骨向分化的影响[J].中南大学学报(医学版), 2018,43(1):1-6. [14] HU T, ZHANG H, YU W, et al. The combination of concentrated growth factor and adipose-derived stem cell sheet repairs skull defects in rats. Tissue Eng Regen Med. 2021;18(5):905-913. [15] SAHIN IO, GOKMENOGLU C, KARA C. Effect of concentrated growth factor on osteoblast cell response. J Stomatol Oral Maxillofac Surg. 2018;119(6):477-481. [16] 李欣,姜志红,柳忠豪.浓缩生长因子提取液对钛片表面MC3T3-E1细胞增殖分化的影响[J].华西口腔医学杂志,2015,33(1):84-87. [17] BORSANI E, BONAZZA V, BUFFOLI B, et al. Beneficial Effects of Concentrated Growth Factors and Resveratrol on Human Osteoblasts In Vitro Treated with Bisphosphonates. Biomed Res Int. 2018;2018: 4597321. [18] DONG K, ZHOU WJ, LIU ZH, et al. The extract of concentrated growth factor enhances osteogenic activity of osteoblast through PI3K/AKT pathway and promotes bone regeneration in vivo. Int J Implant Dent. 2021;7(1):70. [19] KAO CH. Use of concentrate growth factors gel or membrane in chronic wound healing: description of 18 cases. Int Wound J. 2020;17(1):158-166. [20] YUE H, ZHOU L, ZOU R, et al. Promotion of skin fibroblasts collagen synthesis by polydioxanone mats combined with concentrated growth factor extracts. J Biomater Appl. 2019;34(4):487-497. [21] CHEN J, JIAO D, ZHANG M, et al. Concentrated growth factors can inhibit photoaging damage induced by ultraviolet A (UVA) on the human dermal fibroblasts in vitro. Med Sci Monit. 2019;25:3739-3749. [22] 王亚楠,王佐林.浓缩生长因子促进牙龈软组织缺损修复的实验研究[J].口腔颌面外科杂志,2018,28(3):121-126. [23] QIN J, WANG L, SUN Y, et al. Concentrated growth factor increases Schwann cell proliferation and neurotrophic factor secretion and promotes functional nerve recovery in vivo. Int J Mol Med. 2016;37(2): 493-500. [24] 宦俊,窦磊,严崎方,等.浓缩生长因子促人脐静脉血管内皮细胞成血管化作用研究[J].华西口腔医学杂志,2018,36(3):247-251. [25] KAMAL A, SALMAN B, ABDUL RAZAK NH, et al. The efficacy of concentrated growth factor in the healing of alveolar osteitis: a clinical study. Int J Dent. 2020;2020:9038629. [26] 朱梅,孙强,邓佳蕴,等.浓缩生长因子联合骨代用品在美学区拔牙位点保存中的临床应用[J].中国美容医学,2019,28(11):100-103. [27] 赵军伟,汪涌,韩爽.脱矿冻干骨联合浓缩生长因子治疗牙周骨下袋的临床效果评价[J].中国实用口腔科杂志,2021,14(2):166-170. [28] 张梅,邹高峰,常靓,等.下颌磨牙牙体严重缺损伴Ⅱ度根分叉病变的综合治疗[J].北京口腔医学,2021,29(1):27-31. [29] 李敏慧,江烨,杨雪超.浓缩生长因子纤维蛋白治疗牙龈退缩疗效评价及对牙龈成纤维细胞增殖的影响[J].中国美容医学,2020, 29(12):106-108. [30] 于文凤,于兰,吕敏敏,等.血小板浓缩生长因子联合冠向复位瓣修复对牙龈退缩患者根面覆盖效果及美学评价的影响[J].中国美容医学,2019,28(10):117-120. [31] KORKMAZ B, BALLI U. Clinical evaluation of the treatment of multiple gingival recessions with connective tissue graft or concentrated growth factor using tunnel technique: a randomized controlled clinical trial. Clin Oral Investig. 2021;25(11):6347-6356. [32] BARBU HM, IANCU SA, RAPANI A, et al. Guided bone regeneration with concentrated growth factor enriched bone graft matrix (sticky bone) vs. bone-shell technique in horizontal ridge augmentation: a retrospective study. J Clin Med. 2021;10(17):3953. [33] 任静,郑佳俊,黄杰,等.浓缩生长因子在上颌前牙美学区种植中的临床应用[J].中国口腔种植学杂志,2019,24(3):114-117,138. [34] SUN W, LI T, YAO H, et al. Effects of concentrated growth factor and nanofat on aging skin of nude mice induced by D-galactose. Physiol Res. 2021;70(3):425-435. [35] ZHANG T, DAI J, XU Y, et al. Liquid phase concentrated growth factor improves autologous fat graft survival in vivo in nude mice. Aesthetic Plast Surg. 2021;45(5):2417-2422. [36] 付丽,孙悦,翟婧捷,等.3D打印及浓缩生长因子在双侧下牙槽神经移位同期牙种植术中的应用[J].口腔医学研究,2016,32(10): 1003-1005. [37] 王昕,陈小平,赵启明,等.浓缩生长因子注射改善眶周皱纹的临床观察[J].中国美容整形外科杂志,2018,29(7):402-405. [38] 许军旗,高立坤,王艳华.浓缩生长因子联合Biooss引导骨再生在炎症期即刻种植中的价值[J].临床研究,2018,26(11):43-44. [39] 周海兰,陈漫娟,林臻彦,等.预成型钛网及浓缩生长因子在骨增量中的应用1例[J].临床口腔医学杂志,2021,37(6):372-374. [40] KERANMU D, AINIWAER A, NUERMUHANMODE N, et al. Application of concentrated growth factor to autotransplantation with inflammation in recipient area. BMC oral health. 2021;21(1):556. [41] 李勇,程如玉,彭学生,等.富自体浓缩生长因子联合Bio-Oss骨粉在颌骨囊肿中的疗效研究[J].中华全科医学,2018,16(7):1113-1115. [42] YÜCE MO, ADALI E, IŞIK G. The effect of concentrated growth factor (CGF) in the surgical treatment of medication-related osteonecrosis of the jaw (MRONJ) in osteoporosis patients: a randomized controlled study. Clin Oral Investig. 2021;25(7):4529-4541. [43] MASUKI H, OKUDERA T, WATANEBE T, et al. Growth factor and pro-inflammatory cytokine contents in platelet-rich plasma (PRP), plasma rich in growth factors (PRGF),advanced platelet-rich fibrin (A-PRF), and concentrated growth factors (CGF). Int J Implant Dent. 2016;2(1):19. [44] ISLER SC, SOYSAL F, CEYHANLı T, et al. Regenerative surgical treatment of peri-implantitis using either a collagen membrane or concentrated growth factor: a 12-month randomized clinical trial. Clin Implant Dent Relat Res. 2018;20(5):703-712. [45] TALAAT WM, GHONEIM MM, SALAH O, et al. Autologous bone marrow concentrates and concentrated growth factors accelerate bone regeneration after enucleation of mandibular pathologic lesions. J Craniofac Surg. 2018;29(4):992-997. [46] XU Y, QIU J, SUN Q, et al. One-year results evaluating the effects of concentrated growth factors on the healing of intrabony defects treated with or without bone substitute in chronic periodontitis. Med Sci Monit. 2019;25:4384-4389. [47] SURESHBABU NM, RANGANATH A, JACOB B. Concentrated growth factor - surgical management of large periapical lesion using a novel platelet concentrate in combination with bone graft. Ann Maxillofac Surg. 2020;10(1):246-250. [48] KOZER N, CLAYTON AHA. In-cell structural dynamics of an EGF receptor during ligand-induced dimer-oligomer transition. Eur Biophys J. 2020; 49(1):21-37. [49] CHENG B, LI C, ZHAO Y, et al. The impact of postoperative EGFR-TKIs treatment on residual GGO lesions after resection for lung cancer. Signal Transduct Tar. 2021;6(1):73 [50] 石鹏程,纪晓俊.酵母系统表达人表皮生长因子研究进展[J].中国生物工程杂志,2021,41(1):72-79. [51] FORTINO VR, CHEN RS, PELAEZ D, et al. Neurogenesis of neural crest-derived periodontal ligament stem cells by EGF and bFGF. J Cell Physiol. 2014;229(4):479-488. [52] 胡亚暖,姚永明,张泽敏,等.不同浓度EGF对兔ADSCs体外诱导分化为表皮细胞的实验研究[J].中国美容医学,2016,25(7):47-50. [53] 夏荣木,江其昌,杨龙,等.表皮生长因子影响大鼠骨髓间充质干细胞增殖和迁移的信号通路[J].中国组织工程研究,2017,21(29): 4635-4641. [54] BAI W, ZHANG Y, XU W, et al. Isolation and characterization of neural progenitor cells from bone marrow in cell replacement therapy of brain injury. Front Cell Neurosci. 2020;14:49. [55] RAFIEE F, POURTEYMOURFARD-TABRIZI Z, MAHMOUDIAN-SANI MR, et al. Differentiation of dental pulp stem cells into neuron-like cells. Int J Neurosci. 2020;130(2):107-116. [56] MAO Y, MA J, XIA Y, et al. The overexpression of epidermal growth factor (EGF) in HaCaT cells promotes the proliferation, migration, invasion and transdifferentiation to epidermal stem cell immunophenotyping of adipose-derived stem cells (ADSCs). Int J Stem Cells. 2020;13(1):93-103. [57] ZHAO H, ZUO X, REN L, et al. Combined use of bFGF/EGF and all-trans-retinoic acid cooperatively promotes neuronal differentiation and neurite outgrowth in neural stem cells. Neurosci Lett. 2019;690:61-68. [58] ESQUIROL-CAUSSA J, HERRERO-VILA E. Human recombinant epidermal growth factor in skin lesions: 77 cases in EPItelizando project. J Dermatolog Treat. 2019;30(1):96-101. [59] 郭磊,吴韫慧,高瑞.重组人表皮生长因子外用溶液联合半导体激光治疗复发性口腔溃疡的临床观察[J].医药论坛杂志,2018,39(9): 95-96. [60] VISWANATHAN V, JUTTADA U, BABU M. Efficacy of recombinant human epidermal growth factor (regen-D 150) in healing diabetic foot ulcers: a hospital-based randomized controlled trial. Int J Low Extrem Wounds. 2020;19(2):158-164. [61] ALAMOUDI NM, EL ASHIRY EA, FARSI NM, et al. Treatment of oral ulcers in dogs using adipose tissue-derived mesenchymal stem cells. J Clin Pediatr Dent. 2014;38(3):215-222. [62] 文超举,刘春影,裴婷婷,等.3种不同压膜方法对浓缩生长因子膜细胞因子释放及降解的影响[J].口腔医学,2019,39(10):889-894. [63] KIM J, LEE KM, HAN SH, et al. Development of stabilized dual growth factor-loaded hyaluronate collagen dressing matrix. J Tissue Eng. 2021; 12:2041731421999750. |
| [1] | Wang Junxiang, Sun Jiangwei, Bai Bujiafu·Yellisi, Wang Zhaoxin, Nijati·Turson. Effect of three abutment materials on bone stress around maxillary angle implant under dynamic loading [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 398-405. |
| [2] | Chen Jingqiao, Li Ying, Meng Maohua, Xu Xingxing, Wang Qinying, Wang Huan, Lu Jing, Shu Jiayu, Dong Qiang. Research progress in platelet-rich fibrin in stomatology [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 441-446. |
| [3] | Wang Kaiyu, Hu Peng, Wei Zairong, Huang Guangtao, Zhou Jian, He Guijia, Nie Kaiyu. Use of expanders and implants in breast reconstruction complicated with infection [J]. Chinese Journal of Tissue Engineering Research, 2023, 27(3): 461-469. |
| [4] | Xue Yadong, Zhou Xinshe, Pei Lijia, Meng Fanyu, Li Jian, Wang Jinzi . Reconstruction of Paprosky III type acetabular defect by autogenous iliac bone block combined with titanium plate: providing a strong initial fixation for the prosthesis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1424-1428. |
| [5] | Wu Weiyue, Guo Xiaodong, Bao Chongyun. Application of engineered exosomes in bone repair and regeneration [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1102-1106. |
| [6] | Li Jian, Bao Zhengqi, Zhou Pinghui, Zhu Ruizhi, Li Zhixiang, Wang Jinzi. Effects of posterior single open-door laminoplasty and anterior cervical corpectomy fusion on cervical sagittal balance parameters in the treatment of multilevel cervical spondylotic myelopathy [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(6): 949-953. |
| [7] | Peng Kun. Improvement of the treatment effect of osteoporotic fractures: research status and strategy analysis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(6): 980-984. |
| [8] | Wang Hailong, Li Long, Maihemuti·Yakufu, Chen Hongtao, Liu Xu, Yilihamu·Tuoheti. Finite element analysis of stress distribution of acetabular prosthesis in the Lewinnek safety zone [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(6): 843-847. |
| [9] | Gao Wenbo, Ma Zongmin, Li Shuxian, Nie Xiuji. Finite element analysis on the effect of implant length and diameter on initial stability under different bone conditions [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(6): 875-880. |
| [10] | Yuan Jing, Sun Xiaohu, Chen Hui, Qiao Yongjie, Wang Lixin. Digital measurement and analysis of the distal femur in adults with secondary knee valgus deformity [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(6): 881-885. |
| [11] | Zhang Jianguo, Chen Chen, Hu Fengling, Huang Daoyu, Song Liang. Design and biomechanical properties of dental implant pore structure based on three-dimensional finite element analysis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 585-590. |
| [12] | Tan Guozhong, Tu Xinran, Guo Liyang, Zhong Jialin, Zhang Yang, Jiang Qianzhou. Biosafety evaluation of three-dimensional printed gelatin/sodium alginate/58S bioactive glass scaffolds for bone defect repair [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 521-527. |
| [13] | Qiu Peng, Fu Qilin, Liu Min, Lan Yuyan, Wang Pin. Comparison of oral micro-adhesion on polyetheretherketone, zirconium dioxide, and pure titanium abutment [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 540-545. |
| [14] | Chen Shuo, Xiao Dongqin, Li Xingping, Ran Bin, Shi Feng, Zhang Chengdong, Deng Li, Huang Nanxiang, Liu Kang, Feng Gang, Duan Ke. Preparation and characterization of tantalum functional coating on titanium implant [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 546-552. |
| [15] | Baibujiafu·Yelisi, Renaguli·Maihemuti, Aizimaitijiang·Saiyiti, Wang Junxiang, Nijiati·Tuerxun. Stress analysis of maxillary central incisor crown implant restoration in different occlusal modes [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 567-572. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||