2.1 DNA水凝胶的发展史 DNA水凝胶至今已发展了近30年,是核酸纳米技术的重要衍生产物。在1996年,NAGAHARA等[15]首次报道了DNA作为纳米级刚性材料构建宏观材料的可行性与潜力。在2006年后的11年间,多种DNA水凝胶的基础构建方法得到建立[14,25-26]。2020-2025年,DNA水凝胶的转化研究进入快速发展期,每年均有大量研究探索其在生物传感、组织修复及药物递送等领域的应用价值。DNA水凝胶发展的关键时间点及重要内容,见表1。

2.2 DNA水凝胶的构建策略与特性 DNA水凝胶因独特的可编程性和生物相容性而受到广泛关注。根据组成,DNA水凝胶可以分为纯DNA水凝胶和杂化DNA水凝胶;也有相关文献依据交联方式分为物理水凝胶和化学水凝胶[23,33]。纯DNA水凝胶完全由DNA链通过碱基互补配对或物理缠绕组装形成,具有高度的序列可设计性和结构可控性,这种水凝胶的设计可以通过调整DNA序列来实现,赋予其特定的物理和化学性质。杂化DNA水凝胶通过引入其他组分(如聚合物、纳米颗粒或小分子)来增强其功能性和力学性能,常见的杂化方式如聚合物化学接枝、静电吸引和配位作用,同时包含物理作用和化学键的形成。杂化策略可以赋予水凝胶响应性和多功能性,例如,通过与聚合物结合,DNA水凝胶可以获得自愈合能力[34];偶联量子点可以获得示踪能力[19];在水凝胶中引入纳米银离子可提升抗菌性能[35];引入适配体作为交联链可对特定靶标响应[17]。纯DNA水凝胶和杂化DNA水凝胶的比较,见表2。

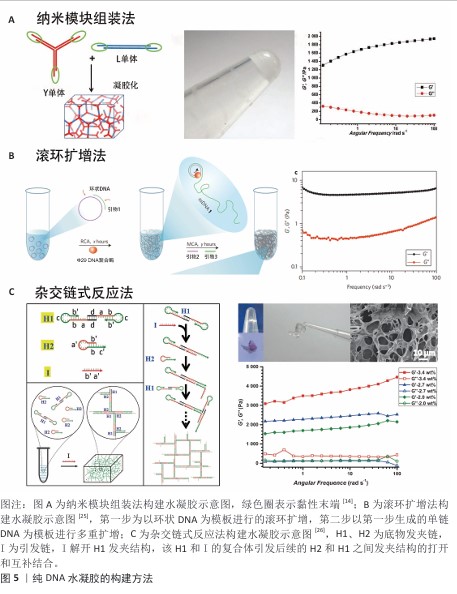
2.2.1 纯DNA水凝胶的构建与特性 纯DNA水凝胶由DNA链通过碱基配对、物理缠结、酶催化连接等作用形成,常用构建方法有纳米模块法、滚环扩增法和杂交链式反应法。纳米模块法是由数条部分互补的短单链DNA经过变性退火形成纳米模块,随后纳米模块间通过酶催化、黏性末端等多种方式连接形成水凝胶。最先由LUO团队利用T4连接酶催化带有黏性末端的分枝状纳米结构(X型、Y型、T型),纳米结构间由磷酸二酯键相连形成三维网状凝胶[28]。LIU团队[29]在Y型单体的末端添加了一段富含胞嘧啶的序列,这段序列在pH=5时发生质子化形成i-motif交联成水凝胶,而在pH=8时解离,这种交联方式赋予了水凝胶对pH值的响应性。为了实现生理条件下的凝胶化,XING等[14]进一步运用带有黏性末端的Y型纳米结构和L型纳米结构(图5A),在无需连接酶的催化下快速实现了纳米结构溶液凝胶化,由于DNA间的氢键处于动态交联,会随着温度的升高和外力影响发生断裂,因此,这种凝胶在温度升高时发生凝胶-溶胶的转变以及剪切稀化的现象;此外,在链内合理设计酶切位点还可赋予水凝胶针对不同酶的响应。
滚环扩增是一种等温酶促扩增技术,在酶催化下以环状DNA为模板合成长单链DNA,随后长单链DNA发生物理缠结而形成水凝胶(图5B)。LUO团队首次通过酶催化生成长单链制备了一种记忆型DNA水凝胶,该凝胶离开水时呈现为无定形状态,而回到水中又可以恢复原本的固体形态[25]。RNA由于较差的稳定性,目前RNA基水凝胶鲜有报道,HAN等[37]在滚环扩增的基础上,同时进行滚环转录合成DNA、RNA多聚体杂交形成水凝胶。多项研究通过该方法制备了水凝胶应用于肿瘤诊断[38]、外泌体分离[38]、组织修复[39]、细胞分离捕获[40]。
杂交链式反应是无需酶催化的等温扩增技术,该方法通过引发链打开DNA的发夹结构而引发链式反应,形成DNA长链结构。WANG
等[26]建立了基于该反应的DNA水凝胶制备方法,此方法需要2条发夹链H1、H2,加入引发链后引发链首先通过链置换打开H1发夹结构,而H1发夹结构又进一步置换了H2发夹结构,使得反应持续进行,最终形成三维的网状结构(图5C),这种水凝胶的机械性能优越,弹性模量可达千帕。
上述3种方法为目前常用的纯DNA水凝胶构建方法,此外还有少数特殊的构建方式,如酶连接质粒DNA[41]、特殊结构交联[42]、天然长链DNA缠绕等[20]。不过,构建纯DNA水凝胶的成本高[41],尤其是纳米模块法形成的水凝胶凝胶力学性能与短单链DNA的浓度和纯度密切相关。参照XING等[14]的研究,以500 μmol/L Y单体和750 μmol/L L单体形成毫升级的水凝胶需数千吸光度值的高效液相色谱纯化短单链DNA,该花费在实际应用中将是难以承受的。扩增法制备水凝胶通常耗时较长,凝胶化过程需数小时至数天[37,43];滚环扩增形成的水凝胶力学性能通常较低,弹性模量G’通常只有几十帕,因此,相关研究尝试引入其他聚合物或者纳米材料增强水凝胶的力学性能和降低构建成本。
2.2.2 杂化DNA水凝胶的构建与特性 杂化DNA水凝胶是由DNA与聚合物分子(如聚丙烯酰胺[15]、多肽[16]、蛋白质等[44])或纳米颗粒(如金纳米颗粒[45]、硅纳米片[46]、量子点[19,47])经过共价、静电吸附、大环主客体作用、π-π堆积或配位作用形成的复合水凝胶。这类水凝胶保留DNA的碱基互补配对能力、酶响应性[48]、温度响应性[48-49]、pH值响应性[50],同时引入的聚合物分子或纳米颗粒可以提升水凝胶的力学性能,赋予额外的光响应性[51-52]、导电性[53]、力响应性[54]、磁响应性和特异靶标的响应性
等[17,55-56],提高水凝胶的预期效能。
将DNA共价接枝作为侧链,随后通过碱基互补配对是构建凝胶的一种常用策略。NAGAHARA等[15]将丙烯酸酯修饰的DNA接枝到聚丙烯酰胺的侧链,随后利用侧链DNA互补交联合成了首个热可逆的杂化DNA水凝胶,该凝胶受热后交联链解离进而水凝胶解聚。PENG等[51]将偶氮苯修饰的DNA作为交联剂引入聚丙烯酰胺,利用偶氮苯在可见光下为反式构象使水凝胶呈收缩态,在紫外光下为顺式构象使水凝胶呈溶胀态,进而实现药物的光响应性释放。多肽和蛋白质作为高分子主链具有更高的生物安全性,例如,LIU团队在多肽和人血清白蛋白上接枝构建了DNA超分子水凝胶,并用于荧光蛋白的负载和定点释放[57-58]。另一类策略是将DNA接枝于纳米颗粒表面,可以通过这些颗粒获得光信号,实现对靶标的检测或示踪,例如,LIU等[45]将DNA通过共价键连接在金纳米颗粒表面使其作为水凝胶的交联和信号单元,并引入金属离子核酸酶的底物链,当环境中存在靶标离子时,核酸酶催化使金纳米颗粒释放到溶液中而产生吸收光的变化;此外,也可借助量子点的荧光效应进行示踪[19]。适配体是人工筛选出对特定靶标具有高亲和力的短链DNA或RNA,可作为交联链引入水凝胶中[17],当适配体与靶标接触后解组装凝胶,可产生信号并加速负载物的释放,实现诊疗的一体化。
物理掺杂是一种简单和直接构建DNA水凝胶的策略,这种策略主要利用DNA的负电性和或碱基堆叠产生的作用力。DNA骨架在生理pH值下带有负电,加入合适的正电性组分可通过静电作用实现凝胶化[46,59],也可通过此方式负载带有正电性的治疗性分子[60]。此外,可以利用氧化石墨烯的碳层结构与ssDNA中的芳香碱基(如胸腺嘧啶)通过π-π堆积形成物理交联,该种方式更适用于滚环扩增生成的单链DNA[61]。
杂化DNA水凝胶的构建方式存在多样性,形成的水凝胶也性质不一,实际应用方向会界定每种水凝胶的特性。力学方面,在接枝形成的DNA水凝胶中,聚合物作为主链的分子质量通常小于DNA,杂化水凝胶的交联程度高,力学性能更为优异[62-63],而直接物理掺杂形成的水凝胶力学性能较弱。相较于纯DNA水凝胶,杂化水凝胶的构建成本因DNA不再作为主链而有所降低,并且具备更优异的性能,但是构建杂化水凝胶的步骤较纯DNA水凝胶繁琐[15,51],并且生物相容性可能会降低。需要注意的是,对于已经形成的凝胶再进行功能化需要用功能化分子渗透水凝胶,这可能会导致空间或静电受阻,因此需要考虑先进行水凝胶的功能化,再进行凝胶化。
2.3 DNA水凝胶在组织修复中的应用
2.3.1 创面修复 DNA水凝胶在创面修复中具有重要的发展潜力和价值,尤其是在糖尿病创面再生方面。糖尿病创面由于持续的细菌感染、过量的活性氧产生、持续的炎症反应和血管生成障碍,使其再生极具挑战性,理想的修复策略需要在创面修复过程中整合并顺序释放杀菌、抗氧化、抗炎和促血管生成的活性物质。LIANG等[64]设计了一种新型可注射多功能DNA水凝胶敷料,将焦磷酸镁晶体作为抗菌功能单元封装在DNA聚合物网络中以缓慢释放镁离子,促进伤口微环境中的血管生成;同时加入抗炎、抗氧化组分姜黄素和抗生素环丙沙星,3种协同作用下的DNA水凝胶具有良好的清除活性氧和抗炎、抗菌能力,有效加速了糖尿病感染创面模型的愈合。另一项研究通过接枝DNA单元和聚乙烯亚胺动态交联、掺杂加热功能的黑磷量子点制备了多功能DNA水凝胶,该水凝胶促进巨噬细胞从促炎M1表型转变为修复M2表型,激活神经元转变为修复状态,加速皮肤神经再生和血管生成,招募髓系细胞,激活适应性免疫反应,增强组织再生能力,促进毛囊和毛发再生[47]。Agilegel是一种基于DNA的多药水凝胶,通过其层次结构能够精确控制血管内皮生长因子α、银纳米簇和白细胞介素10的顺序释放,从而有效促进糖尿病创面的愈合[65]。细胞因子疗法是治疗糖尿病创面的策略之一,采用纳米模块法负载白细胞介素33确保了细胞因子的均匀封装和持续释放,在生理条件下这种DNA水凝胶可维持伤口内白细胞介素33释放至少7 d,并能有效诱导免疫细胞的局部积累,促进局部伤口炎症消退,DNA链同时消除了影响糖尿病创面愈合的过量活性氧[35]。
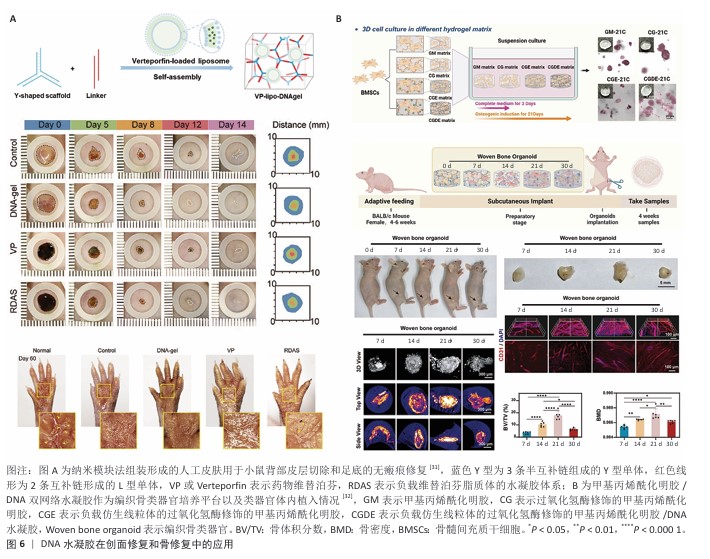
功能性附属器官再生对皮肤康复至关重要,但由于现有治疗方法无法有效预防畸形瘢痕形成,XIONG等[31]提出了一种新型再生导向人工皮肤系统,该系统基于对天然皮肤基质高度仿生设计(图6A),利用DNA组件的可编程性和结构刚性,无需外源细胞移植,能精准引导伤口成纤维细胞的再生过程,有效减少组织纤维化,实现快速无瘢痕创面修复、真皮功能恢复,并成功原位再生多种附属器官。内脏器官的快速出血性伤口处理在临床是一个难题,紧急情况下需介入寻找出血点进行缝合或压迫止血。受启发于中性粒细胞胞外捕获网,研究人员制备了一种液体吸收良好、黏附稳定的DNA水凝胶敷料,在小鼠肝脏出血模型中,DNA水凝胶迅速黏附在伤口上直接压迫止血,同时促进红细胞黏附和聚集,激活血小板,以仿生方式促进凝血级联反应[34]。抗菌肽具有对多药耐药机制的低敏感性,因此将其作为新型抗感染药物的结构模板已经引起了人们的兴趣,然而,如何保持递送的抗菌肽活性是一大难点。DNA自带的负电性可以静电吸附阳离子抗菌肽,一方面,有效降低不恰当的毒性作用;另一方面,随着DNA的降解抗菌肽被逐步释放出来,这种负载抗菌肽L12的DNA水凝胶对金黄色葡萄球菌感染的猪伤口具有显著疗效[60]。为了改善DNA水凝胶对于特殊位置的应用效果,如关节处创面因关节活动水凝胶发生变形、断裂和脱落,ZHOU等[66]设计了具有蟹爪状结构和鲨鱼微槽结构的DNA水凝胶微针,具有高的稳定性和抓握能力,这种水凝胶黏附在关节上即使关节反复变形后仍保持稳定,从而提高了关节创面患者的舒适度。
综上所述,DNA水凝胶在不同创面修复类型中均具有优异的修复效果、灵活的改造特性和构建多功能、多层次缓释平台的潜力。
2.3.2 骨与软骨修复 骨与软骨修复对水凝胶的力学性能要求较高,大部分DNA水凝胶的性能不能满足该要求。目前已有研究尝试通过引入海藻酸钠和琼脂糖作为共编码因子,将水凝胶的弹性模量提升到MPa级,并保留了较高的生物相容性,但尚未验证该水凝胶的体内有效性[36]。有研究提出双网络提升水凝胶的力学性能,如丝素蛋白[44]、甲基丙烯酰化明胶和DNA纳米模块形成互穿网络[32],制备了力学性能优异的杂化水凝胶,从细胞力学角度促进骨与软骨的再生,该水凝胶可在体外促进编织骨器官的形成(图6B),在体内显现出更快速的骨整合作用[32]。干细胞疗法对于骨再生是一种良好的策略,常规水凝胶负载骨间充质干细胞进行注射因剪切力较大会损伤细胞活力,而DNA水凝胶的剪切稀化特性支持微创注射。YAN等[67]通过纳米模块法合成水凝胶负载骨间充质干细胞,由于组装时非共价键的动态变化可以保护骨间充质干细胞,注射后骨间充质干细胞的存活率超过99%;在兔骨关节炎模型中,相较于甲基丙烯酰化明胶水凝胶,DNA水凝胶还可以促进周缘细胞向水凝胶区迁移。
ATHANASIADOU等[68]发现纳米模块法制备的DNA超分子水凝胶可以激活Wnt/β-catenin信号通路和Notch信号通路,促进干细胞的成骨分化。另一种双网络DNA大孔水凝胶采用负载核酸适体和纳米诱导剂来增强骨髓间充质干细胞的招募,并促进其成骨分化,这种工程化水凝胶显著增强了颅骨修复,伴随有良好的基质矿化和新骨形成[20]。
直接负载有效治疗分子也可促进骨再生。ZHANG等[69]使用酶响应DNA水凝胶作为二甲双胍的载体来治疗骨关节炎,随着脱氧核酶降解水凝胶,二甲双胍缓慢释放到关节腔中,该方法可保护二甲双胍不被滑膜液快速清除,从而发挥更佳的抗炎作用。YANG等[70]从促进血管化骨再生角度出发,将具有血管内皮生长因子的模拟肽QK化学接枝到淀粉样纤维上,该复合物可以从水凝胶基质中持续释放并刺激人脐静脉内皮细胞的管状形成和迁移;在颅骨缺损模型中,QK肽和黏土纳米片进一步增强了复合水凝胶引导的体内骨再生,为骨组织再生提供了适宜的微环境,并且水凝胶在恢复过程中逐步降解,并未引起毒性和免疫反应性。
糖尿病性牙槽骨缺损修复因持续的细菌感染、长期的炎症反应和骨愈合延迟在临床是一项挑战。DNA链既作为可成形的支架,用于加载免疫调节的M2巨噬细胞来源细胞外囊泡,也作为抗菌构建块[43]。黏附DNA水凝胶不仅可以保证银纳米团簇和M2巨噬细胞来源细胞外囊泡的时间依赖性持续释放,而且可以作为适合不同形状糖尿病牙槽骨缺损的人工细胞外基质。JING等[56]针对糖尿病状态下基质金属蛋白酶9的高表达设计了一款响应性水凝胶,通过硫醇-烯点击加成反应将硫醇修饰的单链DNA与八臂乙烯磺酸酯功能化的聚乙二醇共聚合,再加入响应基质金属蛋白酶9的适配体连接体以及牙髓干细胞源小细胞外囊泡,在病理缺陷部位注射水凝胶后,触发信号基质金属蛋白酶会将DNA适配体连接体从水凝胶中释放出来,形成结合复合物,进而诱导DNA水凝胶的解体并释放牙髓干细胞源小细胞外囊泡。
上述研究展示了DNA水凝胶可模拟细胞外基质为骨再生提供微环境,作为骨类器官培养平台和骨间充质干细胞的注射保护介质,也可作为响应性平台释放治疗性分子。
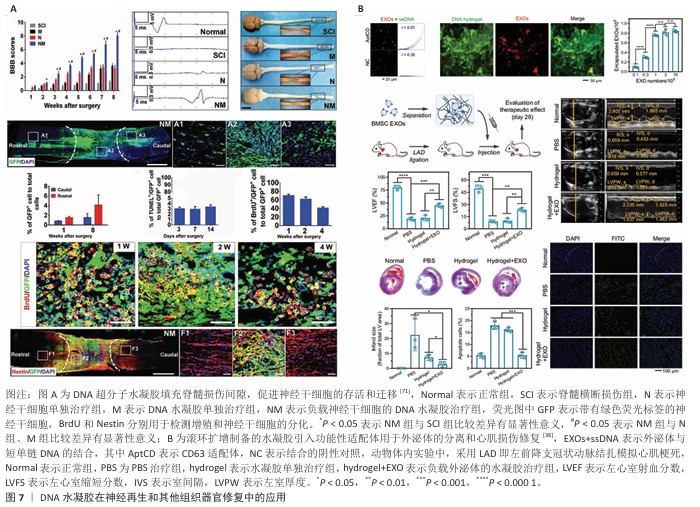
2.3.3 神经再生 脊髓损伤和周围神经损伤是一种复杂的继发性病理过程,涉及中枢与外周神经系统的交互作用,会导致运动或感觉神经功能障碍和创伤性神经瘤的形成,从而对生活质量产生负面影响,给社会造成沉重负担,目前常用治疗策略包括联合神经营养干预、细胞移植和免疫调节疗法等。DNA水凝胶具备良好的生物相容性、可注射、力学性能与神经组织相匹配,是理想的支架材料。顺序工程的DNA水凝胶作为神经干细胞移植的载体,其高渗透性确保了营养物质和分子信号可以成功扩散到组织中。YUAN等[71]运用一种极高渗透性的DNA水凝胶来修复脊髓间隙,这种水凝胶可以负载神经干细胞并为细胞提供增殖和分化的组织基质,从而在病变部位形成一个再生的神经网络,经8周的治疗大鼠后肢功能基本恢复(图7A)。DNA水凝胶的降解能够调节神经前体细胞的分化,DNA水凝胶促进了细胞聚集形成细胞簇,这可能促进了细胞-细胞相互作用,并调整了细胞分化路径[72]。有研究将DNA水凝胶、血管内皮生长因子和神经生长因子结合起来构建一种新型的递送系统,用于周围神经损伤修复,利用X型和T型DNA之间不同的降解速率实现血管内皮生长因子和神经生长因子的双相释放,体外实验表明,DNA凝胶负载血管内皮生长因子和神经生长因子可以促进大鼠施万细胞的增殖、迁移和髓鞘形成,同时保持细胞活力;体内实验表明,负载血管内皮生长因子和神经生长因子的DNA水凝胶在促进长缺损周围神经损伤修复方面的效果优于中空几丁质导管、DNA凝胶或血管内皮生长因子和神经生长因子组[73]。DNA水凝胶表面涂覆层粘连蛋白衍生功能肽-IKVAV肽后,与未修饰的DNA水凝胶和对照组相比显著增强了神经母细胞瘤细胞的生长和分化,神经母细胞瘤细胞在肽修饰的DNA水凝胶上表现出更长的神经突触长度、微管和细胞骨架的动态运动以及内吞机制改变[74]。肽修饰的DNA水凝胶在神经组织工程应用中显示出优越性,有望用于开发神经组织导管。上述研究表明,DNA水凝胶独特的物理力学性能能够调控神经细胞的行为,在神经再生中具有无尽的潜力。
2.3.4 其他组织器官修复 在其他再生修复应用中,DNA水凝胶被相应设计为满足应用需求或诊疗一体化的多功能材料。TANG等[38]通过滚环扩增制备的DNA水凝胶联合白细胞分化抗原63适配体,可实现乳腺癌临床样本外泌体的捕获和miRNA检测,也可捕获骨髓间充质干细胞来源外泌体并封装在水凝胶中,将这种含有外泌体的DNA水凝胶直接注射到大鼠心肌梗死模型的受损心肌上,DNA水凝胶能够在血清环境中逐渐降解并释放出外泌体,缓释的外泌体能够有效改善心肌梗死区域的心脏功能,并防止心肌细胞的凋亡(图7B)。YU等[17]针对脑出血术后可能出现的二次出血损害设计了一款原位植入的诊疗一体化水凝胶,该体系采用了2条部分互补的短链DNA和靶向血红蛋白的适配体,当发生二次出血时,适配体持续捕获血红蛋白介导水凝胶逐步崩解,实现负载的去铁胺按需释放而不影响生理性铁依赖功能,从而抑制神经细胞铁死亡达成“自我治疗”效果。BASU等[46]通过硅酸盐纳米盘与带负电荷的DNA主链静电相互作用和聚乙二醇二缩水甘油醚与DNA的交联,合成了具有化学和物理双交联纳米复合水凝胶,并负载了趋化因子基质细胞衍生因子1α,与不含硅酸盐的纳米复合材料相比具有更强的弹性和机械韧性;此外,硅酸盐纳米盘和基质细胞衍生因子1α之间的静电相互作用导致趋化因子从水凝胶中持续释放,释放的基质细胞衍生因子1α保留了趋化特性。脂质体被认为是遗传疾病和传染病潜在的治疗方法,但它们对高剪切应力敏感,这会导致纳米结构的完整性丧失和活性药物成分的释放。有研究提出了一种快速挤出方法来制备含有DNA水凝胶的脂质体以改善脂质体的稳定性,通过水凝胶封装的脂质体在雾化过程中保持了完整的球形形态,与脂质体直接雾化相比稳定性得到了显著提升[75]。
近年DNA水凝胶在组织修复方面的应用总结,见表3。