Chinese Journal of Tissue Engineering Research ›› 2020, Vol. 24 ›› Issue (20): 3217-3225.doi: 10.3969/j.issn.2095-4344.2546
Previous Articles Next Articles
Nell-1 in bone tissue engineering
Jin Liangyu1, Li Weiming2
- 1Harbin Medical University, Harbin 150000, Heilongjiang Province, China; 2First Affiliated Hospital of Harbin Medical University, Harbin 150001, Heilongjiang Province, China
-
Received:2019-09-05Revised:2019-09-06Accepted:2019-10-15Online:2020-07-18Published:2020-04-13 -
Contact:Li Weiming, MD, Associate chief physician, First Affiliated Hospital of Harbin Medical University, Harbin 150001, Heilongjiang Province, China -
About author:Jin Liangyu, Master candidate, Harbin Medical University, Harbin 150000, Heilongjiang Province, China -
Supported by:China Postdoctoral Science Foundation, No. 2016M601449
CLC Number:
Cite this article
Jin Liangyu, Li Weiming. Nell-1 in bone tissue engineering[J]. Chinese Journal of Tissue Engineering Research, 2020, 24(20): 3217-3225.
share this article
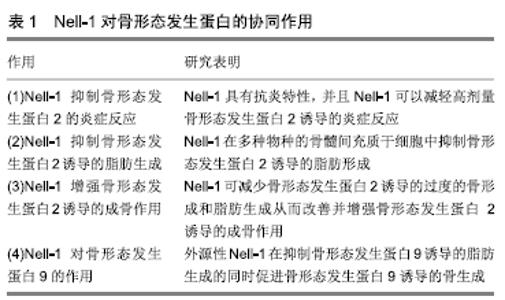
2.1 Nell-1基因的发现 1995年,MATSUHASHI等[1]从9 d的鸡胚中分离出一种包含5个类表皮生长因子(EGF-like)的重复序列编码835个氨基酸的基因并命名为Nel。Northen blot及原位杂交分析显示,在10-17 d的鸡胚组织中广泛存在Nel基因的mRNA,其中脑组织中含量最高。小鸡出生后,其他组织中的Nel基因的mRNA及蛋白表达消失,而脑组织中仍维持较高水平的表达。而在1996年,WATANABE等[2]从人胎儿脑cDNA文库中分离出与鸡胚胎Nel类似的两种基因,故分别命名为Nel样1型基因(Nell-1)和Nel样2型基因(Nell-2)。荧光染色体原位杂交试验显示,人类的Nell-1基因位于11p15.1- p15.2,长度为2 977 bp,包含了编码810个氨基酸的开放阅读框架。在不同的种属之间,Nell-1基因具有较高的保守性,即在人类以及大鼠、小鼠体内该基因cDNA全长序列具有93%的同源性。 接下来的研究发现Nell基因与造血干细胞及B细胞的发育调节、神经系统及直肠肿瘤的发生都存在着一定的联系[3-4],具有在神经组织表达的特异性。当时的研究并未发现其与骨组织有任何相关性,直到1999年,TING等[5]在手术切除的人类单侧颅骨畸形患者的颅骨中发现了Nell-1蛋白表达的上调,而这种先天性畸形的形成就是由于患者的颅缝早闭造成的。mRNA印迹研究显示,人Nell-1只在胚胎脑组织中特异性表达,而在肾、肝、及肺组织检测不到Nell-1的表达。而大鼠Nell-1只在颅骨中的骨祖细胞特异性表达,而在成纤维细胞中完全检测不到Nell-1的表达。这些都说明患者出现颅缝早闭与局部Nell-1的表达增高有密切联系,Nell-1在促进成骨分化方面有一定的作用。自此,人们开始对Nell-1与骨组织的关系进行了大量的科学研究,结果证实Nell-1是一种可以有效促进骨再生的蛋白。 2.2 目前对于Nell-1促进骨再生机制的理解 2.2.1 Nell-1选择性地促进骨软骨祖细胞和骨髓间充质干细胞的分化和骨形成 在以往的对于Nell-1各个方向的研究中,其在体外促进骨软骨细胞分化,在体内促进骨形成,都表现出对靶细胞较高的特异性。 第一,重组Nell-1蛋白在成骨细胞前体细胞系MC3T3和原发性颅骨细胞中,可以刺激并诱导成骨细胞分化、细胞凋亡和矿化;而在成纤维细胞系NIH3T3和原代成纤维细胞中,即使提供适宜的体外分化培养基,仍无法看到上述结果[6-7]。这其中部分原因可能是由于可以与Nell-1结合的受体只在成骨细胞表面表达而不在成纤维细胞表面表达。Nell-1刺激骨原细胞系的靶细胞诱导其高度表达骨桥蛋白、骨钙素、骨形态发生蛋白7基因和蛋白质,以及靶细胞的高度矿化,这些都是成骨细胞晚期阶段或彻底分化的标志物。而在Nell-1过度表达的MC3T3细胞中,作为成骨细胞分化早期的基因标志物的碱性磷酸酶和成骨细胞特异性转录因子(Osterix,OSX)的表达水平却被抑制[8],这意味着Nell-1基因可能在骨分化相对较晚的阶段发挥促骨形成的作用而不是在分化的早期。 第二,Nell-1可以在体外驱动骨髓间充质干细胞向骨软骨细胞系的分化并在体内促进软骨内成骨过程,但其不会使在体外培养的成肌细胞C2C12细胞向成骨细胞转化,也不会诱导体内肌肉中的异位骨形成[9-10]。骨髓间充质干细胞在适当的条件下可以向多个细胞方向分化[11-12]。重组Nell-1蛋白显著增强骨髓间充质干细胞向成骨细胞的分化,这点可以从显著升高的碱性磷酸酶活性和分化培养基明显增多的矿化结节得到证实。 第三,Nell-1在细胞发育的过程中,对骨软骨细胞系的影响比其他谱系的细胞更具有针对性,其意义也更为深远。在CMV-Nell-1转基因小鼠和ENU诱导的Nell-1基因缺失小鼠模型中已经发现胚胎小鼠的发育畸形主要集中表现在骨骼系统[6,13],这点与上述观点完全吻合。因此,Nell-1很可能只选择性的针对特异靶细胞——骨软骨细胞系发挥促进骨软骨细胞分化和骨的形成作用。 2.2.2 Nell-1基因的转录水平直接受Runx2基因的调控,Nell-1作为Runx2的下游基因发挥作用 骨特异性基因芯片分析显示,在AdNell-1转染MC3T3细胞后的第12天,细胞内骨软骨相关基因的表达显著增高并开始出现矿化[6]。基因表达上调2倍以上的包括骨桥蛋白、骨钙素和骨形态发生蛋白7等成骨细胞分化晚期的标志物。然而,Runx2(Runt homology domain transcription factor-2,又被称作Cbfa1),转化生长因子β1,-2,-3及其受体Ⅰ,Ⅱ和Ⅲ,成纤维细胞生长因子受体Ⅰ和Ⅱ,在RNA的表达水平上均未见到明显差异。由此推测Nell-1可能作为这些骨生物学相关关键分子的下游基因而发挥作用[6],或者Nell-1也可能在相对较晚的阶段通过另外的途径来促进成骨细胞的分化。事实上,无论是转化生长因子β1还是成纤维细胞生长因子2都可显著增加体外原代颅盖骨细胞中Nell-1的表达[8],这也可以说明Nell-1是这两个重要骨生长因子的下游转录因子,进一步提示Nell-1可能是人类颅缝早闭形成的一个关键性局部因素。 为了研究Nell-1基因表达的调控,TRUONG等[14]在分析了Nell-1基因启动子后发现了3个与Runx2结合的位点——成骨细胞特异性顺势激活原件2(OSE-2),其存在于2.2 kb的人类Nell-1基因启动子的转录起始位点上游。因此TRUONG等认为Runx2通过与启动序列中的OSE-2位点特异性结合而激活并上调Nell-1的表达。此外,此研究的生物学分析和体外转染实验也进一步证实了大鼠和小鼠的Nell-1启动子中包含功能性的OSE-2位点。Runx2是调控成骨细胞生成及骨再生的主要基因,而确定Nell-1是Runx2的直接下游靶基因的结论,更加奠定了Nell-1在骨组织发育及骨移植材料的组织工程学中的重要地位。 成骨细胞的生成和功能是骨生物学和骨再生学中最核心的概念[15],成骨细胞的生成最初是从间充质干细胞开始,分化为骨祖细胞系,最终经过一系列的分化成为成骨细胞和骨细胞。成骨细胞的功能又反过来依赖于骨基质沉积和已分化的成骨细胞的骨形成。确定未分化的间充质干细胞向骨及软骨祖细胞系分化的最初标志是表达Runx2。 Runx2基因对于成骨细胞的形成和功能是必不可少的[16],也被认为是促进软骨细胞成熟的关键因素[17]。Runx2基因敲除小鼠(Runx2-/-)表现出成骨细胞分化停滞,从而造成矿化骨完全缺乏,最后由于软骨性胸腔而继发呼吸衰竭导致围产期死亡。值得注意的是,在Runx2基因敲除的小鼠模型中(Runx2-/-),通过免疫组织化学和实时PCR检测Nell-1 mRNA和蛋白水平,发现其在颅面骨及小鼠原代颅骨细胞中含量明显减低[18]。此外,ENU诱导的Nell-1基因缺失小鼠因胸廓畸形而死于继发性的呼吸功能不全[15],这点与Runx2纯合子小鼠(Runx2-/-)十分相似。目前,科研者们发现的有效骨诱导因子大多都是Runx2的上游功能基因,例如,骨形态发生蛋白2、骨形态发生蛋白7、胰岛素样生长因子Ⅰ和转化生长因子β1等,这些都是可以上调Runx2转录的因子[19-22]。作为上游基因,这些因子在骨形成的复杂过程中,其不仅仅作用于Runx2基因,这就会比Nell-1更容易产生一些不良反应。因此,这些模型阐明了Runx2对Nell-1在骨软骨细胞系细胞内的直接监管关系,更为重要的是,这些模型充分表明Nell-1很可能是Runx2发挥其促进骨软骨生成及促进骨骼发育成熟作用的关键功能介质,这也充分解释了Nell-1在诱导骨生成方面的高度特异性和有效性的原因。 2.2.3 Nell-1促进骨生成信号通路 Wnt信号既能促进骨生成也能抑制脂肪生成,Wnt配体抑制Pparg和C/Ebpa从而抑制脂肪生成,Wnt信号缺失导致骨细胞分化受到抑制[23-24]。研究表明Nell-1可以激活Wnt信号,Nell-1在成骨细胞中的传导由整合素β1介导。整合素是一类细胞表面蛋白,介导细胞黏附,参与多种细胞因子和其他生长因子的信号传导。Nell-1通过其复杂的基因序列中N-末端TSP-1结构域直接与细胞表面受体整合素β1结合,随后激活典型的Wnt通路[25]。与整合素β1结合的Nell-1激活细胞内级联,促进细胞黏附、增殖和成骨分化。选用LRP5/6受体拮抗剂Frizzled蛋白(FZD)拮抗Wnt信号下游Wnt蛋白与LRP5/6受体的结合,Nell-1诱导的成骨作用减弱[25],使用XAV939(一种细胞内Wnt信号的小分子抑制剂)可阻断Nell-1的下游效应,Nell-1的成骨作用遭到破坏[25]。这些研究进一步表明Nell-1可通过Wnt途径促进骨生成。Wnt信号在一定时间内调控Runx2的基因表达,并通过成纤维细胞生长因子直接或间接激活成骨细胞特异性转录因子OSX[26],因此Nell-1在Wnt信号通路中通过刺激Runx2的表达来刺激成骨细胞分化和成熟。前已述Runx2是Nell-1的体内调节因子,于Nell-1基因上游调节Nell-1的表达,Runx2已显示出通过与其启动子区域中的OSE2位点结合而上调Nell-1[27],这说明Nell-1和Runx2在体内成骨作用中是相互影响的,Nell-1既是Runx2的下游同时也是上游靶点,在成骨信号间的平衡以及Runx2和其他成骨基因的调控中起着重要作用。 Nell-1蛋白通过激活ERK1/2激酶和JNK激酶等MAPK信号通路促进成骨生成。Nell-1作用于可成骨的细胞后ERK和JNK均被磷酸化而激活Runx2使其磷酸化而促进成骨。多潜能干细胞C3H10T1/2中,Nell-1会将ERK和JNK途径同时激活;而在成肌细胞C2C12中,Nell-1只激活JNK1/2/3[10,28]。当JNK信号在成肌细胞中被阻断时,Nell-1的成骨作用减弱但没有完全丧失,这表明Nell-1信号仅部分通过JNK通路。而在骨肉瘤细胞中,Nell-1信号诱导的成骨分化需要完整的JNK信号。综上所述,MAPK信号在Nell-1信号过程中起着重要作用。 Nell-1还被证明可以直接调节Osterix,Osterix是特征明确的转录因子,对成骨细胞的形成至关重要。有趣的是,一项研究发现Osterix是Nell-1表达的负调节剂,但研究结果表明Osterix不会破坏Runx2与Nell-1启动子区域的结合,而是通过降低RNA聚合酶Ⅱ与Nell-1基因的结合来抑制Nell-1转录[27]。OSX与Runx2一起调节Nell-1基因的表达,两者相互拮抗保持Nell-1基因表达的生物学平衡。 Nell-1可以抑制脂肪生成,Hedgehog(HH)信号通路既能成骨又能抑制脂肪生成[29-30]。3种Hedgehog (HH)家族蛋白中的2种:Sonic Hedgehog(SHH) 和Indian Hedgehog(IHH)已被证明在骨骼发育过程中具有至关重要的作用。研究显示Nell-1增加HH信号分子的表达,腺病毒介导的Nell-1过表达也可显著增加HH信号标记物Ihh、Gli和Ptch1等的表达,提示Nell-1可能通过HH信号发挥其抗脂肪生成的作用[31]。HH拮抗剂处理人脂肪源性干细胞后,Nell-1的成骨作用减弱,而HH激动剂处理人脂肪源性干细胞后,Nell-1促进成骨和抑制脂肪生成的作用增强[32-33]。这些结果表明,HH信号通路在Nell-1的成骨作用中起作用,其具体机制尚未阐明。但有研究表明Runx2主要通过HH(IHH)信号通路调控软骨细胞分化和成熟[31]。 骨形态发生蛋白2主要通过结合其特异受体BMPRⅡ和BMPRI,继而激活Smad1/5/8和Smad4使其作用于其下游靶基因而发挥促进成骨细胞分化和矿化功能[34]。除了Smad通路,骨形态发生蛋白2也可以通过激活MAPK通路促进成骨细胞的分化[35]。不过,无论在那种类型的细胞中,Nell-1似乎都没有通过SMAD1/5/8途径启动细胞内信号[36]。这可能说明尽管Nell-1基因和骨形态发生蛋白2有相似的骨诱导效应,但二者之间的功能和机制是不同的。据报道,成纤维细胞生长因子2可以通过MAPK信号通路增加Runx2活性[35],其激活成纤维细胞生长因子受体1,显著增加Runx2的表达,造成小鼠颅缝的过早融合[37]。同样,Nell-1作用于成纤维细胞 1 h后可以大幅增加Runx2的磷酸化,而Ras siRNA可有效降低Runx2的磷酸化。这也说明Nell-1积极密切地参与了Runx2复杂的调控体系中,并在控制骨及软骨分化和骨形成方面扮演着极为关键的角色[38]。新的研究发现,Nell-1促进骨形态发生蛋白2,9的骨生成并抑制骨形态发生蛋白2,9引起的脂肪生成,研究者推测Nell-1这种作用可能是通过Wnt通路完成的[25,39]。 研究发现Nell-1作为Runx2的下游调控因子促进软骨细胞的分化和成熟。Runx2主要通过HH信号通路调控软骨细胞分化和成熟。前文已述Nell-1作为Runx2在成骨过程中的下游调控因子反过来诱导Runx2在成骨细胞谱系中的表达和活化。但与成骨过程中Nell-1和Runx2的互相调控不同,研究结果表明Nell不能诱导软骨细胞中Runx2的表达。与Nell-1可能只在促进骨形成的晚期发挥成骨作用不同,在软骨形成中受Runx2调控的Nell-1不仅参与软骨发育成熟的后期而且还参与软骨发育的起始[38]。进一步研究发现,Nell-1促进软骨形成活动的HH信号通路主要通过RUNX3介导,即RUNX3在Nell-1的下游发挥重要作用。该团队使用染色质免疫沉淀实验的方法确定了活化的T细胞核转录因子1( nuclear factor of activated T-cells cytoplasmic 1,Nfatc1)为Nell-1向Runx3信号转导的关键转录因子,阐明了Nell-1-Nfatc1-Runx3-Ihh级联反应[33]。 2.3 Nell-1促进骨生长及治疗骨质疏松的相关研究 2.3.1 Nell-1局部应用促进骨再生 经过多年研究,Nell-1已被证实为是一种可以有效促进骨组织生长的因子,局部应用对长骨、脊柱生长及颅缝闭合和软骨生长具有良好的促进作用。 (1)Nell-1增强大鼠临界性股骨大段骨缺损模型中的骨再生:LI等[40]以DBX(脱钙骨基质与透明质酸钠的混合物)为载体,将不同浓度的Nell-1蛋白与DBX混合后植入到大鼠临界性大段骨缺损模型中,结果发现在该模型中与磷酸缓冲液和BDX混合的对照组相比,两个不同剂量的Nell-1蛋白治疗组都比对照组表现出明显增多的再生骨量,而且随着蛋白浓度的增加,再生骨量有增多的趋势。 (2)Nell-1在脊柱融合模型中促进骨再生:LI等[41]通过冰冻干燥技术将PBS(对照)或Nell-1蛋白(2.5或5 μg)附着于50 mg的β-磷酸三钙颗粒并将其植入大鼠L4-5椎板及横突间进行脊柱融合手术,4周后Nell-1蛋白治疗组约75%的大鼠脊柱融合成功,且横突间新生骨的体积明显增大;而在没用应用Nell-1蛋白治疗的对照组中,只有25%的大鼠脊柱达到融合标准。 SIU等[42]在椎间融合器中植入以DBM(脱钙骨基质)为载体的Nell-1蛋白并将椎间融合器植入到绵羊脊柱中,结果发现含有Nell-1蛋白的椎间融合器可以显著提高绵羊的脊柱融合率和新生骨骨质量。添加0.6 g/L Nell-1后,脊柱融合率从50%(仅含DBM的对照组)提高到100%,且与对照组相比,椎间融合器内骨形成增加58%,骨密度则增加了47%。此外AGHALOO等[43]发现Nell-1置于载体聚乳酸-羟基乙酸共聚物(PLGA)中可以有效促进小鼠颅骨缺损的骨再生,这些实验都证实Nell-1局部应用可以有效促进骨生长。 2.3.2 Nell-PEG全身给药可促进小鼠骨折愈合及治疗骨质疏松 (1)Nell-1全身给药促进骨生长:Nell-1在动物模型的局部应用中取得了良好的促进骨生成的作用,如颅骨缺损、脊柱融合、股骨大段缺损模型等,但人们对于Nell-1全身应用对骨折愈合的影响知之甚少。TANJAYA等[44]学者应用Nell-1的聚乙二醇化产物NELL-PEG通过尾静脉注射全身递送Nell-1的方式来研究桡骨缺损模型中骨折修复的疗效。他们选择了10只10周龄的雌性小鼠制成小鼠前臂骨折模型,随机将小鼠分成治疗组与对照组,每组5只小鼠,然后对照组每周尾静脉注射PEG化磷酸盐缓冲盐液;治疗组注射NELL-PEG。通过术后第3周时的X射线观察到,治疗组全部小鼠在骨折处均观察到有纤维骨痂相连;对照组在该时间点均没有观察到骨痂形成。从第2周开始,两组的骨折处的骨密度逐渐增加,但治疗组增加的更加明显,且力学测试显示治疗组具有更好的骨强度与硬度;同时也发现骨折周围与骨折愈合相关的新生血管也较对照组多。为了探究NELL-PEG对未骨折骨的影响,分析了下腰椎的L6椎体。L6区域的microCT分析显示,与PBS组相比,NELL-PEG组中骨密度和成骨体积比(BV/TV)显著增加;此外,免疫组织化学显示骨钙蛋白表达也明显增加,这些结果表明NELL-PEG的全身应用不仅可以促进骨折愈合还有增加全身骨量的作用。这对应用Nell-1治疗全身骨疾病,如骨质疏松症等提供了理论依据。 此外,通过侧尾静脉连续5 d注射高剂量Nell-1 (6.25 mg/kg)的体内毒性实验未发现小鼠重要器官有任何病理变化。且聚乙二醇化后,Nell-1的药代动力学得到了提高,半衰期提高了3倍,也未观察到明显毒性[45-46],因此Nell-1在动物模型全身应用中是应当是安全的。 (2)Nell-1与骨质疏松:有学者发现体内缺少Nell-1分子的小鼠会发生骨质疏松症[47],其特征为成骨细胞骨形成与破骨细胞再吸收之间的不平衡,从而引起病理性骨量丢失、骨小梁改变和骨脆性增加,2010年全基因组单核苷酸多态性研究发现,Nell-1与女性骨质疏松症之间存在联系,此后,许多其他研究显示Nell-1和骨质疏松症的治疗有潜在联系。 KWAK等[48]在卵巢切除诱导的骨质疏松大鼠模型中,将冻干在0-50 mm磷酸三钙载体上的50 mL 600 g/L Nell-1注射到一侧股骨骨髓腔中,同时将PBS注射到对侧股骨中作为对照。微计算机断层扫描结果显示卵巢切除+PBS/磷酸三钙对照股骨在卵巢切除后2-8周显示骨量和骨矿物质密度的连续减少。相比之下,Nell-1处理的股骨明显减少卵巢切除诱导的骨吸收,在卵巢切除后8周时Nell-1处理股骨显示出与非骨质疏松大鼠股骨相似的骨量和骨密度水平。组织学显示与对照侧相比,Nell-1处理的股骨骨髓中骨细胞增加,骨髓中的脂肪细胞减少,免疫组织化学显示骨分化标记物骨桥蛋白和骨钙素的免疫染色增加,这说明Nell-1可以有效地增强骨髓中的原位骨生成,可用于预防和治疗骨质疏松。 JAMES等[49]将重组人Nell-1蛋白冻干到与透明质酸(HA)混合的磷酸三钙上并植入到骨质疏松绵羊腰椎椎体模型中,结果重组人Nell-1治疗显著增加腰椎的骨矿物质密度,骨量和皮质宽度;组织学分析显示植入部位周围骨面积和成骨细胞数量显著增加,破骨细胞数量减少;对骨组织的生物力学分析表明,重组人Nell-1处理组有更强的抗应力作用。 前文已述通过尾静脉注射的方法将Nell-1应用于性腺切除后诱导的骨质疏松症小鼠可明显提高疏松骨的骨密度,局部应用也会促进骨质疏松骨局部的骨生成。总之,Nell-1缺乏会引起骨质疏松,Nell-1在治疗骨质疏松中具有一定作用。 2.4 Nell-1与其他促生长因子、细胞等协同促进骨生长 2.4.1 Nell-1对骨形态发生蛋白的协同作用 见表1。 "
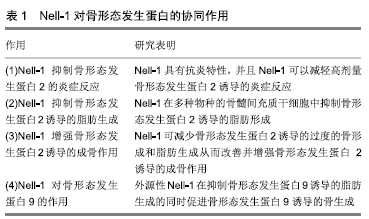

(1)Nell-1抑制骨形态发生蛋白2的炎症反应:骨形态发生蛋白2作为目前唯一被美国FDA批准应用于临床的促进骨再生及修复的骨形态发生蛋白,具有良好的促进骨生长的作用,但却会引起异位骨化、周围软组织炎性肿胀、术后脊神经炎等不良反应。动物模型先前已证实骨形态发生蛋白2治疗的剂量及其炎症反应呈正相 关[50]。但临床骨形态发生蛋白2的治疗起效剂量较高,通常超过诱导人骨形成所需的剂量[51],上述不良反应较难避免。许多研究表明,骨形态发生蛋白2诱导的炎症是软组织肿胀,炎性肿胀和术后脊神经炎的主要原因。SHEN等[52]在骨生成的研究中发现Nell-1可以减弱骨形态发生蛋白2诱导的炎症反应。为了验证这个发现,他们将14只12-14周的雄性Lewis大鼠随机分成4个实验组,将制成的PBS、骨形态发生蛋白2(总剂量0.8 mg)、Nell-1(总剂量0.8 mg)、Nell-1+骨形态发生蛋白2组合(骨形态发生蛋白2总剂量0.8 mg;Nell-1总剂量0.8 mg)饱和可吸收胶原海绵,植入到大鼠股骨表面,制作成大鼠FSD模型,在植入后第3,7和14天进行组织学分析以评估局部炎症。植入处染色切片后发现:单独使用Nell-1组炎症反应最轻;Nell-1+骨形态发生蛋白2组的炎症反应在植入3 d后与骨形态发生蛋白2组相比,炎症反应明显减少,在高倍视野中只能观察到很少的中性粒细胞而第14天的切片中中性粒细胞更少并且仅存在罕见的炎性细胞。在术后3-7 d的急性炎症期,骨形态发生蛋白2组中炎症早期的多核形炎症细胞显著增加,与Nell-1联合组并没有观察到多核形细胞的显著增多。在术后第7-14天的慢性炎症期,与Nell-1联合处理组相比慢性炎症期的单核炎症细胞在骨形态发生蛋白2单独处理组显著增多。总之,观察到用Nell-1可以减轻骨形态发生蛋白2在股骨模型中的促炎作用。免疫组织化学中观察到骨形态发生蛋白2诱导炎性因子肿瘤坏死因子α表达,而Nell-1可以抑制骨形态发生蛋白2对肿瘤坏死因子α的诱导。总的来说,研究的结果首次表明Nell-1具有抗炎特性,并且Nell-1可以减轻高剂量骨形态发生蛋白2诱导的炎症反应。 (2)Nell-1抑制骨形态发生蛋白2诱导的脂肪生成: 骨形态发生蛋白2在小鼠、狗的实验模型及人身上使用后会生成充满脂肪组织的大骨腔,而骨形态发生蛋白2和Nell联合使用较骨形态发生蛋白2单独使用骨量形成将会增加[53-54],脂肪生成的抑制可能与成骨的增加相对应。SHEN等[25]为了分析Nell-1对骨形态发生蛋白2诱导的脂肪生成的影响,选择了脂肪生成的2个重要的转录调节因子Pparg和C/Ebpa作为观察指标。术后2周取FSD标本,PPARg行免疫组织化学后观察。单独使用骨形态发生蛋白2处理的样本在缺损中心的骨小梁周围和小梁之间的细胞中表现出较强的Pparg染色;而Nell-1显著抑制Nell-1+骨形态发生蛋白2共处理动物中骨形态发生蛋白2诱导的Pparg表达。在脂肪形成条件下使用小鼠骨髓间充质干细胞系M2-10B4在体外复制上述实验:在第9天经油红O染色,骨形态发生蛋白2诱导的脂质积累增加超过5倍以上;然而,Nell-1的加入拮抗了骨形态发生蛋白2的促脂作用,显著降低了Pparg和C/Ebpa的表达。因为骨形态发生蛋白2对骨髓间充质干细胞的作用可能是物种依赖性的,并且由于细胞系可能与初代细胞反应不同,研究者用初代大鼠骨髓间充质干细胞和初代人骨髓间充质干细胞进行重复实验证实了Nell-1对骨形态发生蛋白2诱导的脂肪生成的抑制作用。这些结果表明Nell-1在多种物种的骨髓间充质干细胞中抑制骨形态发生蛋白2诱导的脂肪形成。 (3)Nell-1增强骨形态发生蛋白2诱导的成骨作用:从生物学观点来看,骨形态发生蛋白2与Runx2是通过两条相互补充的途径促进骨的再生,骨形态发生蛋白2作用于未分化的间充质干细胞而使向骨软骨母细胞系定向分化的细胞增多,这就意味着,可以作为Nell-1的靶细胞数目增多。接下来,Nell-1便会加强这些已经确定向骨软骨母细胞系转化的间充质干细胞的分化过程。 SHEN等[25]在经过PBS、骨形态发生蛋白2、Nell-1、Nell-1+骨形态发生蛋白2处理过的大鼠FSD模型中,在手术后8周对缺损部位进行了高分辨率2D放射摄影和3D microCT重建,发现用PBS处理的对照组股骨断端没有骨性结合;骨形态发生蛋白单独处理组出现骨融合,但是新形成骨的外周是一个薄的、连续的骨皮质外壳并且远远超出了原来的骨缺损边缘,内部的骨小梁薄而稀疏;经过Nell-1和骨形态发生蛋白2共处理的样本同样产生了骨融合,新形成的骨皮质厚,并且与骨形态发生蛋白2组相比内部骨小梁厚度高且间隔小。对骨量和组织体积的定量microCT分析显示与未治疗相比,所有治疗均显著增加骨量,然而,在仅骨形态发生蛋白2和Nell-1+骨形态发生蛋白2组之间没有观察到骨体积的统计学显著差异;但与单独的骨形态发生蛋白2处理组相比,Nell-1+骨形态发生蛋白2组显著降低了组织体积。此外,计算机模拟生物力学测试表明,与骨形态发生蛋白2组相比,Nell-1+骨形态发生蛋白2组骨强度增加。组织学观察骨形态发生蛋白2单独处理诱导骨折愈合,但新形成的骨骼中含有较多的脂肪组织,骨小梁稀疏且骨皮质薄弱,新生骨延伸至原始骨缺损边缘以外约4 mm;相反,Nell-1+骨形态发生蛋白2组产生紧密的小梁骨,主要局限于缺损部位。连续苏木精-伊红染色切片显示,Nell-1+骨形态发生蛋白2组与单独骨形态发生蛋白处理组相比骨小梁数量,周长和宽度增加,并且骨小梁间距减小。SHEN等又在成骨分化条件下用PBS、800 μg/L Nell-1和/或100 μg/L骨形态发生蛋白2培养M2-10B4细胞,Nell-1+骨形态发生蛋白2组相对于单独的Nell-1或骨形态发生蛋白2显著增加所有的成骨标志物,在初代的人骨髓间充质干细胞中重复这项实验显示Nell-1与骨形态发生蛋白2组合显著增加人骨髓间充质干细胞中的骨钙素和骨桥蛋白表达。 总之这些研究结果表明Nell-1可减少骨形态发生蛋白2诱导的过度骨形成和脂肪生成从而改善并增强骨形态发生蛋白2诱导的成骨作用。 (4)Nell-1对骨形态发生蛋白9的作用:在Nell-1对骨形态发生蛋白9诱导的骨髓间充质干细胞的成骨和成脂影响研究中发现[39],骨形态发生蛋白9能够在AdBMP9感染24 h后诱导间充质干细胞中Nell-1的表达,Nell-1的过表达增强了骨形态发生蛋白9诱导的晚期成骨分化,增强了间充质干细胞中Runx2、Osterix、骨钙素和骨桥蛋白的表达,抑制了早期成骨标志物碱性磷酸酶的表达。而骨形态发生蛋白9上调的Pparg和C/Ebpa脂肪形成相关因子的表达,被过表达的Nell-1所抑制。而外源Nell-1增强骨形态发生蛋白9诱导的骨形成的矿化和成熟,抑制了骨形态发生蛋白9在间充质干细胞中诱导的脂肪形成。总之该研究表明骨形态发生蛋白9能诱导Nell-1表达,而Nell-1的表达又能促进骨形态发生蛋白9诱导的成骨过程。在骨组织工程中,外源性Nell-1在抑制骨形态发生蛋白9诱导的脂肪生成的同时促进骨形态发生蛋白9诱导的骨生成。 2.4.2 人血管周围干细胞与Nell-1协同促进骨生长 LEE等[55]用将人血管周围干细胞和Nell-1与DBX结合后行卵巢切除骨质疏松大鼠L4-5椎板及横突间融合,结果发现0.75×109 L-1人血管周围干细胞+Nell-1 66.6 μg组脊柱融合率更高,达到了83.3%,明显高于其他对照组。这项实验明确证明干细胞和成骨因子(Nell-1)联合应用在促进骨质疏松大鼠成功进行脊柱融合中的巨大潜力。同时发现单独使用相同数量的人血管周围干细胞(0.25×109 L-1)在非骨质疏松大鼠中诱导100%融合,在骨质疏松大鼠中仅实现20%融合[56],这说明骨质疏松骨的再生能力受到严重损害。 2.4.3 Smoothened激动剂(SAG)与Nell-1协同促进骨生长 Hedgehog(HH)信号通路已被证明在骨骼生长发育中有至关重要的作用,SAG是激活HH信号通路的小分子物质。LEE等[57]为了证明SAG与Nell-1具有协同促进骨生长的作用,将两者结合至于PLGA载体中并植入到小鼠颅骨缺损模型中。结果发现SAG+Nell-1组相较其它对照组颅骨愈合最佳,缺损处骨量生成最多,骨密度最高,骨质最好。组织学显示SAG+Nell-1组编织骨和层状骨显著增加,缺损边缘增加最明显,同时该组新生骨周围的新生血管也明显增加。该实验也表明Hh信号激动剂SAG和Nell-1的组合具有潜在的治愈临界大小骨缺损的能力。 2.5 Nell-1促进软骨生长 LEE等[58]以壳聚糖纳米颗粒/藻酸盐凝胶复合物为载体将Nell-1植入到兔的股骨髁软骨缺损模型中,结果发现相比较PBS的对照组,植入Nell-1的缺损模型中再生软骨表面光滑,组织结构上也接近临近的天然软骨,免疫组织化学发现Nell-1组具有更多的Ⅱ型胶原蛋白(软骨基质主要胶原成分)且没有观察到成骨相关因子及肥大软骨细胞因子的表达。这说明Nell-1可以有效促进软骨生成并且避免形成异位骨化及形成低质量的肥大软骨细胞。 LI等[59]将Nell加入到含有转化生长因子β3、骨形态发生蛋白6生长因子的人血管周围干细胞培养基中进行培养,结果发现Nell-1在关节软骨和成熟软骨细胞中高度表达,而且软骨形成分化期间其在人血管周围干细胞中的表达逐渐增加。并且在人血管周围干细胞软骨形成分化过程中,聚蛋白多糖、胶原蛋白Ⅱ等软骨标志物的mRNA表达水平与Nell-1 mRNA的表达水平显著正相关,这表明Nell-1与软骨形成之间的高度相关性。与不含Nell-1的(仅含有转化生长因子β3、骨形态发生蛋白6生长因子)对照组相比,Nell-1可以加速转化生长因子β3及骨形态发生蛋白6诱导的人血管周围干细胞的软骨分化,在PCR分析中相比较对照组人血管周围干细胞的肥大、成骨、纤维化、凋亡的标志物显著减少。同时他们也发现Nell-1增加人血管周围干细胞中骨形态发生蛋白受体和转化生长因子β受体的表达水平,这也意味着促进软骨分化的受体增多。 这些都表明Nell-1不仅可以有效促进软骨再生,且与其他促生长因子联用时避免了软骨形成中细胞骨化、纤维化等不良反应。 2.6 Nell-1与骨组织相关肿瘤 2.6.1 Nell-1在骨良恶性肿瘤中的表达 SHEN等[60]研究发现Nell-1在良、恶性骨肿瘤中均有表达。Nell-1在骨样骨瘤和成骨细胞瘤两种良性骨肿瘤的中心病灶中均匀且显著增加,并且与成骨分化的标志物相关,但尚不清楚Nell-1是在肿瘤骨化中心对肿瘤形成起作用还是Nell-1仅仅是这些肿瘤的可靠标记。在骨肉瘤中Nell-1的免疫反应性表达不一,其染色染色程度与标本的骨化、钙化程度、标本厚度及肿瘤类型等均无明确关系,Nell-1的表达与成骨标志物也没有相关性,但在成纤维细胞型骨肉瘤细胞中表达最好。Nell-1在骨肉瘤中表达的多变性表明在肿瘤骨化之外可能具有其他的生物学作用。 2.6.2 Nell-1在软骨肿瘤中的表达 SHEN等[61]发现所有软骨相关肿瘤中Nell-1表达均增加,在内生软骨瘤,软骨肉瘤和软骨样骨肉瘤中观察到相似的表达程度并且与肿瘤的分级无关,良性和恶性软骨肿瘤细胞均表现出一致的Nell-1染色。但与发现Nell-1在骨肿瘤中表达一样,Nell-1在软骨肿瘤中是具有促进肿瘤形成的作用还是仅仅是肿瘤的可靠标记同样没有阐明。 "

| [1] MATSUHASHI S, NOJI S, KOYAMA E, et al. New gene, nel, encoding a M (r) 93 K protein with EGF-like repeats is strongly expressed in neural tissues of early stage chick embryos . Dev Dyn. 1995;203(2):212-222. [2] WATANABE TK, KATAGIRI T, SUZUKI M, et al.Cloning and characterization of two novel human cDNA(Nell-1 and NELL2) encoding proteins with six EGF-like repeats.Genomics.1996; 38(3):273-276. [3] MAEDA K, MATSUHASHI S, TABUCHI K, et al.Brain specific human genes,Nell-1 and NELL2,are predominantly expressed in neuroblastoma and other embryonal neuroepithlial tumors.Neuol Med Chir(Tokyo).2001.41(12):582-588; discussion 589. [4] LUCE MJ, BURROWS PD.The neuronal EGF-related genes Nell-1 and NELL2 are expressed in hemopoietic cells and developmentally regulated in the B lineage.Gene.1999;231(1-2): 121-126. [5] TING K, VASTARIDS H, MULLIKEN JB, et al.Human Nell-1 expressed in unilateral coronal synostosis.J Bone Miner Res. 1999;14(1):80-9. [6] ZHANG X, KURODA S, CARPENTER D, et al. Craniosynostosis in transgenic mice overexpressing Nell-1. J Clin Invest .2002;110: 861-870. [7] ZHANG X, CARPENTER D, BOKUI N, et al. Overexpression of Nell-1, a craniosynostosis-associated gene, induces apoptosis in osteoblasts during craniofacial development. J Bone Miner Res. 2003;18:2126-2134. [8] AGHALOO T, COWAN CM, CHOU YF, et al.Nell-1-induced bone regeneration in calvarial defects. Am J Pathol.2006;169:903-915. [9] AGHALOO T, JIANG X, SOO C, et al. A study of the role of Nell-1 gene modified goat bone marrow stromal cells in promoting new bone formation. Mol Ther. 2007;15:1872-1880. [10] COWAN CM, JIANG X, HSU T, et al. Synergistic effects of Nell-1 and BMP-2 on the osteogenic differentiation of myoblasts. J Bone Miner Res. 2007;22:918-930. [11] FAHMY-GARCIA S, VAN DRIEL M, WITTE-BUOMA J, et al. Nell- 1, HMGB1 and CCN2 enhance migration and vasculogenesis, but not osteogen⁃ ic differentiation compared to BMP2 .Tissue Eng Part A. 2018 Feb;24(3-4):207-218. [12] LI Y, YANG F, GAO M, et al. miR-149-3p Regulates the Switch between Adipogenic and Osteogenic Differentiation of BMSCs by Targeting FTO. Mol Ther Nucleic Acids. 2019;17:590-600. [13] DESAI J, SHANNON ME, JOHNSON MD, et al. Ne111-deficient mice have reduced expression of extracellular matrix proteins causing cranial and vertebral defects. Human Molecular Genetics. 2006;15:1329-1341. [14] TRUONG T, ZHANG X, PATHMANATHAN D, et al. Craniosynostosis-associated gene Nell-1 is regulated by Runx2. J Bone Miner Res. 2007;22:7-18. [15] DESAI J, SHANNON ME, JOHNSON MD, et al. Ne111-deficient mice have reduced expression of extracellular matrix proteins causing cranial and vertebral defects. Human Molecular Genetics. 2006;15:1329-1341. [16] SHANG N, BHULLAR KS, HUBBARD BP, et al. Tripeptide IRW initiates differentiation in osteoblasts via the RUNX2 pathway.Biochim Biophys Acta Gen Subj. 2019;1863(6):1138-1146. [17] YAN J, LI J, HU J, et al. Smad4 deficiency impairs chondrocyte hypertrophy via the Runx2 transcription factor in mouse skeletal development.J Biol Chem. 2018;293(24):9162-9175. [18] ZHANG X, KO T, PATHMANATHAN D,et al. Craniofacial bone defect in Nell-1 mutant mice associated with disregulated Runx2 and Osx expression. J Bone Miner Res. 2008;23(Suppl):S99. [19] ZHU Z, XIE Q, HUANG Y, et al. Aucubin suppresses Titanium particles mediated apoptosis of MC3T3 E1 cells and facilitates osteogenesis by affecting the BMP2/Smads/RunX2 signaling pathway.Mol Med Rep. 2018;18(3):2561-2570. [20] KNIPPENBERG M, HELDER MN, ZANDIEH DOULABI B, et al. Osteogenesis versus chondrogenesis by BMP-2 and BMP-7 in adipose stem cells. Biochem Biophys Res Commun. 2006;342(3): 902-908. [21] BU SY, HUNT TS, SMITH BJ. Dried plum polyphenols attenuate the detrimental effects of TNF-alpha on osteoblast function coincident with up-regulation of Runx2, Osterix and IGF-I.J Nutr Biochem. 2009;20(1):35-44. [22] HASSAN MQ, TARE RS, LEE SH, et al. BMP2 commitment to the osteogenic lineage involves activation of Runx2 by DLX3 and a homeodomain transcriptional network. J Biol Chem.2006;281: 40515-40526. [23] LI G, LIU J, WANG Y, et al.LNGFR targets the Wnt/β-catenin pathway and promotes the osteogenic differentiation in rat ectomesenchymal stem cells.Sci Rep.2017;7(1):11021. [24] SHEN J, JAMES AW, CHUNG J, et al.Nell-1 promotes cell adhesion and differentiation via Integrinβ1. J Cell Biochem. 2012; 113(12): 3620-3608. [25] SHEN J, JAMES AW, ZHANG X, et al.Novel Wnt Regulator NEL-Like Molecule-1 Antagonizes Adipogenesis and Augments Osteogenesis Induced by Bone Morphogenetic Protein 2. Am J Pathol. 2016;186(2):419-434. [26] JEON M, RAHMAN N, KIM YS. Wnt /β-catenin signaling plays a distinct role in methyl gallate-mediated inhibition of adipogenesis [J/OL].BiochemBiophys Res Commun.2016;479(1):22-27. [27] CHEN F, ZHANG X, SUN S, et al. Nell-1, an osteoinductive factor, is a direct transcriptional target of osterix. PLoS One. 2011;6(9). [28] BOKUI N, OTANI T, IGARASHI K, et al. Involvement of MAPK signaling molecules and Runx2 in the Nell-1-induced osteoblastic differentiation. FEBS Lett. 2008;582:365–371. [29] SPINELLA-JAEGLE S, RAWADI G, KAWAI S, et al. Sonic Hedgehog increases the commitment of pluripotent mesenchymal cells into the osteoblastic lineage and abolishes adipocytic differentiation.J Cell Sci.2001;114(Pt 11):2085e2094. [30] JAMES AW, PANG S, ASKARINAM A, et al. Additive effects of Sonic Hedgehog and Nell-1 signaling in osteogenic versus adipogenic differentiation of human adipose-derived stromal cells. Stem Cells Dev. 2012;21(12):2170e2178. [31] LI C, ZHENG Z, ZHANG X, et al.Nfatc1is a functional transcriptional factor mediating Nell-1-induced Runx3 upregulation in chondrocytes.Int J MolSci.2018;19(1): E168. [32] FONTAINE C, COUSIN W, PLAISANT M, et al. Hedgehog signaling alters adipocyte maturation of human mesenchymal stem cells. Stem Cells Dayt Ohio. 2008;26(4):1037e1046. [33] SINHA S, CHEN JK.Purmorphamine activates the Hedgehog pathway by targeting Smoothened. Nat Chem Biol. 2006;2(1): 29e30. [34] WANG RN, GREEN J, WANG Z, et al. Bone Morphogenetic Protein (BMP) signaling in development and human diseases. Genes Dis. 2014;1(1):87e105. [35] HYUK-SANG KWON, OAKKEE HONG,YANGGYO KANG,et al. Gemigliptin Inhibits IL-1ß–Induced Endothelial-Mesenchymal Transition via BMP2/Smad/MAPK/Runx2 Pathway. Diabetes. 2018;67. [36] BOKUI N, OTANI T, IGARASHI K, et al.Involvement of MAPK signaling molecules and Runx2 in the Nell-1-induced osteoblastic differentiation. FEBS Lett.2008;582:365–371. [37] JUNG JI, PARK KY, LEE Y, et al. Vitamin C-linker–conjugated tripeptide AHK stimulates BMP-2-induced osteogenic differentiation of mouse myoblast C2C12 cells. Differentiation. 2018;101:1-7. [38] LI C, JIANG J, ZHENG Z, et al. Neural EGFL-Like 1 Is a Downstream Regulator of Runt-Related Transcription Factor 2 in Chondrogenic Differentiation and Maturation.Am J Pathol. 2017; 187(5):963-972. [39] WANG J, LIAO J, ZHANG F, et al.NEL-like molecule-1 (Nell-1) Is regulated by bone morphogenetic protein 9 ( BMP9 ) and potentiates BMP9-induced osteogenic differentiation at the expense of adipogenesis in mesenchymal stem cells. Cell Physiol Biochem.2017;41(2):484-500. [40] LI W, ZARA JN, SIU RK,et al. Nell-1 enhances bone regeneration in a rat critical-sized femoral segmental defect model.Plast Reconstr Surg. 2011;127(2):580-577. [41] LI W, LEE M, WHANG J, et al.Delivery of lyophilized Nell-1 in a rat spinal fusion model.Tissue Eng Part A.2010;16(9):2861-2870. [42] SIU RK, LU SS, LI W, et al. Nell-1 protein promotes bone formation in a sheep spinal fusion model. Tissue Eng Part A. 2011; 17(7/8):1123-1135. [43] AGHALOO T, COWAN CM, ZHANG XL, et al.The Effect of Nell-1 and bone morphogenetic protein-2 on calvarial bone regeneration. J Oral Maxillofac Surg.2010;68(2):300-308. [44] TANJAYA J, LORD EL, WANG C, et al. The Effects of Systemic Therapy of PEGylated Nell-1 on Fracture Healing in Mice. Am J Pathol. 2018;188(3):715-727. [45] ZHANG Y, VELASCO O, ZHANG X, et al.Bioactivity and circulation time of PEGylated Nell-1 in mice and the potential for osteoporosis therapy. Biomaterials 2014;35:6614-6621. [46] KWAK JH, ZHANG Y, PARK J, et al. Pharmacokinetics and osteogenic potential of PEGylated Nell-1 in vivo after systemic administration. Biomaterials. 2015;57:73-83. [47] JAMES AW, SHEN J, ZHANG X,et al.Nell-1 in the treatment of osteoporotic bone loss.Nat Commun. 2015;6:7362. [48] KWAK J, ZARA JN, CHIANG M ,et al.Nell-1 injection maintains long-bone quantity and quality in an ovariectomy-induced osteoporotic senile rat model.Tissue Eng Part A.2013;19(3/4): 426-436. [49] JAMES AW, CHIANG M, ASATRIAN G,et al.Vertebralimplantation of Nell-1 enhances bone formation in an osteoporotic sheep model.Tissue Eng Part A.2016;22(11/12):840-849. [50] ZARA JN, SIU RK, ZHANG X, et al. High doses of bone morphogenetic protein 2 induce structurally abnormal bone and inflammation in vivo. Tissue Engineering Part A.Tissue Eng Part A. 2011;17(9-10):1389-1399. [51] LEE KB, MURRAY SS, TAGHAVI CE,et al. Bone morphogenetic protein-binding peptide reduces the inflammatory response to recombinant human bone morphogenetic protein-2 and recombinant human bone morphogenetic protein-7 in a rodent model of soft-tissue inflammation.Spine J. 2011;11(6):568-576. [52] SHEN J, JAMES AW, ZARA JN, et al. BMP2-Induced Inflammation Can Be Suppressed by the Osteoinductive Growth Factor Nell-1. Tissue Eng Part A. 2013;19(21-22):2390-2401. [53] SCIADINI MF, JOHNSON KD.Evaluation of recombinant human bone morphogenetic protein-2 as a bone-graft substitute in a canine segmental defect model. J Orthop Res.2000;18:289-302. [54] COWAN CM, JIANG X, HSU T,et al.Synergistic effects of Nell-1 and BMP-2 on the osteogenic differentiation of myoblasts. J Bone Miner Res. 2007; 22:918-930. [55] LEE S, ZHANG X, SHEN J, et al. Brief Report: Human Perivascular Stem Cells and\r, Nel\r, -Like Protein-1 Synergistically Enhance Spinal Fusion in Osteoporotic Rats. Stem Cells.2015;33(10):3158-3163. [56] CHUNG CG, JAMES AW, ASATRIAN G, et al. Human perivascular stem cell-based bone graft substitute induces rat spinal fusion. Stem Cells Transl Med 2014;3:1231-1241. [57] LEE S, WANG C, PAN HC, et al. Combining Smoothened Agonist (SAG) and NEL-like protein-1 (Nell-1) Enhances Bone Healing. Plast Reconstr Surg. 2017;139(6):1385-1396. [58] LEE M, SIU RK, TING K, et al.Effect of Nell-1 delivery on chondrocyte proliferation and cartilaginous extracellular matrix deposition.Tissue Eng Part A.2010;16(5):1791-1800. [59] LI CS, ZHANG X, PÉAULT B, et al. Accelerated Chondrogenic Differentiation of Human Perivascular Stem Cells with Nell-1. Tissue Eng Part A.2016;22(3-4):272-285. [60] SHEN J, LACHAUD G, KHADARIAN K, et al. Nell-1 expression in benign and malignant bone tumors.Biochem Biophys Res Commun.2015;460(2):368-374. [61] SHEN J, LACHAUD G, SHRESTHA S, et al.Nell-1 expression in tumors of cartilage.J Orthop.2015;12(Suppl 2):S223-229. |
| [1] | Tang Hui, Yao Zhihao, Luo Daowen, Peng Shuanglin, Yang Shuanglin, Wang Lang, Xiao Jingang. High fat and high sugar diet combined with streptozotocin to establish a rat model of type 2 diabetic osteoporosis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1207-1211. |
| [2] | Li Zhongfeng, Chen Minghai, Fan Yinuo, Wei Qiushi, He Wei, Chen Zhenqiu. Mechanism of Yougui Yin for steroid-induced femoral head necrosis based on network pharmacology [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1256-1263. |
| [3] | Wang Shiqi, Zhang Jinsheng. Effects of Chinese medicine on proliferation, differentiation and aging of bone marrow mesenchymal stem cells regulating ischemia-hypoxia microenvironment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1129-1134. |
| [4] | Hou Jingying, Yu Menglei, Guo Tianzhu, Long Huibao, Wu Hao. Hypoxia preconditioning promotes bone marrow mesenchymal stem cells survival and vascularization through the activation of HIF-1α/MALAT1/VEGFA pathway [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 985-990. |
| [5] | Liang Xueqi, Guo Lijiao, Chen Hejie, Wu Jie, Sun Yaqi, Xing Zhikun, Zou Hailiang, Chen Xueling, Wu Xiangwei. Alveolar echinococcosis protoscolices inhibits the differentiation of bone marrow mesenchymal stem cells into fibroblasts [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 996-1001. |
| [6] | Geng Yao, Yin Zhiliang, Li Xingping, Xiao Dongqin, Hou Weiguang. Role of hsa-miRNA-223-3p in regulating osteogenic differentiation of human bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1008-1013. |
| [7] | Lun Zhigang, Jin Jing, Wang Tianyan, Li Aimin. Effect of peroxiredoxin 6 on proliferation and differentiation of bone marrow mesenchymal stem cells into neural lineage in vitro [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1014-1018. |
| [8] | Zhu Xuefen, Huang Cheng, Ding Jian, Dai Yongping, Liu Yuanbing, Le Lixiang, Wang Liangliang, Yang Jiandong. Mechanism of bone marrow mesenchymal stem cells differentiation into functional neurons induced by glial cell line derived neurotrophic factor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1019-1025. |
| [9] | Pei Lili, Sun Guicai, Wang Di. Salvianolic acid B inhibits oxidative damage of bone marrow mesenchymal stem cells and promotes differentiation into cardiomyocytes [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1032-1036. |
| [10] | Hou Guangyuan, Zhang Jixue, Zhang Zhijun, Meng Xianghui, Duan Wen, Gao Weilu. Bone cement pedicle screw fixation and fusion in the treatment of degenerative spinal disease with osteoporosis: one-year follow-up [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(6): 878-883. |
| [11] | Li Shibin, Lai Yu, Zhou Yi, Liao Jianzhao, Zhang Xiaoyun, Zhang Xuan. Pathogenesis of hormonal osteonecrosis of the femoral head and the target effect of related signaling pathways [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(6): 935-941. |
| [12] | Xiao Fangjun, Chen Shudong, Luan Jiyao, Hou Yu, He Kun, Lin Dingkun. An insight into the mechanism of Salvia miltiorrhiza intervention on osteoporosis based on network pharmacology [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 772-778. |
| [13] | Liu Bo, Chen Xianghe, Yang Kang, Yu Huilin, Lu Pengcheng. Mechanism of DNA methylation in exercise intervention for osteoporosis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 791-797. |
| [14] | Deng Zhenhan, Huang Yong, Xiao Lulu, Chen Yulin, Zhu Weimin, Lu Wei, Wang Daping. Role and application of bone morphogenetic proteins in articular cartilage regeneration [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 798-806. |
| [15] | Chen Junyi, Wang Ning, Peng Chengfei, Zhu Lunjing, Duan Jiangtao, Wang Ye, Bei Chaoyong. Decalcified bone matrix and lentivirus-mediated silencing of P75 neurotrophin receptor transfected bone marrow mesenchymal stem cells to construct tissue-engineered bone [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 510-515. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||