Chinese Journal of Tissue Engineering Research ›› 2026, Vol. 30 ›› Issue (32): 8521-8528.doi: 10.12307/2026.453
Previous Articles Next Articles
Hydrogel scaffolds in tissue engineering for urethral repair and reconstruction
Qiu Jiajing1, 2, Huang Liqu2
- 1Nanjing Medical University, Nanjing 210000, Jiangsu Province, China; 2Department of Urology Surgery of Nanjing Children Hospital, Children Hospital Affiliated to Nanjing Medical University, Nanjing 210000, Jiangsu Province, China
-
Accepted:2026-01-29Online:2026-11-18Published:2026-04-29 -
Contact:Qiu Jiajing, MS candidate, Nanjing Medical University, Nanjing 210000, Jiangsu Province, China; Department of Urology Surgery of Nanjing Children Hospital, Children Hospital Affiliated to Nanjing Medical University, Nanjing 210000, Jiangsu Province, China -
About author:Huang Liqu, Associate chief physician, Associate professor, Department of Urology Surgery of Nanjing Children Hospital, Children Hospital Affiliated to Nanjing Medical University, Nanjing 210000, Jiangsu Province, China
CLC Number:
Cite this article
Qiu Jiajing, Huang Liqu. Hydrogel scaffolds in tissue engineering for urethral repair and reconstruction[J]. Chinese Journal of Tissue Engineering Research, 2026, 30(32): 8521-8528.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
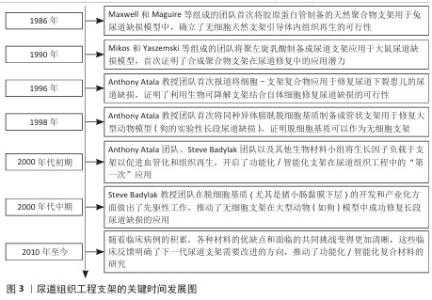
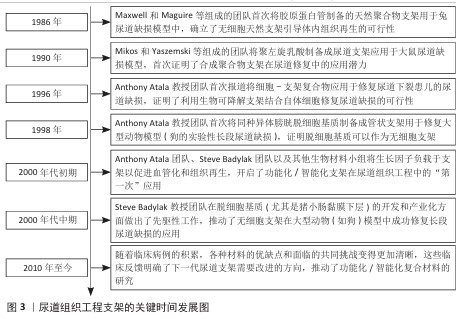
2.1 尿道组织工程支架的设计策略 2.1.1 尿道组织工程 尿道组织主要负责从肾脏过滤后尿液的储存和运输,膀胱作为尿液储存的储存库,输尿管和尿道是尿液运输的通道[8]。尿道组织受先天性或获得性异常影响损伤时,需要通过手术重建的方式来恢复尿道组织的正常功能。其中,尿道下裂和尿道狭窄是泌尿外科极为常见的疾病类型,尿道下裂是小儿泌尿生殖系统最常见的先天性畸形之一,发病率为1/200-1/300,并且逐年上升[9];尿道狭窄是一种常见的成人泌尿系统疾病,可由多种因素引起,例如创伤、炎症、先天性畸形和医学原因造成的损伤。近年来,组织工程技术的快速发展为尿道修复提供了新思路[8]。 组织工程学是一门以细胞生物学和材料科学相结合,进行体外或体内构建组织或器官的新兴学科,以形成在结构和功能上都可以替代天然组织的组织或器官[10]。再生医学的目标是通过开发一种在生物和机械特性上类似于天然组织的功能替代品来恢复组织和器官的功能,并力求最大限度地降低或避免机体发生免疫排斥反应[11]。 2.1.2 尿道支架 组织工程的三大基本要素分别是支架、种子细胞和生长因子,其中最关键是提供理想的支架。从宏观上看,生理尿道主要由一层薄的黏膜层和一层较厚的结缔组织层组成,黏膜层起到尿屏障作用,而结缔组织层较为疏松,能够容纳肌肉细胞、成纤维细胞和丰富的血管,为尿道提供机械支撑和营养[12-13]。因此,理想的尿道支架应该支持细胞的迁移和生长;此外,设计支架的内在物理性质、机械性能和形态特征非常重要,以便为细胞黏附、生长、迁移、增殖和分化提供特定的生物刺激,并指导受体组织细胞或植入细胞的精确重建。尿道的自然愈合过程涉及多个角色扮演者之间的相互作用,例如生长因子、细胞因子、细胞间接触、常驻细胞和迁移细胞的分泌体以及各种信号通路,因此,需要设计添加细胞或活性因子的尿道支架以增强生物活性,进而加速尿道的有序再生[14]。 综上所述,理想的尿道支架应具有以下特征:良好的细胞相容性和生物相容性;具有适宜的孔隙率,能够促进细胞迁移和生物分子扩散;为周围组织提供有效屏障;能够适应外科手术的机械强度,具有与天然尿道相似的力学性能以抵抗膀胱的周期性填充和排空,同时适应尿道的弹性环境;可降解性[10,15]。 迄今为止,应用于尿道组织工程的支架材料主要有3种选择:①脱细胞外基质:如小肠黏膜下层、膀胱脱细胞基质、脱细胞真皮基质、羊膜、尿道脱细胞基质;②天然衍生聚合物支架:如细菌纤维素、丝素蛋白、胶原蛋白和海藻酸钠;③合成聚合物支架:如聚乙醇酸、聚乳酸、聚乳酸-羟乙酸共聚物、聚己内酯材料。水凝胶因可变的几何形状、可调节的强度和与天然细胞外基质非常相似的多孔结构等优点,被广泛用于组织工程领域[15]。尿道组织工程支架的研究发展见图3。 "
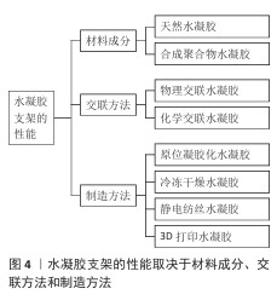
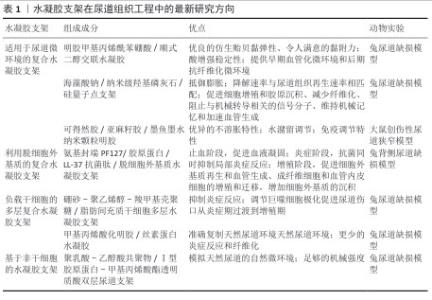
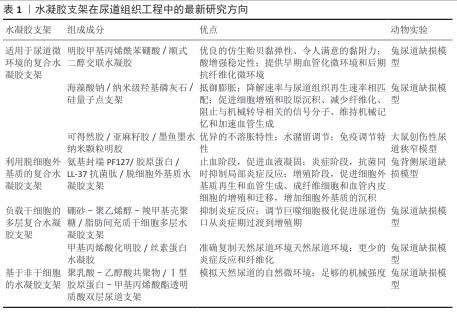
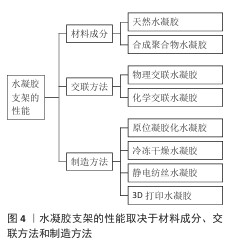
2.2 水凝胶支架的功能化改性 2.2.1 概述 在所有多细胞生物中,细胞由复杂且具有生物活性的支架来支持,即细胞外基质。细胞外基质由蛋白质和多糖的复杂混合物组成,所有这些蛋白质和多糖都以特定方式排列,从而赋予组织相应的特性[5]。作为一种三维聚合物网络,水凝胶支架与天然细胞外基质具有类似的多孔结构,允许细胞黏附和迁移,同时可递送和保留细胞因子,使营养物质和产物能够扩散,最终通过施加机械和生物影响来改变细胞的行为[16-17]。通常,水凝胶支架的性能主要由材料成分、交联方法和制造方法来决定,详见图4。 2.2.2 水凝胶支架的材料成分 依据材料来源,水凝胶支架可划分为天然水凝胶支架(常见的有蛋白质水凝胶支架、多糖水凝胶支架、DNA水凝胶支架、细胞外基质水凝胶支架等)与合成聚合物水凝胶支架(常见的有聚乙烯醇、聚丙烯酸、丙烯酸酯基水凝胶支架等)。蛋白质水凝胶支架在修复皮肤损伤[18]、输送药物以及提升力学性能方面起作用[19-20]。多糖水凝胶支架具备高黏度、低毒性与强吸附能力[21],在减轻局部炎症、降低氧化应激以及调控纤维蛋白溶解系统方面展现出治疗效果[22]。DNA水凝胶拥有可编程性、响应性与生物相容性等特性[23]。细胞外基质水凝支架胶保留了组织或器官的三维结构和一些天然纤维成分以及许多细胞生长因子,在组织工程与再生医学领域应用广泛[23]。天然水凝胶普遍具备良好的生物相容性和生物可降解性,但存在力学性能上的不足,例如刚度和拉伸强度往往较差,这些缺点限制了它们的实际应用范围。 常用的合成聚合物水凝胶支架有聚乙烯醇基水凝胶、聚丙烯酸基水凝胶、聚乙烯醇基水凝胶、聚己内酯基水凝胶等[23],其中聚己内酯基水凝胶因柔软、易于制造、生物降解期长、优异的生物相容性,已被广泛用作组织工程支架[24]。除此之外,还有聚氨酯、聚-N-异丙基丙烯酰胺和黏土纳米复合水凝胶支架等[25]。与天然水凝胶相比,合成聚合物水凝胶支架具有更稳定的性能、更好的力学性能以及可控的结构和性能,可以很好地解决水凝胶支架的力学和黏弹性问题[25],因此在尿道组织工程中成为研究的热点。 2.2.3 水凝胶支架的交联方法 交联方法可以改变水凝胶支架的力学性能。交联方法分为物理交联或化学交联。物理交联的水凝胶是通过非共价相互作用产生的,例如氢键、静电相互作用和疏水力等,物理交联过程具有可逆性。通过物理交联制备水凝胶最常用的方法包括冻融、立体复合物的形成、离子相互作用、氢键、结晶和通过疏水相互作用进行交联[6]。 化学交联水凝胶可以采用多种方式制备,具体包括使用化学交联剂、实施化学或辐射接枝反应、进行缩合反应或加成反应,也可以采用自由基聚合、酶促反应,或者利用高能辐射实现交联。此类交联过程促使聚合物链之间形成共价键,这种键合属于不可逆反应。共价交联结构会对水凝胶的机械强度性能产生显著影响,同时也决定了水凝胶的溶胀程度;此外,交联形成的网络结构还会影响各种颗粒在整个水凝胶基质中的传输行为[6]。 2.2.4 水凝胶的制造方法 制造方式也会对水凝胶的特性产生影响,并决定其应用方向。水凝胶的常见制造方式包括原位凝胶化、冷冻干燥、静电纺丝、3D生物打印等。原位凝胶化制造的水凝胶能通过微创注射送到需要的部位,不仅能提高注射部位细胞或/和药物的留存效果,同时可保护敏感药物不被酶分解破坏。冷冻干燥制造过程的参数设定会干扰内部晶体的演化进程,进而对水凝胶支架的物理属性(如微结构、溶胀率、降解情况等)产生显著影响;在细胞培养过程中,这类水凝胶还可形成大孔径以诱导产生平坦表面,从而促进细胞黏附。静电纺丝制造的水凝胶支架在生物医学领域的应用已较为广泛,该支架不仅能促进细胞黏附与增殖,还可封装细胞和药物以实现定向输送细胞与递送药物,从而促进组织修复。3D生物打印水凝胶拥有工艺简单、成本低、浪费少等优点,但设计出具有合理生物相容性的可打印生物墨水至今仍是一大挑战,尤其在打印加载细胞的复杂3D结构、用于功能性组织构建的场景中[24]。不同制造方式能够生产出具备不同特性的水凝胶支架,从而满足其在特定生物医学应用中的需求。 2.3 水凝胶支架在尿道组织工程中的最新研究方向 尽管天然水凝胶支架具有优异的生物活性,但力学性能的不足限制了其临床应用,因此,研究者转向合成聚合物与天然材料的复合策略,开发具有更好性能的复合水凝胶支架在尿道组织工程中已成为一种趋势。水凝胶支架在尿道组织工程中的最新研究方向,详见表1。 2.3.1 适用于尿道微环境的复合水凝胶支架 尿道微环境是一个用于尿道再生的组织工程新兴概念,即特殊设计的尿道组织工程支架、种子细胞、各种因子和宿主相互作用共同构成的再生微环境[26]。由工程组织移植物和患者有机体环境组成的再生微环境在恢复正常的生理组织功能方面起着至关重要的作用,适当的血管形成、复杂的组织结构以及移植物与宿主之间的功能整合是尿道组织工程的突出问题[26]。稳定的尿道微环境是尿道修复的一个关键因素,而尿道微环境受损则是尿道重建的一个固有障碍。 创伤后的尿道会因损伤重、替代组织稀缺、尿道微环境恶劣及记忆修复效果不佳而出现尿道狭窄的情况,不可避免地引发胶原过度沉积、瘢痕生成,导致修复不足甚至失败。当前已有多种支架被研发用于尿道修复,但这些支架的膨胀现象可导致机械强度降低,不利于尿道修复。此外,这些材料可能给机体带来二次创伤,或引发与炎症相关的免疫反应造成尿道狭窄与纤维化[27]。为解决上述问题,需研发具备适宜稳定性、高耐受性、强抗膨胀性及生物相容性的材料,以实现尿道的快速无瘢痕记忆修复。 HUA等[28]开发了一种尿道微环境适应性强的明胶甲基丙烯酰苯硼酸/顺式二醇交联水凝胶支架,该支架表现出优良的仿生贻贝黏弹性、令人满意的黏附力和酸增强稳定性,这些优点使支架能适应苛刻的尿道微环境,为无瘢痕尿道重建提供早期血管化微环境和后期抗纤维化微环境,这在生理愈合过程的体外分子机制和兔模型中的体内无瘢痕尿道重建中均得到了有效验证,该支架的开发为尿道损伤治疗提供了有前途的替代方案。 YANG等[29]构建了一种尿道微环境响应性的海藻酸钠-纳米羟基磷灰石-硅量子点复合水凝胶支架,纳米级羟基磷灰石和硅量子点交联能够显著提高支架的机械强度,并产生适度的活性氧,更重要的是,该复合支架可对尿道微环境做出反应,触发结构重构并抵御膨胀,通过增强胶原沉积、回忆机械记忆、减少纤维化和炎症、加速血管生成等方式实现无瘢痕记忆修复,为临床转化提供启发性的线索。 在长时间暴露于尿液环境时,传统水凝胶支架会面临过度肿胀、机械性能降低及生物稳定性差的风险,这极大限制了其在尿道微环境中的应用[29]。在排尿或插入导管时,尿道受压会导致水凝胶基质中的水分流失,进而引发水凝胶支架塌陷并丧失功能[30],因此,迫切需要开发适用于尿道组织工程的新型水凝胶支架,在抵御尿液引发的肿胀同时避免因尿道受压出现脱水情况。WU团队[31]在近期研究中设计出一种具备不溶胀特性与水潴留调节能力的生物凝胶,借助可得然胶从无规线圈结构过渡到三螺旋结构的温控多能级组装方式,构建出稳固的初级凝胶网络,保障水凝胶支架在尿液环境中的结构稳定性与不溶胀特性;将亚麻籽胶整合到凝胶网络中实现保水调节,进而避免尿道压迫过程中出现脱水现象;最后,加入具有天然免疫调节特性的墨鱼墨水纳米颗粒,用于调控尿道损伤区域的炎症微环境,最终得到的生物凝胶展现出优异的不溶胀特性、水潴留调节与免疫调节特性,通过适应尿路微环境和增强尿道修复有效预防尿道狭窄发生。这类专门针对尿液微环境设计的新型水凝胶,为解决传统水凝胶在尿道狭窄治疗中的局限提供了一种极具潜力的方案。 由此可见,创伤后尿道微环境的严重损伤是阻碍当前基于尿道组织工程水凝胶支架发展的固有障碍,因此,开发尿道微环境适应性或响应性的水凝胶支架仍是研究重点。 2.3.2 利用脱细胞外基质的复合水凝胶支架 近年来,来源于器官或组织细胞的脱细胞外基质,因优异的生物相容性、促进细胞增殖和迁移的能力以及促血管化特性引起了研究人员的广泛关注。脱细胞是组织工程研究领域的一种新技术,选择性地消除细胞而保留细胞外基质,这种方法不仅可以去除引起免疫原性反应的细胞和DNA成分,还可以保留细胞外基质的生化结构、生物活性和机械完整性[32]。脱细胞外基质水凝胶支架已被广泛应用于再生医学和组织修复[33],然而,这些支架的交联速度缓慢、力学强度弱和支撑性能差等不足仍然是需要面临的挑战[34]。 FANG等[35]将明胶与兔膀胱脱细胞外基质微粒和交联剂1-乙基-3-(3-二甲基-氨丙基-1-碳二亚胺)和N-羟基琥珀酰亚胺混合,制备出一款明胶-脱细胞外基质新型水凝胶支架,不仅弥补了明胶水凝胶支架缺乏生物活性的问题,还改善了脱细胞外基质水凝胶支架力学性能较差的弱点,在局部尿道伤口附近注射该支架可促进组织再生和血管形成。 FANG研究团队[36]创新性地设计了一种一体化全过程修复新型水凝胶支架,即氨基封端的PF127/胶原蛋白/LL-37@脱细胞外基质水凝胶支架,其中氨基封端的PF127水凝胶作为载体显著提升了稳定性,胶原蛋白具有促进血液凝固的作用,LL-37抗菌肽能够实现抗菌抗炎的功效,兔脂肪间充质干细胞的片状脱细胞外基质由于富含各种生长因子和营养物质,因此能够促进成纤维细胞和血管内皮细胞的增殖和迁移,进而实现细胞外基质再生和血管生成,增加细胞外基质的沉积,最终达到促进伤口愈合的目的;在体内实验中,通过兔动物模型证实该水凝胶支架调节了伤口部位的细胞增殖,阻止了瘢痕组织的形成。该结果表明,氨基封端的PF127/胶原蛋白/LL-37@脱细胞外基质水凝胶支架制备方便,具有巨大的临床应用潜力,为临床上治疗尿道损伤提供了新的见解。 利用脱细胞外基质的水凝胶支架属于天然水凝胶支架,因具有优良的生物相容性而被广泛应用于组织工程中,然而力学性能却存在局限性,因此,通过将脱细胞外基质水凝胶与其他物质混合的方式来弥补尿道支架在力学性能上的不足,是当前尿道组织工程的研究热点。 2.3.3 负载干细胞的多层复合水凝胶支架 干细胞具有自我更新能力和多能性,在特定的尿道微环境中,尿路上皮组织中的干细胞能够分化成各种细胞类型,并且它们旁分泌的各种生长因子和生物活性细胞因子能够刺激邻近细胞的生长。此外,干细胞还具有增强血管生成、减少纤维化以及减少炎症反应的作用[37-38],能用作人工组织移植物的一部分,来替换受损尿道[39]。因此,干细胞治疗在尿道组织工程中具有巨大的应用潜力,是近年热门的研究课题。 脂肪组织是动物和人类特别可靠的干细胞来源[40],在特定的尿道微环境中,脂肪间充质干细胞能够表现出分层的上皮样形态,增加上皮特异性蛋白表达,最终分化为尿路上皮样细胞[41]。在最新的研究中,JIN等[42]构建了一款搭载脂肪间充质干细胞的多层水凝胶支架,即聚乙烯醇-硼砂-聚乙烯醇-聚乙烯醇-羧甲基壳聚糖/脂肪间充质干细胞水凝胶支架,聚乙烯醇水凝胶因优良的生物相容性、可降解性、稳定性和良好的机械强度而被认为是尿道修复的理想支架候选;支架内层(即聚乙烯醇-硼砂层)具有自愈和抗菌特性,确保伤口即使在缝合时也能抵抗尿液剧烈的侵蚀;支架外层(即聚乙烯醇-羧甲基壳聚糖层)具有类似细胞外基质的结构,与脂肪间充质干细胞的协同作用产生了有利的再生微环境;组织学和功能学评价结果表明,该水凝胶支架抑制了尿液带来的炎症反应,通过调节巨噬细胞极化来促进尿道伤口从炎症期过渡到增殖期,为尿道无瘢痕愈合提供有利条件。该研究为尿道组织工程支架的设计提供了重要的见解。 颊黏膜组织是另一个有前途的干细胞来源[43]。在一项研究中,研究者使用兔脂肪干细胞和兔颊黏膜干细胞来设计上皮组织以模拟尿道上皮,同时选择甲基丙烯酸化明胶与丝素蛋白的组合作为支架材料,所形成的甲基丙烯酸化明胶/丝素蛋白水凝胶可用于人工尿道组织的生物打印,最终,上皮组织和水凝胶支架的构建体准确复制了天然尿道的特性;研究结果表明,与无干细胞组织相比,将这种载细胞的人工尿道组织整合到宿主生物体中,尿道组织产生的炎症反应和纤维化更少,这为临床研究开辟了新的道路[44]。 总而言之,干细胞和水凝胶的组合可以被视为一种很有前途的组织再生方法,但由于干细胞对细胞活动具有复杂影响,因此应更多地关注水凝胶支架的设计策略。 2.3.4 基于非干细胞的水凝胶支架 上皮组织多覆盖于一些接触外界环境的器官表层,例如口腔、眼睛、膀胱、肠道、尿道等,在保护、吸收、分泌及排泄过程中发挥关键作用[45]。尿道上皮组织损伤后会引发尿道狭窄(每10万人中约有1 200例患者),严重时甚至导致不孕[46]。上皮组织中的上皮细胞对尿道再生至关重要,其形成的连续上皮细胞层能提供抵御腐蚀效应和尿瘘的屏障,进而减少愈合过程中的炎症反应与纤维组织沉积[3],因此,上皮细胞的参与为尿道修复提供了有效的再生策略。此外,发育良好的尿道平滑肌层可提升尿道的力学性能,在拉伸运动与排尿过程中维持尿道结构的稳定状态,能够在一定范围内减少尿道狭窄情况的出现。那么,将平滑肌细胞接种到组织工程尿道中,实现尿道组织的再肌肉化处理,是一种既能修复损伤尿道又能避免尿道狭窄的有效方式[3]。 CHANG等[47]设计出一款能够分别加载兔尿道上皮细胞和兔尿道平滑肌细胞的聚乳酸-乙醇酸共聚物/Ⅰ型胶原蛋白-甲基丙烯酸酯透明质酸双层尿道支架,聚乳酸-乙醇酸共聚物及Ⅰ型胶原蛋白都是具有良好生物相容性的材料,研究人员使用静电纺丝技术制备了聚乳酸-乙醇酸共聚物/Ⅰ型胶原蛋白静电纺丝膜;甲基丙烯酸酯透明质酸水凝胶具有足够的机械强度;该研究将聚乳酸-乙醇酸共聚物/Ⅰ型胶原蛋白静电纺丝膜和甲基丙烯酸酯透明质酸水凝胶结合并成功制备了具有稳定结构的尿道组织修复支架,这种细胞与支架的融合实现了组织工程尿道模拟天然尿道的设计策略。该双层尿道支架在细胞实验中显示出令人满意的生物相容性,在修复兔尿道缺损的体内实验中展现了优异性能,表明它可能对人类尿道的临床修复同样有效,这为组织工程重建尿道提供了一种有前途的策略。 使用各种类型的种子细胞与生物材料相结合来构建组织工程尿道,这提供了一种重建尿道的新方法。迄今为止,各种细胞类型已被探索并应用于尿道再生领域,为临床治疗尿道损伤提供了新的研究方向。 2.4 水凝胶支架设计的未来方向 2.4.1 智能化设计 由于水凝胶的化学成分和性质具有广泛的改性可能性,同时它出色的生物相容性、无毒性、多功能性以及类细胞外基质特性,使得水凝胶成为一种有前途的组织工程材料,并应用于尿道修复的各种功能支架设计,为临床治疗尿道下裂及尿道狭窄等相关尿道重建疾病提供了新思路。尽管,当前水凝胶支架在尿道组织工程中的开发已经具有相当程度,但是它的临床开发潜能和临床转化潜力仍然值得进一步探究。越来越多的新型水凝胶支架的设计与开发正在进行,刺激响应性(例如pH值响应性、温度响应性、压力响应性)、工程化(例如基于工程化多肽材料、基于工程化细胞外囊泡)、无细胞化(例如基于间充质干细胞衍生的外泌体)等新型水凝胶支架的前瞻设计方向逐渐进入大家视野,这些智能化的水凝胶支架被设计出以满足市场和患者不断增长的需求。 (1)刺激响应性新型水凝胶:目前,刺激响应性的水凝胶支架正在被广泛开发,这种新型水凝胶能够在不同的环境中应对各类刺激,并发挥相应的功能。泌尿系统的功能之一是通过消除酸碱的重吸收和排泄来维持电解质平衡并调节局部酸碱性,使得尿道微环境具有相对恒定的pH值。创伤后,维持尿道微环境的pH值稳定是修复和再生尿道组织的强有力策略,这为尿道组织工程支架的设计提供了一个创新方向——pH值响应性水凝胶支架,其可能成为未来的发展热点。WANG等[48]成功构建了一款负载亲疏水结构纳米胶束的活性氧/pH值双响应水凝胶支架,以有效促进感染伤口愈合:首先,将壳聚糖在室温下接枝到α-硫酸的亲水端,再将姜黄素加入聚合物溶液中,通过超声自组装制备出稳定的亲疏水性纳米胶束;胶体通过甲基丙烯酸酐和4-羧苯基硼酸修饰,得到4-羧基苯基硼酸改性甲基丙烯酸化明胶;随后,通过席夫碱形成、硼酸酯键合和自由基聚合,将亲疏水性纳米胶束掺入4-羧基苯基硼酸改性甲基丙烯酸化明胶和氧化软骨素硫酸盐形成的水凝胶中,最终获得活性氧/pH值双响应水凝胶支架。结果表明,该新型水凝胶支架在高活性氧和低pH值环境下表现出卓越的抗氧化活性和强效的抗炎抗氧化性,可有效清除氧自由基并显著抑制细菌生长;体外实验表明,该支架具有优异的生物相容性,能有效促进细胞迁移,促进血管内皮细胞成管,清除细胞内活性氧,并促进巨噬细胞从M1型向M2型的极化;体内实验表明,该支架可显著降低炎症细胞因子水平,促进组织血管生成,并有效加速伤口愈合,说明这种活性氧/pH值双响应水凝胶支架为管理细菌感染伤口提供了有前景且创新的策略。然而,在临床转化方面,未来应进一步研究探讨该支架促进感染伤口修复的机制并开展临床试验。 随着组织工程与再生医学的发展,通过调控局部微环境来促进伤口愈合已经成为一个重要的研究目标。伤口愈合进程具有复杂性与动态性,生物组织在生理及病理层面的变化往往会伴随体温波动[49]。壳聚糖基热敏水凝胶属于智能聚合物材料,能针对环境温度的微妙变化实现可逆的溶胶-凝胶态转变,凭借独特的外部温度响应能力及优良的生物相容性,该材料在伤口修复领域展现出巨大应用潜力[50]。近年来,以热敏性水凝胶为基础的新型伤口闭合技术,不仅解决了传统方法的诸多不足,还为手术伤口愈合提供了更安全、更高效且更便捷的方案[51]。NI研究团队[52]研发出乳酸改性壳聚糖/壳聚糖/β-甘油磷酸酯热敏性水凝胶,添加乳酸改性壳聚糖后水凝胶具有更加规则的针状结构,使热敏性水凝胶的注射性得到大幅提升,同时该技术依托材料自身优良的生物相容性、组织黏附性与温度敏感性,不仅能加速伤口愈合进程,还能通过使用内窥镜注射针对手术切口完成注射水凝胶操作,降低患者更换敷料的频率,防止手术切口受到二次伤害。 水凝胶因可调节的柔软性、韧性、可拉伸性而成为开发柔性传感器的有力候选者[53],通过合理的设计,它们可以被赋予独特的特性,例如抗氧化和抗菌效果。WU等[54]通过将负载银的聚多巴胺纳米颗粒掺入热交联甲基丙烯酰胺壳聚糖和丙烯酰胺网络,最终成功研制出一款多功能水凝胶传感器。研究证实,该水凝胶显示出能对应变和压力做出有效反应的能力,可独立用作应变传感器或压力传感器;此外,由于水凝胶中存在壳聚糖和负载银的聚多巴胺纳米颗粒的生物活性成分,该水凝胶传感器表现出令人满意的生物相容性以及优异的抗氧化和抗菌活性。在泌尿系统中,阴茎海绵体的勃起可引起尿道腔变窄,这不利于尿道微环境中宿主细胞的生长,同时对创伤后尿道狭窄的重建也是一个挑战。压力响应性水凝胶支架的开发能够有效应对这一问题,支架在感受到尿道压力变化后做出响应,并表现出令人满意的抗菌和抗炎活性,进而促进切口的愈合。联合压敏性的机械激活递送机制,还能够实现细胞/药物的精确释放,进一步减弱术后疼痛、降低伤口感染风险并促进切口愈合,这为尿道组织工程支架的设计提供了一种全新的研究方向。 (2)工程化新型水凝胶:随着基因工程技术的发展,从头开始设计的工程化水凝胶将实现顺序调控,具有生物基序的工程化水凝胶因优异的生物相容性和可调性而备受关注。基于工程多肽的材料(如贻贝胶蛋白、弹性蛋白样多肽、丝蛋白、丝素蛋白、卷曲环结构域和亮氨酸拉链肽),通过非共价键(如氢键、π-π、静电相互作用和范德华相互作用)之间的相互作用形成动态且可逆的水凝胶系统[55]。不同的多肽水凝胶可以形成异质的多层结构,能有效地在每个阶段序贯释放所需的药物,同时在时空上调节愈合阶段之间的过渡[56]。 XIE等[56]开发了一种基于工程多肽AC10A和AC10ARGD的双层多功能AA-MAR水凝胶,用于骨髓炎治疗中有效杀菌和抗炎过程的时空调节。ZHU等[57]开发了一种双功能基因工程水凝胶,其中包含NAD依赖性脱乙酰酶sirtuins3负载的纳米载体和聚(癸二酸甘油)-共聚(乙二醇)/聚丙烯酸,该工程水凝胶不仅通过清除衰老相关分泌表型使衰老的骨髓来源干细胞恢复活力,还通过离子螯合创造了缺氧微环境,有效地实施了“由内而外”的策略来增强老年人的骨骼再生。 间充质干细胞释放的细胞外囊泡属于纳米级囊泡,直径在100 nm左右,内部含有microRNA(miRNA)、长链非编码RNA和环状RNA[58]。来源于多能干细胞的工程化细胞外囊泡是再生医学领域中的新兴概念,这类囊泡由胚胎干细胞和诱导多能干细胞释放,可参与细胞信号传导过程中所需生物活性分子的传递。工程化细胞外囊泡适用于再生医学、疾病诊断及水凝胶系统,还可用于针对特定部位的药物递送体系以及依托生物标志物提升图像对比度来开展的疾病诊断。含有工程化细胞外囊泡的水凝胶能构建出基于长效制剂的递送体系,它以可控的方式缓慢释放药物,进而提升组织修复效果[59]。 WANG等研究团队[58]通过控制甲基丙烯酰基的接枝比例合成了可注射明胶甲基丙烯酰水凝胶,同时构建了靶向miR-222工程化的细胞外囊泡,将工程化的细胞外囊泡加载到水凝胶中以构建可注射的负载工程化细胞外囊泡水凝胶贴剂,其中源自工程化的细胞外囊泡与干细胞来源的细胞外囊泡相比能避免伦理问题和免疫排斥问题,而显现出应有优势。该研究结果表明,工程化的细胞外囊泡能从机械水凝胶贴片中可控地释放出来,并精准输送到靶细胞中以改善缺血再灌注损伤,这个过程是通过调节机械信号激活、黏附相关蛋白质组装、打开细胞骨架力通道和核机械转导来实现的。这项研究加深了人们对工程化新型水凝胶的理解,也为人们提供了尿道组织工程支架设计的新方向。 (3)无细胞疗法新型水凝胶:间充质干细胞的裂解产物及分泌组能够调节免疫功能并推动组织修复,这使它成为无细胞治疗策略中一个具有发展前景的方向。相较于直接移植干细胞,无细胞策略具备显著优势,即能够规避细胞移植所带来的多种限制;此外,分泌组可在体外收集、加工并冻存以供后续使用,因此更易于实现标准化制备与长期贮存[60-61]。分泌组涵盖多种间充质干细胞分泌的生物活性分子,如细胞因子、趋化因子、miRNA、各类蛋白、生长因子以及细胞外囊泡(以外泌体和微囊泡为主),这些组分表现出广泛的生物效应,包括抑制炎症、抗细胞凋亡、阻止纤维化、抑制微生物、促进血管生成、抑制肿瘤发生以及协助组织再生等[62-63]。 近年来,以细胞外囊泡特别是外泌体为基础的无细胞治疗策略,因显示出更安全、更稳定的优势而展现出良好的应用前景。研究表明,源自间充质干细胞的外泌体属于纳米级囊泡,直径30-150 nm,不仅能运送多种生物活性成分,还可通过影响成纤维细胞向肌成纤维细胞的转分化过程以及调控免疫微环境来加速伤口愈合;与使用原代间充质干细胞相比,这类外泌体具备免疫原性低、不会引发肿瘤(因缺乏核结构)等特点,因而更适宜作为无细胞治疗的载体[64-65]。在各类来源中,脂肪源性干细胞因获取便捷、增殖能力强成为外泌体的重要来源。由脂肪源性干细胞提取的外泌体能够有效调节创面微环境中胶原代谢的平衡,一方面下调促纤维化因子表达,另一方面上调抗纤维化因子表达,最终实现瘢痕抑制[66]。 WANG等[67]制备了载有脂肪间充质干细胞来源外泌体的明胶甲基丙烯酰水凝胶,在兔耳增生性瘢痕模型中,该水凝胶表现出对增生性瘢痕相当大的预防和治疗潜力,具体表现为:水凝胶恢复了胶原蛋白代谢稳态、抑制了血管内皮生长因子介导的过度新生血管形成,这些发现突出了该水凝胶在调节细胞外基质重塑和血管生成的双重作用机制,提供了一种有前途的无细胞疗法来缓解增生性瘢痕。 ASHRAFI等[68]设计出一种由藻酸盐水凝胶和聚己内酯静电纺丝纳米纤维垫制成的多功能混合支架,将外泌体加载至工程支架中能被可控释放并输送到伤口部位。该研究证明,由纳米纤维支撑的水凝胶上加载外泌体时,可以在皮肤组织修复、再上皮化和胶原蛋白重塑中发挥更明显的作用,这归功于支架的亲疏水性结构能控制外泌体在伤口床中的释放,进而调节伤口微环境中的湿度,同时能防止外泌体的快速清除;此外,该结构还能增强细胞在纳米纤维复合材料上的附着。不仅如此,该研究还发现藻酸盐和外泌体能共同提供止血功效。由此可见,基于无细胞疗法新型水凝胶为尿道组织工程提供了一种有前途的支架设计策略。 2.4.2 临床转化 各项研究结果表明,水凝胶在各领域的创新应用具有很高的实施潜力。许多研究工作仍在进行中,旨在扩大基于水凝胶材料的泌尿系统治疗方法的成就。然而,组织工程的最终目标是将产品有效地应用于临床,尽管现在大部分尿道组织工程中所研发出的水凝胶支架在兔尿道缺损等动物模型中展现出优异的修复尿道潜力,但水凝胶支架的临床转化仍面临诸多挑战。 当前临床转化的主要瓶颈:①力学特性难以适应动态生理环境:天然尿道组织存在周期性的舒张与收缩以及需要耐受尿液流动,现有不少水凝胶支架的机械强度不足,在体内实际应力条件下易发生塌陷、断裂或变形,难以持续地保持管腔结构的稳定,进而影响组织再生过程,同时增加修复手术失败的可能性。②降解能力与组织再生速率不匹配:理想情况下,支架应在新生组织中具备一定力学性能的同时还需要同步降解。然而,在实际体内复杂条件(如pH值、温度、机械应力)下调控水凝胶的降解行为仍较为困难,降解太快会使支撑作用过早丧失;太慢则可能妨碍组织长入,甚至导致异物反应或长期炎症反应。③难以实现血管与神经的有效长入:尿道修复是否成功很大程度上依赖于及时的血运重建和神经再生,以保障营养供应和功能恢复。但目前的水凝胶材料在引导血管和神经有序长入支架内部方面的能力仍有限,常因缺乏内置微通道或高效的生长因子控释系统,而引起局部缺血或功能恢复缓慢。④生物活性调控与递送效率较低:水凝胶虽可作为生物活性成分的载体,但在实现生长因子、药物等精准、稳定、高效递送并保持其活性方面仍有待提升。此外,如何设计具有仿生结构(如各向异性、特定细胞黏附序列)以精确调控细胞行为,也是当前设计的难点。⑤产业化与法规审批存在挑战:水凝胶支架在批量生产中的一致性、无菌处理方式(需兼顾材料完整性和生物活性)、长期贮存稳定性以及符合医疗器械生产质量管理规范)的大规模制备工艺,均是临床转化必须解决的问题,并且水凝胶支架作为“复合型产品”(支架+生物活性成分/细胞),也面临复杂、长期且充满挑战的审批流程。 尽管,目前所制备的水凝胶支架向临床的转化与应用仍是一个重大问题,但这并非无法实现。Tengion公司的Neo-Urinary Conduit是一款将脂肪干细胞来源的平滑肌细胞接种在合成的、可生物降解支架上的组织工程尿道,应用于膀胱切除术后需要尿流改道的膀胱癌患者中,目前已知的1期临床试验中表现出与临床前动物实验一致的积极数据,这在组织工程尿道的临床转化中取得了重要进展[69]。 可能解决的方向:①材料复合与性能增强:通过将天然与合成高分子复合,或掺入纳米纤维、颗粒及微球等增强组分,构建复合型水凝胶,以大幅提高其机械性能、抗疲劳特性和结构稳定性,使支架能够适应尿道部位持续的力学环境。②仿生结构设计与先进制造:借助3D生物打印、静电纺丝等生物制造技术,制备具有多层、管状或各向异性等仿生构造的水凝胶支架,实现对孔结构、表面形貌及生物活性因子分布的精确控制,并通过表面改性促进细胞黏附和定向行为。③响应性材料与可控降解:设计可响应体内微环境变化的智能化水凝胶支架,使它的降解行为与组织再生速率相协调。通过调整交联方式和可降解单元的类型与密度,实现对材料降解过程的更精准调控。④基因工程辅助的材料构建:结合基因工程技术,从头设计和构建具备时序释放功能的水凝胶支架,实现在组织修复不同阶段按需释放特定生物活性分子,以促进伤口愈合。⑤无细胞治疗策略:将间充质干细胞分泌组中的活性成分负载于支架中,以提高其生物活性和植入安全性。⑥多学科协同与标准化体系建设:促进材料科学、生物力学、泌尿外科和监管科学等多领域深度融合,建立统一的支架性能评价体系、体外/体内模型以及符合医疗器械生产规范的制备与质控流程,推动其临床转化。同时,应发展更可靠的体外研究模型(如类器官模型、流体力学仿真系统)、制定标准化生产流程与个性化治疗策略,以提升水凝胶在尿道修复中的适用性,最终促进尿道结构与功能的完整重建。未来应着力推进水凝胶支架从基础研究走向临床实际应用,真正实现其在人体尿道修复与功能恢复方面的治疗价值。"
| [1] CANEPARO C, BROWNELL D, CHABAUD S, et al. Genitourinary Tissue Engineering: Reconstruction and Research Models. Bioengineering. 2021;8(7):99. [2] PASTOREK D, CULENOVA M, CSOBONYEIOVA M, et al. Tissue Engineering of the Urethra: From Bench to Bedside. Biomedicines. 2021; 9(12):1917. [3] NAAHIDI S, JAFARI M, LOGAN M, et al. Biocompatibility of hydrogel-based scaffolds for tissue engineering applications. Biotechnol Adv. 2017;35(5):530-544. [4] WIERZBICKA A, KRAKOS M, WILCZEK P, et al. A comprehensive review on hydrogel materials in urology: Problems, methods, and new opportunities. J Biomed Mater Res B Appl Biomater. 2023;111(3):730-756. [5] CAPANEMA NSV, MANSUR AAP, DE JESUS AC, et al. Superabsorbent crosslinked carboxymethyl cellulose-PEG hydrogels for potential wound dressing applications. Int J Biol Macromol. 2018;106:1218-1234. [6] MOURA LI, DIAS AM, CARVALHO E, et al. Recent advances on the development of wound dressings for diabetic foot ulcer treatment--a review. Acta Biomater. 2013; 9(7):7093-7114. [7] TYEB S, KUMAR N, KUMAR A, et al. Flexible agar-sericin hydrogel film dressing for chronic wounds. Carbohydr Polym. 2018;200:572-582. [8] SINGH A, BIVALACQUA TJ, SOPKO N. Urinary Tissue Engineering: Challenges and Opportunities. Sex Med Rev. 2018;6(1):35-44. [9] VAN DER HORST HJ, DE WALL LL. Hypospadias, all there is to know. Eur J Pediatr. 2017;176(4): 435-441. [10] SCHÄFER FM, STEHR M. Tissue engineering in pediatric urology - a critical appraisal. Innov Surg Sci. 2018;3(2):107-118. [11] CASARIN M, MORLACCO A, DAL MORO F. Tissue Engineering and Regenerative Medicine in Pediatric Urology: Urethral and Urinary Bladder Reconstruction. Int J Mol Sci. 2022;23(12):6360. [12] NIU Y, LIU G, CHEN C, et al. Urethral reconstruction using an amphiphilic tissue-engineered autologous polyurethane nanofiber scaffold with rapid vascularization function. Biomater Sci. 2020;8(8):2164-2174. [13] FRANCO RA, MIN YK, YANG HM, et al. Fabrication and biocompatibility of novel bilayer scaffold for skin tissue engineering applications. J Biomater Appl. 2013;27(5):605-615. [14] FARZAMFAR S, ELIA E, CHABAUD S, et al. Prospects and Challenges of Electrospun Cell and Drug Delivery Vehicles to Correct Urethral Stricture. Int J Mol Sci. 2022;23(18):10519. [15] JIN Y, YANG M, ZHAO W, et al. Scaffold-based tissue engineering strategies for urethral repair and reconstruction. Biofabrication. 2024;17(1). doi: 10.1088/1758-5090/ad8965. [16] CABRAL J, MORATTI SC. Hydrogels for biomedical applications. Future Med Chem. 2011;3(15):1877-1888. [17] EL-SHERBINY IM, YACOUB MH. Hydrogel scaffolds for tissue engineering: Progress and challenges. Glob Cardiol Sci Pract. 2013; 2013(3):316-342. [18] LEI H, ZHU C, FAN D. Optimization of human-like collagen composite polysaccharide hydrogel dressing preparation using response surface for burn repair. Carbohydr Polym. 2020;239:116249. [19] ANAMIZU M, TABATA Y. Design of injectable hydrogels of gelatin and alginate with ferric ions for cell transplantation. Acta Biomater. 2019;100:184-190. [20] KOH LD, CHENG Y, TENG CP, et al. Structures, mechanical properties and applications of silk fibroin materials. Progn Polyme Sci. 2015;46:86-110. [21] JANARTHANAN G, LEE S, NOH I. 3D Printing of Bioinspired Alginate‐Albumin Based Instant Gel Ink with Electroconductivity and Its Expansion to Direct Four‐Axis Printing of Hollow Porous Tubular Constructs without Supporting Materials. Adv Funct Mater. 2021; 31(45):2104441. [22] ZHAO Y, LI X, SUN N, et al. Injectable Double Crosslinked Hydrogel-Polypropylene Composite Mesh for Repairing Full-Thickness Abdominal Wall Defects. Adv Healthc Mater. 2024;13(15):e2304489. [23] FAN MH, PI JK, ZOU CY, et al. Hydrogel-exosome system in tissue engineering: A promising therapeutic strategy. Bioact Mater. 2024;38:1-30. [24] CAO H, DUAN L, ZHANG Y, et al. Current hydrogel advances in physicochemical and biological response-driven biomedical application diversity. Signal Transduct Target Ther. 2021;6(1):426. [25] YUAN N, SHAO K, HUANG S, et al. Chitosan, alginate, hyaluronic acid and other novel multifunctional hydrogel dressings for wound healing: A review. Int J Biol Macromol. 2023; 240:124321. [26] LENG W, LI X, DONG L, et al. The Regenerative Microenvironment of the Tissue Engineering for Urethral Strictures. Stem Cell Rev Rep. 2024;20(3):672-687. [27] MANGIR N, WILSON KJ, OSMAN NI, et al. Current state of urethral tissue engineering. Curr Opin Urol. 2019;29(4):385-393. [28] HUA Y, WANG K, HUO Y, et al. Four-dimensional hydrogel dressing adaptable to the urethral microenvironment for scarless urethral reconstruction. Nat Commun. 2023;14(1):7632. [29] YANG M, ZHANG Y, FANG C, et al. Urine-Microenvironment-Initiated Composite Hydrogel Patch Reconfiguration Propels Scarless Memory Repair and Reinvigoration of the Urethra. Adv Mater. 2022;34(14):e2109522. [30] HOU J, ZHANG X, WU Y, et al. Amphiphilic and Fatigue-Resistant Organohydrogels for Small-Diameter Vascular Grafts. Sci Adv. 2022; 8:eabn5360. [31] WU Z, ZHENG Z, LI C, et al. Nonswellable Curdlan/Linseed Gum Biogel with Water Retention Modulation: A Therapeutic Platform for Post-Traumatic Urethral Stricture Reconstruction. ACS Appl Mater Interfaces. 2025;17(28):40071-40081. [32] CRAPO PM, GILBERT TW, BADYLAK SF. An overview of tissue and whole organ decellularization processes. Biomaterials. 2011;32(12):3233-3243. [33] SALDIN LT, CRAMER MC, VELANKAR SS, et al. Extracellular matrix hydrogels from decellularized tissues: Structure and function. Acta Biomater. 2017;49:1-15. [34] PATI F, JANG J, HA DH, et al. Printing three-dimensional tissue analogues with decellularized extracellular matrix bioink. Nat Commun. 2014;5:3935. [35] FANG W, YANG M, JIN Y, et al. Injectable Decellularized Extracellular Matrix-Based Bio-Ink with Excellent Biocompatibility for Scarless Urethra Repair. Gels. 2023;9(11):913. [36] FANG W, WANG Y, ZHANG K, et al. An Integrated Whole-Process Repair System with Programmed Regulation of Healing Performance Facilitates Urethral Wound Restoration and Scarless Reconstruction. Adv Sci (Weinh). 2025;12(6):e2409930. [37] SHARMA AK, CHENG EY. Growth factor and small molecule influence on urological tissue regeneration utilizing cell seeded scaffolds. Adv Drug Deliv Rev. 2015;82-83:86-92. [38] CAPLAN AI, CORREA D. The MSC: an injury drugstore. Cell Stem Cell. 2011;9(1):11-15. [39] CULENOVA M, ZIARAN S, DANISOVIC L. Cells Involved in Urethral Tissue Engineering: Systematic Review. Cell Transplant. 2019; 28(9-10):1106-1115. [40] BACAKOVA L, ZARUBOVA J, TRAVNICKOVA M, et al. Stem cells: their source, potency and use in regenerative therapies with focus on adipose-derived stem cells - a review. Biotechnol Adv. 2018;36(4):1111-1126. [41] ZHANG M, PENG Y, ZHOU Z, et al. Differentiation of human adipose-derived stem cells co-cultured with urothelium cell line toward a urothelium-like phenotype in a nude murine model. Urology. 2013;81(2): 465.e15-465.e22. [42] JIN Y, WANG Y, YANG R, et al. Multilayered hydrogel scaffold construct with native tissue matched elastic modulus: A regenerative microenvironment for urethral scar-free healing. Biomaterials. 2025;312:122711. [43] BARASA P, BUIVYDAS A, BALTRUKONYTĖ E, et al. Differentiation of Rabbit Stem Cells on Gelatin for Tissue Engineering Applications. IFMBE Proceedings 19th Nordic-Baltic Conference on Biomedical Engineering and Medical Physics. 2023:278-286. doi:10.1007/978-3-031-37132-5_35. [44] BARASA P, SIMOLIUNAS E, GRYBAS A, et al. Development of multilayered artificial urethra graft for urethroplasty. J Biomed Mater Res A. 2025;113(1):e37796. [45] ZHAO M, WANG C, JI C, et al. Ascidian-Inspired Temperature-Switchable Hydrogels with Antioxidant Fullerenols for Protecting Radiation-Induced Oral Mucositis and Maintaining the Homeostasis of Oral Microbiota. Small. 2023;19(27):e2206598. [46] WANG L, WANG K, YANG M, et al. Urethral Microenvironment Adapted Sodium Alginate/Gelatin/Reduced Graphene Oxide Biomimetic Patch Improves Scarless Urethral Regeneration. Adv Sci (Weinh). 2024;11(2):e2302574. [47] CHANG M, TAN Q, BIAN G, et al. A double-layer PLGA/CoI-MeHA tissue engineering scaffold for urethral reconstruction. Front Pharmacol. 2025;16:1555183. [48] WANG J, LIN Y, FAN H, et al. ROS/pH Dual-Responsive Hydrogel Dressings Loaded with Amphiphilic Structured Nano Micelles for the Repair of Infected Wounds. Int J Nanomedicine. 2025;20:8119-8142. [49] SKOK K, DUH M, STOZER A, et al. Thermoregulation: A journey from physiology to computational models and the intensive care unit. Wires Mech Dis. 2021;13:1513. [50] ABDOLLAHI A, MALEK-KHATABI A, RAZAVI MS, et al. The recent advancement in the chitosan-based thermosensitive hydrogel for tissue regeneration. J Drug Deliv Sci Technol. 2023;86:104627. [51] WANG J, HUANG L, WU E, et al. Recent Advances on Chitosan-Based Thermosensitive Hydrogels for Skin Wound Treatment. Biology (Basel). 2025;14(6):619. [52] NI PXZ, YE S, LI RP, et al. Chitosan thermosensitive hydrogels based on lyophilizate powders demonstrate significant potential for clinical use in endoscopic submucosal dissection procedures. Int J Biol Macromol. 2021;184:593-603. [53] WANG Z, WEI H, HUANG Y, et al. Naturally sourced hydrogels: emerging fundamental materials for next-generation healthcare sensing. Chem Soc Rev. 2023;52(9):2992-3034. [54] WU G, SHI W, LIU M, et al. Multifunctional Strain/Pressure Sensor Based on Ag@Polydopamine Nanohybrid Methacrylamide Chitosan/Polyacrylamide Hydrogel for Healthcare Monitoring. ACS Appl Mater Interfaces. 2025;17(6):9879-9890. [55] ZHANG K, ZHANG K, YANG PP, et al. Peptide-based nanoparticles mimic fibrillogenesis of laminin in tumor vessels for precise embolization. ACS Nano. 2020;14:7170-7180. [56] XIE X, WEI J, ZHANG B, et al. A self-assembled bilayer polypeptide-engineered hydrogel for spatiotemporal modulation of bactericidal and anti-inflammation process in osteomyelitis treatment. J Nanobiotechnology. 2022;20(1):416. [57] ZHU Y, SUN L, HOU M, et al. An “inside-out”-guided genetically engineered hydrogel for augmenting aged bone regeneration. Bioact Mater. 2025;51:318-332. [58] WANG Y, MENG D, SHI X, et al. Injectable hydrogel with miR-222-engineered extracellular vesicles ameliorates myocardial ischemic reperfusion injury via mechanotransduction. Cell Rep Med. 2025; 6(3):101987. [59] WANG AYL, KAO HK, LIU YY, et al. Engineered extracellular vesicles derived from pluripotent stem cells: a cell-free approach to regenerative medicine. Burns Trauma. 2025;13:tkaf013. [60] SIPOS F, MŰZES G. Controversies in therapeutic application of mesenchymal stem cell-derived secretome. Biocell. 2022;46(4):903-906. [61] ZUNUNI VAHED S, HEJAZIAN SM, BAKARI WN, et al. Milking mesenchymal stem cells: Updated protocols for cell lysate, secretome, and exosome extraction, and comparative analysis of their therapeutic potential. Methods. 2025;238:40-60. [62] HOSSEINIYAN KHATIBI SM, KHEYROLAHZADEH K, BARZEGARI A, et al. Medicinal signaling cells: a potential antimicrobial drug store. J Cell Physiol. 2020;235(11):7731-7746. [63] ARAVINDHAN S, EJAM SS, LAFTA MH, et al. Mesenchymal stem cells and cancer therapy: insights into targeting the tumour vasculature. Cancer Cell Int. 2021;21(1):158. [64] GONG X, ZHAO Q, ZHANG H, et al. The Effects of Mesenchymal Stem Cells-Derived Exosomes on Metabolic Reprogramming in Scar Formation and Wound Healing. Int J Nanomedicine. 2024;19:9871-9887. [65] LI S, LI Y, ZHU K, et al. Exosomes from mesenchymal stem cells: Potential applications in wound healing. Life Sci. 2024;357:123066. [66] ZHOU Y, ZHANG XL, LU ST, et al. Human adipose-derived mesenchymal stem cells-derived exosomes encapsulated in pluronic F127 hydrogel promote wound healing and regeneration. Stem Cell Res Ther. 2022; 13(1):407. [67] WANG H, GAO X, ZHAO Y, et al. Exosome-Loaded GelMA Hydrogel as a Cell-Free Therapeutic Strategy for Hypertrophic Scar Inhibition. Clin Cosmet Investig Dermatol. 2025;18:1137-1149. [68] ASHRAFI F, EMAMI A, SEFIDBAKHT S, et al. Accelerated healing of full-thickness skin wounds by multifunctional exosome-loaded scaffolds of alginate hydrogel/PCL nanofibers with hemostatic efficacy. Int J Biol Macromol. 2025;307(Pt 4):142271. [69] KATES M, SINGH A, MATSUI H, et al. Tissue-engineered urinary conduits. Curr Urol Rep. 2015;16(3):8. |
| [1] | Jin Yuan, Zhou Jiabing. Applications and advances of hydrogels in bone tissue engineering repair related to sports injuries [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(32): 8512-8520. |
| [2] | Zheng Ying, Li Mengyao, Zheng Fanfan, He Zhao, Zhang Ning, Zou Jialun, Li Youlei, Gao Feng. Mechanism of action of extracellular vesicles loaded with biomaterials in repairing spinal cord injury [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(32): 8544-8554. |
| [3] | Fan Xiao, Li Huiyun, Dou Fuguo, Zhang Nan, Zhang Xinyan. Copper phosphate nanohydrogel dressing promotes skin wound healing in mice [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(32): 8413-8419. |
| [4] | Li Xuanze, Fang Hanhong, Xu Zhe. Preparation and cytocompatibility of sodium alginate-hydroxyapatite-graphene oxide hydrogels [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(32): 8420-8426. |
| [5] | Liu Bangding, Tang Yongliang, Li Ni, Ren Bo. Quercetin-loaded hydrogel materials for treatment of infected bone defects [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(32): 8427-8435. |
| [6] | Chen Shichao, Deng Yunyi, Zhao Renshengjie, Yu Ke, Li Guangwen. Antibacterial properties of photocrosslinkable hydrogel loaded with quercetin-silver nanoparticles for infected wounds [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(32): 8436-8442. |
| [7] | Ding Hao, Gao Yuan, Li Bin, Yu Rui, Wang Jianru, Sun Yudie, Wang Xuanyang, Zhang Wenping, Zhu Mingjun. Potential and application prospects of combined treatment of acute myocardial infarction with hydrogel cardiac patches and traditional Chinese medicine [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(32): 8479-8486. |
| [8] | Fei Xiaoyuan, Xu Jiao, Shi Hui. Application strategies of DNA hydrogels for tissue repair [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(32): 8487-8495. |
| [9] | Li Minghui, Qie Haoyu, Pan Min, Bi Ruijie, Lyu Xiaomeng, Zhang Haoya, Han Yifei. Hydrogel-based drug delivery systems for rheumatoid arthritis treatment [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(32): 8496-8501. |
| [10] | Meng Yihao, Zhang Shuai. Application of self-healing hydrogels for sports injury prevention and rehabilitation#br# [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(32): 8502-8511. |
| [11] | Fang Yulu, Yi Bingcheng, Shen Yanbing, Tang Han, Zhang Yanzhong. Potential of corn husk fibers reinforced chitosan-based hydrogels in cartilage tissue engineering scaffold [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(34): 5493-5501. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||