Chinese Journal of Tissue Engineering Research ›› 2025, Vol. 29 ›› Issue (8): 1650-1658.doi: 10.12307/2025.346
Previous Articles Next Articles
Role of cellular autophagy in cerebral ischemic injury and the regulatory mechanism of traditional Chinese medicine
Zhou Panpan1, Cui Yinglin2, Zhang Wentao2, Wang Shurui2, Chen Jiahui1, Yang Tong2
- 1The Second Clinical Medical College of Henan University of Chinese Medicine, Zhengzhou 450002, Henan Province, China; 2Henan Provincial Hospital of Traditional Chinese Medicine, Zhengzhou 450002, Henan Province, China
-
Received:2024-03-04Accepted:2024-05-11Online:2025-03-18Published:2024-07-06 -
Contact:Cui Yinglin, Master, Chief physician, Doctoral supervisor, Henan Provincial Hospital of Traditional Chinese Medicine, Zhengzhou 450002, Henan Province, China -
About author:Zhou Panpan, MD candidate, The Second Clinical Medical College of Henan University of Chinese Medicine, Zhengzhou 450002, Henan Province, China -
Supported by:Henan Province Chinese Medicine Scientific Research Special Project, Nos. 2023ZY1007, 212102311123, 2019ZY2003, and 2017ZY1020 (to CYL); Research on the Current Situation of Chinese Medicine Health Tourism Development and Countermeasures in Henan Province under the Perspective of Embodiment, No. TCM2022018 (to YT); the Second National Famous Chinese Medicine Practitioners Inheritance Studio Construction Project of the National Administration of Traditional Chinese Medicine in 2022, No. [2022]245 (to CYL)
CLC Number:
Cite this article
Zhou Panpan, Cui Yinglin, Zhang Wentao, Wang Shurui, Chen Jiahui, Yang Tong . Role of cellular autophagy in cerebral ischemic injury and the regulatory mechanism of traditional Chinese medicine[J]. Chinese Journal of Tissue Engineering Research, 2025, 29(8): 1650-1658.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
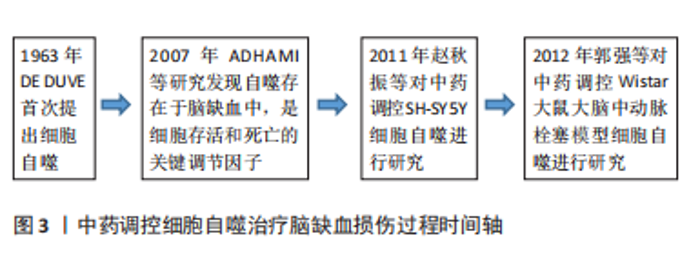
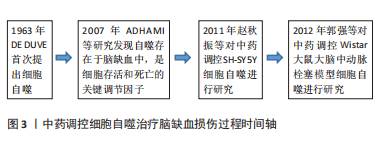
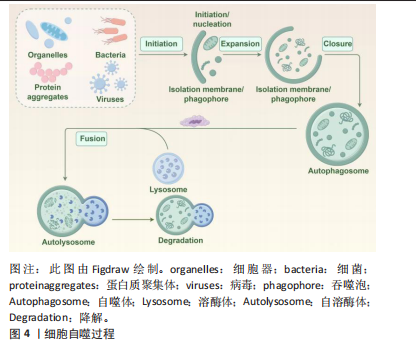
1963年比利时科学家DE DUVE首次提出“细胞自噬”这一概念[10],近年来被视为是细胞凋亡、坏死外的第3种死亡方式,并得到深入研究和发展(图3)。根据自噬机制及功能,将其分为巨自噬、微自噬及分子伴侣介导的自噬3类。自噬过程包括自噬体起始、延伸、成熟及与溶酶体结合等过程。自噬激活后在Ⅲ型磷脂酰肌醇3-激酶(class Ⅲ phosphoinositide 3-kinase,PI3K-Ⅲ)复合物、ULK复合物2个大分子物质参与下形成自噬体前膜,在自噬相关蛋白家族及其他泛素样反应的帮助下延伸包裹内容物,形成自噬小体,之后自噬体膜与溶酶体膜形成自噬溶酶体,所携带的底物被降解为氨基酸、脂肪酸等小分子物质[11-12]。正常情况下,自噬能清除受损的细胞器和变性的蛋白质,维持细胞内环境的稳态。病理状态下,自噬体的形成与自噬通量不等,导致自噬不足或自噬过度,则加重缺血性脑卒中后脑损伤[13]。因此,如何调控自噬,使其维持在有利水平是脑缺血损伤治疗的关键。细胞自噬过程见图4。"
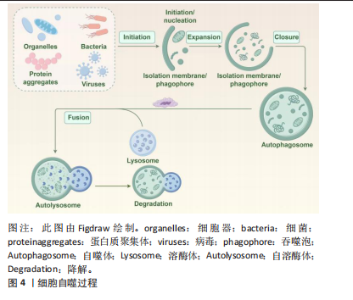
2.2 细胞自噬过程关键蛋白 Beclin-1是首个被发现的自噬调控基因,又称自噬相关基因6,与PI3K-Ⅲ结合形成Beclin-1-Vps34,通过增加自噬关键蛋白在Beclin-1-Vps34复合物上的积累从而启动自噬[14-15],故其表达量与自噬呈正相关。 LC3即微管相关蛋白1轻链3(microtubule-associated protein 1 light chain 3),是自噬相关蛋白8的哺乳动物同源蛋白,在半胱氨酸蛋白酶自噬相关蛋白4的作用下转化为LC3-Ⅰ,接着与磷脂酰乙醇胺结合被转化为LC3-Ⅱ,附着于自噬体膜上[16-17]。因此,LC3-Ⅱ的形成标志着自噬体形成。 p62又称SQSTM蛋白,是负责溶酶体降解的自噬适配器,内部含有多个结构域,可将泛素化的蛋白传递给LC3,并定位于自噬体上,最终在溶酶体中降解,故自噬"
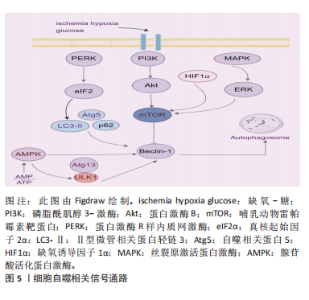
发生时p62表达下降[18-19]。 2.3 自噬相关信号通路 2.3.1 PI3K/Akt/mTOR信号通路 PI3K/Akt是一种经典的自噬信号传导通路,哺乳动物雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR)为其下游信号[20]。PI3K分为Ⅰ,Ⅱ,Ⅲ型,其中Ⅲ型PI3K与Beclin-1形成复合物,从而启动自噬。mTOR在细胞生长、增殖和自噬方面发挥重要调控作用[21]。mTOR分为mTOR复合物1(mTORC1)和mTOR复合物2(mTORC2),其中mTORC1是自噬的主要调节靶点[22]。mTORC1被p-Akt激活后磷酸化ULK1和自噬相关蛋白13可抑制自噬的发生,相反,使用雷帕霉素靶蛋白抑制剂则可诱导自噬的发生[23]。 2.3.2 PERK-eIF2α信号通路 蛋白激酶R样内质网激酶(PRKR-like endoplasmic reticulum kinase,PERK)是一种位于内质网膜上具有丝氨酸/苏氨酸结构域的Ⅰ型跨膜蛋白,eIF2α是PERK的下游信号分子[24]。缺氧刺激时,内质网分子伴侣葡萄糖调节蛋白78与PERK解离,蛋白激酶R样内质网激酶磷酸化后磷酸化下游真核起始因子2α,在p62、自噬相关蛋白5、LC3-Ⅱ等信号分子的作用下,激活细胞自噬[25]。反之,抑制PERK/eIF2α信号通路可减少自噬相关蛋白Beclin-1的过度激活,抑制自噬水平[26]。 2.3.3 AMPK-mTOR信号通路 腺苷酸活化蛋白激酶(adenosine monophosphate-activated protein kinase,AMPK)是一种AMP活化的丝氨酸/苏氨酸蛋白激酶,由催化亚基α和调节亚基β、γ组成,是主要的能量传感器之一。当AMP/ATP比值上调时,AMPK磷酸化,从而激活磷酸化TSC2及mTORC1中的Raptor蛋白,以抑制mTORC1活性,诱导自噬[27]。此外,腺苷酸活化蛋白激酶还可磷酸化ULK1的Ser555、Ser317和Ser777位点,直接激活ULK1,增强自噬。 2.3.4 丝裂原激活蛋白激酶介导的信号通路 丝裂原激活蛋白激酶由c-Jun氨基末端激酶,p38(α,β,γ和δ)、细胞外调节蛋白激酶1/2、细胞外调节蛋白激酶5家族构成,在脑缺血后被激活,传导细胞应激[28]。研究发现,c-Jun氨基末端激酶、p38活化受到抑制时,LC3-Ⅱ/LC3-Ⅰ比例降低,Beclin-1表达降低,细胞自噬水平降低[28]。 此外,调节细胞自噬的信号通路还包括核因子κB信号通路[29]、SIRT1/FOXO3a信号通路[30]、缺氧诱导因子1α/mTOR信号通路等[31]。见图5。"
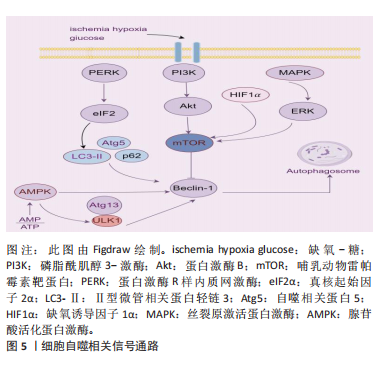

2.4 自噬参与脑缺血损伤的作用机制 2.4.1 自噬导致轴突变性 王琦[32]在SD大鼠大脑中动脉栓塞术后14 d,经甘氨酸银浸镀经染,观察到丘脑与黑质部位大量轴突变性坏死,证实了这一观点。研究发现,大鼠脑缺血再灌注损伤后1 d,Beciln-1表达开始增加,7 d达顶峰,且随着活化半胱氨酸天冬氨酸蛋白酶3的表达升高,神经元的凋亡显著增加[33]。此外已证实,在大脑中动脉栓塞前30 min腹腔注射10 mg/kg自噬抑制剂LY294002,大鼠脑梗死范围显著减小[34]。体外实验研究发现,给予自噬抑制剂3-甲基腺嘌呤处理PC12细胞,经缺氧-葡萄糖剥夺再灌注后,可显著拮抗缺氧-葡萄糖剥夺再灌注诱导的自噬和细胞损伤[35];类似的,给予自噬抑制剂ZSTK474后,可减轻缺氧-葡萄糖剥夺再灌注诱导的脑微血管内皮细胞损伤,保护血脑屏障[36]。以上研究结果均证实自噬在脑缺血过程中具有损伤作用。 2.4.2 自噬抑制神经元死亡 研究发现,丁香酚预处理可改善大脑中动脉栓塞大鼠神经功能缺损,减少梗死体积,而给予雷帕霉素后,促进了梗死体积及细胞凋亡的降低;反之,给予3-甲基腺嘌呤抑制自噬,则导致相反的结果。此外,体内实验研究结果显示,丁香酚预处理增加了缺氧-葡萄糖剥夺再灌注处理的HT22细胞的活力并抑制了细胞凋亡[37]。最新研究显示,大脑中动脉栓塞模型大鼠侧脑室注射自噬抑制剂Baf-A1或AMPK抑制剂Compound C,由于自噬活性降低,导致NOD样受体蛋白3、白细胞介素1β及白细胞介素18表达升高,细胞凋亡增加[38]。 自噬是脑缺血中重要的神经保护机制,线粒体自噬作为选择性自噬的一种,通过清除功能障碍的线粒体,减少细胞凋亡,保护神经细胞。脑缺血时,线粒体内活性氧的过表达使核因子κB、干扰素调节因子1等表达上调,释放多种促炎因子,导致免疫炎症反应,加重脑损伤[39]。 此外,研究发现,在缺氧-葡萄糖剥夺再灌注处理的小鼠海马神经元细胞(HT22)中,G蛋白偶联受体APJ配体(Apelin-36)通过上调线粒体自噬,抑制氧化应激,减少线粒体功能障碍,保护HT22细胞[40]。另有研究表明,大脑中动脉栓塞大鼠给予midivi-1(线粒体分裂抑制剂),可进一步加重线粒体功能障碍和神经损伤[41]。以上研究结果均表明自噬对缺血神经元具有保护作用。 2.4.3 自噬维持细胞代谢及内环境稳态 自噬是一种保守的分解代谢过程,脑缺血后自噬的发生对调节细胞代谢、维持内环境的稳态具有重要的意义。AMPK是重要的能量代谢调节因子,在能量剥夺(ATP耗竭和AMP增加)条件下,可作为一种“腺苷酸电荷”调节激酶,增加ATP分解代谢途径,并降低消耗性ATP的合成,从而维持细胞能量代谢平衡[42]。若再灌注期间ATP得不到补充,应激性自噬激活大量溶酶体,导致神经元坏死性死亡[43]。 2.5 中药对自噬的调控作用 2.5.1 中药复方 (1)补阳还五汤:补阳还五汤出自《医林改错》,由黄芪、当归、川芎、赤芍、地龙、桃仁及红花组成,具有益气活血、祛瘀通络之功[44]。马秀娟等[45]观察补阳还五汤对大脑中动脉栓塞模型大鼠AMPK/mTOR/ULK1自噬信号通路的调控机制,发现其通过抑制AMPK磷酸化,促进下游mTOR和ULK1磷酸化,降低LC3Ⅱ/Ⅰ及p-AMPK/AMPK比值,抑制过度自噬引起的神经细胞死亡,减轻脑组织损伤。此外,单玉栋等[46]也通过实验证实,补阳还五汤通过调控PI3K/Akt信号通路,降低LC3Ⅱ/Ⅰ表达,促进p62表达,保护大脑中动脉栓塞/再灌注大鼠神经功能。 (2)芪蛭胶囊:芪蛭胶囊以“黄芪、水蛭、地龙、丹参、川芎、当归、葶苈子、石菖蒲、郁金”药物为组成,具有益气活血、祛瘀通络化痰之效[47]。庄晓彤等[48]发现,芪蛭胶囊具有拮抗脑缺血再灌注损伤、保护神经元的作用,通过促进自噬相关蛋白LC3表达,降低p62表达,从而激活细胞自噬,发挥神经保护作用。蒋希成等[47]亦发现,芪蛭胶囊可下调大脑中动脉栓塞/再灌注大鼠脑组织p-mTOR、p-P70S6K蛋白表达,增强细胞重塑能力,减少细胞自噬性死亡。此外,有文献报道,芪蛭胶囊可降低大脑中动脉栓塞大鼠脑组织含水量、神经功能评分,减少p-Akt的表达,增加半胱氨酸组织蛋白酶B、天冬氨酸组织蛋白酶D的表达,从而激活神经元自噬,减轻再灌注损伤,保护脑神经功能[49]。 (3)痰热清注射液:痰热清注射液由金银花、连翘、黄芩、熊胆粉和山羊角组成,经萃取精制而成的中药制剂,具有清热化痰、解毒解痉之效[50]。李中浩[51]通过痰热清注射液腹腔注射对大脑中动脉栓塞大鼠神经功能影响的实验研究发现,该方可缩小大脑中动脉栓塞大鼠脑梗死体积,上调BCL2/BAX比例,降低LC3Ⅱ/Ⅰ表达,增加神经元特异核蛋白含量,降低胶质纤维状酸性蛋白、半胱氨酸天冬氨酸蛋白酶8含量,提示痰热清注射液通过激活apeline信号通路以抑制细胞凋亡和自噬,减轻再灌注损伤。 (4)益气通脉方:崔应麟教授从“元气”出发,重新认识缺血性脑卒中病机,认为“元气亏虚”为本,“瘀血、痰浊”为标,借王清任“补阳还五汤”组方原则,加以“祛浊”之功,自拟益气通脉方。方中药物:人参、丹参、土鳖虫、水蛭、三七、大黄,具有益气活血、化瘀通脉祛浊之效[52]。葛文静等[53]研究显示,益气通脉方可降低大脑中动脉栓塞大鼠脑组织中BAX、p-PI3K、p-Akt的表达水平,提高BCL2、Beclin-1的表达,减少神经元凋亡,保护受损脑组织。 (5)温阳复元方:温阳复元方由白附片、黄芪、党参、桂枝、淫羊藿、石菖蒲、三七组成,具有温阳益气、化痰通络之功[54]。胡跃强等[55]就温阳复元方对缺血再灌注损伤大鼠的影响研究发现,该方可减轻大鼠脑皮质损伤及脑水肿,降低c-Jun氨基末端激酶1、Beclin 1、Bcl-2、LC3B蛋白和mRNA表达水平,提示温阳复元方通过抑制JNK1/Bcl-2/Beclin-1通路,抑制细胞凋亡和自噬,改善缺血再灌注损伤大鼠神经功能。 (6)柔肝通络汤:周慎教授自拟柔肝通络汤(制首乌、桑椹、枸杞子、丹参、当归尾、赤芍、葛根、地龙、山楂),具有养阴活血通络之功效,治疗缺血性脑卒中阴虚血瘀证,临床效果显著[56]。龙华君等[57]研究发现,柔肝通络汤可改善大脑中动脉栓塞大鼠神经功能,缩小脑梗死灶,减轻神经元损伤,降低自噬相关蛋白Beclin-1、LC3表达,减轻缺血再灌注损伤。 (7)清热化瘀方:清热化瘀方组成包括水牛角、丹参、赤芍、川芎、水蛭、地龙、酒大黄、胆南星、天竺黄、牛膝10味中药,功效为清热解毒、化瘀通络。宋春林等[58]研究发现,清热化瘀方可降低大脑中动脉栓塞大鼠神经功能评分,减轻神经元病理损伤,降低细胞凋亡率,增加Beclin-1和LC3蛋白表达,降低半胱氨酸天冬氨酸蛋白酶3表达,提示清热化瘀方通过调节细胞自噬发挥神经保护作用。此外,秦红玲等[59]通过体内外实验研究发现,清热化瘀方可降低PC12细胞及脑缺血再灌注大鼠Nix、Beclin-1、LC3表达,提高miR-137表达及神经元存活率,提示清热化瘀方通过调控miR-137/Nix轴,改善大鼠缺血再灌注损伤,保护神经元。 由上可知,中药复方补阳还五汤、芪蛭胶囊、痰热清注射液及温阳复元方等均可通过调控自噬相关信号通路及蛋白表达,抑制神经元自噬性死亡,减轻脑缺血再灌注损伤,发挥神经保护作用,见表1。 2.5.2 中药有效成分 (1)萜类:白果内酯B是从银杏叶中提取的倍半萜类化合物,具有抗炎、抗氧化、改善线粒体功能等作用[60]。华骏[61]研究发现,白果内酯B干预缺氧-葡萄糖剥夺处理的神经元细胞株N2a,可促进细胞内BcL-2、LC3-Ⅱ和Beclin-1表达,降低BAX、活化半胱胺酸蛋白酶3、p62表达,减少细胞坏死和凋亡,表明白果内酯B通过促进神经元自噬并抑制神经元凋亡,减轻脑损伤。另有文献报道,白果内酯B通过激活Akt/内皮型一氧化氮合酶通道,促"


进内皮型一氧化氮合酶和Akt的磷酸化,抑制细胞自噬和凋亡,以改善神经功能[62]。 银杏内酯K亦是银杏叶的提取物成分。ZHANG等[63]研究发现银杏内酯K预处理可促进缺氧-葡萄糖剥夺诱导的星形胶质细胞增殖和迁移,并通过激活AMPK/m-TOR/ULK1通路,介导自噬相关蛋白表达,抑制细胞凋亡,提高细胞活力。同时应用复合物C阻断了这种保护作用,证实银杏内酯K通过调控AMPK/mTOR/ULK1通道诱导保护性自噬。 (2)生物碱类:异钩藤碱是一种从钩藤中提取的四环羟吲哚生物碱,具有抗炎、抑制神经元死亡和调节自噬等多种作用[64]。成家宏等[65]探讨异钩藤碱对缺血性脑卒中模型大鼠脑损伤及神经元自噬的影响,结果发现异钩藤碱能抑制缺氧诱导因子1α表达,激活mTOR,调控自噬关键蛋白,从而抑制神经元过度自噬,减少神经元凋亡,减轻脑损伤。 巴豆生物碱是从巴豆中分离出来的一种鸟嘌呤核苷类似物,具有抗炎、抗肿瘤、调节免疫等作用[66]。赵洪云等[67]研究巴豆生物碱对大脑中动脉栓塞/再灌注大鼠神经元损伤及自噬的影响,发现巴豆生物碱通过激活细胞外调节蛋白激酶1/2通路,下调Beclin-1、LC3-Ⅱ蛋白及mRNA表达,降低经元凋亡率,发挥神经保护作用,且高剂量效果最佳。 (3)黄酮类:葛根素是从葛根中提取的异黄酮类化合物,具有抗凋亡、抑制自噬、神经保护等作用[68]。WANG等[69]发现,葛根素预处理能激活APMK-mTOR-ULK1通道,调节相关靶点蛋白表达,减少大脑中动脉栓塞/再灌注大鼠海马CA1区自噬体的形成,减轻自噬,保护神经元。此外,田华等[70]亦通过实验证实,葛根素通过下调脑缺血再灌注小鼠大脑皮质自噬相关蛋白5及LC3Ⅰ/Ⅱ表达,提高小鼠平衡能力,发挥神经保护作用。 黄芩素是从黄芪根中提取的一种生物活性成分,具有抗炎、抑制凋亡、调节自噬等作用[71]。YANG等[72]发现,黄芩素可显著缩小梗死面积,促进PI3K/Akt/mTOR通路磷酸化,抑制神经元自噬,证实黄芩素可通过调控PI3K/Akt/mTOR途径,抑制细胞自噬,减轻大鼠脑缺血再灌注亚急性期损伤。 (4)皂苷类:三七总皂苷是三七的主要活性成分,具有保护血脑屏障、减轻脑含水量、减少细胞凋亡等多种作用[73]。乔园等[74]观察三七总皂苷对脑缺血再灌注模型小鼠自噬的影响,发现其可降低Beclin-1表达及LC3-Ⅱ/LC3-Ⅰ比例,上调p62表达,抑制神经元自噬。此外,芦君[75]也证实,三七总皂苷呈剂量依赖性上调Wnt3a、β-catenin表达,促进Wnt3a/β-catenin通道激活,调节神经元自噬。 黄芪甲苷是黄芪的主要活性成分之一,具有调节自噬、抗炎、抗血小板聚集、保护神经等作用[76]。张怡[77]在体外实验研究中发现,黄芪甲苷可激活AMPK/DDiT4/mTOR通路,提高缺氧-葡萄糖剥夺再灌注HT22细胞内Beclin-1表达及LC3Ⅱ/LC3Ⅰ,降低P62蛋白表达,增加自噬小体数量,提高自噬水平,保护缺氧-葡萄糖剥夺再灌注 HT22细胞。 (5)木脂素类:五味子醇甲是一种从五味子中分离出的木脂素类化合物。既往研究表明,五味子醇甲能减少细胞凋亡、抑制炎症及氧化应激以减轻脑缺血损伤[78]。WANG等[79]研究发现,五味子醇甲可减轻缺氧-葡萄糖剥夺再灌注 PC12细胞损伤,降低AMPK磷酸化,增加mTOR/p-mTOR表达,抑制细胞自噬,此外,给予MPK诱导剂AICAR预处理,可部分逆转五味子醇甲神经保护作用,提示五味子醇甲通过调节AMPK/mTOR通路,抑制缺氧-葡萄糖剥夺诱导的自噬,保护神经元。 (6)苯酞类:藁本内酯是当归和川芎的主要活性成分,具有抗凋亡、抗炎和调节能量代谢等作用[80-81]。MAO等[82]研究证实,藁本内酯通过调控PINK1/Parkin通道,增强线粒体功能,从而促进线粒体自噬,改善缺血诱导的神经元损伤。 (7)多酚类:姜黄素是从姜黄根部提取的一种多酚类化合物,具有减少细胞死亡、改善血脑屏障、抗炎和抗氧化应激等药理作用[83]。HOU 等[84]通过体外PC12 细胞缺氧-葡萄糖剥夺再灌注研究发现,姜黄素可抑制自噬和缺氧诱导因子1α表达,从而减少细胞死亡和凋亡,此外,给予3-甲基腺嘌呤处理效果一致,提示姜黄素通过调节自噬与缺氧诱导因子1α的关系,发挥神经保护作用。 迷迭香酸是从迷迭香中分离出来的一种多酚类物质,具有抗炎、调节自噬、抑制凋亡等作用[85]。刘书涵[86]的研究发现,迷迭香酸通过上调小胶质细胞Sirt3的表达,激活PI3K/Akt/mTOR通路,抑制细胞自噬,从而有效减少脑缺血中神经组织损伤,并抑制小胶质细胞极化和凋亡。 (8)多糖类:枸杞多糖是枸杞的主要活性成分,具有抗肿瘤、免疫调节和抗氧化应激等作用[87]。鱼洋[88]的体外实验研究发现,枸杞多糖能激活PI3K/Akt/mTOR通路,上调p-Akt、p-mTOR表达,下调活化半胱胺酸蛋白酶3、LC3-Ⅱ表达水平,抑制缺氧-葡萄糖剥夺再灌注诱导的细胞自噬性死亡和凋亡,保护神经元。 (9)菲醌类:丹参酮ⅡA是从丹参的根茎部提取的一种活性化合物,具有抗炎、抗氧化、调节自噬等作用[89]。ZHU等[90]对海马神经元细胞HT-22进行缺氧-葡萄糖剥夺再灌注,建立了脑缺血体外模型,经丹参酮ⅡA干预后显示,其可通过激活PI3K/Akt/mTOR信号通路,抑制细胞自噬,增加细胞活力,减少细胞死亡。 (10)其他:红景天苷是从红景天中提取的苯丙素糖苷类化合物,具有抗炎、抑制凋亡、调节自噬等作用[91]。LI等[92]研究发现,红景天苷可降低经缺氧-葡萄糖剥夺再灌注处理的PC12细胞乳酸脱氢酶活性,上调TSC2的表达,增加细胞活力,减少细胞凋亡,表明红景天苷通过调节AMPK/TSC2/mTOR通路诱导自噬,减轻脑缺血损伤。 由上可得,中药有效成分萜类、生物碱、黄酮、皂苷、木脂素、苯酞类等均通过调节脑缺血中细胞自噬,减少细胞损伤,从而发挥脑保护作用。见表2。"

| [1] 中华医学会神经病学分会,中华医学会神经病学分会脑血管病学组.中国急性缺血性脑卒中诊治指南2018[J].中华神经科杂志, 2018,51(9):666-682. [2] 樊冰,王阳,宁绍爽.疏血通对急性脑梗死患者认知行为学及神经影像学的影响[J].中华中医药学刊,2022,40(11):100-103. [3] LEVARD D, BUENDIA I, LANQUETIN A, et al. Filling the gaps on stroke research:Focus on inflammation and immunity. Brain Behav Immun. 2021;91(1):649-667. [4] KIM E. CHO S. CNS and peripheral immunity in cerebral ischemia: Partition and interaction. Experimental Neurology. 2021;335(10):1135-1138. [5] 张庆军,李宁,游桦,等.缺血性脑小血管病的危险因素分析及对急性脑梗死患者认知功能的影响[J].山西医药杂志,2021,50(1):44-46. [6] 王陇德,刘建民,杨弋,等.我国脑卒中防治仍面临巨大挑战——《中国脑卒中防治报告2018》概要[J].中国循环杂志,2019,34(2):105-119. [7] POWERS WJ, RABINSTEIN AA, ACKERSON T, et al. Guidelines for the Early Management of Patients With Acute Ische-mic Stroke: 2019 Update to the 2018 Guidelines for the Ear-ly Management of Acute Ischemic Stroke:A Guideline for Health-care Professionals From the American Heart Association/AmericanStroke Association. Stroke. 2019;50(12):e344-e418. [8] 苏占清,夏毅,宁厚旭,等.急性脑梗死中医病因病机、辨证研究概述及简评[J].世界科学技术-中医药现代化,2022,24(6):2481-2486. [9] 邱文然,徐榛敏,申伟,等.中医药治疗缺血性脑卒中优势定位评价情况概述[J].中国实验方剂学杂志,2022,28(12):225-232. [10] HARNETT MM, PINEDA MA, LATRÉ DE LATÉ P, et al. From Christian de Duve to Yoshinori Ohsumi: More to autophagy than just dining at home. Biomed J.2017;40(1):9-22. [11] DIKIC I, ELAZAR Z. Mechanism and medical implications of mammalian autophagy. Nat Rev Mol Cell Biol. 2018;19(6):349-364. [12] DECUYPERE JP,CEULEMANS LJ, AGOSTINIS P, et al. Autophagy and the Kidney: Implications for Ischemia-Reperfusion Injury and Therapy. Am J Kidney Dis. 2015;66(4):699-709. [13] WOLF MS, BAYIR H, KOCHANEK PM, et al. The role of autophagy in acute brain injury: A state of flux? Neurobiol Dis. 2019;122:9-15. [14] LIU R, ZHANG S, WAN R, et al. Effect of Beclin-1 gene silencing on autophagy and apoptosis of the prostatic hyperplasia epithelial cells. Clinics (Sao Paulo). 2022;77:100076. [15] HOU K, XU D, LI F, et al. The progress of neuronal autophagy in cerebral ischemia stroke: Mechanisms, roles and research methods. J Neurol Sci. 2019;400:72-82. [16] KHAMINETS A, BEHL C, DIKIC I. Ubiquitin-Dependent And Independent Signals In Selective Autophagy. Trends Cell Biol. 2016;26(1):6-16. [17] WEI H, LI Y, HAN S, et al. cPKCy-modulated autophagy in neurons alleviates ischemic injury in brain of mice with ischemic stroke through Akt-mTOR pathway. Transl Stroke Res. 2016;7(6):497-511. [18] RICARDO A, MALENE H, DAVID W. The selective autophagy receptor SQSTM1/p62 improves lifespan and proteostasis in an evolutionarily conserved manner. Autophagy. 2020;16(4):772-774. [19] CHEN Y, LI Q, LI Q, et al. p62/SQSTM1,a central but unexploited target:advances in its physiological/pathogenic functionsand small molecular modulators. J Med Chem. 2020;63(18):10135-10157. [20] Rong L, Li Z, Leng X, et al. Salidroside induces apoptosis and protective autophagyin human gastric cancer AGS cells through thePI3K/Akt/mTOR pathway. Biomed Pharmacother. 2020;122:109726. [21] MAIESE K. Targeting molecules to medicine with mTOR, autophagy and neurodegenerative disorders. Br J Clin Pharmacol. 2016;82(5): 1245-1266. [22] WANG Y, ZHANG H. Regulation of Autophagy by mTOR Signaling Pathway. Adv Exp Med Biol. 2019;1206:67-83. [23] FU J, YANG Y, ZHU L, et al. Unraveling the Roles of Protein Kinases in Autophagy: An Update on Small-Molecule Compounds for Targeted Therapy. J Med Chem. 2022;65(8):5870-5885. [24] SHI M, CHAI Y, ZHANG J, et al.Endoplasmic Reticulum Stress-Associated Neuronal Death and Innate Immune Response in Neurological Diseases. Front Immunol. 2022;12:794580. [25] BHARDWAJ M, LELI NM, KOUMENIS C, et al. Regulation of autophagy by canonical and non-canonical ER stress responses. Semin Cancer Biol. 2020;66:116-128. [26] 杨楠,丁锚,闫峰,等.远隔缺血预适应对脑缺血再灌注损伤大鼠缺血半暗带区PERK/p-eIF2α通路及自噬的影响[J].首都医科大学学报,2021,42(2):225-231. [27] TAMARGO-GÓMEZ I, MARIÑO G. AMPK: Regulation of Metabolic Dynamics in the Context of Autophagy. Int J Mol Sci. 2018;19(12):3812. [28] SUN J, NAN G. The Mitogen-Activated Protein Kinase (MAPK) Signaling Pathway as a Discovery Target in Stroke. J Mol Neurosci. 2016;59(1):90-98. [29] LIU Y, SONG Y, ZHU X. MicroRNA-181a Regulates Apoptosis and Autophagy Process in Parkinson’s Disease by Inhibiting p38 Mitogen-Activated Protein Kinase (MAPK)/c-Jun N-Terminal Kinases (JNK) Signaling Pathways. Med Sci Monit. 2017;23:1597-1606. [30] 戴瑶瑶,舒梦琦,魏汝恒,等.脑血管内皮细胞自噬的发生机制及其在缺血性脑卒中病理过程中的作用研究进展[J].实用心脑肺血管病杂志,2024,32(1):129-133. [31] 王哲义.丹参酮ⅡA磺酸钠调控HIF1α/mTOR介导细胞自噬干预缺血性脑卒中的机制研究[D].北京:北京中医药大学,2022. [32] 王琦.芪仙通络方对MCAO大鼠远隔损害部位轴突再生的影响及机理研究[D].长沙:湖南中医药大学,2021. [33] WANG L, DAI M, GE Y, et al. EGCG protects the mouse brain against cerebral ischemia/ reperfusioninjury by suppressing autophagy via the AKT/AMPK/mTOR phosphorylation pathway. Front Pharmacol.2022;13:921394. [34] LI J, WAN K, LIU M, et al. Dexmedetomidine alleviates cerebral ischemia-reperfusion injury via inhibiting autophagy through PI3K/Akt/mTOR pathway. J Mol Histol. 2023;54(3):173-181. [35] WANG G, WANG T, ZHANG Y, et al. Schizandrin Protects against OGD/R-Induced Neuronal Injury by Suppressing Autophagy:Involvement of the AMPK/mTOR Pathway. Molecules. 2019;24(19):3624. [36] HUA Y, ZHAI Y, WANG G, et al. Tong-Qiao-Huo-Xuedecoctionactivates PI3K/Akt/mTOR pathway to reduce BMECs autophagy after cerebral ischemia/reperfusion injury. J Ethnopharmacol.2022;298:115585. [37] SUN X, WANG D, ZHANG T, et al. Eugenol Attenuates Cerebral Ischemia-Reperfusion Injury by Enhancing Autophagy via AMPK-mTOR-P70S6K Pathway. Front Pharmacol. 2020;11:84. [38] 翟晶雯.异氟醚激活AMPK/ULK1通路增强自噬抑制NLRP3改善CIRI模型大鼠认知功能的作用研究[D].石河子:石河子大学,2023. [39] ZHANG L, WEI W. Anti-inflammatory and immunoregulatory effects of paeoniflorin and total glucosides of paeony. Pharmacol Ther. 2020; 207:107452. [40] SHAO Z, DOU S, ZHU J, et al. Apelin-36ProtectsHT22CellsAgainst Oxygen-GlucoseDeprivation/Reperfusion-Induced Oxidative Stress and Mitochondrial Dysfunction by Promoting SIRT1-Mediated PINK1/Parkin-Dependent Mitophagy. Neurotox Res. 2021;39(3):740-753. [41] MAO Z, TIAN L, LIU J, et al. Ligustilide ameliorates hippocampal neuronal injury after cerebral ischemia reperfusion through activating PINK1/Parkin-dependent mitophagy. Phytomedicine. 2022;101:154111. [42] Carling D. AMPK signalling in health and disease. Curr Opin Cell Biol. 2017;45:31-37. [43] HOU K, XU D, LI F, et al. The progress of neuronal autophagy in cerebral ischemia stroke: Mechanisms, roles and research methods. J Neurol Sci. 2019;400:72-82. [44] 辛紫媛,刘真一,高萍,等.补阳还五汤通过激活大鼠海马区沉默信息调节因子1减轻脑缺血/再灌注损伤后炎症反应的机制[J].中国药理学通报,2023,39(9):1787-1793. [45] 马秀娟,赵艳萌,王文良,等.补阳还五汤通过AMPK/mTOR/ULK1信号通路调控自噬减轻大鼠脑缺血/再灌注损伤[J].中国药理学通报,2022,38(1):147-152. [46] 单玉栋,赵艳萌,靳晓飞,等.补阳还五汤通过PI3K/AKT通路调控自噬抗大鼠脑缺血/再灌注损伤的作用[J].中国药理学通报, 2023,39(2):386-391. [47] 蒋希成,鞠丽丽,段芳芳,等.芪蛭胶囊对大鼠脑缺血再灌注损伤相关因子mTOR、P70S6K蛋白表达水平的影响[J].时珍国医国药, 2021,32(6):1293-1296. [48] 庄晓彤,段芳芳,鞠丽丽,等.芪蛭胶囊对大鼠脑缺血再灌注损伤相关因子p-Akt、Cathepsin表达的影响[J]. 中国中医急症,2021, 30(5): 753-756+765. [49] 段芳芳,陆雪健,鞠丽丽,等.芪蛭胶囊对脑缺血再灌注损伤大鼠自噬相关因子LC3、p62表达水平的影响[J].时珍国医国药,2023, 34(1):13-16. [50] 李莎莎.基于内质网应激通路研究痰热清注射液对急性脑梗死大鼠的治疗机制[D].北京:北京中医药大学,2021. [51] 李中浩.痰热清注射液对脑梗死后apelin信号通路及细胞凋亡和自噬的影响[D].北京:北京中医药大学,2022. [52] 丁培娜.益气通脉方对缺血性中风急性期气虚血瘀痰阻型的疗效及血清VEGF、AngⅡ含量的影响[D].郑州:河南中医药大学,2022. [53] 葛文静,陈芳芳,庞伯通,等.益气通脉方调控PI3K/AKT信号通路改善脑缺血再灌注损伤大鼠神经元凋亡[J].中医学报,2024,39(1): 63-70. [54] 张鼎,李方存,姜明贺,等.温阳复元方对脑缺血再灌注损伤大鼠JNK1/Bcl-2/Beclin 1信号通路相关蛋白及基因表达的影响[J].中华中医药杂志,2023,38(11):5208-5213. [55] 胡跃强,唐农,何乾超,等.温阳复元方治疗缺血性脑卒中恢复期患者的临床疗效及其机制[J].中国老年学杂志,2018,38 (19):4627-4629. [56] 及晓梦,刘雨,周慎,等.柔肝通络汤治疗脑梗死急性期40例临床观察[J].湖南中医杂志,2019,35(2): 6-8. [57] 龙华君,杨颖,李映辰,等.柔肝通络汤对MCAO大鼠自噬蛋白Beclin1及LC3表达的影响[J].时珍国医国药,2023,34(8):1845-1849. [58] 宋春林,龚方,刘伍才,等.清热化瘀方调节凋亡与自噬减轻大鼠急性脑缺血损伤的作用研究[J].光明中医,2023,38(11):2101-2103+2191. [59] 秦红玲,胡跃强,谭露露,等.清热化瘀方调控miR-137/Nix通路介导的线粒体自噬改善大鼠脑缺血-再灌注损伤[J].中药材,2023, 46(1):191-196. [60] LU J, XIE L, LIU K, et al. Bilobalide: A review of its pharmacology, pharmacokinetics, toxicity, and safety. Phytother Res. 2021;35(11): 6114-6130. [61] 华骏.白果内酯对缺血性脑损伤的神经保护作用及其机制研究[D].南京:南京医科大学,2017.
[62] ZHENG Y, WU Z, YI F, et al. By Activating Akt/eNOS Bilobalide B Inhibits Autophagy and Promotes Angiogenesis Following Focal Cerebral Ischemia Reperfusion. Cell Physiol Biochem. 2018;47(2):604-616. [63] ZHANG Y, MIAO JM. Ginkgolide K promotes astrocyte proliferation and migration after oxygen-glucose deprivation via inducing protective autophagy through the AMPK/mTOR/ULK1 signaling pathway. Eur J Pharmacol. 2018;832:96-103. [64] DENG Y, TAN R, LI F, et al. IsorhynchophyllineAmelioratesCerebral Ischemia/Reperfusion Injury by Inhibiting CX3CR1-Mediated Microglial Activation and Neuroinflammation. Front Pharmacol. 2021;12:574793. [65] 成家宏,孟毅,乔明亮.异钩藤碱对缺血性脑卒中模型大鼠脑损伤及神经元自噬的影响[J].中医药导报,2022,28(5):13-17+51. [66] 胡静,秦贝贝,马琳,等.巴豆化学成分、药理作用及其质量标志物预测分析[J].中草药,2021,52(21):6743-6754. [67] 赵洪云,王建平,张杰.巴豆生物碱通过ERK1/2通路对脑缺血再灌注大鼠海马神经元损伤及自噬的影响[J].卒中与神经疾病,2022, 29(3):199-204+214. [68] 金明睿,张梅.葛根素对脑缺血保护作用及其机制的研究进展[J].青岛大学学报(医学版),2023,59(1):155-158. [69] WANG JF, MEI ZG, FU Y, et al. Puerarin protects rat brain against ischemia/reperfusion injury by suppressing autophagy via the AMPK-mTOR-ULK1 signaling pathway. Neural Regen Res. 2018;13(6):989-998. [70] 田华,郭连军,刘富,等.葛根素下调Atg5、LC3Ⅰ/Ⅱ蛋白对缺血再灌注脑损伤小鼠的神经保护作用[J].中国临床药理学杂志, 2023,39(4):508-512. [71] 王恺迪,张丽梅,黎晓.自噬及自噬调节剂在脑缺血中的研究进展[J].赣南医学院学报,2021,41(2):109-114. [72] YANG S, WANG H, YANG Y, et al. Baicalein administered in the subacute phase ameliorates ischemia-reperfusion-induced brain injury by reducing neuroinflammation and neuronal damage. Biomed Pharmacother. 2019;117:109102. [73] 项昌培,周瑞,张毅,等.三七中皂苷类成分及其抗脑缺血分子机制研究进展[J].中国中药杂志,2020,45(13):3045-3054. [74] 乔园,穆庆丽,吴启航,等.三七总皂苷对脑缺血再灌注小鼠脑组织自噬水平的调节机制分析[J].中医药学报,2023,51(7):22-26. [75] 芦君.三七总皂苷对脑梗死大鼠神经细胞Wnt/β-连环素信号通路的影响[J].安徽医药,2022,26(12):2395-2398. [76] 曹奇,董宝强,张小卿,等.基于自噬调控的黄芪提取物生物学活性作用机制探讨[J].中华中医药学刊,2021,39(7):144-147. [77] 张怡.黄芪甲苷基于AMPK/DDiT4/mTOR信号通路调控自噬抗脑缺血再灌注损伤的研究[D].石家庄:河北中医学院,2020. [78] ZHOU F, WANG M, JU J, et al. Schizandrin Aprotectsagainstcerebral ischemia-reperfusion injury by suppressing inflammation and oxidative stress and regulating the AMPK/Nrf2 pathway regulation. Am J Transl Res. 2019;11(1):199-209. [79] WANG G, WANG T, ZHANG Y, et al. Schizandrin Protects against OGD/R-Induced Neuronal Injury by Suppressing Autophagy: Involvement of the AMPK/mTOR Pathway. Molecules. 2019;24(19):3624. [80] 李茜,李永秋,张冬森,等.藁本内酯通过下调miR-292-5p表达改善氧糖剥夺对PC12细胞的促凋亡和炎症因子表达效应[J].免疫学杂志,2022,38(8):705-710. [81] 田丽宇.基于AMPK/PGC-1α通路改善能量代谢障碍探讨藁本内酯对缺血性脑卒中线粒体功能的保护作用[D].合肥:安徽中医药大学,2023. [82] MAO Z, TIAN L, LIU J, et al.Ligustilide ameliorates hippocampal neuronal injury after cerebral ischemia reperfusion through activating PINK1/Parkin-dependent mitophagy. Phytomedicine. 2022;101:154111. [83] 孙玉,李鹏,杨鹏飞.姜黄素抗脑缺血再灌注损伤的药理学研究进展[J].神经药理学报,2021,11(4):38-48. [84] HOU Y, WANG J, FENG J. The neuroprotective effects of curcumin are associated with the regulation of the reciprocal function between autophagy and HIF-1α in cerebral ischemia-reperfusion injury. Drug Des Devel Ther. 2019;13:1135-1144. [85] 赵玉霞,陈莺倩.迷迭香酸通过AMPK/mTOR通路减轻新生大鼠缺血缺氧性脑损伤研究[J].中草药,2021,52(22):6897-6903. [86] 刘书涵.迷迭香酸通过调节小胶质细胞极化表型减轻缺血性脑卒中损伤的机制研究[D].长春:吉林大学,2023. [87] 李杏英,潘燕婷,李勇华.枸杞多糖对小鼠脑缺血再灌注损伤的神经保护作用及其机制[J].中国临床药理学杂志,2017,33(20):2054-2057. [88] 鱼洋.枸杞多糖对脑缺血再灌注损伤的作用及机制研究[D].西安:中国人民解放军空军军医大学,2019. [89] 王哲义,孙怿泽,邓欣祺,等.丹参酮类脂溶性成分及其干预缺血性脑卒中机制的研究进展[J].中草药,2022,53(4):1181-1190. [90] ZHU Y, TANG Q, WANG G, et al. Tanshinone IIA Protects Hippocampal Neuronal Cells from Reactive Oxygen Species Through Changes in Autophagy and Activation of Phosphatidylinositol 3-Kinase, Protein Kinas B, and Mechanistic Target of Rapamycin Pathways. Curr Neurovasc Res. 2017;14(2):132-140. [91] 徐浩群,张文静,娄原,等.红景天苷对脑缺血损伤的保护作用及机制研究进展[J].中国实验方剂学杂志,2023,29(15):256-266. [92] LI C, CHI J, DAI H, et al. Salidroside attenuates cerebral ischemia/reperfusion injury by regulating TSC2-induced autophagy. Exp Brain Res. 2023;241(1):113-125. |
| [1] | Li Yiwen, Liu Feixiang, Zhang Yunke. Regulation of lysosome function by stem cells in treatment of lysosomal storage diseases [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(1): 145-152. |
| [2] | Liu Lingyun, He Guixin, Qin Weibin, Song Hui, Zhang Liwen, Tang Weizhi, Yang Feifei, Zhu Ziyi, Ou Yangbin . Improvement of myocardial injury by traditional Chinese medicine: mitochondrial calcium homeostasis mediates macrophage autophagy and pyroptosis pathway [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(6): 1276-1284. |
| [3] | Jiang Qiyu, Zeng Huiyan. A novel analysis and prediction method for potential mechanisms of traditional Chinese medicine based on artificial intelligence and omics data-driven approach [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(35): 7552-7561. |
| [4] | Zhu Chuanxi, Qiu Long, Li Lingxu, Ji Guangcheng. Chinese herbal prescription combined with head acupuncture exercise therapy improves limb spasticity in rats with ischemic stroke [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(35): 7571-7577. |
| [5] | Zhu Jiaping, Gao Bo, Lou Chunbiao, Yang Fengyong, Yang Kun. Monomeric traditional Chinese medicine in the treatment of rheumatoid arthritis: regulation of T cell balance [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(32): 6955-6962. |
| [6] | Xu Zhenhua, Li Yanjie, Qin Hewei, Liu Haoyuan, Zhu Bochao, Wang Yupu. Traditional Chinese medicine monomer in treatment of neuroinflammation after spinal cord injury: effects of nuclear transcription factor kappa B signaling pathway [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(3): 590-598. |
| [7] | Liu Yuan, Qu Yuan, Wan Yakun, Guo Jingyu, Jiang Ping. Transcriptomic analysis and drug prediction of basement membrane-related genes in different traditional Chinese medicine patterns of rheumatoid arthritis [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(25): 5486-5500. |
| [8] | Fang Yuting, Peng Hong, Pang Yujie. Inflammatory signaling pathways in traditional Chinese medicine for treating fever after lumbar interbody fusion surgery [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(21): 4568-4575. |
| [9] | Zhang Shuo, Cui Yinglin, Zhou Panpan, Li Yile, Wang Lei, Zou Qianqian. Role of endoplasmic reticulum stress-autophagy in cerebral ischemia-reperfusion injury and the regulatory mechanism of traditional Chinese medicine [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(20): 4325-4332. |
| [10] | Shen Xiaoqiu, Wang Zhentao, Qiu Yueqing, Song Chenghao. Traditional Chinese medicine monomers regulate ferroptosis to combat myocardial ischemia-reperfusion injury [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(20): 4333-4340. |
| [11] | Yang Yike, Ren Yafeng, Li Bing, Shang Wenya, Huang Jing, Guo Jia, Liu Huiyao . Regulatory mechanisms and therapeutic strategies for cellular autophagy after spinal cord injury [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(18): 3885-3896. |
| [12] | Dong Zhengqin, Zheng Qi, Wu Guanmao, Wang Wenna, Chen Leqin. Irisin: a new link between exercise, disease and health [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(18): 3897-3905. |
| [13] | Cao Panxia, Peng Zining, Liu Shanshan, Fei Tiantian, Liang Tengyun, Zhang Mengwen, Wu Hong. AMP-activated protein kinase mediates macrophage fatty acid oxidation: an approach to prevent and treat atherosclerosis with traditional Chinese medicine [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(18): 3906-3914. |
| [14] | Zhou Panpan, Yang Tong, Wang Shurui, Cui Yinglin . Role of ferroptosis in ischemic brain injury and the regulatory mechanism of traditional Chinese medicine [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(17): 3675-3683. |
| [15] | Lai Yue, Lin Xuan, Xu Miao, Liu Huan, Shen Jianlin, Huang Wenhua. Medication pattern and mechanism of marine traditional Chinese medicine in the treatment of osteoporosis [J]. Chinese Journal of Tissue Engineering Research, 2025, 29(17): 3713-3723. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||