Chinese Journal of Tissue Engineering Research ›› 2022, Vol. 26 ›› Issue (18): 2938-2944.doi: 10.12307/2022.706
Previous Articles Next Articles
Action and mechanism of autologous bone marrow aspiration concentrate in the treatment of knee osteoarthritis
Zhao Jirong1, Yang Tao2, Xu Jiancheng1, Zhao Ning1, Xue Xu1, Ma Tong1
- 1Gansu Provincial Hospital of TCM, Lanzhou 730050, Gansu Province, China; 2Gansu University of Traditional Chinese Medicine, Lanzhou 730030, Gansu Province, China
-
Received:2021-09-15Accepted:2021-11-11Online:2022-06-28Published:2022-01-30 -
Contact:Yang Tao, Master candidate, Gansu University of Traditional Chinese Medicine, Lanzhou 730030, Gansu Province, China -
About author:Zhao Jirong, Chief physician, Doctoral supervisor, Gansu Provincial Hospital of TCM, Lanzhou 730050, Gansu Province, China -
Supported by:Gansu Health Industry Scientific Research Plan Project, No. GSWSKY-2019-28 (to XJC); Lanzhou Innovative Talents Project, No. 2018-RC-99 (to ZJR)
CLC Number:
Cite this article
Zhao Jirong, Yang Tao, Xu Jiancheng, Zhao Ning, Xue Xu, Ma Tong. Action and mechanism of autologous bone marrow aspiration concentrate in the treatment of knee osteoarthritis[J]. Chinese Journal of Tissue Engineering Research, 2022, 26(18): 2938-2944.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
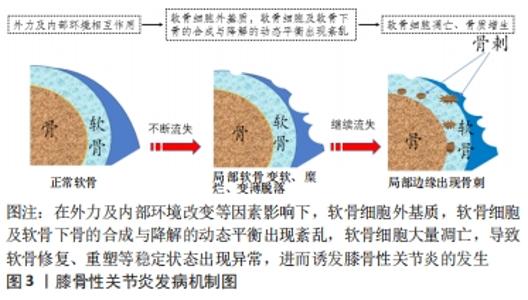
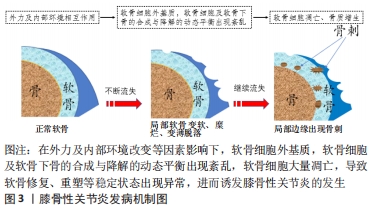
2.1 膝骨性关节炎可能的发病机制研究 膝关节有3个间室:胫股内侧间室,连接胫骨内侧平台和股骨内侧髁;胫股外侧间室,连接胫骨外侧平台和股骨外侧髁;髌股关节,连接髌骨和股骨,这3个隔室一起工作,形成1个改进的铰链关节,使膝关节能够屈曲、伸直,并能够稍微旋转。以前,膝骨性关节炎被认为是衰老和“磨损”的机械后果的正常结果,因此出现了“退行性关节病”这一名词。然而,现在人们认识到骨性关节炎是由多因素、复杂的结构及机械因素相互作用的结果,其包括关节完整性、遗传易感性、局部炎症、机械力以及细胞和生物化学等过程[5]。骨性关节炎涉及滑膜关节的3个主要组织:关节软骨、骨及滑膜[6]。一些研究者认为膝骨性关节炎的病理与增生相关的炎症和软骨细胞的凋亡引起的软骨退行性病变有关[7-8]。 随着人年龄的增长,软骨下血管的数量减少,导致软骨相关的生理生化异常。此外软骨细胞不能合成透明质酸和聚葡萄糖的长链结构,导致关节软骨局部软化,丧失弹性,磨损及结构损伤,此病理过程继续导致继发性关节纤维化,从而出现膝关节僵硬。而关节软骨覆于软骨下骨之上,包括表面非钙化软骨与深层钙化软骨,在维持关节环境稳定中发挥着重要的功能。而钙化软骨具有小分子的渗透性,在非钙化软骨与软骨下骨的生物化学的相互作用中担任重要角色。由于关节软骨与软骨下骨密切接触,二者之间存在密切的生物化学与生物力学交流,在保护关节退行性改变中发挥着重要的作用。当软骨下骨改变,可使上覆的软骨受到异常的剪切力和张力,导致继发性软骨损伤和退行性改变;在关节软骨损伤或丧失后,传递到下层骨骼的应力也将显著增加,进而诱导软骨下骨损伤[9]。较多研究证实,在外力及内部环境改变等因素影响下[10-13],软骨细胞外基质,软骨细胞及软骨下骨的合成与降解的动态平衡出现紊乱,软骨细胞大量凋亡,导致软骨修复、重塑等稳定状态出现异常,进而诱发膝骨性关节炎的发生,见图3。"

上述病理改变发生后,常引起患者膝关节疼痛、功能障碍、畸形等症状,发病率及致残率高,严重影响患者的生活质量[14],而骨髓抽吸浓缩物作为一种具有预防性或者再生性的治疗膝骨性关节炎的方式,其或可从根本上抑制或者逆转膝骨性关节炎的病程。 2.2 骨髓抽吸浓缩物治疗膝骨性关节炎的相关研究 较多临床前动物实验研究发现骨髓抽吸浓缩物能够有效治疗膝骨性关节炎。DESANDO等[15]研究发现在兔骨关节炎模型中,骨髓间充质干细胞优先向半月板迁移,骨髓抽吸浓缩物则向关节软骨迁移,而联合透明质酸钠会消除这种差异,并且有助于细胞向软骨细胞迁移,这可能与透明质酸影响巨噬细胞激活有关,巨噬细胞对祖细胞的激活有重要的意义。WANG等[16]研究表明关节腔内注射自体富血小板血浆和骨髓抽吸浓缩物在山羊骨关节炎模型中具有较好的治疗效果,并且骨髓抽吸浓缩物比富血小板血浆具有更好的软骨保护作用。完整的半月板对健康的膝关节至关重要,而无血管性半月板撕裂显示出较差的再生能力,因此该区域病变易使患者患膝骨性关节炎,KOCH等[17]通过髌骨外侧入路使24只新西兰大白兔的半月板暴露,进行软组织松解后使外侧半月板向前脱位,在中间部的无血管区域用手术刀造成长约4 mm的纵向半月板撕裂,然后试验组采用半月板缝合联合骨髓抽吸浓缩物治疗,对照组采用半月板缝合联合富血小板血浆,干预6周后对照组显示半月板未愈合,仍有撕裂,显微镜下观察到最轻微的愈合反应迹象,而试验组能够发现完整的缺损填充组织,只观察到半月板表面破裂,并且修复组织中的Ⅱ型胶原和蛋白多糖处于中等水平;干预12周时,对照组仍有明显的半月板撕裂,显微镜下填充组织中观察不到Ⅱ型胶原和蛋白多糖,而试验组一半模型缺损组织几乎完全填充,并且大部分模型的修复组织被半月板样细胞浸润,蛋白多糖染色清晰,说明骨髓抽吸浓缩物能够促进半月板无血管区域损伤的修复,预防膝骨性关节炎的发生。 上述基础研究结果表明骨髓抽吸浓缩物能通过修复损伤的关节软骨及半月板而发挥治疗膝骨性关节炎的作用,并且其对半月板的修复作用强于临床常用的富血小板血浆技术,其联合透明质酸对关节软骨的修复作用强于骨髓间充质干细胞联合透明质酸,因此猜想,临床使用骨髓抽吸浓缩物治疗膝骨性关节炎时,联合富血小板血浆及透明质酸可能会取得更好的效果,并且可以根据膝骨性关节炎患者关节软骨及半月板损伤程度的不同选择合适的联合物或者载体来治疗。文章就骨髓抽吸浓缩物治疗膝骨性关节炎的基础研究作一总结,见表1。"

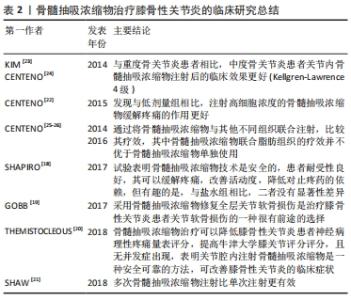
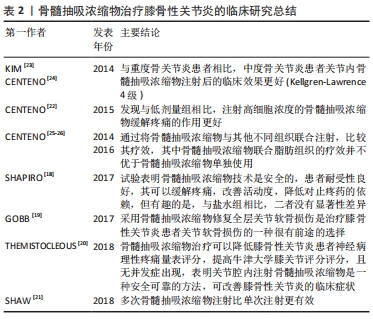
除了动物实验研究外,较多临床类研究也证实了骨髓抽吸浓缩物可作为一种有效的治疗膝骨性关节炎的手段。SHAPIRO等[18]的单盲随机对照试验表明骨髓抽吸浓缩物技术是安全的,患者耐受性良好,其可以缓解疼痛,改善活动度,降低对止疼药的依赖,但有趣的是,与盐水组相比,二者没有显著性差异。GOBBI等[19]研究表明采用骨髓抽吸浓缩物修复全层关节软骨损伤是治疗膝骨性关节炎患者关节软骨损伤的一种很有前途的选择。THEMISTOCLEOUS等[20]对在单个中心接受骨髓抽吸浓缩物关节腔注射治疗的233例膝骨性关节炎患者的数据进行了回顾性评估,对纳入研究的121例膝骨性关节炎患者进行了统计分析,神经病理性疼痛量表(Neuropathic pain scale,NPS)由8.33分下降到4.49分,牛津大学膝关节评分(Oxford Knee Score,OKS)由20.20分上升至32.29分,且没有出现并发症,结果表明关节腔内注射骨髓抽吸浓缩物是一种安全可靠的方法,可改善膝骨性关节炎的临床症状。另外SHAW等[21]研究表明多次骨髓抽吸浓缩物注射比单次注射更有效;CENTENO等[22]研究发现与低剂量组相比,注射高细胞浓度的骨髓抽吸浓缩物缓解疼痛的作用更好;有2项研究证明与重度骨性关节炎患者相比,中度骨性关节炎患者关节内骨髓抽吸浓缩物注射后的临床效果更好(Kellgren-Lawrence 4级) [23-24];还有研究通过将骨髓抽吸浓缩物与其他不同组织联合注射,比较其疗效,其中骨髓抽吸浓缩物联合脂肪组织的疗效并不优于骨髓抽吸浓缩物单独使用[25-26]。上述临床研究进一步表明骨髓抽吸浓缩物技术可以降低膝骨性关节炎患者疼痛数字量表评分,缓解疼痛,提高膝关节功能评分,改善关节活动度,降低患者对止疼药的依赖,并且发现对中度骨性关节炎患者效果更好,多次注射比单次注射更有效,高细胞浓度的骨髓抽吸浓缩物对于缓解疼痛效果更佳。 文章就骨髓抽吸浓缩物治疗膝骨性关节炎的临床研究概况作一总结,见表2。"

总之,多项体外实验研究、动物实验及临床试验研究都证实了骨髓抽吸浓缩物将是一种安全可靠有前途的治疗膝骨性关节炎的方法。但是临床类研究局限性较高,随机对照试验较少,大多为回顾性研究和病例对照研究,总体证据水平较低,而且研究异质性较大。 2.3 骨髓抽吸浓缩物治疗膝骨性关节炎的物质基础及作用机制研究 骨髓抽吸物含有复杂的细胞成分,包括间充质干细胞、血小板、白细胞、红细胞、造血及非造血前体细胞。骨髓抽吸浓缩物是描述从骨髓分离的骨髓成分和间充质干细胞的混合物的常用术语[27]。 2.3.1 骨髓间充质干细胞 骨髓抽吸浓缩物之所以能够治疗膝骨性关节炎,离不开其主要成分骨髓间充质干细胞。传统的治疗膝骨性关节炎的方法旨在减轻患者疼痛,维持或改善关节功能,降低致残率,并不能再生关节软骨。近年来,研究发现第一类被识别分离的间充质干细胞即骨髓间充质干细胞因其对组织具有修复性,甚至可通过细胞间直接相互作用或分泌生物活性因子发挥免疫调节和抗炎作用而被认为是治疗骨性关节炎的一种很有前途的选择[28-29]。骨髓间充质干细胞不仅具有较强的自我更新能力,而且具有多向分化的潜能,并且具有来源方便,不受伦理学问题干扰,易分离、培养、扩增和纯化的优点,因此是临床治疗疾病的理想种子细胞,亦是精准化个体干细胞治疗的首选细胞[30]。骨髓间充质干细胞可以向软骨细胞分化[31],因此学者对骨髓间充质干细胞移植治疗膝骨性关节炎进行了一系列的临床研究。 LAMO-ESPINOSA等[32]在一项多中心随机对照临床试验中,将30例诊断为膝骨性关节炎的患者随机分为单纯关节腔内注射透明质酸组(对照组)及透明质酸联合10×106或100×106培养的自体骨髓间充质干细胞组(试验组),随访12个月,发现透明质酸联合骨髓间充质干细胞组目测类比评分显著降低,从开始评估时出现并保持到最后一次评估,但有趣的是这种疼痛的减轻与骨髓间充质干细胞的给药剂量无关,而仅用透明质酸治疗就能在前6个月降低WOMAC评分,但这种改善并没有长期持续,但是当患者接受骨髓间充质干细胞治疗时,WOMAC评分在12个月时显著降低。CENTENO等[33]从膝骨性关节炎患者的骨髓抽吸物中分离并体外培养间充质干细胞,然后将其经皮注入到受试者的关节腔内,注射后24周,患者膝关节功能明显改善,目测类比评分显著降低,并且核磁定量分析结果显示关节软骨和半月板体积明显增加。OROZCO等[34]将4×107个体外培养的自体骨髓间充质干细胞注射到12例膝骨性关节炎患者的关节腔内,随访1年发现,所有患者的膝关节相关功能指数都得到改善,核磁检查T2WI的横向弛豫时间图定量显示损伤关节软骨面积降低27%,并且其中11例膝关节软骨质量均提高。虽然研究表明骨髓间充质干细胞能够显著降低膝骨性关节炎患者的目测类比评分,改善相关功能指数,修复损伤的关节软骨,但是考虑到严格的法规与细胞操作和扩增的相关问题,培养的骨髓间充质干细胞虽然已在临床前环境中得到广泛探索,但其在临床实践中的应用极其有限。相反,符合最低限度操作标准,允许在一步治疗中直接获得骨髓抽吸浓缩物(骨髓抽吸浓缩物),已被广泛运用于治疗软骨损伤的临床实践中,并且最近被提议作为治疗退行性骨科疾病的一种有前途的注射方法[35-36]。 2.3.2 转化生长因子β 骨髓抽吸浓缩物除了含有骨髓间充质干细胞外,还含有大量的的骨髓源性血小板,他们的性质不同于制备富血小板血浆的外周血中的血小板[37]。这些血小板含有大量的生长因子、趋化因子及细胞因子,研究表明骨髓抽吸浓缩物中含有来自转化生长因子β超家族的生长因子[38-39],其与软骨细胞增殖及间充质干细胞分化有密切的关系。 转化生长因子β蛋白家族有超过35位以上的成员,在哺乳动物中,转化生长因子β家族包括3个成员:转化生长因子β1,β2,β3,虽然这3个成员在分子结构上高度同源,但是每个成员都具有不同的生物学活性与表达模式[40]。健康的关节软骨基质中含有大量的转化生长因子β及其亚型(高达300 ng/g),多以潜伏的形式存在,主要形式为转化生长因子β2(60%-85%)。研究发现转化生长因子β能够发动间充质干细胞的聚集,聚集后转化生长因子β相关信号通路进一步刺激软骨细胞增殖,抑制其肥大与成熟[41]。在此过程中,转化生长因子β主要通过促进软骨细胞表达软骨特异的细胞外基质分子(Ⅱ型胶原和Agc1)而促进软骨组织的形成。转化生长因子β除了能够促进关节软骨的形成,还能够在软骨下骨内诱导前驱细胞分化成成骨细胞,促进成骨细胞晚期成熟。骨稳态的维持有赖于骨重塑,成骨细胞、骨细胞、破骨细胞共同调节软骨下骨重塑和骨矿盐代谢,破骨细胞吸收时,激活转化生长因子β诱导巢蛋白阳性的骨髓间充质干细胞迁移到骨重塑点,分化为成骨细胞,促进骨及血管的形成,从而有序的调节骨重建过程。 2.3.3 血小板衍生生长因子 骨髓抽吸浓缩物中存在的另一个关键生长因子是血小板衍生生长因子。血小板衍生生长因子主要由血小板产生[42],是一种二聚体阳离子糖蛋白,包括血小板衍生生长因子AA,BB,AB,CC,DD共5种分型[43]。其受体为一种细胞膜酪氨酸激酶,包括受体α和β两种形式,血小板衍生生长因子通过激活其受体对细胞进行调节,研究发现血小板衍生生长因子对间充质干细胞的迁移、分化、矿化等有重要的调节作用[44-45]。SETIAWAN等[46]将32只12周龄的Wistar大鼠通过关节腔内注射碘乙酸单钠诱导大鼠膝关节骨性关节炎后随机分为两组,试验组大鼠关节内注射重组人血小板衍生生长因子和透明质酸,对照组未予注射,4周后将大鼠处死后用酶联免疫吸附法检测大鼠血清中ⅡA型前胶原N末端肽与Ⅱ型胶原C端肽(CTX-Ⅱ)的水平,研究发现对照组膝关节滑膜组织增厚,股骨远端和胫骨近端出现骨赘,关节表面软骨出现溶解病变,其病理学特征为软骨表面纤维化,软骨细胞减少,Ⅱ型胶原纤维结构排列松散,钙化区血管浸润;而试验组膝关节滑膜肥厚,骨赘不明显,软骨表面较光滑,病理特征表现为表面软骨细胞较多,聚集软骨细胞较少,Ⅱ型胶原纤维形态中等排列,从而得出重组血小板衍生生长因子BB能够改善软骨细胞对Ⅱ型胶原的合成代谢过程,并抑制以软骨细胞体积增加,血清ⅡA型前胶原N末端肽升高和血清CTX-Ⅱ水平降低为特征的分解代谢。SUYASA等[47]研究发现在小鼠膝关节骨关节炎模型中应用重组血小板衍生生长因子BB和透明质酸对膝关节软骨有再生作用,其特点是软骨细胞数量增多,软骨糖蛋白40水平降低。 2.3.4 其他生长因子 对于局灶性软骨缺损的治疗,骨髓抽吸浓缩物能够刺激软骨细胞细胞外基质合成的生长因子浓度升高,这些因子包括胰岛素样生长因子、成纤维细胞生长因子18、骨形态发生蛋白1,7[48],这些生长因子已被证明可以降低软骨细胞分解代谢的活性。 胰岛素样生长因子家族由配体胰岛素样生长因子1,2、细胞表面受体胰岛素样生长因子1R,2R、至少6种不同的胰岛素样生长因子结合蛋白以及众多的调节胰岛素样生长因子活性的胰岛素样生长因子BP蛋白酶组成。大量研究表明胰岛素样生长因子1是软骨稳态的重要介质,能够促进软骨修复、诱导软骨细胞分化、促进蛋白多糖合成[49-50]。胰岛素样生长因子1是一种由70个氨基酸构成的小多肽,结构上与胰岛素前体相关,其在关节软骨代谢中的作用在健康和疾病中均有广泛的研究。EKENSTEDT等[51]研究发现胰岛素样生长因子1对维持关节软骨的完整性有重要的意义,长期胰岛素样生长因子1缺乏会加重没有骨病变的膝骨性关节炎患者软骨损伤的程度。GOODRICH等[52]研究发现胰岛素样生长因子1基因修饰的软骨细胞可以成功的过度表达胰岛素样生长因子1以加速透明样软骨的早期形成,并且能够阻止滑膜慢性炎症的发生。 成纤维细胞生长因子家族是一种由22种结构相关蛋白质组成多功能信号分子,其中18种能够作为配体结合到4种酪氨酸激酶受体(成纤维细胞生长因子R1-4)上,另外4种(成纤维细胞生长因子11-14)属于胞内蛋白不与受体反应[53]。而目前成纤维细胞生长因子家族中的成纤维细胞生长因子2和成纤维细胞生长因子18因其在软骨组织工程中的作用而被广泛研究[54]。有研究发现成纤维细胞生长因子18通过作用于成纤维细胞生长因子R4来调节自噬,进而影响软骨基质的产生,生长板软骨细胞在出生后的发育过程中会诱发自噬,自噬能够调节Ⅱ型胶原的分泌,而Ⅱ型胶原是软骨细胞外基质的主要成分[55]。MORI等[56]根据基因分析确定了成纤维细胞生长因子18为保护或再生关节软骨的有效分子,并发现了Timp1是关节软骨细胞中成纤维细胞生长因子18的新型下游分子。REKER等[57]研究发现重组人成纤维细胞生长因子18能够刺激全膝关节置换后的膝骨性关节炎患者的关节软骨再生。 另外骨髓抽吸浓缩物中含有骨形态发生蛋白,骨形态发生蛋白是具有多种功能的高度保守的蛋白,可调节细胞外基质,在骨重塑过程中发挥重要作用。骨形态发生蛋白可调节骨诱导和软骨形成[58-59],已有研究证明骨形态发生蛋白2可以调节转录因子SOX9的表达和活性,从而促进骨软骨的分化,同时,骨形态发生蛋白可通过调节蛋白多糖的合成在软骨保护和修复中发挥重要作用[60]。 文章就骨髓抽吸浓缩物治疗膝骨性关节炎的物质基础及作用机制作一总结,见表3。"

| [1] 刘月驹,秦士吉,李升,等.膝关节失衡综合征在骨科临床中的应用[J].河北医科大学学报,2015,36(5):598. [2] 王斌,邢丹,董圣杰,等.中国膝骨关节炎流行病学和疾病负担的系统评价[J].中国循证医学杂志,2018,18(2):134-142. [3] SINGH A K, KALAIVANI M, KRISHNAN A, et al. Prevalence of osteoarthritis of knee among elderly persons in urban slums using american college of rheumatology (ACR) criteria. J Clin Diagn Res. 2014; 8(9):9-11. [4] MILLER RH. Joint loading in runners does not initiate knee osteoarthritis. Exerc Sport Sci Rev. 2017;45(2):87-95. [5] MICHELLE L. Knee osteoarthritis: a primer. Perm J. 2017;21:16-183. [6] SAMUELS J, KRASNOKUTSKY S, ABRAMSON SB. Osteoarthritis:a tale of three tissues. Bull Nyu Hosp Jt Dis. 2008;66(3):244-250. [7] HWANG HS, KIM HA. Chondrocyte apoptosis in the pathogenesis of osteoarthritis. Int J Mol Sci. 2015;16(11):26035-26054. [8] TEMPLE-WONG MM, REN S, QUACH P, et al. Hyaluronan concentration and size distribution in human knee synovial fluid: variations with age and cartilage degeneration. Arthritis Res Ther. 2016;18(1):1-8. [9] LI G, YIN J, GAO J, et al. Subchondral bone in osteoarthritis: insight into risk factors and microstructural changes. Arthritis Res Ther. 2013;15(6): 223. [10] 田胜兰,王国延,杨扬.人甲壳质酶蛋白40通过PI3K/Akt信号通路调控膝骨性关节炎兔软骨细胞的凋亡[J].中国组织工程研究, 2020,24(32):5108-5113. [11] HUSSAIN SM, NEILLY DW, BALIGA S, et al. Knee osteoarthritis: a review of management options. Scott Med J. 2016;61(1):7-16. [12] PRIMORAC D, MOLNAR V, ROD E, et al. Knee osteoarthritis: a review of pathogenesis and state-of-the-art non-operative therapeutic considerations. Genes (Basel). 2020;11(8):854. [13] SHI GX, TU JF, WANG TQ, et al. Effect of electro-acupuncture (EA) and manual acupuncture (MA) on markers of inflammation in knee osteoarthritis. J Pain Res. 2020;13:2171-2179. [14] 刘搏宇,李宏宇,席立成,等.不同剂量体外冲击波治疗膝骨性关节炎近期疗效比较[J].中国矫形外科杂志,2020,28(11):908-912. [15] DESANDO G, BARTOLOTTI I, CAVALLO C, et al. Short-term homing of hyaluronan-primed cells: therapeutic implications for osteoarthritis treatment. Tissue Eng Part C Methods. 2018;24(2):121-133. [16] WANG Z, ZHAI C, FEI H, et al. Intraarticular injection autologous platelet‐rich plasma and bone marrow concentrate in a goat osteoarthritis model. J Orthop Res. 2018;36(8):2140-2146. [17] KOCH M, HAMMER S, FUELLERER J, et al. Bone marrow aspirate concentrate for the treatment of avascular meniscus tears in a one-step procedure-evaluation of an in vivo model. Int J Mol Sci. 2019; 20(5):1120. [18] SHAPIRO SA, KAZMERCHAK SE, HECKMAN MG, et al. A prospective, single-blind, placebo-controlled trial of bone marrow aspirate concentrate for knee osteoarthritis. Am J Sports Med. 2017;45(1):82-90. [19] Gobbi A, Scotti C, Karnatzikos G, et al. One-step surgery with multipotent stem cells and Hyaluronan-based scaffold for the treatment of full-thickness chondral defects of the knee in patients older than 45 years. Knee Surg Sports Traumatol Arthrosc. 2017;25(8):2494-2501. [20] THEMISTOCLEOUS GS, CHLOROS GD, KYRANTZOULIS IM, et al. Effectiveness of a single intra-articular bone marrow aspirate concentrate (BMAC) injection in patients with grade 3 and 4 knee osteoarthritis. Heliyon. 2018;4(10):e00871. [21] SHAW B, DARROW M, DERIAN A. Short-term outcomes in treatment of knee osteoarthritis with 4 bone marrow concentrate injections. Clin Med Insights Arthritis Musculoskelet Disord. 2018;11: 1179544118781080. [22] CENTENO CJ, AL-SAYEGH H, BASHIR J, et al. A dose response analysis of a specific bone marrow concentrate treatment protocol for knee osteoarthritis. BMC Musculoskelet Disord. 2015;16:258. [23] KIM JD, LEE GW, JUNG GH, et al. Clinical outcome of autologous bone marrow aspirates concentrate (BMAC) injection in degenerative arthritis of the knee. Eur J Orthop Surg Traumatol. 2014;24(8):1505-1511. [24] CENTENO CJ, PITTS JA, AL-SAYEGH H, et al. Efficacy and safety of bone marrow concentrate for osteoarthritis of the hip: treatment registry results for 196 patients. J Stem Cell Res Ther. 2014;4(242):2. [25] CENTENO C, PITTS J, AL-SAYEGH H, et al. Efficacy of autologous bone marrow concentrate for knee osteoarthritis with and without adipose graft. Biomed Res Int. 2014;2014:370621. [26] CENTENO C J, AL-SAYEGH H, FREEMAN MD, et al. A multi-center analysis of adverse events among two thousand, three hundred and seventy two adult patients undergoing adult autologous stem cell therapy for orthopaedic conditions. Int Orthop. 2016;40(8):1755-1765. [27] SALTZMAN BM, KUHNS BD, WEBER AE, et al. Stem cells in orthopedics: a comprehensive guide for the general orthopedist. Am J Orthop. 2016;45(5):280-326. [28] CAPLAN AI. Review: mesenchymal stem cells:cell-based reconstructive therapy in orthopedics. Tissue Eng. 2005;11(7-8):1198-1211. [29] CHEN FH, TUAN RS. Mesenchymal stem cells in arthritic diseases. Arthritis Res Ther. 2008;10(5):223-223. [30] 高祎,杨柳.骨髓间充质干细胞移植应用于骨科的研究进展[J].中华骨科杂志,2017,37(2):121-128. [31] DE LUCA P, KOUROUPIS D, VIGANÒ M, et al. Human diseased articular cartilage contains a mesenchymal stem cell-like population of chondroprogenitors with strong immunomodulatory responses. J Clin Med. 2019;8(4):423. [32] LAMO-ESPINOSA JM, GONZALO M, BLANCO JF, et al. Intra-articular injection of two different doses of autologous bone marrow mesenchymal stem cells versus hyaluronic acid in the treatment of knee osteoarthritis: long-term follow up of a multicenter randomized controlled clinical trial (phase I/II). J Transl Med. 2018;16(1):213. [33] CENTENO CJ, BUSSE D, KISIDAY J, et al. Increased knee cartilage volume in degenerative joint disease using percutaneously implanted, autologous mesenchymal stem cells, platelet lysate and dexamethasone. Pain Physician. 2008;9(3):246-251. [34] OROZCO L, MUNAR A, SOLER R, et al. Treatment of knee osteoarthritis with autologous mesenchymal stem cells:a pilot study. Transplantation. 2013;95(12):1535-1541. [35] IMAM M A, HOLTON J, HORRIAT S, et al. A systematic review of the concept and clinical applications of bone marrow aspirate concentrate in tendon pathology. Sicot J. 2017;3:58. [36] FILARDO G, PERDISA F, ROFFI A, et al. Stem cells in articular cartilage regeneration. J Orthop Surg Res. 2016;11(1):1-15. [37] CASSANO JM, KENNEDY JG, ROSS KA, et al. Bone marrow concentrate and platelet-rich plasma differ in cell distribution and interleukin 1 receptor antagonist protein concentration. Knee Surg Sports Traumatol Arthrosc. 2018;26(1):333-342. [38] MIYAZAWA K, SHINOZAK M I, HARA T, et al. Two major Smad pathways in TGF-beta superfamily signalling. Genes Cells. 2010;7(12):1191-1204. [39] MARIANI E, PULSATELLI L, FACCHINI A. Signaling pathways in cartilage repair. Int J Mol Sci. 2014;15(5):8667-8698. [40] Chen S, Liu S, Ma K, et al. TGF-β signaling in intervertebral disc health and disease. Osteoarthritis Cartilage. 2019;27(8):1109-1117. [41] 张立智,卫禛,张世民.转化生长因子β信号在骨关节炎中的作用[J].中华骨与关节外科杂志,2019,12(9):727-732. [42] KIM JM, LIN C, STAVRE Z, et al. Osteoblast-osteoclast communication and bone homeostasis. Cells. 2020;9(9):2073. [43] 雷文龙,施斌.血小板衍生生长因子BB在口腔种植领域中的作用[J].国际口腔医学杂志,2014,41(2);199-203. [44] YANG F, LI WB, QU YW, et al. Bone marrow mesenchymal stem cells induce M2 microglia polarization through PDGF-AA/MANF signaling. World J Stem Cells. 2020;12(7):633-658. [45] 刘慧,陈慧鸿,廖红兵.破骨细胞衍生的偶联因子鞘氨醇-1-磷酸及血小板衍生生长因子BB对成骨细胞的调节作用[J].中国组织工程研究,2019,23(23):3739-3745. [46] SETIAWAN IGNY, SUYASA IK, ASTAWA P, et al. Recombinant platelet derived growth factor-BB and hyaluronic acid effect in rat osteoarthritis models. J Orthop. 2019;16(3):230-233. [47] SUYASA IK, LESTARI AAW, SETIAWAN IGNY. Recombinant platelet-derived growth factor-BB and hyaluronic acid stimulates knee cartilage regeneration by forming higher chondrocytes count and lower YKL-40 level in rats model. J Clin Orthop Trauma. 2020; 11(Suppl 1):S76-S79. [48] FORTIER LA, BARKER JU, STRAUSS EJ, et al. The role of growth factors in cartilage repair. Clin Orthop Relat Res. 2011;469(10):2706-2715. [49] YANG YH, ARD MB, HALPER JT, et al. Type i collagen-based fibrous capsule enhances integration of tissue-engineered cartilage with native articular cartilage. Ann Biomed Eng. 2014;42(4):716. [50] CUCCHIARINI M, MADRY H. Overexpression of human IGF-I via direct rAAV-mediated gene transfer improves the early repair of articular cartilage defects in vivo. Gene Ther. 2014;21(9):811-819. [51] EKENSTEDT KJ, SONNTAG WE, LOESER RF, et al. Effects of chronic growth hormone and insulin-like growth factor 1 deficiency on osteoarthritis severity in rat knee joints. Arthritis Rheum. 2006;54(12): 3850-3858. [52] GOODRICH LR, HIDAKA C, ROBBINS PD, et al. Genetic modification of chondrocytes with insulin-like growth factor-1 enhances cartilage healing in an equine model. J Bone Joint Surg Br. 2007;89(5):672-685. [53] 李嘉怡,刘双全,邵瑞,等.成纤维细胞生长因子18对骨和软骨发育[J].中南医学科学杂志,2019,47(1):102-105, 112. [54] ELLMAN MB, AN H S, MUDDASANI P, et al. Biological impact of the fibroblast growth factor family on articular cartilage and intervertebral disc homeostasis. Gene. 2008;420(1):82-89. [55] CINQUE L, FORRESTER A, BARTOLOMEO R, et al. FGF signalling regulates bone growth through autophagy. Nature. 2015;528(7581):272-275. [56] MORI Y, SAITO T, CHANG SH, et al. Identification of fibroblast growth factor-18 as a molecule to protect adult articular cartilage by gene expression profiling. J Biol Chem. 2014;289(14):10192-10200. [57] REKER D, SIEBUHR AS, THUDIUM CS, et al. Sprifermin (rhFGF18) versus vehicle induces a biphasic process of extracellular matrix remodeling in human knee OA articular cartilage ex vivo. Sci Rep. 2020;10(1):6011. [58] FU HD, WANG HR, LI DH. BMP-7 accelerates the differentiation of rabbit mesenchymal stem cells into cartilage through the Wnt/β-catenin pathway. Exp Ther Med. 2017;14(6):5424-5428. [59] MALYSHEVA KV, SPASYUK IM, PAVLENKO OK, et al. Generation of optimized preparations of bone morphogenetic proteins for bone regeneration. Ukr Biochem J. 2016;88(6):87-97. [60] 赵晋,闫振宇,张立智.骨性关节炎软骨和软骨下骨之间信号通路[J].中华骨质疏松和骨矿盐疾病杂志,2016,9(2):193-198. |
| [1] | Yao Xiaoling, Peng Jiancheng, Xu Yuerong, Yang Zhidong, Zhang Shuncong. Variable-angle zero-notch anterior interbody fusion system in the treatment of cervical spondylotic myelopathy: 30-month follow-up [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1377-1382. |
| [2] | Wu Cong, Jia Quanzhong, Liu Lun. Relationship between transforming growth factor beta1 expression and chondrocyte migration in adult articular cartilage after fragmentation [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1167-1172. |
| [3] | Xiao Hao, Liu Jing, Zhou Jun. Research progress of pulsed electromagnetic field in the treatment of postmenopausal osteoporosis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(8): 1266-1271. |
| [4] | An Weizheng, He Xiao, Ren Shuai, Liu Jianyu. Potential of muscle-derived stem cells in peripheral nerve regeneration [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1130-1136. |
| [5] | Tian Chuan, Zhu Xiangqing, Yang Zailing, Yan Donghai, Li Ye, Wang Yanying, Yang Yukun, He Jie, Lü Guanke, Cai Xuemin, Shu Liping, He Zhixu, Pan Xinghua. Bone marrow mesenchymal stem cells regulate ovarian aging in macaques [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 985-991. |
| [6] | Fang Xiaolei, Leng Jun, Zhang Chen, Liu Huimin, Guo Wen. Systematic evaluation of different therapeutic effects of mesenchymal stem cell transplantation in the treatment of ischemic stroke [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1085-1092. |
| [7] | Zhang Jinglin, Leng Min, Zhu Boheng, Wang Hong. Mechanism and application of stem cell-derived exosomes in promoting diabetic wound healing [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1113-1118. |
| [8] | Hou Jingying, Guo Tianzhu, Yu Menglei, Long Huibao, Wu Hao. Hypoxia preconditioning targets and downregulates miR-195 and promotes bone marrow mesenchymal stem cell survival and pro-angiogenic potential by activating MALAT1 [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1005-1011. |
| [9] | Liang Xuezhen, Yang Xi, Li Jiacheng, Luo Di, Xu Bo, Li Gang. Bushen Huoxue capsule regulates osteogenic and adipogenic differentiation of rat bone marrow mesenchymal stem cells via Hedgehog signaling pathway [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1020-1026. |
| [10] | He Junjun, Huang Zeling, Hong Zhenqiang. Interventional effect of Yanghe Decoction on synovial inflammation in a rabbit model of early knee osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 694-699. |
| [11] | Lin Xuchen, Zhu Hainian, Wang Zengshun, Qi Tengmin, Liu Limin, Suonan Angxiu. Effect of xanthohumol on inflammatory factors and articular cartilage in a mouse mode of osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(5): 676-681. |
| [12] | He Yunying, Li Lingjie, Zhang Shuqi, Li Yuzhou, Yang Sheng, Ji Ping. Method of constructing cell spheroids based on agarose and polyacrylic molds [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 553-559. |
| [13] | He Guanyu, Xu Baoshan, Du Lilong, Zhang Tongxing, Huo Zhenxin, Shen Li. Biomimetic orientated microchannel annulus fibrosus scaffold constructed by silk fibroin [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 560-566. |
| [14] | Chen Xiaoxu, Luo Yaxin, Bi Haoran, Yang Kun. Preparation and application of acellular scaffold in tissue engineering and regenerative medicine [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 591-596. |
| [15] | Kang Kunlong, Wang Xintao. Research hotspot of biological scaffold materials promoting osteogenic differentiation of bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 597-603. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||