Chinese Journal of Tissue Engineering Research ›› 2020, Vol. 24 ›› Issue (14): 2256-2262.doi: 10.3969/j.issn.2095-4344.2600
Previous Articles Next Articles
Research progress in constructing animal models of Staphylococcus aureus-associated
osteomyelitis
Liu Jinyue1, Zhang Mengqi2, Qing Mingsong2, Zhao Chuntao2, Peng Jiachen1, 2
- 1Department of Joint Surgery, Affiliated Hospital of Zunyi Medical University, Zunyi 563000, Guizhou Province, China; 2Department of Orthopaedics, Affiliated Hospital of Zunyi Medical University, Zunyi Medical University-Rochester University Orthopedics Research Center, Zunyi 563000, Guizhou Province, China
-
Received:2019-09-16Revised:2019-09-18Accepted:2019-11-25Online:2020-05-18Published:2020-03-16 -
Contact:Peng Jiachen, MD, Professor, Chief physician, Department of Joint Surgery, Affiliated Hospital of Zunyi Medical University, Zunyi 563000, Guizhou Province, China; Department of Orthopaedics, Affiliated Hospital of Zunyi Medical University, Zunyi Medical University-Rochester University Orthopedics Research Center, Zunyi 563000, Guizhou Province, China -
About author:Liu Jinyue, Master candidate, Department of Joint Surgery, Affiliated Hospital of Zunyi Medical University, Zunyi 563000, Guizhou Province, China -
Supported by:the National Natural Science Foundation of China, No. 81760400
CLC Number:
Cite this article
Liu Jinyue, Zhang Mengqi, Qing Mingsong, Zhao Chuntao, Peng Jiachen.
Research progress in constructing animal models of Staphylococcus aureus-associated
osteomyelitis
share this article
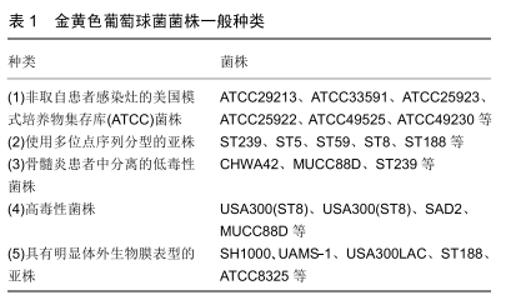
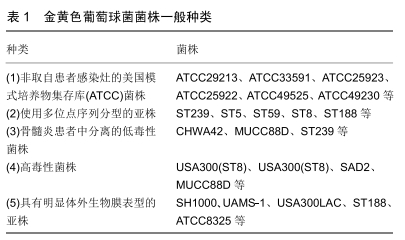
2.1 金黄色葡萄球菌性骨髓炎模型构建中模型动物的选择 模型动物中最常用的动物是兔、大鼠和小鼠,而大型动物如狗、猪和山羊具有较大的骨骼和关节,可以应用近似人体内固定装置和关节假体,但由于实验成本高,且具有攻击性,目前还没有将其作为常规实验动物[7]。 大鼠和小鼠均具有能耐受广谱抗生素治疗、体积小容易处置、对空间的需求低、生长时间短、产仔数大、饲养成本低等优点,成为大多数骨髓炎发病机制研究的首选模式动物[4,8],然而,鼠体型和解剖特点限制了生物载药系统的研究。鼠不能模拟人类对脂多糖,细胞毒素和SAgs的抗性,这被认为是金黄色葡萄球菌感染的鼠模型的主要缺陷[4]。在分子水平上,鼠模型很难反映出人体炎症性疾病的分子机制,到目前为止,金黄色葡萄球菌感染的小鼠模型未能预测人类临床试验的结果[9],SALGADO-PABóN等[4]甚至认为,对小鼠模型的依赖,阻碍了对金黄色葡萄球菌菌株毒力的理解。 在骨髓炎模型的相关报道中,兔性格温顺,大小合适,易于操作,饲养成本较大型动物低,解剖结构与人类类似,可以更好地模拟人类骨髓炎的发展过程,占该领域所有报道研究的35%,新西兰兔是最适合骨感染研究的品系[10]。然而兔对麻醉药、镇痛药、抗生素敏感性更高,需要专门的护理以减少动物疼痛和异常行为,另外一个限制是需严格控制病原菌,因此需要为兔提供特定的SPF设施[11]。兔的胫骨(60.9%)和股骨(27%)是使用最多的手术部位,其大小允许按部分关节成形术和骨折复位内、外固定的要求植入类似于人类使用的矫形装置[12]。作为感染动物而言,兔的免疫反应与人类在自然感染时产生的免疫反应相似,具有相同的抗原亚群和相同的细菌清除机制,兔对再感染产生免疫力,且兔的免疫系统在遗传上比啮齿动物的基因更接近人类,在组织和细胞组织上仅有很小的差异,其对感染的敏感性和发病机制与人类相似[13]。由于这些原因,研究者们期望兔可以用来预测人类骨髓炎进展[4,14]。 2.2 金黄色葡萄球菌性骨髓炎模型常用亚株 在之前的相关研究中,更多学者使用的金黄色葡萄球菌菌株为非取自患者感染灶的美国模式培养物集存库(ATCC)菌株[14-16],还有一些研究人员使用多位点序列分型(multilocus sequence typing,MLST)的亚株构建骨髓炎模型[14,17-18];就细菌毒力而言,部分研究者使用骨髓炎患者中分离的低毒性菌株、部分高毒性菌株构建骨髓炎模型并研究毒力对骨感染模型构建的影响[17-18];具有明显体外生物膜表型亚株常被用来构建生物膜模型[14,19-20](金黄色葡萄球菌菌株一般种类见表1)。抗生素敏感菌株最常引起内置物相关感染,SHIELS等[21]利用特质明确的甲氧西林敏感性骨髓炎分离亚株Uams(ATCC49230)成功制备内置物相关骨髓炎模型。生物发光菌株如甲氧西林敏感的Xen29菌株和耐甲氧西林的Xen 31、耐甲氧西林UAMS-1的发光型Xen40常被用来动态观察感染部位菌量变化[21-22]。然而,细菌的毒力与感染类型的关系仍存在争议,一方面,一些研究已经肯定了高毒性的菌株会引起严重的感染[23];另一方面,最近的一项研究并没有找到毒性升高与感染严重程度之间的关联[24]。TUCHSCHERR等[17]对多部位临床骨髓炎分离菌株进行研究发现低细胞毒性菌株比高毒性菌株这在宿主细胞中的存活率更高,更易发展为慢性感染,低细胞毒性菌株的分离物,将有助于优化复杂难治性骨感染的治疗策略。 "

2.3 金黄色葡菌浓度及接种方式 目前文献报道的接种方式分为动、静脉注射接种、局部注射接种[25]。EMSLIE等[26]初次报告了从鸡翼静脉注射细菌制备纯血源性骨髓炎模型。POUHSIDES等[27]向兔股动脉内注入1 mL不等量[1×104-5×108个菌落形成单位(Colony-Forming Units,CFU)]MR金黄色葡萄球菌菌株,发现接种量≤3× 108 CFU/mL所有实验兔均存活,4周后仅有20%实验兔出现血源性感染,而接种≤1×108 CFU/mL不会导致全身或局部感染,接种量为5×108 CFU/mL实验组所有兔均在48-72 h死于脓毒性休克,说明血源性骨髓炎造模具有相当的难度和不稳定性。 另一种方法为局部注射接种,包括钻孔后注射细菌和置入物浸泡细菌悬液后置入。有研究者通过实验证实,细菌接种同时使用硬化剂封闭是构建骨髓炎模型的必要条件[28]。另一些人使用骨蜡来限制细菌并削弱骨骼清除感染的能力[29-30]。就细菌浓度而言,为了促进感染迹象,通常使用远远超过1×103 CFU的细菌计数[28],SMELTZER等[31]用兔制备骨缺损感染模型研究中发现,至少需植入1×105 CFU菌液才能保证实验的成功率在95%以上。但高浓度的细菌负荷不能很好模拟临床初次手术或者翻修手术的特征,对于已经造成置入物相关感染的患者,再次植入内植物时认为是一个相对无菌的环境,只能假设有少量不可被检测到的细菌残留,因此,使用接种细菌浓度远远超过103 CFU菌液构建动物模型时很难模拟临床情况进行研究。部分研究者开始考虑使用低浓度菌株构建骨髓炎模型,HARRASSER等[15]发现使用低剂量细菌浓度(1×102和1×103 CFU)也可以有效的诱导局部感染,这可能与选择合适的金黄色葡萄球菌亚株(ATCC25923)、细菌活性较好有关。由于几种关键参数例如细菌浓度,细菌菌株,骨缺损大小、部位,植入物构型,植入物位置在各种模型之间不同,使得彼此之间的比较变得困难,对骨感染的影响还有待进一步研究。 2.4 骨感染动物模型的构建 在人骨感染发展进程中,将发病时间在4周内的骨髓炎称为急性骨髓炎,多为血源性骨髓炎;感染时程超过4周的骨髓炎称为慢性骨髓炎,多由手术、开放性骨折或者由周围组织蔓延感染引起的外源性骨髓炎。但骨髓炎发病机制复杂,且变异度高,所以上述分类方法难以应用于临床[1],且在动物模型中由于模式动物、造模方法的差异,更难以通过感染时间节点区分急慢性骨髓炎动物模型,但文献中多为慢性骨髓炎动物模型。骨感染动物模型的构建与菌株接种方式、菌液浓度、置入物的种类与置入部位、骨缺损等因素密切相关,即使消除了大多数混杂因素,也难以统一量化,近年来各国研究者对此不断进行改进并逐渐量化感染过程。 2.4.1 置入物相关骨髓炎动物模型的制备 置入物相关骨髓炎模型通常通过局部注入细菌后置入内置物或将细菌感染后的内置物置入动物骨组织中,为模拟内固定术后或翻修术后骨感染过程,细菌浓度低,排除了骨折、骨缺损等相关因素影响。早期由Norden报道的骨髓炎模型构建方法,在兔胫骨内先注射硬化剂鱼肝油酸钠后注射金黄色葡萄球菌,并在90%的感染胫骨中培养出细菌,该方法得到国内外许多研究者的进一步改进,目前已成为制备慢性骨髓炎的常用方法[32]。在Norden模型基础上,有众多研究者报道应用局部抗生素载体以评估新型抗生素治疗,MISTRY等[32]在兔胫骨钻1 mm小孔进入骨髓腔,注射耐甲氧西林金黄色葡萄球菌(MRSA)悬液进入骨髓腔后以骨蜡封闭开孔,诱导骨髓炎成功后,置入抗生素复合骨水泥探究其安全性及抗菌有效性。随后更多研究者将克氏针或金属丝等作为金属异物置入大鼠胫骨骨髓腔诱导慢性骨髓炎。干骺端固定诱发骨髓炎在骨科置入物的临床应用中更常见,HARRASSER等[15]在大鼠胫骨干骺端钻孔后置入一特制实心钛螺丝,植入物与骨组织能最大贴合,避免了空心内置物为细菌提供受保护空间从而逃脱了宿主的防御机制的缺点。临床内置物置入术后或人工关节置换术后,由于血源性感染常会诱发置入物相关骨髓炎,为模拟这一感染类型,SHIELS等[21]将钛克氏针置入大鼠双侧股骨骨髓腔内,于鼠尾静脉中注入1×104-1×109 CFU/mL金黄色葡萄球菌300 μL,当注射浓度达107 CFU/mL时,75%大鼠出现临床意义的骨感染。 既往研究多数为骨髓炎定性模型,由于缺乏能动态时序性量化细菌负荷、细菌活性和骨溶解的体内模型,骨感染研究进展受到了限制。LI等[22]将细针从鼠胫骨干骺端经皮植入制备置入物相关骨感染模型,该模型通过金黄色葡萄球菌特异性nuc基因进行实时定量PCR(RTQ-PCR)检测、生物发光成像(BLI)技术、血清学监测,首次定量描述分析了细菌负荷和活性、骨溶解和体液免疫的动态变化。ODEKERKEN等[29]在兔胫骨骨髓腔置入由金黄色葡萄球菌接种的2 cm钛钉后骨蜡封闭缺口,证实2周后可以区分是否出现内置物感染,并通过改良X射线评分系统、钙结合荧光检测,时序性动态分析植入物感染及骨溶解过程,然而一些重要参数如生物发光细菌诱导种植体感染或种植体表面生物膜形成过程评估未包含在内。 2.4.2 开放性骨折相关骨髓炎动物模型的制备 开放性骨折骨髓炎模型为模拟骨科开放性骨折内固定术后骨感染,对模式动物制作骨折模型后用钢板螺钉内固定,相对于单纯内置物相关骨髓炎模型、骨缺损模型,细菌浓度高,受到骨折术后稳定性的影响,但排除了骨缺损影响。ASHHURST等[30]于1982年使用钢锯造成兔胫骨骨折,用钢板固定,首次报道了这一动物模型。HAMEL等[33]在此基础上进行改进,对兔双侧胫骨截骨后注入108 CFU/mL耐甲氧西林金黄色葡萄球菌,予以髓内钉固定。置入物的稳定性是影响骨感染结果的一个重要因素,这些模型由于技术限制缺乏旋转稳定性,为解决这一问题,TER BOO等[34]造成兔肱骨骨折后,用金黄色葡萄球菌污染的钢板、螺钉进行固定,以评估抗生素涂层抗菌效果。LOVATI等[35]对大鼠右股骨中段行截骨术后以4颗1.5 mm双皮质螺钉及一块不锈钢四孔迷你板固定,成功制备了大鼠骨折相关骨髓炎模型。ZHANG等[36]使用不锈钢板固定右肱骨干后再用线锯进行截骨术,同时使用肱骨也减少了手术肢体的负重,重要的是,强烈建议在截骨术完成前进行部分钢板固定,以克服解剖复位的困难。 2.4.3 骨髓炎骨缺损动物模型的构建 骨髓炎骨缺损动物模型一般需要作一大小骨缺损后注入菌液封口,排除了内置物、骨折等相关因素影响。由于动物骨髓炎骨缺损模型受创伤方式、骨缺损大小、缺损部位血供、对软组织损伤程度、接种细菌浓度及接种方式等多种因素的影响,很难形成统一的量化标准[37]。临床上骨缺损部位常发生在负重骨,胫骨、股骨等负重骨成为优选部位[14]。WANG等[16]采用Norden方法在兔胫骨骨髓腔作一0.3 mm钻孔,注入0.1 mL含3×107 CFU/mL金黄色葡萄球菌的肉汤,骨蜡封口,操作简单,较好地形成节段性骨缺损感染模型。GAO等[38]通过测定1 cm临界尺寸的桡骨缺损建立的家兔骨髓炎模型,评估载抗生素支架预防或治疗骨髓炎效果。TROMBETTA等[39]去除小鼠中段股骨后用生物发光氙接种的钛螺钉固定股骨建立一期、二期翻修模型,将含有利福平、西沙他星的磷酸钙支架置入骨缺损部位,验证抗生素的释放动力学。为了更好地模拟临床,一些作者倾向于在没有硬化剂的情况下直接注射细菌,ZAHAR等[40]在兔胫骨干骺端作一5 mm骨缺损后直接注入金黄色葡萄球菌菌液,成功诱导骨髓炎,感染率为67.5%。硬化剂虽然可以提高成功率,但引起宿主无菌性炎症反应,对结果造成偏倚,关于硬化剂的使用仍存在争议。 2.4.4 生物膜模型的构建 在不同的动物模型中金黄色葡萄球菌通过生物膜中建立的慢性骨髓炎来逃避宿主免疫反应[1,10,41]。大约60%的骨感染与生物膜有关[41],生物膜的形成是置入物相关感染机制的核心,目前大量研究者希望通过生物膜模型揭示生物膜感染机制及治疗措施。大多数生物膜模型为体外模型,SWEENEY等[20]在1 cm3牛股骨骨块钻孔接种10 μL金黄色葡萄球菌培养液后培养72 h制备体外生物膜模型,以评估抗生素清除类似坏死骨表面的成熟生物膜的能力。NISHITANI等[19]用金黄色葡萄球菌亚株SH1000、UAMS-1、USA300LAC污染的不锈钢钢针感染C57BL/6和Balb/c小鼠,证明植入物上的生物膜在第1天内建立,然后在Balb/c小鼠感染生物膜第3天达到峰值的强烈增殖期,在C57BL/6小鼠中持续至第7天,生物膜形成在第14天达到顶峰。SURDU-BOB等[42]研究了不同表面积的各种异物,以增加生物膜形成和感染定位的机会,基于棉网的模型提供了更高的表面积,形成感染时间最短,具有最高的动物存活率(90%)和最高的疾病发病率(90%)。此外,该方法确保了对动物的最小侵入和减少痛苦,并且在治疗施用之前可以容易地去除异物。传统体外模型多局限于二维细胞培养,不能模拟体内骨髓环境。RAIC等[43]开发了一种三维体外膜型,以3D打印仿生支架模拟与人体骨小梁相似的空间结构,人造血干细胞、祖细胞、间充质干细胞模拟人类骨髓环境,能在体外模拟人体内金黄色葡萄球菌生物膜附着和成熟过程,为生物膜感染的早期研究和治疗提供了基础。 置入物、开放性骨折、骨缺损、生物膜形成导致感染的病因、疾病发展机制及治疗进展是目前骨科研究热点[1,35],上述骨髓炎动物模型为模拟临床骨髓炎疾病发展过程中的实际情况进行分类,动态分析并量化了骨感染过程,但骨髓炎发病机制复杂,且变异度高,常为开放性骨折、内置物、骨缺损、细菌生物膜形成等多种混杂因素共同影响,难以进行单因素横向分析比较,但仍增加了对金黄色葡萄球菌分子发病机制和感染的保护性免疫机制的正确认识,为临床新的预防及干预措施的研究提供了依据。 2.5 骨感染动物模型评价方式 在金黄色葡萄球菌性骨髓炎模型构建完成后,骨髓炎模型的观察及相关指标的检测是判断造模是否成功及感染严重程度的重要指标。常用的检测方法除常规大体观的观察,还包括组织学、影像学、微生物学检测等多个方面。 影像学评价:骨髓炎病变必须达1 cm3并导致骨矿物质含量减少30%-50%时才能被X射线识别,故常规放射摄影在早期检测急性骨髓炎缺乏敏感性和特异性,特别是在使用低细菌浓度来产生感染的情况下,CT和MRI常在骨感染发生后3-5 d即能发现病变,但其图像质量会受到内置物所产生的伪影所影响,还会因为对组织的水肿和瘢痕过于敏感而对诊断产生误差[44]。随着影像学技术的发展,通过高分辨率(10.5 μm)微计算机断层扫描(micro-CT)分析骨感染部位,选择某一更加均匀、一致、对比性较强的骨溶解区域加以标记,即可使用该面积测量来定量描述该组的溶骨性皮质损伤的最大尺寸,使大体观察到的影像学变化能够更精确的转换为数值进行比较[45]。18F-FDG PET/CT作为尖端功能成像,受到内置物的影响很小,对于确认或排除慢性骨髓炎有很高的诊断准确性,AFZELIUS等[44]的研究中,18F-FDG PET/CT在急性期感染时甚至可以识别<0.01 cm3骨髓炎病变,但因其具有较强的电离辐射,且造价昂贵,在一些欠发达国家和地区仍未普及,因而限制其使用。现大量研究集中监测动物模型血液学、放射学等参数并结合组织学或细菌培养结果了解感染进展,但常需预定时间点处死多个实验动物组,需要大量的动物,ODEKERKEN等[29]结合了基于感染引起的骨形态学变化的X射线照片和micro-CT评分、及基于多个组织形态学感染参数的累积组织学评分所改良的评分系统对感染进行明确分类并纵向评估骨感染状态,所注射的3种钙结合荧光团能够动态观察骨溶解、骨重建过程,可有效减少实验动物数量。虽然先进的影像学技术已经用于定位、定量研究活动性感染区域,但即使是与细菌结合的靶向成像方法也不能区分浮游生物和固有细菌,也没有办法在清创术中、术后真正识别生物膜,且这些技术在动物研究与临床应用之间存在巨大的差距[41]。 微生物学评价:量化细菌负荷的传统方法是菌落计数(CFU),由于钙化基质和生物膜不能有效地从受感染的骨中提取活细菌以量化体内细菌负荷,在早期的研究中,LI等[22]展示了两种克服这一障碍的方法:nuc RTQ-PCR技术和生物荧光成像技术(BLI)。nuc RTQ-PCR是一种成功使用的高度特异性和敏感性的量化金黄色葡萄球菌负荷的方法。虽然RTQ-PCR研究结果证明其能够量化体内细菌负荷,但因无法区分生物膜内代谢活性菌和休眠菌,不能从活体动物中提取nuc基因限制了其使用,利用荧光素、吲哚青绿和IRDye-800CW的光学成像技术有鉴别感染部位表面和附近浮游微生物的潜力[41]。随着金黄色葡萄球菌研究领域的深入,开发一种生物膜形成前后细菌代谢活性的替代结果的测量方法非常具有价值。NISHITANI等[19]利用BLI技术监测生物发光细菌光子,无需处死动物即可了解细菌代谢状态,并通过测量标记区域细菌数量,量化细菌生长过程。 目前并无单一微生物学或影像学检查方式明确骨感染。在急性骨髓炎动物模型中,细菌代谢活性强,骨病变通常发生在骨感染3-5 d后,常规影像学检查缺乏敏感性和特异性,且图像易收到内置物伪影的影响[44],nuc RTQ-PCR技术和生物荧光成像技术(BLI)等微生物学检测能够早期动态监测并量化骨感染过程;对于慢性骨髓炎动物模型,并无文献报道微生物学、影像学何种检查方式更具有优势,此时细菌代谢趋于稳定,微生物学检测虽然能够量化细菌负荷变化,但无法区分代谢活性菌和休眠菌,micro-CT、MRI等影像学技术能动态观察骨溶解、骨重建过程,且18F-FDG PET/CT等尖端成像技术确认或排除慢性骨髓炎有很高的诊断准确性[44]。 "

| [1] SCHMITT SK. Osteomyelitis.Infect Dis Clin North Am.2017; 31(2):325-338. [2] BIRT MC, ANDERSON DW, BRUCE TOBY E, et al. Osteomyelitis: Recent advances in pathophysiology and therapeutic strategies.J Orthop.2017;14(1):45-52. [3] KUBES JN, FRIDKIN SK. Factors affecting the geographic variability of antibiotic-resistant healthcare-associated infections in the United States using the CDC Antibiotic Resistance Patient Safety Atlas.Infect Control Hosp Epidemiol. 2019;40(5):597-599. [4] SALGADO-PABÓN W, SCHLIEVERT PM. Models matter: the search for an effective Staphylococcus aureus vaccine.Nat Rev Microbiol. 2014;12(8):585-591. [5] HORST SA, HOERR V, BEINEKE A, et al. A Novel Mouse Model of Staphylococcus aureus Chronic Osteomyelitis That Closely Mimics the Human Infection.Am J Pathol. 2012; 181(4):1206-1214. [6] DELEO FR, CHAMBERS HF. Reemergence of antibiotic-resistant Staphylococcus aureus in the genomics era.J Clin Invest. 2009;119(9):2464-2474. [7] HOHMER EA, KIRKHAM J, WOOD D, et al. Long bone defect models for tissue engineering applications: criteria for choice.J Tissue Eng Part B Rev.2010;16(2): 263-271. [8] PERLMAN RL. Mouse Models of Human Disease: An Evolutionary Perspective.Evol Med Public Health. 2016; 2016(1):170-176. [9] FOWLER VG, PROCTOR RA. Where does a Staphylococcus aureus vaccine stand? Clin Microbiol Infect. 2014;20(6): 66-75. [10] PEARCE AI, RICHARDS RG, MILZ S, et al. Animal models for implant biomaterial research in bone: A review. Eur Cell Mater.2007;13(3):1-10. [11] MAPARA M, THOMAS BS, BHAT KM. Rabbit as an animal model for experimental research.J Dent Res J.2012;9(1): 111-118. [12] MILLER RJ, THOMPSON JM, ZHENG J, et al. In Vivo Bioluminescence Imaging in a Rabbit Model of Orthopaedic Implant-Associated Infection to Monitor Efficacy of an Antibiotic-Releasing Coating.J Bone Joint Surg Am. 2019; 101(4):e12. [13] ESTEVES PJ, ABRANTES J, BALDAUF HM, et al. Author Correction: The wide utility of rabbits as models of human diseases.Exp Mol Med. 2019;51(7):71. [14] BOTTAGISIO M, COMAN C, LOVATI AB. Animal models of orthopaedic infections. A review of rabbit models used to induce long bone bacterial infections.J Med Microbiol. 2019; 68(4):506-537. [15] HARRASSER N, GORKOTTE J, OBERMEIER A, et al. A new model of implant-related osteomyelitis in the metaphysis of rat tibiae.BMC Musculoskelet Disord. 2016;17:152. [16] WANG Q, CHEN C, LIU W, et al. Levofloxacin loaded mesoporous silica microspheres/nano-hydroxyapatite/ polyurethane composite scaffold for the treatment of chronic osteomyelitis with bone defects. Scientific Reports. 2017,7: 41808. [17] TUCHSCHERR L, PÖLLATH C, SIEGMUND A, et al. Clinical S. aureus Isolates Vary in Their Virulence to Promote Adaptation to the Host.Toxins (Basel). 2019;11(3). pii: E135. [18] WANG Y, LIU Q, LIU Q, et al. Phylogenetic analysis and virulence determinant of the host-adapted Staphylococcus aureus lineage ST188 in China.Emerg Microbes Infect. 2018; 7(1):45. [19] NISHITANI K, SUTIPORNPALANGKUL W, DE MESY BENTLEY KL, et al. Quantifying the natural history of biofilm formation in vivo during the establishment of chronic implant-associated Staphylococcus aureus osteomyelitis in mice to identify critical pathogen and host factors.J Orthop Res. 2015;33(9):1311-1319. [20] SWEENEY E, LOVERING AM, BOWKER KE, et al. An in vitro biofilm model of Staphylococcus aureus infection of bone.J Letters in Applied Microbiology.2019;68(4):294-302. [21] SHIELS SM, BEDIGREW KM, WENKE JC. Development of a hematogenous implant-related infection in a rat model.BMC Musculoskelet Disord. 2015;16:255. [22] LI D, GROMOV K, SØBALLE K, et al. Quantitative mouse model of implant-associated osteomyelitis and the kinetics of microbial growth, osteolysis, and humoral immunity.J Orthop Res. 2008;26(1):96-105. [23] SEIDL K, BAYER AS, MCKINNELL JA, et al. In vitro endothelial cell damage is positively correlated with enhanced virulence and poor vancomycin responsiveness in experimental endocarditis due to methicillin-resistant Staphylococcus aureus.J Cellular Microbiology.2011;13(10):1530-1541. [24] MAISEM L, ANNE-CATRIN U, LOWY FD, et al. Evolutionary Trade-Offs Underlie the Multi-faceted Virulence of Staphylococcus aureus.J PLOS Biology.2015;13(9):e1002229-. [25] BURR DB, COOK LT, CILENTO EV, et al. A method for radiographically measuring true femoral rotation.Clin Orthop Relat Res. 1982;(167):139-144. [26] EMSLIE KR, OZANNE NR, NADE SM. Acute haematogenous osteomyelitis: An experimental model.J Pathol. 1983;141(2):157-167. [27] POULTSIDES LA, PAPATHEODOROU LK, KARACHALIOS TS, et al. Novel model for studying hematogenous infection in an experimental setting of implant-related infection by a community-acquired methicillin-resistant S. aureus Strain.J Orthop Res. 2008;26(10):1355-1362. [28] SVENSSON S, SUSKA F, EMANUELSSON L, et al. Osseointegration of titanium with an antimicrobial nanostructured noble metal coating.Nanomedicine. 2013; 9(7):1048-1056. [29] ODEKERKEN JC, ARTS JJ, SURTEL DA, et al.A rabbit osteomyelitis model for the longitudinal assessment of early post-operative implant infections.J Orthop Surg Res. 2013;8:38. [30] ASHHURST DE, HOGG J, PERREN SM.A method for making reproducible experimental fractures of the rabbit tibia.Injury. 1982;14(3):236-242. [31] SMELTZER MS, THOMAS JR, HICKRAON SG, et al. Characterization of a rabbit model of staphylococcal osteomyelitis.J Orthop Res. 1997;15(3):414-421. [32] MISTRY S, ROY S, MAITRA NJ, et al. A novel, multi-barrier, drug eluting calcium sulfate/biphasic calcium phosphate biodegradable composite bone cement for treatment of experimental MRSA osteomyelitis in rabbit model.J Control Release. 2016;239:169-181. [33] HAMEL A, CAILLON J, JACQUELINE C, et al. Internal device decreases antibiotic’s efficacy on experimental osteomyelitis. J Child Orthop. 2008;2(3):239-243. [34] TER BOO GA, ARENS D, METSEMAKERS WJ, et al. Injectable gentamicin-loaded thermo-responsive hyalu-ronic acid derivative prevents infection in a rabbit model.J Acta Biomater.2016;43(7):185-194. [35] LOVATI AB, ROMANÒ CL, BOTTAGISIO M, et al.Modeling Staphylococcus epidermidis-Induced Non-Unions: Subclinical and Clinical Evidence in Rats.PLoS One. 2016;11(1): e0147447. [36] ZHANG X, MA YF, WANG L, et al. A rabbit model of implant-related osteomyelitis inoculated with biofilm after open femoral fracture.J Exp Ther Med.2017;14(5): 4995-5001. [37] GAJDOBRANSKI D, MITKOVIC M, NADA VUCKOVIĆ, et al. Influence of Different Methods of Internal Bone Fixation on Characteristics of Bone Callus in Experimental Animals.J Srpski arhiv za celokupno lekarstvo.2014;142(1-2):40-47. [38] GAO J, HUANG G, LIU G, et al.A biodegradable antibiotic-eluting PLGA nanofiber-loaded deproteinized bone for treatment of infected rabbit bone defects.J Biomater Appl. 2016;31(2):241–249. [39] TROMBETTA RYAN P, NINOMIYA MARK J, EL-ATAWNEH IHAB M, et al. Calcium Phosphate Spacers for the Local Delivery of Sitafloxacin and Rifampin to Treat Orthopedic Infections: Efficacy and Proof of Concept in a Mouse Model of Single-Stage Revision of Device-Associated Osteomyelitis.J Pharmaceutics.2019;11(2):94. [40] ZAHAR A, KOCSIS G, CITAK M, et al. Use of antibiotic- impregnated bone grafts in a rabbit osteomyelitis model.J Technol Heal Care.2017;25(5):929-938. [41] SAEED K, MCLAREN AC, SCHWARZ EM, et al. 2018 international consensus meeting on musculoskeletal infection: Summary from the biofilm workgroup and consensus on biofilm related musculoskeletal infections.J Orthop Res. 2019; 37(5):1007-1017. [42] SURDU-BOB CC, COMAN C, BARBUCEANU F, et al. The influence of foreign body surface area on the outcome of chronic osteomyelitis.J Med Eng Phys.2016;38(9):870–876. [43] RAIC A, RIEDEL S, KEMMLING E, et al.Biomimetic 3D in vitro model of biofilm triggered osteomyelitis for investigating hematopoiesis during bone marrow infections.J Acta Biomater. 2018;73(4):250-262. [44] AFZELIUS P, NIELSEN OL, SCHØNHEYDER HC, et al. An untapped potential for imaging of peripheral osteomyelitis in paediatrics using [18 F]FDG PET/CT-the inference from a juvenile porcine model.EJNMMI Res. 2019;9(1):29. [45] KOEFOED M, ITO H, GROMOV K, et al. Biological Effects of rAAV-caAlk2 Coating on Structural Allograft healing.Molecular Therapy.2005;12(2):212-218. |
| [1] | Hua Haotian, Zhao Wenyu, Zhang Lei, Bai Wenbo, Wang Xinwei. Meta-analysis of clinical efficacy and safety of antibiotic artificial bone in the treatment of chronic osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(6): 970-976. |
| [2] | Li Xingping, Xiao Dongqin, Zhao Qiao, Chen Shuo, Bai Yiguang, Liu Kang, Feng Gang, Duan Ke. Preparation and properties of copper-loaded antibacterial functional film on titanium surface [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 553-557. |
| [3] | Liu Fei, Cui Yutao, Liu He. Advantages and problems of local antibiotic delivery system in the treatment of osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 614-620. |
| [4] | Li Wenhui, Liu Guobin. Knowledge mapping analysis on the international research of diabetic foot: a visual analysis based on CiteSpace [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(20): 3178-3184. |
| [5] | Chen Yutong, Li Chenchen, Liu Yang, Zheng Yaqin, Yang Xihua, An Meiwen. Establishment of an acute radioactive skin injury model in Wistar rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(2): 237-241. |
| [6] | Wang Yan, Dong Benchao, Wang Ying, Sun Lei, Lu Bin, Bai Haohao, Tian Aixian, Ma Jianxiong, Ma Xinlong. Animal models of osteonecrosis of the femoral head: modeling methods and characteristics [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(2): 292-297. |
| [7] | Ma Dujun, Peng Liping, Chen Feng, Jiang Shunwan, Jiang Jinting, Gao Kun, Lin Zhanpeng. Research strategy of gene editing technology in the gene treatment of osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(2): 298-303. |
| [8] | Tian Lin, Shi Xiaoqing, Mao Jun, Zhang Nongshan, Zhang Li, Xing Runlin, Wang Peimin. Meta-analysis of vacuum-sealing drainage combined with antibiotic bone cement in the treatment of chronic osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(16): 2618-2624. |
| [9] | Xu Canhong, Meng Lin, Dong Panfeng, Zhan Huasong, Song Shilei. Masquelet technique in treatment of infectious nonunion: a meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(15): 2445-2452. |
| [10] | Liu Hong, Wan Zhe, Zhang Zhen, Zhang Qin. Relationship between root resorption and intrusive force during maxillary molar intrusion in Beagle dogs [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(14): 2172-2176. |
| [11] | Mo Caifeng, Cheng Xiaoyang, Liao Ming, He Dongling, Huang Zhi. A Guangxi Bama minipig model of Trimeresurus stejnegeri snakebite: modeling and evaluation [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(11): 1688-1692. |
| [12] | Xiong Guobing, Liu Aibo, Wang Shize, Wang Yu, Qiu Mingxing. Urine turbulent shear stress system of bionic human bladder based on bacterial biofilm reactor: in vitro construction#br# [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(10): 1560-1565. |
| [13] | Ruan Guangping, Yao Xiang, Cai Xuemin, Li Zian, Pang Rongqing, Pan Xinghua. Effect of umbilical cord mesenchymal stem cell transplantation for treating systemic lupus erythematosus in a tree shrew model [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(1): 90-95. |
| [14] | Ma Jinchao, Liu Tiansheng, Liu Aipeng, Wang Hao, Wang Qi, Liang Yongjian, Wang Lin, Di Haiwei. Photodynamic antimicrobial chemotherapy for repairing a rabbit model of osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(8): 1254-1259. |
| [15] | Wang Jing, Lu Changfeng, Peng Jiang, Zhu Chen, Xu Wenjing, Cheng Xiaoqing, Fang Jie, Zhu Yaqiong, Zhao Yanxu, Jiang Wen, Xu Hongguang, Wang Yu. Establishment and evaluation of traumatic neuroma model [J]. Chinese Journal of Tissue Engineering Research, 2020, 24(5): 716-719. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||