Chinese Journal of Tissue Engineering Research ›› 2020, Vol. 24 ›› Issue (11): 1769-1776.doi: 10.3969/j.issn.2095-4344.1995
Previous Articles Next Articles
Selection of animal models of osteoarthritis
Liu Xiaochen1, Fu Weili2
- 1West China School of Medicine, Sichuan University, Chengdu 610041, Sichuan Province, China; 2Department of Orthopedics, West China Hospital of Sichuan University, Chengdu 610041, Sichuan Province, China
-
Received:2019-04-01Revised:2019-04-17Accepted:2019-06-12Online:2020-04-18Published:2020-02-29 -
Contact:Fu Weili, MD, Associate professor, Department of Orthopedics, West China Hospital of Sichuan University, Chengdu 610041, Sichuan Province, China -
About author:Liu Xiaochen, West China School of Medicine, Sichuan University, Chengdu 610041, Sichuan Province, China -
Supported by:the National Natural Science Foundation of China, No. 31741046; the Basic Research Foundation of Central Colleges and Universities, No. 2015SCU04A40; the Innovation Spark Project Library of Sichuan University, No. 2018SCUH0034; the Health and Family Planning Commission of Sichuan Province, No. 18ZD017
CLC Number:
Cite this article
Liu Xiaochen, Fu Weili. Selection of animal models of osteoarthritis[J]. Chinese Journal of Tissue Engineering Research, 2020, 24(11): 1769-1776.
share this article

2.1 实验动物的选择 有各种各样的动物被用作人类骨关节炎模型的塑造,不同的动物在大小、关节解剖、生物习性和生长发育等方面都有不同。有小的啮齿动物模型,如小鼠,大的动物模型如猪、羊,还有与人类最为相似的灵长动物模型。不同动物模型有不同的关节解剖结构和特定的关节组织特征,这些将影响骨关节炎在特定关节内的发展。人类虽然与其他的哺乳动物在关节结构、半月板、韧带和软骨的相对尺寸上比较相似,但各个物种间关节内部的形态结构差异仍然很大。而膝关节的大小、形态,以及与股骨和胫腓骨的关系都会影响膝关节的生物力学结构,从而造成不同动物的关节组织退变的速度和形态及病理变化可能截然不同。而且关节的总解剖结构、软骨细胞密度和代谢差异不仅会影响特定骨关节炎模型的结果,还会影响特定模型治疗干预的结果[2]。不同的动物可能在某一方面与人类相似,如关节结构、大小或者生活习性,因而可以用于不同因素或损伤导致的骨关节炎模型的塑造。而不同的动物在实验中有着他们各自的优缺点,人们可以根据实际情况选择应用不同的动物模型。而要选择骨关节炎动物模型进行骨关节炎研究,必须考虑以下参数:动物护理、成本、易用性、疾病进展以及对特定治疗方案的反应[3]。见表1。 "

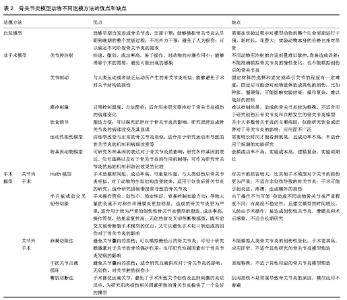
2.1.1 小鼠 作为一种常用的实验动物,同人类一样为哺乳动物,其解剖结构有相似之处,生物力学相似,都有发生骨关节炎的可能。小鼠的骨骼成熟时间约为10周。其有易于获取、价格便宜、容易饲养、寿命短、基因测序结果完善,基因序列容易控制、能塑造自发骨关节炎,可直接用于塑造骨关节炎模型等特点。因而小鼠能够在实验中大量应用,可以支持大批量的实验研究,使实验的成本降低且易于重复;模型的造模时间短,发展快,有利于缩短实验周期;能够支持与遗传或基因有关的骨关节炎病因研究;有自发骨关节炎模型[4]。但小鼠体型小,关节结构与受力与人类有一些差别、基因与人类有很大不同、在解剖及观察上有困难,无法进行关节镜等操作、软骨细胞层相比于大型动物要少,因而小鼠不能完全模拟人类基因对骨关节炎的影响;不适合手术诱导的骨关节炎模型;无法很好的模拟骨关节炎在软骨损伤上的逐渐进展;取材困难[1]。且只有骨骼成熟的小鼠才能用于骨关节炎模型,但很难判断小鼠的骨骼成熟程度。小鼠在容易获得的同时也有了很多的限制。 2.1.2 大鼠 在解剖结构与生物力学上与小鼠相似,其骨骼成熟时间约为3个月,并且有与小鼠相同的易于获取、容易饲养、实验周期短,易于重复等优点。虽仍不适合关节镜等操作,但手术取材及关节内实验操作相对方便,软骨较厚,拥有更复杂的结构,感染风险小,不易死亡,关节承重与人类更接近,价格虽相对于小鼠稍贵,但其体型较大,可供采集的材料多,但大鼠不易塑造自发骨关节炎的模型。因而大鼠有利于塑造手术或关节腔内注射形成的骨关节炎模型;可用关节腔内注射或外科手术重现部分或全部的骨关节炎软骨损伤,更适合被用来测试软骨修复的方法,如基因治疗、干细胞移植、软骨细胞植入或生长因子刺激等[1];且大鼠模型对于药物干预、行为和结构的评估方面的适应力允许其进行机械研究,而由于成本大和伦理问题,这在较大的哺乳动物身上不便实现[5]。大鼠也有着与小鼠相似的局限性。 2.1.3 豚鼠 也有着与小鼠、大鼠相似的解剖结构、生物力学构造和生活特点,与之相关的优缺点便不再赘述。豚鼠的骨骼成熟时间为4-6个月。因豚鼠膝关节为内翻对齐,其骨关节炎主要好发部位为膝关节的内侧面;其病理改变与人类骨关节炎相似,能够表现出渐进性的退行性改变。虽然豚鼠的骨骼要在4个月的时候才会生长停止,但是其软骨和骨骼的早期自发性变化在出生后2个月便可看到,持续到第18个月[1];豚鼠性格温顺、活动不多。因而其主要用于塑造自发的骨关节炎模型,观察时间不是很长,不适和用于运动造成的骨关节炎模型塑造。 2.1.4 兔 也是一种常用的实验动物,骨骼成熟时间为八九个月。其虽与人类一样为哺乳动物,但相比于鼠在关节的结构和生物力学上与人类相似,兔的关节结构虽与人类相似,但生物力学上与人的关节有差异,其关节组织的结构和分布也与人类不同,不适合功能性研究[1]。兔的软骨较薄,关节软骨还可自发愈合,且没有转基因品系。但它相比于小鼠体型更大,且关节大体与人类关节类似,手术操作方便,大小也适宜组织结构和组织液的提取[1],易于获取,容易饲养,但相比于鼠类价格要高,如果要进行大规模的实验研究花费更大。但体型大有利于实验结果的观察研究。因而兔适用于早期骨关节炎模型的塑造[6],不适于自发性骨关节炎的模型研究,应用类型没有小鼠广泛。其适合骨关节炎模型的手术造模[7],也能使用MRI进行模型的评估。 2.1.5 狗 也属于哺乳动物,其骨骼成熟时间为9-18个月,且膝关节与人类非常相似,应用更为广泛。狗的骨关节炎病因、症状与治疗方法也与人类相似[8]。狗模型普遍,容易进行对比研究;狗在其他方面比如胃肠道结构也与人类相似;狗属于大型动物,相比于小型动物更利于手术操作,大小合适提取组织结构和组织液;且容易训练[1]。狗也拥有膝骨关节炎的自发模型。也因为狗的体型大,其造价更为昂贵,饲养成本大,无法负担大量的实验研究;狗与人在生物力学方面还是有一定的不同,且没有转基因品系。因而狗可以进行夹板固定和运动疗法、肠内疗法,可以应用于自发性骨关节炎的模型研究,适合手术造模等。 2.1.6 羊 羊的骨骼成熟时间约为2年。相对于其他小型动物,羊的体积与关节结构与人类更加相似,山羊的膝关节解剖结构最接近人类的膝关节,适合进行骨关节炎模型的塑造[9]。羊与其他大型动物相比要便宜一些,性格温顺,容易驯服和饲养;没有自发模型;但相比于小动物更适合用于手术塑造的骨关节炎模型;这类反刍动物有特殊的消化系统,可以改变药物的生物利用度[1];且其实验成本较高,所需特定饲养条件,而且难以形成骨关节炎,造模需要的损伤比其他动物要更大。因而羊不适合口服药物的治疗,无法塑造自发骨关节炎模型,适合塑造手术及其他方法形成的骨关节炎模型。 2.1.7 马 马的骨关节炎与人类骨关节炎有十分相似的特点,比如关节软骨的进行性和永久性恶化,以及骨关节炎通常发生在年轻的运动员/马或者是年老的个体上[10]。马的骨关节炎通常影响掌指关节,有取材方便,手术容易操作等优点。但马的价格更为昂贵,需要的活动空间更大,且造模和实验周期长,每次实验应用个体少,应用不广泛。因而马可以使用撞击、制动、运动损伤和手术等方法塑造骨关节炎模型,用这些模型模拟马骨关节的退行性改变可以很好的模拟人类骨关节炎。主要适用于研究运动员和年老个体的骨关节炎退行性改变相关实验,也可以用于测试相关治疗的效果。 2.1.8 灵长类 灵长类动物不仅与人类在关节结构、化学和生物力学方面最为相似,塑造的骨关节炎模型也与人骨关节炎十分相近。而且灵长类动物在其他很多方面也与人类相似,可以研究多种因素对于骨关节炎的影响,比如肥胖等[11]。但灵长类动物价格高、造模时间长、实验周期长,难以进行大量实验;动物来源少,难以饲养,实验难度较大,医疗成本高。因此虽然按照与人类骨关节炎相似的标准来说,灵长类动物是最合适的模型动物,但由于种种原因并不经常被使用。其适用于研究治疗人类骨关节炎的药物疗效,为药物应用到人体做准备,是药物临床试验的选择。 2.2 塑造动物模型方法的选择 越来越多的人认为骨关节炎是一种全身性的关节疾病,它可以分为不同的类型,每一种都有不同的致病机制,甚至一些相同的骨关节炎类型也有不同的致病机制[12]。引发骨关节炎的危险因素有机械性和非机械性的,机械因素包括前交叉韧带断裂、半月板撕裂、肌肉无力和错位等,而非机械因素包括遗传、肥胖、年龄、性别和炎症。这些危险因素和损伤都可能成为骨关节炎的病因,也能够形成拥有不同特点的骨关节炎。 人们研究了许多不同的方法来塑造动物的骨关节炎模型,但因为这些动物与人类的关节并非一致,且人工塑造的骨关节炎与人类患有的骨关节炎也有差距,至今没有任何一个骨关节炎动物模型能完美的满足人们的所有研究需求。不同的动物模型有不同的优缺点,能够适应不同有关骨关节炎的研究。在选择应用哪一个骨关节炎模型时,要根据自身的研究需要来选择。是模仿创伤性的、年龄相关的、代谢性的,甚至是尚未完全阐明机制的骨关节炎模型,还是要研究药物、行为、饮食,甚至是环境对于骨关节炎的影响,都可以根据不同骨关节炎模型的特征来选择最合适的造模方法。见表2。 "
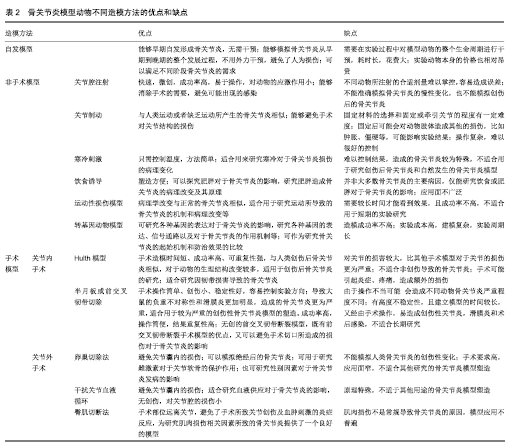

2.2.1 自发模型 某些动物随着年龄的增长可以自发的患上骨关节炎。STR/ort小鼠和Dunkin Hartley豚鼠是公认的自发骨关节炎模型,它们能够早期自发形成骨关节炎,且与人类骨关节炎相似[9,13]。这种天生的骨关节炎动物模型能够模拟骨关节炎从早期到晚期的整个发展过程,不用外力干预,避免了人为损伤,且发病过程和病理损伤与人类原发的骨关节炎十分相似[3],可以满足不同阶段骨关节炎的需求[14]。但自发的骨关节炎模型需要在实验过程中对模型动物的整个生命周期进行干预,耗时长,花费大[15]。且实验动物本身的价格也相对昂贵。这种模型适于研究年龄相关的骨关节炎的发病机制,或用于研究某些治疗方法对于整个骨关节炎病程的影响。不适合测试新疗法,而适合确定某种治疗方法的长期有效性,也能够用来模拟研究衰老导致的关节炎[16]。 2.2.2 非手术模型 无创模型不破坏皮肤和关节囊,而且是完全无菌的,能够避免手术或其他侵入性损伤造成的创伤对动物模型的影响,更符合骨关节炎的病理过程。非手术模型相比于手术模型更加简单,实验程序更快,不需要进行技术要求高的手术[17]。但是非手术模型对于不同动物所需的造模方法难以掌控,容易造成误差,且形成的骨关节炎模型没有手术模型能够更好的模拟创伤改变。 (1)关节腔注射:关节腔注射是向关节腔内注射不同功能的药物,这些药物通过各种不同的机制损害关节软骨或韧带,形成类似于骨关节炎的病理改变。常见用于注射的药物有胶原酶、碘醋酸盐、碘乙酸盐、木瓜蛋白酶等[5,18-22]。注射模型具有快速,微创,成功率高,易于操作,对动物的应激作用小的优点[6],且能够消除手术的需要,避免可能出现的感染。但不同动物所注射的合适剂量难以掌控,容易造成误差[23],且这种方法塑造的骨关节炎模型与人类正常的骨关节炎发展过程不同[15]。不能准确模拟骨关节炎的慢性变化[3],也不能模拟创伤后的骨关节炎。这种方法塑造的骨关节炎模型适合进行短期的实验研究,它们主要用于研究疼痛的机制以及药物治疗的靶点[9],也可以用来研究不同的生物机制在骨关节炎发展中的作用。但是不适于用作对于自然发生骨关节炎的和创伤后骨关节炎的研究。 (2)关节制动:关节制动通过各种方法固定或牵引关节,使关节应力发生不同程度的改变,从而造成不同程度的关节损伤[24]。这种方法塑造的骨关节炎模型更符合骨关节炎的病理过程,与人类运动或者缺乏运动所产生的骨关节炎相似[25]。而且能够避免手术对关节结构的损伤。但固定材料的选择和固定或牵引关节的程度有一定难度,且固定后可能会对动物肢体造成其他的损伤,比如肿胀、僵硬等,可能影响实验结果。这种模型过程繁琐,并未比其他骨关节炎模型有很大优势。且这种造模方法需要在选择时充分考虑各种因素,尽可能一次固定到位,避免耗材。此种模型主要用于研究外界因素对于骨关节炎的影响。 (3)寒冷刺激:寒冷也是诱发关节损伤的因素之一,能够造成软骨的直接损伤和破坏关节腔内环境,导致关节软骨和滑膜的退行性改变[26]。一些患有骨关节炎的人群有寒冷刺激的病史,这种模型适合用来研究寒冷对于骨关节炎损伤的病理变化。但是用寒冷刺激诱发骨关节炎难以控制结果,造成的骨关节炎较为特殊,不适合用于研究创伤后骨关节炎和自然发生的骨关节炎模型。 (4)饮食诱导:肥胖是骨关节炎的危险因素之一。动物在实验中的体质量会影响骨关节炎的进展,增高的体质量会导致关节负质量增加、关节创伤、关节不稳和关节代谢的改变[27]。而且高脂饮食和高胆固醇水平也会导致软骨损伤的增加及增加骨关节炎的严重程度[2]。通过高脂饮食诱导塑造肥胖导致的骨关节炎模型可以探究肥胖对于骨关节炎的影响,研究肥胖造成骨关节炎的病理改变及其原理[28-31]。 (5)运动性损伤模型:过度运动会增加患骨关节炎的风险。长期运动或关节过度负重的人群很容易造成关节不同程度的损伤,导致骨关节炎和关节功能障碍。动物可以通过在轮子上或跑步机上奔跑或者通过加压超载来塑造骨关节炎模型,模拟关节损伤[32]。这种模型的病理学改变与正常的骨关节炎相似[33]。不过需要较长时间才能看到效果,且成功率不高。不适合用于短期的实验研究,适合用于研究运动所导致的骨关节炎的机制和病理改变等。 (6)转基因动物模型:是应用基因技术添加或敲除某些基因建立的。转基因小鼠目前被广泛用作骨关节炎研究的模型[23]。基因动物模型主要用于研究各种基因的表达对于骨关节炎的影响,研究各种基因的表达、信号通路以及对于骨关节炎的作用机制等。其可用于研究骨关节炎的起始机制和防治效果的比较,也可利用转基因骨关节炎动物模型来测试某一基因对防止、延缓或逆转骨关节炎形态变化的作用。不过这种动物模型造模成功率不高,且实验成本高,建模复杂,实验周期长。 2.2.3 手术模型 手术诱导的骨关节炎模型进展快,效果明显,是短期研究的最佳选择。但是手术会干扰其他关节组织,可能影响疾病进展;也会造成额外的创伤,有感染的风险;而且手术操作对于技术的要求相对较高,技术不熟练可能造成动物模型的骨关节炎轻重程度不一,且更有可能造成额外的创伤和感染;手术导致的关节损伤与自然发展的骨关节炎不同,没有人类骨关节炎自然发生的过程,而是直接进展到了骨关节炎的后期损伤阶段,不适合用于早期骨关节炎及自然发生的骨关节炎的研究。但是手术模型的过程与人类创伤性骨关节炎发展类似,十分适合创伤后骨关节炎的研究。 (1)关节内手术:应用最为广泛,通过破坏关节结构(韧带和半月板)引起关节退行性变,改变了关节的稳定性和生物力学特点,造成明确而迅速的关节损伤。手术造模时间短、成功率高、可重复性强,与人类创伤后骨关节炎相似,适合模拟创伤引起的骨关节炎模型。但由于手术操作人员的熟练度不同,会造成不同的关节内损伤,影响到后期骨关节炎的严重程度。造成不同实验所造成的骨关节炎严重程度不一致,对照困难[2]。而且打开关节囊的手术可能引起炎症、疼痛,造成额外的损伤,甚至造成动物步态的改变。这会产生混淆效应,除关节损伤之外的创伤可能对于实验造成影响[17]。而且通过手术诱导产生的动物模型可能影响关节的初始结构,不适用于早期骨关节炎和自然发生的骨关节炎的研究。 Hulth模型:是一种经典的手术造模方式,主要通过切除前后交叉韧带、内侧副韧带及内侧半月板造成关节失稳,术后任其活动,不将伤肢固定,使关节面间磨损增加,促使关节软骨退变[23],形成与人类骨关节炎相似的病理改变。这种模型通过破坏维持关节稳定的韧带,使关节受力不均衡,导致局部软骨受力增加,致使关节软骨变形,造成骨关节炎。这种方法对关节的损害较大,比其他手术模型对于关节的损伤更为严重。有人在其基础上做出了改进,将模型动物内侧半月板以及前交叉韧带切断,但不切断后交叉韧带。改进的Hulth法减小了手术创伤,缩短了造模时间,且建立了稳定的骨关节炎模型,适用于中早期骨关节炎的基础研究[26]。Hulth模型与半月板或前交叉韧带切除相比对于动物的生理结构改变较多,适用于创伤后骨关节炎的研究。该类模型适合研究因韧带损害导致的骨关节炎的治疗及骨关节炎的关节置换等方面[23]。 半月板或前交叉韧带切除:人类最易发生的关节损伤就是半月板或者交叉韧带的损伤。半月板或前交叉韧带切除是啮齿动物常用的模型。 全内侧半月板切除术和韧带修复继发性骨关节炎模型会导致关节僵硬和严重的退行性改变,造成软骨下骨缺损和骨赘形成[34],以及肌肉损伤[35]。半月板切除术是将内侧副韧带横断和半月板切开诱导的骨关节炎,这种损伤会导致关节表面不稳定和关节不协调,与人类创伤后骨关节炎相似[5]。半月板切除的手术操作简单、创伤小、稳定性好,容易控制实验方向,能够较好的模拟骨关节炎所造成的疼痛。且与关节腔内注射药物诱导的骨关节炎模型相比,半月板切除术导致大鼠的负重不对称性和滑膜炎更加明显,造成的骨关节炎更为严重[5]。因而半月板切除术诱导的骨关节炎模型适合用于较为严重的创伤性骨关节炎模型的塑造,也可用于塑造多种动物的骨关节炎模型。 而前交叉韧带断裂是人类常见的关节损伤,前交叉韧带切断法是将关节前交叉韧带切断,造成关节应力改变,从而使软骨细胞发生改变,导致骨关节炎[23]。前交叉韧带切除模型也是外科骨关节炎模型中应用最频繁的一种。它会使关节软骨永久不稳定,导致滑膜炎症和软骨下骨硬化[3],能够很好的反映骨关节炎的病理过程,形成的骨关节炎模型比关节腔内注射胶原酶所造成的关节损伤更严重[7,36],且比半月板模型骨关节炎发展更慢。其成功率高,操作简便,结果重复性高,骨关节炎进展迅速。但其有高度不稳定性,且建立模型的时间较长,又经由手术操作,易造成创伤性关节炎,滑膜炎和术后感染。适合用于创伤性骨关节炎模型的塑造,但不适合长期研究[15]。后来,有的实验人员使用了无创的前交叉韧带断裂模型,这种模型既有前交叉韧带断裂手术模型的优点,又可以避免手术切口所造成的损伤对于骨关节炎的影响[25]。 (2)关节外手术:关节外的手术可以避免关节囊内的损伤。LIU等[37]通过切除囊外内侧副韧带而不损伤关节囊建立早期软骨退变的骨关节炎动物模型。这种方法与关节囊内的手术相比,可以在不破坏关节和滑膜液初始结构和含量的前提下建立动物模型。这种方法建立的动物骨关节炎模型的软骨退变较轻,退变速度较慢,适合早期骨关节炎的模型塑造,但不适合塑造中晚期的骨关节炎模型。结果有高度可重复性,进展迅速,适合短期研究[3]。另外也有一些其他的从关节外塑造骨关节炎模型的方法,能够从不同的方面塑造骨关节炎模型,排除了关节结构破坏对于骨关节炎发展的影响,更好的模拟了人类的骨关节炎模型。 卵巢切除法:其原理是人类绝经后雌激素缺乏,会导致骨质疏松,软骨细胞改变,从而导致骨关节炎。切除卵巢可以模拟绝经后的骨关节炎[33,38]。但不能模拟人类骨关节炎的创伤性变化[3]。此模型也可用于研究雌激素对于关节软骨的保护作用[39]。也可研究性别因素对于骨关节炎发病的影响。但此模型手术要求高,且应用面窄,不适合其他研究的骨关节炎模型塑造。 干扰关节血液循环:据研究表明,病理性血管生成可以加重骨关节炎的发展[40]。血管通道是影响骨关节炎炎症发展的重要因素[41]。且破坏关节血流与能够造成骨关节炎[42]。这种模型适合研究血液供应对于骨关节炎的影响,无创伤,对关节腔的损伤小。不适于其他用途的骨关节炎模型塑造。 臀肌切断法:此方法主要通过将关节运动有关的肌肉或其神经切断,从而改变关节的生物力学环境,增加下肢负荷,从而引起软骨的衰弱和退化,促使骨关节炎的发生[12]。这种塑造骨关节炎模型的手术部位远离关节,避免了手术所致关节创伤及血肿刺激的炎症反应,为研究肌肉损伤相关因素所致的骨关节炎提供了一个良好的模型。此种模型可以用于研究关节附近肌肉的功能改变导致骨关节炎的危险因素及其能够导致骨关节炎的严重程度研究。 "

| [1] THYSEN S, LUYTEN FP, LORIES RJ.Targets, models and challenges in osteoarthritis research. Dis Model Mech. 2015; 8(1):17-30. [2] VAN DER KRAAN PM. Factors that influence outcome in experimental osteoarthritis.Osteoarthritis Cartilage. 2017;25(3): 369-375. [3] KIM JE, SONG DH, KIM SH, et al.Development and characterization of various osteoarthritis models for tissue engineering. PLoS One. 2018;13(3):e0194288. [4] BLAKER CL, CLARKE EC, LITTLE CB,.et al.Using mouse models to investigate the pathophysiology, treatment, and prevention of post-traumatic osteoarthritis.J Orthop Res. 2017; 35(3):424-439. . [5] MAPP PI, SAGAR DR, ASHRAF S, et al.Differences in structural and pain phenotypes in the sodium monoiodoacetate and meniscal transection models of osteoarthritis. Osteoarthritis Cartilage. 2013;21(9):1336-1345. [6] HERMETO LC, DEROSSI R, OLIVEIRA RJ, et al.Effects of intra-articular injection of mesenchymal stem cells associated with platelet-rich plasma in a rabbit model of osteoarthritis.Genet Mol Res. 2016; 15(3). doi: 10.4238/gmr.15038569. [7] HERMETO LC, ROSSI R, JARDIM PH,et al.Comparison between two different experimental models of osteoarthritis in rabbits. Intra-articular collagenase injection and anterior cruciate ligament transection.Acta Cir Bras. 2016;31(9):602-607. [8] PASHUCK TD, KUROKI K, COOK CR, et al.Hyaluronic acid versus saline intra-articular injections for amelioration of chronic knee osteoarthritis: A canine model.J Orthop Res.2016;34(10): 1772-1779. [9] KUYINU EL, NARAYANAN G, NAIR LS, et al.Animal models of osteoarthritis: classification, update, and measurement of outcomes.J Orthop Surg Res. 2016;11:19. [10] MANINCHEDDA U, LEPAGE OM, GANGL M, et al.Development of an equine groove model to induce metacarpophalangeal osteoarthritis: a pilot study on 6 horses. PLoS One.2015;10(2): e0115089. [11] OGAWA S, AWAGA Y, TAKASHIMA M, et al.Antinociceptive effect of clinical analgesics in a nonhuman primate model of knee osteoarthritis. Eur J Pharmacol.2016;786:179-185. [12] EGLOFF C, SAWATSKY A, LEONARD T, et al.Effect of muscle weakness and joint inflammation on the onset and progression of osteoarthritis in the rabbit knee. Osteoarthritis Cartilage.2014; 22(11):1886-1893. [13] STAINES KA, POULET B, WENTWORTH DN, et al.The STR/ort mouse model of spontaneous osteoarthritis-an update. Osteoarthritis Cartilage. 2017;25(6):802-808. [14] YAN JY, TIAN FM, WANG WY, et al.Age dependent changes in cartilage matrix, subchondral bone mass, and estradiol levels in blood serum,in naturally occurring osteoarthritis in Guinea pigs. Int J Mol Sci. 2014;15(8):13578-13595. [15] HOLYOAK DT, TIAN YF, VAN DER MEULEN MC, et al. Osteoarthritis: Pathology, Mouse Models, and Nanoparticle Injectable Systems for Targeted Treatment.Ann Biomed Eng. 2016;44(6):2062-2075. [16] CHIUSAROLI R, VISENTINI M, GALIMBERTI C, et al.Targeting of ADAMTS5's ancillary domain with the recombinant mAb CRB0017 ameliorates disease progression in a spontaneous murine model of osteoarthritis.Osteoarthritis Cartilage. 2013; 21(11):1807-1810. [17] CHRISTIANSEN BA, GUILAK F, LOCKWOOD KA,et al. Non-invasive mouse models of post-traumatic osteoarthritis.Osteoarthritis Cartilage. 2015;23(10):1627-1638. [18] MORAIS SV, CZECZKO NG, MALAFAIA O, et al.Osteoarthritis model induced by intra-articular monosodium iodoacetate in rats knee. Acta Cir Bras. 2016;31(11):765-773. [19] DAI L, ZHANG X, HU X, et al.Silencing of miR-101 Prevents Cartilage Degradation by Regulating Extracellular Matrix-related Genes in a Rat Model of Osteoarthritis. Mol Ther. 2015;23(8): 1331-1340. [20] BRYDEN LA, NICHOLSON JR, DOODS H, et al.Deficits in spontaneous burrowing behavior in the rat bilateral monosodium iodoacetate model of osteoarthritis: an objective measure of pain-related behavior and analgesic efficacy. Osteoarthritis Cartilage. 2015 Sep;23(9):1605-1612. [21] LI Y, ZHANG Y, CHEN C, et al., Establishment of a rabbit model to study the influence of advanced glycation end products accumulation on osteoarthritis and the protective effect of pioglitazone. Osteoarthritis Cartilage. 2016;24(2):307-314. [22] FUENTES R, VEUTHEY C, ARIAS A, et al.Injection in temporomandibular joint of rats. Description of technical protocol. Pol J Vet Sci. 2017; 20(2):207-211. [23] 卢向阳,唐芳,马武开,等骨关节炎动物模型的研究进展[J]. 风湿病与关节炎, 2017,6(2):63-67,75. [24] ZHOU Q, WEI B, LIU S, et al.Cartilage matrix changes in contralateral mobile knees in a rabbit model of osteoarthritis induced by immobilization.BMC Musculoskelet Disord. 2015;16: 224. [25] RAMME AJ, LENDHEY M, RAYA JG, et al.A novel rat model for subchondral microdamage in acute knee injury: a potential mechanism in post-traumatic osteoarthritis. Osteoarthritis Cartilage. 2016;24(10):1776-1785. [26] 陈志达,林瀚洋,余志毅,等.膝骨关节炎动物模型研究进展[J]. 风湿病与关节炎, 2016,5(1):67-70. [27] COLLINS KH, REIMER RA, SEERATTAN RA, et al.Using diet-induced obesity to understand a metabolic subtype of osteoarthritis in rats. Osteoarthritis Cartilage.2015;23(6):957-965. [28] ASOU Y, IWATA M, OCHI H, et al.Pleiotropic Functions of High Fat Diet in the Etiology of Osteoarthritis. PLoS ONE [Electronic Resource].2016;11(9):e0162794. [29] VUOLTEENAHO K, KOSKINEN A, MOILANEN E.Leptin -a link between obesity and osteoarthritis. applications for prevention and treatment.Basic Clin Pharmacol Toxicol. 2014;114(1): 103-108. [30] KC R, LI X, FORSYTH CB, et al.Osteoarthritis-like pathologic changes in the knee joint induced by environmental disruption of circadian rhythms is potentiated by a high-fat diet.Sci Rep. 2015 Nov 20;5:16896. [31] SUN AR, PANCHAL SK, FRIIS T, et al.Obesity-associated metabolic syndrome spontaneously induces infiltration of pro-inflammatory macrophage in synovium and promotes osteoarthritis. PLoS ONE [Electronic Resource].2017;12(8): e0183693. [32] KHORASANI MS, DIKO S, HSIA AW, et al.Effect of alendronate on post-traumatic osteoarthritis induced by anterior cruciate ligament rupture in mice.Arthritis Res Ther. 2015;17:30. [33] MIYATAKE K, MUNETA T, OJIMA M,et al.Coordinate and synergistic effects of extensive treadmill exercise and ovariectomy on articular cartilage degeneration.BMC Musculoskelet Disord. 2016;17:238. [34] REZENDE MU, HERNANDEZ AJ, OLIVEIRA CR, et al. Experimental osteoarthritis model by means of medial meniscectomy in rats and effects of diacerein administration and hyaluronic acid injection. Sao Paulo Med J. 2015;133(1):4-12. [35] VAN DER POEL C, LEVINGER P, TONKIN BA, et al.Impaired muscle function in a mouse surgical model of post-traumatic osteoarthritis.Osteoarthritis Cartilage. 2016;24(6):1047-1053. [36] SILVA JMS, ALABARSE PVG, TEIXEIRA VON, et al.Muscle wasting in osteoarthritis model induced by anterior cruciate ligament transection. PLoS One.2018;13(4): e0196682. [37] LIU Z, HU X, MAN Z, et al.A novel rabbit model of early osteoarthritis exhibits gradual cartilage degeneration after medial collateral ligament transection outside the joint capsule.Sci Rep. 2016;6:34423. [38] ANDERSSON A, BERNARDI AI, STUBELIUS A, et al.Selective oestrogen receptor modulators lasofoxifene and bazedoxifene inhibit joint inflammation and osteoporosis in ovariectomised mice with collagen-induced arthritis.Rheumatology (Oxford). 2016; 55(3):553-563. [39] 金刚.骨关节炎动物模型研究进展[J].中国民族民间医药, 2014,(13): 24-26. [40] CUI Z, CRANE J, XIE H, et al.Halofuginone attenuates osteoarthritis by inhibition of TGF-beta activity and H-type vessel formation in subchondral bone. Annals of the Rheumatic Diseases. 016;75(9): 1714-1721. [41] BINKS DA, GRAVALLESE EM, BERGIN D, et al.Role of vascular channels as a novel mechanism for subchondral bone damage at cruciate ligament entheses in osteoarthritis and inflammatory arthritis.Ann Rheum Dis. 2015;74(1):196-203. [42] 张君涛,吴超超.膝关节骨性关节炎动物模型研究进展[J].重庆医学, 2018,47(15):2061-2063,2067. |
| [1] | Huang Dengcheng, Wang Zhike, Cao Xuewei. Comparison of the short-term efficacy of extracorporeal shock wave therapy for middle-aged and elderly knee osteoarthritis: a meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1471-1476. |
| [2] | Peng Zhihao, Feng Zongquan, Zou Yonggen, Niu Guoqing, Wu Feng. Relationship of lower limb force line and the progression of lateral compartment arthritis after unicompartmental knee arthroplasty with mobile bearing [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1368-1374. |
| [3] | Liu Xiangxiang, Huang Yunmei, Chen Wenlie, Lin Ruhui, Lu Xiaodong, Li Zuanfang, Xu Yaye, Huang Meiya, Li Xihai. Ultrastructural changes of the white zone cells of the meniscus in a rat model of early osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1237-1242. |
| [4] | Kong Desheng, He Jingjing, Feng Baofeng, Guo Ruiyun, Asiamah Ernest Amponsah, Lü Fei, Zhang Shuhan, Zhang Xiaolin, Ma Jun, Cui Huixian. Efficacy of mesenchymal stem cells in the spinal cord injury of large animal models: a meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1142-1148. |
| [5] | Shi Yangyang, Qin Yingfei, Wu Fuling, He Xiao, Zhang Xuejing. Pretreatment of placental mesenchymal stem cells to prevent bronchiolitis in mice [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 991-995. |
| [6] | Lun Zhigang, Jin Jing, Wang Tianyan, Li Aimin. Effect of peroxiredoxin 6 on proliferation and differentiation of bone marrow mesenchymal stem cells into neural lineage in vitro [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1014-1018. |
| [7] | Duan Liyun, Cao Xiaocang. Human placenta mesenchymal stem cells-derived extracellular vesicles regulate collagen deposition in intestinal mucosa of mice with colitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1026-1031. |
| [8] | Liu Xin, Yan Feihua, Hong Kunhao. Delaying cartilage degeneration by regulating the expression of aquaporins in rats with knee osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 668-673. |
| [9] | Ma Zetao, Zeng Hui, Wang Deli, Weng Jian, Feng Song. MicroRNA-138-5p regulates chondrocyte proliferation and autophagy [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 674-678. |
| [10] | Cao Xuhan, Bai Zixing, Sun Chengyi, Yang Yanjun, Sun Weidong. Mechanism of “Ruxiang-Moyao” herbal pair in the treatment of knee osteoarthritis based on network pharmacology [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 746-753. |
| [11] | Li Yonghua, Feng Qiang, Tan Renting, Huang Shifu, Qiu Jinlong, Yin Heng. Molecular mechanism of Eucommia ulmoides active ingredients treating synovitis of knee osteoarthritis: an analysis based on network pharmacology [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 765-771. |
| [12] | Song Shan, Hu Fangyuan, Qiao Jun, Wang Jia, Zhang Shengxiao, Li Xiaofeng. An insight into biomarkers of osteoarthritis synovium based on bioinformatics [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 785-790. |
| [13] | Deng Zhenhan, Huang Yong, Xiao Lulu, Chen Yulin, Zhu Weimin, Lu Wei, Wang Daping. Role and application of bone morphogenetic proteins in articular cartilage regeneration [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 798-806. |
| [14] | Chen Junyi, Wang Ning, Peng Chengfei, Zhu Lunjing, Duan Jiangtao, Wang Ye, Bei Chaoyong. Decalcified bone matrix and lentivirus-mediated silencing of P75 neurotrophin receptor transfected bone marrow mesenchymal stem cells to construct tissue-engineered bone [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 510-515. |
| [15] | Liu Yang, Gong Yi, Fan Wei. Anti-hepatoma activity of targeted Pluronic F127/formononetin nanocomposite system in vitro [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 526-531. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||