Chinese Journal of Tissue Engineering Research ›› 2019, Vol. 23 ›› Issue (33): 5385-5391.doi: 10.3969/j.issn.2095-4344.1841
Previous Articles Next Articles
Mesenchymal stem cells: present status and prospect for its application in peripheral nerve injury
Cao Lizhi1, Feng Naibo2, Wang Juan1, Chen Jiafeng1
- 1The First Hospital of Jilin University, Changchun 130000, Jilin Province, China; 2The Second Hospital of Jilin University, Changchun 130000, Jilin Province, China
-
Revised:2019-06-12Online:2019-11-28Published:2019-11-28 -
Contact:Chen Jiafeng, Professor, The First Hospital of Jilin University, Changchun 130000, Jilin Province, China -
About author:Cao Lizhi, Master candidate, The First Hospital of Jilin University, Changchun 130000, Jilin Province, China
CLC Number:
Cite this article
Cao Lizhi, Feng Naibo, Wang Juan, Chen Jiafeng . Mesenchymal stem cells: present status and prospect for its application in peripheral nerve injury[J]. Chinese Journal of Tissue Engineering Research, 2019, 23(33): 5385-5391.
share this article
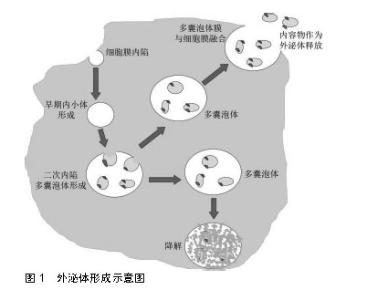
2.1 间充质干细胞在周围神经损伤修复中的应用 由于间充质干细胞具有向骨、软骨、肌肉、脂肪和肌腱等多系分化的巨大潜能而在再生医学领域备受关注[13-14]。许多研究表明,间充质干细胞可以通过分泌生长因子、细胞因子和黏附分子等方式,促进全身组织缺损和损伤的修复或愈合[15-16]。早期研究表明许旺细胞能够促进中枢神经和周围神经的功能恢复和组织学再生。2001年,Dezawa等[17]首次报道了骨髓间充质干细胞在大鼠坐骨神经损伤模型修复中的应用。他们通过局部移植的方式将骨髓间充质干细胞移植到坐骨神经断端处,在术后3周发现了丰富的神经纤维再生现象,通过共聚焦显微镜和免疫电镜观察到骨髓间充质干细胞对再生的神经纤维有髓鞘化作用。他们基于此研究结果阐明了骨髓间充质干细胞诱导神经再生的主要作用机制:骨髓间充质干细胞通过局部产生神经营养因子来诱导轴突生长并将骨髓间充质干细胞直接转化为髓磷脂细胞系用于神经修复。间充质干细胞诱导神经再生的机制在此后的多项研究中再次得到证实[18],同时研究表明间充质干细胞有分化为许旺细胞样细胞的能力[19-21]。因此后期的多项研究直接将间充质干细胞替代许旺细胞应用于周围神经损伤并取得很好的治疗效果。基于此作用机制,间充质干细胞可单独使用或作为各种组织工程神经修复材料的组成部分,以改善修复效果,促进损伤神经的再生。 间充质干细胞的再生特性只是其引起巨大关注的主要原因之一。多项研究证明,这类细胞还具有强大的免疫特性,这也是它们成为组织工程研究热点的另一个关键因素。间充质干细胞缺乏HLA-DR(一种主要的组织相容性复合物Ⅱ类抗原)的表达,使其免疫原性明显低于其他细胞类型[22-24]。间充质干细胞还可以通过抑制促炎细胞因子的产生和刺激抗炎细胞因子、抗原特异性T细胞的产生来减轻炎症反应[25]。在此前的周围神经损伤修复研究中,局部炎症反应常常带来严重的后果,甚至导致神经修复失败,因此这种免疫特性在神经损伤修复中显得更加重要。间充质干细胞抑制炎症、减轻慢性神经疼痛的研究已经得到了多项研究的支持,主要参与此功能的细胞因子包括转化生长因子β[26-27]、白细胞介素10[28]、肿瘤坏死因子诱导蛋白6[29-31]、肝细胞生长因子1[32-33]、金属蛋白酶等[34-35]。 间充质干细胞具有丰富的来源,其中脂肪组织来源间充质干细胞因其含量丰富、易于获取、易增殖、强大的促血管生成功能和较少的伦理限制而被广泛应用于临床及研究工作[36-37]。研究表明脂肪间充质干细胞具有较强的电动力学特性,使其具有更好的抗缺氧和抗氧化应激能力[38]。脂肪间充质干细胞与内源性干细胞相互协同,通过释放大量生长因子,帮助产生神经外膜样结构以修复轴突损伤部位。最新的研究发现相比于内源性干细胞,脂肪间充质干细胞具有更强的诱导运动神经元增殖从而恢复神经诱发电位的能力[39-40]。 此外,研究还发现分化型和未分化型间充质干细胞对周围神经损伤修复均有一定的促进作用。虽然未分化型间充质干细胞在体外操作的风险更小,并且与分化型间充质干细胞相比具有更强的增殖能力,但有几项研究报道了分化型间充质干细胞对周围神经损伤修复具有更佳的治疗效果,这是由于分化型间充质干细胞对神经突起的生长刺激作用更强,同时也会生成更多的神经营养因子和髓磷脂碱性蛋白[41-42],这也对后期的研究有很大的指导意义。 间充质干细胞在特定体外条件下优越的促进组织再生、减轻炎症反应、分化为许旺细胞的能力使其在周围神经修复方面备受关注。间充质干细胞可以通过直接移植到损伤部位、鞘内直接注射、全身注射或负载于神经导管和支架等多种方式应用于周围神经损伤修复。间充质干细胞还可与纳米材料复合应用,设计出理想的人工神经移植物。此外,也可通过纳米凝胶等材料包载间充质干细胞并将其传递到周围神经损伤区域进行修复。综上所述,间充质干细胞是组织工程中的理想种子细胞,在周围神经修复方面有着巨大的应用前景。 2.2 间充质干细胞外泌体在周围神经损伤修复中的应用 外泌体是细胞外囊泡的一种,存在于多种体液中,是间充质干细胞旁分泌的主要形式[43]。它们是由细胞质内的多囊体与质膜融合而成,随后以外泌体的形式释放到细胞外环境中,见图1。在周围神经损伤修复时,间充质干细胞外泌体主要参与细胞间通讯并维持局部微环境的动态与静态平衡,并且还能刺激血管生成、促进轴突成长和髓鞘化,减轻局部炎症反应[44]。 Lopez-Verrilli等[45]研究显示了未分化许旺细胞分泌的外泌体能够被轴突特异性内化,体外实验显示外泌体显著促进了轴突再生,并在随后的动物实验中观察到外泌体可以明显增强坐骨神经损伤的再生修复。这一结果对神经系统功能的理解开拓了新的思维,也为后续的神经修复研究提供新的策略。随后,林浩东团队在2018年使用脂肪间充质干细胞来源外泌体对坐骨神经损伤修复进行了研究[46]。结果显示脂肪间充质干细胞来源外泌体能有效刺激坐骨神经损伤后的纤维再生,并且通过减少许旺细胞凋亡、减轻其自噬作用,促进Büngner带形成,进而加速了坐骨神经损伤修复。 间充质干细胞外泌体促进周围神经损伤修复的作用机制可总结以下2个方面。首先,外泌体信使RNA和微小RNA是一个主要的介导途径。Lopez-Leal等[47]研究发现在受损轴突周围检测到大量的外泌体,随后实验测试分析了外泌体来源的微小RNA-9和微小RNA-19处于过表达状态,参与了神经元的分化成熟过程,进一步促进了周围神经损伤的修复过程。在其他多项研究中也证明了信使RNA和其他的微小RNA如微小RNA-219、微小RNA-222等也参与到髓鞘的修复过程,完善了间充质干细胞外泌体在周围神经损伤修复中的作用机制[48-49]。此外,研究表明外泌体参与周围神经损伤修复的另一项主要方式是通过外泌体蛋白介导的。外泌体内负载着大量的遗传物质,同时也负载着丰富的蛋白质。Bucan等[50]在2019年最新的研究报道中使用脂肪间充质干细胞来源外泌体用于坐骨神经损伤修复。此研究证实了脂肪间充质干细胞来源外泌体在体内可以内化为许旺细胞并能够刺激许旺细胞增殖,这个发现也表明了外泌体及其运载的物质可以在细胞之间进行转换。在这项研究中作者首次证实了间充质干细胞外泌体中含有包括胶质细胞源性神经营养因子、脑源性神经营养因子和胰岛素样生长激素1等在内的多种生长因子。间充质干细胞分泌的外泌体还可以激活PI3K/AKT、ERK和STAT3信号通路,使多种生长因子(如胰岛素样生长因子1和神经生长因子等)表达增多,进而发挥对神经损伤的修复和保护功能[51]。 间充质干细胞外泌体技术的应用,成功克服了间充质干细胞通过移植进行周围神经损伤修复时存在的多项困难,彻底解决了存在的宿主排斥问题,同时也节约了细胞增殖培养所需的时间。更重要的是,间充质干细胞外泌体具有同样优越的促神经损伤修复的功能,在未来的应用中将会得到更多重视。 2.3 间充质干细胞组织工程神经移植物在周围神经损伤修复中的应用 支架技术是近些年组织工程领域研究的热点。神经导管是一种人工设计的可以连接在神经断端两侧的管状支架填充物,它成功模拟了人体神经的结构和功能。神经导管具有诱导神经轴突再生,防止周围组织浸润神经断端影响神经修复的功能。更为主要的是神经导管内部可以负载合适的种子细胞,以促进神经缺损修复。 虽然在多项研究中单纯将间充质干细胞通过局部注射的方式移植到神经损伤的断端促进神经修复,并取得很好的修复效果。但是越来越多的研究者注意到,这种方式虽然可以在一定程度上实现神经修复目的,但是不可控的周围组织浸润,严重影响了正常的神经结构重建,并且有很大概率出现神经瘢痕组织,对修复后的神经功能产生很大影响。因此神经导管技术的出现,成功解决了相关问题。首先,神经导管提供一个支架支撑作用,为神经轴突的再生诱导提供了空间支持;其次,神经导管可以为负载的间充质干细胞提供一个空间,可以更大程度发挥间充质干细胞的促进神经修复、抑制炎症等效果。神经导管负载间充质干细胞成功将两者的优势结合在一起,既实现了神经导管的神经生长引导功能,又实现了间充质干细胞的促进神经生长、调控损伤区域微环境的作用。 2.3.1 骨髓间充质干细胞组织工程神经移植物在周围神经损伤修复中的应用 骨髓间充质干细胞主要来源于骨髓组织,具有强大的成骨、软骨和脂肪等分化潜能。研究表明,骨髓间充质干细胞可向外胚层和内胚层来源的神经元样、胶质样细胞分化,这为骨髓间充质干细胞用于神经损伤修复提供理论依据。此外,骨髓间充质干细胞不会刺激T细胞的显著增殖,也不是CD8+T细胞的靶向细胞,因此将其应用于自体移植或异体移植时,能够逃避体内免疫细胞的杀伤清除,从而进一步发挥修复作用。 Costa等[52]将骨髓间充质干细胞负载于聚乙醇酸神经导管支架中用于大鼠面神经缺损修复,结果显示骨髓间充质干细胞可以成功整合于导管中,在神经组织内存活并维持表型长达6周时间。在另一项研究,研究人员将骨髓间充质干细胞负载于壳聚糖神经导管,观察到细胞在导管内存活并增殖8-16周的时间,成功促进了 8 mm神经缺损的修复[53]。此团队在后续的研究中证明负载骨髓间充质干细胞的壳聚糖神经导管不仅能够加快神经修复效率,同时可以改善再生神经纤维的数量和质量,获得与自体神经移植相当的治疗效果[54]。 神经导管材料的降解产物常常会引起局部的免疫反应,使损伤部位处于炎症状态,从而影响了修复效果。然而在Hsu团队[55]的研究中,研究人员使用层粘连蛋白对壳聚糖神经导管进行修饰,增强了骨髓间充质干细胞在导管中的黏附能力,并且观察到骨髓间充质干细胞成功抑制了壳聚糖降解所引起的局部炎症反应,获得了更好的促进神经修复效果。 此外,邱超等[56]将骨髓间充质干细胞移植到损伤部位后,观察到良好的轴突再生及功能恢复,更为重要的是,作者还验证了骨髓间充质干细胞可以有效保护损伤区域的宿主许旺细胞,使其维持正常细胞形态,从而发挥支持神经再生的功能。 2.3.2 脂肪间充质干细胞组织工程神经移植物在周围神经损伤修复中的应用 脂肪间充质干细胞来源广泛,是最易取材应用的一类间充质干细胞。在2001年由Zuk首次报道脂肪间充质干细胞获取方法后便广受研究者青睐。与骨髓间充质干细胞相似,脂肪间充质干细胞也具有多向分化潜能,并在后期的实验中证实了脂肪间充质干细胞具有向神经元样细胞、神经细胞分化的潜能。脂肪间充质干细胞还具有分离培养方法简便、扩增能力强等优点。脂肪间充质干细胞在周围神经损伤修复中的应用研究也在多种动物模型中开展。2013年Ghoreishian等[57]从犬类脂肪组织中提取了未分化的自体脂肪间充质干细胞,用于修复犬类面神经损伤。他们将未分化脂肪间充质干细胞包封在藻酸盐水凝胶中,成功修复了7 mm的神经缺损间隙。在后续的研究中,Allbright等[58]也使用脂肪间充质干细胞负载于水凝胶中用于大鼠坐骨神经缺损修复,获得良好的修复效果,展现出一种可靠的修复策略。 Sowa团队[59]在2016年报道了一项有趣的研究。他们将脂肪间充质干细胞和许旺细胞分别负载于明胶水凝胶导管,然后移植到小鼠坐骨神经损伤处,比较它们的神经再生能力,观察脂肪间充质干细胞在体内的存活情况,并观察其在周围神经损伤部位是否分化为许旺细胞。结果显示,脂肪间充质干细胞移植能够促进轴突再生、髓鞘形成及失神经肌肉萎缩恢复,这一效果与许旺细胞移植修复效果相当。脂肪间充质干细胞移植后在体内存活至少4周时间,但脂肪间充质干细胞并未分化为许旺细胞。 尽管脂肪间充质干细胞作为周围神经损伤修复种子细胞具有多项明显优势,但是仍有部分问题亟待证明。最主要的问题是,脂肪间充质干细胞经过多代增殖后会出现生物特性改变,在体内环境的成瘤危险性需要进一步检测验证。 2.3.3 脐带间充质干细胞组织工程神经移植物在周围神经损伤修复中的应用 脐带间充质干细胞是一类具有高度增殖能力的细胞,与骨髓间充质干细胞相比取材更为方便,细胞含量也更为丰富。与脂肪间充质干细胞相比,脐带间充质干细胞受到污染的可能性更低。研究还表明脐带间充质干细胞相比于其他类型间充质干细胞具有最强的神经分化能力,为其在周围神经损伤修复应用提供可靠理论依据。 陈传煌等[60]在先前的一项研究中,使用脐带间充质干细胞移植于大鼠坐骨神经断端,显示出优越的促神经生长的效果,有效延缓了肌肉的失神经萎缩,维持了失神经肌肉的正常形态及功能。此外在2018年,Cui等[61]报道了功能性胶原导管与脐带间充质干细胞结合促进犬坐骨神经切断后再生修复的研究。结果表明,功能性胶原导管可以为神经再生提供机械支持,同时结合脐带间充质干细胞有效促进了神经再生和功能恢复。 多项研究表明脐带间充质干细胞具有优秀的促神经修复效果,为临床周围神经损伤修复提供了思路和方法,但若应用于临床还有很多问题需要解决。如何实现细胞的定向分化,如何确定移植体内的细胞有无异质性,也将是未来研究的重点内容。 在另外的一项研究中,Ladak等[62]将间充质干细胞负载于胶原神经导管,通过体外实验观察到同样的促神经轴突生长现象,然而在体内实验中,与自体神经移植组相比,神经导管/间充质干细胞组却没有达到很好重建神经结构和功能修复的效果。这种结果相反的研究值得深思,更提醒合理设计细胞-支架导管组合的重要性。 总之,间充质干细胞组织工程神经移植物作为神经移植替代物可以很好的为间充质干细胞提供空间支持,并且防止损伤部位周围组织向神经断端的浸润,为周围神经损伤修复提供了充足的操作空间。在后期研究中,组织工程神经移植物同时负载细胞和神经营养生长因子会扩大这种多功能复合支架材料的优势,更好地应用于神经修复组织工程。 2.4 间充质干细胞基因工程在周围神经损伤中的应用 基因修饰的间充质干细胞在组织工程研究中越来越受到重视。基因组编辑是一项令人印象深刻的技术,其操作方法是将治疗基因片段插入到目标细胞,使得目标细胞重新整合编程从而在目标细胞中表达或抑制某些基因的作用。许旺细胞、胶质细胞、感觉神经元和运动神经元均可用于基因修饰。在神经修复组织工程领域,基因修饰的主要目的是设计目标细胞使其可以过量释放生长因子、迁移分子和黏附分子,并能够抑制缺陷基因的表达。神经营养因子3、神经营养因子4、胶质细胞源性神经营养因子、脑源性神经营养因子、神经生长因子、血小板衍生生长因子、碱性成纤维细胞生长因子和亲胆碱能神经元因子均是适合于外周神经基因传递的主要神经生长因子。这些生长因子可以为间充质干细胞的存活和轴突生长提供合适的微环境。 Zhang等[63]在2015年的一项研究中,使用脑源性神经营养因子和睫状神经营养因子转染的骨髓间充质干细胞用于大鼠坐骨神经损伤的治疗。结果显示脑源性神经营养因子和睫状神经营养因子转染的骨髓间充质干细胞结合神经移植可以明显提高坐骨神经功能指数,肌肉活动恢复程度更佳,并且再生神经髓鞘厚度增加,提示这种方式可以有效促进神经轴突生长,利于周围神经损伤修复。 研究显示微小RNA在神经发育和干细胞向神经细胞分化方面发挥重要作用。研究人员试图通过操纵特定微小RNA的表达,以促进间充质干细胞向神经组细胞或神经细胞分化。例如Wang等[64]研究结果表明JMJD1C可以通过表观遗传学维持微小RNA-302表达,从而抑制干细胞的神经分化,因此通过敲除JMJD1C可以有利于干细胞的神经分化能力。Hu等[65-66]通过调控脂肪间充质干细胞的微小RNA-218,并将其用于大鼠坐骨神经损伤修复,显示出良好的修复效果,是一种有效的周围神经损伤修复策略。 基因工程技术可以使间充质干细胞在神经修复方面的优势更加明显。通过人为合理调控间充质干细胞的目标基因表达或抑制,从而促进间充质干细胞向神经细胞分化,并分泌理想的神经营养因子,从而获得更好的周围神经损伤修复效果。"
| [1]Lee SK, Wolfe SW. Peripheral nerve injury and repair. J Am Acad Orthop Surg. 2000;8(4):243-252.[2]Wong JN, Olson JL, Morhart MJ, et al. Electrical stimulation enhances sensory recovery: a randomized controlled trial. Ann Neurol. 2015; 77(6):996-1006.[3]Attal N, Rouaud J, Brasseur L, et al. Systemic lidocaine in pain due to peripheral nerve injury and predictors of response. Neurology. 2004; 62(2):218-225.[4]Campbell WW. Evaluation and management of peripheral nerve injury. Clin Neurophysiol. 2008;119(9):1951-1965.[5]Winfree CJ. Peripheral nerve injury evaluation and management. Curr Surg. 2005;62(5):469-476.[6]Lv W, Deng B, Duan W, et al. Schwann Cell Plasticity is Regulated by a Weakened Intrinsic Antioxidant Defense System in Acute Peripheral Nerve Injury. Neuroscience. 2018;382:1-13.[7]Barton MJ, John JS, Clarke M, et al. The Glia Response after Peripheral Nerve Injury: A Comparison between Schwann Cells and Olfactory Ensheathing Cells and Their Uses for Neural Regenerative Therapies. Int J Mol Sci. 2017;18(2): E287.[8]Yousefi F, Lavi Arab F, Nikkhah K, et al. Novel approaches using mesenchymal stem cells for curing peripheral nerve injuries. Life Sci. 2019;221:99-108.[9]Moattari M, Kouchesfehani HM, Kaka G, et al. Evaluation of nerve growth factor (NGF) treated mesenchymal stem cells for recovery in neurotmesis model of peripheral nerve injury. J Craniomaxillofac Surg. 2018;46(6):898-904.[10]Wu W, Zhang S, Chen Y, et al. Biological Function and Mechanism of Bone Marrow Mesenchymal Stem Cells-packed Poly (3,4-ethylenedioxythiophene) (PEDOT) Scaffolds for Peripheral Nerve Injury: The Involvement of miR-21-Notch Signaling Pathway. Curr Neurovasc Res. 2017;14(1):19-25.[11]李陈,肖玉周.不同来源的间充质干细胞生物学特性差异研究进展[J].创伤外科杂志, 2014,16(1):75-78.[12]方洪松,周建林,彭昊,等.不同来源间充质干细胞生物学特性差异[J].中国组织工程研究, 2015,19(32):5243-5248.[13]Li X, Ding J, Zhang Z, et al. Kartogenin-Incorporated Thermogel Supports Stem Cells for Significant Cartilage Regeneration. ACS Appl Mater Interfaces. 2016;8(8):5148-5159.[14]Eren F, Öksüz S, Küçükodaci Z, et al. Targeted mesenchymal stem cell and vascular endothelial growth factor strategies for repair of nerve defects with nerve tissue implanted autogenous vein graft conduits. Microsurgery. 2016;36(7):578-585.[15]Saghizadeh M, Kramerov AA, Svendsen CN, et al. Concise Review: Stem Cells for Corneal Wound Healing. Stem Cells. 2017;35(10): 2105-2114.[16]Berry E, Liu Y, Chen L, et al. Eicosanoids: Emerging contributors in stem cell-mediated wound healing. Prostaglandins Other Lipid Mediat. 2017;132:17-24.[17]Dezawa M, Takahashi I, Esaki M, et al. Sciatic nerve regeneration in rats induced by transplantation of in vitro differentiated bone-marrow stromal cells. Eur J Neurosci. 2001;14(11):1771-1776.[18]Zhang P, He X, Liu K, et al. Bone marrow stromal cells differentiated into functional Schwann cells in injured rats sciatic nerve. Artif Cells Blood Substit Immobil Biotechnol. 2004;32(4):509-518.[19]Zheng Y, Huang C, Liu F, et al. Reactivation of denervated Schwann cells by neurons induced from bone marrow-derived mesenchymal stem cells. Brain Res Bull. 2018;139:211-223.[20]Wakao S, Matsuse D, Dezawa M. Mesenchymal stem cells as a source of Schwann cells: their anticipated use in peripheral nerve regeneration. Cells Tissues Organs. 2014;200(1):31-41.[21]Fu X, Tong Z, Li Q, et al. Induction of adipose-derived stem cells into Schwann-like cells and observation of Schwann-like cell proliferation. Mol Med Rep. 2016;14(2):1187-1193.[22]Hong SJ, Traktuev DO, March KL. Therapeutic potential of adipose-derived stem cells in vascular growth and tissue repair. Curr Opin Organ Transplant. 2010;15(1):86-91.[23]Zhao S, Wehner R, Bornhäuser M, et al. Immunomodulatory properties of mesenchymal stromal cells and their therapeutic consequences for immune-mediated disorders. Stem Cells Dev. 2010;19(5):607-614.[24]Giacoppo S, Bramanti P, Mazzon E. The transplantation of mesenchymal stem cells derived from unconventional sources: an innovative approach to multiple sclerosis therapy. Arch Immunol Ther Exp (Warsz). 2017;65(5):363-379.[25]Tse WT, Pendleton JD, Beyer WM, et al. Suppression of allogeneic T-cell proliferation by human marrow stromal cells: implications in transplantation. Transplantation. 2003;75(3):389-397.[26]Yoo SW, Chang DY, Lee HS, et al. Immune following suppression mesenchymal stem cell transplantation in the ischemic brain is mediated by TGF-β. Neurobiol Dis. 2013;58:249-257.[27]Echeverry S, Shi XQ, Haw A, et al. Transforming growth factor-beta1 impairs neuropathic pain through pleiotropic effects. Mol Pain. 2009; 5:16.[28]Qu X, Liu X, Cheng K, et al. Mesenchymal stem cells inhibit Th17 cell differentiation by IL-10 secretion. Exp Hematol. 2012;40(9):761-770.[29]Sala E, Genua M, Petti L, et al. Mesenchymal Stem Cells Reduce Colitis in Mice via Release of TSG6, Independently of Their Localization to the Intestine. Gastroenterology. 2015; 149(1): 163-176.e20.[30]Lin QM, Zhao S, Zhou LL, et al. Mesenchymal stem cells transplantation suppresses inflammatory responses in global cerebral ischemia: contribution of TNF-α-induced protein 6. Acta Pharmacol Sin. 2013;34(6):784-792.[31]Kota DJ, Wiggins LL, Yoon N, et al. TSG-6 produced by hMSCs delays the onset of autoimmune diabetes by suppressing Th1 development and enhancing tolerogenicity. Diabetes. 2013;62(6):2048-2058.[32]Okunishi K, Dohi M, Fujio K, et al. Hepatocyte growth factor significantly suppresses collagen-induced arthritis in mice. J Immunol. 2007;179(8):5504-5513.[33]Bai L, Lennon DP, Caplan AI, et al. Hepatocyte growth factor mediates mesenchymal stem cell–induced recovery in multiple sclerosis models. Nat Neurosci. 2012;15(6):862-870.[34]Castellano JM, Mosher KI, Abbey RJ, et al. Human umbilical cord plasma proteins revitalize hippocampal function in aged mice. Nature. 2017;544(7651):488-492.[35]Kawasaki Y, Xu ZZ, Wang X, et al. Distinct roles of matrix metalloproteases in the early- and late-phase development of neuropathic pain. Nat Med. 2008;14(3):331-336.[36]Adams AM, Arruda EM, Larkin LM. Use of adipose-derived stem cells to fabricate scaffoldless tissue-engineered neural conduits in vitro. Neuroscience. 2012;201:349-356.[37]Liu Y, Zhang Z, Qin Y, et al. A new method for Schwann-like cell differentiation of adipose derived stem cells. Neurosci Lett. 2013;551: 79-83.[38]El-Badawy A, Amer M, Abdelbaset R, et al. Adipose Stem Cells Display Higher Regenerative Capacities and More Adaptable Electro-Kinetic Properties Compared to Bone Marrow-Derived Mesenchymal Stromal Cells. Sci Rep. 2016;6:37801.[39]Faghihi F, Mirzaei E, Ai J, et al. Erratum to: Differentiation Potential of Human Chorion-Derived Mesenchymal Stem Cells into Motor Neuron-Like Cells in Two- and Three-Dimensional Culture Systems. Mol Neurobiol. 2016;53(3):1873.[40]Qu J, Zhang H. Roles of Mesenchymal Stem Cells in Spinal Cord Injury. Stem Cells Int. 2017;2017:5251313.[41]Wassef MA, Fouad H, Sabry D, et al. Therapeutic efficacy of differentiated versus undifferentiated mesenchymal stem cells in experimental type I diabetes in rat. Biochem Biophys Rep. 2016; 5:468-475.[42]Lee HJ, Kang KS, Kang SY, et al. Immunologic properties of differentiated and undifferentiated mesenchymal stem cells derived from umbilical cord blood. J Vet Sci. 2016;17(3):289-297.[43]Witwer KW, Buzás EI, Bemis LT, et al. Standardization of sample collection, isolation and analysis methods in extracellular vesicle research. J Extracell Vesicles. 2013;2:20360.[44]Yousefi F, Ebtekar M, Soudi S, et al. In vivo immunomodulatory effects of adipose-derived mesenchymal stem cells conditioned medium in experimental autoimmune encephalomyelitis. Immunol Lett. 2016;172: 94-105.[45]Lopez-Verrilli MA, Picou F, Court FA. Schwann cell-derived exosomes enhance axonal regeneration in the peripheral nervous system. Glia. 2013;61(11):1795-1806.[46]Yin G, Liu C, Lin Y, et al. Effect of exosomes from adipose-derived stem cells on peripheral nerve regeneration. Zhongguo Xiu Fu Chong Jian Wai Ke Za Zhi. 2018;32(12):1592-1596.[47]Lopez-Leal R, Court FA. Schwann Cell Exosomes Mediate Neuron-Glia Communication and Enhance Axonal Regeneration. Cell Mol Neurobiol. 2016;36(3):429-436.[48]Pusic AD, Kraig RP. Youth and environmental enrichment generate serum exosomes containing miR-219 that promote CNS myelination. Glia. 2014;62(2):284-299.[49]Zhou S, Shen D, Wang Y, et al. microRNA-222 targeting PTEN promotes neurite outgrowth from adult dorsal root ganglion neurons following sciatic nerve transection. PLoS One. 2012;7(9):e44768.[50]Bucan V, Vaslaitis D, Peck CT, et al. Effect of Exosomes from Rat Adipose-Derived Mesenchymal Stem Cells on Neurite Outgrowth and Sciatic Nerve Regeneration After Crush Injury. Mol Neurobiol. 2019; 56(3):1812-1824.[51]Shabbir A, Cox A, Rodriguez-Menocal L, et al. Mesenchymal Stem Cell Exosomes Induce Proliferation and Migration of Normal and Chronic Wound Fibroblasts, and Enhance Angiogenesis In Vitro. Stem Cells Dev. 2015;24(14):1635-1647.[52]Costa HJ, Bento RF, Salomone R, et al. Mesenchymal bone marrow stem cells within polyglycolic acid tube observed in vivo after six weeks enhance facial nerve regeneration. Brain Res. 2013;1510:10-21.[53]Zheng L, Cui HF. Use of chitosan conduit combined with bone marrow mesenchymal stem cells for promoting peripheral nerve regeneration. J Mater Sci Mater Med. 2010;21(5):1713-1720.[54]Zheng L, Cui HF. Enhancement of nerve regeneration along a chitosan conduit combined with bone marrow mesenchymal stem cells. J Mater Sci Mater Med. 2012;23(9):2291-2302.[55]Hsu SH, Kuo WC, Chen YT, et al. New nerve regeneration strategy combining laminin-coated chitosan conduits and stem cell therapy. Acta Biomater. 2013;9(5):6606-6615.[56]邱超,郑亚妮,许硕贵.骨髓间充质干细胞移植对周围神经损伤后施旺细胞的影响[J].组织工程与重建外科杂志, 2018,14(1):28-30.[57]Ghoreishian M, Rezaei M, Beni BH, et al. Facial nerve repair with Gore-Tex tube and adipose-derived stem cells: an animal study in dogs. J Oral Maxillofac Surg. 2013;71(3):577-587.[58]Allbright KO, Bliley JM, Havis E, et al. Delivery of adipose-derived stem cells in poloxamer hydrogel improves peripheral nerve regeneration. Muscle Nerve. 2018;58(2):251-260.[59]Sowa Y, Kishida T, Imura T, et al. Adipose-Derived Stem Cells Promote Peripheral Nerve Regeneration In Vivo without Differentiation into Schwann-Like Lineage. Plast Reconstr Surg. 2016;137(2):318e-330e.[60]陈传煌,杨涛,杨万章,等.脐带间充质干细胞移植可延缓大鼠失神经肌肉的萎缩[J].中国组织工程研究,2014,18(1):69-74.[61]Cui Y, Yao Y, Zhao Y, et al. Functional collagen conduits combined with human mesenchymal stem cells promote regeneration after sciatic nerve transection in dogs. J Tissue Eng Regen Med. 2018;12(5): 1285-1296.[62]Ladak A, Olson J, Tredget EE, et al. Differentiation of mesenchymal stem cells to support peripheral nerve regeneration in a rat model. Exp Neurol. 2011;228(2):242-252.[63]Zhang YR, Ka K, Zhang GC, et al. Repair of peripheral nerve defects with chemically extracted acellular nerve allografts loaded with neurotrophic factors-transfected bone marrow mesenchymal stem cells. Neural Regen Res. 2015;10(9):1498-1506.[64]Wang J, Park JW, Drissi H, et al. Epigenetic regulation of miR-302 by JMJD1C inhibits neural differentiation of human embryonic stem cells. J Biol Chem. 2014;289(4):2384-2395.[65]Hu F, Sun B, Xu P, et al. MiR-218 Induces Neuronal Differentiation of ASCs in a Temporally Sequential Manner with Fibroblast Growth Factor by Regulation of the Wnt Signaling Pathway. Sci Rep. 2017;7: 39427.[66]Hu F, Zhang X, Liu H, et al. Neuronally differentiated adipose-derived stem cells and aligned PHBV nanofiber nerve scaffolds promote sciatic nerve regeneration. Biochem Biophys Res Commun. 2017;489(2): 171-178. |
| [1] | Pu Rui, Chen Ziyang, Yuan Lingyan. Characteristics and effects of exosomes from different cell sources in cardioprotection [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 1-. |
| [2] | Lin Qingfan, Xie Yixin, Chen Wanqing, Ye Zhenzhong, Chen Youfang. Human placenta-derived mesenchymal stem cell conditioned medium can upregulate BeWo cell viability and zonula occludens expression under hypoxia [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(在线): 4970-4975. |
| [3] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [4] | Hou Jingying, Yu Menglei, Guo Tianzhu, Long Huibao, Wu Hao. Hypoxia preconditioning promotes bone marrow mesenchymal stem cells survival and vascularization through the activation of HIF-1α/MALAT1/VEGFA pathway [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 985-990. |
| [5] | Shi Yangyang, Qin Yingfei, Wu Fuling, He Xiao, Zhang Xuejing. Pretreatment of placental mesenchymal stem cells to prevent bronchiolitis in mice [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 991-995. |
| [6] | Liang Xueqi, Guo Lijiao, Chen Hejie, Wu Jie, Sun Yaqi, Xing Zhikun, Zou Hailiang, Chen Xueling, Wu Xiangwei. Alveolar echinococcosis protoscolices inhibits the differentiation of bone marrow mesenchymal stem cells into fibroblasts [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 996-1001. |
| [7] | Fan Quanbao, Luo Huina, Wang Bingyun, Chen Shengfeng, Cui Lianxu, Jiang Wenkang, Zhao Mingming, Wang Jingjing, Luo Dongzhang, Chen Zhisheng, Bai Yinshan, Liu Canying, Zhang Hui. Biological characteristics of canine adipose-derived mesenchymal stem cells cultured in hypoxia [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1002-1007. |
| [8] | Geng Yao, Yin Zhiliang, Li Xingping, Xiao Dongqin, Hou Weiguang. Role of hsa-miRNA-223-3p in regulating osteogenic differentiation of human bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1008-1013. |
| [9] | Lun Zhigang, Jin Jing, Wang Tianyan, Li Aimin. Effect of peroxiredoxin 6 on proliferation and differentiation of bone marrow mesenchymal stem cells into neural lineage in vitro [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1014-1018. |
| [10] | Zhu Xuefen, Huang Cheng, Ding Jian, Dai Yongping, Liu Yuanbing, Le Lixiang, Wang Liangliang, Yang Jiandong. Mechanism of bone marrow mesenchymal stem cells differentiation into functional neurons induced by glial cell line derived neurotrophic factor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1019-1025. |
| [11] | Duan Liyun, Cao Xiaocang. Human placenta mesenchymal stem cells-derived extracellular vesicles regulate collagen deposition in intestinal mucosa of mice with colitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1026-1031. |
| [12] | Pei Lili, Sun Guicai, Wang Di. Salvianolic acid B inhibits oxidative damage of bone marrow mesenchymal stem cells and promotes differentiation into cardiomyocytes [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1032-1036. |
| [13] | Wang Xianyao, Guan Yalin, Liu Zhongshan. Strategies for improving the therapeutic efficacy of mesenchymal stem cells in the treatment of nonhealing wounds [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1081-1087. |
| [14] | Zhao Min, Feng Liuxiang, Chen Yao, Gu Xia, Wang Pingyi, Li Yimei, Li Wenhua. Exosomes as a disease marker under hypoxic conditions [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1104-1108. |
| [15] | Wang Shiqi, Zhang Jinsheng. Effects of Chinese medicine on proliferation, differentiation and aging of bone marrow mesenchymal stem cells regulating ischemia-hypoxia microenvironment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1129-1134. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||