Chinese Journal of Tissue Engineering Research ›› 2018, Vol. 22 ›› Issue (34): 5565-5570.doi: 10.3969/j.issn.2095-4344.0687
Previous Articles Next Articles
Properties of bacterial cellulose in wound repair
Zhang Weijia, Liu Ying
- School of Pharmacy, Xinhua College of Sun Yat-Sen University, Guangzhou 510000, Guangdong Province, China
-
Received:2018-09-01Online:2018-12-08Published:2018-12-08 -
Contact:Liu Ying, Assistant teacher, School of Pharmacy, Xinhua College of Sun Yat-Sen University, Guangzhou 510000, Guangdong Province, China -
About author:Zhang Weijia, Master, Lecturer, School of Pharmacy, Xinhua College of Sun Yat-Sen University, Guangzhou 510000, Guangdong Province, China -
Supported by:The 2014 High Education Science Project in Guangdong Province during the Twelfth Five-Year Period, No. 2014GXJK208
CLC Number:
Cite this article
Zhang Weijia, Liu Ying. Properties of bacterial cellulose in wound repair[J]. Chinese Journal of Tissue Engineering Research, 2018, 22(34): 5565-5570.
share this article

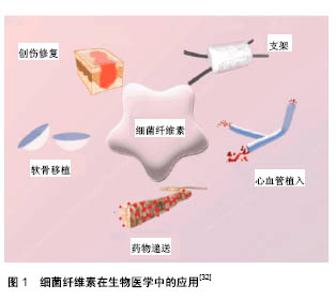
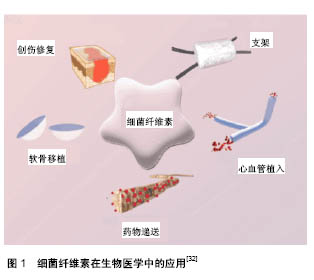
2.1 细菌纤维素的性质特征 2.1.1 化学和微观结构 细菌纤维素在化学结构上与植物纤维素相同,都是由β-D-葡萄糖通过β-1,4-糖苷键结合形成的线型高分子聚合物(β-1,4-葡聚糖),相邻的毗喃葡萄糖的六个碳原子呈稳定的椅式结构,而数个β-1,4-葡聚糖间又通过氢键作用形成稳定的不溶于水的聚合物。在显微镜下观察发现,产细菌纤维素的细菌细胞壁侧面有一列50-80个轴向排列的小孔,小孔分泌直径约1.78 nm的纤维素微纤丝。随着分泌量的增加,微纤丝平行延伸,相邻的几根微纤丝通过氢键相互连接,形成直径3.0-4.0 nm的微纤束。微纤束进一步伸长、缠绕,合并形成一根长度不定、宽30-100 nm、厚3-8 nm的细菌纤维条。纤维条互相交织,形成不规则网状或絮状多孔结构[9]。 2.1.2 降解性能 降解性能对生物医用材料来说是一项值得关注和考量的特性,尤其对于体内植入材料,可降解性显得格外重要。随着科学家对医用材料开发和挖掘的逐渐深入,无需术后清除的可降解材料受到越来越多医生和患者的喜爱。然而,降解性和机械强度往往不能两全其美,材料的降解一般会使得其机械强度随之降低。对于创面修复材料而言,机械强度与可降解性相比显得略为重要。探索降解性能和机械强度之间的平衡点,研发新型的可适应损伤部位修复规律的生物材料,是众多科学家追求的终极目标。 科学家对细菌纤维素的降解性能有着不同的看 法[10],一方认为人体不含纤维素酶,也没有利于纤维素降解的强酸强碱环境,故细菌纤维素在体内很难降解;另一方则认为,细菌纤维素以亚稳态结构的Iα纤维素为主(约占60%),相较于其他纤维素(只含30%Iα纤维素)而言对纤维素酶更为敏感。Li等[10]对红茶菌发酵形成的细菌纤维素进行体内植入研究,将细菌纤维素管植入大鼠大腿肌肉内贴近坐骨神经处,发现6周后材料开始轻度降解。 2.2 细菌纤维素的理化和机械性能 材料的理化和机械性能与其化学和微观结构密切相关。细菌纤维素稳定的化学机构及超精细纳米三维网络结构,使其与其他生物材料相比具有独特的理化和机械性能,如高结晶度、高持水性、高抗张强度和弹性模量等。 但细菌纤维素的理化和机械性能还与诸多因素有关,如菌种[11]、培养基成分[12]、培养条件[13]、纳米纤维的排列和结合方式等[14]。Xie[12]研究了不同碳源组成的细菌纤维素的溶胀率和保水率,分别可达到自身体积的54.4-76.8倍和4.7-8.0倍。Mohite等[13]在摇动培养条件下产生了粒径为1.44 μm的细菌纤维素球,其孔隙率高达181.81%,结晶度为81%,杨氏模量和抗张强度分别为(15.71±0.15) MPa和14.94 MPa,且热稳定性良好。如果能使得纳米纤维丝定向排列,并增加纤维间的相互作用力,能显著提高细菌纤维素的机械性能。Yao等[14]采用湿纺法使细菌纤维素纳米丝定向结合成长纤维,使杨氏模量提高到16.4 GPa,抗张强度提高到248.6 MPa;在纳米纤维相互交联时,用3价的Fe3+替代单价的Na+可提高界面间的相互作用,使得干膜的杨氏模量和抗张强度分别提高到22.9 GPa和357.5 MPa,即使在湿润状态下也能达到15.9 GPa和262.2 MPa。 复合材料是医用材料的发展趋势,可实现不同材料间的优势互补。对于细菌纤维素而言,和其他材料复合是改变其固有特性和增加其应用范围的一种常见手段。研究发现,细菌纤维素与其他材料复合会不同程度的影响其机械强度。与细菌纤维素相比,采用浸泡和冷冻干燥法制成的细菌纤维素-壳聚糖膜,孔径更小,持水量变化不明显,抗张强度和断裂拉伸率有所降低,而杨氏模量增加[15]。采用一步法原位合成的细菌纤维素-氧化石墨烯纳米复合水凝胶,当氧化石墨烯质量分数为0.48%时,抗张强度和杨氏模量分别增强38%和120%[16]。 2.3 细菌纤维素的生物相容性 生物相容性是评价材料与人体之间相互作用的一系列指标。医用材料的生物相容性评价主要采用医疗器械生物学评价,即GB/T16886 (ISO10993) 的系列标准进行,常用的评价手段包括:遗传、致癌和生殖毒性实验,血液相容性实验,体外细胞毒性实验,体内植入实验,刺激与致敏实验、全身毒性实验等。 按照GB/T16886的建议,医用材料应根据使用部位、用法和用途进行选择性评价。短期(≤24 h)或长期 ( > 24 h-30 d)用于创面修复的医用材料,主要从细胞毒性、致敏和刺激或皮内反应3个指标入手。Liu等[17]研究发现许旺细胞能在细菌纤维素膜表面正常生长和迁移,与普通培养基相比,细菌纤维素浸出液对许旺细胞的生长、增殖及S-100蛋白的表达无明显影响。Wang等[18]将细菌纤维素与成纤维细胞复合培养并植入裸鼠皮下,结果显示该复合物很好地融入裸鼠正常皮肤,细胞在细菌纤维素表面形成连续的细胞层,表明细菌纤维素非常适合细胞贴附和增殖。Zheng等[19]采用亚急性毒性实验、细胞毒性实验评价细菌纤维素的生物相容性,认为细菌纤维素及其酶解物对成骨细胞无明显细胞毒性;将细菌纤维素浸提液经尾静脉注射Wistar大鼠,连续注射约2周,各试验组大鼠的血液学参数和血清生化指标与对照组大鼠比较均无显著差异(P > 0.05)。Li等[10]对细菌纤维素管进行肌肉植入研究,发现其仅引起局部轻微炎症反应,1周左右即明显缓解,表现出良好的体内生物相容性和血液相容性。Lima等[20]使用大鼠硬脑膜损伤模型评价细菌纤维素膜的生物相容性,在120 d的观察周期中,细菌纤维素未引发免疫反应、慢性炎症反应及神经毒性。 生物相容性是医用材料最基本的要求,对医用材料进行生物安全性评价是其进入临床前的关键环节,并应该贯穿于医用材料开发的各个阶段。细菌纤维素表现出优越的生物相容性,无论是体外细胞实验还是体内植入研究,都表明细菌纤维素是一种理想的生物医用材料。 2.3.1 体外生物相容性 在细菌纤维素膜上培养许旺细胞,利用显微镜(光和扫描电子)、细胞增殖分析、流式细胞仪和RT-PCR等方法检测观察到细胞形态和功能无显著差异。Liu等[17]的研究发现,L929细胞和人类成骨细胞可在天然细菌纤维素膜上增殖。Yao等[14]评估了细菌纤维素膜植入小鼠皮下后的生物反应,在手术后的7,15,30,60和90 d内对细菌纤维素膜和周围组织的组织学切片进行了分析,结果发现在考察期间未发现任何机体排斥反应,术后7,15和30 d观察到多形核细胞和淋巴细胞,表明有轻微的炎症反应,但在术后的60,90 d没有发现炎症细胞浸润。人静脉内皮细胞在细菌纤维素水凝胶中具有较强的增殖能力,表明细胞在细菌纤维素膜上的具有较好的水平增长和垂直迁移能力。由于细菌纤维素水凝胶的不同梯度氧气供应能力,研究发现细菌纤维素水凝胶内的细胞渗透被限制在一定程度的氧气中。研究表明,人成骨细胞能够附着在更大的细菌纤维素颗粒上。 Liu等[17]制备细菌纤维素-明胶复合材料并评价了其生物相容性,将NIH3T3成纤维细胞种植于细菌纤维素、细菌纤维素/明胶复合材料上并培养48 h,结果发现细胞具有良好的附着力和增殖能力,但在细菌纤维素-明胶复合材料中的生物相容性比细菌纤维素要好。由此表明细菌纤维素-明胶支架的生物活性较好,可用于伤口包扎和组织工程支架。类似地,Wang等[18]报道了由原花青素通过交联合成的细菌纤维素/明胶复合材料,结果表明复合材料上纤维母细胞的增殖、渗透和附着力与原生细菌纤维素相比提高了。事实上,明胶是一种由细胞外基质衍生而来的多肽,也是一种变性的胶原蛋白,其具有良好的生物相容性、低免疫原性、黏性、促进细胞生长的黏附性和低成本等特性。与原生细菌纤维素相 比[19],其他复合材料,如细菌纤维素-多晶硅(乙二醇)、细菌纤维素-壳聚糖和细菌纤维素胶原蛋白,表现出更好的NIH3T3细胞活性。与原生的细菌纤维素膜相比,人类脂肪干细胞在细菌纤维素-聚(2-羟乙基甲基丙烯酸酯)中的增殖程度更低。采用原位合成方法合成的细菌纤维素胶原复合材料,具有潜在的组织工程应用前景。细菌纤维素-胶原复合材料的高生物降解性、低抗原性和细胞结合性是医疗用途的生物材料必须具备的显著特征。从考察细菌纤维素生物相容性的研究中可以推断细,菌纤维素膜不会表现出基因毒性和免疫活性。用单细胞凝胶电泳和沙门氏菌实验对细菌纤维素纳米纤维的体外基因毒性进行了评估,沙门氏菌实验表明细菌纤维素纳米纤维是非诱变或基因毒性的,而彗星分析表明其无明显的DNA损伤作用。Zheng等[19]评估了在饮食中掺入发酵来源的细菌纤维素对F344大鼠的影响,结果显示28 d内无宏观变化,血液学检测结果也无不良反应。此外,从血液生化结果看也无其他不良影响,因此,可判断在28 d的饮食中加入细菌纤维素对F344大鼠无不良影响。 2.3.2 体内生物相容性 Lima等[20]对细菌纤维素的生物相容性进行了详细的系统评估,植入Wistar大鼠皮下后,植入物保持其形状,在12周内没有任何明显的炎症迹象。研究人员发现,利用改良的多层发酵方法制得的细菌纤维素薄膜细胞毒性较低,对人类脂肪干细胞具有良好的促增殖作用。在背部全层皮肤损伤的Balb/c小鼠模型中,其他敷料相比,细菌纤维素组在第7天伤口区域有明显的新鲜组织再生和毛细血管形成。这些结果表明细菌纤维素具有良好的生物相容性与临床应用潜力。Qiu等[21]对比了细菌纤维素与其他两种敷料Vaseline gauze和Algisite M在大鼠模型中的疗效,结果显示与其他组相比,细菌纤维素组在第14天的伤口愈合速度更快,无发现毒性作用。将滚动法合成的细菌纤维素空心管被植入到肌间隙,数据显示细菌纤维素在移植后6周内没有发现对神经组织的毒性作用。另一项关于生物相容性的研究表明,细菌纤维素/马铃薯淀粉复合材料具有良好的生物相容性,复合材料周围有新的血管生成。 2.4 细菌纤维素在创面修复中的研究与应用 见表1。 自19世纪被发现以来,细菌纤维素一直被认为是性能优越的天然生物医用材料。研究表明,细菌纤维素具有减轻瘢痕增生[21]、促进细胞增殖和迁移等作用[22-23],因而成为创伤修面领域的热点材料。而近年来对细菌纤维素创面修复材料的开发更多集中于复合材料的形式。Lin等[15]采用浸泡和冻干法制备了细菌纤维素-壳聚糖膜,该医用膜有优越的持水性、机械强度和杨氏模量,无细胞毒性,且对大肠杆菌和金黄色葡萄球菌表现出有效抑制,在大鼠皮肤缺损模型中,细菌纤维素-壳聚糖比起细菌纤维素和透气胶膜具有更好的皮肤再生效果。Pandey等[24]制备了一种细菌纤维素和聚丙烯酰胺的复合水凝胶微粒,该水凝胶的细胞相容性良好,无皮肤刺激性,对伤口收缩有明显的效果,可促进上皮形成,加速成纤维细胞增殖,有望作为一种新型敷料用于二度烧伤创面的修复。Yu等[25]采用微流体工艺制备了一种中空的细菌纤维素微球,这种中空微球作为功能性单元自发地聚集形成新型的可注射支架,体外三维细胞培养发现其可促进细胞增殖和分布,促进组织再生,并快速SD大鼠皮肤伤口愈合。 然而,真正能应用到临床上的细菌纤维素产品并不多,美国乔治亚洲科尔奎特一家公司生产的Dermafill是其中最具有代表性的产品之一。Dermafill是一种半透明的细菌纤维素膜,其微观结构和人体自身的胶原蛋白相似,高蒸腾速率促进液体平衡,覆盖于伤口表面隔离环境污染,它在使用时变得透明,有利于观察伤口,在伤口愈合后,Dermafill自动脱落或浸泡生理盐水后易于剥离,避免伤口二次伤害。Dermafill对皮肤撕裂和下肢溃疡等创面的愈合均有良好的效果[26-27]。2014年,中国也有一款同类型产品“创舒”注册上市,是目前国内唯一一款细菌纤维素医用伤口敷料。 细菌纤维素在生物医学领域的首个主要应用是与创伤修复有关。Czaja等[28]是提出细菌纤维素替代损伤皮肤的先驱,自此之后,大量文献报道了其在创伤修复方面的应用。纤维素敷料被推荐作为治疗伤口的临时覆盖物,包括压疮、皮肤撕裂、静脉停滞、缺血性和糖尿病伤口、二级烧伤、皮肤移植供体部位、创伤性擦伤和撕裂,以及作为活检的部位。一些用于牙周病重建的细菌纤维素创伤敷料也已上市,如:BioFill®、Bioprocess®、XCell®、和Gengiflex®。 BioFill®生物膜是首个被用于伤口敷料的细菌纤维素生物膜产品,具有以下特点:成本低,良好的伤口黏附性、透气性、弹性、透明性、耐久性,是细菌的物理屏障,可止血,易操作。此外,BioFill®加速愈合、缓解疼痛的有效性,也在300多例患者中得到证实。虽然这些伤口敷料的止痛机制尚不完全清楚,但一些学者认为其修复机制可能与纤维素氢键对离子的吸附有关,也可能是纳米细菌纤维素的3D网络模拟皮肤表面结构,为愈合和再生创造了有利条件。需要指出的是,正如许多研究人员所认为的那样,在应用于非治疗下肢溃疡时,将细菌纤维素作为伤口敷料明显缩短了治疗时间或伤口愈合时间。Czaja等[28]提出将湿细菌纤维素作为一种新型的伤口敷料应用于局部重度烧伤。因为湿细菌纤维素能够为快速伤口清洁,提供良好的湿润环境,因此在加快愈合方面呈现出优异的效果。与此同时,Fu等[29]将细菌纤维素伤口敷料(DermafillTM,AMD/Ritmed,Tonawanda,NY)用于慢性创伤治疗,发现使用细菌纤维素后75%上皮化的平均时间从315 d减少到81 d。 除了上面提到的直接使用之外,还需要改进和修饰来增强功能。细菌纤维素可通过性质或功能的改良形成纳米复合材料,目前已有细菌纤维素的纳米复合材料通过这种方法被制造出来,例如机械性能得到了改善的纳米复合材料细菌纤维素/胶原蛋白、细菌纤维素-明胶复合材料,其热稳定性、弹性模量和抗拉强度均有所增强。 Fu等[30]研究了细菌纤维素纤维-芦荟纳米复合薄膜的制备。他们通过在细菌纤维素培养基中添加体积分数30%的芦荟胶,获得机械强度、结晶度、吸水能力和水蒸气渗透性(透气性)均有所增强的生物聚合物膜。有研究制备了一种可用于治疗Ⅲ度烧伤的伤口敷料,这种敷料是由超氧化物歧化酶(一种抗氧化剂)或poviargol(一种抗生素)浸渍的。此外,用高岭土(凝血剂)制得的细菌纤维素复合材料,被证明是一种良好的伤口愈合材料,其长期效果与短期相当。伤口愈合包扎产品设计的最大特点之一是提高了纳米复合材料的储水能力,换言之,增加了长时间保持水分的能力。Gao等[31]发现细菌纤维素/壳聚糖复合材料呈现的脱水速度非常缓慢,因此,细菌纤维素/壳聚糖可用于需要频繁更换敷料的伤口,如皮肤溃疡、压疮、烧伤等的治疗。Gao等[31]最近报道了细菌纤维素/壳聚糖复合材料在大鼠模型皮肤伤口愈合中的效果。研究人员发现,这种合成物不会对动物细胞产生任何毒性作用。此外,对组织再生过程的评价显示,用细菌纤维素/壳聚糖复合材料治疗的伤口比用细菌纤维素或其他市面上可用的敷料材料愈合得更快,组织再生速度更快。 尽管细菌纤维素已被广泛应用于生物医疗领域,但仍有很多值得探索的地方。Gao等[31]合成了一种大型的类似器官的3D细菌纤维素水凝胶,它可能应用于植入式组织和器官支架,如肾脏或肝脏,其结构特性、力学性能和生物相容性较好。有研究在32只兔体内植入细菌纤维素,考察其炎症反应和声带的愈合情况,在动物声带一侧植入0.25 mm2细菌纤维素膜,另一侧则是0.3 mL的蒸馏水,结果表明植入120 d后细菌纤维素材料相对稳定,无不良反应,表明细菌纤维素是声带替代的有用材料,因其稳定性较好,不引起炎症反应。现也有大量文献报道了细菌纤维素纳米复合材料在3D打印方面的应用。有研究通过梯度回声磁共振成像(MRI)设计了一种基于细菌纤维素的耳型模拟材料,细菌纤维素是用一个负硅酮模具进行生物打印的,细菌被引导入模具中,合成细菌纤维素,重现外耳形态。这项研究表明细菌纤维素是一种有前景的组织工程材料,具有耳软骨的机械性能,可用于模拟构建患者的耳形。 "

| [1] Zahedmanesh H, Mackle JN, Sellborn A, et al. Bacterial cellulose as a potential vascular graft: Mechanical characterization and constitutive model development. Biomed Mater Res B Appl Biomater. 2011;97(1): 105-113. [2] Malm CJ, Risberg B, Bodin A, et al. Small calibre biosynthetic bacterial cellulose blood vessels: 13-months patency in a sheep model. Scand Cardiovasc J. 2012;46(1):57-62. [3] Fontana JD, Franco VC, de Souza SJ, et al. Nature of plant stimulators in the production of Acetobacter xylinum ("tea fungus") biofilm used in skin therapy. J Appl Biochem Biotechnol. 1991;28-29:341-351. [4] Yano H, Sugiyama J, Nakagaito A, et al. Optically Transparent Composites Reinforced with Networks of Bacterial Nanofibers. Adv Mater. 2005;17:153-155. [5] Brackmann C, Zaborowska M, Sundberg J, et al. In situ imaging of collagen synthesis by osteoprogenitor cells in microporous bacterial cellulose scaffolds. Tissue Eng Part C Methods. 2012;18(3):227-234. [6] Shi Q, Li Y, Sun J, et al. The osteogenesis of bacterial cellulose scaffold loaded with bone morphogenetic protein-2. Biomaterials. 2012;33:6644-6649. [7] Bodin A, Concaro S, Brittberg M, et al. Bacterial cellulose as a potential meniscus implant. J Tissue Eng Regen Med. 2007;1(5): 406-408. [8] Svensson A, Nicklasson E, Harrah T, et al. Bacterial cellulose as a potential scaffold for tissue engineering of cartilage. Biomaterials. 2005;26(4):419-431. [9] Zhu CL, Li F, You QS, et al. Preparation of Nanometer Biomaterial Bacterial Cellulose and Observation of its Ultra-structure. J Biomedical Eng. 2008;27:287-290. [10] Li F, Zhu CL, You QS, et al. In vivo Evaluation of theBiocompatibility of Tissue-engineered Tubular Nanometer Bacterial Cellulose. Chin J Biomed Eng. 2009;28:760-765. [11] Kim SS, Lee SY, Park KJ, et al. Gluconacetobacter sp. gel_SEA623-2, bacterial cellulose producing bacterium isolated from citrus fruit juice. Saudi J Biol Sci. 2017;24(2):314-319. [12] Xie JJ. Preparation and evaluation of antibacterial bacterial cellulose membranes impregnated silver nanoparticles. Shanghai: Donghua University, 2012:199-203. [13] Mohite BV, Patil SV. Physical, structural, mechanical and thermal characterization of bacterial cellulose by G. hansenii NCIM 2529. Carbohydr Polym. 2014;106:132-141. [14] Yao J, Chen S, Chen Y, et al. Macrofibers with High Mechanical Performance Based on Aligned Bacterial Cellulose Nanofibers. ACS Appl Mater Interfaces. 2017;9(24):20330-20339. [15] Lin WC, Lien CC, Yeh HJ, et al. Bacterial cellulose and bacterial cellulose-chitosan membranes for wound dressing applications. Carbohydr Polym. 2013;94(1):603-611. [16] Si H, Luo H, Xiong G, et al. One-step in situ biosynthesis of graphene oxide-bacterial cellulose nanocomposite hydrogels. Macromol Rapid Commun. 2014;35(19):1706-1711[17] Liu W, Gu WY, Zhou XJ, et al. In vitro biocompatibility of bacterial cellulose and Schwann cells. Acad J Sec Mil Med Uni. 2015;36(3): 324-329. [18] Wang ZL, Jia YY, Shi Y, et al. Research on Characterization and Biocompatibility of Nano-bacterial Cellulose Membrane. Chem J Chin Univ. 2009;30(8)1553-1558. [19] Zheng Q, Xi TF, Chen YM, et al. Biocompatibility research of the bacterial cellulose. Chin J Pharm Anal. 2010;7:1389-1392. [20] Lima FM, Pinto FC, Andrade-da-Costa BL, et al. Biocompatible bacterial cellulose membrane in dural defect repair of rat. J Mater Sci Mater Med. 2017;28:37. [21] Qiu J, Liu DL, Zhang Y, et al. Effects of bacterial cellulose on reducing hypertrophic scar in rabbit ears. J Clin Rehabil Tissue Eng Res, 2011;15(25):4597-4601. [22] Sanchavanakit N, Sangrungraungroj W, Kaomongkolgit R, et al. Growth of human keratinocytes and fibroblasts on bacterial cellulose film. Biotechnol Prog. 2006;22(4):1194-1199.[23] Bodin A, Ahrenstedt L, Fink H, et al. Modification of nanocellulose with a xyloglucan-RGD conjugate enhances adhesion and proliferation of endothelial cells:implications for tissue engineering. Biomacromolecules. 2007;8(12):3697-3704. [24] Pandey M, Mohamad N, Low WL, et al. Microwaved bacterial cellulose-based hydrogel microparticles for the healing of partial thickness burn wounds. Drug Deliv Transl Res. 2017;7(1):89-99. [25] Yu J, Huang TR, Lim ZH, et al. Production of Hollow Bacterial Cellulose Microspheres Using Microfluidics to Form an Injectable Porous Scaffold for Wound Healing. Adv Healthc Mater. 2016;5(23): 2983-2992. [26] Solway DR, Consalter M, Levinson DJ. Microbial cellulose wound dressing in the treatment of skin tears in the frail elderly. Wounds. 2010;22(1):17-19. [27] Portal O, Clark WA, Levinson DJ. Microbial cellulose wound dressing in the treatment of nonhealing lower extremity ulcers. Wounds. 2009; 21(1):1-3. [28] Czaja W, Krystynowicz A, Bielecki S, et al. Microbialcellulose-the natural power to heal wounds. Biomaterials. 2006;27:145-151. [29] Fu LN, Zhang Y, Li C, et al. Skin tissuerepair materials from bacterial cellulose by a multilayer fermentation method. J Mater Chem. 2012;22: 12349-12357. [30] Fu L, Zhang J, Yang G. Present status and applications of bacterial cellulose-based materials for skin tissue repair. Carbohydr Polym. 2013;92(2):1432-1442. [31] Gao C, Wan Y, Yang C, et al. Preparation andcharacterization of bacterial cellulose sponge with hierarchical pore structureas tissue engineering scaffold. J Porous Mater. 2011;18:139-145.[32] De Oliveira Barud HG, da Silva RR, da Silva Barud H, et al. A multipurpose natural and renewable polymer in medical applications: Bacterial cellulose.Carbohydr Polym.2016;153:406-420. |
| [1] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [2] | Zeng Yanhua, Hao Yanlei. In vitro culture and purification of Schwann cells: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1135-1141. |
| [3] | Xu Dongzi, Zhang Ting, Ouyang Zhaolian. The global competitive situation of cardiac tissue engineering based on patent analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 807-812. |
| [4] | Wu Zijian, Hu Zhaoduan, Xie Youqiong, Wang Feng, Li Jia, Li Bocun, Cai Guowei, Peng Rui. Three-dimensional printing technology and bone tissue engineering research: literature metrology and visual analysis of research hotspots [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 564-569. |
| [5] | Chang Wenliao, Zhao Jie, Sun Xiaoliang, Wang Kun, Wu Guofeng, Zhou Jian, Li Shuxiang, Sun Han. Material selection, theoretical design and biomimetic function of artificial periosteum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 600-606. |
| [6] | Liu Fei, Cui Yutao, Liu He. Advantages and problems of local antibiotic delivery system in the treatment of osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 614-620. |
| [7] | Li Xiaozhuang, Duan Hao, Wang Weizhou, Tang Zhihong, Wang Yanghao, He Fei. Application of bone tissue engineering materials in the treatment of bone defect diseases in vivo [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 626-631. |
| [8] | Zhang Zhenkun, Li Zhe, Li Ya, Wang Yingying, Wang Yaping, Zhou Xinkui, Ma Shanshan, Guan Fangxia. Application of alginate based hydrogels/dressings in wound healing: sustained, dynamic and sequential release [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 638-643. |
| [9] | Chen Jiana, Qiu Yanling, Nie Minhai, Liu Xuqian. Tissue engineering scaffolds in repairing oral and maxillofacial soft tissue defects [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 644-650. |
| [10] | Xing Hao, Zhang Yonghong, Wang Dong. Advantages and disadvantages of repairing large-segment bone defect [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 426-430. |
| [11] | Chen Siqi, Xian Debin, Xu Rongsheng, Qin Zhongjie, Zhang Lei, Xia Delin. Effects of bone marrow mesenchymal stem cells and human umbilical vein endothelial cells combined with hydroxyapatite-tricalcium phosphate scaffolds on early angiogenesis in skull defect repair in rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3458-3465. |
| [12] | Wang Hao, Chen Mingxue, Li Junkang, Luo Xujiang, Peng Liqing, Li Huo, Huang Bo, Tian Guangzhao, Liu Shuyun, Sui Xiang, Huang Jingxiang, Guo Quanyi, Lu Xiaobo. Decellularized porcine skin matrix for tissue-engineered meniscus scaffold [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3473-3478. |
| [13] | Mo Jianling, He Shaoru, Feng Bowen, Jian Minqiao, Zhang Xiaohui, Liu Caisheng, Liang Yijing, Liu Yumei, Chen Liang, Zhou Haiyu, Liu Yanhui. Forming prevascularized cell sheets and the expression of angiogenesis-related factors [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3479-3486. |
| [14] | Liu Chang, Li Datong, Liu Yuan, Kong Lingbo, Guo Rui, Yang Lixue, Hao Dingjun, He Baorong. Poor efficacy after vertebral augmentation surgery of acute symptomatic thoracolumbar osteoporotic compression fracture: relationship with bone cement, bone mineral density, and adjacent fractures [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3510-3516. |
| [15] | Liu Liyong, Zhou Lei. Research and development status and development trend of hydrogel in tissue engineering based on patent information [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3527-3533. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||