Chinese Journal of Tissue Engineering Research ›› 2018, Vol. 22 ›› Issue (26): 4253-4258.doi: 10.3969/j.issn.2095-4344.0732
Previous Articles Next Articles
Bone tissue engineering scaffolds and bone repair materials: composite bone graft materials have a bright future in clinical practice
Zhang Di-feng1, Yu Xiao2, Pang Qing-jiang2
- 1Ningbo University Medical School, Ningbo 315211, Zhejiang Province, China; 2Ningbo No. 2 Hospital, Ningbo 315000, Zhejiang Province, China
-
Received:2018-02-09 -
Contact:Yu Xiao, M.D., Associate chief physician, Ningbo No. 2 Hospital, Ningbo 315000, Zhejiang Province, China -
About author:Zhang Di-feng, Master candidate, Ningbo University Medical School, Ningbo 315211, Zhejiang Province, China -
Supported by:the Young Medical Talent Culture Project of Zhejiang Province, No. 2015-70; the General Project for Medicine and Health in Zhejiang Province in 2018, No. 2018ky156; the Clinical Special Fund for Joint Diseases in Ningbo, No. 2013-88
CLC Number:
Cite this article
Zhang Di-feng, Yu Xiao, Pang Qing-jiang. Bone tissue engineering scaffolds and bone repair materials: composite bone graft materials have a bright future in clinical practice[J]. Chinese Journal of Tissue Engineering Research, 2018, 22(26): 4253-4258.
share this article

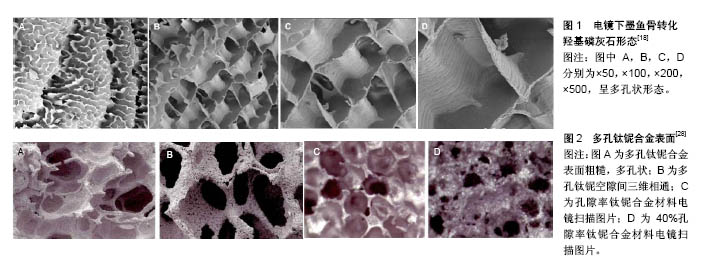
2.1 纳入资料基本概况 纳入的文献包括自体骨及异体骨类文章4篇[1-4], 促骨形成细胞类文章12篇[5-16],新型复合材料类文章14篇[17-30],支架材料类文章14篇[31-44]。就骨修复及支架材料的研究进展进行综述,旨在探讨目前各类骨移植支架材料的优点与不足,寻求进一步开发新型骨移植材料的方向。 2.2 自体骨及异体骨 自体骨移植,通常取自髂骨,有时也会取于股骨远端或胫骨近端,特别是自体髂骨移植物在目前矫形手术中最常用,无免疫排斥反应,并具有骨诱导、骨传导和成骨作用,被普遍认为是植骨融合的金标准[1]。自体骨皮质移植物可掺入宿主骨缺损区,生物相容性良好并提供生物力学结构支持。但是自体骨移植手术时间延长等局限性,常伴有供区出血、神经损伤、疼痛和感染等并发症,尤其是老年患者骨再生能力有限,供体部位发病率增加[2],并且对于长骨缺损修复修复不能满足供骨数量。 异体骨包括同种异体骨和异种异体骨。同种异体骨来源于其他人的骨,大多数都是从尸体中获取或者募捐获得;异种异体骨大多来源于动物的骨组织。异体骨组织缺少细胞成分,只存在较弱的骨诱导和骨传导能力,适用于幼儿、老年人、手术风险大及无法获取足够多的移植骨患者。由于异体骨来源广,增加了免疫排斥反应及传播疾病的风险,对于深冻骨和冻干骨也不能排除此风险[3],异体骨多被制备为新鲜冷冻骨及冻干骨。Rafael等[4]报道用30个新鲜冷冻骨治疗16例后牙槽萎缩的患者,6个月后发现异体骨存活率达96.66%提示异体骨移植对此类病例是足可信赖的选择。 2.3 促骨形成细胞 骨髓间充质干细胞(mesenchymal stem cells,MSC)的骨组织工程一直是治疗大骨缺损的重要研究领域之一。干细胞治疗大段骨缺损可能会在未来实现并解决当前外科手术如Masquelet技术和Ilizarov技术相关的几个问题[5]。在体内,骨形成包括来自于骨髓间充质干细胞的成骨修复细胞、再生模版的存在和相关调节作用。人骨髓间充质干细胞因具有自我更新的能力、多向分化潜能和免疫调节的特性,是治疗的理想细胞来源,而且其能影响细胞因子、趋化因子、生长因子的分泌及细胞外基质,促进血管生成,减少炎症,增强组织修复,促进愈合。Mark等[6]研究报道聚辛枸橼酸盐和生物玻璃材料能有为人骨髓间充质干细胞成骨分化提供有利的条件,并能诱导骨愈合和再生[6]。而对于关节软骨的增殖愈合也有较好的效果。近年来,组织工程已在三维支架上培养组织来替代相关的骨组织,把兔骨髓间充质干细胞接种到聚乳酸-羟基乙酸复合物支架上,分别观察 1,2,3周后,细胞呈高增殖,Ⅱ型胶原、Ⅸ型胶原、蛋白聚糖和SOX9高表达,表明多能非联合的兔骨髓间充质干细胞有能力分化成软骨细胞,可以作为未来的功能组织工程软骨[7]。Khojasteh等[8]研究将自体髂骨植骨中用颊脂肪垫脂肪干细胞来治疗颌骨的萎缩,干细胞与髂骨块联合应用可增加新骨的形成并能减少继发性骨吸收。 区别于传统骨移植物和直接注入生长因子的复合人工骨,基因治疗是一种非常理想而具有发展潜力的新型植骨替代方式。基因治疗即通过基因转移或基因转染等手段将遗传物质转运进细胞,再利用该细胞合成这个基因编码的蛋白而发挥治疗作用。但基因治疗的安全性有待进一步验证,目前仍处于动物实验阶段。RNA干扰(RNAi)是一种创新的生物学机制,降低了基因表达,通过已知的不同方法破坏典型的转录产物(mRNA),小RNA包括miRNA和siRNA[9]。然而,近年来siRNA的应用已经超出了基础研究领域,开始治疗领域的研究,在骨再生的情况下,骨形态发生蛋白(BMP)抑制剂降低siRNA的表达,并增强骨形成的表达,通过药物传递系统来提高移植骨愈合情况[10]。Betz等[11]研究发现,采用鼠皮下脂肪组织片段进行转基因处理,使其能表达BMP-7,再植入鼠骨缺损部位,结果骨缺损处修复较单纯脂肪片段植入更快、更彻底、更牢固。 生长因子是由特定细胞产生,在不同生理过程中发挥效用的一些多肽,它们在骨组织修复过程中起着重要调控作用。常见的生长因子包括骨形态发生蛋白、胰岛素样生长因子、转化生长因子β、血小板源性生长因子、集落刺激因子等。自Urist于1965 年发现骨形态发生蛋白以来,广泛应用于各个方面。骨形态发生蛋白是转化生长因子B超家族成员之一,已知大约有25种不同的BMP,其中BMP-2,4,7,9参与骨和软骨的生长发育及重建过程[12]。 重组人骨形态发生蛋白 2 椎体融合方面效果良好,朱德志[13]报道将腰椎不稳症患者90例随机分为以重组人骨形态发生蛋白2(rhBMP-2)结合纳米晶胶原基材(nHAC)治疗(治疗组)和单纯以纳米晶胶原基材治疗(对照组)两组,术后3个月治疗组深静脉血栓发生率、感染发生率、肺部并发症发生率明显低于对照组,提示重组人骨形态发生蛋白2结合纳米晶胶原基材治疗临床疗效较佳。 近年来应用富血小板血浆(PRP)、高压氧治疗已被证明能使骨折修复效果明显。Schneppendahl等[14]用自体骨移植骨缺损大鼠模型,并用富血小板血浆和高压氧治疗,能有效提高承重骨的愈合效果。Schneppendahl等[15]报道应用自体松质骨移植治疗骨缺损时,联合应用富血小板血浆能有效提高骨愈合情况。 其他生长因子包含转化生长因子(TGF-β)、血管内皮生长因子(VEGF)、血小板衍生因子(PDGF)、表皮细胞生长因子(EGF)和集落刺激因子(CGF)等,也是研究的热点,有报道称其能促进细胞分裂,促进炎症和干细胞迁移,促进创面愈合和组织再生。血管内皮生长因子在动物实验中显示具有加速血管生成和骨组织更新的作用。Park等[16]研究报道将富血小板纤维蛋白,集落刺激因子及人工骨植入骨缺损区,用酶联免疫吸附测定法定量分析和微观分析纤维蛋白原的结构,来比较各个区域的骨愈合情况,结果发现同种异体骨移植材料新骨生长情况最佳,而集落刺激因子的新骨形成量是富血小板纤维蛋白的1.5倍。如何选择合适的生长因子或复合生长因子的浓度、剂量、载体等问题时今后生长因子研究的方向 2.4 新型复合材料 各种海洋生物外壳是一个重要的骨修复材料来源,以碳酸钙及羟基磷灰石为主体的生物材料富含Ca2+及CO32-,具有良好的生物相容性,与人体骨成长过程之间具有一定的相似之处。杨宝凯等[17]报道在大耳白兔桡骨缺损修复实验中将30只大耳白兔分为天然牡蛎壳纳米体复合型骨材料组和空白对照组,发现天然牡蛎壳纳米体复合型骨材料修复骨缺损可以获得更好的桡骨抗弯曲强度,并促进新骨形成。黄谢山等[18]报道墨鱼骨转化羟基磷灰石并将其与MG63细胞体外培养并考察其细胞相容性,证实墨鱼骨转化羟基磷灰石材料对细胞的生长无明显影响且无明显毒性,可作为新型骨组织工程细胞支架材料(图1)。天然来源的碳酸钙可作为新的骨替代材料。乌贼骨的主要成分是碳酸钙,Mousumi等[19]研究报道将乌贼制成胶原-羟基磷灰石支架,并采用大鼠骨髓间质干细胞来测试其生物相容性,结果表明其明显提高了细胞增殖率和大鼠骨髓间充质干细胞碱性磷酸酶的活性,改变后的乌贼支架能作为一种新的骨组织支架。 纳米材料因其纳米尺度效应所表现出的特殊的物理、化学和生物学特性被广泛用于骨组织工程复合支架。碳纳米管是日本科学家Iijima于1991年发现的由石墨片层按照一定螺旋角卷曲而成的直径为纳米级的空心小管[20]。姚梦竹等[21]报道采用粒子致孔法、热致相分离(冷冻干燥法)、微球聚集法、静电纺丝和三维打印等方法,可实现碳纳米管与无机材料、天然可降解高分子材料、人工合成可降解高分子材料等的复合,构建复合骨组织工程支架。Tanaka等[22]报道将缺陷大小的临界尺寸的三维多孔碳纳米管支架(CNTps)植入小鼠颅骨缺陷处,并评价其骨传导能力和体内的重组人骨形成蛋白2释放情况,其与多孔羟基磷灰石陶瓷(IP CHAS)进行比较,结果表明碳纳米支架有显著的细胞增殖和骨再生。近年来有研究指出,碳纳米管也可以单独作为支架应用于骨的再生[23]。 生物玻璃通常是一种应用于骨再生的玻璃陶瓷。最重要的生物玻璃是45S5,由45% SiO2,24.5% Na2O,24.5% CaO,and 6% P2O5组成,不同的化学物的比例,对于生物相容性是非常重要[24]。生物玻璃也常混入其他一起物质,如聚己内酯、壳聚糖、聚乙烯醇/壳聚糖胶原和羟基磷灰石等,生物玻璃中加入其他物质能有更好的生物相容性和力学。在细胞和动物实验研究表明,有介孔的生物玻璃中加入聚L-乳酸,能增强细胞附着、增殖和增强碱性磷酸酶(ALP)成骨细胞的活性,并具有优良的生物相容性的复合物[25]。另有研究显示生物玻璃45S5和β-磷酸三钙和羟基磷灰石混合的双向生物陶瓷,在体内研究中,植入40只Wistar大鼠中,其表现出较高的生物相容性,并能与骨组织整合,术后30 d,材料完全吸收,骨再生过程开始[26]。 金属及其合金材料,包括钽、钛、锰、镁等复合材料,具有有优良的生物相容性及适宜的机械强度等优点,但金属假体受到腐蚀、肌肉重新附着、感染等原因会导致假体松动或假体折断,弹性模量及控制腐蚀的发生率对于金属植入来讲是重要的,如钛镁合金等材料能大幅度降低腐蚀的发生[27]。金属多孔材料近年来已成为医学领域研究的方向。开放的多孔结构为骨组织长入提供了足够的表面积,骨长入的同时,与材料整合,获得机械稳定性,提高了材料的生物相容性,同时多孔结构降低了材料的弹性模量[28](图2)。 有研究显示将富含骨形态发生蛋白2浓缩纤维蛋白凝胶填满被激光熔化的多孔钛,并将其移植与严重节段性股骨缺损的大鼠,通过µCT扫描来评估骨再生、骨质量和骨移植情况,12周后发现,形成的新骨贯穿整个多孔钛并且机械稳定性优于从前[29]。在同种异体移植中使用钽金属小梁作为替代物也是近期研究重点。钽金属小梁与自体骨髓间充质干细胞相比,钽金属小梁增强细胞抗拉的特性,并促进细胞生长、分化和移植的能力[30]。 2.5 支架材料 单纯骨髓间充质干细胞植入体内成骨能力较低,主要原因是由于缺乏细胞支架,骨髓易流失,不能在植入部位形成有效的细胞浓度。细胞支架不仅为细胞成长提供支持和保护,更重要的是调节细胞的形态发生过程,影响细胞生存、迁移、增殖和功能代谢,这种生物材料支架可为细胞提供生存的三维空间,有利于细胞获得足够的营养物质、进行气体交换、排除废料,使细胞在预制形态的三维支架上生长,再将这种黏附上细胞的材料植入骨缺损部位,在生物材料逐步降解的同时,种植的骨细胞不断增殖,从而达到修复骨组织缺损的目的。在骨组织工程中作为支架材料具有较好的发展前景[31-32]。 丝蛋白是一种从蚕丝和蛛丝等天然原料中提取的天然高分子纤维蛋白。丝胶蛋白是一种胶样蛋白,可将蚕丝纤维黏合在一起形成蚕茧,具有免疫原性,能刺激机体产生免疫应答并引起Ⅰ型变应性反应。丝蛋白可促进种子细胞的黏附、增殖和分化,并具有力学性能优异、速度可调、生物相容性高,成骨性能良好等特点[33]。Calabrese等[34]采用超声法制备了丝素,多聚左旋赖氨酸凝胶和丝素,左旋谷氨酸凝胶,发现两种凝胶均能够包裹骨髓间充质干细胞,并且促进其增殖分化,前者促进成骨分化,后者既能促进成骨又能向成脂分化。Fini等[35]用可注射的丝心蛋白凝胶作为支架材料修复兔股骨远端基准大小的骨松质缺损,相对于聚合物支架材料而言,丝心蛋白凝胶能更有效地促进骨再生和骨组织的发育成熟;而且丝心蛋白凝胶不会引起炎症反应,在体内12周的时间内能够不完全降解。Diab等[36]将负载骨形成发生蛋白2的凝胶注人大鼠股骨大段缺损区,12周后获得了完全愈合,证实丝素水凝胶在大段骨缺损有着重要的应用价值。Zhang等[37]体外实验证实丝素凝胶负载血管内皮生长因子或骨形成发生蛋白2能够增强骨再生能力,并且两种因子具有良好的叠加效应。将其用于修复兔股骨髁缺损,获得满意的结果。 但是丝素凝胶支架存在力学强度不足,在体内难以承担外界应力,需要结合内固定系统应用。Meinel等[38]用丝蛋白支架材料结合骨髓基质细胞来修复鼠股骨的节段性缺损结果证实,丝蛋白作为支架材料坚固耐用,具有较好的力学性能,可用于修复承重部位的骨节段缺损。另外,丝蛋白支架材料除用于骨组织的重建外,还广泛应用于关节软骨、韧带和肌腱等骨骼附属结构再生方面的研究。Panas-Perez等[39]将丝素纤维与胶原按照不同的比例混合制成支架,发现在支架的丝素纤维数大于25%的情况下支架的抗拉强度能够达到或超过人体前交叉韧带的抗拉强度(38 MPa)。这证明了丝素纤维有着优越的力学性能,能够满足人体前交叉韧带重建的需要。Li等[40-41]将丝素支架的一端装有磷酸钙,考虑到磷酸钙的易碎性,其外围又装有聚醚醚酮锚钉。在用该丝素-磷酸钙-聚醚醚酮复合物重建猪的前交叉韧带时,作者将有磷酸钙-聚醚醚酮的-端放在股骨端,胫骨端则用挤压螺钉固定,术后3,6 个月取标本进行组织学和力学检测,发现该丝素-磷酸钙-聚醚醚酮复合物与骨愈合良好。这些研究证明了用蚕丝支架重建前交叉韧带的可行性。 异种脱蛋白松质骨也具有良好的支架性能。通过脱脂、脱钙、脱蛋白、深低温冷冻、γ-射线辐照等物理、化学的方法,均能不同程度减少异种骨抗原。脱蛋白骨的生物力学性能较好,原因是Ⅰ型胶原的主体被共价嘧啶交叉键牢固的相互连接不易于溶解[42]。Salama[43]和同事们证实了异种脱蛋白松质骨复合自体骨髓在实验动物和人都能增强成骨化,在这些实验中,异种脱蛋白骨的作用就象一个骨传导支架,为再血管化和成骨细胞的分化提供一个稳定的环境。石玲玲等[44]应用异种脱蛋白骨管复合骨基质明胶(BMG)、骨形态发生蛋白(BMP)、骨膜细胞与复合脱钙骨基质(DBM)、自体红骨髓(RBM)作比较,植入后24周,异种骨管复合骨形态发生蛋白、异种脱蛋白骨管复合骨基质明胶、骨膜细胞完全修复,成骨活跃程度,骨再生量和重建髓腔结构等方面均显著,表明异种脱蛋白皮质骨管复合骨基质明胶、骨形态发生蛋白及骨膜细胞能够有效修复大段骨缺损。 "
| [1] Soucacos PN, Johnson EO, Babis G, et al. An update on recent advances in bone regeneration. Injury. 2008;39 Suppl 2:S1-4. [2] Lomas R, Chandrasekar A, Board TN, et al. Bone allograft in the U.K.:perceptions and realities. Hip Int. 2013;23(5): 427-433.[3] Ghanaati S, Barbeck M, Booms P, et al. Potential lack of “standardized” processing techniques for production of allogeneic and xenogeneic bone blocks for application in humans. Acta Biomater. 2014;10(8):3557-3562.[4] Rafael RD, Felipe PS, Erick RS, et al. Corticocancellous fresh-frozen allograft bone blocks for augmenting atrophied posterior mandibles in humans. Clin Oral Implants Res. 2016; 27(1):39-46.[5] Watanabe Y, Harada N, Sato K, et al. Stem cell therapy: is there a future for reconstruction of large bone defects? Injury. 2016;47 Suppl 1:S47-51.[6] Mark R, Ehsan Z, Malliga R, et al. Osteogenic differentiation of mesenchymal stem cells on a poly (octanediol citrate)/ bioglass composite scaffold in vitro. Mater Design. 2016;(109): 434-442.[7] Rahman RA, Sukri NM, Nazir NM, et al. The potential of 3-dimensional construct engineered from poly (lactic-co-glycolic acid)/fibrin hybrid scaffold seeded with bone marrow mesenchymal stem cells for in vitro cartilage tissue engineering. Tissue Cell. 2015;47(4):420-430.[8] Khojasteh A, Sadeghi N, et al. Application of buccal fat pad-derived stem cells in combination with autogenous iliac bone graft in the treatment of maxillomandibular atrophy: a preliminary human study. Int J Oral Maxillofac Surg. 2016;45(7): 864-871.[9] Ozcan G, Ozpolat B, Coleman RL, et al. Preclinical and clinical development of siRNA-based therapeutics. Adv Drug Deliv Rev. 2015;87:108-119.[10] Ghadakzadeh S, Mekhail M, Aoude A, et al. Small players ruling the hard game: sirna in bone regeneration. J Bone Miner Res. 2016;31(7):1481.[11] Betz VM, Rosin T, Manthey S, et al. An expedited approach for sustained delivery of bone morphogenetic protein-7 to bone defects using gene activated fragments of subcutaneous fat. J Gene Med. 2016;18(8):199-207.[12] Schmidt-bleek K, Willie BM, Schwabe P, et al. BMPs in bone regeneration: less is more effective, a paradigm-shift. Cytokine Growth Factor Rev. 2016;27:141-148. [13] 朱德志.重组人骨形态发生蛋白-2结合纳米晶胶原基骨材料治疗腰椎不稳症的临床效果及安全性评价[J].中国综合临床,2016, 4(32): 358-361.[14] Schneppendahl J, Grassmann JP, Jungbluth P, et al. Synergistic effects of HBO and PRP improve bone regeneration with autologous bone grafting. Injury. 2016; 47(12): 2718-2725.[15] Schneppendahl J, Jungbluth P, Logters TT, et al. Treatment of a diaphyseal long-bone defect with autologous bone grafts and platelet-rich plasma in a rabbit model. Vet Comp Orthop Traumatol. 2015;28(3):164-71.[16] Park HC, Kim SG, Oh JS, et al. Early bone formation at a femur defect using cgf and prf grafts in adult dogs: a compatative study. Implant Dent. 2016;25(3):387-393.[17] 杨宝凯,张旭斌.天然牡蛎壳纳米体复合型骨材料修复骨缺损[J].中国组织工程研究,2015,19(21):3297-3301.[18] 黄谢山,刘明,王江.墨鱼骨转化羟基磷灰石制备及细胞相容性[J].中国组织工程研究,2014,18(16):2532-2537.[19] Mousumi S, Young-Ki M, Byong-Taek L, et al. Collagen- hydroxyapatite coated unprocessed cuttlefish bone as a bone substitute. Mater Lett. 2016;181:156-160.[20] Sumio L. Helical microtubules of graphitic carbon. Nature. 1991; 354(6348):56-58.[21] 姚梦竹,盛晓霞,林军,等.碳纳米管在骨组织工程支架中的研究进展[J].浙江大学学报,2016,45(2):161-169.[22] Tanaka M, Sato Y, Zhang M, et al. In Vitro and In Vivo Evaluation of a Three-Dimensional Porous Multi-Walled Carbon Nanotube Scaffold for Bone Regeneration. Nanomaterials. 2017;7(2):E46.[23] Tanaka M, Sato Y, Nomura H, et al. A three-dimensional block structure consisting exclusively of carbon nanotubes serving as bone regeneration scaffold and as bone defect filler. PLoS One. 2017;12(2):e0172601. [24] Hench LL. The story of bioglass. J Mater Sci Mater Med. 2006; 17(11):967-978. [25] Niu Y, Guo L, Liu J, et al. Bioactive and degradable scaffolds of the mesoporous bioglass and poly( L -lactide) composite for bone tissue regeneration. J Mater Chem B. 2015;3(15): 2962-2970.[26] Fernández CA, Martinz CA, Prado MO, et al. Bone Regeneration with Wharton´s Jelly-Bioceramic-Bioglass Composite. Procedia Mate Sci. 2015.[27] Tang Z , Xie Y, Yang F, et al. Porous tantalum coatings prepared by vacuum plasma spraying enhance bmscs osteogenic differentiation and bone regeneration in vitro and in vivo. PLoS One. 2013;8(6):e66263. [28] 李泳.多孔钛铌合金的表征、生物相容性及在缺损性植骨中的研究[D].长沙:中南大学,2012.[29] de Maat Mp, Verhaar JA, Jahr H, et al. full regeneration of segmental bone defects using porous titanium implants loaded with BMP-2 containing fibrin gels. Eur Cells Mater. 2015;29:141-153. [30] Smith JO, Sengers BG, Aarvold A, et al. Tantalum trabecular metal-addition of human skeletal cells to enhance bone implant interface strength and clinical application. J Tissue Eng Regen Med. 2014;8(4):304-313.[31] Wang Y, Kim HJ, Vunjak-Novakovic G, et al. Stem cellbased tissue engineering with silk biomaterials. Biomaterials. 2006; 27(36):6064-6082.[32] Gamradt SC, Lieberman JR. Bone graft for revision hip arthroplasty: biology and future applications. Clin Orthop Relat Res. 2008;(417):183-194.[33] Mottaghitalab F, Hosseinkhanin H, Shokrgozar MA, et al. Silk as a potential candidate for bone tissue engineering. J Control Release. 2015;(215):112-128.[34] labrese R, Kaplan DL. Silk ionomers for encapsulation and differentiation of human MSCs. Biomaterials. 2012;33(30): 7375-7385.[35] Fini M, Motta A, Torricelli P, et al. The healing of confined critical size cancellous defects in the presence ofsilk fibroin hydrogel. Biomaterials. 2015;26(17):3527-3536.[36] Diab T, Pritchard EM, Uhrig BA, et al. A silk hydrogel-based delivery system of bone morphogenetic protein for the treatment of large bone defects. J Mech Behav Biomed Mater. 2012;11:123-131.[37] Zhang W, Wang X, Wang S, et al. The use of injectable sonicalion-induced silkhydrogel for VEGF l 65 and BMP-2 delivery for elevation of the maxillary sinus floor. Biomaterials. 2011;32(35):9415-9424.[38] Meinel L, Betz O, Fajardo R, et al. Silk based biomaterials to heal critical sized femur defects. Bone. 2016;39(4):922-931.[39] Panas-Perez E, Gatt CJ, Dunn MG. Development of a silk and collagen fiber scaffold for anterior cruciate ligament reconstruction. J Mater Sci Mater Med. 2013;24(1):257-265.[40] Li X, He J, Bian W, et al. A Rovel silk-based artif icial ligament and tricalcium phosphate/polyether ether ketone anchor for anterior cruciate ligament reconstruction -safety and efficacy in a porcine model. Acta Biomater. 2014;10(8):3696-3704.[41] Li X, He J, Bian W, et al. A novel silk-TCP-PEEK construct for anterior cruciate ligament reconstruction: an off-the shelf alernative to a bone-tendon-bone autograft. Biofabrication. 2014;6(1):015010.[42] Boiret N, Rapatel C, Veyrat-Masson R, et al. Characterization of nonexpanded mesenchymal progenitor cells from normal adult human bone marrow. Exp Hematol. 2005;33(2): 219-225.[43] Salama K, Yamazaki S, Katashima T, et al. Silk-pectin hydrogel with superior mechanical properties, biodegradability, and biocompatibility. Macromol Biosci. 2014;14(6):799-806.[44] 石玲玲,丁真奇,郭林新,等.异种脱蛋白骨管复合不同移植材料修复大段骨缺损的实验研究[J].中国骨与关节损伤杂志,2010, 25(12):1089-1091. |
| [1] | Zhang Tongtong, Wang Zhonghua, Wen Jie, Song Yuxin, Liu Lin. Application of three-dimensional printing model in surgical resection and reconstruction of cervical tumor [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1335-1339. |
| [2] | Zeng Yanhua, Hao Yanlei. In vitro culture and purification of Schwann cells: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1135-1141. |
| [3] | Xu Dongzi, Zhang Ting, Ouyang Zhaolian. The global competitive situation of cardiac tissue engineering based on patent analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 807-812. |
| [4] | Wu Zijian, Hu Zhaoduan, Xie Youqiong, Wang Feng, Li Jia, Li Bocun, Cai Guowei, Peng Rui. Three-dimensional printing technology and bone tissue engineering research: literature metrology and visual analysis of research hotspots [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 564-569. |
| [5] | Chang Wenliao, Zhao Jie, Sun Xiaoliang, Wang Kun, Wu Guofeng, Zhou Jian, Li Shuxiang, Sun Han. Material selection, theoretical design and biomimetic function of artificial periosteum [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 600-606. |
| [6] | Liu Fei, Cui Yutao, Liu He. Advantages and problems of local antibiotic delivery system in the treatment of osteomyelitis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 614-620. |
| [7] | Li Xiaozhuang, Duan Hao, Wang Weizhou, Tang Zhihong, Wang Yanghao, He Fei. Application of bone tissue engineering materials in the treatment of bone defect diseases in vivo [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 626-631. |
| [8] | Zhang Zhenkun, Li Zhe, Li Ya, Wang Yingying, Wang Yaping, Zhou Xinkui, Ma Shanshan, Guan Fangxia. Application of alginate based hydrogels/dressings in wound healing: sustained, dynamic and sequential release [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 638-643. |
| [9] | Chen Jiana, Qiu Yanling, Nie Minhai, Liu Xuqian. Tissue engineering scaffolds in repairing oral and maxillofacial soft tissue defects [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 644-650. |
| [10] | Xing Hao, Zhang Yonghong, Wang Dong. Advantages and disadvantages of repairing large-segment bone defect [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 426-430. |
| [11] | Chen Siqi, Xian Debin, Xu Rongsheng, Qin Zhongjie, Zhang Lei, Xia Delin. Effects of bone marrow mesenchymal stem cells and human umbilical vein endothelial cells combined with hydroxyapatite-tricalcium phosphate scaffolds on early angiogenesis in skull defect repair in rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3458-3465. |
| [12] | Wang Hao, Chen Mingxue, Li Junkang, Luo Xujiang, Peng Liqing, Li Huo, Huang Bo, Tian Guangzhao, Liu Shuyun, Sui Xiang, Huang Jingxiang, Guo Quanyi, Lu Xiaobo. Decellularized porcine skin matrix for tissue-engineered meniscus scaffold [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3473-3478. |
| [13] | Mo Jianling, He Shaoru, Feng Bowen, Jian Minqiao, Zhang Xiaohui, Liu Caisheng, Liang Yijing, Liu Yumei, Chen Liang, Zhou Haiyu, Liu Yanhui. Forming prevascularized cell sheets and the expression of angiogenesis-related factors [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3479-3486. |
| [14] | Liu Chang, Li Datong, Liu Yuan, Kong Lingbo, Guo Rui, Yang Lixue, Hao Dingjun, He Baorong. Poor efficacy after vertebral augmentation surgery of acute symptomatic thoracolumbar osteoporotic compression fracture: relationship with bone cement, bone mineral density, and adjacent fractures [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3510-3516. |
| [15] | Liu Liyong, Zhou Lei. Research and development status and development trend of hydrogel in tissue engineering based on patent information [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3527-3533. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||