Chinese Journal of Tissue Engineering Research ›› 2026, Vol. 30 ›› Issue (29): 7612-7618.doi: 10.12307/2026.296
Previous Articles Next Articles
Interaction between vascular-lymphatic system imbalance and immune microenvironment in intervertebral disc degeneration
Du Yaxin1, Zhao Xiaojuan2, Wu Ruixia1, Dong Yizhi1, Song Xinyue1, Fu Hongyang1, She Yitong1, Zhang Jialin1, Zhu Yong3
- 1Inner Mongolia Medical University, Hohhot 010107, Inner Mongolia Autonomous Region, China;2The Second Affiliated Hospital of Inner Mongolia Medical University, Hohhot 010030, Inner Mongolia Autonomous Region, China; 3Peking University Cancer Hospital, Inner Mongolia Hospital (Affiliated Cancer Hospital of Inner Mongolia Medical University), Hohhot 010000, Inner Mongolia Autonomous Region, China
-
Received:2025-09-25Revised:2025-12-19Online:2026-10-18Published:2026-03-04 -
Contact:Zhu Yong, MD, PhD, Chief physician, Professor, Peking University Cancer Hospital, Inner Mongolia Hospital (Affiliated Cancer Hospital of Inner Mongolia Medical University), Hohhot 010000, Inner Mongolia Autonomous Region, China -
About author:Du Yaxin, MS candidate, Rehabilitation therapist, Inner Mongolia Medical University, Hohhot 010107, Inner Mongolia Autonomous Region, China -
Supported by:National Natural Science Foundation of China, No. 82060404 (to ZY); Inner Mongolia Autonomous Region Higher Education Innovation Team Project, No. NMGIRT2229 (to ZY); Central Government Guiding Local Science and Technology Development Fund Project, No. 2022ZY0181 (to ZY); Intervertebral Disc Degeneration University Innovation Team Project, No. YKD2023TD005 (to ZY)
CLC Number:
Cite this article
Du Yaxin, Zhao Xiaojuan, Wu Ruixia, Dong Yizhi, Song Xinyue, Fu Hongyang, She Yitong, Zhang Jialin, Zhu Yong. Interaction between vascular-lymphatic system imbalance and immune microenvironment in intervertebral disc degeneration[J]. Chinese Journal of Tissue Engineering Research, 2026, 30(29): 7612-7618.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
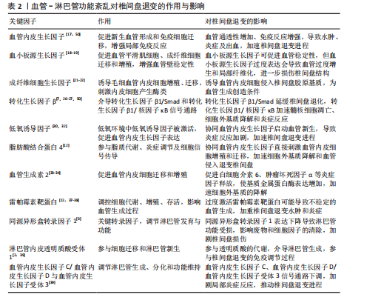
与其他调控因子(脂肪酸结合蛋白4、血管生成素2、雷帕霉素靶蛋白等),淋巴管相关因子包括转录因子(同源异形盒转录因子1)、跨膜蛋白(血管内皮生长因子受体3、淋巴管内皮细胞蛋白)、其他调控因子(淋巴管内皮透明质酸受体1)。 2.2.1 血管新生相关因子 (1)生长因子 血管内皮生长因子:血管内皮生长因子是血管生成的关键因子。AMARO等[13]对217例椎间盘退变患者进行了血管内皮生长因子基因多态性分析,结果显示基因多态性与椎间盘退变呈负相关,提示血管内皮生长因子基因变异可能是椎间盘退变的风险预测因素。AYDIN等[14]发现血管内皮生长因子基因变异可能通过影响血管生成,导致椎间盘退变的发生。CHEN等[15]研究表明,在退化椎间盘中加入血管内皮生长因子抑制剂贝伐珠单抗可降低基质金属蛋白酶3表达、增加Ⅱ型胶原合成,减轻椎间盘退化程度。SHEN等[16]发现褪黑激素能够抑制血管内皮生长因子与其受体的结合,从而发挥抗血管生成作用,因此,褪黑激素可能是预防椎间盘退变的药物。以上研究均证实了血管内皮生长因子在椎间盘退变过程中对炎症因子、胶原代谢、新生血管等方面均起着重要作用,可能是椎间盘退变的治疗靶点。另一方面,虽然血管内皮生长因子促进血管生成为退变椎间盘提供了必要的营养供应,但是新生血管结构不稳定导致血管通透性增加,引起局部炎症、水肿、出血等,可能会进一步加速椎间盘的退变进程[17]。综上所述,血管内皮生长因子可与内皮细胞表面受体结合,促进内皮细胞的增殖、迁移和管腔形成,最终形成新的血管,并且血管内皮生长因子基因发生变异也会影响血管生成,抑制血管内皮生长因子表达可减轻椎间盘退变。 血小板源生长因子:血小板源生长因子是一类由血小板、巨噬细胞、内皮细胞等分泌的生长因子家族,包含血小板源生长因子A、B、C、D等亚型,主要通过结合血小板源生长因子受体α/β激活下游信号通路调控细胞增殖、迁移、血管生成和组织修复。血小板源生长因子在正常和退变椎间盘中存在表达差异,在不同状态下血小板源生长因子在椎间盘退变中的作用具有双重性。研究发现,在椎间盘退变早期,血小板源生长因子可通过抑制细胞焦亡和调节丝裂原活化蛋白激酶信号通路参与抑制椎间盘退变的发生和发展[18]。XU等[19]通过研究发现,血小板源生长因子可增加Ⅱ型胶原蛋白表达,进而逆转髓核细胞退化,还可以通过与胰岛素样生长因子产生协同作用,延缓椎间盘退变。随着研究的深入,SUN等[20]通过单细胞测序发现lumt细胞亚群与椎间盘退变期间纤维环血管形成有关,而血小板源生长因子受体α是lumt细胞亚群特异性表达的标志物之一,表明血小板源生长因子受体α可能介导椎间盘退变时血管侵入纤维环细胞的过程,进而加重椎间盘退变。因此,未来研究方向应结合单细胞测序技术等深入探究血小板源生长因子在不同退变阶段及细胞亚群中的特异性作用,为椎间盘退变的精准治疗提供依据。 成纤维细胞生长因子:成纤维细胞生长因子包括碱性成纤维细胞生长因子和酸性成纤维细胞生长因子,是一类调控细胞增殖、分化和组织修复的重要多肽类生长因子。在骨关节炎和椎间盘退变等退行性疾病中,成纤维细胞生长因子可刺激毛细血管内皮细胞增殖,其中碱性成纤维细胞生长因子较酸性成纤维细胞生长因子的效力更强,同时促使内皮细胞迁移,诱导内皮细胞侵入三维胶原基质并组织成类似毛细血管的小管,还可以刺激内皮细胞产生蛋白酶体激活因子等蛋白酶,参与细胞外基质降解,为血管生成创造条件[21-22]。TOLONEN等[23]对人退变椎间盘进行免疫组化研究,发现所有退变椎间盘都表现为碱性成纤维细胞生长因子免疫阳性,并且在不同的椎间盘区域有不同表达。碱性成纤维细胞生长因子主要分布在血管及纤维环损伤附近的细胞内,说明其参与了椎间盘损伤后的血管生成。郭义等[24]发现血府逐瘀汤能上调退变椎间盘中血管内皮生长因子、碱性成纤维细胞生长因子和转化生长因子蛋白的表达,促进微血管生成。LU等[25]研究兔椎间盘退变过程中成纤维细胞生长因子18的作用,发现成纤维细胞生长因子18过表达组中基质金属蛋白酶3、含Ⅰ型血小板结合蛋白基序的解聚蛋白样金属蛋白酶5、Bax表达降低,Bcl-2蛋白表达增加,裂解型caspase3阳性百分比较低,表明成纤维细胞生长因子18可通过削减髓核细胞凋亡及基质降解酶的表达减缓椎间盘退变进程。从总体上来看,成纤维细胞生长因子在椎间盘退变过程中的作用也许存在剂量依赖或者阶段分化特征,需要更多研究才能明确其详细机制。 转化生长因子β:转化生长因子β是一种多功能细胞因子,在哺乳动物中由33个基因编码,几乎在所有细胞类型和组织中广泛表达。转化生长因子β信号传导可以刺激多种细胞反应,对胚胎发育、伤口愈合和健康免疫稳态尤为关键。在椎间盘退变中,转化生长因子β可通过多种信号途径发挥作用,其中比较经典的包括通过激活转化生长因子β1/Smad2/3信号通路延缓椎间盘退化,也可以通过转化生长因子β1/核因子κB信号通路导致髓核细胞凋亡、细胞外基质降解和炎症反应,从而加速椎间盘退变[26-27],表明转化生长因子β1在生物过程中作用的复杂性。CUI等[7]发现转化生长因子β1通过促进血管生成素2加重退行性髓核细胞炎症和纤维化,提示转化生长因子β1可能参与椎间盘退变过程中的血管形成,进而加速退变进程。WANG等[28]对小鼠退变椎间盘进行血管成像,结果显示软骨终板血管体积增加,这与以往研究一致;转化生长因子β1能够抑制软骨终板中破骨细胞分化和异常的骨相关血管生成来缓解椎间盘退变,体现了转化生长因子β1在血管生成中的两面性作用。由于转化生长因子β在多种生物过程中的重要性,需要与其他生长因子和信号通路相结合才能更全面地了解其在椎间盘退变中的复杂作用。 (2)低氧诱导因子:低氧诱导因子是低氧环境下稳定并激活的转录因子,主要包含低氧诱导因子1α和低氧诱导因子2α,在细胞适应低氧环境时发挥重要作用。椎间盘退变后软骨终板功能降低,局部区域氧气供应短缺,产生低氧环境,这时低氧诱导因子被激活,进而影响血管生成、能量代谢及细胞存活的基因表达。研究发现,过表达低氧诱导因子1α可以增加人髓核细胞中P胶原和聚集蛋白的表达,减缓椎间盘退变进程[29];同时,低氧诱导因子激活可以增加血管内皮生长因子的表达和分泌,从而间接促进椎间盘内形成新生血管[30]。在骨代谢疾病中,低氧诱导因子1α作为耦合血管生成和成骨的重要途径,可在不同条件下双向调节巨噬细胞向破骨细胞的分化[31]。SONG等[32]研究发现,低氧诱导因子1α通过血管内皮生长因子/蛋白激酶B/雷帕霉素靶蛋白信号通路耦合成骨和血管生成,进一步说明了低氧诱导因子1α在椎间盘退变血管生成过程中的作用。 (3)脂肪酸结合蛋白4:脂肪酸结合蛋白4是脂肪酸结合蛋白家族成员之一,主要在脂肪细胞、巨噬细胞和部分上皮细胞中高表达,能够与长链脂肪酸、类花生酸等结合,参与脂质代谢、炎症调节及细胞信号传导。脂肪酸结合蛋白4具有促血管生成作用,主要在滑膜炎、类风湿性关节炎和肿瘤疾病代谢中发挥重要作用。HAN等[12]通过研究确定了脂肪酸结合蛋白4是椎间盘退变和肥胖之间的潜在调节因子,脂肪酸结合蛋白4通过促进脂质过氧化和晚期糖基化终产物的生成激活晚期糖基化终产物受体,进而触发核因子κB信号通路,核因子κB的活化导致促炎因子白细胞介素1β、肿瘤坏死因子α和基质金属蛋白酶的过度表达,从而加速细胞外基质的降解;同时,脂肪酸结合蛋白4通过上调血管内皮生长因子的表达直接刺激血管内皮细胞的增殖和迁移,加剧血管侵入退变椎间盘。但与之相关研究较少,未来可进一步研究。 (4)血管生成素2:血管生成素2是血管生成素家族成员之一,它通过与酪氨酸激酶受体Tie2结合在血管生成和炎症调控中发挥重要作用。血管生成素2的功能具有双向性:在缺乏血管内皮生长因子时,血管生成素2通过拮抗血管生成素1的稳定作用破坏血管内皮细胞与基质的接触,诱导血管退化;当血管内皮生长因子存在时,血管生成素2协同促进血管内皮细胞的迁移和增殖。血管生成素2还可以激活核因子κB等炎症通路促进白细胞介素6、肿瘤坏死因子α等炎症因子释放,增加基质金属蛋白酶的表达[33]。AO等[34]研究表明,机械应力可以介导血管生成素2的表达调控低氧诱导因子1α/核因子κB信号通路,影响血管生成和基质降解。CUI等[7]的研究表明,转化生长因子β1通过介导血管生成素2加重退行性髓核细胞炎症和纤维化,说明血管生成素2在血管形成过程中起着介质作用。YU等[35]发现长链非编码RNA GAS5通过降低血管生成素2的表达减少了髓核细胞凋亡、抑制了椎间盘退变。这些研究均表明血管生成素2在椎间盘退变中促进血管形成的介导作用,为预防和治疗椎间盘退变提供了新的思路和方法。 (5)雷帕霉素靶蛋白:雷帕霉素靶蛋白是一种丝氨酸/苏氨酸激酶,属于磷脂酰肌醇3-激酶相关激酶家族,在各种退行性疾病中起着至关重要的作用[36]。雷帕霉素靶蛋白在椎间盘退变中主要通过调控蛋白质合成和细胞代谢调节细胞的能量状态和氧气需求,影响血管生成过程。既往研究发现,磷脂酰肌醇3-激酶/蛋白激酶B/雷帕霉素靶蛋白通路是调控椎间盘血管生成的核心通路,调控雷帕霉素靶蛋白可有效减轻髓核细胞损伤、延缓椎间盘退变[37-38]。HAN等[12]发现在肥胖相关退变椎间盘中,脂肪酸结合蛋白4通过雷帕霉素靶蛋白C1信号轴上调血管内皮生长因子表达,促进病理性血管生成,而雷帕霉素可通过抑制雷帕霉素靶蛋白C1减少脂肪酸结合蛋白4的表达,从而减轻血管生成和细胞外基质的降解。 2.2.2 淋巴管相关因子 椎间盘退变过程中关于淋巴管的作用及机制尚未完全明确,相关研究较少,目前已经明确椎间盘退变过程伴随着淋巴管障碍,但具体作用机制仍不明确。研究表明,退变椎间盘中淋巴管数量减少而炎症细胞较多,推测可能由于退变区域的废物和炎症因子等无法及时清除从而加剧了退变椎间盘的局部免疫反应和组织损伤,导致椎间盘退变[3]。 同源异型盒转录因子1是淋巴管发育的关键转录因子,主要调节淋巴管内皮细胞的增殖与迁移。在淋巴系统发育过程中,同源异型盒转录因子1激活血管内皮生长因子受体3和淋巴管内皮细胞蛋白等基因促使淋巴管从静脉系统中分离出来,形成独立的网络结构。淋巴管内皮透明质酸受体1是同源异型盒转录因子1调控的靶基因之一,可能参与细胞迁移和淋巴管新生。在实验研究中,淋巴管内皮透明质酸受体1常常和同源异型盒转录因子1一起被当作淋巴管内皮的双重标记。KASHIMA等[2]对儿童和成人的椎骨和椎间盘进行免疫组织化学染色,发现正常椎间盘和椎骨中未见淋巴管存在,而淋巴管仅存在于骨膜外、椎旁韧带以及周围的结缔组织中;然而,在退变椎间盘组织中不仅检测到CD31?/CD34?等血管标志物,还检测到淋巴管内皮透明质酸受体1阳性/淋巴管内皮细胞蛋白阳性淋巴管,推测退变椎间盘中的淋巴管可能来源于周围结缔组织中的淋巴管。SALO等[39]对猪椎间盘进行研究,发现与淋巴管生成相关的血管内皮生长因子C和血管内皮生长因子D在椎间盘退变实验组和对照组中均有表达,同时血管内皮生长因子受体3作为上述两者的受体也是淋巴管内皮细胞的标志物,在实验样本中的表达高于对照组;此外,在纤维环中看到一些表达淋巴管内皮透明质酸受体1的微小淋巴管,说明该实验性猪椎间盘退变模型中的淋巴管可能上调。ZOU等[3]的研究在健康椎间盘纤维环中检测到淋巴管标记基因同源异形盒转录因子1、DSP和JUP的表达,免疫组化染色也证实了淋巴管内皮透明质酸受体1和同源异型盒转录因子1在纤维环组织中的表达,这些结果清楚地表明了健康椎间盘中存在淋巴管;在退变椎间盘组中,同源异型盒转录因子1和淋巴管内皮透明质酸受体1的表达明显下降,而CD31和内黏蛋白的表达明显升高,说明健康椎间盘中淋巴管较多而炎症细胞较少,而退变椎间盘中淋巴管数量减少、炎症细胞增多且不能被有效清除,导致炎症加重;并且在大鼠椎间盘退变模型中,过表达同源异型盒转录因子1可减少髓核细胞死亡、恢复纤维环的排列、逆转退变纤维环中同源异型盒转录因子1的下降趋势。经过学者们的不断探索,发现在健康和退变椎间盘中均存在淋巴管,在退变早期淋巴管生成上调,这可能是椎间盘早期退变的一种代偿方式;但随着椎间盘退变进程的持续进展,淋巴管的代偿能力逐渐降低、数量也减少,最后不能有效地清除炎症因子,加快椎间盘退变进程。 近年来,研究者们逐渐认识到可利用单细胞测序技术和生物信息学分析等手段进行椎间盘与淋巴功能的相关研究,更深入地揭示淋巴管相关因子在椎间盘退变过程中的具体作用。SONG等[40]通过生物信息学分析对椎间盘退变中的免疫浸润生物标志物进行检测,发现椎间盘退变患者的T细胞、淋巴细胞、B细胞和 NK细胞减少,而单核细胞、中性粒细胞和CD8 T细胞增加,提示椎间盘退变过程中可能存在免疫细胞的重新分布和免疫微环境的改变。淋巴管作为免疫系统的一部分,可能通过调节免疫细胞的迁移和归巢参与椎间盘退变的免疫调节过程。HUANG等[41]通过生物信息学分析发现,在椎间盘退变中淋巴管内皮透明质酸受体1参与了透明质酸的代谢过程,可能与透明质酸合酶2、透明质酸酶1共同发挥调节作用,具体机制是:miR663AHG/HEIH/hsa-circ-0003600表达增加可能抑制miR-4741,并间接上调透明质酸合酶2/透明质酸酶1/淋巴管内皮透明质酸受体1表达,淋巴管内皮透明质酸受体1的表达增加可能使得代谢废物有效排除,从而延缓椎间盘退变的发展。冯阳等[42]通过流式细胞仪对腰椎间盘退行性疾病患者和健康志愿者的外周血进行淋巴细胞亚群检测,发现腰椎间盘退行性改变可能与外周血各淋巴细胞亚群改变有关,并且CD4+ T细胞增多、自然杀伤细胞增多以及CD4+/CD8+比值增高可能加速腰椎间盘退变,暗示这可能成为腰椎间盘退变性疾病的防治靶点。LIN等[11]利用机器学习算法建立并验证了能够有效识别椎间盘退变患者淋巴管相关基因诊断模型,该模型锁定了5个淋巴管相关基因:MET、HIP、SPRY1、CSF1和TOX,这5个基因可能是椎间盘退变患者的潜在治疗靶点。 综上所述,目前学者们已经认识到淋巴管在椎间盘退变中的重要作用,但是相关研究仍停留在理论阶段,后续仍需进一步探究。 2.3 椎间盘退变中血管-淋巴管紊乱机制与影响 血管异常增生是椎间盘退变过程中的一个病理特点[43]。部分学者认为血管增生是退变椎间盘的一种防御性机制,新生血管为椎间盘带来额外的营养,试图减缓退变进程。另一种观点则认为这种异常的血管增生不但加重了椎间盘内的炎症反应,而且促进了免疫细胞的浸润,进一步加速了椎间盘的结构破坏和功能丧失[44-48]。此外,淋巴管在椎间盘退变中的作用也渐渐被重视起来,在退变椎间盘中淋巴管的功能可能受到损害,导致炎症反应加重、退变加速[3,49],见表2。 2.4 椎间盘退变中的免疫微环境变化及影响 2.4.1 免疫微环境的变化 免疫细胞浸润:椎间盘退变过程中局部免疫细胞浸润逐渐增多,以巨噬细胞、T细胞和B细胞尤为明显,这些免疫细胞积聚既是椎间盘退变过程中的一个迹象,又加强了局部免疫反应[51]。CLAYTON等[52]通过研究发现,损伤椎间盘中有中性粒细胞、巨噬细胞和单核细胞等免疫细胞浸润,指出免疫细胞浸润和血管生成在急性椎间盘损伤响应中相关联;从基因层面来看,上调的差异表达基因中,血管生成和T细胞调节相关的生物过程最为富集,如促血管生成基因血管内皮生长因子、血小板源生长因子、Nrp1和Hspb1主要由中性粒细胞、外纤维环调节,与T细胞调节有关的基因Hs2-dmb1、Iglas3、Irf1、Hsbp1、Icam1、Ccl2主要由巨噬细胞、中性粒细胞、Krt18?髓核细胞和外纤维环调节,说明了在免疫细胞浸润过程中相关基因的表达变化与血管生成相关基因的表达相互关联。 免疫耐受性的丧失:在正常生理条件下,髓核被纤维环和软骨终板覆盖在一个特殊的封闭空间,是体内最大的免疫豁免组织,这种低免疫反应性使得免疫耐受性得以维持,但随着椎间盘退变的发展,髓核暴露于免疫系统,大量免疫细胞浸润诱导免疫反应,局部慢性炎症产生,免疫耐受性慢慢消失,椎间盘退变加重[40,44,51]。SONG等[40]通过生信分析和基因验证实验发现,椎间盘退变患者存在明显的免疫细胞浸润,包括活化的B细胞、CD8+ T细胞和自然杀伤细胞,这些浸润的免疫细胞释放大量炎症因子(如肿瘤坏死因子α和白细胞介素1β)使得髓核组织失去豁免,进一步加重椎间盘退变。 细胞因子的变化:椎间盘退变时,促炎细胞因子和趋化因子的水平明显上升,特别是肿瘤坏死因子α、白细胞介素1β、白细胞介素6和白细胞介素17[53-54],这些变化不但增加免疫细胞浸润,还通过激活一些信号通路,如核因子κB、丝裂原激活蛋白激酶信号通路,进一步加重椎间盘退变[55]。WANG等[56]的研究发现,一种电磁场氧化铁纳米颗粒能够激活p38丝裂原激活蛋白激酶通路推进腰椎间盘退行性疾病患者的成骨和血管生成。EASSON等[57]研究指出,对椎间盘施加压力负荷后,持续的压力会导致核因子κB活性增加与白细胞介素6、血管内皮生长因子A的生成,造成细胞外基质退行性改变。以上研究表明,椎间盘退变后细胞因"
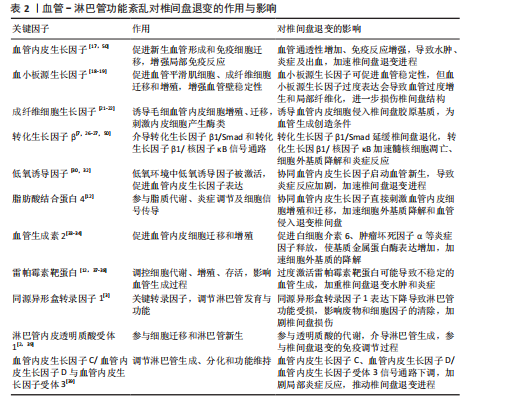

子的变化会导致血管新生增多,从而促进椎间盘退变。 2.4.2 免疫微环境变化对椎间盘退变的长期影响 加速椎间盘退变进程:椎间盘退变过程中会产生具有不同特性的免疫细胞,这些免疫细胞的释放会引起椎间盘炎症反应和血管生成,使细胞外基质降解[51]。BINCH等[58]对人类椎间盘的神经营养因子及其受体、神经肽和血管生成因子的天然基因表达进行了研究,发现严重退化和免疫细胞浸润的椎间盘中白细胞介素1β和白细胞介素6水平显著升高,进而增加髓核细胞中神经生长因子受体和血管内皮生长因子的表达,促进神经元和血管的生成,同时也增加基质降解酶的产生,导致椎间盘退变。 局部慢性疼痛:椎间盘退变过程中免疫微环境变化与慢性疼痛的发生存在联系,免疫细胞分泌细胞因子(如肿瘤坏死因子α、白细胞介素6等)激活痛觉神经元,引起疼痛感知增强。BINCH等[59]对人退变椎间盘进行相关检测,发现信号素3C在含有血管及神经的样本中显著增加,暗示信号素3C可能在退化过程中促进神经支配和血管形成,并引发腰痛症状。ZHENG等[60]通过研究证实,神经轴突导向因子1可促进椎间盘退化过程中神经支配及血管生成,诱发椎间盘源性腰痛,CRISPR/Cas9敲低神经轴突导向因子1可以抑制脊髓超敏反应。CHEN等[61]发现椎间盘内各种蛋白水解酶(如氨肽酶)的表达水平与椎间盘内微血管形成、神经纤维长入之间存在线性关系,可能与椎间盘源性腰痛的发生有关。以上发现有助于对椎间盘退变的分子水平和病理生理学机制进一步研究。 修复能力降低:免疫微环境发生变化(如免疫细胞过度活跃、慢性炎症反应出现)让椎间盘在退变时失去有效的修复机制,细胞再生能力被削弱,椎间盘自我修复潜力降低。有研究表明,将生长分化因子5注射到小鼠椎间盘内可有效改善椎间盘退化,而且不会促使血管长入椎间盘内部[62],这种方法在修复椎间盘结构和功能方面比较稳定,或许能给椎间盘退变的治疗带来新思路。 2.5 椎间盘退变中血管-淋巴管紊乱与免疫微环境调控的相互作用 血管-淋巴管紊乱增加了免疫细胞浸润、加剧局部炎症反应,导致椎间盘基质的降解和退变进程的加速。在退变椎间盘中,血管内皮生长因子表达升高可能有利于椎间盘内的营养物质供应,但同时基质金属蛋白酶3等促炎因子表达也随之增加,抑制Ⅱ型胶原蛋白的合成,从而加重了椎间盘退变程度[15]。椎间盘退变后淋巴管数量减少,导致免疫细胞和废物清除受阻,局部炎症反应持续存在,进一步加重退变程度[3]。 免疫微环境变化不仅影响免疫细胞的活性和浸润,还会对血管-淋巴管产生调节作用。ZHANG等[10]发现,巨噬细胞浸润可诱导退变椎间盘组织中髓核纤维化和病理性血管生成。还有研究发现,趋化因子基质细胞衍生因子1通过磷脂酰肌醇3-激酶/蛋白激酶B通路在退化椎间盘的血管生成中发挥作用[63]。与此同时,持续的免疫反应通过促炎因子的分泌抑制了淋巴管的正常功能,进一步削弱其清除代谢废物和免疫细胞的能力。例如,血管内皮生长因子C和血管内皮生长因子D通过与血管内皮生长因子受体3结合调节淋巴管的生成与维持,但在持续的免疫激活下,血管内皮生长因子C/血管内皮生长因子受体3信号通路下调导致淋巴管功能受损,免疫细胞迁移和废物清除的效率降低,进一步加剧局部免疫微环境失衡[39]。还有研究强调了细胞焦亡后免疫微环境变化对椎间盘血管化、神经纤维支配以及淋巴管浸润方面的调节作用[64]。将免疫微环境与椎间盘退变过程中的血管-淋巴管功能相联系,可能为深入理解椎间盘退变的机制提供一个新的角度。 综上所述,在椎间盘退变过程中,血管-淋巴管紊乱与免疫微环境调控相互作用是一个复杂且精细的过程,在椎间盘退变的特定阶段和特定微环境下,血管-淋巴管与免疫微环境变化的时序及动态调控问题仍需进一步研究。"

| [1] FOURNIER DE, KISER PK, SHOEMAKER JK, et al. Vascularization of the human intervertebral disc: A scoping review. JOR Spine. 2020;3(4): e1123. [2] KASHIMA TG, DONGRE A, ATHANASOU NA. Lymphatic involvement in vertebral and disc pathology. Spine (Phila Pa 1976). 2011;6(11): 899-904. [3] ZOU F, LU X, WANG S, et al. Revealing the presence of lymphatic vessels within intervertebral discs: Novel insights into disc degeneration. Innovation (Camb). 2025;6(6): 100865. [4] CAPOSSELA S, BERTOLO A, GUNASEKERA K, et al. VEGF vascularization pathway in human intervertebral disc does not change during the disc degeneration process. BMC Res Notes. 2018;11(1):333. [5] DAVID G, CIUREA AV, IENCEAN SM, et al. Angiogenesis in the degeneration of the lumbar intervertebral disc. J Med Life. 2010; 3(2):154-161. [6] DOU Y, ZHANG Y, LIU Y, et al. Role of macrophage in intervertebral disc degeneration. Bone Res. 2025;13(1):15. [7] CUI L, WEI H, LI Z, et al. TGF-β1 aggravates degenerative nucleus pulposus cells inflammation and fibrosis through the upregulation of angiopoietin-like protein 2 expression. Eur Rev Med Pharmacol Sci. 2020;24(23):12025-12033. [8] SUN Z, ZHAO H, LIU B, et al. AF cell derived exosomes regulate endothelial cell migration and inflammation: Implications for vascularization in intervertebral disc degeneration. Life Sci. 2021;265:118778. [9] YI Y, CHEN H, ZHANG S, et al. Exogenous Klotho ameliorates extracellular matrix degradation and angiogenesis in intervertebral disc degeneration via inhibition of the Rac1/PAK1/MMP-2 signaling axis. Mech Ageing Dev. 2022; 207:111715. [10] ZHANG S, WANG P, HU B, et al. Inhibiting Heat Shock Protein 90 Attenuates Nucleus Pulposus Fibrosis and Pathologic Angiogenesis Induced by Macrophages via Down-Regulating Cell Migration-Inducing Protein. Am J Pathol. 2023;193(7):960-976. [11] LIN M, LI S, WANG Y, et al. Machine learning-based diagnostic model of lymphatics-associated genes for new therapeutic target analysis in intervertebral disc degeneration. Front Immunol. 2024;15:1441028. [12] HAN L, LI F, WU H, et al. Targeting FABP4 to Inhibit AGEs-RAGE/NF-κB Signalling Effectively Ameliorates Nucleus Pulposus Dysfunction and Angiogenesis in Obesity-Related Intervertebral Disc Degeneration. Cell Prolif. 2025;58(9):e70021. [13] AMARO A, GUERRA AB, DEFINO MP, et al. Vascular endothelial growth factor gene variations as a risk predictor in disc degeneration. Einstein (Sao Paulo). 2017;15(4): 403-408. [14] AYDIN HE, YIGIT S, KAYA I, et al. VEGF and eNOS variants may influence intervertebral disc degeneration. Nucleosides Nucleotides Nucleic Acids. 2022;41(10):982-993. [15] CHEN Q, WANG J, XIA Q, et al. Treatment outcomes of injectable thermosensitive hydrogel containing bevacizumab in intervertebral disc degeneration. Front Bioeng Biotechnol. 2022;10:976706. [16] SHEN C, LI Y, CHEN Y, et al. Melatonin prevents the binding of vascular endothelial growth factor to its receptor and promotes the expression of extracellular matrix-associated genes in nucleus pulposus cells. Exp Ther Med. 2020;20(5):106. [17] HUANG Y, XIAO J, LEUNG VY, et al. Lumbar intervertebral disc allograft transplantation: the revascularisation pattern. Eur Spine J. 2018;27(3):728-736. [18] ZHANG W, GONG Y, ZHENG X, et al. Platelet-Derived Growth Factor-BB Inhibits Intervertebral Disc Degeneration via Suppressing Pyroptosis and Activating the MAPK Signaling Pathway. Front Pharmacol. 2021;12:799130. [19] XU G, ZHANG C, ZHU K, et al. [Effects of lentivirus-mediated insulin-like growth factor 1 and platelet derived growth factor genes on nucleus pulposus tissue of human degenerated intervertebral disc]. Zhongguo Xiu Fu Chong Jian Wai Ke Za Zhi. 2020;34(7):907-914. [20] SUN H, WANG H, ZHANG W, et al. Single-cell RNA sequencing reveals resident progenitor and vascularization-associated cell subpopulations in rat annulus fibrosus. J Orthop Translat. 2023;38:256-267. [21] KIM JH, HAM CH, KWON W. Current Knowledge and Future Therapeutic Prospects in Symptomatic Intervertebral Disc Degeneration. Yonsei Med J. 2022; 63(3):199-210. [22] LI H, ZHANG J, YUAN D, et al. Role of signaling pathways in age-related orthopedic diseases: focus on the fibroblast growth factor family. Mil Med Res. 2024;11(1):40. [23] TOLONEN J, GRONBLAD M, VANHARANTA H, et al. Growth factor expression in degenerated intervertebral disc tissue. An immunohistochemical analysis of transforming growth factor beta, fibroblast growth factor and platelet-derived growth factor]. Eur Spine J. 2006;15(5):588-596. [24] 郭义,林俊.血府逐瘀汤影响退变椎间盘髓核组织内蛋白水解酶和微血管生成的机制[J].中国老年学杂志,2020,40(22):4841-4846. [25] LU S, LIN C. Lentivirus-mediated transfer of gene encoding fibroblast growth factor-18 inhibits intervertebral disc degeneration. Exp Ther Med. 2021;22(2):856. [26] ZHANG X, LI G, TAN F, et al. MARCHF8-mediated ubiquitination via TGFBI regulates NF-kappaB dependent inflammatory responses and ECM degradation in intervertebral disc degeneration. PLoS One. 2025;20(1):e314021. [27] YANG H, YUAN C, WU C, et al. The role of TGF-beta1/Smad2/3 pathway in platelet-rich plasma in retarding intervertebral disc degeneration. J Cell Mol Med. 2016;20(8):1542-1549. [28] WANG K, WU Z, GONG C, et al. TGF-β1 Inhibits Osteoclast Differentiation and Abnormal Angiogenesis in Intervertebral Disc Degeneration: Evidence from RNA Sequencing and Animal Studies. Orthop Surg. 2024;16(1):167-182. [29] LIU Z, LI C, MENG X, et al. Hypoxia-inducible factor-lalpha mediates aggrecan and collagen Pi expression via NOTCH1 signaling in nucleus pulposus cells during intervertebral disc degeneration. Biochem Biophys Res Commun. 2017;488(3):554-561. [30] LI Y, LIU S, PAN D, et al. The potential role and trend of HIF-1alpha in intervertebral disc degeneration: Friend or foe? (Review). Mol Med Rep. 2021;23(4):239. [31] CHEN W, WU P, YU F, et al. HIF-1alpha Regulates Bone Homeostasis and Angiogenesis, Participating in the Occurrence of Bone Metabolic Diseases. Cells. 2022;11(22):3552. [32] SONG S, ZHANG G, CHEN X, et al. HIF-1alpha increases the osteogenic capacity of ADSCs by coupling angiogenesis and osteogenesis via the HIF-1alpha/VEGF/AKT/mTOR signaling pathway. J Nanobiotechnology. 2023;21(1):257. [33] WANG K, LIU W, SONG Y, et al. The role of angiopoietin-2 in nucleus pulposus cells during human intervertebral disc degeneration. Lab Invest. 2017;97(8):971-982. [34] AO X, LI Y, JIANG T, et al. Angiopoietin-2 Promotes Mechanical Stress-induced Extracellular Matrix Degradation in Annulus Fibrosus Via the HIF-1alpha/NF-kappaB Signaling Pathway. Orthop Surg. 2023;15(9): 2410-2422. [35] YU X, LIU Q, WANG Y, et al. Depleted Long Noncoding RNA GAS5 Relieves Intervertebral Disc Degeneration via microRNA-17-3p/Ang-2. Oxid Med Cell Longev. 2022;2022:1792412. [36] CHEN H, ZHOU J, ZHANG G, et al. Emerging role and therapeutic implication of mTOR signalling in intervertebral disc degeneration. Cell Prolif. 2023;56(1):e13338. [37] ZHANG C, LI Z, LI L, et al. Achyranthoside D (AD) improve intervertebral disc degeneration through affect the autophagy and the activation of PI3K/Akt/mTOR pathway. J Orthop Surg (Hong Kong). 2022;30(3):773407346. [38] YURUBE T, BUCHSER WJ, ZHANG Z, et al. Rapamycin mitigates inflammation-mediated disc matrix homeostatic imbalance by inhibiting mTORC1 and inducing autophagy through Akt activation. JOR Spine. 2024;7(1):e1303. [39] SALO J, KAIGLE HOLM A, INDAHL A, et al. Expression of vascular endothelial growth factor receptors coincide with blood vessel in-growth and reactive bone remodelling in experimental intervertebral disc degeneration. Clin Exp Rheumatol. 2008;26(6):1018-1026. [40] SONG C, ZHOU D, CHENG K, et al. Bioinformatics-based discovery of intervertebral disc degeneration biomarkers and immune-inflammatory infiltrates. JOR Spine. 2024;7(1):e1311. [41] HUANG J, LI Y, YE Z, et al. Prediction of a Potential Mechanism of Intervertebral Disc Degeneration Based on a Novel Competitive Endogenous RNA Network. Biomed Res Int. 2021;2021:6618834. [42] 冯阳,严旭,王永魁,等.腰椎间盘退变性疾病与外周血淋巴细胞亚群的关系[J].中国组织工程研究,2020,24(17):2630-2635. [43] DE CAMPOS MF, DE OLIVEIRA CP, NEFF CB, et al. STudies of molecular changes in intervertebral disc degeneration in animal model. Acta Ortop Bras. 2016;24(1):16-21. [44] KIM JH, HAM CH, KWON W. Current Knowledge and Future Therapeutic Prospects in Symptomatic Intervertebral Disc Degeneration. Yonsei Med J. 2022;63(3):199-210. [45] KWON W, MOON H J, KWON T, et al. Influence of rabbit notochordal cells on symptomatic intervertebral disc degeneration: anti-angiogenic capacity on human endothelial cell proliferation under hypoxia. Osteoarthritis Cartilage. 2017;25(10):1738-1746. [46] KWON W, MOON HJ, KWON T, et al. The Role of Hypoxia in Angiogenesis and Extracellular Matrix Regulation of Intervertebral Disc Cells During Inflammatory Reactions. Neurosurgery. 2017;81(5):867-875. [47] 陈紫轩,徐波,黄泽灵,等.椎间盘退变过程中血管新生的研究进展[J].医学研究杂志, 2024,53(7):10-13. [48] ZHANG S, TONG M, LI S, et al. The Role of Microvascular Variations in the Process of Intervertebral Disk Degeneration and Its Regulatory Mechanisms: A Literature Review. Orthop Surg. 2024;16(11):2587-2597. [49] PRAVDYUK NG, NOVIKOVA AV, SHOSTAK NA, et al. Immunomorphogenesis in Degenerative Disc Disease: The Role of Proinflammatory Cytokines and Angiogenesis Factors. Biomedicines. 2023;11(8):2184. [50] SWAHN H, MERTENS J, OLMER M, et al. Shared and Compartment-Specific Processes in Nucleus Pulposus and Annulus Fibrosus During Intervertebral Disc Degeneration. Adv Sci (Weinh). 2024; 11(17):e2309032. [51] XU H, LI J, FEI Q, et al. Contribution of immune cells to intervertebral disc degeneration and the potential of immunotherapy. Connect Tissue Res. 2023;64(5):413-427. [52] CLAYTON SW, SEBASTIAN A, WILSON SP, et al. Single cell RNA sequencing reveals shifts in cell maturity and function of endogenous and infiltrating cell types in response to acute intervertebral disc injury. Exp Cell Res. 2025;451(1):114691. [53] TAN J, LI Z, LIU L, et al. IL-17 in intervertebral disc degeneration: Mechanistic insights and therapeutic implications. Cell Biol Int. 2022;46(4):535-547. [54] WANG N, CHEN S, XIE Y, et al. The Sanbi Decoction alleviates intervertebral disc degeneration in rats through intestinal flora and serum metabolic homeostasis modulation. Phytomedicine. 2024;127:155480. [55] PENG B, LI Q, CHEN J, et al. Research on the role and mechanism of IL-17 in intervertebral disc degeneration. Int Immunopharmacol. 2024;132:111992. [56] WANG T, ZHAO H, JING S, et al. Magnetofection of miR-21 promoted by electromagnetic field and iron oxide nanoparticles via the p38 MAPK pathway contributes to osteogenesis and angiogenesis for intervertebral fusion. J Nanobiotechnology. 2023;21(1):27. [57] EASSON GWD, SAVADIPOUR A, ANANDARAJAH A, et al. Modulation of TRPV4 protects against degeneration induced by sustained loading and promotes matrix synthesis in the intervertebral disc. FASEB J. 2023;37(2): e22714. [58] BINCH ALA, COLE AA, BREAKWELL LM, et al. Expression and regulation of neurotrophic and angiogenic factors during human intervertebral disc degeneration. Arthritis Res Ther. 2014;16(5):416. [59] BINCH ALA, COLE AA, BREAKWELL LM, et al. Class 3 semaphorins expression and association with innervation and angiogenesis within the degenerate human intervertebral disc. Oncotarget. 2015;6(21): 18338-18354. [60] ZHENG B, LI S, XIANG Y, et al. Netrin-1 mediates nerve innervation and angiogenesis leading to discogenic pain. J Orthop Translat. 2023;39:21-33. [61] CHEN D, JIANG X. Correlation Between Proteolytic Enzymes and Microangiogenesis in Degenerative Intervertebral Disc Nucleus. J Invest Surg. 2021;34(6):679-684. [62] GUO S, CUI L, XIAO C, et al. The Mechanisms and Functions of GDF-5 in Intervertebral Disc Degeneration. Orthop Surg. 2021;13(3):734-741. [63] ZHANG H, WANG P, ZHANG X, et al. SDF1/CXCR7 Signaling Axis Participates in Angiogenesis in Degenerated Discs via the PI3K/AKT Pathway. DNA Cell Biol. 2019;38(5): 457-467. [64] GE Y, CHEN Y, GUO C, et al. Pyroptosis and Intervertebral Disc Degeneration: Mechanistic Insights and Therapeutic Implications. J Inflamm Res. 2022;15:5857-5871. [65] BOTELHO CM, RODRÍGUEZ-CABELLO JC, BARBOSA MA. Harnessing Thrombospondin-1-Enabled Decellularized Nucleus Pulposus Matrices and Elastin-Like Recombinamers to Rebuild an Avascular Analogue of the Intervertebral Disc. J Biomed Mater Res A. 2025;113(5):e37911. |
| [1] | Zhu Xiaolong, Zhang Wei, Yang Yang. Visualization analysis of research hotspots and cutting-edge information in the field of intervertebral disc regeneration and repair [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2391-2402. |
| [2] | Wu Yanting, Li Yu, Liao Jinfeng. Magnesium oxide nanoparticles regulate osteogenesis- and angiogenesis-related gene expressions to promote bone defect healing [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(8): 1885-1895. |
| [3] | Jiang Xinghai, Song Yulin, Li Dejin, Shao Jianmin, Xu Junzhi, Liu Huakai, Wu Yingguo, Shen Yuehui, Feng Sicheng. Vascular endothelial growth factor 165 genes transfected into bone marrow mesenchymal stem cells to construct a vascularized amphiphilic peptide gel module [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(8): 1903-1911. |
| [4] | Han Teng, Ma Hong, Yang Ruoyi, Luo Yi, Li Chao. Oral squamous cell carcinoma-derived exosomal delivery of angiopoietin-2 is involved in tumor angiogenesis [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(7): 1755-1767. |
| [5] | Guo Jiachen, Gao Jun, Dai Wenhao, Liao Huayuan, Jiang You, Zhang Xi . Effect of compressive stress microenvironment on cytokines during fracture healing [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(4): 908-916. |
| [6] | Cao Wenqi, Feng Xiuzhi, Zhao Yi, Wang Zhimin, Chen Yiran, Yang Xiao, Ren Yanling. Effect of macrophage polarization on osteogenesis-angiogenesis coupling in type 2 diabetic osteoporosis [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(4): 917-925. |
| [7] | Yang Xiao, Bai Yuehui, Zhao Tiantian, Wang Donghao, Zhao Chen, Yuan Shuo. Cartilage degeneration in temporomandibular joint osteoarthritis: mechanisms and regenerative challenges [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(4): 926-935. |
| [8] | Wang Zhengye, Liu Wanlin, Zhao Zhenqun. Mechanism by which vascular endothelial growth factor A targets regulation of angiogenesis in the treatment of steroid-induced osteonecrosis of the femoral head [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(3): 671-679. |
| [9] | Yang Hu, Zheng Yu, Jia Chengming, Wang Tong, Zhang Guangfei, Ji Yaoyao. Immune microenvironment regulates bone regeneration [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(3): 701-710. |
| [10] | You Chenyang, Jiang Chao, Che Yanjun. Synergistic imbalance in lumbar core muscles and novel targeted interventions for intervertebral disc degeneration [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(28): 7323-7331. |
| [11] | Yang Ning, Han Zekui, Wang Xinyu, Huang Yiping, Han Jiaqi, Wang Yu, Duan Feng. Differences in angiogenesis and osteogenic effects between autogenous bone and mixed bone in guided bone regeneration [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(24): 6207-6213. |
| [12] | Li Huaying, Li Hao, Peng Wuxun, Dong Wentao. Mechanism of cuproptosis in the diagnosis and treatment of orthopedic-related diseases [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(24): 6275-6281. |
| [13] | Kan Weiyi, Wang Linrong, Cheng Leping. The interaction and balance between cellular senescence and tissue repair [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(24): 6297-6305. |
| [14] | Zhong Haotian, Li Jianwen, Han Weichao, Li Songbo. Traditional Chinese Medicine compound formula and effective ingredients for treating intervertebral disc degeneration: a multi-targeted and holistic regulation concept [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(24): 6316-6327. |
| [15] | Wang Wei, Chen Jun, Jia Shaohui, Xue Xinxuan, Dong Kunwei. Mechanisms by which exercise regulates gut microbiota in the prevention and treatment of non-alcoholic fatty liver disease [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(24): 6328-6336. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||

