Chinese Journal of Tissue Engineering Research ›› 2026, Vol. 30 ›› Issue (24): 6275-6281.doi: 10.12307/2026.226
Previous Articles Next Articles
Mechanism of cuproptosis in the diagnosis and treatment of orthopedic-related diseases
Li Huaying1, Li Hao1, Peng Wuxun1, 2, Dong Wentao1, 2
- 1Guizhou Medical University, Guiyang 550004, Guizhou Province, China; 2Department of Emergency Orthopedics, Affiliated Hospital of Guizhou Medical University, Guiyang 550004, Guizhou Province, China
-
Received:2025-06-27Revised:2025-10-18Online:2026-08-28Published:2026-02-03 -
Contact:Dong Wentao, Associate professor, Master’s supervisor, Guizhou Medical University, Guiyang 550004, Guizhou Province, China; Department of Emergency Orthopedics, Affiliated Hospital of Guizhou Medical University, Guiyang 550004, Guizhou Province, China -
About author:Li Huaying, MS candidate, Guizhou Medical University, Guiyang 550004, Guizhou Province, China -
Supported by:National Natural Science Foundation of China, No. 82260429 (to PWX); Joint Fund of Guizhou Provincial Science and Technology Department, No. Qiankehe Foundation-ZK[2023] General 345 (to DWT)
CLC Number:
Cite this article
Li Huaying, Li Hao, Peng Wuxun, Dong Wentao. Mechanism of cuproptosis in the diagnosis and treatment of orthopedic-related diseases[J]. Chinese Journal of Tissue Engineering Research, 2026, 30(24): 6275-6281.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
2.1 铜死亡在骨科相关疾病中研究进展的关键时间点、发现及研究意义 见表1。 2.2 骨与关节中的铜稳态 在骨组织中,铜对于调节骨稳态至关重要。铜离子对骨细胞的作用具有时间依赖性和浓度依赖性,不同浓度铜离子对骨细胞的增殖、分化和矿化等的影响存在显著差异。骨与关节中铜稳态的维持对于促进骨骼发育并维持骨骼和软骨稳态至关重要[6],该部分内容旨在探讨铜离子对骨与关节组织内各种细胞成分的调节作用。 2.2.1 软骨细胞 研究表明,在生理情况下,软骨细胞中的铜离子高于其他组织[7],突出了铜离子在软骨细胞代谢中的重要作用。研究表明,铜离子能够在一定浓度范围内促进软骨细胞的增殖和分化,增强软骨基质的合成[8];通过上调软骨细胞特异性基因的表达(如SRY框"
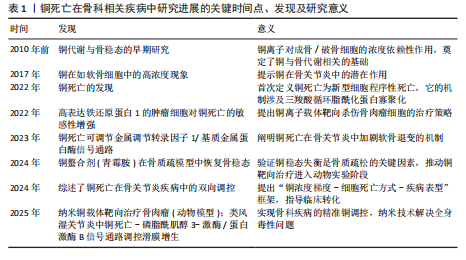
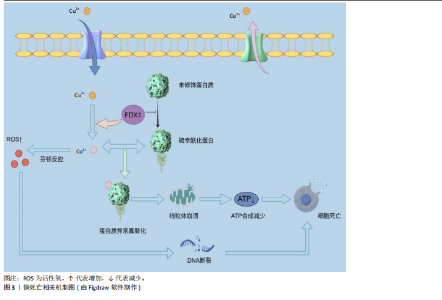
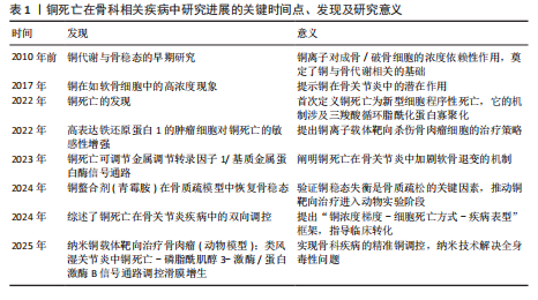
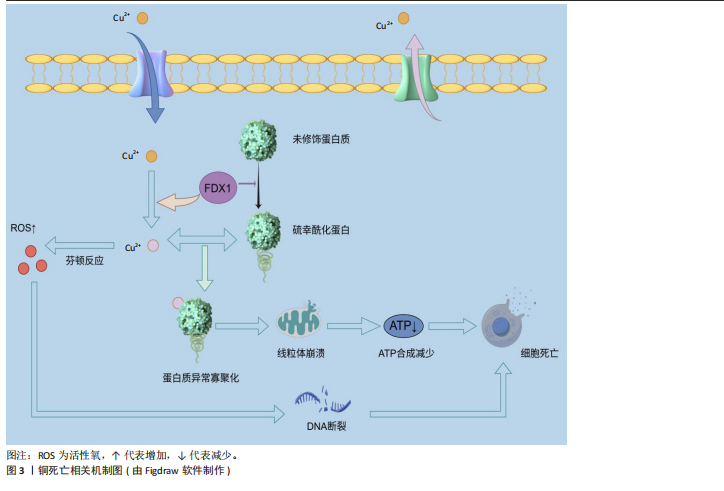
转录因子、聚集蛋白聚糖和Ⅱ型胶原蛋白)促进软骨细胞的成熟。铜离子还可以促进软骨形成调节蛋白(包括胰岛素样生长因子1、胰岛素样生长因子结合蛋白3和碱性磷酸酶)的分泌来促进软骨细胞增殖和软骨修复。最佳浓度铜离子可增强骨髓来源的间充质干细胞向软骨细胞的分化[9],通过增强赖氨酸氧化酶活性和胶原蛋白交联酶活性来促进软骨内的胶原蛋白交联,从而维持关节软骨生物力学特性和软骨强度。生理浓度的铜离子还抵消了与骨分解代谢相关标志物的上调,这对于维持软骨完整性至关重要。基于铜离子对软骨细胞的正面影响,凸显了它在治疗骨关节炎方面的巨大潜力。 2.2.2 成骨细胞 从成骨的角度看,铜离子通过上调骨相关基因(如碱性磷酸酶和骨桥蛋白)及下游基因表达有助于骨矿化[10]。不同浓度铜离子对成骨细胞矿化功能的影响不同,低浓度铜离子可以促进成骨细胞的矿化功能,而高浓度铜离子可能抑制成骨细胞的矿化功能,导致细胞毒性[5]。铜离子在一定浓度范围内可促进成骨细胞的增殖与分化、诱导血管内皮生长因子生成,血管内皮生长因子增加内皮细胞中骨形态发生蛋白2的表达,促进成骨的分化与矿化。研究表明,最佳浓度铜离子可上调Wnt/β-catain信号通路的关键成分(如轴抑制蛋白2、糖原合成激酶3等)来增强成骨生物活性,刺激成骨细胞的增殖与活性,这在增强骨形成方面起关键作用[11]。铜离子可通过干预成骨分化过程促进成骨分化。在成骨分化的过程中,骨髓间充质干细胞倾向于进行有氧糖酵解并将葡萄糖代谢为乳酸,有氧糖酵解中重要的调节因子是缺氧诱导因子1α-葡萄糖转运蛋白1型信号通路,而敲低缺氧诱导因子1α可抑制成骨分化[11]。研究表明,铜离子作为糖酵解代谢必须的微量元素,可通过激活缺氧诱导因子1α-葡萄糖转运蛋白1型信号通路刺激糖酵解,促骨髓间充质干细胞向成骨细胞分化[12]。 2.2.3 破骨细胞 铜离子对破骨细胞的作用具有双向性,可促进破骨细胞的分化与骨吸收活性,也能在特定条件下抑制破骨细胞功能,具体作用取决于铜离子的浓度、微环境等因素[13]。局部低活性氧是破骨细胞分化的必要条件[14],低浓度铜离子(1-10 μmol/L)通过活性氧/活化T细胞核因子胞质1轴增强破骨细胞分化和活化,促进骨吸收。高浓度铜离子(> 50 μmol/L)可通过诱导铜死亡促使破骨细胞凋亡,减少破骨细胞细胞数量。铜作为酶辅助因子,可通过影响酶的活性调节破骨细胞的活性和吸收,也可通过影响炎症因子影响破骨细胞。例如,白细胞介素6具有明显促进破骨细胞分化的功能,铜改性钴铬颗粒能够下调炎症因子肿瘤坏死因子α、白细胞介素6表达降低核因子κB受体配体激活剂和破骨细胞相关特异性转录标志基因的表达[15],从而抑制破骨细胞的分化。因此,靶向铜死亡有望成为治疗骨质疏松的新治疗策略。 2.2.4 滑膜细胞 在滑膜细胞中,铜稳态的维持对于滑膜细胞的代谢至关重要。铜作为多种酶的辅因子,参与细胞代谢过程,如线粒体呼吸链中的细胞色素需要铜的参与将能量从细胞分子中释放出来,为滑膜细胞提供动力。铜离子具有抗菌活性,能够增强巨噬细胞的吞噬能力,提高机体的抗感染能力[16],有助于滑膜细胞在炎症环境中的生存和修复。除此之外,铜离子还参与抗氧化防御机制,如超氧化物歧化酶活性就依赖于铜离子的存在,可帮助清除体内的自由基[17],从而保护滑膜细胞免受氧化应激的损害。 2.3 铜死亡 铜死亡是由细胞内铜离子过量所致的细胞死亡模式,该死亡机制复杂多样,与三羧酸循环与氧化应激密切相关。三羧酸循环是糖、脂肪以及氨基酸代谢的枢纽,是细胞代谢的重要环节,因此,细胞内的铜稳态对于维持细胞正常功能至关重要。铜离子的摄入增多和排出减少都会导致细胞内铜离子过量,过量的铜离子与三羧酸循环中的硫幸酰化蛋白质相结合并诱导其寡聚化[18],导致蛋白毒性应激,最终导致细胞死亡(图3)。研究表明,铁氧还蛋白1是介导铜死亡的关键因子,它不仅可以将一价铜还原为更具有毒性的二价铜,还是蛋白硫幸酰化的上游调节因子。蛋白硫幸酰化是一种赖氨酸翻译后修饰,目前已知的蛋白质硫幸酰化仅发生在4种酶上,分别是二氢硫辛酰胺支链转酰酶E2、甘氨酸裂解系统蛋白H、二氢硫辛酰胺S-琥珀酰转移酶以及二氢硫辛酰胺S-乙酰转移酶,这4种酶都是三羧酸循环中丙酮酸脱氢酶复合体的重要组成部分。铁氧还蛋白1促进蛋白质硫幸酰化,铜离子结合硫幸酰化蛋白质并增强其寡聚化,从而使线粒体膜电位崩溃以及ATP生成减少,诱导细胞膜破裂、细胞死亡。氧化应激是指细胞或生物体内氧化物质过度产生或是消除能力减弱导致体内氧化和抗氧化作用失衡的一种状态,倾向于氧化。铜离子可通过芬顿反应增加活性氧的产生,并激活与氧化应激相关的信号通路,损伤DNA,干扰线粒体功能以及破坏细胞膜完整性,从而达到杀伤细胞的目的。 研究表明,尽管铜死亡与铁死亡的模式不相同,但是两者之间有一定相关性,两者均通过活性氧积累并涉及线粒体通透性转换孔的激活从而触发细胞损伤[19]。“铁死亡”这一概念是2012年提出的,是一种铁依赖性的、脂质过氧化驱动的程序性细胞死亡方式[20]。研究表明,双硫仑/铜复合物可加速游离铁积累和脂质过氧化来促进铁死亡[21],过量的铜离子可通过谷胱甘肽/GPH4/TAX1BP1轴导致脂质过氧化,增强细胞对铁死亡的敏感性。 2.4 铜死亡在骨科相关疾病中的作用及其机制 骨科相关疾病(骨关节炎、骨质疏松、类风湿关节炎和骨肉瘤)的病理过程复杂多样,并不是由单一的细胞功能障碍所致,而是多种细胞的相互作用的结果。研究表明,铜死亡与以上疾病相关联,铜死亡通过多种机制影响骨细胞并使其发生功能障碍,最终导致疾病的发生与发展(图4)。因此,了解铜死亡对骨细胞的作用及机制对于骨关节炎、骨质疏松等骨科相关疾病的治疗至关重要。 2.4.1 骨关节炎 骨关节炎是一种以关节软骨退化、损伤和骨质增生为主要特征的退行性关节疾病,多见于老年人[22-23]。骨关节炎的发病机制较为复杂,涉及多种因素相互作用,如遗传因素、炎症反应及软骨细胞代谢紊乱等[24-26]。骨关节炎的主要表现为疼痛、僵硬和关节畸形,临床治疗方法包括早期的疼痛缓解和晚期关节置换,尽管这些治疗方法可在一定程度上缓解骨关节炎,但仍然存在局限性。因此,了解铜死亡对骨关节炎的作用机制对后续治疗至关重要。 铜死亡通过多种机制干扰软骨细胞的正常代谢,导致软骨基质降解和软骨细胞死亡,多种机制相互关联、共同作用,最终导致软骨的损伤和退化。研究表明,骨关节炎患者血清中铜水平高于健康人[27],说明软骨损伤与高水平铜含量相关。金属调节转录因子1是骨关节炎的生物标志物,在铜死亡时,金属调节转录因子1的功能紊乱会加剧氧化应激,进而激活核因子κB,间接调控基质金属蛋白酶和血小板反应蛋白解整合素金属肽酶5的表达,从而促进细胞外基质降解和分解代谢。正常情况下,当细胞内铜离子过量时,金属调节转录因子1可结合过量的铜离子形成稳定的复合物,减少细胞内游离的铜离子,减轻细胞毒性,防止铜死亡;而当铜死亡发生时,过量的铜离子会诱导金属调节转录因子1的表达来抵御细胞毒性,金属调节转录因子1的激活会导致基质金属蛋白酶(如基质金属蛋白酶1、基质金属蛋白酶3、基质金属蛋白酶13)转录"

和激活,这些酶可降解软骨基质中胶原蛋白和蛋白多糖,最终导致软骨退变和关节损伤。铜死亡导致软骨损伤还与三羧酸循环相关,三羧酸循环不仅是细胞有氧呼吸过程中的关键环节,也是多种细胞代谢途径的交汇点,对于维持细胞的正常生理功能至关重要。铜死亡时,过量的铜离子直接与三羧酸循环中硫辛酰化蛋白乙酰转移酶和二氢硫幸酸琥珀酰基转移酶结合并诱导其寡聚化,在此过程中还会抑制铁硫簇蛋白的合成,影响线粒体电子传递链功能,进而影响细胞线粒体能量代谢,诱导蛋白毒性应激,最终导致软骨细胞死亡[4]。 除此之外,谷氨酰胺酶是谷氨酰胺代谢的关键酶,对于维持软骨细胞的和合成代谢和分解代谢至关重要。研究表明,在骨关节炎软骨细胞中谷氨酰胺的表达通常是下降的,在铜死亡过程中谷氨酰胺酶的表达受到抑制,谷氨酰胺代谢产物(如a酮戊二酸和谷胱甘肽)减少,导致软骨细胞合成代谢和分解代谢失衡以及抗氧化能力下降[28]。铜死亡过程会通过芬顿反应产生大量的活性氧导致氧化应激,损伤软骨细胞,同时,铜死亡诱导的氧化应激抑制谷胱甘肽还原酶和合成酶来加速谷胱甘肽的消耗并减少其合成,从而降低细胞内谷胱甘肽含量,影响软骨细胞抗氧化能力。总之,铜死亡通过多种机制促进软骨细胞损伤,最终导致骨关节炎的发生发展。 在骨关节炎的病理过程中,铜稳态失衡导致的软骨细胞死亡是关键环节,通过靶向调控这一过程为骨关节炎的治疗提供新的方向,例如,特异性铜螯合剂可有效降低滑液中异常升高的铜离子浓度,抑制金属调节转录因子1的的过度激活,从而减轻基质金属蛋白酶的表达,保护软骨细胞外基质免受降解;除此之外,还可在分子层面进行干预,通过靶向三羧酸循环中的酯酰化蛋白可以阻断铜离子诱导的蛋白毒性应激,使用铁氧还蛋白1抑制剂或是敲除铁氧还蛋白1可减轻软骨细胞线粒体功能障碍,维持细胞代谢稳态;针对氧化应激环节,开发铜死亡特异性抗氧化剂可有效与铜死亡过程中产生的活性氧中和,保护软骨细胞,延缓骨关节炎的发展。 2.4.2 骨质疏松 骨质疏松是一种以骨密度降低和骨微结构破坏为主要特征的代谢性骨病,与年龄相关,主要发生于老年人,尤其是绝经后的女性患者[29]。骨质疏松会导致骨骼脆性增加,使骨骼受到轻微外力时发生骨折[30-31],骨折部位常发生于髋部、脊椎、腕部及肩部[32]。骨质疏松早期临床表现不明显,被称为“沉默的疾病”,晚期可变现为疼痛、乏力和活动受限等,常见治疗方法包括抑制破骨细胞活性和诱导骨形成,药物治疗包括钙剂补充、维生素D、降钙素等[33-34],尽管这些药物可有效治疗骨质疏松,但仍存在局限性。铜离子作为人体内必须的微量元素与骨质疏松的发生相关[35],研究表明骨质疏松女性患者的血清铜低于健康人[36],铜的摄入量与骨密度呈正相关,与骨质疏松风险呈负相关[37]。 铜离子诱导的细胞死亡取决于细胞内铜的积累,会诱导一种独特的细胞死亡方式,骨质疏松的发生是由于骨髓微环境变化和成骨细胞与破骨细胞之间的稳态失衡[38-39],而铜死亡的相关代谢机制与这些细胞有关。例如,谷氨酰胺在成骨细胞能量代谢中不仅作为重要的代谢燃料,还通过多种机制支持细胞的增殖、分化和抗氧化能力,对骨骼的发育和维持至关重要[40-41],谷氨酰胺与铜死亡相关,在铜死亡过程中,谷氨酰胺酶活性受到抑制导致谷氨酰胺浓度降低,因此,成骨细胞能量代谢受到影响;此外,铜死亡诱导的氧化应激也在骨质疏松中起重要作用,氧化应激会抑制成骨细胞的增殖、分化和矿化能力,最终导致骨形成减少,高水平的活性氧可阻断成骨细胞分化过程,减少骨基质的合成。氧化应激除了影响成骨细胞之外,还可促进破骨细胞的分化和活性,活性氧通过激活核因子kB等信号通路促进破骨细胞生成,破坏骨吸收与骨形成的平衡,从而加剧骨质疏松的发展[42]。 骨质疏松的发生与铜稳态失衡密切相关,通过靶向铜死亡通路为骨质疏松的治疗提供新的思路。研究表明,铜螯合剂(例如青霉胺、四硫钼酸盐)可选择性清除病理状态下过量的铜离子,从而减轻成骨细胞的铜死亡,恢复成骨细胞的分化与矿化功能。同时,通过调控关键分子铁氧还蛋白1和金属调节转录因子1的表达改善线粒体功能、抑制氧化应激,从而保护成骨细胞并抑制破骨细胞过度活化。除铜螯合剂之外,铜离子载体(如伊利司莫)的精准投递系统也是一种潜在策略,通过纳米技术将铜离子运输至骨组织微环境,可在局部形成高浓度铜区域,从而诱导破骨细胞铜死亡,同时还能避免全身的铜毒性。 2.4.3 类风湿关节炎 类风湿性关节炎是一种慢性系统性自身免疫性疾病,主要累及关节,表现为关节滑膜的慢性炎症、增生和关节软骨及软骨的破坏以及血管翳形成[43-44],临床表现为关节僵硬、疼痛和畸形。类风湿关节炎的发病机制复杂多样,涉及遗传、环境、免疫系统异常激活及炎症相关因子的释放[45-47]。目前类风湿关节炎的治疗主要包括药物治疗、非药物治疗以及调整生活方式来缓解疾病的进展[48],但是,由于类风湿关节炎发病机制的复杂多样性,在治疗效果上仍然具有局限性,因此,阐明类风湿关节炎新的发病机制与治疗靶点,对类风湿关节炎的临床疗效有至关重要的意义。近年来的研究发现,铜死亡在类风湿关节炎的发病机制中起着至关重要的作用。 类风湿关节炎患者的血清和滑膜中铜离子水平明显升高[49],说明铜稳态失衡与类风湿关节炎的发病机制相关。成纤维样滑膜细胞是关节滑膜内主要细胞类型之一,正常情况下它分泌滑液并合成细胞外基质以维持关节稳态,参与组织修复和营养交换。类风湿关节炎患者的滑膜中铜离子浓度升高[49],过量的铜离子与三羧酸循环中脂酰化成分结合并影响线粒体功能,诱导蛋白质异常寡聚化,最终诱导成纤维样滑膜细胞死亡,最终导致疾病的发生;同时,过量铜离子会通过芬顿反应产生大量的活性氧导致氧化应激[50],导致滑膜细胞和关节组织的氧化损伤,活性氧通过激活核因子kB和丝裂原活化蛋白激酶等促炎信号通路促进促炎因子和趋化因子的释放,慢性氧化应激与炎症形成恶性循环,加速关节的破坏。在类风湿关节炎中,成纤维样滑膜细胞的异常活化是驱动滑膜炎症和关节破坏的核心因素[51],铜离子通过激活磷脂酰肌醇3-激酶/蛋白激酶B/丝裂原活化蛋白激酶通路促进成纤维样滑膜细胞的增殖、迁移和侵袭能力,同时上调成纤维样滑膜细胞中基质金属蛋白酶并增强其活性,加速细胞外基质和软骨的降解。铜作为血管生成的辅助因子,促进滑膜组织血管内皮生长因子的表达、增强血管的通透性和新生血管形成,异常活化的成纤维样滑膜细胞与新生血管形成血管翳并侵入软骨和骨组织,导致关节畸形和功能丧失。 类风湿关节炎患者滑膜组织中的铜离子浓度异常升高,通过靶向调控铜死亡通路为类风湿关节炎的治疗提供了新思路。研究表明,铜螯合剂(如青霉胺和曲恩汀)可选择性清除滑膜局部过量的铜离子,减轻氧化应激,从而减轻炎症反应;还能抑制异常激活的磷脂酰肌醇3-激酶/蛋白激酶B/丝裂原活化蛋白激酶信号通路,从而降低成纤维样滑膜细胞的增殖和侵袭能力,延缓类风湿关节炎的发生发展[52]。 2.4.4 骨肉瘤 骨肉瘤是最常见的原发性恶性骨肿瘤,以肿瘤细胞直接产生类骨质为特征,多发生于青少年和儿童[53],临床症状主要表现为疼痛、肿胀和病理性骨折。骨肉瘤的发病机制复杂多样,涉及遗传学、肿瘤微环境及信号通路失调等多种机制,目前的治疗方法包括手术治疗、放疗、化疗、靶向治疗及免疫治疗[54],尽管目前治疗方案已取得了显著疗效,但在某些方面仍然具有局限性,如放疗虽可缓解疼痛和病理性骨折,但长期放疗可导致放疗区域继发骨肉瘤。铜离子载体(如双硫仑联合铜)可诱导铜死亡,对骨肉瘤细胞具有杀伤作用,尤其是针对传统疗法耐药和转移性病例。 铜稳态与肿瘤细胞的增殖、转移和血管生成密切相关,不同浓度铜离子对肿瘤细胞的影响不同。低浓度(0.1-10 μmol/L)铜离子通过激活丝裂原活化蛋白激酶/细胞外信号调节蛋白激酶信号通路增强细胞周期蛋白的表达,从而促进骨肉瘤U2OS细胞的增殖,还可促进内皮细胞的迁移。中等浓度的铜离子(10-50 μmol/L)具有双重作用,既可通过芬顿反应产生大量活性氧,损伤DNA并导致细胞周期停滞,也可通过激活腺苷酸活化蛋白激酶/哺乳动物雷帕霉素靶蛋白通路诱导保护性自噬。高浓度(> 50 μmol/L)铜离子诱导铜死亡,过量的铜离子与铁氧还蛋白1结合后诱导线粒体三羧酸循环中脂酰化蛋白异常寡聚化:一方面,导致蛋白毒性应激,最终诱导肿瘤细胞的凋亡;另一方面,导致线粒体功能障碍、ATP产生减少,肿瘤细胞能量供应不足,从而诱导肿瘤细胞的死亡[55]。铁氧还蛋白1是铜离子载体诱导细胞死亡的关键调节分子,骨肉瘤患者细胞中铁氧还蛋白1高表达,通过促进肿瘤细胞迁移而加剧骨肉瘤的恶行肿瘤,而这种高表达铁氧还蛋白1的肿瘤细胞对铜死亡尤其敏感[4]。铜离子作为金属离子本身具有毒性,需要肿瘤靶向铜运输系统来避免铜毒性。铜离子载体伊利司莫通过将铜离子特异性运送至线粒体选择性杀伤高表达铁氧还蛋白1的肿瘤细胞,从而达到治疗骨肉瘤的效果。"

| [1] JIANG F, LU C, ZENG Z, et al. Global burden of disease for musculoskeletal disorders in all age groups, from 2024 to 2050, and a bibliometric-based survey of the status of research in geriatrics, geriatric orthopedics, and geriatric orthopedic diseases. J Orthop Surg Res. 2025; 20(1):179. [2] KOLASINSKI SL, NEOGI T, HOCHBERG MC, et al. 2019 American College of Rheumatology/Arthritis Foundation Guideline for the Management of Osteoarthritis of the Hand, Hip, and Knee. Arthritis Care Res (Hoboken). 2020;72(2):149-162. [3] LEBOFF MS, GREENSPAN SL, INSOGNA KL, et al. The clinician’s guide to prevention and treatment of osteoporosis. Osteoporos Int. 2022;33(10):2049-2102. [4] TSVETKOV P, COY S, PETROVA B, et al. Copper induces cell death by targeting lipoylated TCA cycle proteins. Science. 2022;375(6586):1254-1261. [5] ZHANG Z, TANG H, DU T, et al. The impact of copper on bone metabolism. J Orthop Translat. 2024;47:125-131. [6] HAN J, LUO J, WANG C, et al. Roles and mechanisms of copper homeostasis and cuproptosis in osteoarticular diseases. Biomed Pharmacother. 2024;174:116570. [7] ROCZNIAK W, BRODZIAK-DOPIERAŁA B, CIPORA E, et al. Factors that Affect the Content of Cadmium, Nickel, Copper and Zinc in Tissues of the Knee Joint. Biol Trace Elem Res. 2017; 178(2):201-209. [8] WANG Y, ZHANG W, YAO Q. Copper-based biomaterials for bone and cartilage tissue engineering. J Orthop Translat. 2021;29:60-71. [9] LU Y, CHEN J, LI L, et al. Hierarchical functional nanoparticles boost osteoarthritis therapy by utilizing joint-resident mesenchymal stem cells. J Nanobiotechnology. 2022;20(1):89. [10] TAN J, REN L, XIE K, et al. Functionalized TiCu/TiCuN coating promotes osteoporotic fracture healing by upregulating the Wnt/β-catenin pathway. Regen Biomater. 2023;10:rbac092. [11] TAN Z, ZHOU B, ZHENG J, et al. Lithium and Copper Induce the Osteogenesis-Angiogenesis Coupling of Bone Marrow Mesenchymal Stem Cells via Crosstalk between Canonical Wnt and HIF-1α Signaling Pathways. Stem Cells Int. 2021;2021:6662164. [12] ZHA K, TAN M, HU Y, et al. Regulation of metabolic microenvironment with a nanocomposite hydrogel for improved bone fracture healing. Bioact Mater. 2024;37:424-438. [13] BERNHARDT A, BACOVA J, GBURECK U, et al. Influence of Cu(2+) on Osteoclast Formation and Activity In Vitro. Int J Mol Sci. 2021;22(5):2451. [14] AGIDIGBI TS, KIM C. Reactive Oxygen Species in Osteoclast Differentiation and Possible Pharmaceutical Targets of ROS-Mediated Osteoclast Diseases. Int J Mol Sci. 2019;20(14):3576. [15] LU Y, XU X, YANG C, et al. Copper modified cobalt-chromium particles for attenuating wear particle induced-inflammation and osteoclastogenesis. Biomater Adv. 2023;147: 213315. [16] LIANG DY, LIANG PC, YI QQ, et al. Copper coating formed by micro-arc oxidation on pure Mg improved antibacterial activity, osteogenesis, and angiogenesis in vivo and in vitro. Biomed Microdevices. 2021;23(3):39. [17] SKOPP A, BOYD SD, ULLRICH MS, et al. Copper-zinc superoxide dismutase (Sod1) activation terminates interaction between its copper chaperone (Ccs) and the cytosolic metal-binding domain of the copper importer Ctr1. Biometals. 2019;32(4):695-705. [18] TANG D, CHEN X, KROEMER G. Cuproptosis: a copper-triggered modality of mitochondrial cell death. Cell Res. 2022;32(5):417-418. [19] TANG D, CHEN X, KANG R, et al. Ferroptosis: molecular mechanisms and health implications . Cell Res. 2021;31(2):107-125. [20] HIRSCHHORN T, STOCKWELL BR. The development of the concept of ferroptosis. Free Radic Biol Med. 2019;133:130-143. [21] REN X, LI Y, ZHOU Y, et al. Overcoming the compensatory elevation of NRF2 renders hepatocellular carcinoma cells more vulnerable to disulfiram/copper-induced ferroptosis. Redox Biol. 2021;46:102122. [22] LOESER RF, GOLDRING SR, SCANZELLO CR, et al. Osteoarthritis: a disease of the joint as an organ. Arthritis Rheum. 2012;64(6):1697-1707. [23] GLYN-JONES S, PALMER AJ, AGRICOLA R, et al. Osteoarthritis. Lancet. 2015;386(9991): 376-387. [24] BLIDDAL H. [Definition, pathology and pathogenesis of osteoarthritis]. Ugeskr Laeger. 2020;182(42):V06200477. [25] WANG L, HE C. Nrf2-mediated anti-inflammatory polarization of macrophages as therapeutic targets for osteoarthritis. Front Immunol. 2022;13:967193. [26] LI T, PENG J, LI Q, et al. The Mechanism and Role of ADAMTS Protein Family in Osteoarthritis. Biomolecules. 2022;12(7):959. [27] YAZAR M, SARBAN S, KOCYIGIT A, et al. Synovial fluid and plasma selenium, copper, zinc, and iron concentrations in patients with rheumatoid arthritis and osteoarthritis. Biol Trace Elem Res. 2005;106(2):123-232. [28] LIU L, ZHANG W, LIU T, et al. The physiological metabolite α-ketoglutarate ameliorates osteoarthritis by regulating mitophagy and oxidative stress. Redox Biol. 2023;62:102663. [29] LIN J, ZHU J, WANG Y, et al. Chinese single herbs and active ingredients for postmenopausal osteoporosis: From preclinical evidence to action mechanism. Biosci Trends. 2017;11(5):496-506. [30] JOHNSTON CB, DAGAR M. Osteoporosis in Older Adults. Med Clin North Am. 2020;104(5): 873-884. [31] COMPSTON JE, MCCLUNG MR, LESLIE WD. Osteoporosis. Lancet. 2019;393(10169):364-376. [32] AUDE M, JEAN-JACQUES B, LAURA I, et al. Fracture distribution in postmenopausal women: a FRISBEE sub-study. Arch Osteoporos. 2022;18(1):3. [33] ARCEO-MENDOZA RM, CAMACHO PM. Postmenopausal Osteoporosis: Latest Guidelines. Endocrinol Metab Clin North Am. 2021;50(2):167-178. [34] BROWN C. Osteoporosis: Staying strong. Nature. 2017;550(7674):S15-S17. [35] CHEN J, JIANG Y, SHI H, et al. The molecular mechanisms of copper metabolism and its roles in human diseases. Pflugers Arch. 2020;472(10):1415-1429. [36] MUTLU M, ARGUN M, KILIC E, et al. Magnesium, zinc and copper status in osteoporotic, osteopenic and normal post-menopausal women. J Int Med Res. 2007; 35(5):692-695. [37] FAN Y, NI S, ZHANG H. Associations of Copper Intake with Bone Mineral Density and Osteoporosis in Adults: Data from the National Health and Nutrition Examination Survey. Biol Trace Elem Res. 2022;200(5):2062-2068. [38] KONDRIKOV D, ELMANSI A, BRAGG RT, et al. Kynurenine inhibits autophagy and promotes senescence in aged bone marrow mesenchymal stem cells through the aryl hydrocarbon receptor pathway. Exp Gerontol. 2020;130:110805. [39] KYLMAOJA E, NAKAMURA M, TUUKKANEN J. Osteoclasts and Remodeling Based Bone Formation. Curr Stem Cell Res Ther. 2016; 11(8):626-633. [40] YU Y, NEWMAN H, SHEN L, et al. Glutamine Metabolism Regulates Proliferation and Lineage Allocation in Skeletal Stem Cells. Cell Metab. 2019;29(4):966-78.e4. [41] DEVIGNES CS, CARMELIET G, STEGEN S. Amino acid metabolism in skeletal cells. Bone Rep. 2022;17:101620. [42] MANOLAGAS SC. From estrogen-centric to aging and oxidative stress: a revised perspective of the pathogenesis of osteoporosis. Endocr Rev. 2010;31(3):266-300. [43] FIRESTEIN GS, MCINNES IB. Immunopathogenesis of Rheumatoid Arthritis. Immunity. 2017;46(2):183-196. [44] SMOLEN JS, ALETAHA D, MCINNES IB. Rheumatoid arthritis. Lancet. 2016; 388(10055):2023-2038. [45] WU D, LUO Y, LI T, et al. Systemic complications of rheumatoid arthritis: Focus on pathogenesis and treatment. Front Immunol. 2022;13: 1051082. [46] MUELLER AL, PAYANDEH Z, MOHAMMADKHANI N, et al. Recent Advances in Understanding the Pathogenesis of Rheumatoid Arthritis: New Treatment Strategies. Cells. 2021;10(11):3017. [47] DEANE KD, DEMORUELLE MK, KELMENSON LB, et al. Genetic and environmental risk factors for rheumatoid arthritis. Best Pract Res Clin Rheumatol. 2017;31(1):3-18. [48] LIN YJ, ANZAGHE M, SCHÜLKE S. Update on the Pathomechanism, Diagnosis, and Treatment Options for Rheumatoid Arthritis. Cells. 2020; 9(4):880. [49] XIN L, YANG X, CAI G, et al. Serum Levels of Copper and Zinc in Patients with Rheumatoid Arthritis: a Meta-analysis. Biol Trace Elem Res. 2015;168(1):1-10. [50] KWOK ML, CHAN KM. Oxidative stress and apoptotic effects of copper and cadmium in the zebrafish liver cell line ZFL. Toxicol Rep. 2020;7:822-835. [51] BARTOK B, FIRESTEIN GS. Fibroblast-like synoviocytes: key effector cells in rheumatoid arthritis. Immunol Rev. 2010; 233(1):233-255. [52] KHAIRNAR SI, MAHAJAN UB, PATIL KR, et al. Disulfiram and Its Copper Chelate Attenuate Cisplatin-Induced Acute Nephrotoxicity in Rats Via Reduction of Oxidative Stress and Inflammation. Biol Trace Elem Res. 2020; 193(1):174-184. [53] MIRABELLO L, TROISI RJ, SAVAGE SA. Osteosarcoma incidence and survival rates from 1973 to 2004: data from the Surveillance, Epidemiology, and End Results Program. Cancer. 2009;115(7):1531-1543. [54] BELAYNEH R, FOURMAN MS, BHOGAL S, et al. Update on Osteosarcoma. Curr Oncol Rep. 2021;23(6):71. [55] YE L, YU C, XIA J, et al. Multifunctional nanomaterials via cell cuproptosis and oxidative stress for treating osteosarcoma and OS-induced bone destruction. Mater Today Bio. 2024;25:100996. |
| [1] | Yu Cenqi, Liu Yang, Yu Jiangfeng, Kang Kang, Deng Yaoge, Xia Xiaowei, Zhang Yijian, Zhu Xuesong. Biomimetic Black Phosphorus Nanosystem Regulates Synovial Macrophage Polarization for Osteoarthritis Treatment [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(在线): 1-13. |
| [2] | Liu Wenlong, Dong Lei, Xiao Zhengzheng, Nie Yu. Finite element analysis of tibial prosthesis loosening after fixed-bearing unicompartmental knee arthroplasty for osteoporosis [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2191-2198. |
| [3] | Chen Long, Wang Xiaozhen, Xi Jintao, Lu Qilin. Biomechanical performance of short-segment screw fixation combined with expandable polyetheretherketone vertebral body replacement in osteoporotic vertebrae [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2226-2235. |
| [4] | Zhang Nan, Meng Qinghua, Bao Chunyu. Characteristics and clinical application of ankle joint finite element models [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2343-2349. |
| [5] | Chen Huiting, Zeng Weiquan, Zhou Jianhong, Wang Jie, Zhuang Congying, Chen Peiyou, Liang Zeqian, Deng Weiming. Tail anchoring technique of vertebroplasty in treatment of osteoporotic vertebral compression fractures with intravertebral cleft: a finite element analysis [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2145-2152. |
| [6] | Zeng Xuan, Weng Rui, Ye Shicheng, Tang Jiadong, Mo Ling, Li Wenchao. Two lumbar rotary manipulation techniques in treating lumbar disc herniation: a finite element analysis of biomechanical differences [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2153-2161. |
| [7] | Cheng Qisheng, Julaiti·Maitirouzi, Xiao Yang, Zhang Chenwei, Paerhati·Rexiti. Finite element analysis of novel variable-diameter screws in modified cortical bone trajectory of lumbar vertebrae [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2162-2171. |
| [8] | Chen Qiuhan, Yang Long, Yuan Daizhu, Wu Zhanyu, Zou Zihao, Ye Chuan. Peri-knee osteotomy for treatment of knee osteoarthritis: optimization of treatment strategies [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2303-2312. |
| [9] | Zhang Zizheng, Luo Wang, Liu Changlu. Application value of finite element analysis on unicompartmental knee arthroplasty for medial knee compartmental osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2313-2322. |
| [10] |
Dong Chunyang, Zhou Tianen, Mo Mengxue, Lyu Wenquan, Gao Ming, Zhu Ruikai, Gao Zhiwei.
Action mechanism of metformin combined with Eomecon chionantha Hance dressing in treatment of deep second-degree burn wounds#br#
#br#
[J]. Chinese Journal of Tissue Engineering Research, 2026, 30(8): 2001-2013.
|
| [11] | Li Qingbin, Lin Jianhui, Huang Wenjie, Wang Mingshuang, Du Jiankai, Lao Yongqiang. Bone cement filling after enlarged curettage of giant cell tumor around the knee joint: a comparison of subchondral bone grafting and non-grafting [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(8): 1896-1902. |
| [12] | Yang Xuetao, Zhu Menghan, Zhang Chenxi, Sun Yimin, Ye Ling. Applications and limitations of antioxidant nanomaterials in oral cavity [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(8): 2044-2053. |
| [13] | Hu Xiongke, Liu Shaohua, Tan Qian, Liu Kun, Zhu Guanghui. Shikonin intervention with bone marrow mesenchymal stem cells improves microstructure of femur in aged mice [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(7): 1609-1615. |
| [14] | Liu Anting, Lu Jiangtao, Zhang Wenjie, He Ling, Tang Zongsheng, Chen Xiaoling. Regulation of AMP-activated protein kinase by platelet lysate inhibits cadmium-induced neuronal apoptosis [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(7): 1800-1807. |
| [15] | Li Hao, Tao Hongcheng, Zeng Ping, Liu Jinfu, Ding Qiang, Niu Chicheng, Huang Kai, Kang Hongyu. Mitogen-activated protein kinase signaling pathway regulates the development of osteoarthritis: guiding targeted therapy with traditional Chinese medicine [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(6): 1476-1485. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||