Chinese Journal of Tissue Engineering Research ›› 2026, Vol. 30 ›› Issue (28): 7428-7436.doi: 10.12307/2026.817
Previous Articles Next Articles
Oxidative stress and osteoporosis: a bibliometric analysis of literature from SCI core database
Guo Jun1, Lu Zheng1, Yu Jinling1, Hao Yuanyuan1, Liu Kaishun1, Liu Xuexia1, Huang Yourong2
- 1Department of Orthopedics, Wuzhou Traditional Chinese Medicine Hospital, Wuzhou 543000, Guangxi Zhuang Autonomous Region, China; 2Ruikang Hospital Affiliated to Guangxi University of Chinese Medicine, Nanning 530011, Guangxi Zhuang Autonomous Region, China
-
Received:2025-07-06Revised:2025-12-08Online:2026-10-08Published:2026-02-25 -
Contact:Huang Yourong, Chief physician, Professor, Ruikang Hospital Affiliated to Guangxi University of Chinese Medicine, Nanning 530011, Guangxi Zhuang Autonomous Region, China -
About author:Guo Jun, MS, Associate chief physician, Master’s supervisor, Department of Orthopedics, Wuzhou Traditional Chinese Medicine Hospital, Wuzhou 543000, Guangxi Zhuang Autonomous Region, China -
Supported by:Guangxi Natural Science Foundation (General Project), No. 2023GXNSFAA026075 (to HYR); Guangxi Zhuang Autonomous Region Huang Yourong Gui School of Traditional Chinese Medicine Master Training Project, No. [2022]6 (to HYR)
CLC Number:
Cite this article
Guo Jun, Lu Zheng, Yu Jinling, Hao Yuanyuan, Liu Kaishun, Liu Xuexia, Huang Yourong. Oxidative stress and osteoporosis: a bibliometric analysis of literature from SCI core database[J]. Chinese Journal of Tissue Engineering Research, 2026, 30(28): 7428-7436.
share this article
Add to citation manager EndNote|Reference Manager|ProCite|BibTeX|RefWorks
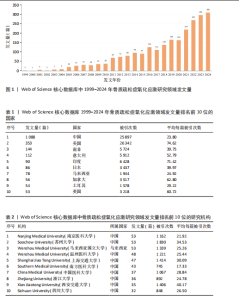
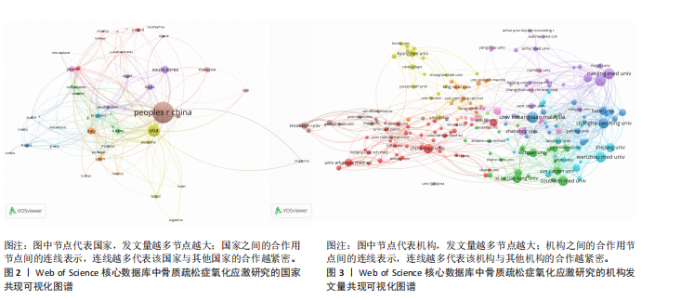
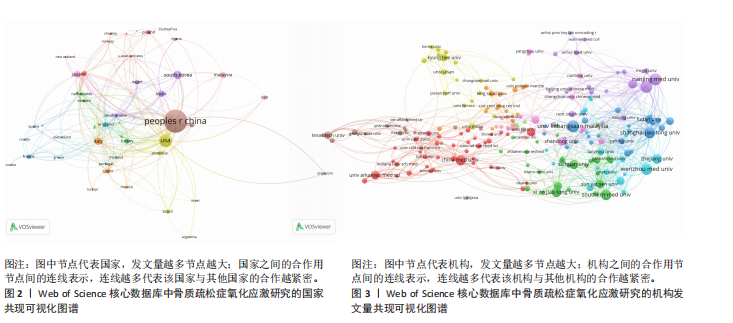
2.1 氧化应激与骨质疏松症领域发文量分析 最终共检索到文献2 558篇,按照纳入标准和排除标准,通过研究者的检索、筛选及裁定,最终纳入2 416篇文献。数据统计显示,1999-2024年,氧化应激与骨质疏松症领域研究发文量呈现出显著增长趋势,反映了该领域研究的逐步深入和研究热度的不断提升,发文量最少年份为2000年(1篇),最多为2024年(309篇),见图1。1999-2010年是研究的起步阶段,发文量较少,增长较为缓慢,例如1999年仅有2篇,2010年也仅增长到38篇。2011-2016年是快速增长阶段,发文量从2011年的69篇增长至2016年的126篇,首次突破百篇,显示出该领域的研究逐渐受到关注。2019-2024年发文量增长尤为显著,2020年后更是发生大幅跃升,至2024年达到309篇,这种快速增长可能与科研技术的进步、全球人口老龄化加剧、氧化应激在骨质疏松症中的重要作用被广泛认可以及政策支持和资金投入的增加密切相关。结合近年来的高增长态势,预计未来几年该领域的研究热度将持续上升,发文量有望继续增长,研究内容也将更加深入和多样化,例如针对分子机制、抗氧化剂治疗作用以及临床试验等方向的进一步探索。 2.2 氧化应激与骨质疏松症领域研究发文国家分析 1999-2024年骨质疏松症氧化应激研究领域发文量排名前10位的国家及其共现可视化图谱,见表1,图2。中国以1 088篇的发文量位列第一,显示出中国在该领域的主导地位,但平均每篇被引次数为23.80,在前10国家中排名靠后,表明中国的研究影响力仍有提升空间。美国以353篇发文量排名第二,但被引次数高达26 342次,平均每篇被引次数高达74.62,充分体现了美国研究质量的国际影响力。南非以144篇的发文量排名第三,平均每篇被引次数为39.75,表明南非具有一定的国际认可度。意大利和印度分别以112篇和90篇的发文量排名第四和第五,平均每篇被引次数分别为52.79和71.42,尤其是印度,尽管发文量较少,但研究质量较高。日本、马来西亚、加拿大、土耳其和英国分列第六至第十位,其中加拿大的平均每篇被引次数为62.80,仅次于美国和印度,显示出较高的研究质量。总体来看,美国在该领域的研究质量和影响力最为突出,而中国则以绝对的发文量占据主导地位,但研究成果的国际认可度有待进一步提高;同时,印度、加拿大和意大利等国在较高的平均每篇被引次数方面表现不俗,展示了高质量的研究贡献。 2.3 氧化应激与骨质疏松症领域发文机构分析 1999-2024年骨质疏松症氧化应激研究领域发文量前10位机构及其合作网络分析,见表2,图3。中国机构占据主导地位(9所),合作网络广度与强度显著提升了研究影响力,例如上海交通大学(合作数值28)和苏州大学(合作数值20)分别以1 414次和1 830次被引次数位居前列,并且西安交通大学(合作数值21)以平均每篇40.17次被引成为质量标杆,表明高合作度对成果传播的推动作用。部分机构如南京医科大学(合作数值5)和四川大学(合作数值7)虽合作较少,但平均被引次数达21.92和26.50,凸显独立研究的学术价值;而中国医科大学(合作数值7)以28.84次均被引进一步印证研究深度。唯一的非中国机构马来西亚国立"
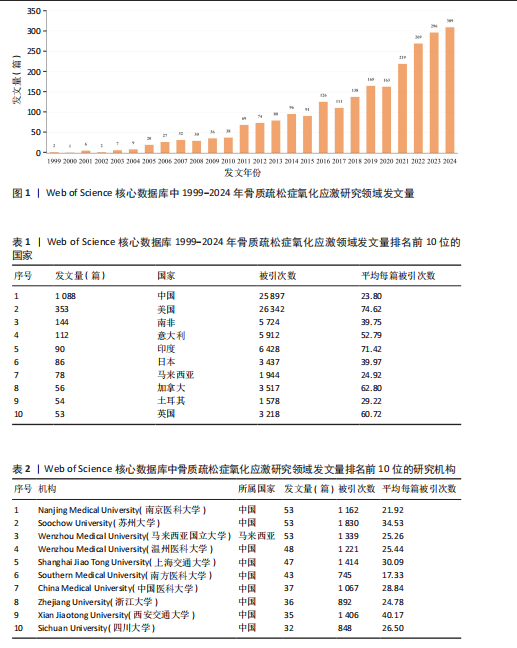
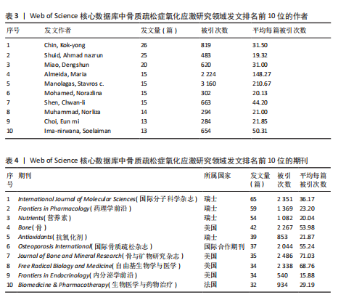
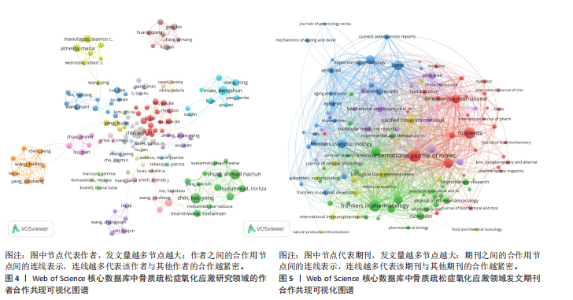
大学(合作数值2)尽管发文量与中国机构持平(53篇),但被引次数(1 339次)和合作水平较低,反映国际合作的局限性。此外,合作网络的实际效益存在差异:南方医科大学(合作数值17)虽合作广泛,但被引次数(745次)和均被引(17.33)偏低,提示合作可能侧重数量而非质量;浙江大学(合作数值16)的中等被引表现(24.78次均被引)表明合作方向需优化。总体来看,中国机构通过密集协同创新形成显著优势,但未来需加强国际协作、提升合作质量,并平衡独立研究深度与成果扩散效率,以进一步推动该领域的全球发展。 2.4 氧化应激与骨质疏松症领域发文作者和作者共被引分析 1999-2024年氧化应激与骨质疏松症领域发文量前10位的作者及其合作网络分析,见表3,图4。研究影响力两极分化,Almeida和Manolagas发文量虽同为15篇,但被引次数高、平均每篇被引次数远超其他作者,成果学术价值高,而发文量高的Chin和Shuid被引次数及平均被引次数较低,成果传播效率或创新性有限;合作网络与质量关联,Manolagas和Almeida同属紧密合作团队形成高质量成果,Ima-nirwana和Shen独立或小范围合作也能产出高影响力研究,跨团队作者Choi和Chin发文量高但被引表现不一,反映合作广度与深度平衡问题;国际作者主导,高被引国际学者Manolagas和Almeida影响力显著,发文量前10中仅少数兼顾数量与质量,多数中国学者发文量高但被引表现中等;合作模式多样,部分合作群组研究方向可能边缘,Manolagas-Almeida团队小规模紧密合作易成学术标杆,重复出现作者活跃于多个团队可能促进跨领域创新,但存在研究深度不足风险。总之,该领域学术影响力依赖少数核心作者突破性研究和高效合作,高发文量作者需平衡合作广度与深度,未来应加强国际团队协同,整合中国学者数量与国际团队质量优势,优化合作方向、提升成果原创性和传播效率。 2.5 氧化应激与骨质疏松症领域发文期刊分析 1999-2024年骨质疏松症氧化应激研究领域发文前10位的期刊及期刊合作共现可视化图谱,见表4,图5。瑞士期刊在发文量上占据主导地位,但美国期刊以更高的单篇影响力成为领域标杆。《Journal of Bone and Mineral Research》(美国)以35篇发文量获得2 486次被引,平均每篇被引71.03次,位列影响力榜首,凸显该期刊的学术权威性;《Free Radical Biology and Medicine》(美国)和《Bone》(美国)分别以68.76和53.98次均被引紧随其后,表明美国期刊在基础研究与临床转化中的核心地位。瑞士期刊如《International Journal of Molecular Sciences》(均被引36.17次)虽发文量最高(65篇),但影响力显著低于美国期刊,而《Nutrients》(均被引20.04次)则进一步反映瑞士期刊数量优势与质量不均衡的矛盾。国际合作期刊《Osteoporosis International》以37篇"
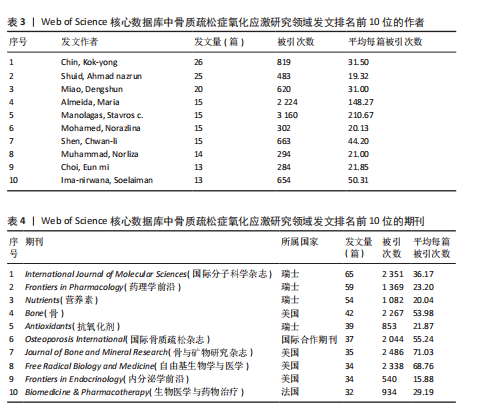

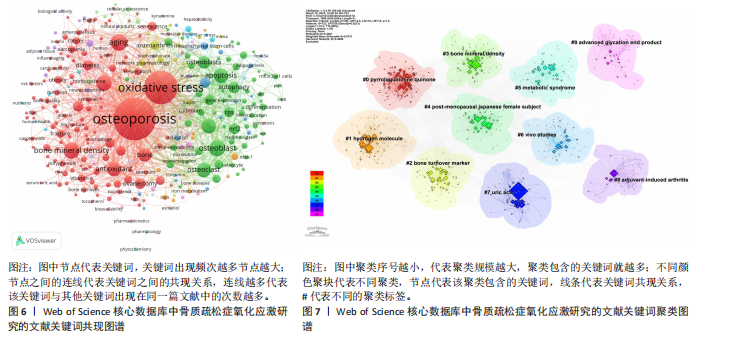
发文量获2 044次被引(均被引55.24次),表现亮眼,凸显跨国合作对成果传播的推动作用。此外,法国期刊《Biomedicine & Pharmacotherapy》(均被引29.19次)和中国未上榜的现象,暗示非英语国家期刊的国际影响力仍待提升。值得注意的是,高影响力期刊多聚焦于骨骼生物学(如《Bone》)和氧化应激机制(如《Free Radical Biology and Medicine》),而发文量高的瑞士期刊更偏向综合性分子科学(如《International Journal of Molecular Sciences》),研究方向的分化可能影响期刊的学术深度。未来需加强高质量研究向高影响力期刊的倾斜,同时推动国际合作期刊的多元化发展,平衡数量与质量,以提升该领域的全球协同创新能力。 2.6 氧化应激与骨质疏松症领域关键词分析 2.6.1 关键词共现分析 1999-2024年骨质疏松症氧化应激研究关键词频率分析及关键词共现图谱,见表5、图6。研究核心聚焦于“骨质疏松”(918次)与“氧化应激”(571次)的相互作用机制。关键词关联性显示,氧化应激通过“活性氧”和“炎症”加剧骨代谢失衡,具体表现为“成骨细胞”与“破骨细胞”动态平衡的破坏,进而影响“骨密度”(139次)。此外,“衰老”和“糖尿病”作为风险因素与氧化应激协同促进骨质疏松进展,而“自噬”和“Nrf2”则指向细胞防御机制对氧化损伤的调控作用。高频关键词中,“卵巢切除术”凸显雌激素缺乏模型的广泛应用,“抗氧化物”与“抗氧化剂”则反映干预策略的研究热点。值得注意的是,“成骨作用”和“细胞凋亡”等关键词进一步细化研究路径,表明该领域正从宏观机制向分子调控层面深入。总体来看,研究主题高度集中于氧化应激对骨代谢的病理影响及干预靶点,未来需加强跨学科整合(如代谢疾病关联)及新型抗氧化疗法的临床转化探索。 2.6.2 关键词聚类分析 针对骨质疏松症中氧化应激研究的文献关键词聚类分析,见表6、图7。氧化应激研究涉及骨代谢失衡、细胞衰老、炎症反应等多种生物学过程。动物模型,如去卵巢大鼠和小鼠/大鼠模型,被广泛用于模拟绝经后骨质疏松症和探索分子机制,同时研究还紧密关联人群与临床,特别是绝经后女性这一高风险群体及特定人群和代谢性疾病患者的骨质变化。在分子机制与治疗靶点方面,研究聚焦于核因子κB受体活化因子配体信号通路、成骨分化与细胞衰老以及晚期糖基化终产物等关键领域。此外,关键聚类亮点如代谢综合征、佐剂诱导性关节炎和晚期糖基化终产物等进一步拓展了研究的广度和深度。潜在交叉领域包括抗氧化剂干预策略、多疾病交互作用以及转化医学方向。然而,数据也存在一定的局限性,需要在未来的研究中加以解决。综上所述,骨质疏松症中氧化应激研究领域的研究集中在氧化应激对骨代谢的影响机制上,未来可重点关注抗氧化剂干预、多疾病交互作用及转化医学应用等领域。 2.6.3 关键词时间线分析 关键词时间线图谱展示了1999-2024年骨质疏松症与氧化应激领域研究的主题演变及热点发展,见图8。早期(1999-2010年)研究集中于骨质疏松症的基础"

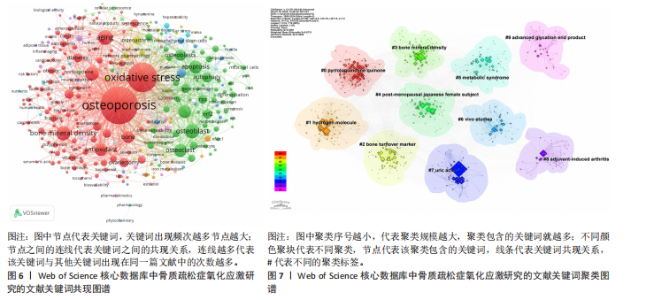
机制,如“氧化应激”“骨质流失”“骨代谢”等,重点探讨氧化应激在骨代谢失衡中的作用。“活性氧”及“氧化损伤”等关键词揭示了氧化应激对骨质流失的影响。2010年后,研究逐渐转向分子标志物领域,如“骨转换标志物”和“骨密度”,为骨质疏松症的早期诊断提供了新思路。同时“炎症”和“凋亡”的研究表明,炎症因子和细胞凋亡在骨质疏松症发病机制中具有重要作用。2015年之后,研究进一步拓展至特定人群及相关疾病领域,如“绝经后日本女性”等关键词突出特定人群的关注;而“代谢综合征”和“高脂饮食”等则反映出代谢性疾病与骨质疏松症的关联。此外,“高级糖化终产物”表明糖化应激与代谢紊乱对骨健康的影响受到了重视。近年来(2020-2024年),研究聚焦新兴治疗策略与干预手段,如“吡咯喹啉醌”和“氢分子”等新型抗氧化剂的潜力以及“活体研究”在验证骨质疏松症治疗中的作用。总体来看,1999-2024年的研究从基础机制到临床应用逐步深化,热点从氧化应激的基础研究扩展到特定人群、代谢性疾病及创新治疗方法。未来研究可能更关注精准医学及多"
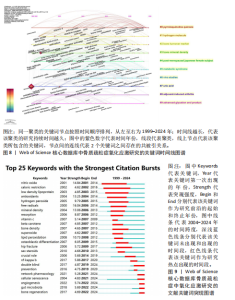
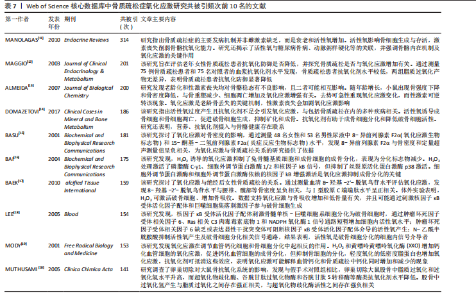
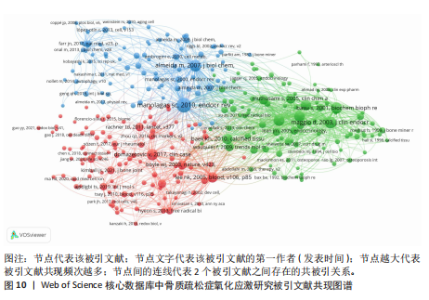
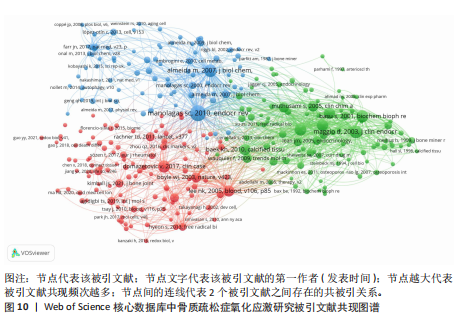
组学技术的应用,为骨质疏松症的防治提供更全面解决方案。 2.6.4 关键词突现分析 1999-2024年,骨质疏松症氧化应激领域的关键词突现图谱清晰展示了重要研究主题随时间的变化轨迹,见图9。早期(2000-2010年),研究聚焦于氧化应激及其相关分子的作用机制,“一氧化氮”“自由基”“过氧化氢”等氧化应激相关因子引文突现显著,凸显了氧化应激在骨质疏松症中的关键作用;同时“抗氧化剂”“维生素C”等关键词的突现,反映了对抗氧化治疗方法的初步关注。2006年后,研究转向骨代谢与骨质变化的定量评估,“骨密度”“矿物密度”“骨吸收”等关键词突现,并且对“类胡萝卜素”“脂质过氧化”等分子机制的深入研究,进一步揭示了代谢与氧化应激在骨质疏松症中的复杂交织。2010年之后,研究热点扩展至细胞与分子水平的调控机制,“性类固醇”“成骨细胞分化”“核因子kB”等关键词的突现,表明研究开始关注炎症信号通路、激素调控及骨形成过程,同时“髋部骨折”“预防”等主题的出现,体现了对骨折风险和预防策略的重视。近年(2020-2024年),研究热点进一步聚焦新兴领域,“网络药理学”“细胞衰老”“肠道菌群”“骨再生”等关键词的突现,标志着精准医学、多组学技术以及微生态干预正成为研究前沿,积极探索骨质疏松症的创新治疗策略。总体来看,骨质疏松症氧化应激研究从基础机制逐步深入到分子标志物、临床应用及创新治疗方法,展现了该领域研究的多维度拓展与动态发展态势。 2.7 氧化应激与骨质疏松症领域文献共被引分析 1999-2024年骨质疏松症中氧化应激研究共被引频次前10位的文献及其共现图谱,见表7、图10。氧化应激为骨质疏松发病的重要机制,它通过双重调控成骨与破骨细胞动态平衡直接影响骨代谢。MANOLAGAS等[11]的研究表明,骨质疏松的主因并非传统认知的雌激素缺乏,"
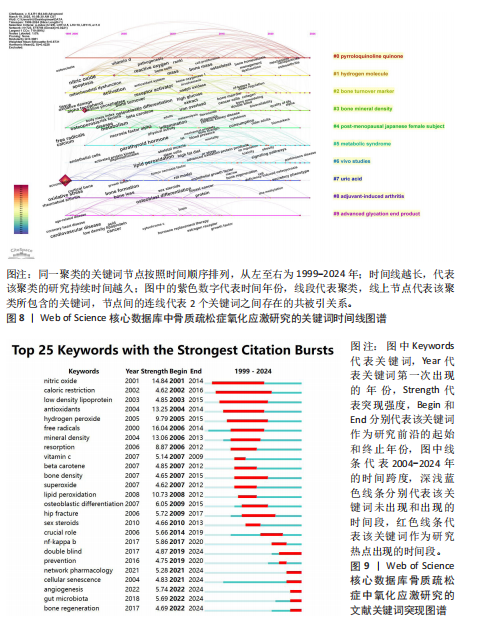

而是衰老与活性氧累积的协同效应,活性氧通过抑制成骨细胞分化、激活破骨细胞及诱导骨细胞凋亡,导致骨密度下降[16,18]。此外,绝经后性激素丧失与衰老共同加剧氧化应激[13]。 研究还揭示氧化应激的复杂性,它在血管钙化中促进成骨分化,却抑制骨细胞功能,提示病理机制的多样性[19]。在临床转化方面,尿液8-异前列腺素F2α等生物标志物为评估氧化应激与骨密度关联提供了工具,而患者血浆抗氧化剂水平降低则支持营养干预的潜力[13,15]。 未来需深入解析活性氧信号网络(如p38丝裂原活化蛋白激酶、核因子κB受体活化因子配体通路),开发靶向抗氧化疗法,并探索跨疾病(如糖尿病、心血管病)的氧化应激交互作用,以推动精准治疗策略的临床转化。"

| [1] REID IR, BILLINGTON EO. Drug therapy for osteoporosis in older adults. Lancet. 2022; 399(10329):1080-1092. [2] SHEPSTONE L, LENAGHAN E, COOPER C, et al. Screening in the community to reduce fractures in older women (SCOOP): a randomised controlled trial. Lancet. 2018;391(10122):741-747. [3] RINONAPOLI G, RUGGIERO C, MECCARIELLO L, et al. Osteoporosis in Men: A Review of an Underestimated Bone Condition. Int J Mol Sci. 2021;22(4):2015. [4] SU Y, ZHOU B, KWOK T. Fracture risk prediction in old Chinese people-a narrative review. Arch Osteoporos. 2023;19(1):3. [5] LIU Y, HUANG X, TANG K, et al. Prevalence of osteoporosis and associated factors among Chinese adults: a systematic review and modelling study. J Glob Health. 2025;15:4009. [6] 章晓云,曾浩,黎征鹏,等.骨质疏松症的发病机制及中医药治疗研究进展[J].中国实验方剂学杂志,2025,31(1):311-320. [7] ZHANG C, LI H, LI J, et al. Oxidative stress: A common pathological state in a high-risk population for osteoporosis. Biomed Pharmacother. 2023;163:114834. [8] ZHOU X, TIAN X, CHEN J, et al. Youthful Stem Cell Microenvironments: Rejuvenating Aged Bone Repair Through Mitochondrial Homeostasis Remodeling. Adv Sci (Weinh). 2025; 12(10):e2409644. [9] KOKOL P, BLAZUN VH, ZAVRSNIK J. Application of bibliometrics in medicine: a historical bibliometrics analysis. Health Info Libr J. 2021;38(2):125-138. [10] NINKOV A, FRANK JR, MAGGIO LA. Bibliometrics: Methods for studying academic publishing. Perspect Med Educ. 2022;11(3):173-176. [11] MANOLAGAS SC. From estrogen-centric to aging and oxidative stress: a revised perspective of the pathogenesis of osteoporosis. Endocr Rev. 2010;31(3):266-300. [12] MAGGIO D, BARABANI M, PIERANDREI M, et al. Marked decrease in plasma antioxidants in aged osteoporotic women: results of a cross-sectional study. J Clin Endocrinol Metab. 2003;88(4):1523-1527. [13] ALMEIDA M, HAN L, MARTIN-MILLAN M, et al. Skeletal involution by age-associated oxidative stress and its acceleration by loss of sex steroids. J Biol Chem. 2007;282(37):27285-27297. [14] DOMAZETOVIC V, MARCUCCI G, IANTOMASI T, et al. Oxidative stress in bone remodeling: role of antioxidants. Clin Cases Miner Bone Metab. 2017;14(2):209-216. [15] BASU S, MICHAELSSON K, OLOFSSON H, et al. Association between oxidative stress and bone mineral densit]. Biochem Biophys Res Commun. 2001;288(1):275-279. [16] BAI XC, LU D, BAI J, et al. Oxidative stress inhibits osteoblastic differentiation of bone cells by ERK and NF-kappaB. Biochem Biophys Res Commun. 2004;314(1):197-207. [17] BAEK KH, OH KW, LEE WY, et al. Association of oxidative stress with postmenopausal osteoporosis and the effects of hydrogen peroxide on osteoclast formation in human bone marrow cell cultures. Calcif Tissue Int. 2010;87(3):226-235. [18] LEE NK, CHOI YG, BAIK JY, et al. A crucial role for reactive oxygen species in RANKL-induced osteoclast differentiation. Blood. 2005;106(3): 852-859. [19] MODY N, PARHAMI F, SARAFIAN TA, et al. Oxidative stress modulates osteoblastic differentiation of vascular and bone cells. Free Radic Biol Med. 2001;31(4):509-519. [20] MUTHUSAMI S, RAMACHANDRAN I, MUTHUSAMY B, et al. Ovariectomy induces oxidative stress and impairs bone antioxidant system in adult rats. Clin Chim Acta. 2005;360(1-2):81-86. [21] DOMAZETOVIC V, MARCUCCI G, IANTOMASI T, et al. Oxidative stress in bone remodeling: role of antioxidants. Clin Cases Miner Bone Metab. 2017;14(2):209-216. [22] TAO H, LI X, WANG Q, et al. Redox signaling and antioxidant defense in osteoclasts. Free Radic Biol Med. 2024;212:403-414. [23] GUO Z, WU J, HU Y, et al. Exogenous iron caused osteocyte apoptosis, increased RANKL production, and stimulated bone resorption through oxidative stress in a murine model. Chem Biol Interact. 2024;399:111135. [24] WEI L, CHAI S, YUE C, et al. Resveratrol protects osteocytes against oxidative stress in ovariectomized rats through AMPK/JNK1-dependent pathway leading to promotion of autophagy and inhibition of apoptosis. Cell Death Discov. 2023;9(1):16. [25] HE Y, LIU T, PENG X, et al. Molecular mechanism of mitochondrial autophagy mediating impaired energy metabolism leading to osteoporosis. Biochim Biophys Acta Mol Basis Dis. 2025;1871(3): 167685. [26] ZHOU Y, SU Z, LIU G, et al. The Potential Mechanism of Soy Isoflavones in Treating Osteoporosis: Focusing on Bone Metabolism and Oxidative Stress. Phytother Res. 2025;39(3):1645-1658. [27] SUN Y, HUANG D, ZHANG Y. The bone-vascular axis: the link between osteoporosis and vascular calcification. Mol Cell Biochem. 2025;480(6): 3413-3427. [28] KARTHIK V, GUNTUR AR. Energy Metabolism of Osteocytes. Curr Osteoporos Rep. 2021;19(4): 444-451. [29] SIDDIQUI JA, PARTRIDGE NC. CCL2/Monocyte Chemoattractant Protein 1 and Parathyroid Hormone Action on Bone. Front Endocrinol (Lausanne). 2017;8:49. [30] HENRY ÓC, O’NEILL L. Metabolic Reprogramming in Stromal and Immune Cells in Rheumatoid Arthritis and Osteoarthritis: Therapeutic Possibilities. Eur J Immunol. 2025;55(4):e202451381. [31] AKAB SM, ABOZEID HE, ELAZAB SA, et al. Relation between bone mineral density and oxidative stress in Egyptian patients with chronic kidney disease: a cross sectional study. BMC Nephrol. 2025;26(1):197. [32] HUANG R, WANG H, SHEN Z, et al. Increased Glycemic Variability Evaluated by Continuous Glucose Monitoring is Associated with Osteoporosis in Type 2 Diabetic Patients. Front Endocrinol (Lausanne). 2022;13:861131. [33] YAN T, NISAR MF, HU X, et al. Pyrroloquinoline Quinone (PQQ): Its impact on human health and potential benefits: PQQ: Human health impacts and benefits. Curr Res Food Sci. 2024;9:100889. [34] LI J, ZHANG J, XUE Q, et al. Pyrroloquinoline quinone alleviates natural aging-related osteoporosis via a novel MCM3-Keap1-Nrf2 axis-mediated stress response and Fbn1 upregulation. Aging Cell. 2023;22(9):e13912. [35] PERVEEN I, BUKHARI B, NAJEEB M, et al. Hydrogen Therapy and Its Future Prospects for Ameliorating COVID-19: Clinical Applications, Efficacy, and Modality. Biomedicines. 2023;11(7):1892. [36] HUANG L. Molecular hydrogen: a therapeutic antioxidant and beyond. Med Gas Res. 2016; 6(4):219-222. [37] CARNOVALI M, BANFI G, MARIOTTI M. Molecular Hydrogen Prevents Osteoclast Activation in a Glucocorticoid-Induced Osteoporosis Zebrafish Scale Model. Antioxidants (Basel). 2023;12(2): 345. [38] SAUTCHUK RJ, YU C, MCARTHUR M, et al. Role of the Mitochondrial Permeability Transition in Bone Metabolism and Aging. J Bone Miner Res. 2023;38(4):522-540. |
| [1] | Xu Canli, He Wenxing, Wang Yuping, Ba Yinying, Chi Li, Wang Wenjuan, Wang Jiajia. Research context and trend of TBK1 in autoimmunity, signaling pathways, gene expression, tumor prevention and treatment [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(在线): 1-11. |
| [2] | Chen Huiting, Zeng Weiquan, Zhou Jianhong, Wang Jie, Zhuang Congying, Chen Peiyou, Liang Zeqian, Deng Weiming. Tail anchoring technique of vertebroplasty in treatment of osteoporotic vertebral compression fractures with intravertebral cleft: a finite element analysis [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2145-2152. |
| [3] | Zeng Xuan, Weng Rui, Ye Shicheng, Tang Jiadong, Mo Ling, Li Wenchao. Two lumbar rotary manipulation techniques in treating lumbar disc herniation: a finite element analysis of biomechanical differences [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2153-2161. |
| [4] | Cheng Qisheng, Julaiti·Maitirouzi, Xiao Yang, Zhang Chenwei, Paerhati·Rexiti. Finite element analysis of novel variable-diameter screws in modified cortical bone trajectory of lumbar vertebrae [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2162-2171. |
| [5] | Liu Wenlong, Dong Lei, Xiao Zhengzheng, Nie Yu. Finite element analysis of tibial prosthesis loosening after fixed-bearing unicompartmental knee arthroplasty for osteoporosis [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2191-2198. |
| [6] | Chen Long, Wang Xiaozhen, Xi Jintao, Lu Qilin. Biomechanical performance of short-segment screw fixation combined with expandable polyetheretherketone vertebral body replacement in osteoporotic vertebrae [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2226-2235. |
| [7] | Zhu Xiaolong, Zhang Wei, Yang Yang. Visualization analysis of research hotspots and cutting-edge information in the field of intervertebral disc regeneration and repair [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2391-2402. |
| [8] | Wen Fayan, Li Yan, Qiang Tianming, Yang Chen, Shen Linming, Li Yadong, Liu Yongming. Unilateral biportal endoscopic technology for treatment of lumbar degenerative diseases: global research status and changing trends [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(9): 2380-2390. |
| [9] | Lai Yu, Chen Yueping, Zhang Xiaoyun. Research hotspots and frontier trends of bioactive materials in treating bone infections [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(8): 2132-2144. |
| [10] | Hu Xiongke, Liu Shaohua, Tan Qian, Liu Kun, Zhu Guanghui. Shikonin intervention with bone marrow mesenchymal stem cells improves microstructure of femur in aged mice [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(7): 1609-1615. |
| [11] | Wen Guangwei, Zhen Yinghao, Zheng Taikeng, Zhou Shuyi, Mo Guoye, Zhou Tengpeng, Li Haishan, Lai Yiyi. Effects and mechanisms of isoginkgetin on osteoclastogenesis [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(6): 1348-1358. |
| [12] | Wu Zhilin, , He Qin, Wang Pingxi, Shi Xian, Yuan Song, Zhang Jun, Wang Hao . DYRK2: a novel therapeutic target for rheumatoid arthritis combined with osteoporosis based on East Asian and European populations [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(6): 1569-1579. |
| [13] | Zhang Haiwen, Zhang Xian, Xu Taichuan, Li Chao. Bibliometric and visual analysis of the research status and trends of senescence in osteoporosis [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(6): 1580-1591. |
| [14] | Huang Jie, Zeng Hao, Wang Wenchi, Lyu Zhucheng, Cui Wei. Visualization analysis of literature on the effect of lipid metabolism on osteoporosis [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(6): 1558-1568. |
| [15] | Yang Zeyu, Zhi Liang, Wang Jia, Zhang Jingyi, Zhang Qingfang, Wang Yulong, Long Jianjun. A visualized analysis of research hotspots in high-frequency repetitive transcranial magnetic stimulation from the macroscopic perspective [J]. Chinese Journal of Tissue Engineering Research, 2026, 30(5): 1320-1330. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||