Chinese Journal of Tissue Engineering Research ›› 2020, Vol. 24 ›› Issue (28): 4474-4484.doi: 10.3969/j.issn.2095-4344.2291
Previous Articles Next Articles
Research status of dynamic three-dimensional tissue culture driving methods
Yang Yong1, Lü Chenze2, Xu Ming’en1, 2, Wang Ling1, 2
1College of Automation, Hangzhou Dianzi University, Hangzhou 310018, Zhejiang Province, China; 2Zhejiang Provincial Key Lab of Medical Information and Three-Dimensional Bio-Printing, Hangzhou Dianzi University, Hangzhou 310018, Zhejiang Province, China
-
Received:2019-10-28Revised:2019-10-31Accepted:2019-12-13Online:2020-10-08Published:2020-08-31 -
Contact:Wang Ling, Professor, College of Automation, Hangzhou Dianzi University, Hangzhou 310018, Zhejiang Province, China; Zhejiang Provincial Key Lab of Medical Information and Three-Dimensional Bio-Printing, Hangzhou Dianzi University, Hangzhou 310018, Zhejiang Province, China -
About author:Yang Yong, Master candidate, College of Automation, Hangzhou Dianzi University, Hangzhou 310018, Zhejiang Province, China -
Supported by:the National Natural Science Foundation of China, No. 61675059
CLC Number:
Cite this article
Yang Yong, Lü Chenze, Xu Ming’en, , Wang Ling, . Research status of dynamic three-dimensional tissue culture driving methods[J]. Chinese Journal of Tissue Engineering Research, 2020, 24(28): 4474-4484.
share this article
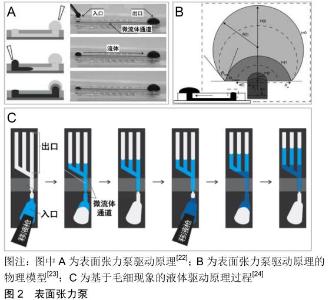
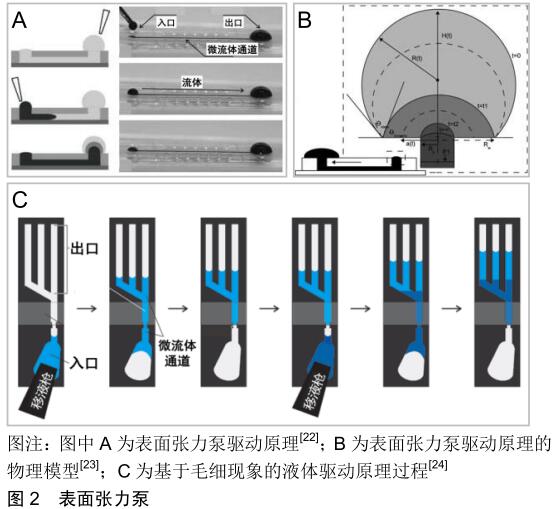
2.1 微流控技术中常用驱动方法 常见的微流控驱动方法根据驱动原理可分为被动驱动和主动驱动[18-19]。被动驱动 一般是指无需任何外部驱动方法,流体自发性流动的驱动方法,具有低成本、结构简单、无需任何驱动源等优点。主动驱动一般是指具有驱动装置,通过外力作用使液体产生流动的驱动方法,一般可以通过调节不同的驱动参数来控制流体的流动方式和流速变化;根据流体流动特性可以分为连续流动驱动和脉动流动驱动[20-21]。连续流动驱动下的流体以匀速或变速连续不断的流动,其平均速度和瞬时速度均便于测量;脉动连续流动下流体以脉冲流的形式流动,其瞬时速度难以测量,一般只能测量平均速度;根据流体是否可以实现循环流动可分为开环流动驱动和闭环流动驱动。开环流动驱动的流体从微流控装置的入口端流入,从出口端流出,流出后的流体不会再回到微流控装置内,并且入口端液体存储器内的液体可以很方便的被填充,以维持导管内流体的可持续流动。闭环流动驱动可以为导管内的流体提供可持续的循环流动。由于驱动原理对流动特性和循环方式有很大的影响,所以文章针对主动驱动和被动驱动对常见的微流体驱动方法进行综述。 2.1.1 被动驱动 表面张力泵:是一种利用表面张力泵送流体的被动驱动方法,其原理是将液体引入微流体通道并在出口处形成大液滴,然后通过在入口处引入较小液滴,由于入口处小液滴产生的压力大于出口处大液滴产生的压力,从而驱动微流道内流体流动,直到出口处的液滴的曲率半径达到平衡为止。MEYVANTSSON等[22]将表面张力泵和微流控技术相结合设计了一个易于使用的微流体平台,如图2A所示,该平台可用于低通量手动操作以及高通量实验室自动化。BERTHIER等[23]针对于表面张力泵开发了一种物理模型,如图2B所示,可用于分析表面张力泵的驱动原理和不同阶段的流量计算。此外,表面张力还是影响毛细现象的核心作用,毛细现象也有被用于微流体的驱动。JUNCKER等[24]基于毛细现象设计了一种流体自下而上运动的微流控装置,如图2C所示,通过移液枪不断的将流体引入微流道内,直至微流道全部充满流体为止。该装置驱动流体流动的毛细管作用力是微流道中凹液面与通道入口液面的压力差造成,随着微流道内的液体逐渐充满,压力差逐渐减少,速度也逐渐降低,最终流体停止运动。 表面张力泵结构简单、体积小,无需任何驱动装置和连接各培养室的复杂管道。表面张力泵是基于微量液体的表面张力驱动流体流动,来很大程度上依赖于流体自发性运动,只能驱使流体产生严格单向、连续的开环流动方式。表面张力泵驱动的流体流量一般为微升级别的液滴,产生的流体流速很小,难以通过人为控制来调节所产生的流速大小和流速范围,并且需要通过在入口处不断填充液滴来维持流体,适合于短时间内的微量流体泵送。 "
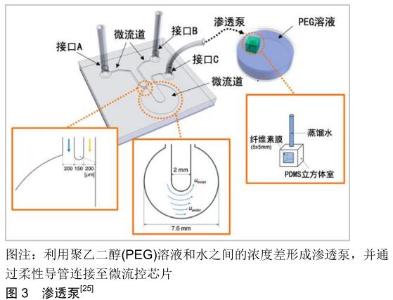
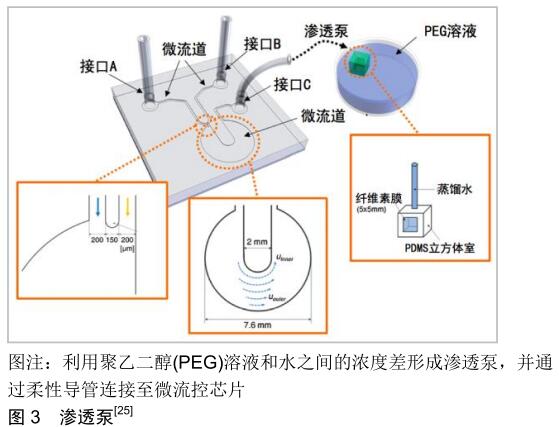
渗透泵:是一种利用两种不同溶液的浓度差来泵送流体的被动驱动方法,其工作原理是利用驱动剂溶液和样品溶液的浓度差来驱动流体流动。PARK等[25]设计了一种具有纤维素膜窗口的渗透泵,如图3所示,其中纤维素膜是一种多孔性有机薄膜,可用于分隔两种不同浓度的溶液。利用液态聚二甲基硅氧烷作为黏结剂,将纤维素膜和固态聚二甲基硅氧烷立方体室黏合在一起形成渗透泵,并使用柔性聚乙烯管连接到微流控芯片。通过使用聚乙二醇溶液作为驱动剂和去离子水作为样品溶液,成功构建了渗透泵系统。 渗透泵可以在几乎恒定的流速下为流体提供缓慢的流动,可以通过改变驱动剂溶液的浓度以及半透膜的表面积和孔径大小来控制渗透泵的泵送速率。驱动剂溶液的浓度越高流速越大,半透膜的表面积和孔径越大流速也越大。但驱动剂溶液的浓度、半透膜的表面积和孔径所能调节的范围有限,导致渗透泵的流速可调节范围变小。由于渗透泵的原理是基于液体从低浓度溶液通过半透膜进入高浓度溶液的渗透作用,因此渗透泵驱动流体产生的也是一种严格单向、连续的开环流动方式。此外,渗透泵可通过不断向储液池中添加液体及增加驱动剂溶液浓度来延长流体流动,适合于长时间内的流体泵送。但渗透泵通常需要复杂的渗透装置,不利于微流控装置的集成化。 "
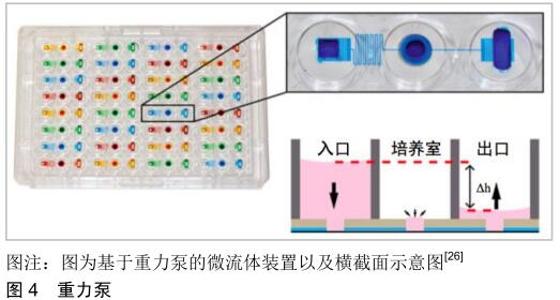
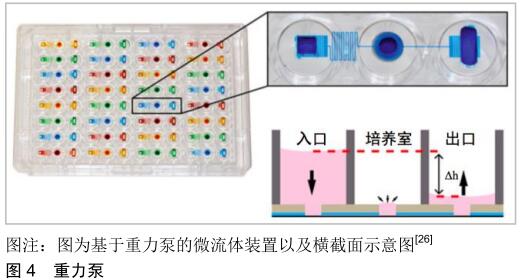
重力泵:是一种驱使流体自上而下运动的被动驱动方法,其原理是2个不同高度的液体储存器内的液体在重力影响下从高储层向低储层的流动,随着2个存储器液面高度差的降低,液体流动的速率也会逐渐降低,当2个液体储存器内液面高度差消失时,液体停止流动。CHEN等[26]利用96孔板设计了一种具有32个独立流动单元组成的微流体灌注阵列,每个独立流动单元由入口、出口和细胞培养室组成,通过在入口添加300 μL培养基及出口添加30 μL培养基来形成液面高度差,从而在重力影响下驱动流体流动,该微流控装置的结构示意图如图4所示。 重力泵仅仅依靠流体自身的重力作用,一般只能驱动流体产生自上而下、连续的开环流动方式,并且流速大小随着时间的推移不断降低,不能产生流速恒定的流体流动。重力泵可以在进口处通过不断地添加液体以实现可持续流动,但这终究难以实现长时间的流体流动。 "
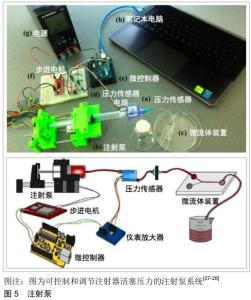
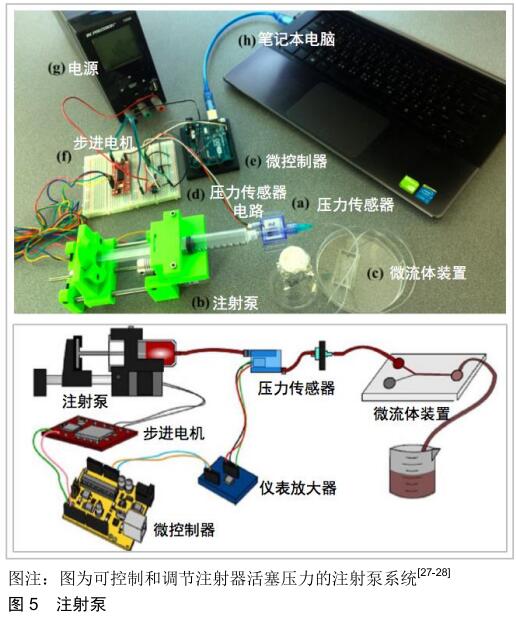
2.1.2 主动驱动 注射泵:是利用活塞或气体等方式产生的正压力将注射器内存储的液体材料输送至液体导管的一种驱动装置。CHEN等[27]开发了一种能够控制和调节输送到微流控装置入口流体压力的注射泵系统,该系统由注射泵、压力传感器和可编程微控制器3部分组成,可为微流控装置提供精确的流量控制。此外,该团队的LAKE等[28]设计了一种低成本的注射泵系统,可以使用闭环压力控制输出的流量压力,无需昂贵的精密工程部件。注射泵系统的示意图如图5所示。 注射泵最突出的优点是结构简单、成本低,能为微流控装置提供稳定的流速控制和流量计算,这对于具有精准流速控制要求的应用是一个不错的选择。然而,注射泵一般只能驱动流体产生严格单向、连续的开环流动方式,并且由于注射器的储存体积有限,不适合长时间内的流体泵送。注射泵虽然以通过计算机编程控制注射器活塞实现流体的脉动流动,但需要制作高精度的控制系统的电机以实现对注射器活塞的精准控制。并且,注射泵一般只能泵送单个注射器内的液体,难以实现流体的长时间泵送。尽管采用多个注射泵可能会实现多个容器内的液体的泵送,但这不仅会提高实验成本,而且操作难度也会显著提高。 "
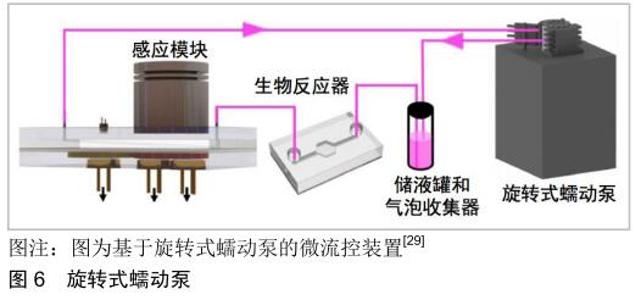
蠕动泵:根据驱动原理可以分为旋转式蠕动泵和阀门式蠕动泵。旋转式蠕动泵是通过将柔性导管缠绕在具有滚轮的转子上,当转子转动时,滚轮在不同的位置处连续挤压柔性导管,将导管内的液体以蠕动的流动特征挤出。这种基于转子旋转的蠕动泵,可以通过顺时针或逆时针改变转子的旋转方向以实现柔性导管内液体流动方向的控制。如图6所示,SHAEGH等[29]通过使用旋转式蠕动泵驱动液体流动,开发了一套集成光学传感模块的微流体循环灌注平台。SKARDAL等[30]设计并制造了一种模块化微流体装置,该装置通过组装由聚二甲基硅氧烷制造的独立组件形成,每个组件通过导管以串联的方式连接到旋转式蠕动泵,实现了该平台模块化“即插即用”和循环灌注功能。 "
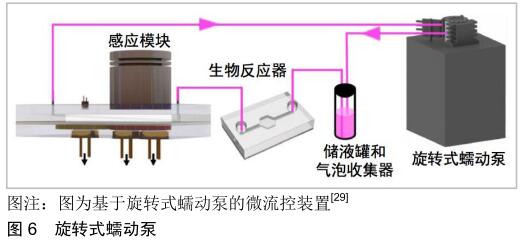
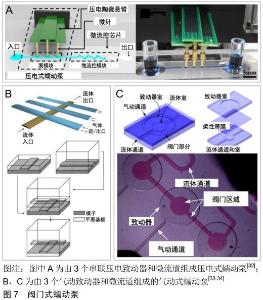
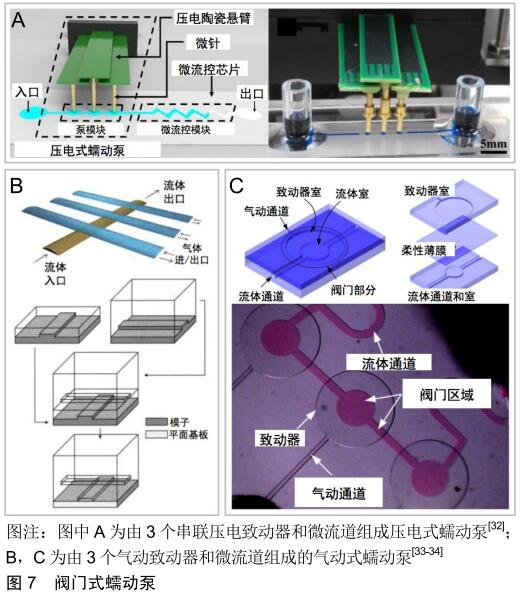
阀门式蠕动泵是通过多个串联致动器按照一定的致动顺序来改变微流道的形状,从而促使微流控芯片内流体形成类似于蠕动的流动方式。其中致动器和微流道之间通常使用柔性薄膜隔开,起到旋转式蠕动泵中柔性导管接受周期性挤压使流体流动的功能。致动器的基本原理是利用压电、气动等方式促使柔性薄膜变形从而实现微流道内流体流动。因此常见的阀门式蠕动泵有压电式蠕动泵和气动式蠕动泵。20世纪90年代,SMITS等[31]首次设计出了由压电薄膜致动器和止回阀组成的硅微型压电式蠕动泵。该微型泵通过标准光刻技术制造,根据逆压电效应,压电材料可以在电场的作用下发生形变,利用压电材料形变施加的力作用于柔性薄膜,从而驱动微流道流体流动。2019年,MA等[32]设计了一种新型的压电式蠕动泵,如图7A所示,该泵由3个压电致动器和微流体通道组成,可以为液体提供8.4 nL/s的高精度流速。2000年,UNGER等[33]通过在微流道上安装3个气动微阀,结合标准软光刻工艺成功制造了一种基于硅橡胶薄膜的气动式蠕动泵,并首次使用气动微型阀门实现了半圆形微流道内流体的流动,如图7B所示,该气动式蠕动泵是利用气体对柔性薄膜施加正压或者负压来促使其发生形变,从而驱动流体流动。基于类似的工作原理,JEONG等[34]使用聚二甲基硅氧烷制造了一种由3个串联气动致动器和微流体通道组成的微型蠕动泵,如图7C所示,气动致动器包括一个较小的圆形流体腔和一个较大的圆形气体腔,两个腔室之间通过柔性薄膜隔开。 蠕动泵最突出的优点是能产生方向可控、脉动的流体流动,可以很方便的形成开环或闭环流动方式,可通过调节旋转式蠕动泵转子的旋转速度、方向及阀门式蠕动泵致动器的致动时间、制动顺序来控制流体流速和流动方向,但是蠕动泵的周期性挤压瞬间产生的脉冲流可能会造成液体回流现象。旋转式蠕动泵的柔性导管会随着时间的推移而发生不可逆的形变和损伤,不利于长时间的流体泵送;相对于旋转式蠕动泵,阀门式蠕动泵体积更小,有利于微流控装置的微型化和集成化。但压电式蠕动泵的制动器一般使用硅晶片微加工技术,成本较高。气动蠕动泵的每个致动器都需要独立的气动源,这就造成一个芯片同时需要多路气动源来驱动。 "
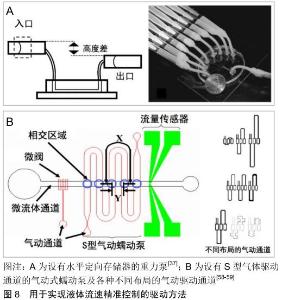
2.2 流速精准控制 流体流动会产生剪切力,组织生长微环境的剪切力是由人体体液流动作用于体内组织单位面积的摩擦力。研究表明,剪切力对细胞的形态变化、迁移能力、功能表达及增殖和凋亡具有重要影响[47-52]。并且,人体体内大部分细胞受到的剪切力大小各不相 同[53],甚至会产生10倍以上的差异。例如,内皮细胞受到的理论剪切力约为0.15 mN/cm2[54],而正常肝组织中产生的流体剪切力一般小于1 μN/cm2[55]。微流控技术中剪切力的大小是由液体的黏稠度、流动速度和流道的尺寸、形状、表面粗糙度等因素共同决定的。虽然通过流道设计和流速控制可以调节流体流动产生的剪切力范围,但体外模型的流道尺寸大小往往决定着通过三维组织的培养基体积大小,如果培养基的总体积过大则会导致代谢产物浓度太低,无法真实体现组织对药物的反应,并且不利于相关指标的检测。因此,为了更好地模拟体内真实微环境,体外模型的流道尺寸一般选择百微米到毫米级别,对剪切力的调节作用有限。相比于流道设计,流速范围可以很方便的通过驱动参数来调节,实现剪切力范围的精准控制。 除了液体的流速之外,液体的不同流动方式也使得组织受到的剪切力刺激产生差异。人体体液的流动方式主要包括连续流动和脉动流动,这两种流动方式对于体外模型的动态培养都具有重要意义。连续的培养基流动是细胞动态培养实验中最基本的流动方式。PRZYBYLA等[56]通过使用微流体连续灌注培养小鼠胚胎干细胞,连续流动的培养基不断去除小鼠胚胎干细胞的分泌因子,并观察到细胞分泌因子的减少导致小鼠胚胎干细胞脱离其稳定的自我更新状态。脉动的流动环境是人体体内许多细胞所处的动态环境,例如血管内皮细胞。ESTRADA等[57]利用蠕动泵设计并制造了内皮细胞培养模型,该模型可模拟心脏脉冲流以及脉动流动下的剪切力分布,与静态条件下培养的细胞相比,内皮细胞培养模型培养的细胞表现出细胞骨架肌动蛋白丝的排列和β-连环蛋白的高表达水平。因此,为了更好地模拟体内真实微环境,需要根据不同研究对象在体内的真实状态选择不同的驱动方法,要求所选的驱动方法让培养基以特定速度和流动方式通过培养的三维组织,以产生与体内环境一致的剪切力,避免对三维组织的损伤或者导致体外模型无法正确的反应体内组织的功能。 不同驱动方法根据自身的特点可以产生连续或脉动的流动方式,并且在流速控制方面有各自的优缺点。表面张力泵只能驱使流体产生连续的流动方式,难以调节所产生的的流速大小和流速范围;渗透泵产生的也是一种连续的流体流动方式,其流速大小和流速范围受驱动剂溶液及半透膜的表面积和孔径大小的限制,难以调控;重力泵产生的是连续的流动方式,其流速随着液面高度差的降低而逐渐减少,不能产生稳定的流体流动。为了满足恒定速度的流体流动需求,ZHU等[37]利用表面张力将液体存储器设置为水平定向存储器,通过固定两个存储器高度差以保持恒定的液压压降,如图8A所示,微流道流体流速大小只取决于2个存储器之间的高度差,不会随着时间的推移而变化,从而实现匀速流动,有效解决了重力泵典型的流速随液面差变化不断降低的问题,并且最终通过微流体细胞动态培养实验证明了该装置的实用性。但该设计仍存在一定的局限性,例如,液体存储器的水平定向需要利用表面张力来实现,这就显著限制了存储器的几何形状大小和结构设计;注射泵一般被用于驱动流体产生连续的流动方式,虽然可通过计算机编程控制注射器活塞实现流体的脉动流动,但需要制作高精度的控制系统的电机以实现对注射器活塞的精准控制。此外,注射泵最突出的优点是它能通过高精度的电机和气压输出控制为微流控装置提供精准的流速控制和流量计算,这对于具有精准流速控制要求的应用是一个不错的选择;蠕动泵根据自身的特性只能产生脉动的流动方式,旋转式蠕动泵的流速大小取决于蠕动泵转子的旋转速度和蠕动泵柔性导管的直径,转子旋转速度越大流速越大,柔性导管的直径越小流速越大,但由于蠕动泵具有脉动的特性,使用直径较大的导管时,在转子挤压导管的一瞬间产生的流速会突然变大,因此体外模型的动态培养需要使用直径较小的柔性导管来实现组织培养过程中的低流速需求,并且柔性导管会随着时间的推移而发生不可逆的形变和损伤,而且柔性导管同时兼具韧性和柔软非常难,因此旋转式蠕动泵在低流速范围内难以实现流速的精准控制。阀门式蠕动泵可以通过致动器的致动时间来控制流速变化。WANG等[58]设计了一种基于S型气体驱动通道的气动式蠕动泵,如图8B所示,仅需一个气动源就可以驱动多个致动器,其基本布局是在气动驱动通道的不同位置处与微流道相交,每个相交点通过柔性薄膜隔开,形成多个串联的基于膜的气动致动器。这种气动式蠕动泵的基本原理是利用气体在S型通道中的流动阻力使得通道内的气压逐渐升高,促使相邻气动致动器的弹性薄膜依次产生蠕动性脉动,驱动微流道内流体流动。实验数据表明该蠕动微泵在137.8 kPa的气体压力和9 Hz的操作频率下,可以提供7.43 μL/min的最大泵送速率。为了进一步降低泵送流速、扩大流速范围,该团队的WU[44]和HUANG等[59]对原始设计进行了改进,他们通过调整气动微通道的形状和尺寸来调节致动器的依次致动时间,调节流体泵送速率,并通过制造了各种不同布局的气动驱动通道扩大了流体流速范围。 "
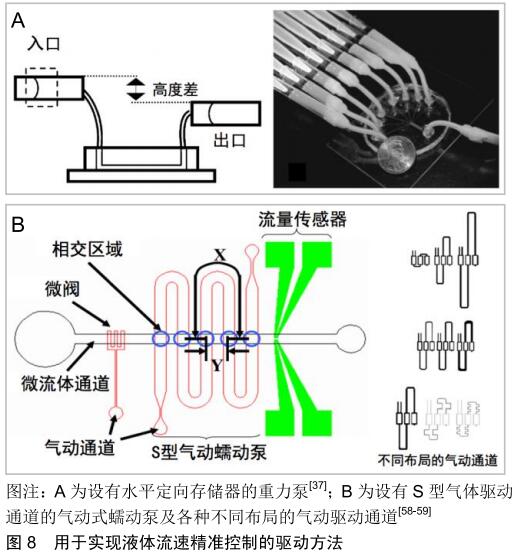
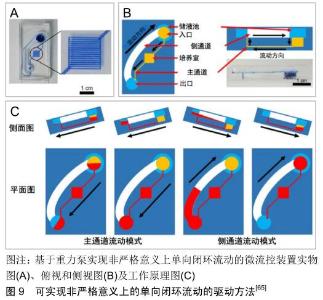
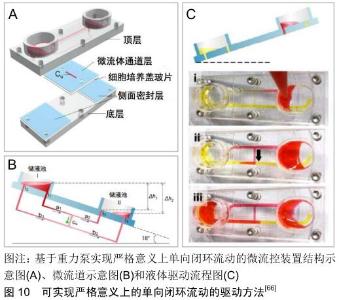
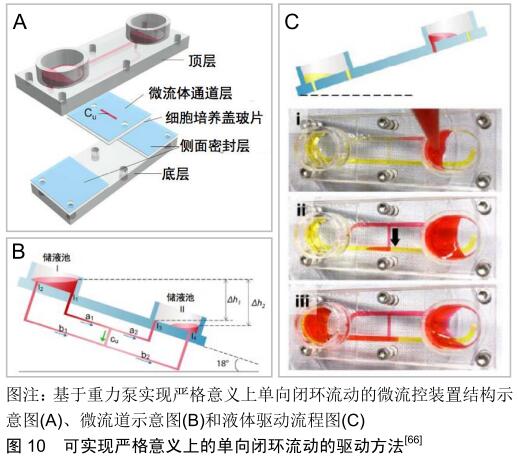
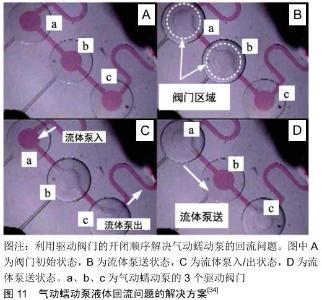
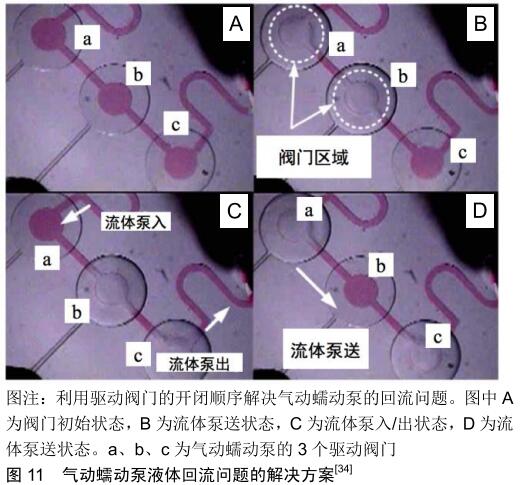
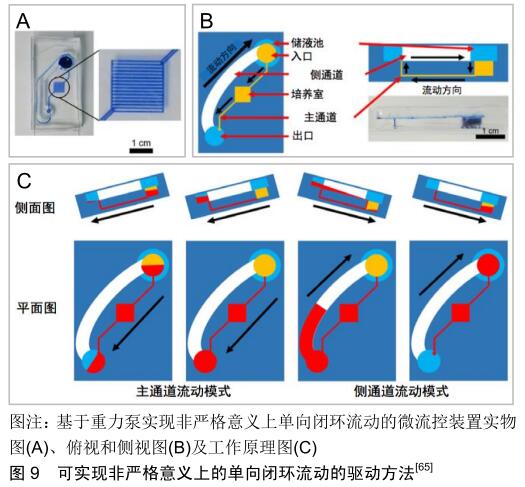
2.3 闭环流动 前面提到通过选择不同的驱动方法可实现培养基的开环流动和闭环流动。由于培养基的闭环流动对于模拟细胞所处微环境非常重要[60-61],首先,培养基的闭环流动有利于维持细胞所需的营养物质水平和培养基内相关检测物的浓度,降低检测难度。目前,组织培养的检测手段主要包括组织切片染色和检测培养基内相关指标,其中组织切片染色会对组织造成不可逆的损伤,而培养基检测实现的是一种在线无损的检测手段。其次,在药物动力学研究中培养基的闭环流动有利于实现药物的充分利用和均匀分布,减少药物用量。最后,培养基的闭环流动有利于增加培养基与组织的充分反应时间,减少培养基的用量,节约成本。因此,体外动态三维组织培养模型要求能实现培养基的闭环流动。 驱动方法自身的特性决定了是否可以实现闭环的流动方式。表面张力泵、渗透泵和注射泵一般只能被用于产生单向、开环的流动方式,难以实现培养基的循环流动。传统的重力泵只能用于产生自上而下、开环的流体流动,但是通过借助周期性的倾斜平台可以实现闭环的流动方式。SUNG等[62]设计了一种基于PK-PD模型的微流体装置,利用倾斜平台周期性的摇摆运动实现了重力泵的闭环流动模式。通过不断改变摇摆平台倾斜角度实现培养基来回往复的流动,每当摇摆平台来回摆动时,培养基的流动方向就会发生改变,形成一种双向流动的闭环流动模式。然而这种双向的闭环流动模式不能满足人体体液单向流动的生理学特性。研究表明单向流动模式对于细胞的生长具有重要影响,例如,血管内皮细胞的排列分布是由体液单向流动模式下所产生的流体剪切力方向决定[63-64]。因此,LEE等[65]为了解决这个问题开发了一种基于重力泵的新型微流控芯片,如图9所示,该芯片拥有不同几何形状的主通道和侧通道,可根据摇摆平台的倾斜方向进行选择性流体流动,实现器官芯片的微流体单向再循环流动。这种产生单向流体流动方式的基本原理是:侧通道的尺寸被设计得远大于主通道尺寸,这使得侧通道拥有足够小的液压阻力,导致流体从入口经过主通道流动到出口后,在倾斜平台的诱导下大部分流体会经过侧通道回到入口,只有很小一部分的流体会经过主通道产生双向流动。虽然与侧通道的流体流量相比,经过主通道的流量可忽略不计,但这仍不是真正意义上的单向闭环流动。WANG等[66]设计了一种可以实现单向闭环流动模式的“UniChip”芯片,如图10所示,该芯片也是一个基于重力驱动,结合周期性摇摆平台的微流体装置,其创新点在于设有一个防回流机制,能够实现流体严格意义上的单向流动。该机制基本原理是在2个存储器之间的水平方向上设有2个高度不同的侧通道,在垂直方向上设置主通道以连接2个侧通道,通过摇摆平台的周期性运动使两个侧通道流体形成再循环的流动,进而为主通道提供单向再循环的流体流动。总之,重力泵仅仅依靠流体自身的重力作用,难以实现单向闭环的流动模式,虽然有很多研究者通过特殊流道设计成功实现了重力驱动下的单向闭环流动模式,但这些研究都需要借助周期性运动的倾斜平台;蠕动泵根据自身的特性可以很方便地实现培养基流动方向可控的闭环流动,但当蠕动泵挤压柔性导管或微流道后抬起的一瞬间会产生回流现象,当回流产生时培养基的流动可以近似的认为是一种双向的流动模式。为了解决这个问题,JEONG等[34]通过优化驱动阀门的开闭顺序,保持3个驱动阀门始终形成一个橡胶密封阀的结构,如图11所示,有效限制了气动蠕动泵驱动过程中流体的回流现象。 "
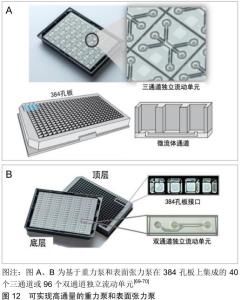
2.4 生物实验环境 利用体外组织培养模型模拟体内生理条件,需要在无菌、室温和一定的营养条件下才能使细胞维持其结构和功能。微流控驱动方法由于自身的结构设计不同,导致驱动方法对组织培养环境产生不同的影响。表面张力泵和重力泵无需庞大的驱动装置和复杂的流道结构,使得整个组织培养系统可被置于培养箱内培养,有利于体外组织的无菌培养;渗透泵由于其庞大的渗透装置和复杂的工作原理使得其难以适应体外组织所需的培养环境;注射泵和蠕动泵需要驱动装置才能驱使培养基流动,为了满足体外组织培养环境的特定需求,在组织培养过程中一般将细胞培养部分置于培养箱内,驱动装置置于培养箱外,两者之间通过导管相连接。然而,注射泵和旋转式蠕动泵所驱动的培养基是直接通过导管输送,这种设计会造成导管内不必要的培养基浪费,并且培养箱内外的温度差异会造成导管内培养基的温度差异,影响细胞的正常培养。通过气体驱动培养基流动可以很好地解决这个问题,气动式蠕动泵利用气体通过导管间接驱动微流道内培养基流动,有效避免了培养基暴露于培养箱内外不同的温度环境下。基于相同的原理,注射泵也可实现气体驱动培养基流动。 2.5 高通量 新药研发过程中,在临床前研究和审批之前需要对几万种潜在化合物进行临床前评估和验证,这个过程可能需要近10年时间,花费数十亿美元,并且成功率极低[67]。尽管利用体外模型可有效代替动物实验来进行临床前药物评估,但体外模型用于药理、毒理和药物筛选的时候仍需要大量的实验量,进而导致需要尽可能提高实验通量。因此,为了实现体外组织培养模型的高通量应用,要求驱动方法可实现培养基的高通量泵送,以实现多个实验的同时进行,节约人力资源和实验成本。 表面张力泵和重力泵结构简单、体积小,有利于实现集成化和高通量。CHEN等[26]和GORAL等[68]都充分利用96孔板的孔室在同一块孔板上集成了32个独立微流控流动单元,可以同时进行不同条件下的实验。不同的是前者是基于重力泵驱动,后者是基于静态压力驱动。荷兰公司 Mimetas 提供了一种用于高通量的人体组织和疾病模型OrganoPlates?[69-70],如图12所示,该模型是一种通用的三维细胞培养体外模型,可用于体外培养肾脏、肠、皮肤等人体组织。OrganoPlates?利用重力或表面张力作为驱动力,以标准384孔板的形式集成了96个双通道或40个三通道独立流动单元。并且该公司提供的重力泵系统Perfusion Rocker可以同时将4个OrganoPlates?平台置于同一个平台上后一同放入培养箱,通过周期性地倾斜平台可以实现细胞的长期动态培养。 "

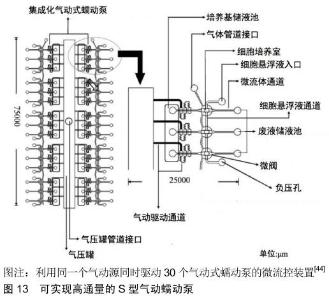
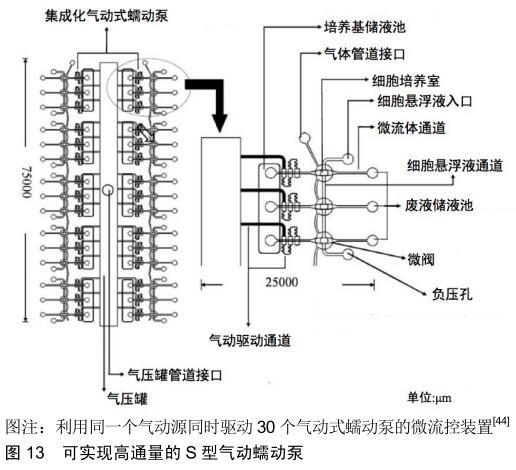
渗透泵和注射泵需要复杂的驱动装置,难以实现集成化和高通量;旋转式蠕动泵一般只能同时泵送单个导管的流体流动,难以实现高通量泵送。尽管有研究者通过在旋转式蠕动泵的旋转转子集成多个柔性导管形成多通道蠕动泵,但这种多通道蠕动泵的每个柔性导管可能会因为受力不均匀,导致每个通道的流速存在着细微差异性;压电式蠕动泵和气动式蠕动泵是基于微型阀门制造的阀门式蠕动泵,相对于旋转式蠕动泵,阀门式蠕动泵体积更小,有利于微流控装置的微型化和集成化,实现高通量。由于压电式蠕动泵一般使用硅晶片微加工技术成本较高,在进行高通量实验时会显著增加实验成本。因此,近几年压电微泵材料的发展趋势已经逐渐从微加工玻璃或硅晶片转向聚二甲基硅氧烷和聚甲基丙烯酸甲酯等低成本光学透明材料[32]。并且,压电式薄膜致动器的制造过程复杂,使得压电式蠕动微泵的应用受到了极大限制。相比于压电式蠕动泵,气动式蠕动泵的阀门致动器一般由聚二甲基硅氧烷制作,使用气体作为驱动力,结构更简单,成本更低,易于实现大批量生产和高通量。德国TissUse公司提供了一种气动式蠕动泵系统 HUMIMIC Starter,该系统可以通过气动式蠕动泵的气动通道同时驱动培养箱内的4个器官芯片。基于同样的原理,英国公司CN Bio也提供了一种气动式蠕动泵系统PhysioMimixTM,该系统可以承载并驱动3个器官芯片及每个芯片上的12个微流道。WU等[44]通过使用同一个气动源同时驱动30个气动式蠕动泵,并和30个微生物培养室集成在一起,如图13所示,每个集成气动微泵的泵送速率在统计学上保持一致,实现了气动式蠕动泵在体外组织培养模型中培养基的高通量泵送。 "
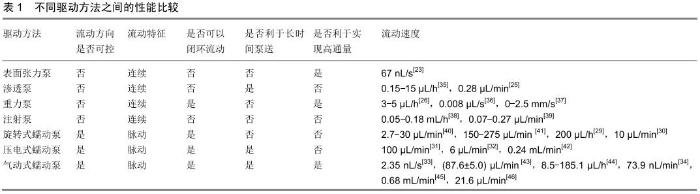
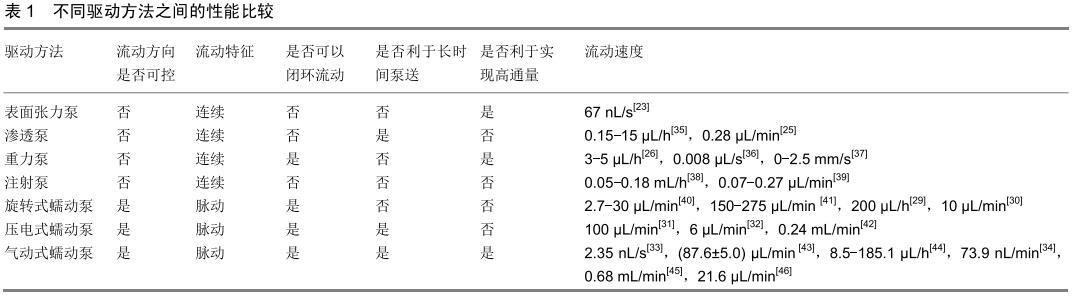
2.6 总结 文章主要综述了动态三维组织培养系统的驱动方法研究现状分析,总结了常见的驱动方法优缺点,对不同驱动方法之间的性能进行了比较分析,如表1所示。具体分析如下所示:①表面张力泵结构简单、体积小,有利于实现动态三维组织培养系统的高通量;但表面张力泵只能产生单向、连续、非闭环以及短时间内的流体流动,对于需要模拟体液脉动闭环流动的长期动态三维组织培养实验,表面张力泵并不是一个很好的选择;②相比于表面张力泵,渗透泵的优点在于能实现动态三维组织的长期培养,但由于需庞大的渗透装置,不利于动态三维组织培养实验的高通量;③相比于表面张力泵,重力泵的优点在于可以实现中培养基的闭环流动,有利于构建动态三维组织培养系统中更高仿生度的微环境;④相比于表面张力泵,注射泵的优点在于可实现流速的精准控制,但不利于动态三维组织培养实验的高通量;⑤蠕动泵可以产生方向可控、脉动、闭环的流体流动,但旋转式蠕动泵不利于实现动态三维组织的长期和高通量培养;相比于旋转式蠕动泵,压电式蠕动泵有利于动态三维组织的长期培养,而气动式蠕动泵既利于动态三维组织的长期培养,又利于动态三维组织的高通量培养。 此外,文章还针对动态三维组织培养系统中驱动方法的需求,为从事这方面研究的人梳理了思考的顺序和优先级,在构建动态三维组织培养系统时研究者需要优先考虑以下几点:①动态三维组织培养系统中研究对象在体内所处的真实微环境,例如根据组织在体内受到的剪切力大小,判断驱动方法需要产生的流速大小和控制精度;根据组织在体内所处体液的流动特性,判断驱动方法需要产生的连续或脉动的流体流动方式;②动态三维组织培养系统中研究对象在实验过程中的检测手段,如果需要检测组织自身的相关指标,则闭环流动和开环流动的驱动方法都可以满足需求;如果需要检测培养基中相关指标,则优先考虑闭环流动的驱动方法;③动态三维组织培养系统中驱动方法所需的培养环境和实验通量,例如为了增加实验通量,优先考虑微型化和集成化高的驱动方法。 "
|
[1] ORBACH SM, LESS RR, KOTHARI A, et al. In Vitro Intestinal and Liver Models for Toxicity Testing.ACS Biomater Sci Eng. 2017;3(9):1898-1910.
[2] TAŠKOVA K, FONTAINE JF, MROWKA R, et al. Evaluation of in vivo and in vitro models of toxicity by comparison of toxicogenomics data with the literature.Methods. 2017;132: 57-65.
[3] NIEMAN GF, SATALIN J, ANDREWS P, et al. Preemptive mechanical ventilation based on dynamic physiology in the alveolar microenvironment: Novel considerations of time-dependent properties of the respiratory system.J Trauma Acute Care.2018;85(6):1081-1091.
[4] LI W, YAN Z, REN J, et al. Manipulating cell fate: dynamic control of cell behaviors on functional platforms.Chem Soc Rev2018;47(23):8639-8684.
[5] YAMAGISHI M, HORI Y, UEMURA S, et al. Time evolution of microenvironment around cells regulated by the secretion activity and culture density of the cells//International Symposium on Micro-nanomechatronics & Human Science. IEEE,2018.
[6] MORONI L, BURDICK JA, HIGHLEY C, et al. Biofabrication strategies for 3D in vitro models and regenerative medicine. Nat Rev Mater.2018;3(5):21-37.
[7] RYAN AJ, BROUGHAM CM, GARCIARENA CD, et al. Towards 3D in vitro models for the study of cardiovascular tissues and disease.Drug Discov Today.2016; 21(9):1437-1445.
[8] FIGTREE GA, BUBB KJ, TANG O, et al. Vascularized Cardiac Spheroids as Novel 3D in vitro Models to Study Cardiac Fibrosis.Cells Tissues Organs.2017; 204(3-4):191-198.
[9] FERRARINI M, STEIMBERG N, BONIOTTI J, et al. 3D-Dynamic Culture Models of Multiple Myeloma.Methods Mol Biol.2017;1612:177-190.
[10] JIN L, XU Q, KUDDANNAYA S, et al. Fabrication and Characterization of Three Dimensional Core-Shell Structure Nanofibers Designed for 3D Dynamic Cell Culture.ACS Appl Mater InteR.2017;9(21):17718-17726.
[11] PENDERECKA K, IBBS M, KALUZNA A, et al. Implementation of a dynamic culture condition to the heterotypic 3D breast cancer model.J Biomed Mater Res B.2019; 8:1-12.
[12] JARVIS M, ARNOLD M, OTT J, et al. Microfluidic co-culture devices to assess penetration of nanoparticles into cancer cell mass.Bioeng Transl Med.2017;2(3):268-277.
[13] ZHAO Y, YAN X, LI B, et al. Three-dimensional co-culture microfluidic model and its application for research on cancer stem-like cells inducing migration of endothelial cells. Biotechnol Lett.2017;39(9):1425-432.
[14] LI R, ZHANG X, LV X, et al. Microvalve controlled multi-functional microfluidic chip for divisional cell co-culture. Anal Biochem.2017;539:48-53.
[15] MASSAI D, BOLESANI E, DIAZ DR, et al. Sensitivity of human pluripotent stem cells to insulin precipitation induced by peristaltic pump-based medium circulation: considerations on process development OPEN.Sci Rep-UK.2017;7(1):3950.
[16] YEH SL, LIN TR, PENG CC, et al. A microfluidic device to study effects of physical stimulation and steroid treatment on lung epithelial cell surfactant protein expression//International Conference on Solid-state Sensors.IEEE, 2017.
[17] LI J, WEI J, LIU Y, et al. A microfluidic design to provide a stable and uniform in vitro microenvironment for cell culture inspired by the redundancy characteristic of leaf areoles.Lab Chip. 2017;17(22):3921-3933.
[18] WANG X, ZHAO D, PHAN DTT, et al. A hydrostatic pressure- driven passive micropump enhanced with siphon-based autofill function.Lab Chip. 2018;18(15):2167-2177.
[19] WANG YN, FU LM. Micropumps and biomedical applications- A review. Microelectron Eng.2018;195:121-138.
[20] HOROBIN JT, SIMMONDS MJ, NANDAKUMAR D, et al. Speed Modulation of the HeartWare HVAD to Assess In Vitro Hemocompatibility of Pulsatile and Continuous Flow Regimes in a Rotary Blood Pump.Artif Organs.2018;42(9):879-890.
[21] JOOHYUNG L, ZACHARY E, HIMALI S, et al. A microfluidic cardiac flow profile generator for studying the effect of shear stress on the valvular endothelial cell.Lab Chip. 2018;18(19): 2946-2956.
[22] MEYVANTSSON I, WARRICK JW, HAYES S, et al. Automated cell culture in high density tubeless microfluidic device arrays. Lab Chip.2008;8(5):717-724.
[23] BERTHIER E, BEEBE DJ. Flow rate analysis of a surface tension driven passive micropump.Lab Chip. 2007;7(11): 1475-1478.
[24] JUNCKER D, SCHMID H, DRECHSLER U, et al. Autonomous microfluidic capillary system.Anal Chem. 2002;74(24):6139-6144.
[25] PARK JY, YOO SJ, HWANG CM, et al. Simultaneous generation of chemical concentration and mechanical shear stress gradients using microfluidic osmotic flow comparable to interstitial flow.Lab Chip.2009;9(15):2194-2202.
[26] CHEN SYC, HUNG PJ, LEE PJ. Microfluidic array for three-dimensional perfusion culture of human mammary epithelial cells.Biomed Microdevices.2011;13(4):753-758.
[27] CHEN MC, LAKE JR, HEYDE KC, et al. Three-dimensional Printing of Thermoplastic Materials to Create Automated Syringe Pumps with Feedback Control for Microfluidic Applications. Jove-J Vis Exp.2018;138:e57553.
[28] LAKE JR, HEYDE KC, RUDER WC. Low-cost feedback- controlled syringe pressure pumps for microfluidics applications. PLoS One.2017;12(4):e0175089.
[29] SHAEGH SAM, FERRARI FD, ZHANG YS, et al. A microfluidic optical platform for real-time monitoring of pH and oxygen in microfluidic bioreactors and organ-on-chip devices. Biomicrofluidics.2016;10(4):044111.
[30] SKARDAL A, MURPHY SV, DEVARASETTY M, et al. Multi-tissue interactions in an integrated three-tissue organ-on-a-chip platform.Sci Rep-UK.2017;7(1):8837.
[31] SMITS JG. Piezoelectric micropump with three valves working peristaltically. Sensor Actuat A-Phys.1990;21(1-3):203-206.
[32] MA T, SUN S, LI B, et al. Piezoelectric peristaltic micropump integrated on a microfluidic chip.Sensor Actuat A-Phys. 2019; 292:90-96.
[33] UNGER MA, CHOU HP, THORSEN T, et al. Monolithic Microfabricated Valves and Pumps by Multilayer Soft Lithography. Science.2000;288(5463):113-116.
[34] JEONG OC, KONISHI S. Fabrication of a peristaltic micro pump with novel cascaded actuators.J Micromech Microeng. 2008;18(2):025022.
[35] PARK JY, KIM SK, WOO DH, et al. Differentiation of Neural Progenitor Cells in a Microfluidic Chip‐Generated Cytokine Gradient.Stem Cells.2009; 27(11):2646-2654.
[36] CHO BS, SCHUSTER TG, ZHU X, et al. Passively Driven Integrated Microfluidic System for Separation of Motile Sperm. Anal Chem.2003;75(7):1671-1675.
[37] ZHU XY, CHU LY, CHUEH BH, et al. Arrays of horizontally- oriented mini-reservoirs generate steady microfluidic flows for continuous perfusion cell culture and gradient generation. Analyst.2004;129(11):1026-1031.
[38] PARK JY, MORGAN M, SACHS AN, et al. Single cell trapping in larger microwells capable of supporting cell spreading and proliferation.Microfluid Nanofluid.2010;8(2):263-268.
[39] HUNG PJ, LEE PJ, SABOUNCHI P, et al. Continuous perfusion microfluidic cell culture array for high-throughput cell-based assays.Biotechnol Bioeng.2005;89(1):1-8.
[40] WANG J, HEO J, HUA SZ, et al. Spatially resolved shear distribution in microfluidic chip for studying force transduction mechanisms in cells.Lab Chip. 2009;10(2):235-239.
[41] VINAYAKUMAR KB, NADIGER G, SHETTY VR, et al. Packaged peristaltic micropump for controlled drug delivery application. Rev Sci Instrum.2017;88(1):015102.
[42] CHENG CH, YANG AS, LIN CJ, et al. Characteristic studies of a novel piezoelectric impedance micropump.Microsyst Technol.2017;23(6):1709-1717.
[43] POURMAND A, SHAEGH SAM, GHAVIFEKR HB, et al. Fabrication of Whole-Thermoplastic Normally Closed Microvalve, Micro Check Valve, and Micropump.Sensor Actuat B-Chem.2017;262:625-636.
[44] WU MH, HUANG SB, CUI Z, et al.A high throughput perfusion-based microbioreactor platform integrated with pneumatic micropumps for three-dimensional cell culture. Biomed Microdevices.2008;10(2):309-319.
[45] AU AK, BHATTACHARJEE N, HOROWITZ LF, et al. 3D-printed microfluidic automation.Lab Chip.2015;15(8): 1934-1941.
[46] LEE YS, BHATTACHARJEE N, FOLCH A, et al. 3D-Printed Quake-Style Microvalves and Micropumps.Lab Chip. 2018; 18(8):1207-1214.
[47] ARORA S, LAM AJY, CHEUNG C, et al. Determination of critical shear stress for maturation of human pluripotent stem cell derived endothelial cells towards an arterial subtype. Biotechnol Bioeng.2018;116(5):1164-1175.
[48] WANG XL, ZHANG YY, FENG T, et al Fluid Shear Stress Promotes Autophagy in Hepatocellular Carcinoma Cells.Int J Biol Sci.2018;14(10):1277-1290.
[49] MEZA D, MUSMACKER B, STEADMAN E, et al. Endothelial Cell Biomechanical Responses are Dependent on Both Fluid Shear Stress and Tensile Strain. Cell Mol Bioeng. 2019;12(4): 311-325.
[50] YU L, MA X, SUN J, et al. Fluid shear stress induces osteoblast differentiation and arrests the cell cycle at the G0 phase via the ERK1/2 pathway.Mol Med Rep.2017;16(6):8699-8708.
[51] LANDWEHR GM ,KRISTOF AJ, RAHMAN SM, et al. Biophysical analysis of fluid shear stress induced cellular deformation in a microfluidic device.Biomicrofluidics. 2018; 12(5):054109.
[52] DELON LC, GUO ZB, OSZMIANA A, et al. A systematic investigation of the effect of the fluid shear stress on Caco-2 cells towards the optimization of epithelial organ-on-chip models. Biomaterials.2019;225:119521.
[53] BIROL S, FUCUCUOGLU R, CADIRCI S, et al. Investigation on the effects of variable shear stress on monocyte cell morphology.Micro Nano Lett.2017; 12(11):881-885.
[54] HUH D, MATTHEWS BD, MAMMOTO A, et al. Reconstituting Organ-Level Lung Functions on a Chip.Science. 2010;328 (5986):1662-1668.
[55] YAN Z, SU G, GAO W, et al. Fluid shear stress induces cell migration and invasion via activating autophagy in HepG2 cells.Cell Adhes Migr.2019;13(1):152-162.
[56] PRZYBYLA LM, VOLDMAN J. Attenuation of extrinsic signaling reveals the importance of matrix remodeling on maintenance of embryonic stem cell self-renewal.P Natl Acad Sci USA.2012;109(3):835-840.
[57] ESTRADA R, GIRIDHARAN GA, NGUYEN MD, et al. Endothelial Cell Culture Model for Replication of Physiological Profiles of Pressure, Flow, Stretch, and Shear Stress in Vitro. Anal Chem.2011;83(8):3170-3177.
[58] WANG CH, LEE GB. Pneumatically driven peristaltic micropumps utilizing serpentine-shape channels.J Micromech Microeng.2006;16(2):341-348.
[59] HUANG SB, WU MH, CUI Z, et al. A membrane-based serpentine-shape pneumatic micropump with pumping performance modulated by fluidic resistance.J Micromech Microeng.2008;18(4):045008.
[60] SOENKSEN LR, KASSIS T, NOH M, et al. Closed-loop feedback control for microfluidic systems through automated capacitive fluid height sensing.Lab Chip.2018;18(6):902-914.
[61] KANG YJ. Periodic and simultaneous quantification of blood viscosity and red blood cell aggregation using a microfluidic platform under in-vitro closed-loop circulation. Biomicrofluidics. 2018;12(2):024116.
[62] SUNG JH, KAM C, SHULER ML, et al. A microfluidic device for a pharmacokinetic–pharmacodynamic (PK-PD) model on a chip.Lab Chip.2010;10(4):446-455.
[63] ZHENG W, JIANG B, WANG D, et al. A microfluidic flow-stretch chip for investigating blood vessel biomechanics. Lab Chip. 2012;12(18):3441-3450.
[64] LANGILLE BL, ADAMSON SL. Relationship between blood flow direction and endothelial cell orientation at arterial branch sites in rabbits and mice.Circ Res.1981;48(4):481-488.
[65] LEE DW, CHOI N, SUNG JH. A microfluidic chip with gravity-induced unidirectional flow for perfusion cell culture. Biotechnol Progr.2019;35(1): UNSP e2701.
[66] WANG YI, SHULER ML. UniChip enables long-term recirculating unidirectional perfusion with gravity-driven flow for microphysiological systems.Lab Chip. 2018;18(17): 2563-2574.
[67] ZHANG Z, TANG W. Drug metabolism in drug discovery and development.Acta Pharm Sin B.2018;8(5):31-42.
[68] GORAL VN, ZHOU C, LAI F, et al. A continuous perfusion microplate for cell culture.Lab Chip.2013;13(6):1039-1043.
[69] VAN DV, ZHU D, RAMAKERS C, et al.Perfused 3D angiogenic sprouting in a high-throughput in vitro platform. Angiogenesis. 2019;22(1):157-165.
[70] VAN DUINEN V, VAN D HA, TRIETSCH SJ, et al. 96 perfusable blood vessels to study vascular permeability in vitro. Sci Rep-UK.2017;7(1):18071. |
| [1] | Wang Zhengdong, Huang Na, Chen Jingxian, Zheng Zuobing, Hu Xinyu, Li Mei, Su Xiao, Su Xuesen, Yan Nan. Inhibitory effects of sodium butyrate on microglial activation and expression of inflammatory factors induced by fluorosis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1075-1080. |
| [2] | Liu Bo, Chen Xianghe, Yang Kang, Yu Huilin, Lu Pengcheng. Mechanism of DNA methylation in exercise intervention for osteoporosis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(5): 791-797. |
| [3] | Cheng Jun, Tan Jun, Zhao Yun, Cheng Fangdong, Shi Guojia. Effect of thrombin concentration on the prevention of postoperative cerebrospinal leakage by fibrin glue [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 570-575. |
| [4] | Li Li, Ma Li. Immobilization of lactase on magnetic chitosan microspheres and its effect on enzymatic properties [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(4): 576-581. |
| [5] | Li Yanle, Yue Xiaohua, Wang Pei, Nie Weizhi, Zhang Junwei, Tan Yonghai, Jiang Hongjiang. Intramedullary nail fixation versus plate fixation in the treatment of displaced midshaft clavicular fractures in adults: a meta-analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(3): 471-476. |
| [6] | Wang Xinting, Xu Dandi, Zhang Junxia, Su Hailong Wang Qi. Stability of load-bearing cross barrier of different arch structures [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(24): 3838-3843. |
| [7] | Li Shanshan, You Ran, Guo Xiaoxiao, Zhao Lu, Wang Yanling, Chen Xi. Advances in the mechanisms of optic nerve regeneration [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(23): 3740-3745. |
| [8] | Wang Zhen, Lin Haiqi, He Fei, Lin Wentao. Exercise activates skeletal muscle satellite cells: exercise prevention and treatment for age-related sarcopenia and muscle injury [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(23): 3752-3759. |
| [9] | Liu Fang, Shan Zhengming, Tang Yulei, Wu Xiaomin, Tian Weiqun. Effects of hemostasis and promoting wound healing of ozone sustained-release hydrogel [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(22): 3445-3449. |
| [10] | Cui Tiantian, Yi Lan, Ouyang Hougan, Wu Huiting, Ouyang Yanchu, Chen Chu. Effect of thermosensitive moxibustion in a rat model of pelvic inflammation based on trifocal focal membrane theory [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(20): 3168-3172. |
| [11] | Xu Hui, Kang Bingxin, Zhong Sheng, Gao Chenxin, Zhao Chi, Qiu Guowei, Sun Songtao, Xie Jun, Xiao Lianbo, Shi Qi. Pressing local acupoints plus adjustion of the knee joint in a sitting position for treating knee osteoarthritis: a randomized controlled trial [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(2): 216-221. |
| [12] | Lu Mingfeng, Zhao Lilian, Xing Jisi, He Lilei, Xu Ting, Wang Changbing. Posttraumatic progression of cartilage degeneration following anterior cruciate ligament reconstruction: a second-look arthroscopic analysis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(2): 222-227. |
| [13] | Bao Sairong, Zhang Qiming, Yang Xingping, Liu Chunlong. Immediate effects of extracorporeal shock wave on muscle tone, stiffness, and elasticity of wrist flexor in stroke patients [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(2): 228-231. |
| [14] | Li Yu, Huang Peng, Wang Hong, Wang Anli. Dominant and non-dominant side knee isokinetic characteristics of Chinese calisthenics athletes [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(2): 232-236. |
| [15] | Chen Yutong, Li Chenchen, Liu Yang, Zheng Yaqin, Yang Xihua, An Meiwen. Establishment of an acute radioactive skin injury model in Wistar rats [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(2): 237-241. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||