Chinese Journal of Tissue Engineering Research ›› 2017, Vol. 21 ›› Issue (35): 5715-5720.doi: 10.3969/j.issn.2095-4344.2017.35.023
Previous Articles Next Articles
Research progress of lower cervical pedicle screw fixation
Hao Shen-shen, Liu Zhi-bin, Wang Fei
- Department of Orthopedics, Affiliated Hospital of Yan’an University, Yan’an 716000, Shaanxi Province, China
-
Online:2017-12-18Published:2018-01-02 -
Contact:Wang Fei, Master, Associate chief physician, Department of Orthopedics, Affiliated Hospital of Yan’an University, Yan’an 716000, Shaanxi Province, China -
About author:Hao Shen-shen, Studying for master’s degree, Department of Orthopedics, Affiliated Hospital of Yan’an University, Yan’an 716000, Shaanxi Province, China -
Supported by:the Social Research & Developmet Project of Shaanxi Province, No. 2015SF115; the Technology Huimin Project of Yan’an City, No. 2016HM-10-03
CLC Number:
Cite this article
Hao Shen-shen, Liu Zhi-bin, Wang Fei. Research progress of lower cervical pedicle screw fixation [J]. Chinese Journal of Tissue Engineering Research, 2017, 21(35): 5715-5720.
share this article
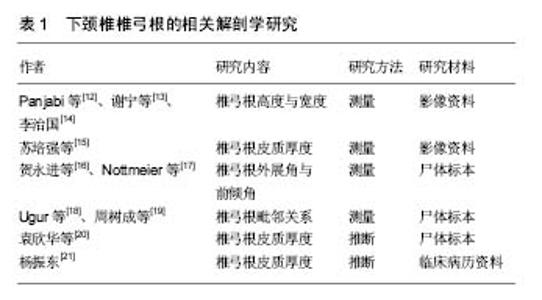
2.1 下颈椎椎弓根解剖学研究 由于下颈椎椎弓根的三维结构并不总是一致[9],椎弓根毗邻神经、血管、肌肉等复杂而重要的结构,如椎弓根前内侧紧贴硬膜外窦且硬膜外窦在椎管内,前外侧紧贴椎动脉。如果进钉偏出内或外侧都可能出现严重的并发症而发生危险,被一些手术医生视为手术的高危区域[10]。术中并发症包括显露过程中引起的局部神经血管损伤和椎弓根穿破引起的脊髓、神经根、椎动脉损伤及脑脊液漏等;术后并发症包括早期出现的颈深部血肿、内置物松脱断折、取骨区不适、感染等和晚期出现的植骨不融合、临位颈椎不稳、二次返修手术等[11]。同时手术切口暴露较小,术中操作受限,这就要求术者术前必须对椎弓根及其周围的局部解剖形态有非常清晰准确的了解。一旦出现置钉偏差可导致多种并发症,严重的可危及生命。鉴于此,许多学者对下颈椎进行了深入的解剖学研究(见表1)。"
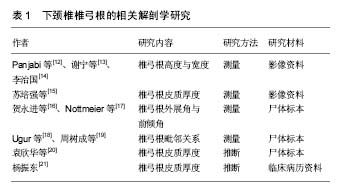
Panjabi等[12]研究发现,C3-C6椎弓根高度与宽度分别为6.7-7.6 mm与5.7-6.3 mm。谢宁等[13]通过对国人颈椎椎弓根的研究得出相似的结论,并认为两者之间的差异呈现一定的规律。李治国[14]采用CT方法测量48例术前患者C3-C6颈椎椎弓根的相关参数,得出椎弓根高度分别为C3(6.45±1.25) mm,C4(7.03±1.38) mm,C5(7.62±1.40) mm,C6(7.78±1.35) mm;椎弓根宽度分别为C3(5.47±0.86) mm,C4(5.39±0.83) mm,C5(5.82±1.47) mm,C6(5.76±1.03) mm;并将此相关参数与徒手测量所得相关参数进行统计学分析,发现两者间差异无显著性意义。苏培强等[15]研究发现,不同节段下颈椎椎弓根内侧与外侧壁皮质骨厚度差异明显,内侧皮质骨厚度显著大于外侧,最薄的皮质骨总处于外侧壁,尤以C3和C4最明显。贺永进等[16]应用螺旋CT测量10具保存完好的颈部标本,并应用容积成像和多平面成像技术测量下颈椎的相关参数,发现下颈椎椎弓根的外展角与前倾角平均值分别为(42.03±7.57)°与(76.32±12.05)°。Nottmeier等[17]对下颈椎椎弓根的相关参数做了相似的研究,统计C3-C6得出结论椎弓根外展角35°-45°,前倾角90°-100°,椎弓根松皮质骨4.7-6.4 mm,宽度4.5-4.9 mm。Ugur 等[18]对20具尸体标本下颈椎测量显示椎弓根与上位神经根、椎弓根与硬脊膜之间80%的标本没有间隙,而与下位神经根间距为1.0-2.5 mm,并发现神经根平均直径由C3至C6逐渐增大。周树成等[19]应用游标卡尺和量角器对32具成人C3-C7颈椎标本进行了椎弓根与局部相邻神经间距的测量,发现椎弓根与其上神经根的间距为1.18- 1.40 mm,并按从上到下的顺序逐渐增大;与其下神经根间距为2.33-3.11 mm,并按从上到下的顺序逐渐减小;与硬脊膜的间距为2.75-3.33 mm,并未发现各椎体之间的规律;椎弓根与椎动脉和硬膜外窦之间紧密接触,几乎没有距离。袁欣华等[20]测试椎弓根通道上壁、下壁、内侧壁、外侧壁的穿透力和突破力,发现内侧壁的穿透力和突破力均明显较其他壁大,反证了内侧壁较外侧壁厚。有研究则从并发症方面分析反证了内侧壁较厚。 从解剖结构上分析,下颈椎椎弓根粗细、长短、走向个体之间差异较大,即不同个体之间,椎弓根存在差异,并且即使是同一个体之间,不同的椎弓根也存在差异。通过分析椎弓根的长度、宽度、高度等相关参数,可以为临床治疗提供参考。研究表明,椎弓根是有“力核”之称的脊柱中最强硬部位,椎弓根中间少量的松质骨能够对螺钉起到很好的把持力,椎弓根螺钉固定可以贯通脊柱的前、中、后三柱,在对整个脊柱起到稳定固定作用的同时,由于左右椎弓根互成近似直角的特殊结构,使得置入的螺钉具有较强的抗侧弯、轴向扭转、平面移位等作用[21]。 2.2 置钉固定的生物力学 判断一种固定方式是否可靠、有效,离不开生物力学实验分析。许多学者对颈椎椎弓根螺钉固定效果进行了生物力学测试,研究表明经椎弓根置钉内固定所提供的稳定性明显优于其他内固定技术方法,甚至有学者报道其稳定性超过前后路联合内固定技术的稳定性[22](见表2)。"
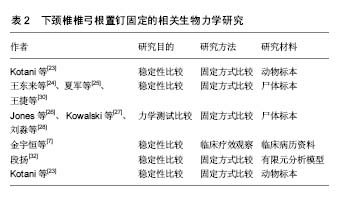
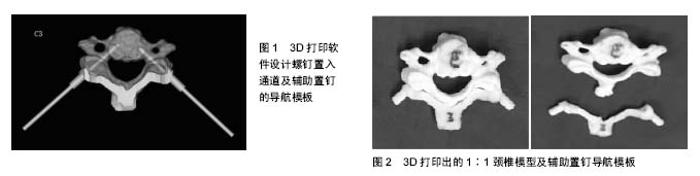
王东来等[23]在8具新鲜标本上比较5种不同颈椎内固定方法的稳定性,从生物力学上证实了经椎弓根置钉在三维运动稳定性方面明显优越性。Kotani等[22]进行了较为详细的研究,通过小牛颈椎模型测定了7种不同的颈椎内固定方法的生物力学稳定性,认为对于颈椎单节段后柱不稳者,各种后路内固定均可达到完整颈椎的稳定性;然而对于两节段三柱不稳者,椎弓根螺钉内固定可克服一般内固定的旋转稳定性不足的问题,具有明显的优越性。夏军等[24]研究4种不同内固定技术在椎弓根损伤模型的初始稳定性,发现椎弓根螺钉固定的效果接近于前路自锁钢板加后块钢板固定的稳定性,优于单纯前路或后路固定的稳定性。Jones等[25]在56个新鲜颈椎骨上对比椎弓根螺钉和侧块螺钉两种固定方式的拔出强度,发现椎弓根钉拔出力(677 N)明显大于侧块螺钉拔出力(355 N);并且椎弓根螺钉因较侧块螺钉钉道长而不易发生松钉和脱钉,尤以侧块较小的C6和C7明显。Kowalski等[26]运用50具新鲜下颈椎标本对椎弓根置钉的生物力学进行了测试,结果显示螺钉在切除了侧块骨质的椎弓根与标准椎弓根之间的抗拔出力方面差异无显著性意义,不同节段之间差异亦无显著性意义。刘淼等[27]用100个下颈椎标本进行了椎体螺钉置钉与椎弓根螺钉置钉之间在固定稳定性、轴向拔出力、疲劳加载后轴向拔出力等方面的生物力学测试,认为椎弓根螺钉在即时拔出力、即时拔出刚度方面的生物力学性能显著优于椎体螺钉置钉;在疲劳拔出力、疲劳拔出刚度方面的生物力学性能虽无明显差异,但在统计学方面椎弓根螺钉置钉的优势更显著;进一步提示椎弓根螺钉置钉的可行性、优越性。朱瑜琪[28]推荐经椎弓根置钉应用于不稳定颈椎的固定,因其无论从临床应用角度,还是从生物力学及形态学方面分析都可取得令人满意的效果。王捷等[29]也认为此法是恰当的固定失稳颈椎方法。朱道平等[30]报道后路经椎弓根螺钉固定不仅有利于复位,而且能有效维持术后颈椎序列,具有良好的生物力学稳定性。金宇恒等[7]推荐多节段固定应用经椎弓根置钉固定,因其在抗扭转和抗伸展方面生物力学稳定性最佳。段扬[31]建立椎弓根螺钉固定、侧块螺钉固定、经关节突螺钉固定3种后路下颈椎螺钉固定下的三维有限元模型并进行了生物力学测试,发现椎弓根螺钉固定系统应力集中于螺钉与钛棒衔接部分;在各种工况下的应力峰值均远低于钛合金屈服强度,引起固定物疲劳断裂的可能性较低;并推荐椎弓根螺钉固定作为后路治疗三柱损伤的首选方式。 由于下颈椎椎弓根螺钉固定具有优越的生物力学稳定性,其应用的适应证也逐渐扩大。目前主要适用于各种创伤引起的颈椎骨折、脱位;颈椎肿瘤、结核等;风湿、类风湿、退行性变致颈椎不稳;脊髓型颈椎病[32];需要矫治的颈椎畸形;颈椎破坏性骨关节病;不能用侧块螺钉的颈椎;对内固定强度要求较高者;术前或术后需要进行气管切开等。 2.3 3D打印技术辅助置钉的应用 下颈椎因解剖位置、形态的特殊性,局部毗邻重要组织结构,特别是神经组织,一旦损伤可导致严重的并发症,甚至可危及生命。螺钉的进针点或进针角度一旦发生偏差可突破椎弓根皮质、降低螺钉的稳定性和损伤毗邻的神经血管,螺钉过长可突破椎体前缘而造成局部组织损伤,螺钉过短可因对椎弓根的抗拔出力降低而导致固定不牢固,螺钉的直径过大可胀破椎弓根皮质而造成神经血管损伤,直径过小则可因未切入骨皮质而无法提供可靠的固定。传统徒手置钉时对进针点判断、进针角度把握、螺钉长度与直径选择优为重要,手术部位必须清晰而充分暴露;在实际手术过程中需要多次透视,势必增加放射线暴露时间及医疗费用。计算机导航辅助置钉技术可有效地减小上述弊端,并提供精准置钉;然而计算机导航辅助置钉技术存在自身的缺点[33]。3D打印技术辅助置钉的出现又克服了计算机导航辅助置钉技术的部分弊端,而且也为颈椎返修手术等复杂手术提供了一种新思路,具有明显优势。 3D打印技术应用于医学领域,因其能够实现个体化、精准化治疗,被认是精准医学发展史上的新篇章[34]。3D打印技术应用于下颈椎手术,可优化术前策划,良好的术前策划是手术成功的关键,特别对于经下颈椎椎弓根置钉此类风险较大的手术,或是新开展的手术,术前策划尤为重要[35]。应用相关软件可在计算机上标记出椎弓根轴线,旋转和透明处理模型图像,从而调整螺钉及钉道位置至最佳(见图1)[36]。术前即可打印出病变颈椎的1∶1模型及个性化辅助置钉导板,并可在模型上模拟手术过程、熟练手术操作、预计手术结果,这对于术前规划及术中操作十分有用(见图2)[37]。传统的骨科手术主要依靠病变部位X射线片及CT等影像学资料作为依据进行手术准备,但平面影像中常存在相互遮挡重影或伪影的干扰,远没有1∶1模型提供的解剖信息多[38];同时平面影像需要术者具备良好的空间想象力。因此对于下颈椎病变此类即复杂又精细的手术,手术难度势必增大;同时也难于使患者及家属对手术的理解,不利于医患之间沟通。利用3D打印技术制作出的1∶1模型可直观地呈现于眼前,便于医患间的沟通,增进医患双方的配合。在组织工程方面,3D打印技术制造的人工骨不仅可采用可降解支架材料,使得人工骨可成为人体器官的一部分,参与代谢和生长,随着支架材料在体内的自动降解,新骨生成与支架材料的降解速率相匹配[39],而且在具有与人体骨一致的形状和力学性能的同时,还具有一致的功能梯度[40]。设计具有生物活性的人工器官、细胞的三维结构,以细胞、生长因子等为基础的3D 生物打印是目前3D打印技术最前沿和最具发展前景的研究领域[41]。 应用3D打印技术辅助置钉的关键在于制做3D打印个性化导航模板。具体制作方法如下:首先对目标椎体进CT扫描,扫描层厚度约1 mm,将扫描数据以Dicom保存,再将Dicom格式的数据导入3D图像生成、编辑、处理软件,如Mimics(Materialise公司),生成目标椎体的三维模型,并以STL格式导出。将STL格式数据导入逆向工程软件,如Imageware(EDS公司)、Geomagic Studio(Geomagic公司)、UG(Siemens公司)等,提取出椎板、棘突、关节突后面的表面解剖形态,设计最佳置钉通道,建立反向模板,将最佳置钉通道与反向模板拟合成一体,形成带有导向孔定位的导航模板,仍以STL格式保存,导入3D打印机,打印出椎体模型和置钉导板。该方法学习曲线较短,易于掌握,定位准确,减少术中过度剥离,降低置钉难度;模板制作相对便利,成本较低,不需要其他辅助设备;操作简单,术中无需注册和射线透视,只需在置钉完成后一次透视即可,减少了术者与患者在射线下的暴露时间;个体化导航模板只涉及单个椎体,不受患者体位变化的影响;对于颈椎有解剖变异畸形者,导航模板也不受影响。随着临床上颈椎内固定技术的应用越来越广泛,颈椎返修手术随之也会越来越多,术后的颈椎解剖结构发生很大的变异,依靠解剖定位来确定螺钉进针点已成为不可能,再次螺钉置入的难度、手术时间、术中出血量、手术的危险性均会相应的增加,3D打印个性化导航模板将为临床医生处理这些复杂手术提供一种新思路。 宋柯等[42]实验发现3D打印个性化导航模板在计算机上模拟置钉与尸体上置钉两者间差异无显著性意义。张振辉等[43]在8具尸体标本上用3D打印导航模板成功置入64枚螺钉,准确率达97%,并认为该方法能提高置钉准确率,增加手术安全性。宁金沛等[44]用3D打印导航模板辅助在7例患者中成功置入24枚椎弓根螺钉,23枚完全在椎弓根内,1枚穿破椎弓根外壁,但距离小于 1.2 mm,术后未出现相关的神经血管并发症,螺钉位置可接受率达100%。Bozkus等[45]在术中用3D打印椎弓根导航模板成功置入8枚螺钉于4例患者椎弓根中,术后CT显示螺钉进针部位、方向、长度、直径等准确、合适。白宇哲等[46]报道采用数控机床制造出5个金属材质的个体化下颈椎椎弓根置钉导板共置入10枚螺钉,术后CT扫描螺钉均位于椎弓根内,计算水平面绝对偏差值为(0.44± 0.23) mm,矢状面绝对偏差值为(0.37±0.20) mm,虚拟置入直经3.5 mm螺钉实验中,所有螺钉均位于非临界螺钉位置。Paiva等[47]运用3D打印技术顺利完成了1例颈椎尤文肉瘤患者术前计划制定及术中风险评估。3D打印模型还能有效保护椎动脉及神经根,提高置钉成功率,确保手术安全性[48]。 3D打印技术辅助置钉也有其缺点,如导航模板制做过程中,某些环节如数据的转换、打印材料的质地、冷却温度的控制、打印机的打印精度等会直接影响到其精确性;对CT要求比较高,CT扫描要求层厚度在1 mm左右;模板的制作相对耗时,可能会限制在急诊手术中的应用;由于导板多为树脂或高分子材料,消毒及术中安置过程中可能发生导板变形、断裂等;术区软组织剥离不完全,导板置钉是假设脊柱后方无软组织的情况,这与实际情况不相符合[49];导板的制作缺乏统一的标准,如设计、制造、检验等。王飞等[50]设计的带有导向通道的3D打印辅助置钉导板,创造性运用低温等离子消毒,克服了导板高温易变形的缺点,进一步确保了置钉的准确性。尽管3D打印辅助置钉技术仍有部分缺点,随着研究及应用的深入,这些缺点会被逐一解决的。"

| [1] 石向明,王辉,董巍,等.64层CT精细扫描构建下颈椎三维有限元模型及验证[J]. 河北医药,2012,34(14):2104-2106.[2] Alshami AM. Prevalence of spinal disorders and their relationships with age and gender. Saudi Med J. 2015;36(6): 725-730.[3] 黄宏,段伯良. 颈椎生理曲度与颈椎病[J]. 右江医学,2002, 30(4):319-319.[4] 范凌,潘显明,屈波,等. 下颈椎退变不稳的诊断和外科治疗[J]. 重庆医科大学学报, 2011,36(4):493-495.[5] 李宏达,夏群,白剑强,等.健康成人下颈椎在体三维瞬时运动特点研究[J]. 中国修复重建外科杂志,2015,29(12):1494-1499.[6] Abumi K, Itoh H, Taneichi H, et al. Transpedicular screw fixation for traumatic lesions of the middle and lower cervical spine: description of the techniques and preliminary report. J Spinal Disord. 1994;7(1):19-28.[7] 金宇恒,杨光,郝玉刚,等. 颈椎椎弓根钉棒系统内固定在下颈椎骨折脱位治疗中的临床应用[J]. 中国医学前沿杂志:电子版, 2015, 7(11):69-73.[8] Abumi K, Shono Y, Kotani Y, et al. Indirect posterior reduction and fusion of the traumatie herniated dise by using a cervical pedicle screw system. J Neurosurg. 2000;92(1):30-37. [9] 傅一山, 陈正形. 颈椎弓根置钉的影像学测量[J]. 中国脊柱脊髓杂志, 2001, 11(1):29-31.[10] Cao J, He F, He L, et al. Experimental study on screw insertion in lower cervical pedicle assisted by multi-spiral computerized tomography three dimensional reconstruction techniques. Zhongguo Xiufu Chongjian Waike Zazhi. 2010; 24( 5) : 525-530.[11] 王东来,唐天驷,黄士中,等.下颈椎椎弓根内固定的解剖学研究与临床应用[J].中华骨科杂志,1998,18(11):659-662.[12] Panjabi MM, Duranceau J, Goel V, et al. Cervical human vertebrae. Quantitative three-dimensional anatomy of the middle and lower regions. Spine. 1991;16(8):861-869.[13] 谢宁,李家顺,贾连顺,等. 颈椎后结构的影像学测量及其临床意义[J].中国脊柱脊髓杂志,1999,9(5): 266-268. [14] 李治国. 颈椎椎弓根形态个体化术前应用CT测量评价的临床意义[J]. 中国CT和MRI杂志, 2016,14(6):130-132.[15] 苏培强,曾时兴,刘尚礼,等. 术前CT测量对颈椎椎弓根形态个体化评价的意义[J]. 中国临床解剖学杂志, 2007, 25(5): 515-517.[16] 贺永进,李长红,刘志斌. 多层螺旋CT扫描三维重建技术测量下颈椎椎弓根相关参数的可行性研究[J]. 广西医科大学学报, 2016, 33(2):286-289.[17] Nottmeier EW,Pirris SM. Placement of thoracic transvertebral pedicle screws using 3D image guidance. J Neurosurg Spine. 2013;18(5):479-483.[18] U?ur HC, Attar A, Uz A, et al. Surgical anatomic evaluation of the cervical pedicle and adjacent neural structures. Neurosurgery. 2000;47(5):1162-1168.[19] 周树成,张鹏. 下颈椎椎弓根相邻解剖结构的应用研究[J]. 局解手术学杂志, 2016,25(1):30-32.[20] 袁欣华,庞清江,许柯,等.下颈椎椎弓根通道穿透力及突破力的生物力学研究[J]. 现代实用医学,2012,24(10):1096-1098+1201.[21] 胡宗,杨广忠.下颈椎椎弓根螺钉固定的相关研究进展[J].兵团医学,2011,27(1):37-40.[22] Kotani Y, Cunningham BW, Abumi K, et al. Biomechanical analysis of cervical stabilization systems. An assessment of transpedicular screw fixation in the cervical spine. Spine. 1994;19(22):2529-2539. [23] 王东来,唐天驷,黄士中. 五种颈椎内固定方法的稳定性生物力学评价[J]. 中华外科杂志, 1999, 37(5):301-303.[24] 夏军,顾昕,黄煌渊. 四种下颈椎内固定技术初始稳定性的生物力学比较[J]. 中华创伤骨科杂志, 2004, 6(4):430-433.[25] Jones EL, Heller JG, Silcox DH, et al. Cervical pedicle screws versus lateral mass screws. Anatomic feasibility and biomechanical comparison. Spine. 1997;22(9):977-982.[26] Kowalski JM, Lucwig SC, Hutton WC, et al. Cervical spine pedicle screws: a biomechanical comparison of two insertion techniques. Spine. 2000;25(22):2865-2867.[27] 刘淼,尚显文,宁旭,等.椎弓根螺钉及颈椎体螺钉置入内固定后的生物力学及稳定性比较[J].中国组织工程研究,2016,20(35): 5210-5215.[28] 朱瑜琪.颈椎椎弓根螺钉置入固定失稳颈椎[J].中国组织工程研究,2012,16(39):7358-7365. [29] 王捷,郭志辉,潘子毅. 下颈椎后路三种内固定稳定性的生物力学测试和评价[J]. 中国中医骨伤科杂志, 2007, 15(10):4-10.[30] 朱道平,刘克斌,黄奎. 后路减压固定治疗伴椎间盘突出的下颈椎骨折脱位[J]. 骨科, 2014, 5(2):98-101.[31] 段扬. 下颈椎后路内固定技术的有限元比较研究[D].南方医科大学,2011.[32] 孙程帅,李雷,孟伟宁. 颈椎后路椎弓根螺钉内固定术治疗脊髓型颈椎病患者的疗效分析[J]. 沈阳医学院学报, 2016, 18(4):245-247.[33] 李书纲,盛林, 赵宏,等. 计算机导航技术在脊柱椎弓根钉固定中的应用[J]. 中华医学杂志, 2009, 89(11):736-739.[34] Hwang TJ, Kiang C, Paul M. Surgical applications of 3-dimensional printing and precision medicine. JAMA. 2015; 141(4):305-306.[35] Giesel FL, Hart AR, Hahn HK, et al. 3D reconstructions of the cerebral ventricles and volume quantification in children with brain malformations. Acad Radiol. 2009;16(5):610-617.[36] 王远政,田晓滨,刘洋,等. Mimics及颈椎模型用于下颈椎椎弓根个体化置钉的应用研究[J]. 第三军医大学学报, 2012,34(15): 1543-1547. [37] Guarino J, Tennyson S, Mc Cain G, et al. Rapid prototyping technology for surgeries of the pediatric spine and pelvis: benefits analysis. J Pediatr Orthop. 2007;27( 8) : 955-960.[38] Gelalis ID, Paschos NK, Pakos EE, et al. Accuracy of pedicle screw placement: a systematic review of prospective in vivo studies comparing free hand, fluoroscopy guidance and navigation technique. Eur Spine J. 2012;21(2):247-255.[39] 房岩,孙刚,丛茜,等. 仿生材料学研究进展[J]. 农业机械学报, 2006,37(11):163-167. [40] 王镓垠,柴磊,刘利彪,等. 人体器官3D打印的最新进展[J]. 机械工程学报,2014,50(23):119-127.[41] Langer R. Tissue engineering: perspectives, challenges, and future directions. Tissue Eng. 2007;13(1):1-2.[42] 宋柯,付茂庆,孔祥雪,等. 生物安全性的下颈椎后路经椎弓根固定的个性化导航模板研究[J]. 中国临床解剖学杂志,2012, 30(5):509-512.[43] 张振辉,王庆德,梅伟,等. 快速成型个体化导航模板辅助颈椎椎弓根螺钉的置入[J]. 中国组织工程研究,2017,21(3):340-344.[44] 宁金沛,吴卫东,覃求,等. 3D打印个体化导航模板在胸椎和颈椎椎弓根螺钉植入的临床应用[J].实用骨科杂志, 2015,21(5): 385-389.[45] Bozkus H, Ames CP, Chamberlain RH, et al. Biomechanical analysis of rigid stabilization techniques for three-column injury in the lower cervical spine. Spine. 2005;30(8):915-922.[46] 白宇哲,李长树, 徐楚,等. 数控机床技术在下颈椎个体化导向模板制作中的应用[J]. 中国临床解剖学杂志, 2015, 33(3): 284-287.[47] Paiva WS, Amorim R, Bezerra DA, et al. Application of the stereo-lithography technique in complex spine surgery. Arg Neurop Siguiatr. 2007;65(2B):443-445.[48] 李浩,李承鑫,张学军,等. 3D 打印模型辅助后路内固定治疗儿童颈椎畸形[J].中华小儿外科杂志,2015,36(3) : 192-196.[49] 刘运潮,侯树勋,张宇鹏. 脊柱椎弓根螺钉置钉技术研究进展[J]. 中国骨与关节杂志, 2016, 5(8):596-601.[50] 王飞,刘志斌,张建华,等. 3D打印导航模板在辅助寰枢椎椎弓根螺钉置入中的应用价值[J]. 中国脊柱脊髓杂志, 2017, 27(1): 61-68.[51] 曹珺,代耀军,何飞. 下颈椎经椎弓根内固定的生物力学稳定性分析[J]. 中国组织工程研究与临床康复,2008,12(44): 8725-8728.[52] 朱彦昭,徐荣明,吴建民. 下颈椎椎弓根螺钉内固定的研究进展[J]. 中医正骨, 2010, 22(8):62-65. |
| [1] | Wang Jianping, Zhang Xiaohui, Yu Jinwei, Wei Shaoliang, Zhang Xinmin, Xu Xingxin, Qu Haijun. Application of knee joint motion analysis in machanism based on three-dimensional image registration and coordinate transformation [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(在线): 1-5. |
| [2] | Zhang Yufang, Lü Meng, Mei Zhao. Construction and verification of a full spine biomechanical model of adolescent scoliosis [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1351-1356. |
| [3] | Bai Zixing, Cao Xuhan, Sun Chengyi, Yang Yanjun, Chen Si, Wen Jianmin, Lin Xinxiao, Sun Weidong. Construction and biomechanical analysis of ankle joint finite element model in gait cycle [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1362-1366. |
| [4] | Liu Feng, Feng Yi. Finite element analysis of different Kirschner wire tension bands on transverse patella fractures during gait cycle [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1367-1371. |
| [5] | Yao Xiaoling, Peng Jiancheng, Xu Yuerong, Yang Zhidong, Zhang Shuncong. Variable-angle zero-notch anterior interbody fusion system in the treatment of cervical spondylotic myelopathy: 30-month follow-up [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(9): 1377-1382. |
| [6] | Zhang Jinglin, Leng Min, Zhu Boheng, Wang Hong. Mechanism and application of stem cell-derived exosomes in promoting diabetic wound healing [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1113-1118. |
| [7] | An Weizheng, He Xiao, Ren Shuai, Liu Jianyu. Potential of muscle-derived stem cells in peripheral nerve regeneration [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(7): 1130-1136. |
| [8] | Wen Mingtao, Liang Xuezhen, Li Jiacheng, Xu Bo, Li Gang. Mechanical stability of Sanders II type calcaneal fractures fixed by two internal fixation methods [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(6): 838-842. |
| [9] | Huang Hao, Hong Song, Wa Qingde. Finite element analysis of the effect of femoral component rotation on patellofemoral joint contact pressure in total knee arthroplasty [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(6): 848-852. |
| [10] | Zheng Yongze, Zheng Liqin, He Xingpeng, Chen Xinmin, Li Musheng, Li Pengfei, Lin Ziling. Extended finite element modeling analysis of femoral neck fracture based on ABAQUS software [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(6): 853-857. |
| [11] | Liu Yuhang, Zhou Jianqiang, Xu Xuebin, Qu Xingyue, Li Ziyu, Li Kun, Wang Xing, Li Zhijun, Li Xiaohe, Zhang Shaojie. Establishment and validation of finite element model of lower cervical spine in 6-year-old children [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(6): 870-874. |
| [12] | Duan Chao, Shang Xiaoqiang, Duan Xianglin, Yang Ping, Tao Shengxiang. Stability of patellar claw versus loop plate combined with patellar claw for the treatment of comminuted fractures of the lower pole of the patella [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(6): 934-937. |
| [13] | Chen Xiaoxu, Luo Yaxin, Bi Haoran, Yang Kun. Preparation and application of acellular scaffold in tissue engineering and regenerative medicine [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 591-596. |
| [14] | Kang Kunlong, Wang Xintao. Research hotspot of biological scaffold materials promoting osteogenic differentiation of bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 597-603. |
| [15] | Shen Jiahua, Fu Yong. Application of graphene-based nanomaterials in stem cells [J]. Chinese Journal of Tissue Engineering Research, 2022, 26(4): 604-609. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||